Спосіб визначення якості фармацевтичних препаратів серцево-судинної дії на основі триметазидину дигідрохлориду у кристалічній формі
Номер патенту: 94753
Опубліковано: 10.06.2011
Автори: Приходько Роман Миколайович, ШТЕЙНГАРТ Марк Вольфович
Формула / Реферат
Спосіб визначення якості фармацевтичних препаратів серцево-судинної дії, що містять триметазидину дигідрохлорид у кристалічній формі, який відрізняється тим, що для дослідження таблеток триметазидину дигідрохлориду використовують рентгеноструктурний аналіз при випромінюванні 1,5405Ǻ і порівнюють отримані параметри з параметрами індивідуальних інгредієнтів у кристалічній формі, визначають параметри незалежного відтворювання компонентів та за їх відхиленням судять про якість препарату, кінетику розчинення триметазидину та про фізико-механічні властивості таблеток.
Текст
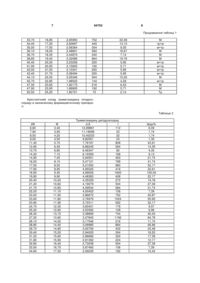
Спосіб визначення якості фармацевтичних препаратів серцево-судинної дії, що містять три 3 94753 Проте при цьому не досягається рівномірного вивільнення триметазидину дигідрохлориду протягом доби, особливо найменше його вивільнення перед ранковим застосуванням, а в цей час найчастіше за все трапляються критичні моменти серцевої діяльності. Тому створено препарати з пролонгованим вивільненням діючої речовини. Відомо матриксну таблетку триметазидину дигідрохлориду на основі твердої матриці. У складі використовується манітол як наповнювач для створення матриці, а також застосовується грануляція лікарської і допоміжної речовин і воску монтанового розчином еудрагіту RS PO 100 [UA 12297 МПК 2006 А61К 31/495]. В цих таблетках кристалічні речовини мають такий склад від маси таблетки, мас.%: триметазидину дигідрохлорид 22,15 манітол 8,85 мікрокристалічна целюлоза 13,30. Відомо матриксну таблетку, в якій використовується інші допоміжні речовини: кальцію дифосфат як наповнювач і гідроксипропілметилцелюлоза як регулятор швидкості розчинення. В цих таблетках кристалічні речовини мають такий склад: триметазидин - 17,5 мас. %, кальцію дигідрофосфат - 40,45 мас. % від маси таблетки [UA 80087 МПК СD А61К31/495]. Таким чином, промислові способи приготування таблеток триметазидину з різними формами вивільнення використовують кристалічні наповнювачі (манітол або кальцію дифосфат, мікрокристалічну целюлозу) та аморфні речовини для забезпечення механічних властивостей таблетки і різноманітних програм розчинення. Якість такого препарату визначають відомими методами - показниками загальними для цієї лікарської форми, міцність, стираність, однорідність ваги, кількісний зміст, показниками специфічними для цього препарату - кінетика вивільнення, характер матриці в ретардних формах. Лікарська форма містить комплекс лікарської і допоміжних речовин. І вищеназвані показники не можуть передати, яким чином відбувається вивільнення такого комплексу в організмі ссавців. В останні роки з'явились роботи, в яких використовується як один із показників якості - рентгеностру 4 ктурне визначення лікарської форми, її компонентів. В тих випадках, коли в лікарській формі, як наприклад в триметазидині, є значна кількість кристалічних речовин, цей показник може бути впроваджений для характеристики лікарської форми, захисту її від фальсифікації, визначення порядку вивільнення не тільки діючої речовини, але і його комплексу з допоміжними речовинами. Таблетка є багатокомпонентним продуктом, який має як кристалічні компоненти, так і аморфні компоненти. Аморфні компоненти можуть на дериватограмі, або ніяк не проявлятись, або проявлятись у вигляді гало. Кристалічні компоненти проявляються сукупністю частин найбільш значимих за інтенсивністю дериватограм своїх компонентів. При виготовленні таблеток можуть бути не тільки накладки інтенсивності різних компонентів, що викликає труднощі в їх розшифруванні. Можливо також утворення твердих розчинів компонентів, деяка зміна кутів 2 Ө більше, ніж допустима методикою рентгеноструктурного аналізу. Всі ці показники є специфічними для кожного препарату, не можуть бути передбачені апріорі і можуть бути використані в практичних умовах для вирішення зазначених задач. Використання рентгеноструктурного аналізу для цих умов відомо в літературі. CHALLENGES IN DETECTING CRYSTALLINE PHASE IN AN AMORPHOUS MATRIX M. Davidovich, M. Fakes, S. Futernik, S. Desikan, B. Huang, B. Sarsfield and K. Volk Pharmaceutical Research Institute Bristol-Myers Squibb Company, New Brunswick, NJ 08901, XRD CHARACTERIZATION OF CRYSTALLINITY AND MICROSTRUCTURE OF PHARMACEUTICAL COMPOSITES Luca Lutterottia,b, Mauro Bortolottia, Lorenzo Magarottoa,c, Ezio Petriccib aDpt. of Materials Engineering and Industrial Technology, University of Trento, Italy bGNR Analytical Instruments Group, Ital Structures, Riva del Garda (TN), Italy cSistiana, 204, Duino Aurisina, 34013, Trieste, Italy (The pharmaceutical Powder X-ray Diffraction Symposium, 14-16 February 2006, Somerset, New Jersey, USA). Найближчим аналогом до винаходу, що заявляється, є триметазидину дигідрохлорид, який має наступну кристалічну структурну [UA №28550, C07D 209/00, 2007] 2θ° Θ° d, Å 10,08 16,88 17,8 21,50 24,24 25,31 26,68 28,14 29,57 30,62 31,63 32,24 33,28 5,04 8,44 8,90 10,60 12,12 12,655 13,34 14,07 14,785 15,31 15,815 16,12 16,64 13,03 7,80 7,40 6,22 5,45 5,22 4,96 4,711 4,48 4,33 4,20 4,12 4,00 Інтенсивність Імп/сІ 4710 10852 1172 933 7900 10493 661 9083 2952 2713 1183 1064 1183 Iотн. % 43,4 100 10,8 8,6 72,8 96,7 60,9 83,7 27,2 25,0 10,9 9,8 10,9 5 34,22 35,16 35,83 39,42 41,00 43,22 44,70 45,80 47,10 49,35 52,18 94753 17,11 17,58 17,915 19,71 20,50 21,61 22,35 22,90 23,55 24,675 26,09 3,89 3,79 3,72 3,39 3,27 3,11 3,01 2,94 2,86 2,74 2,60 В цьому патенті зазначено, що для точнішої характеристики максимумів, які визначають наявність кристалічних структур з певними міжплощинними відстанями, було застосовано випромінювання 2,29Ǻ. Проте більшість досліджень застосовують для цієї мети випромінювання 1,5405Ǻ, тому результати важко порівнювати. При такому режимі дифрактометр має більш значну інерційність і більш вірогідна можливість не визначення окремих параметрів дифрактограми. В патенті немає інформації, які зразки субстанції вивчались і чи була попередня підготовка зразків, наприклад, перекристалізація. В основу винаходу поставлено задачу знайти спосіб визначення якості фармацевтичних препаратів серцево-судинної дії, що містять триметазидину дигідрохлорид, який дозволив би ідентифікувати фармацевтичний препарат за його вивільненням для запобігання фальсифікації. 6 1530 2127 3657 1183 3538 8725 1291 1183 2952 1769 2474 14,1 19,6 33,7 10,9 32,6 80,4 11,9 10,9 27,2 16,3 22,8 Поставлену задачу вирішують тим, що в способі визначення якості фармацевтичних препаратів серцево-судинної дії, що містять триметазидину дигідрохлорид у кристалічній формі, згідно з винаходом, для дослідження таблеток триметазилину дигідрохлориду використовують рентгеноструктурний аналіз при випромінюванні 1,5405Ǻ і порівнюють отримані параметри з параметрами індивідуальних інгредієнтів у кристалічній формі, визначають параметри незалежного відтворювання компонентів та за відхиленням судять про якість препарату, а за кінетикою розчинення триметазидину про фізико-механічні властивості таблеток. Кристалічний склад фармацевтичного препарату триметазидину дигідрохлориду з фіксованою дозою 20 мг в таблетках, в яких як кристалічний наповнювач використовують манітол Таблиця 1 2Ө 6,80 8,10 9,40 10,60 11,40 12,90 14,80 16,20 16,90 18,00 18,80 19,70 20,50 21,10 21,80 23,10 23,50 24,80 26,00 27,30 28,70 29,40 30,70 31,40 31,80 32,80 Ө 3,40 4,05 4,70 5,30 5,70 6,45 7,40 8,10 8,45 9,00 9,40 9,85 10,25 10,55 10,90 11,55 11,75 12,40 13,00 13,65 14,35 14,70 15,35 15,70 15,90 16,40 d,Ǻ 12,99861 10,91510 9,40828 8,34574 7,76181 6,86245 5,98546 5,47121 5,24614 4,92795 4,72001 4,50636 4,33228 4,21042 4,07678 3,85021 3,78557 3,59000 3,42697 3,26666 3,11042 3,03794 2,91219 2,84885 2,81392 2,73038 I 32 16 696 280 296 96 1520 328 704 352 3360 448 1240 2000 760 704 3080 416 728 464 1024 1296 200 376 384 504 Io =I/Imax*100 0,95 0,48 20,71 8,33 8,81 2,86 45,24 9,76 20,95 10,48 100,00 13,33 36,90 59,52 22,62 20,95 91,67 12,38 21,67 13,81 30,48 38,57 5,95 11,19 11,43 15,00 Тр Тр тальк М м+тр Тр м+тр+мкц м+тр+тал. м+тр Тр м+тр Тр м+тр м+тр м+тр м+тр м+тр М м+тр Тр м+тр м+тр Тр м+тр м+тр м+тр 7 94753 8 Продовження таблиці 1 33,70 34,40 35,00 36,10 36,70 38,80 40,40 41,90 43,00 43,40 44,10 45,70 47,30 47,90 50,50 16,85 17,20 17,50 18,05 18,35 19,40 20,20 20,95 21,50 21,70 22,05 22,85 23,65 23,95 25,25 2,65950 2,60697 2,56364 2,48801 2,44870 2,32086 2,23256 2,15605 2,10341 2,08494 2,05346 1,98522 1,92173 1,89905 1,80721 752 440 304 560 240 664 200 192 200 200 504 144 216 192 72 М тр+м м+тр М М М м+тр м+тр м+тр м+тр М м+тр М М Тр 22,38 13,10 9,05 16,67 7,14 19,76 5,95 5,71 5,95 5,95 15,00 4,29 6,43 5,71 2,14 Кристалічний склад триметазидину гигідрохлориду в зазначеному фармацевтичному препараті Таблиця 2 2Ө 6,80 7,90 8,50 9,00 11,40 12,90 13,70 14,30 14,90 16,20 17,00 17,90 18,90 19,80 20,40 21,20 21,70 22,20 23,00 23,60 23,90 24,70 25,20 26,30 27,20 28,10 28,80 29,70 30,40 31,20 31,80 32,80 33,50 34,60 Ө 3,40 3,95 4,25 4,50 5,70 6,45 6,85 7,15 7,45 8,10 8,50 8,95 9,45 9,90 10,20 10,60 10,85 11,10 11,50 11,80 11,95 12,35 12,60 13,15 13,60 14,05 14,40 14,85 15,20 15,60 15,90 16,40 16,75 17,30 Триметазидину дигідрохлорид d,Ǻ I 12,99861 112 11,19098 32 10,40233 32 9,82551 24 7,76181 808 6,86245 264 6,46347 80 6,19359 168 5,94551 400 5,47121 768 5,21550 960 4,95525 416 4,69526 1840 4,48383 408 4,35329 272 4,19079 504 4,09534 584 4,00422 136 3,86672 752 3,76976 1024 3,72311 592 3,60431 176 3,53392 128 3,38856 744 3,27845 1192 3,17546 216 3,09985 864 3,00793 432 2,94025 304 2,86666 320 2,81392 224 2,73038 504 2,67492 136 2,59235 192 Iвідн% 6,09 1,74 1,74 1,30 43,91 14,35 4,35 9,13 21,74 41,74 52,17 22,61 100,00 22,17 14,78 27,39 31,74 7,39 40,87 55,65 32,17 9,57 6,96 40,43 64,78 11,74 46,96 23,48 16,52 17,39 12,17 27,39 7,39 10,43 9 94753 10 Продовження таблиці 2 35,30 36,00 36,90 37,80 38,70 40,60 42,40 43,50 45,40 46,40 48,20 49,30 17,65 18,00 18,45 18,90 19,35 20,30 21,20 21,75 22,70 23,20 24,10 24,65 2,54253 2,49469 2,43588 2,37993 2,32663 2,22203 2,13177 2,08038 1,99764 1,95689 1,88793 1,84835 288 160 248 104 128 200 160 120 40 160 24 64 15,65 8,70 13,48 5,65 6,96 10,87 8,70 6,52 2,17 8,70 1,30 3,48 Кристалічний склад манітолу в зазначеному фармацевтичному препараті Таблиця 3 2Ө 6,20 7,20 10,50 11,60 14,70 16,90 18,80 19,80 20,50 21,20 21,80 23,50 24,80 26,00 26,80 28,40 29,70 31,50 31,90 32,80 33,70 34,50 35,10 36,20 36,70 40,20 42,00 43,00 44,20 45,80 47,30 48,10 Ө 3,10 3,60 5,25 5,80 7,35 8,45 9,40 9,90 10,25 10,60 10,90 11,75 12,40 13,00 13,40 14,20 14,85 15,75 15,95 16,40 16,85 17,25 17,55 18,10 18,35 20,10 21,00 21,50 22,10 22,90 23,65 24,05 d,Ǻ 14,25513 12,27734 8,42499 7,62843 6,02595 5,24614 4,72001 4,48383 4,33228 4,19079 4,07678 3,78557 3,59000 3,42697 3,32646 3,14259 3,00793 2,84004 2,80533 2,73038 2,65950 2,59964 2,55656 2,48136 2,44870 2,24321 2,15114 2,10341 2,04905 1,98112 1,92173 1,89162 Визначені незалежно кристали триметазидину дигідрохлориду мають наступні міжплощинні відстані: d Ǻ=12,99, 10,52, 6,86, 4,93, 3,27, 2,91, 1,81. I 280 80 20 40 60 80 240 3680 280 440 2840 240 1000 1080 40 80 600 60 240 680 440 320 200 160 120 140 200 40 440 160 160 680 I=I/Imax*100 7,61 2,17 0,54 1,09 1,63 2,17 6,52 100,00 7,61 11,96 77,17 6,52 27,17 29,35 1,09 2,17 16,30 1,63 6,52 18,48 11,96 8,70 5,43 4,35 3,26 3,80 5,43 1,09 11,96 4,35 4,35 18,48 Кристалічний склад таблеток триметазидину дигідрохлориду з фіксованою дозою 35 мг, в яких як кристалічний наповнювач використовують манітол і мікрокристалічну целюлозу (мкц) 11 94753 12 Таблиця 4 2Ө 6,70 8,40 9,70 10,50 11,40 12,50 13,00 13,60 14,70 16,20 16,90 18,00 18,80 19,90 20,60 21,50 23,00 23,40 23,80 24,60 25,40 26,20 27,30 28,70 29,60 30,50 31,30 31,80 32,70 33,60 34,40 35,20 36,10 36,80 37,80 38,70 40,50 42,00 42,80 43,50 44,10 45,50 46,30 47,20 48,10 Ө 3,35 4,20 4,85 5,25 5,70 6,25 6,50 6,80 7,35 8,10 8,45 9,00 9,40 9,95 10,30 10,75 11,50 11,70 11,90 12,30 12,70 13,10 13,65 14,35 14,80 15,25 15,65 15,90 16,35 16,80 17,20 17,60 18,05 18,40 18,90 19,35 20,25 21,00 21,40 21,75 22,05 22,75 23,15 23,60 24,05 d,Ǻ 13,18555 10,52048 9,11324 8,42062 7,75778 7,07746 6,80635 6,50739 6,02282 5,46837 5,24342 4,92539 4,71756 4,45921 4,30923 4,13084 3,86472 3,79955 3,73659 3,61686 3,50473 3,39950 3,26497 3,10881 3,01630 2,92931 2,85624 2,81246 2,73708 2,66580 2,60561 2,54821 2,48671 2,44100 2,37869 2,32542 2,22613 2,15003 2,11167 2,07930 2,05239 1,99245 1,95986 1,92457 1,89064 I 56 56 1160 144 592 216 320 264 720 600 664 400 1880 496 784 2840 1000 2000 1600 360 648 376 520 920 480 168 216 176 280 272 152 152 176 136 136 224 200 112 96 144 144 32 40 56 120 Кристалічний склад триметазидину дигідрохлориду у зазначеному фармацевтичному препараті Io =I/Imax*100 1,97 1,97 40,85 5,07 20,85 7,61 11,27 9,30 25,35 21,13 23,38 14,08 66,20 17,46 27,61 100,00 35,21 70,42 56,34 12,68 22,82 13,24 18,31 32,39 16,90 5,92 7,61 6,20 9,86 9,58 5,35 5,35 6,20 4,79 4,79 7,89 7,04 3,94 3,38 5,07 5,07 1,13 1,41 1,97 4,23 тр тр тальк м м+тр м+тр тр м+тр+тал. м+тр+мкц м+тр м+тр тр м+тр тр тр? м+тр м+тр м тр+тальк м ? м тр м м тр м+тр м м+т м м+тр м м м м м м м м м м м+тр м м м 13 94753 14 Таблиця 5 2Ө 6,80 7,90 8,50 9,00 11,40 12,90 13,70 14,30 14,90 16,20 17,00 17,90 18,90 19,80 20,40 21,20 21,70 22,20 23,00 23,60 23,90 24,70 25,20 26,30 27,20 28,10 28,80 29,70 30,40 31,20 31,80 32,80 33,50 34,60 35,30 36,00 36,90 37,80 38,70 40,60 42,40 43,50 45,40 46,40 48,20 49,30 Ө 3,40 3,95 4,25 4,50 5,70 6,45 6,85 7,15 7,45 8,10 8,50 8,95 9,45 9,90 10,20 10,60 10,85 11,10 11,50 11,80 11,95 12,35 12,60 13,15 13,60 14,05 14,40 14,85 15,20 15,60 15,90 16,40 16,75 17,30 17,65 18,00 18,45 18,90 19,35 20,30 21,20 21,75 22,70 23,20 24,10 24,65 Триметазидину дигідрохлорид d,Ǻ I 12,99861 112 11,19098 32 10,40233 32 9,82551 24 7,76181 808 6,86245 264 6,46347 80 6,19359 168 5,94551 400 5,47121 768 5,21550 960 4,95525 416 4,69526 1840 4,48383 408 4,35329 272 4,19079 504 4,09534 584 4,00422 136 3,86672 752 3,76976 1024 3,72311 592 3,60431 176 3,53392 128 3,38856 744 3,27845 1192 3,17546 216 3,09985 864 3,00793 432 2,94025 304 2,86666 320 2,81392 224 2,73038 504 2,67492 136 2,59235 192 2,54253 288 2,49469 160 2,43588 248 2,37993 104 2,32663 128 2,22203 200 2,13177 160 2,08038 120 1,99764 40 1,95689 160 1,88793 24 1,84835 64 Кристалічний склад манітолу в зазначеному фармацевтичному препараті Iвідн% 6,09 1,74 1,74 1,30 43,91 14,35 4,35 9,13 21,74 41,74 52,17 22,61 100,00 22,17 14,78 27,39 31,74 7,39 40,87 55,65 32,17 9,57 6,96 40,43 64,78 11,74 46,96 23,48 16,52 17,39 12,17 27,39 7,39 10,43 15,65 8,70 13,48 5,65 6,96 10,87 8,70 6,52 2,17 8,70 1,30 3,48 15 94753 16 Таблиця 6 2Ө 6,20 7,20 10,50 11,60 14,70 16,90 18,80 19,80 20,50 21,20 21,80 23,50 24,80 26,00 26,80 28,40 29,70 31,50 31,90 32,80 33,70 34,50 35,10 36,20 36,70 40,20 42,00 43,00 44,20 45,80 47,30 48,10 Ө 3,10 3,60 5,25 5,80 7,35 8,45 9,40 9,90 10,25 10,60 10,90 11,75 12,40 13,00 13,40 14,20 14,85 15,75 15,95 16,40 16,85 17,25 17,55 18,10 18,35 20,10 21,00 21,50 22,10 22,90 23,65 24,05 d,Ǻ 14,25513 12,27734 8,42499 7,62843 6,02595 5,24614 4,72001 4,48383 4,33228 4,19079 4,07678 3,78557 3,59000 3,42697 3,32646 3,14259 3,00793 2,84004 2,80533 2,73038 2,65950 2,59964 2,55656 2,48136 2,44870 2,24321 2,15114 2,10341 2,04905 1,98112 1,92173 1,89162 I 280 80 20 40 60 80 240 3680 280 440 2840 240 1000 1080 40 80 600 60 240 680 440 320 200 160 120 140 200 40 440 160 160 680 I=I/Imax*100 7,61 2,17 0,54 1,09 1,63 2,17 6,52 100,00 7,61 11,96 77,17 6,52 27,17 29,35 1,09 2,17 16,30 1,63 6,52 18,48 11,96 8,70 5,43 4,35 3,26 3,80 5,43 1,09 11,96 4,35 4,35 18,48 Кристалічний склад мікрокристалічної целюлози в зазначеному фармацевтичному препараті Таблиця 7 Кут 2θ° Кут Ө° d, A° I імп/c 14,9 16,4 22,50 34,50 7,451 8,2 11,25 17,25 5,945 5.405 3,95 2,60 2120 2120 7360 720 Визначені незалежно кристали триметазидину дигідрохлориду мають наступні міжплощинні відстані: d Ǻ=13,18, 10,52, 6,86, 4,93, 3,27, 2,91, 1,81. Таким чином, більшість показників триметазидину дигідрохлориду в цій ретардній формі відповідає разовому препарату. Кристалічний склад ретардної форми триметазидину дигідрохлориду має Відносна інтенсивність, % 28,8 28,8 100 9,78 додаткову кристалічну фазу з брегівським кутом 2Ө=25,4 і d= 3,505. Кристалічний склад таблеток триметазидину дигідрохлориду з фіксованою дозою 35 мг, в яких як кристалічний наповнювач використовують кальцію гідрофосфат дигідрат 17 94753 18 Таблиця 8 2Ө 6,80 8.40 11,70 15,00 16,20 17,00 17,90 18,40 18,90 19,30 20,00 21,00 21,80 23,50 26,60 27,30 28,80 29,40 30,70 31,40 32,80 34,30 35,60 37,00 39,90 41,70 42,30 43,30 44,90 45,50 47,80 48,60 49,00 50,50 50,80 Ө 3,40 4,20 5,85 7,50 8,10 8,50 8,95 9,20 9,45 9,65 10,00 10,50 10,90 11,75 13,30 13,65 14,40 14,70 15,35 15,70 16,40 17,15 17,80 18,50 19,95 20,85 21,15 21,65 22,45 22,75 23,90 24,30 24,50 25,25 25,40 d,Ǻ 12,99187 10,52048 7,55953 5,90303 5,46837 5,21280 4,95268 4,81921 4,69283 4,59646 4,43714 4,22805 4,07467 3,78361 3,34928 3,26497 3,09824 3,03636 2,91068 2,84737 2,72897 2,61298 2,52049 2,42827 2,25821 2,16480 2,13547 2,08844 2,01767 1,99245 1,90181 1,87235 1,85800 1,80628 1,79631 I 15 24 3960 40 112 175 184 216 352 256 264 1264 224 440 136 120 96 1394 472 80 56 528 64 220 104 304 240 112 80 192 120 256 112 312 144 Io =I/Imax*100 0,38 0,61 100,00 1,01 2,83 4,42 4,65 5,45 8,89 6,46 6,67 31,92 5,66 11,11 3,43 3,03 2,42 35,20 11,92 2,02 1,41 13,33 1,62 5,56 2,63 7,68 6,06 2,83 2,02 4,85 3,03 6,46 2,83 7,88 3,64 Тр Тр кф+тр Кф+тр Тр Тр Тр Тр К Кф Тр кф+тр к кф+тр кф+тр кф кф+тр кф+тр кф+тр кф+тр кф+тр кф+тр кф+тр кф+тр кф+тр кф+тр(н.ф) кф+ тр(н.ф) кф+тр кф кф кф(н.ф) кф(н.ф) кф(н.ф) кф кф Кристалічний склад триметазидину дигідрохлорид у зазначеному фармацевтичному препараті Таблиця 9 2Ө 6,80 7,90 8,50 9,00 11,40 12,90 13,70 14,30 14,90 16,20 17,00 17,90 18,90 Ө 3,40 3,95 4,25 4,50 5,70 6,45 6,85 7,15 7,45 8,10 8,50 8,95 9,45 Триметазидину дигідрохлорид d,Ǻ I 12,99861 112 11,19098 32 10,40233 32 9,82551 24 7,76181 808 6,86245 264 6,46347 80 6,19359 168 5,94551 400 5,47121 768 5,21550 960 4,95525 416 4,69526 1840 Iвідн% 6,09 1,74 1,74 1,30 43,91 14,35 4,35 9,13 21,74 41,74 52,17 22,61 100,00 19 94753 20 Продовження таблиці 9 19,80 20,40 21,20 21,70 22,20 23,00 23,60 23,90 24,70 25,20 26,30 27,20 28,10 28,80 29,70 30,40 31,20 31,80 32,80 33,50 34,60 35,30 36,00 36,90 37,80 38,70 40,60 42,40 43,50 45,40 46,40 48,20 49,30 9,90 10,20 10,60 10,85 11,10 11,50 11,80 11,95 12,35 12,60 13,15 13,60 14,05 14,40 14,85 15,20 15,60 15,90 16,40 16,75 17,30 17,65 18,00 18,45 18,90 19,35 20,30 21,20 21,75 22,70 23,20 24,10 24,65 4,48383 4,35329 4,19079 4,09534 4,00422 3,86672 3,76976 3,72311 3,60431 3,53392 3,38856 3,27845 3,17546 3,09985 3,00793 2,94025 2,86666 2,81392 2,73038 2,67492 2,59235 2,54253 2,49469 2,43588 2,37993 2,32663 2,22203 2,13177 2,08038 1,99764 1,95689 1,88793 1,84835 408 272 504 584 136 752 1024 592 176 128 744 1192 216 864 432 304 320 224 504 136 192 288 160 248 104 128 200 160 120 40 160 24 64 22,17 14,78 27,39 31,74 7,39 40,87 55,65 32,17 9,57 6,96 40,43 64,78 11,74 46,96 23,48 16,52 17,39 12,17 27,39 7,39 10,43 15,65 8,70 13,48 5,65 6,96 10,87 8,70 6,52 2,17 8,70 1,30 3,48 Кристалічний склад кальцію гідрофосфат дигідрат у зазначеному фармацевтичному препараті Таблиця 10 2Ө 11,60 13,10 20,90 23,40 25,60 26,40 28,50 29,30 30,50 31,30 32,50 32,80 34,30 35,80 37,10 39,10 39,60 Ө 5,80 6,55 10,45 11,70 12,80 13,20 14,25 14,65 15,25 15,65 16,25 16,40 17,15 17,90 18,55 19,55 19,80 кальцію гідро фосфат дігідрат d,Ǻ I 7,62843 4200 6,75812 200 4,25026 3120 3,80152 320 3,47960 80 3,37595 1600 3,13179 120 3,04808 3200 2,93083 1360 2,85773 200 2,75490 400 2,73038 360 2,61434 1080 2,50816 120 2,42321 480 2,30374 40 2,27580 120 I=I/Imax*100 100,00 4,76 74,29 7,62 1,90 38,10 2,86 76,19 32,38 4,76 9,52 8,57 25,71 2,86 11,43 0,95 2,86 21 94753 22 Продовження таблиці 10 40,10 41,20 42,00 43,30 44,60 45,40 47,80 48,50 49,20 50,20 50,80 20,05 20,60 21,00 21,65 22,30 22,70 23,90 24,25 24,60 25,10 25,40 2,24857 2,19104 2,15114 2,08953 2,03159 1,99764 1,90279 1,87695 1,85188 1,81731 1,79724 Визначені незалежно кристали триметазидину дигідрохлориду мають наступні міжплощинні відстані: d Ǻ=12,99, 10,52, 5,47, 5,21, 4,95, 4,82, 4,38. В усіх трьох варіантах виконання таблетки на основі твердої матриці мають більші значення інтенсивностей, ніж з гідрофільною матрицею, більш виражений кристалічний склад. Розчинення таблетки відбувається за 12 або 24 години. Дослідження кристалічних складів різних зразків субстанції здійснювали в наступних умовах: дифрактометр ДРОН 3, сцинтиляційний детектор. 360 120 520 560 200 80 240 80 360 280 520 8,57 2,86 12,38 13,33 4,76 1,90 5,71 1,90 8,57 6,67 12,38 о Мідний антикатод =1,5405А , напруга 40 кВ, сила струму 40 мА Розміщення - о Діапазон вимірювань 5-40 Безперервна реєстрація на папері з уточненням положення шляхом точкової реєстрації з часом вимірювання на етапі 10 с. о Приріст перед кожним вимірюванням 0,02 . Тим самим методом дослідженні кристалічні склади запресованих порошків триметазидину дигідрохлориду двох фірм - Sochinas (Швейцарія) і Orgasynth (Франція), які приведені в таблицях 11 і 12. Таблиця 11 Кристалічний склад триметазидину дигідрохлориду фірми Sochinas 2Ө 6,80 7,90 8,50 9,00 11,40 12,90 13,70 14,30 14,90 16,20 17,00 17,90 18,90 19,80 20,40 21,20 21,70 22,20 23,00 23,60 23,90 24,70 25,20 26,30 27,20 28,10 28,80 Ө 3,40 3,95 4,25 4,50 5,70 6,45 6,85 7,15 7,45 8,10 8,50 8,95 9,45 9,90 10,20 10,60 10,85 11,10 11,50 11,80 11,95 12,35 12,60 13,15 13,60 14,05 14,40 Триметазидину дигідрохлорид Sochinas d,Ǻ I 12,99861 112 11,19098 32 10,40233 32 9,82551 24 7,76181 808 6,86245 264 6,46347 80 6,19359 168 5,94551 400 5,47121 768 5,21550 960 4,95525 416 4,69526 1840 4,48383 408 4,35329 272 4,19079 504 4,09534 584 4,00422 136 3,86672 752 3,76976 1024 3,72311 592 3,60431 176 3,53392 128 3,38856 744 3,27845 1192 3,17546 216 3,09985 864 Iвідн% 6,09 1,74 1,74 1,30 43,91 14,35 4,35 9,13 21,74 41,74 52,17 22,61 100,00 22,17 14,78 27,39 31,74 7,39 40,87 55,65 32,17 9,57 6,96 40,43 64,78 11,74 46,96 23 94753 24 Продовження таблиці 11 29,70 30,40 31,20 31,80 32,80 33,50 34,60 35,30 36,00 36,90 37,80 38,70 40,60 42,40 43,50 45,40 46,40 48,20 49,30 14,85 15,20 15,60 15,90 16,40 16,75 17,30 17,65 18,00 18,45 18,90 19,35 20,30 21,20 21,75 22,70 23,20 24,10 24,65 3,00793 2,94025 2,86666 2,81392 2,73038 2,67492 2,59235 2,54253 2,49469 2,43588 2,37993 2,32663 2,22203 2,13177 2,08038 1,99764 1,95689 1,88793 1,84835 432 304 320 224 504 136 192 288 160 248 104 128 200 160 120 40 160 24 64 23,48 16,52 17,39 12,17 27,39 7,39 10,43 15,65 8,70 13,48 5,65 6,96 10,87 8,70 6,52 2,17 8,70 1,30 3,48 Таблиця 12 Кристалічний склад триметазидину дигідрохлориду фірми Orgasynth 2Ө 5,9 6,8 8,0 10,2 11,40 12,2 12,90 13,70 14,30 14,90 16,30 17,00 17,90 18,90 19,90 20,60 21,20 21,70 22,20 23,00 23,50 23,90 24,70 25,20 26,30 27,20 28,80 29,70 30,40 31,20 32,80 33,50 Триметазидину дигідрохлорид фірми Orgasinth Ө d,Ǻ I 2,95 14,98 24 3,4 13,0 160 4,00 11,05 16 5,1 8,67 16 5,70 7,761 1152 6,1 7,25 48 6,45 6,86 64 6,85 6,46 16 7,15 6,19 144 7,45 5,95 128 8,15 5,44 608 8,50 5,22 1288 8,95 4,96 704 9,45 4,7 1840 9,95 4,46 528 10,30 4,31 344 10,60 4,19 248 10,85 4,09 312 11,10 4,00 144 11,50 3,87 456 11,75 3,79 656 11,95 3,72 896 12,35 3,60 136 12,60 3,53 88 13,15 3,39 336 13,60 3,28 824 14,40 3,10 1160 14,85 3,01 416 15,20 2,94 304 15,60 2,87 360 16,40 2,73 336 16,75 2,67 96 І відн.% 1,3 8,7 0,9 0,9 62,6 2,6 3,5 0,9 7,8 6,96 33,0 70,0 38,3 100,00 28,7 18,7 13,5 17,0 7,8 24,8 35,6 48,7 7,4 4,8 18,3 44,8 63,0 22,6 13,9 19,6 18,3 5,2 25 94753 26 Продовження таблиці 12 34,60 35,50 36,00 36,90 37,80 38,40 38,9 40,60 42,50 43,50 45,30 46,60 47,20 48,30 49,50 17,30 17,75 18,00 18,45 18,90 19,20 19,45 20,30 21,25 21,75 22,65 23,30 23,60 24,15 24,75 2,59 2,54 2,49 2,44 2,39 2,34 2,32 2,22 2,13 2,08 2,00 1,95 1,93 1,88 1,84 Порівняння таблиць показує, що триметазидину дигідрохлорид немає поліморфізму. Отримані дані можуть бути основою для дослідження, в яких структури субстанції можуть визначати відтворюваність технологічного процесу та їх вплив на фізико-механічні властивості таблетки. При виготовлені лікарських таблетованих форм використовували кристалічні допоміжні речовини, які мають інші кристалофізичні властивості. Кристалічні структури цих допоміжних речовин, одержані при тих же умовах експерименту. 296 288 144 280 64 152 160 256 1440 104 40 184 56 40 72 16.1 15,65 7,8 15,2 3,5 8,3 8,7 13,9 7,8 5,7 2,2 10,0 3,0 2,2 3,9 Мікрокристалічна целюлоза найчастіше самостійно не відтворюється в кристалічних структурах таблеток, а разом з іншими аморфними допоміжними речовинами впливає на висоту окремих груп піків над базовою лінією дифрактограми в деяких діапазонах кутів, відповідаючи положенням максимумів на дифрактограмі цієї допоміжної речовини. В таблиці 13 наведений кристалічний склад таблеток „Тридуктан 20 мг”, які виготовляються ВАТ „Фарма Старт”. Таблиця 13 2Ө 6,80 8,10 9,40 10,60 11,40 12,90 14,80 16,20 16,90 18,00 18,80 19,70 20,50 21,10 21,80 23,10 23,50 24,80 26,00 27,30 28,70 29,40 30,70 31,40 31,80 32,80 Ө 3,40 4,05 4,70 5,30 5,70 6,45 7,40 8,10 8,45 9,00 9,40 9,85 10,25 10,55 10,90 11,55 11,75 12,40 13,00 13,65 14,35 14,70 15,35 15,70 15,90 16,40 Тридуктан, табл 20 мг, Sochinas d,Ǻ I Io =I/Imax*100 12,99861 32 0,95 10,91510 16 0,48 9,40828 696 20,71 8,34574 280 8,33 7,76181 296 8,81 6,86245 96 2,86 5,98546 1520 45,24 5,47121 328 9,76 5,24614 704 20,95 4,92795 352 10,48 4,72001 3360 100,00 4,50636 448 13,33 4,33228 1240 36,90 4,21042 2000 59,52 4,07678 760 22,62 3,85021 704 20,95 3,78557 3080 91,67 3,59000 416 12,38 3,42697 728 21,67 3,26666 464 13,81 3,11042 1024 30,48 3,03794 1296 38,57 2,91219 200 5,95 2,84885 376 11,19 2,81392 384 11,43 2,73038 504 15,00 Тр Тр Тальк М М+тр Тр м+тр+мкц м+тр+тал. м+тр Тр м+тр Тр м+тр м+тр м+тр м+тр м+тр М м+тр Тр м+тр м+тр Тр м+тр м+тр м+тр 27 94753 28 Продовження таблиці 13 33,70 34,40 35,00 36,10 36,70 38,80 40,40 41,90 43,00 43,40 44,10 45,70 47,30 47,90 50,50 16,85 17,20 17,50 18,05 18,35 19,40 20,20 20,95 21,50 21,70 22,05 22,85 23,65 23,95 25,25 2,65950 2,60697 2,56364 2,48801 2,44870 2,32086 2,23256 2,15605 2,10341 2,08494 2,05346 1,98522 1,92173 1,89905 1,80721 752 440 304 560 240 664 200 192 200 200 504 144 216 192 72 22,38 13,10 9,05 16,67 7,14 19,76 5,95 5,71 5,95 5,95 15,00 4,29 6,43 5,71 2,14 М тр+м м+тр М М М м+тр м+тр м+тр м+тр М м+тр М М Тр В таблиці 14 наведений кристалічний склад таблеток Предуктал фірми SERVIER Таблиця 14 2Ө 6,70 8,50 9,40 10,50 11,40 12,80 14,70 16,20 16,90 17,90 18,80 19,80 20,60 21,20 21,80 23,50 24,80 25,30 26,00 27,20 28,70 29,60 30,50 31,30 31,80 32,80 33,70 34,40 35,00 36,10 36,80 38,70 40,40 40,80 42,00 Ө 3,35 4,25 4,70 5,25 5,70 6,40 7,35 8,10 8,45 8,95 9,40 9,90 10,30 10,60 10,90 11,75 12,40 12,65 13,00 13,60 14,35 14,80 15,25 15,65 26,48 16,40 16,85 17,20 17,50 18,05 18,40 19,35 20,20 20,40 21,00 Предуктал, табл 20 мг d,Ǻ I 13,18127 32 10,39355 32 9,40035 784 8,41789 416 7,75526 248 6,91000 120 6,02087 1392 5,46660 312 5,24172 672 4,95107 416 4,71603 3960 4,48005 448 4,30784 1240 4,18725 1920 4,07334 752 3,78238 4080 3,58698 408 3,51721 248 3,42408 560 3,27568 416 3,10780 1128 3,01532 1096 2,92836 176 2,85532 336 1,72746 464 2,72808 408 2,65725 744 2,60477 320 2,56148 240 2,48591 432 2,44021 200 2,32467 760 2,23068 160 2,20973 120 2,14933 144 Io =I/Imax*100 0,78 0,78 19,22 10,20 6,08 2,94 34,12 7,65 16,47 10,20 97,06 0,11 30,39 47,06 18,43 100,00 10,00 6,08 13,73 10,20 27,65 26,86 4,31 8,24 11,37 10,00 18,24 7,84 5,88 10,59 4,90 18,63 3,92 2,94 3,53 Тр М+тр Тальк М М+тр Тр М+тр+мкц М+тр+тал. М+тр Тр М+тр Тр М+тр М+тр М+тр М+тр М Тр М+тр Тр М+тр М+тр тр Тр+ м М+тр М+ тр М М М М М М М+тр М+тр М+тр 29 94753 30 Продовження таблиці 14 43,00 43,50 44,20 45,00 47,30 48,00 21,50 21,75 22,10 22,50 23,65 24,00 2,10163 2,07863 2,04732 2,01276 1,92011 1,89373 192 168 672 95 160 176 Обидва препарати Предуктал SERVIER, Франція, та Тридуктан ВАТ „Фарма Старт”, Україна, виготовляються методом вологої грануляції при використанні розчину полівінілпиролідону. Незважаючи на те, що триметазидину дигідрохлорид немає поліморфних форм, маси для таблету 4,71 4,12 16,47 2,33 3,92 4,31 М+тр М+тр М М+тр М М вання під час грануляції піддаються дії підвищеної температури і вологості, що може бути причиною утворення додаткових структурних фаз. Тому були виготовлені таблетки методом прямого пресування, кристалічний склад яких наведений в наступній таблиці 15. Таблиця 15 2Ө 6,80 8,10 9,40 10,50 11,40 12,90 14,80 16,20 16,90 18,00 18,80 19,70 20,50 21,10 21,80 23,10 23,50 24,80 26,00 27,30 28,70 29,40 30,50 31,40 31,80 32,80 33,70 34,40 35,00 36,10 36,70 38,80 40,40 41,90 43,00 43,40 44,10 45,70 47,30 47,90 50,50 Ө 3,40 4,05 4,70 5,25 5,70 6,45 7,40 8,10 8,45 9,00 9,40 9,85 10,25 10,55 10,90 11,55 11,75 12,40 13,00 13,65 14,35 14,70 15,25 15,70 15,90 16,40 16,85 17,20 17,50 18,05 18,35 19,40 20,20 20,95 21,50 21,70 22,05 22,85 23,65 23,95 25,25 Тридуктан, табл. 20 мг, пряме пресування d,Ǻ I Io =I/Imax*100 12,99861 48 1,38 10,91510 32 0,92 9,40828 1248 35,86 8,42499 272 7,82 7,76181 296 8,51 6,86245 72 2,07 5,98546 1468 42,18 5,47121 220 6,32 5,24614 728 20,92 4,92795 208 5,98 4,72001 3480 100,00 4,50636 344 9,89 4,33228 1384 39,77 4,21042 2000 57,47 4,07678 936 26,90 3,85021 608 17,47 3,78557 3360 96,55 3,59000 408 11,72 3,42697 668 19,20 3,26666 400 11,49 3,11042 1176 33,79 3,03794 1152 33,10 2,93083 176 5,06 2,84885 368 10,57 2,81392 360 10,34 2,73038 472 13,56 2,65950 808 23,22 2,60697 480 13,79 2,56364 280 8,05 2,48801 560 16,09 2,44870 200 5,75 2,32086 792 22,76 2,23256 160 4,60 2,15605 192 5,52 2,10341 200 5,75 2,08494 208 5,98 2,05346 592 17,01 1,98522 176 5,06 1,92173 248 7,13 1,89905 176 5,06 1,80721 80 2,30 Тр Тр Тальк М м+тр Тр м+тр+мкц м+тр+тал. м+тр Тр м+тр Тр м+тр м+тр м+тр м+тр м+тр М м+тр Тр м+тр м+тр Тр Тр м+тр м+тр М Тр+м м+тр М М М м+тр м+тр м+тр м+тр М м+тр М М Тр 31 94753 Манітол як допоміжну речовину використовують також в твердій матриці для ретардної форми триметазидину дигідрохлориду [патент UA 12297, А61К 31/495, 2006]. Таблетки Тридуктан МВ мають такий вміст: діючу речовину триметазидину дигідрохлорид у кількості 15-30 мас.%, переважно 17,525 % від маси таблетки - ядра, мікрокристалічну целюлозу в кількості 10-17 %, переважно 12-14 % 32 від маси таблетки - ядра, поліметакрилат, який незалежно від РН повільно пропускає водні розчини, в кількості 18-27 %, переважно 20-26 % від маси таблетки, як гідрофобні полімери використовуються різні види восків в кількості 20-31 % загальної маси таблетки - ядра. Кристалічний склад цього препарату наведений в таблиці 16. Таблиця 16 2Ө 6,70 8,40 9,70 10,50 11,40 12,50 13,00 13,60 14,70 16,20 16,90 18,00 18,80 19,90 20,60 21,50 23,00 23,40 23,80 24,60 25,40 26,20 27,30 28,70 29,60 30,50 31,30 31,80 32,70 33,60 34,40 35,20 36,10 36,80 37,80 38,70 40,50 42,00 42,80 43,50 44,10 45,50 46,30 47,20 48,10 Ө 3,35 4,20 4,85 5,25 5,70 6,25 6,50 6,80 7,35 8,10 8,45 9,00 9,40 9,95 10,30 10,75 11,50 11,70 11,90 12,30 12,70 13,10 13,65 14,35 14,80 15,25 15,65 15,90 16,35 16,80 17,20 17,60 18,05 18,40 18,90 19,35 20,25 21,00 21,40 21,75 22,05 22,75 23,15 23,60 24,05 Тридуктан - МВ, табл 35 мг, Sochinas d,Ǻ I 13,18555 56 10,52048 56 9,11324 1160 8,42062 144 7,75778 592 7,07746 216 6,80635 320 6,50739 264 6,02282 720 5,46837 600 5,24342 664 4,92539 400 4,71756 1880 4,45921 496 4,30923 784 4,13084 2840 3,86472 1000 3,79955 2000 3,73659 1600 3,61686 360 3,50473 648 3,39950 376 3,26497 520 3,10881 920 3,01630 480 2,92931 168 2,85624 216 2,81246 176 2,73708 280 2,66580 272 2,60561 152 2,54821 152 2,48671 176 2,44100 136 2,37869 136 2,32542 224 2,22613 200 2,15003 112 2,11167 96 2,07930 144 2,05239 144 1,99245 32 1,95986 40 1,92457 56 1,89064 120 Io =I/Imax*100 1,97 1,97 40,85 5,07 20,85 7,61 11,27 9,30 25,35 21,13 23,38 14,08 66,20 17,46 27,61 100,00 35,21 70,42 56,34 12,68 22,82 13,24 18,31 32,39 16,90 5,92 7,61 6,20 9,86 9,58 5,35 5,35 6,20 4,79 4,79 7,89 7,04 3,94 3,38 5,07 5,07 1,13 1,41 1,97 4,23 Тр Тр тальк М м+тр м+тр тр м+тр+тал. м+тр+мкц м+тр м+тр тр м+тр тр тр? м+тр м+тр М тр+тальк М Тр М Тр М М Тр м+тр М м+т М м+тр М М М М М М М М М М м+тр М М М 33 94753 В препараті фірми SERVIER Предуктал MR інша допоміжна кристалічна речовина, і кристаліч 34 ний склад має значення, наведені в таблиці 17 Таблиця 17 2Ө 6,80 8.40 11,70 15,00 16,20 17,00 17,90 18,40 18,90 19,30 20,00 21,00 21,80 23,50 26,60 27,30 28,80 29,40 30,70 31,40 32,80 34,30 35,60 37,00 39,90 41,70 42,30 43,30 44,90 45,50 47,80 48,60 49,00 50,50 50,80 Ө 3,40 4.20 5,85 7,50 8,10 8,50 8,95 9,20 9,45 9,65 10,00 10,50 10,90 11,75 13,30 13,65 14,40 14,70 15,35 15,70 16,40 17,15 17,80 18,50 19,95 20,85 21,15 21,65 22,45 22,75 23,90 24,30 24,50 25,25 25,40 Предуктал - МR, табл 35 мг d,Ǻ I 12,99187 15 10.52048 24 7,55953 3960 5,90303 40 5,46837 112 5,21280 175 4,95268 184 4,81921 216 4,69283 352 4,59646 256 4,43714 264 4,22805 1264 4,07467 224 3,78361 440 3,34928 136 3,26497 120 3,09824 96 3,03636 1394 2,91068 472 2,84737 80 2,72897 56 2,61298 528 2,52049 64 2,42827 220 2,25821 104 2,16480 304 2,13547 240 2,08844 112 2,01767 80 1,99245 192 1,90181 120 1,87235 256 1,85800 112 1,80628 312 1,79631 144 В цій кристалічній структурі з׳являються деякі відміни від сумішей компонентів, які утворюють таблетку. По-перше, максимальне значення інтенсивності визначається в таблетках при іншому куті випромінювання, ніж в окремих компонентах, подруге, відносні значення інтенсивностей тримета Io =I/Imax*100 0,38 0.61 100,00 1,01 2,83 4,42 4,65 5,45 8,89 6,46 6,67 31,92 5,66 11,11 3,43 3,03 2,42 35,20 11,92 2,02 1,41 13,33 1,62 5,56 2,63 7,68 6,06 2,83 2,02 4,85 3,03 6,46 2,83 7,88 3,64 Тр Тр кф+тр Кф+тр Тр Тр Тр Тр К Кф Тр кф+тр К кф+тр кф+тр Кф кы+тр кф+тр кф+тр кф+тр кф+тр кф+тр кф+тр кф+тр кф+тр кф+тр(н.ф) кф+ тр(н.ф) кф+тр Кф Кф кф(н.ф) кф(н.ф) кф(н.ф) Кф Кф зидину дигідрохлориду значно нижчі, ніж для суми інгредієнтів триметазидину дигідрохлориду і кальцію гідрофосфату дигідрат. Аналіз наведених кристалічних складів показує, що триметазидину дигідрохлорид незалежно відтворюється в препаратах при наступних умовах Таблиця 18 Предуктал 20мг 2Ө 6,7 12,80 17,92 27,2 30,5 dǺ 13,18 6,91 4,95 3,27 2,92 I від % 0,78 2,94 10,20 10,20 4,31 35 94753 36 Продовження таблиці 18 Тридуктан 20мг Тридуктан пряме пресування Тридуктан МВ Предуктал МR У кристалічній структурі тридуктану МВ з׳являється нове значення для незалежного відтворення діючої речовини, яке має значну відносну інтенсивність і може бути показником відмінності даного препарату від препаратів разової дії. Цей результат може бути доказом того, що в цій системній матриці існують нові кристалічні фази. Важливе значення має можливість прогнозування розчинення таблеток триметазидину дигідрохлориду за результатами ренгеноструктурного аналізу для створення методів не руйнуючого контролю для запобігання фальсифікації препарату та для прогнозування якості таблеток в критичних зонах технологічного режиму. Таке рішення стало 6,8 12,9 18,0 27,3 30,70 50,50 6,8 8,1 12,9 18,0 27,3 30,50 50,5 6,7 8,1 13,0 18,0 25,4 27,3 30,5 6,8 8,4 16,2 17,00 17,90 20,00 12,99 6,86 4,93 3,26 2,91 1,80 12,99 10,91 6,86 4,92 3,26 2,93 1,80 13,18 10,5 6,81 4,92 3,50 3,26 2,93 12,99 10,52 5,47 5,21 4,95 4,44 0,95 2,86 10,48 13,81 5,95 2,14 1,38 0,92 2,07 5,98 11,49 5,06 2,30 1,97 1,97 11,2 14,08 22,8 18,31 5,06 10,38 0,61 2,42 4,42 4,65 6,62 можливим за рахунок аналізу інтенсивності випромінювання. Для різних видів таблеток триметазидину гідрохлориду існують такі вимоги розчинення: для таблеток по 20 мг за 45 хвилин повинно перейти в розчин не менш як 75 % триметазидину. Для таблеток пролонгованої дії "ретард" по 35 мг у розчин повинно перейти: за 1 годину 25-45 %, за 2 години 43-63%, за 8 годин не менш ніж 80%. Значення інтенсивностей триметазидину дигідрохлориду у вищенаведених кристалічних структурах для таблеток, які виготовлені з однієї субстанції і допоміжних речовин, наведені в таблиці 19. Таблиця 19 2Ө Триметазидин субстанція 6,8 12,9 18,0 27,3 30,7 112 264 416 1192 304 2Ө Манітол Інтенсивність триметазидину Разрахункова в Таблетках Разов дії ретард 23 26 53 60 83 94 240 270 Інтенсивність манітолу Разрахункова в Таблетках Разов дії ретард Тридуктан 20 мг Предуктал 32 96 352 464 200 32 120 416 416 176 Тридуктан 20 мг Предуктал 20мг Тридуктан Тридуктан МВ 20 мг 35мг Пряме пресув. 48 56 76 320 203 460 400 520 176 176 Тридуктан 20мг Тридуктан МВ Пряме пре35мг сув 37 94753 38 Продовження таблиці 19 10,5 24,8 33,7 35,00 36,1 36,8 38,7 47,3 48,0 20 1000 440 200 160 120 Відсутня 160 680 2Ө Манітол Тридуктан 11,4 14,7 16,9 18,8 20,6 21,2 21,8 23,5 26,0 28,7 29,6 31,3 31,8 32,8 34,4 35,0 40,4 42,0 43,0 43,5 8 Відсут. 340 90 150 40 70 10 55 Відсут. 42 Відсут. Відсут. 55 Відсут. 230 60 Інтенсивність манітолу з Тридуктаном Разрахункова в Таблетках Разов дії ретард 176 180 100 96 220 224 450 442 150 60 250 200 1083 470 257 112 367 120 232 248 290 274 84 40 125 100 330 161 174 100 90 72 80 60 20 20 20 20 Доза триметазидину дигідрохлориду в таблетках разової дії дорівнює 20 % і 22,5 %, тобто інтенсивність в таблетках разової дії в 1,5-2,0 рази перевищує теоретичне значення інтенсивності, а в таблетках ретардної дії в 2,5-3,0 рази вище. В таблетках Предуктал MR, в яких використовується кальцію гірофосфат дигідрат, значення інтенсивності значно нижчі ніж теоретичні. Показники манітолу, наведені в таблиці 8, показують, що їх значення в таблетках значно вищі, ніж в самому манітолі, запресованому в таблетку окремо, без інших компонентів. Якщо взяти до уваги інтенсивність випромінювання, розраховану на кількість манітолу в таблетці, то такий ефект спостерігається для більшості брегівських кутів манітолу, окрім 2Ө=48º. Але в ретардній формі інтенсивність манітолу значно менша, ніж в препаратах разової дії, причому інтенсивність в таблетках, одержаних прямім пресуванням, не відрізняється від таблеток, одержаних вологою грануляцією. Тобто часткове розчинення, механічні впливи, потім сушка не впливають на розподіл кристалічних фаз. Фази, які містять кристали триметазидину і манітолу з однаковими міжплощинними відстанями і в таблетках об'єднуються, теж мають інтенсивності, значно вищі, ніж можна очікувати з правила 280 416 752 304 560 240 664 216 192 416 408 176 240 432 200 760 160 176 Тридуктан 20 мг Предуктал 20мг 296 1520 704 3360 1240 2000 760 3080 728 1024 1296 376 384 504 440 304 160 192 200 200 248 1392 672 3960 1240 1920 752 4080 560 1128 1096 336 464 408 440 300 200 144 192 162 272 408 808 280 560 200 792 248 176 144 360 272 20 176 136 224 56 120 Тридуктан 20мг Тридуктан МВ Пряме пре35мг сув 296 1468 728 3480 1384 2000 936 3360 668 1176 1152 368 360 472 480 208 160 192 200 208 592 720 664 1880 784 2840 2000 376 920 480 216 176 280 152 152 200 112 96 144 адитивності. В ретардному препараті інтенсивності для цих фаз менші, ніж для препаратів разової дії, крім фази з 2Ө=11,4. Крім того, в ретардному препараті з׳являється нова кристалічна фаза, яка існує тільки в препараті з манітолом при 2Ө=25,4. Проведений аналіз свідчить, що утворені в таблетках триметазидину дигідрохлориду структури являються самостійними структурами діючої речовини з кристалічними допоміжними речовинами. Ці структури можна використовувати для контролю за виробництвом, прогнозування розчинності діючої речовини та безруйнівного контролю для запобігання фальсифікації. В літературі добре відомий факт того, що аморфна форма лікарської речовини має більшу розчинність, ніж кристалічна. Відомо, що аморфна форма не дає виражених значень як відносної, так абсолютної інтенсивностей. Аналіз відносної та абсолютної інтенсивності наведеної у таблиці 8, 9 показує, що значення інтенсивності для триметазидину в ретардних формах при незалежному його визначенні значно вище, ніж розраховані за правилами адитивності, і вищі, ніж в таблетках швидкого вивільнення. Таблетки Предукталу MR мають менші значення інтенсивності, ніж таблетки Тридуктану МВ. Таким чином, ці дані показують, що тверда матриця, яка покладена в основу Тридуктану 39 94753 МВ, має більшу кристалічність, ніж гідрофільна матриця Предукталу MR, вищі значення відносної та абсолютної інтенсивності, що вивільнення в Комп’ютерна верстка А. Крулевський 40 такий матриці може бути більш продовженим і досягати 24 годин. Підписне Тираж 24 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for determination of quality of pharmaceutical preparations of cardiovascular effect on basis of trimetazidine dihydrochloride in crystalline form
Автори англійськоюShteinhart Mark Volfovych, Prykhodko Roman Mykolaiovych
Назва патенту російськоюСпособ определения качества фармацевтических препаратов сердечно-сосудистого действия на основе триметазидина дигидрохлорида в кристаллической форме
Автори російськоюШтейнгарт Марк Вольфович, Приходько Роман Николаевич
МПК / Мітки
МПК: G01N 33/15, G01N 23/207
Мітки: якості, серцево-судинної, спосіб, триметазидину, визначення, основі, фармацевтичних, форми, препаратів, кристалічний, дії, дигідрохлориду
Код посилання
<a href="https://ua.patents.su/20-94753-sposib-viznachennya-yakosti-farmacevtichnikh-preparativ-sercevo-sudinno-di-na-osnovi-trimetazidinu-digidrokhloridu-u-kristalichnijj-formi.html" target="_blank" rel="follow" title="База патентів України">Спосіб визначення якості фармацевтичних препаратів серцево-судинної дії на основі триметазидину дигідрохлориду у кристалічній формі</a>
Попередній патент: Прокатний стан для обробки безшовних труб
Випадковий патент: Спосіб одержання системи зубних елайнерів "easy align" для корекції зубощелепних аномалій