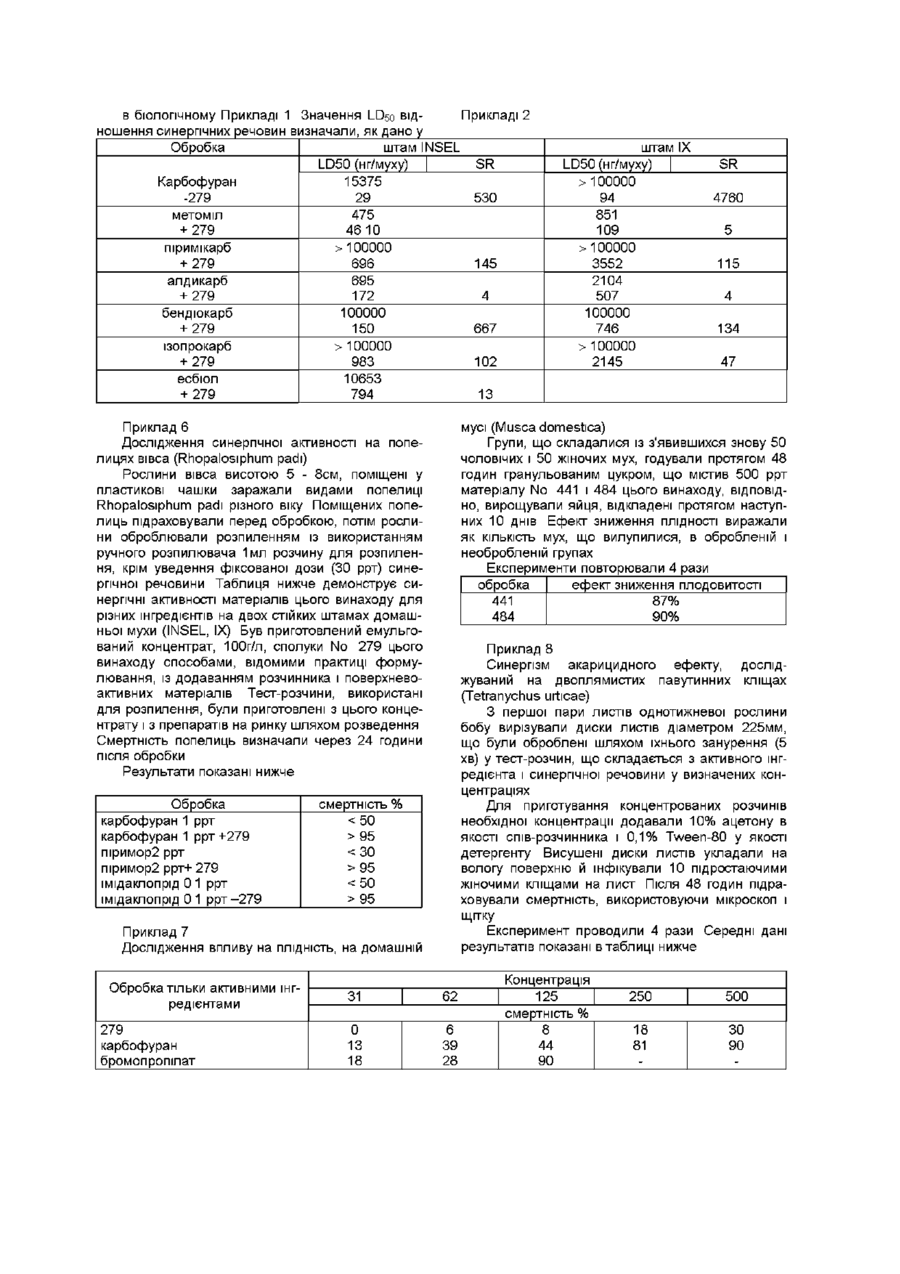
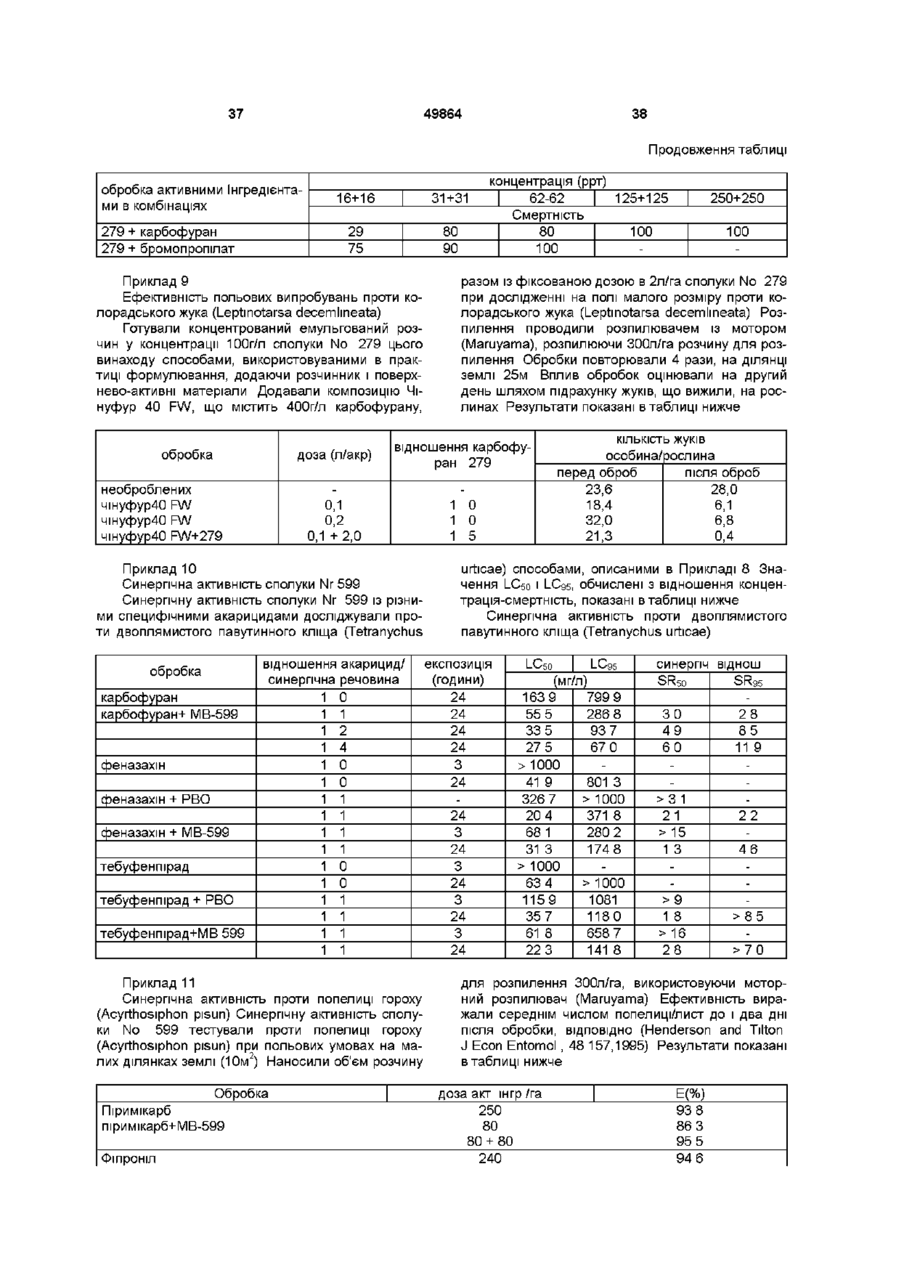
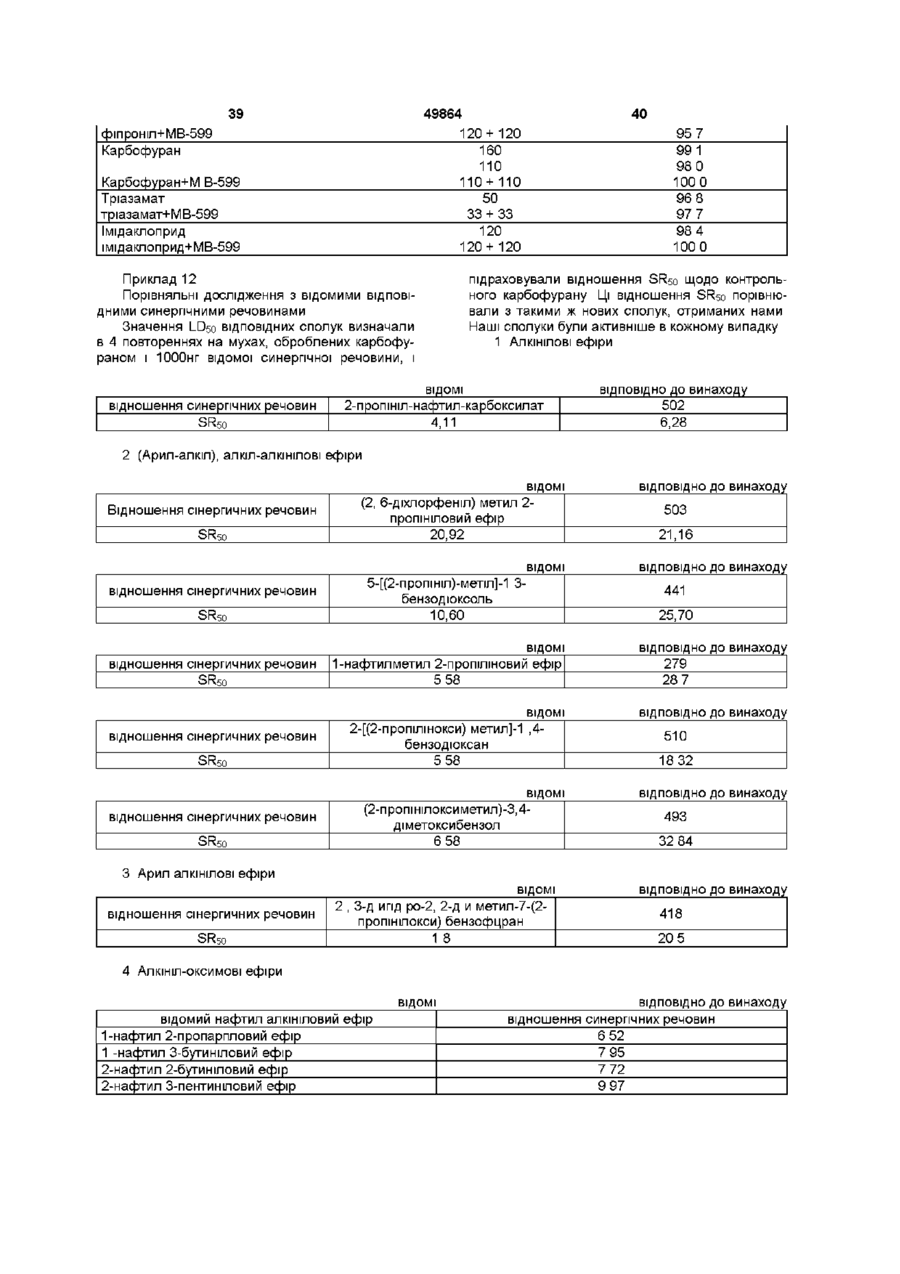
Пестицидні сполуки, спосіб їх одержання, композиції на їх основі та спосіб знищення паразитів
Номер патенту: 49864
Опубліковано: 15.10.2002
Автори: БЕРТОК Бела, Цудор Ірен, Чіз Ласло, Арваі Геза, ПАП Ласло, Баконьварі Ільдіко, Секей Іштван, Куруцне Р.Жужа
Формула / Реферат
1. Сполуки загальної формули І, їх оптично активні ізомери й солі
,I
де
Аr - аліциклічний, ароматичний або гетероциклічний замісник, що містить один або більшу кількість гетероатомів і який, необов'язково, заміщений одним або декількома алкокси-, метилендіокси-, алкіл-, галоген-, галоалкіл- або нітрогрупами і/або конденсований з бензольним кільцем,
R1, R2 - незалежно, Н, алкіл, алкеніл, галоалкіл, феніл, заміщений феніл, циклоалкіл,
R3, R4 - незалежно, Н, алкіл, алкеніл, галоалкіл, феніл, заміщений феніл, циклоалкіл, або
R3, R4 є, разом, =O,
Υ – С, РО або
YR3R4 разом -CR9=N-група,
X - -O-,-NR10-,
R9 - Н, алкіл, феніл, заміщений феніл,
R10 - Н, алкіл,
R5, R6, R7, R8 є, незалежно, Н, алкілом, алкенілом, галоалкілом або
Ar-(CR1R2)m-(YR3R4)n-X- разом утворюють карбоксимідну групу,
Е - Н, галоген, метил,
m - 0, 1, 2,
n - 0, 1,
o - 0, 1, 2,
p - 0, 1, 2,
за умови, що сума атомів або груп -(CR1R2)m-(YR3R4)n-X-(CR5R6)o-(CR7R8)p місткового скелета дорівнює 3 і скелет утворює з атомами містка лінійний ланцюг, що складається з 6 атомів та закінчується, переважно, метильною групою,
з наступною умовою, що коли Аr відповідає нафтильній групі, Υ означає С-атом, Χ означає O-атом, R3 і R4 спільно не можуть означати =O.
2. Сполуки загальної формули ІА і їх оптично активні ізомери
,IA
де Аr, R1, R2 R5, R6, R7, R8, Y, Е, m, o і p мають значення, вказані в пункті 1.
3. Сполуки загальної формули IВ і їх оптично активні ізомери
,IB
де Аr, R1, R2, R5, R6, R7, R8, R10, Y, Е, m, о і p мають значення, вказані в пункті 1.
4. Сполуки загальної формули IC і їх оптично активні ізомери
,IC
де Аr, R1, R2, R3, R4, R5, R6, R7, R8, Е, m, n, о і p мають значення, вказані в пункті 1.
5. Сполуки загальної формули ID і їх солі і оптично активні ізомери
,ID
де Аr, R1, R2, R3, R4, R5, R6, R7, R8, R10, Е, m, n, о і p мають значення, вказані в пункті 1.
6. Сполуки загальної формули ІЕ і їх солі і оптично активні ізомери
,IE
де Аr, R1, R2, R3, R4, R5, R6, R7, R8, R10, Е, m, n, о і p мають значення, вказані в пункті 1.
7. Сполуки загальної формули IF і їх оптично активні ізомери,
,IF
де Аr, R1, R2, R5, R6, R7, R8, R9, Е, m, о і p мають значення, вказані в пункті 1.
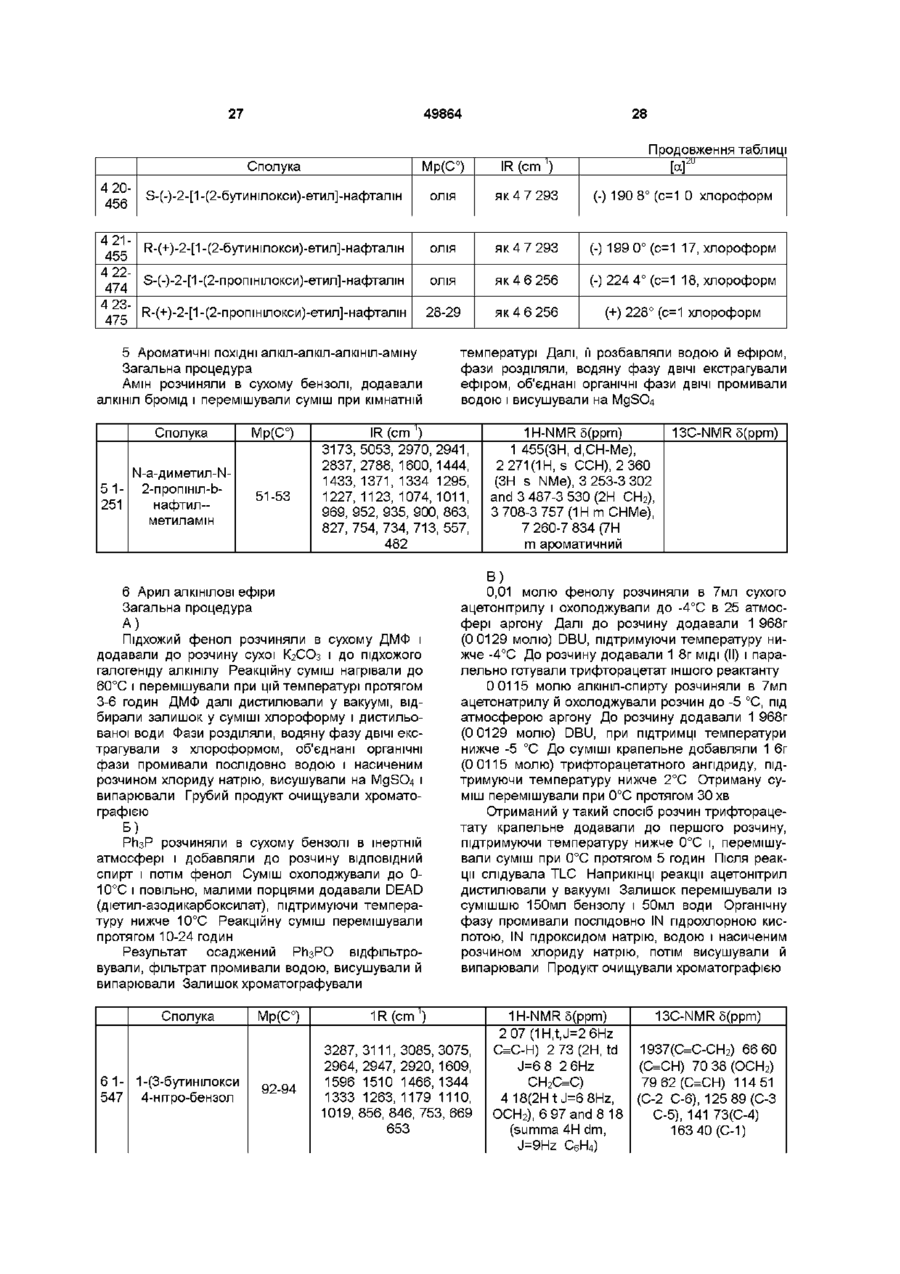
8. Сполуки згідно з пунктом 1,
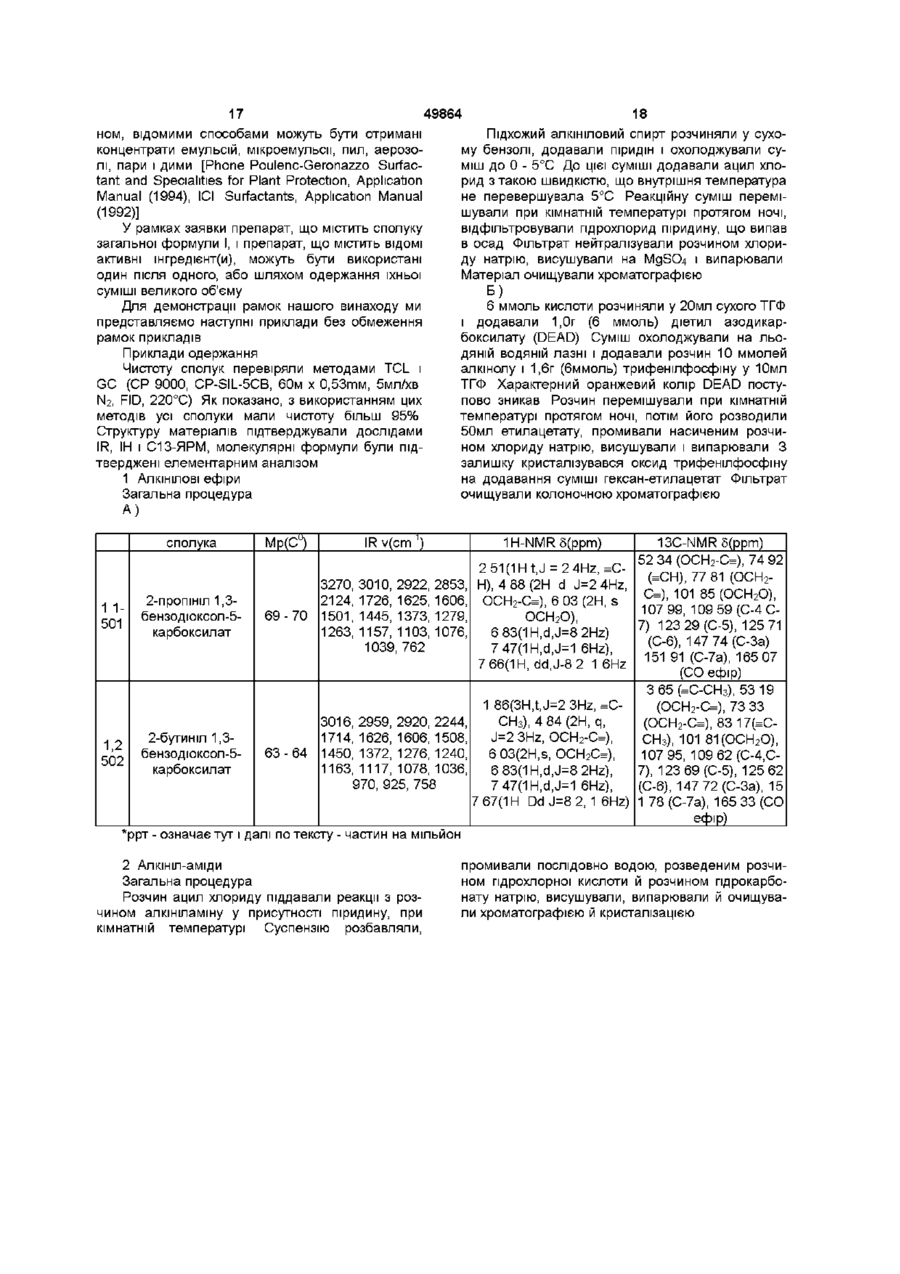
1-нафтилметил-2-бутиніловий етер,
2-пропініл-1,3-бензодіоксол-5-карбоксилат,
1-[(2-бутинілоксі)етил]-3,4-диметоксибензол,
2,6-дихлор-1-(2-бутинілоксиметил)бензол,
1-[1-(2-бутинілокси)пропіл]нафталін,
R-(+)-2-[1-(2-бутинілоксі)етил]нафталін,
5-[(бут-2-инілокси)метил]-1,3-бензодіоксол,
5-[2-метил-1-(2-бутинілокси)пропіл]-1,3-бензодіоксол,
5-[(бут-2-инілокси)фенілметил]-1,3-бензодіоксол,
2-[(2-бутинілокси)метил]-1,4-бензодіоксан,
2,3-дигідро-2,2-диметил-7-(3-пентилокси)бензофуран.
9. Спосіб одержання сполук загальної формули І
,I
де Аr, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, Χ, Υ, Е, m, n, о і p мають значення, вказані в пункті 1, який характеризується тим, що
а) для одержання сполук загальної формули ІА, де Аr, R1, R2, R5, R6, R7, R8, Y, Е, m, о і p мають значення, вказані в пункті 1, піддають взаємодії сполуки загальної формули II і III
,II
,III
де Аr, R1, R2, R5, R6, R7, R8, Y, Е, m, о і p мають значення, вказані в пункті 1, А і В є групами, придатними для утворення естерного зв'язку,
б) для одержання сполук загальної формули IВ, де Аr, R1, R2, R5, R6, R7, R8, R10, Y, Е, m, о і p мають значення, вказані в пункті 1, піддають взаємодії сполуки загальної формули IV і V
,IV
,V
де Аr, R1, R2, R5, R6, R7, R8, Y, Е, m, о і p мають значення, вказані в пункті 1, і С і D є групами, придатними для утворення амідного зв'язку,
в) для одержання сполук загальної формули IC, де Аr, R1, R2, R5, R6, R7, R8, Е, m, n, ο і p мають значення, вказані в пункті 1, R3 і R4, незалежно, означають Н, алкіл, алкеніл, галоалкіл, феніл, заміщений феніл, піддають взаємодії сполуки загальної формули VI і VII
,VI
,VII
де Аr, R1, R2, R5, R6, R7, R8, Е, m, n, о і p мають значення, вказані в пункті 1, R3 і R4, незалежно, означають Н, алкіл, алкеніл, галоалкіл, феніл, заміщений феніл, F і G є групами, придатними для утворення етерного зв'язку,
г) для одержання сполук загальної формули ID, де Ar-(CR1R2)m-(CR3R4)n-N є карбоксимідною групою, R5, R6, R7, R8, Е, о і p мають значення, вказані в пункті 1, карбоксимід загальної формули VIII піддають реакції із сполукою загальної формули IX
,VIII
,IX
де R5, R6, R7, R8, Е, о і p мають значення, вказані в пункті 1, і Lg є групою, що відходить,
д) для одержання сполук загальної формули ІЕ, де Аr, R1, R2, R3, R4, R5, R6, R7, R8, R10, Е, m, n, о і p мають значення, вказані в пункті 1, піддають взаємодії сполуки загальної формули X і XI
,X
,XI
де Аr, R1, R2, R3, R4, R5, R6, R7, R8, Е, m, n, о і p мають значення, вказані в пункті 1, Η і І являють собою групи, придатні для утворення
групи, де R10 має те ж значення, як визначено в пункті 1,
е) для одержання сполук загальної формули IF, де Аr, R1, R2, R5, R6, R7, R8, R9, Е, m, о і p мають значення, вказані в пункті 1, піддають взаємодії сполуки загальної формули XII і IX
,IX
,XII
де Аr, R1, R2, R5, R6, R7, R8, R9, Е, m, n, о і p мають значення, вказані в пункті 1, і Lg є групою, що відходить, і, якщо бажано, одержану в такий спосіб сполуку трансформують у її солі або виділяють із її солей і, якщо бажано, відокремлюють оптично активні ізомери.
10. Пестицидна композиція, що містить як активний інгредієнт 0,0001 - 99,9 мас. % сполуки загальної формули І
,I
де Аr, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, E, m, n, о і p мають значення, вказані в пункті 1, і, необов'язково, інший(і) пестицидно активний(і) інгредієнт(и), крім носіїв і інших допоміжних матеріалів.
11. Артроподицидна композиція, що містить як активний інгредієнт 0,0001 - 99,9 мас. % сполуки загальної формули І
,I
де Аr, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, E, m, n, о і p мають значення, вказані в пункті 1, і, необов'язково, інший(і) артроподицидно активний(і) інгредієнт(и), крім носіїв і інших допоміжних матеріалів.
12. Композиція згідно з пунктом 11, яка відрізняється тим, що містить як інший активний інгредієнт похідні ацетаміду: наприклад, оксаміл; бензоїлсечовини: наприклад, флуциклоксурон, гексафлумурон, тефлубензурон, трифлумурон; бензоїлсечовиноподібні IGR сполуки; біциклогептадієни: наприклад, гептенофос; дифеніли: наприклад, етофенпрокс, бромопропілат, метоксихолор, темефос, тетрадифон; карбамати: наприклад, амінокарб, алдікарб, алдоксикарб, асулам, бендіокарб, бенфуракарб, карбарил, карбетамід, карбофуран, карбосульфан, діетофенкарб, діоксакарб, етіофенкарб, фенобукарб, феноксикарб, фуратіокарб, ізопрокарб, метоміл, оксаміл, піримікарб (піримор), пропоксур, тіодикарб, тіофанокс, ксилікарб; похідні карбамоїлоксиму: наприклад, аланікарб, бутокарбоксим; циклодієни: наприклад, алдрин, хлордан, ендосульфан, гептахлор; діазоли: фіпроніл; гідразиди: RH 5992, RH 5849, CGA 215'944; аналоги нереїстоксину: наприклад, бенсултап; нітроімідазолідиніленаміни: наприклад, імідаклоприд; органофосфорні сполуки: наприклад, хіналфос, діазинон, фосалон, диметоат, азинфос-метил; оловоорганічні сполуки: наприклад, азоциклотин, цигексатин, фенбутатин оксид SSI-121; феноксисполуки: наприклад, діафентіурон; піразоли: наприклад, піразофос; піретроїди: наприклад, алетрин, біоалетрин (есбол), акринатрин, фенвалерат, емпентрин, пралетрин, ресметрин, МТІ-800, флуфенпрокс, перметрин, тетраметрин, циперметрин і їх ізомери і комбінації ізомерів; піридазинони: наприклад, піридабен; похідні піридинів: наприклад, хлорпірифос; похідні піримідинів: наприклад, піриміфос-етил, піриміфос-метил; піроли: наприклад, AC 303-t, 630; хіназоліни: наприклад, феназахін; похідні терпеноїдів: наприклад, метопрен; тетразини: наприклад, клофентезин, Szl-121 (флуфензин); тіадіазини: наприклад, бупрофезин; тіазолідини: наприклад, гекситіазокс; триазоли: наприклад, ісазофос, RH 7988; хлоровані вуглеводні: ліндан; макроциклічні лактони; тебуфенпірад; фенпіроксимат; триазамат.
13. Композиція згідно з будь-яким з пунктів 11 і 12, що містить як активний інгредієнт загальної формули 1 одну або більшу кількість наступних сполук:
1-нафтилметил-2-бутиніловий етер,
2-пропініл-1,3-бензодіоксол-5-карбоксилат,
1-[(2-бутинілоксі)етил]-3,4-диметоксибензол,
2,6-дихлор-1-(2-бутинілоксиметил)бензол,
1-[1-(2-бутинілокси)пропіл]нафталін,
R-(+)-2-[1-(2-бутинілоксі)етил]нафталін,
5-[(бут-2-инілокси)метил]-1,3-бензодіоксол,
5-[2-метил-1-(2-бутинілокси)пропіл]-1,3-бензодіоксол,
5-[(бут-2-инілокси)фенілметил]-1,3-бензодіоксол,
2-[(2-бутинілокси)метил]-1,4-бензодіоксан,
2,3-дигідро-2,2-диметил-7-(3-пентилокси)бензофуран.
14. Композиція згідно з будь-яким з пунктів 11-13, що містить як активний інгредієнт 0,0001 - 99,9 мас. % сполуки загальної формули І, де Аr, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, E, m, n, о і p мають значення, вказані в пункті 1, і карбамат, придатний для знищення членистоногих, переважно, карбофуран.
15. Композиція згідно з пунктом 14, що містить як сполуку загальної формули І (2-бутинілоксиметил)-3,4-диметоксибензол.
16. Композиція згідно з пунктом 14, що містить як сполуку загальної формули І 5-[(бут-2-инілокси)метил]-1,3-бензодіоксол.
17. Спосіб знищення паразитів, переважно членистоногих, що включає обробку паразитів, переважно членистоногих, придатною кількістю композиції згідно з будь-яким з пунктів 10 або 11, при бажанні, композиції, що містять сполуки загальної формули І, де Аr, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, E, m, n, о і p мають значення, вказані в пункті 1, використовують з композиціями, що містять відомі активні інгредієнти, або у вигляді суміші, або послідовно.
Текст
1 Сполуки загальної формули І, їх оптично активні ізомери й солі Ar-(CR R )m-(YR R )n-X- разом утворюють карбоксимідну групу, Е - Н, галоген, метил, т - 0 , 1, 2, п-0, 1, о-О, 1, 2, Р-0, 1, 2, за умови, що сума атомів або груп -(CR1R2)m(YRSR4)n-X-(CR5R6)0-(CR7R8)p місткового скелета дорівнює 3 і -С=С-Е скелет утворює з атомами містка ЛІНІЙНИЙ ланцюг, що складається з 6 атомів та закінчується, переважно, метильною групою, з наступною умовою, що коли Аг відповідає нафтильній групі, Y означає С-атом, X означає О-атом, R31 R4 спільно не можуть означати =0 2 Сполуки загальної формули ІА і їх оптично активні ізомери Ar-(CR1R2)m-{YR3R4)n-X-(CR5Rs)0-(CR7R8}p-CEC-E ІА де Аг, R1, R2 R5, R6, R7, R8, Y, Е, т , о і р мають значення, вказані в пункті 1 3 Сполуки загальної формули IB і їх оптично активні ізомери Де Аг - аліциклічний, ароматичний або гетероциклічний замісник, що містить один або більшу КІЛЬКІСТЬ гетероатомів і який, необов'язково, заміщений одним або декількома алкокси-, метилендіокси-, алкіл-, галоген-, галоалкіл- або нітрогрупами і/або конденсований з бензольним кільцем, R1, R - незалежно, Н, алкіл, алкеніл, галоалкіл, феніл заміщений феніл, циклоалкіл, R3, R - незалежно, Н, алкіл, алкеніл, галоалкіл, феніл, заміщений феніл, циклоалкіл, або R3, R4 є, разом, =0, Y - С, РО або YR3R4 разом -CR9=N-rpyna, X--O-.-NR10-, R9 - Н, алкіл, феніл, заміщений феніл, R 1 0 -H, алкіл, R5, R6, R7, R8 є, незалежно, Н, алкілом, алкенілом, галоалкілом або и О О Ar-(CR i R 2 ) m -Y-N-(CR 5 R6) 0 -{CR 7 R8) p -C=C-E І! і О R10 IB де Аг, R1, R2, R5, R6, R7, R8, R10, Y, E, m, о і р мають значення, вказані в пункті 1 4 Сполуки загальної формули 1С і їх оптично активні ізомери Ar-(CR1R2)m-(CR3R4)n-O-(CR5R6)o-(CRrR8)D-C=C-E 1С де Аг, R1, R2, R3, R4, R5, R6, R7, R8, E, m, п, о і р мають значення, вказані в пункті 1 (О 00 З 49864 5 Сполуки загальної формули Ю і їх солі і оптично активні ізомери 1 2 Ar-(CR R ) m -Y-A II О 5 6 7 8 B-(CR R )O-(CR R ) С = с . ID 1 2 3 4 5 6 7 8 10 де Аг, R , R , R , R , R , R , R , R , R , E, m, n, о і p мають значення, вказані в пункті 1 6 Сполуки загальної формули IE і їх солі і оптично активні ізомери 2 3 5 7 Ar-(CWH )m-(CR R%~H~(CR R%'(CR n%-C=C-E R10 1 2 5 6 7 є 8 де Аг, R , R , R , R , R , R , Y, E, m, о і р мають значення, вказані в пункті 1, А і В є групами, придатними для утворення естерного зв'язку, б) для одержання сполук загальної формули 1 2 5 6 7 8 10 IB, де Аг, R , R , R , R , R , R , R , Y, E, m, о і р мають значення, вказані в пункті 1, піддають взаємодії сполуки загальної формули IV і V 1 2 Ar-{CR R ) -Y-C IE 1 2 3 4 5 6 7 8 10 де Аг, R , R , R , R , R , R , R , R , R , E, m, п, о і р мають значення, вказані в пункті 1 7 Сполуки загальної формули IF і їх оптично активні ізомери, IF де Аг, R1, R2, R5, R6, R7, R8, R9, E, m, о і р мають значення, вказані в пункті 1 8 Сполуки згідно з пунктом 1, 1-нафтилметил-2-бутиніловий етер, 2-пропініл-1,3-бензодюксол-5-карбоксилат, 1-[(2-бутинілоксі)етил]-3,4-диметоксибензол, 2,6-дихлор-1-(2-бутинілоксиметил)бензол, 1-[1-(2-бутинілокси)пропіл]нафталш, р.(+)-2-[і-(2-бутинілоксі)етил]нафталін, 5-[(бут-2-инілокси)метил]-1,3-бензодюксол, 5-[2-метил-1-(2-бутинілокси)пропіл]-1,3бензодюксол, 5-[(бут-2-инілокси)фенілметил]-1,3-бензоДІОКСОЛ, 2-[(2-бутинілокси)метил]-1,4-бензодюксан, 2,3-дипдро-2,2-диметил-7-(3-пентилокси)бензофуран 9 Спосіб одержання сполук загальної формули І де Аг, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X, Y, Е, т , п, о і р мають значення, вказані в пункті 1, який характеризується тим, що а) для одержання сполук загальної формули ІА, де Аг, R1, R , R5, R6, R7, R8, Y, E, m, о і р мають значення, вказані в пункті 1, піддають взаємодії сполуки загальної формули II і III О 5 S JV 7 8 D~(CR R )O~(CR R )-C=C-E ,v де Аг, R1, R2, R5, R6, R7, R8, Y, E, m, о і р мають значення, вказані в пункті 1, і С і D є групами, придатними для утворення амідного зв'язку, в) для одержання сполук загальної формули 1С, де Аг, R1, R, R5, R6, R7, R8, Е, т , п, о і р мають значення, вказані в пункті 1, R3 і R4, незалежно, означають Н, алкіл, алкеніл, галоалкіл, феніл, заміщений феніл, піддають взаємодії сполуки загальної формули VI і VII Ar-(CR 1 R 2 ) m -(CR3R4) n -F G-{CR5RS)O-(CR7R8)D-C = C - E ,vn де Аг, R1, R2, R5, R6, R7, R8, E, m, n, о і р мають значення, вказані в пункті 1, R3 і R4, незалежно, означають Н, алкіл, алкеніл, галоалкіл, феніл, заміщений феніл, F і G є групами, придатними для утворення етерного зв'язку, г) для одержання сполук загальної формули Ю, де Ar-(CR1R2)rn-(CR3R4)n-N є карбоксимідною групою, R5, R6, R7, R , Е, о і р мають значення, вказані в пункті 1, карбоксимід загальної формули VIII піддають реакції із сполукою загальної формули IX Ar-(CR1R2)m-(CR2R3)n-NH Lg-(CR 5 R 6 ) O -(CR 7 R8) D -C = C - E де R5, R6, R7, R8, Е, о і р мають значення, вказані в пункті 1, і Lg є групою, що відходить, 49864 д) для одержання сполук загальної формули 1 3 4 5 6 7 8 10 IE, де Аг, R , R , R , R , R , R , R , R , R , E, m, п, о і р мають значення, вказані в пункті 1, піддають взаємодії сполуки загальної формули X і XI 1 2 3 4 Ar-(CR R )m»(CR R )^H ,х С-Е 1 2 3 4 5 6 7 8 де Аг, R , R , R , R , R , R , R , R , E, m, п, о і р мають значення, вказані в пункті 1, Н і І являють собою групи, придатні для утворення R10 групи, де R має те ж значення, як визначено в пункті 1, є) для одержання сполук загальної формули IF, де Аг, R1, R2, R5, R6, R7, R8, R9, E, m, о і р мають значення, вказані в пункті 1, піддають взаємодії сполуки загальної формули XII і IX (CR7R8) -С =С-Е -C=N-OH 1 2 5 6 7 ,хн 8 де Аг, R , R , R , R , R , R , R9, E, m, п, о і р мають значення, вказані в пункті 1, і Lg є групою, що відходить, і, якщо бажано, одержану в такий спосіб сполуку трансформують у її солі або виділяють із її солей і, якщо бажано, відокремлюють оптично активні ізомери 10 Пестицидна композиція, що містить як активний інгредієнт 0,0001 - 99,9 мас % сполуки загальної формули І де Аг, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, Е, т , п, о і р мають значення, вказані в пункті 1, і, необов'язково, ІНШИЙ(І) пестицид но активний(і) шгредієнт(и), крім носіїв і інших допоміжних матеріалів 11 Артроподицидна композиція, що містить як активний інгредієнт 0,0001 - 99,9 мас % сполуки загальної формули І AHCR 1 R2) -{YR3R")-X-(CR5R6)O-(CR7R8)D-C БС-Е де Аг, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, Е, т , п, о і р мають значення, вказані в пункті 1, і, необов'язково, ІНШИЙ(І) артроподицидно актив ний(і) шгредієнт(и), крім носіїв і інших допоміжних матеріалів 12 Композиція ЗГІДНО З пунктом 11, яка відрізняється тим, що містить як інший активний інгредієнт ПОХІДНІ ацетаміду наприклад, оксаміл, бензоілсечовини наприклад, флуциклоксурон, гексафлумурон, тефлубензурон, трифлумурон, бензоілсечовиноподібні IGR сполуки, біциклогептадієни наприклад, гептенофос, дифеніли наприклад, етофенпрокс, бромопропілат, метоксихолор, темефос, тетрадифон, карбамати наприклад, амінокарб, алдікарб, алдоксикарб, асулам, бендюкарб, бенфуракарб, карбарил, карбетамід, карбофуран, карбосульфан, діетофенкарб, дюксакарб, етюфенкарб, фенобукарб, феноксикарб, фуратюкарб, ізопрокарб, метоміл, оксаміл, піримікарб (піримор), пропоксур, тюдикарб, тюфанокс, ксилікарб, ПОХІДНІ карбамоілоксиму наприклад, аланікарб, бутокарбоксим, циклодієни наприклад, алдрин, хлордан, ендосульфан, гептахлор, діазоли фіпроніл, гідразиди RH 5992, RH 5849, CGA 215'944, аналоги нереістоксину наприклад, бенсултап, нітроімідазолідиніленаміни наприклад, імідаклоприд, органофосфорні сполуки наприклад, хіналфос, діазинон, фосалон, диметоат, азинфос-метил, оловоорганічні сполуки наприклад, азоциклотин, цигексатин, фенбутатин оксид SSI-121, феноксисполуки наприклад, діафентіурон, піразоли наприклад, піразофос, піретроіди наприклад, алетрин, бюалетрин (есбол), акринатрин, фенвалерат, емпентрин, пралетрин, ресметрин, МТІ-800, флуфенпрокс, перметрин, тетраметрин, циперметрин і їх ізомери і комбінації ізомерів, піридазинони наприклад, піридабен, ПОХІДНІ піридинів наприклад, хлорпірифос, ПОХІДНІ піримідинів наприклад, піриміфос-етил, піриміфос-метил, піроли наприклад, AC 303-t, 630, хіназоліни наприклад, феназахін, ПОХІДНІ терпеноідів наприклад, метопрен, тетразини наприклад, клофентезин, Szl-121 (флуфензин), тіадіазини наприклад, бупрофезин, тіазолідини наприклад, гекситіазокс, триазоли наприклад, ісазофос, RH 7988, хлоровані вуглеводні ліндан, макроциклічні лактони, тебуфенпірад, фенпіроксимат, триазамат 13 Композиція ЗГІДНО З будь-яким з пунктів 11 і 12, що містить як активний інгредієнт загальної формули 1 одну або більшу КІЛЬКІСТЬ наступних сполук 1-нафтилметил-2-бутиніловий етер, 2-пропініл-1,3-бензодюксол-5-карбоксилат, 1-[(2-бутинілоксі)етил]-3,4-диметоксибензол, 2,6-дихлор-1-(2-бутинілоксиметил)бензол, 1-[1-(2-бутинілокси)пропіл]нафталш, р.(+)-2-[і-(2-бутинілоксі)етил]нафталін, 5-[(бут-2-инілокси)метил]-1,3-бензодюксол, 5-[2-метил-1-(2-бутинілокси)пропіл]-1,3бензодюксол, 5-[(бут-2-инілокси)фенілметил]-1,3бензодюксол, 2-[(2-бутинілокси)метил]-1,4-бензодюксан, 2,3-дипдро-2,2-диметил-7-(3пентилокси)бензофуран 14 Композиція ЗГІДНО З будь-яким з пунктів 1113, що містить як активний інгредієнт 0,0001 - 99,9 мас % сполуки загальної формули І, де Аг, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, E, m, п, о і р мають значення, вказані в пункті 1, і карбамат, придатний для знищення членистоногих, переважно, карбофуран 15 Композиція ЗГІДНО З пунктом 14, що містить як сполуку загальної формули І (2бутинілоксиметил)-3,4-диметоксибензол 16 Композиція ЗГІДНО З пунктом 14, що містить як сполуку загальної формули І 5-[(бут-2инілокси)метил]-1,3-бензодюксол 17 Спосіб знищення паразитів, переважно 49864 8 членистоногих, що включає обробку паразитів, переважно членистоногих, придатною КІЛЬКІСТЮ композиції згідно з будь-яким з пунктів 10 або 11, при бажанні, композиції, що містять сполуки загальної формули І, де Аг, R , R2, R3, R4, R , R6, R7, R8, R9, R10, Е, т , п, о і р мають значення, вказані в пункті 1, використовують з композиціями, що містять ВІДОМІ активні інгредієнти, або у вигляді суміші, або послідовно Даний винахід відноситься до пестицид них сполук загальної формули І, пестицидних композицій, що містять активні інгредієнти загальної формули І, а також пестицидних синергічних речовин загальної формули І, посилених пестицидною сполукою з відомими пестицид ними активними інгредієнтами і способу їх одержання У загальній формулі І замісники мають наступні значення Аг = аліциклічному, ароматичному одному, або більше гетероатому, що містить гетероциклічну частку, вибірково заміщену однією або більш алкокси, метилендюкси, алкіл, галоген, галоалкіл, або нітро групою, і/або конденсованою з бензольним кільцем, R1, R = незалежно, водню, алкілу, алкенілу, галоалкілу, фенілу, заміщеному фенілу, циклоалкілу, R3, R4 = незалежно, водню, алкілу, алкенілу, галоалкілу, фенілу, заміщеному фенілу фенілу, циклоалкілу, або R3, R4, спільно, є = 0, Y = с, = РО, або R9 YR3R4, спільно, утворюють -C=N-rpyny; Х=-О-, - N R R9 = водню, алкілу, фенілу, заміщеному фенілу, R = водню, алкілу, R5, R6, R7, R8 є, незалежно, воднем, алкілом, алкенілом, галоалкілом або Ar-(CR 1 R 2 )m-(YR 3 R 4 )n-X- утворюють, спільно, карбоксимідну групу, Е = водню, галогену, метилу, 171 = 0,1,2, п = 0,1, 0 = 0,1,2, р = 0,1,2, з умовою, що сума атомів або груп мосту (CR1R2)rn-(CR3R4)n-X-(CR5R6)o-(CR7R8)p дорівнює З і -С=С-Е кістяк з атомами мосту утворюють ЛІНІЙНИЙ ланцюг, що складається з 6 атомів, переважно, із метильною групою на КІНЦІ, далі, з умовою, що, якщо Аг є нафтильною групою, Y означає С-атом, X означає О-атом, R3 і R спільно, не можуть означати = 0 Винахід містить у собі також солі й оптично активні ізомери сполук загальної формули І Менші групи у сполуках загальної формули І подані сполуками основної формули ІА, IB, 1С, ID, IE, IF, їхніми солями й оптично активними ізомерами, де значення замісників ті ж, що визначені вище Переважними представниками сполук загальної формули І є 1-нафтил-метил 2-бутиніл ефір, 2-пропініл-1,3-бензодюксол-5-карбоксилат, 1 -[(2-бутинілокси)-етил]-3,4-диметоксибензол, 2,6-дихлоро-1 -(2-бутинілоксиметил)бензол, 1 -[1 -(2-бутинілокси)пропіл]нафталш, R-(+)-2-[ 1 -(2-бутинілокси)етил]нафталш, 5-[(бут-2-інілокси)метил]-1,3-бензодюксол 5-[2-метил-}-(2-бутинілокси)пропіл]-1,3 бензодюксол, 5-[(бут-2-шілокси)фенілметил]-1,3-бензоДІОКСОЛ, 2-[(2-бутинілокси)метил]-1,4,бензодюксан, 2,3-дипдро-2,2-диметил-7-(3-пентилокси)бензофуран У терміні Аг ароматичною групою, переважно, є фенільна або нафтильна група Аг, як гетероциклічна частка, може містити один або більш О, S, N гетероатомів, Аг може, переважно, представляти бензодюксол-, бензодюксан-, 2-бензофуран, 7бензофуран-долі Аліциклічна група, переважно, може бути конденсована з бензильним кільцем, таким чином, наприклад, може представляти інданову групу, або 1,2,3,4-тетрапдронафтильну групу Карбоксимідна група може, переважно, представляти фталимідну частку Ароматичні, гетероциклічні й аліЦИКЛІЧНІ Аг групи, вибірково, заміщені Сі 4 алкокси, метилендюкси-, Сі 4 алкіл-, галоген, Сі 4 галоалкіл- або нітро групами Сполуки, що не є токсичними, або лише слабко токсичні по окремості, але узяті разом із пестицидом, переважно, артроподицидною речовиною, помітно збільшують силу останнього, називаються синергічними речовинами Ці речовини можуть, у принципі, діяти декількома шляхами, однак, в основному, вони роблять свою дію за допомогою блокування метаболізму активної субстанції Метаболізм може проходити через окисні, гідролітичні, кон'югативні або абсорбційні реакції і їхні варіації В даний час не існує чіткого прикладу синергічних речовин, що діють на рівні рецептора, не грають вони важливої ролі й у практиці Сила 49864 синергічної речовини, наприклад, у випадку інсектицидів, характеризується так називаною SR пропорцією синергічної речовини, поданою в такий спосіб інсектициду SR50 = LD5Q інсектицид-- синергічна речовина Чим більше значення SRso відрізняється від 1, тим вище сила синергічної речовини Використання синергічних речовин в антроподицидних препаратах дуже привабливо, оскільки вони дають можливість одержання нових препаратів із практично усіма представниками даної сфери Ці нові препарати, у порівнянні з попередніми, обіцяють бути менш дорогими, менш токсичними, більш селективними, менш небезпечними для навколишнього середовища, такими, що пригнічують розвиток усталеності, і активними також на штамах, які вже виробили усталеність Слідом за відкриттям синергічних речовин і виявленням механізму їхньої дії пішли широкомасштабні дослідження й розробки нових синергічних речовин, що продовжувалися із середини 60-х до кінця 70-х років Результатом цих досліджень стало створення лише декількох молекул, що дійсно знайшли застосування (у даний час існує менше 10 зареєстрованих інсектицидних синергічних речовин) Ці сполуки мають велике наукове значення в дослідженнях усталеності (К F Raffa and Т М Pnester, J Agnc Entomol , 2(l),27-45,(1985)), однак, лише 2-3 молекули, приведені в якості продуктів у Посібнику з Пестицидів (Pesticide Manual), і лише дві речовини (РВО, MGK264) дійсно знаходяться на ринку Область застосування обмежена декількома чинниками непросто знайти ХІМІЧНИЙ інструмент, що міг би використовуватися селективно й безпечно, і відношення вартість/ефективність якого було б конкурентоспроможне в порівнянні з такими ж відношенням активного інгредієнта Для того, щоб синергічна речовина була економічно придатною, вона повинна мати високу силу, діяти при малих дозах (не перевищуючих вихідної дози активного інгредієнта) На основі їхніх ХІМІЧНИХ структур, ВІДОМІ В даний час антроподицидні синергічні сполуки можуть бути розділені на наступні групи ПОХІДНІ 1,3-метилендюксифенілу (MDP), гомологи О-2-пропінілу й пропінілу і їх ПОХІДНІ (ефіри, оксим-ефіри, складні ефіри), ПОХІДНІ N-алкілу, складні ефіри фосфору, ІНШІ ПОХІДНІ, наприклад, тюціанати, політало ефіри і т д Сполуки можуть також бути розділені на групи на основі мішені, що атакується ними, [К F Raffa and Т М Pnester, J Agnc Entomol, 2(l), 27-45, (1985)], але цей поділ є скоріше теоретичним, менше точним, насамперед тому, що ДІЙСНІ метаболічні процеси не ВІДОМІ повністю Метаболізм більшості сполук проходить послідовно, але може проходити також одночасно, і за різними механіз 10 мами, таким чином, поділ менше інформативний, навіть, якщо ми рахуємо перший крок каскадної деградації за вирішальний За метаболічну деградацію більшості артроподицидів відповідає, у першу чергу, оксигеназна система У літературі вважається, що сполуки цієї групи виявляють свою активність, в основному, за допомогою блокування ферменту цитохрому Р450 окисної системи мікросом [John E Cassida, J Agr Food Chem , 18(5), 753-772, (1970), R M Sacher, R L Metcalf and T R Fukuto, J Agr Food Chem, 16(5) 779-786, (1968)] Ферменти, що формують структурно аналогічну групу так називаних ізоферментів, складають велику частину детоксифікаційної системи організмів [Ortiz de Montellano, Р R , Ed Cytochrom P-450 Structure Mech and Biochem , Plenum New York, (1986)] Вони здійснюють детоксифікацію через моно-оксигенування субстрату, у результаті чого утворюється більш полярний продукт, який, можливо, після наступних трансформацій може бути елімінований організмом Система руйнує самі різні структури тим самим шляхом Тому вони також позначаються як оксигенази змішаної функції (MFO) і полісубстратні монооксигенази (PSMO) На підставі цього очікується, що поверхня ферменту є неспецифічною також і для синергічної речовини На противагу цьому, ми виявили, що сполуки можуть бути оптимізовані Для виділення й тестування ферментів цитохрому Р-450 комах існують доступні стандартні способи [J G Scott and S S T Lee, Arch Insect Biochem, and Phys , 24, 1-19, (1993)] Ферменти різних видів можуть показувати великі подібності, але вони можуть також значно відрізнятися друг від друга Синерпсти, ВІДОМІ В літературі і досліджувані нами, належать до групи 0-2- пропінілу й гомологів пропінілу і їх похідних (ефірів, оксим-ефірів, складних ефірів) Як показано в літературі, вони виявляють різну силу у різних видів, це означає, що окисна здатність видів до деякої міри варіює Це є причиною високої селективності комаха/ссавець і високої селективності синергічної речовини, що є характерною рисою цієї групи сполук Ці селективності що не можуть бути безпосередньо пояснені способом дії, приведеним вище, є основами розробки і безпечного застосування З іншого боку, це служить причиною того, що ці сполуки не стали комерційне доступними Для всіх отриманих і оцінених сполук групи, поки що, ми можемо сказати, в основному, те, що їхня дія була зв'язана винятково з бічним пропініловим ланцюгом, цей ланцюг був заміщений в алельній позиції різними ариловими кільцями, головним чином, через атом кисню ВІДОМІ сполуки, поки що, можуть бути розділені на наступні групи феніл пропарплові ефіри [Felling et ah, J Arg Food Chem , 18(5), 78, (1970)], бензил пропарплові ефіри [Ciba Geigy, Ger Offen, 2 235 005(1972)], бензалдоксим пропарплові ефіри [Ciba Geigy, Ger Offen, 2016190(1970)], пропарплові складні ефіри нафтоікової кислоти [Hoffman-La Roche, Beig Patent, 867849(1978)], алкінілфталиміди [FMC, Ger Patent, 1217 693 (1966)], 12 11 49864 пропарплові складні ефіри фенілфосфонікової автори не представили детально взаємозвязку, і кислоти [Niagara Chem Div, FMC Corp , Technical не одержали найбільш активних представників, що Data Sheet on NIA 16824, (1968)] знижують і підвищують ГІДНОСТІ цих груп сполук Перші дві групи підрозділяються на додаткові Ми експериментально перевірили, порівняли й групи через високу МІНЛИВІСТЬ ароматичної групи й проаналізували біологічну дію відомих сполук, а замісників Так, ВІДОМІ нафтил пропарплові ефіри також нових, отриманих нами, похідних, і виявили [Hoffman-La Roche, US 3 362 871 (1968), Qba структурний елемент, відповідальний за дію цих Geigy, Ger Often, 2 100 325 (1971)], 4сполук На підставі цього ми одержали нові сполупдроксихшолін пропарплові ефіри [Alkaloida, HU ки, що по активності значно перевершують своїх 210 557, (1992)], метилендюксибензил пропарплопопередників і сполучать у собі ті властивості, що ві ефіри [Sumitomo, JP, 03 01177, (1973)] і альфагарантують ефективність на більшості видів і з заміщені метилендюксибензил пропарплові ефіри більшістю відомих активних інгредієнтів [Sumitomo, JP, 6124585, 6124586 (1986)] Невіддільною частиною даного винаходу є відкриття того, що в оптимальних сполуках носієм У результаті досліджень нафтил пропшілових активності служить потрійний зв'язок алкінільної ефірів був зроблений висновок, що бутинілові ефіструктури з насиченим електронами Аг кільцем, ри, у першу чергу, 3-бутинілові ефіри, є більш сищо з'єднується з потрійним зв'язком через мобільльними в порівнянні з аналогічними пропарпловиний міст, який складається з трьох атомів Атоми ми й пентиніловими ефірами [R М Sacher et ah, J мосту й кільця МІНЛИВІ і можуть мати замісників Agr Food Chem, 16, 779-786, (1968)] Цікаво, одДля збільшення активності кращим є уводити линак, що продовження цієї роботи не пішло, відпофільні й насичені електронами атоми й замісникриття не було також і запатентовано Детальний ки Таким чином, атомами мосту можуть бути (крім аналіз наявних у літературі даних наводить на атомів вуглецю) гетероатоми кисню, сірки, азоту й думку про те, що пропшіловий бічний ланцюг не фосфору Ці атоми можуть бути з'єднані простим може бути замінений на ГОМОЛОГІЧНІ бічні ланцюги, або множинним зв'язками один з одним і, вибіркооскільки публікації й патенти відносяться далі до во, із додатковими замісниками, що містять вищепохідних пропарплу Для того, щоб з'ясувати це згадані гетероатоми, які можуть бути заміщені допротиріччя, ми одержали сполуки, про які йде модатковими функціональними групами або ва, і виявили, що у противагу тому, що було опипохідними Атоми можуть заміняти один одного сано в літературі, похідне 2-бутинілу (те, що закінПерший елемент мосту зі своїм замісником може чується метильною групою) є більш сильним у утворювати кільце, яке може бути приєднане до порівнянні з похідним 3-бутинілу, альфа-ізомери є ароматичного кільця, і, таким чином, може являти більш сильними в порівнянні з аналогічними бетасобою частину насиченої електронами частки У ізомерами, і похідне 3-пентинілу сильніше, ніж покільце, з'єднане з мостом, також, можуть бути ввехідне 2-бутинілу Ці дані добре узгоджуються з дені перераховані вище гетероатоми, і ефект монашою теорією, і приведені в літературі дані, маже бути додатково посилений за допомогою ввебуть, послужили причиною того, що цей напрямок дення алкокси, галоген, алкіл, галоалкіл або нітро не було продовжено іншими дослідниками Існує замісників Кільце може бути 5-, 6-, або 7-членним, також протиріччя й у відношенні активності похідможе бути зв'язане з додатковим кільцем, побудоних 4-пентинілфталиміду хоча вони й виявилися ваним ВІДПОВІДНО до вищезгаданого принципу, і сильними синергічними речовинами алетрину, може включати перший елемент мосту Сполуки, у вони виявляють антагонізм у відношенні піретрину яких ацетиленовий водень алкінільного бічного [HJaffe, J L Neumeyer, J Med Chem, 13, 901, ланцюга заміщений метильною групою, показують (1970)] У цих структурах, до того ж, алкініловий більш високу активність у порівнянні з аналогами, ланцюг закінчується потрійним зв'язком Гібридні що мають термінальний потрійний зв'язок Дотриваріації цих структур, називані N-алкілокси-омуючи ці правила, ми можемо одержати нові заміпропарпл-фталимідами, теж були отримані, посники, за допомогою яких можна модифікувати трійний зв'язок тут також знаходиться в термінавластивості сполук ВІДПОВІДНО ДО ВИМОГИ (липофільній позиції [Sumitomo, NL, 6 600 916 (1966)] Підльність, трансламшарність, систематичність, і т і) сумовуючи, зазначене, можна сказати, що області застосування найбільш активні представники групи, незважаючи на показану в деяких тестах високу активність і, чудові якості по їхньому відношенню синергічна Серед ізомерів оптично активних сполук, наречовина/активний інгредієнт [D J Henessy, Bioприклад, а-метил-заміщених похідних бензилу, chemical Toxicology of Insecticides, Ed , R D O'Bnan Р(+)енантюмери сильніше, ніж S (-)енантюмери & I Yamamoto, Academic Press, 105-114, (1970)], Різниця МІЖ активностями ізомерів зростає зі збініколи не були застосовані у практиці Для цього є льшенням активності рацемічної суміші декілька причин їхня активність не досягала сили Розроблені нами сполуки є новими, вони харапопередніх, що добре зарекомендували себе, поктеризуються неординарною селективністю ссахідних, вони показували активність лише у вузьковець/комаха і високою силою, що виявляється при му діапазоні, їхня сила була високо видозалежнизькій дозі відносно активного інгредієнта Це ною, і усередині окремих видів вона сильно приписується украй високій рецепторній споріднезалежала від "опору" індивіда Таким чином, їх ності наших сполук У порівняльних експериментах безпечне й широке застосування не було гарантоіндекси наших сполук значно перевершували такі вано раніше ВІДОМІ синергічні сполуки активних інгредієнтів, чий метаболізм заснований на мікросомальному окисленні Ця висока активність і селективУсі алкінільні сполуки, перераховані вище, є ність були продемонстровані на польових похідними загальної оптимальної структури, але 14 13 49864 дослідженнях, проведених на малих ділянках Тебуфенпірад, Фенпіроксимат, Сполуки не виявляли фітотоксичності, не відокреТріазамат млювалися від активних інгредієнтів, їхні фізикоВищезгадані ВІДОМІ активні інгредієнти, описані ХІМІЧНІ параметри добре збігалися з такими ж пав 8-му і 10-му Виданнях Довідника по Пестицидах раметрами активного інгредієнта При сполученні (8th and 10th Edition of the Pesticide Manual, Euroцих особливостей співвідношення доpean Patent Application No 0635499 (SZI-121), за/ефективність/ціна, яке раніше було перешкодою A G Chem New Compound review vol 11 (1993) і цьому винаходові, може бути переважно модифіковано, і заявка стає можливою Сполуки загальної формули І можуть бути, найбільш переважно, використані для посилення З використанням активних сполук загальної ефекту карбаматів, переважно, карбофурану Ми формули І може бути, переважно, посилений виявили, що сполуки мають подвійну дію, вони є ефект наступних відомих артроподицидних активчудовими речовинами, що підсилюють артроподиних інгредієнтів цидні активні інгредієнти, і вони перешкоджають ПОХІДНІ ацетаміду наприклад, оксаміл, індивідуальному росту артроподу шляхом ушкоСполуки бензоілсечовини наприклад, флуцидження біосинтезу екдисону, матеріалу, що грає клоксурон, гексафлумурон, тефлубензурон, трифцентральну роль у рості артроподу Таким чином, лумурон, існує недвозначне взаємовідношення між синергіБензоілсечовино-подібні IGR сполуки, чними активностями й активностями, що ушкоБіциклогептадієнові сполуки наприклад, гепджують індивідуальний ріст Останній з названий тенофос, ефектів, крім видатної метаболізм-блокуючої актиДифенільні сполуки з пересічними мостами вності сполук, є також наслідком факту, що ці манаприклад, етофенпрокс, бромопропілат, метокситеріали, у контрасті з іншими, раніше відомими холор, темефос, тетрадифон, родинами сполук, практично не розпадаються, або Карбамати наприклад, амінокарб, алдикарб, розпадаються тільки вкрай повільно в організмі алдоксикарб, асулам, бендюкарб, бенфуракарб, артроподу Таким чином, будучи використаними карбаріл, карбетамід, карбофуран, карбосульфан, єдино, тривалий період, у залежності від фаз ендієтофенкарб, дюксакарб, етюфенкарб, фенобудокринної регуляції, вони здатні блокувати синтез карб, феноксикарб, фуратюкарб, ізопрокарб, мегормонів і перешкоджати деградації ендо- і екзобітоміл, оксаміл, піримікарб (піримор), пропоксур, отиків Унаслідок нагромадження токсинів в оргатюдикарб, тюфанокс, ксилілкарб, нізмі, комахи стають нездатними жити, вони не ПОХІДНІ карбамоілоксиму наприклад, аланіхарчуються, продукція яєць знижується і репродукарб, бутокарбоксим, кція зупиняється Циклодієни наприклад, алдрін, хлордан, ендосульфан, гептахлор, Крім цих посилених активностей, значення токсичності сполук на ссавцях не збільшувалися Це Діазолі фіпроніл, може бути віднесене до різниць у значеннях елекГідразиди RH 5992, RH 5849, CGA 215'944, тронних потенціалів систем мікросомального окиАналоги нереістоксину наприклад, бенсульслення у ссавцях і у артроподі Тоді як значення тап окисного потенціалу вищих організмів високі, і тоНітроімідазолідиніленаміни наприклад, імідаму вони здатні пробивати електронний бар'єр сиклопрід, нергічних речовин, що знаходяться в комплексі, Органофосфорні сполуки наприклад, хіналокисна система артроподу з и невеликим потенціфос, діазинон, фосалон, диметоат, ацинфосалом не здатна окислювати і таким способом виметил, даляти комплексні молекули з поверхні ферменту, Сполуки органотину наприклад, азоциклотин, приводячи до паралічу системи Це є причиною, цигексатин, фенбутатін оксид SSI-121, чому сполуки можуть бути використані безпечно й Фенокси сполуки наприклад, діафентіурон, селективно Швидка, вища за середню, деградація Піразолі наприклад, піразофос, й виведення сполук із ссавців, обумовлені високою Піретроіди наприклад, алетрин, бюалетрин активністю їхніх ферментів і швидким зв'язуванням (есбол), акріатрин, фенвалерат, емпентрин, праферментів, забезпечують те, що, у контрасті з арлетрин, ресметрин, МТ1-800, флуфенпрокс, пертроподом, ці матеріали не підсилюють ефекти бюметрин, тетраметрин, циперметрин і їхні ізомери, і тиків, виявлених або ужитих організмом ссавців, і комбінації ізомерів, тому вони безпечні Ефект був продемонстроваПіридазинони наприклад, піридабен, ний нами на різних видах артроподу Використані ПОХІДНІ піридинів наприклад, хлорпірифос єдино, або в якості синергічної речовини, сполуки ПОХІДНІ піримідинів наприклад, піриміфосбули активні на комахах, попелицях і також на етил, піриміфос-метил, кліщах У СВІТЛІ вищесказаного, цей факт знову Піролі наприклад, AC 303-t, 630, відноситься до якісно відмінної детоксифікаційної Хіназоліни наприклад, феназахін, системи ссавців Дуже цінною перевагою наших ПОХІДНІ терпеноідів наприклад, метопрен, сполук є те, що при використанні їх на видах з Тетразини наприклад, хлофентезин, Szl-121 розвинутою усталеністю, токсична доза може бути (флуфензин), знижена стосовно початкової дози відомого активТіадіазини наприклад, бупрофезш, ного інгредієнта (виміряної на чутливих штамах) Тіазолідин наприклад, гекситіазокс, Цього не спостерігалося з іншими синергічними Триазолі наприклад, ісазофос, RH 7988, речовинами Це уможливлює безпечне й ефективХлориновані вуглеводні ліндан, не обертання зі стійкими популяціями у ВІДПОВІДМакроциклІЧНІ лактони, S y m p o s i u m S e r i e s 5 0 4 p 2 7 2 , В І Д П О В І Д Н О ) 16 15 49864 1 ності з сучасними правилами R Крім очікуваних переваг, згаданих вище групи, де R має те ж значення, яке визначено (сполуки уможливлюють розвиток препаратів, які вище, менш дорогі, менш токсичні на ссавцях, селективні є) для одержання сполук загальної формули 1 2 5 6 7 8 9 і можуть пригнічувати усталеність), за допомогою IF, де Аг, R , R , R , R , R , R , R , E, m, о і р мають цих сполук можуть бути обновлені добре ВІДОМІ ті ж значення, які визначені вище, сполуки загаль1 2 активні інгредієнти, чий ринок упав в останні роки ної формули XII і IX піддають реакції, де Аг, R , R , 5 6 8 9 через усталеність, що розвилася до них (КарбоR , R , R , R , R , Е, т , п, о і р мають ті же значенфуран, Хіналфос, Картап, Метоміл) Наші сполуки ня, які визначені вище, і Lg являє собою залишкозабезпечують нове використання й можливості ву групу, і якщо бажано, отримана в такий спосіб ринку, тому що вони підсилюють ефективність сполука може бути трансформована в його солі, менш активних матеріалів (Ресметрин, Бюалетабо може бути вивільнена з його солей, і, якщо рин, Піримікарб і т д ) до рівня найбільш активних бажано, можуть бути відділені оптично активні сполук без збільшення їхньої токсичності РВО, що ізомери знаходиться на ринку у великих кількостях, у приДля одержання сполук загальної формули 1, родних ресурсах розкладається повільно - у зроспереважно таючій вартості, і який не є привабливим унаслідок а) кислий галід загальної формули II піддають приписуваного йому ефекту, що викликає пухлину, реакції з алкінолом загальної формули III, або картакож може бути замінений за допомогою наших боксилікову кислоту загальної формули II піддають сполук реакції з алкініловим галогенідом загальної формули III у присутності кислотозв'язуючого агента, Одержання сполук загальної формули 1 відріабо карбоксилікову кислоту загальної формули II зняється в залежності від різних груп сполук, і мопіддають реакції з алкінолом загальної формули III же бути проведено ХІМІЧНИМИ способами, характеу присутності активатора, переважно, діетил азорними для одержання цих груп дикарбоксилату і трифенілфосфшу або дициклогеТак ксилкарбодиіміду і кислого каталізатора, а) для одержання сполук загальної формули 1 5 6 7 8 ІА, де Аг, R , R , R , R , R , R Y, E, m, о і р мають б) кислий галід загальної формули II піддають ті ж значення, які визначені вище, сполуки загальреакції з первинним або вторинним алкініламіном 1 2 ної формули II і III піддають реакції, де Аг, R , R , загальної формули V, або карбоксамід загальної R5, R6, R7, R8 Y, Е, т , о і р мають ті ж значення, які формули IV піддають реакції з алкініловим галогевизначені вище, А і В є групами, що підходять для нідом загальної формули V, оптимально, у присутформування ефірного зв'язку, ності кислото-зв'язуючого агента, б) для одержання сполук загальної формули в) спирт загальної формули VI піддають реакIB, де Аг, R1, R2, R5, R6, R7, R8, R10,Y, E, m, о і р ції з алкініловим галогенідом загальної формули мають ті ж значення, які визначені вище, сполуки VII, або галогенід загальної формули VI піддають загальної формули VI і VII піддають реакції, де Аг, реакції з алкінолом загальної формули VII у присуR1, R2 R5 R6, R R8, Y, Е, т , о і р мають ті ж знатності основи, або спирт загальної формули VI і чення, які визначені вище, і С і D є групами, що алкінол загальної формули VII піддають реакції у підходять для формування амідного зв'язку, присутності активатора, переважно, діетил азодикарбоксилату і трифенілфосфшу або дициклогекв) для одержання сполук загальної формули силкарбодиіміду і кислого каталізатора, 1С, де Аг, R1, R2, R5 R6, R7, R8, Е, т , п, о і р мають ті ж значення, які визначені вище, R3 і R4, незалег) карбоксимід загальної формули VIII піддажно, означають Н, алкіл, алкеніл, галоалкіл, феніл, ють реакції у присутності основи з алкініловим заміщений феніл, сполуки загальної формули VI і галогенідом або -месилатом, -тосилатом, VII піддають реакції, де Аг, R1, R2, R5, R6, R , R8, Е, трифтороацетатом загальної формули IX, або m п, о і р мають ті ж значення, які визначені вище, д) вторинний амін загальної формули X підR і R4 можуть, незалежно, означати Н, алкіл, алдають реакції з алкініловим галогенідом загальної кеніл, галоалкіл, феніл, заміщений феніл, F і G є формули XI, або галогенід загальної формули X групами, що підходять для формування ефірного піддають реакції з вторинним аміном загальної зв'язку, формули XI у присутності основи, або г) для одержання сполук загальної формули є) алдоксим або кетоксим загальної формули Ю, де Ar-(CR1R2)m-(CR2R4)n-N є карбоксимідною XII піддають реакції у присутності основи з алкініл групою R5, R6, R R8, Е, о і р мають ті ж значення, галогенідом або -месилатом, -тосилатом, які визначені вище, карбоксимід загальної формутрифтороацетатом загальної формули IX ли VIII піддають реакції із сполукою загальної фоСполуки, отримані й заявлені нами, є новими, рмули IX, де R5, R6, R , R8, Е, о і р мають ті ж знавони не розкриті в літературі, їхні структури були чення, які визначені вище, і Lg являє собою досліджувані після обчищення, обчищення перевізалишкову групу, рене методами TLC і GC Молекулярна формула сполук підтверджена елементарним аналізом, і д) для одержання сполук загальної формули структури були виразно підтверджені дослідженIE, де Аг, R1, R2, R3, R4, R5, R6, R7, R8, R, E, m, п, о і нями IR, ІН-і 13С-ЯМР р мають ті ж значення, які визначені вище, сполуки загальної формули X і XI піддають реакції, де Аг, Матеріали можуть бути формульовані як неR1, R2, R3, R4, R* R6, R7, R8, E, m, п, о і р мають ТІ залежні композиції або в суміші з іншими відомими ж значення, які визначені вище, Н і І являють соартроподицидними активними інгредієнтами, і згібою груп, ПІДХОЖІ для формування дно з метою заявки, можуть бути використані ВІДОМІ ноем й ІНШІ додаткові матеріали Таким чи-N 18 17 49864 ном, відомими способами можуть бути отримані Підхожий алкініловий спирт розчиняли у сухоконцентрати емульсій, мікроемульсм, пил, аерозому бензолі, додавали піридін і охолоджували сулі, пари і дими [Phone Poulenc-Geronazzo Surfacміш до 0 - 5°С До цієї суміші додавали ацил хлоtant and Specialities for Plant Protection, Application рид з такою швидкістю, що внутрішня температура Manual (1994), ICI Surfactants, Application Manual не перевершувала 5°С Реакційну суміш перемі(1992)] шували при кімнатній температурі протягом ночі, відфільтровували пдрохлорид піридину, що випав У рамках заявки препарат, що містить сполуку в осад Фільтрат нейтралізували розчином хлоризагальної формули І, і препарат, що містить ВІДОМІ ду натрію, висушували на МдЭСч і випарювали активні шгредієнт(и), можуть бути використані Матеріал очищували хроматографією один після одного, або шляхом одержання їхньої суміші великого об'єму Б) Для демонстрації рамок нашого винаходу ми 6 ммоль кислоти розчиняли у 20мл сухого ТГФ представляємо наступні приклади без обмеження і додавали 1,0г (6 ммоль) діетил азодикаррамок прикладів боксилату (DEAD) Суміш охолоджували на льодяній водяній лазні і додавали розчин 10 ммолей Приклади одержання алкінолу і 1,6г (бммоль) трифенілфосфшу у Юмл Чистоту сполук перевіряли методами TCL і ТГФ Характерний оранжевий колір DEAD постуGC (СР 9000, CP-SIL-5CB, 60м х 0,53тм, 5мл/хв пово зникав Розчин перемішували при кімнатній N2, FID, 220°C) Як показано, з використанням цих температурі протягом ночі, потім його розводили методів усі сполуки мали чистоту більш 95% 50мл етилацетату, промивали насиченим розчиСтруктуру матеріалів підтверджували дослідами ном хлориду натрію, висушували і випарювали З IR, ІН і С13-ЯРМ, молекулярні формули були підзалишку кристалізувався оксид трифенілфосфшу тверджені елементарним аналізом на додавання суміші гексан-етил ацетат Фільтрат 1 АЛКІНІЛОВІ ефіри очищували колоночною хроматографією Загальна процедура А) сполука 11501 1,2 502 Мр(Си) IR v(cm ') 13C-NMR5(ppm) 52 34 (OCH2-C=), 74 92 2 51(1Ht,J = 2 4Hz, =C(=CH), 77 81 (OCH23270, ЗОЮ, 2922,2853, Н), 4 88 (2Н d J=2 4Hz, C=), 101 85(OCH2O), 2124, 1726, 1625, 1606, ОСН2-С=), 6 03 (2Н, s 2-пропініл 1,3107 99, 109 59(C-4C69-70 1501, 1445, 1373, 1279, ОСН2О), бензодюксол-57) 123 29(C-5), 125 71 1263, 1157, 1103, 1076, 6 83(1H,d,J=8 2Hz) карбоксилат (C-6), 147 74(C-3a) 1039, 762 7 47(1H,d,J=1 6Hz), 151 91 (C-7a), 165 07 7 66(1 Н, dd,J-8 2 1 6Hz (CO ефір) 3 65(=C-CH3), 53 19 1 86(3H,t,J=2 3Hz, =C(OCH2-C=), 73 33 CH3), 4 84(2H, q, 3016, 2959, 2920,2244, (OCH2-C=), 83 17(=СJ=2 3Hz, OCH2-C=), 1714, 1626, 1606, 1508, 2-бутиніл 1,3СНз), 101 81(ОСН2О), 6 03(2H,s, OCH2C=), 63-64 1450, 1372, 1276, 1240, бензодюксол-5107 95, 109 62(С-4,С1163, 1117, 1078, 1036, 6 83(1H,d,J=8 2Hz), карбоксилат 7), 123 69(С-5), 125 62 970, 925, 758 7 47(1H,d,J=1 6Hz), (С-6), 147 72(С-За), 15 7 67(1 H Dd J=8 2, 1 6Hz)1 78(С-7а), 165 33 (CO ефір) ррт - означає тут і далі по тексту - частин на мільйон 2 Алкініл-аміди Загальна процедура Розчин ацил хлориду піддавали реакції з розчином алкініламшу у присутності піридину, при кімнатній температурі Суспензію розбавляли, 1H-NMR5(ppm) промивали послідовно водою, розведеним розчином пдрохлорної кислоти й розчином гідрокарбонату натрію, висушували, випарювали й очищували хроматографією й кристалізацією 19 20 49864 Таблиця Сполука 21523 2 2535 2 3541 2 4542 М-(2-бутиніл)-3,4метилен-дюксибензамід Мр(С°) 143-144 1 82(3H, t,J=2 4Hz CH3-C=),4 16(2H m, 3334 3075 2918, 1641, NH-CH2-C=) 6 02(2H 1620 1605, 1546, s, (CH2O)2), 6 23 (NH) 1500, 1485 1313, 681 (1H,dd,J=0 6, 7 8 1264 1239, 1042 Hz, H-4), 7 28-7 34 (2H M, H-6, H-7) І\І-(2-бутиніл)-2нафтамід 1 08(3H,t,J=2 1 Hz, 3295 (NH), 3055 2922 CH3-C=),3 38(1H,sNH) 2913 2850 1641, 1629 4 10(2H m CH2-C=), 133-134 7 60 (2H m) 8 0 (3H 1602, 1541, 1414, 1309 776 756 m), 8 49(1 H, s H-1), 9 03(1 H t J=5 3Hz) N-(2-nponmin)-1нафтамід 3229 (NH), 3046 2963 2927 2118 1635 161S 1590 1576 105-106 1531 1415 1301 1245 1033 788 773,759 519 Г\І-(2-бутиніл)-1нафтамід 1 83(3H,t J=2 1 Hz, 5276 (NH), 3046, 3011, CH3-C=), 4 25 (2H q 2917 2856, 1632 1618, J=2 1HzCH2-C=) 6 25 120-122 591 1577,1522, 1444, (1H, s NH) 7 31-7 60 432, 1287, 1258 783 (3H m) 7 85 (2H m), 3 32(1 H, m) З АЛКІНІЛИМІДИ Загальна процедура До розчину фталиміду у сухому ДМФ додавали 1 молярний еквівалент сухого карбонату калію і до цієї суспензії капельно додавали розчин толуоСполука 31537 IH-NMR 5(ppm) IR v(cm ') М-(бут-2-ініл)фталимід 2 27(3H t J=2 4Hz HC=), 4 24(2H q J=2 4 СН2-С^), 6 52(1H broads NH) 7 35(1 H t j=8 1 Hz) 7 50(3H m) 7 84 (2H m) 8 26 (1H m) лу в 1 молярному еквіваленті алкініл броміду Суспензію перемішували при 80°С протягом 3 годин, потім її переливали на крижану воду, збирали кристали і кристалізували з 96% етанолу 1H-NMR5(ppm) IR v(cm ') 3090, 3040 (Н-С ароматич) 2957, 2920 (СН 1 76(ЗН, t, J=2,3Hz аліфат), 2234 (С=С) СН3-С=), 4 32 (2Н q, 1768 1718 (CO), J=2 3 Hz, N-CN3-C=), 216-218 1609(С=Сароматич) 1468, 1431, 1397, 1354, 7 86-7 91 (4H m, apoматич ) 1333, 1126, 1090,952, 775, 732, 712, 629, 560, 532 Мр(С°) 4 (Арил-алкіл)-, алкіл-алкініл ефіри 4 0 Одержання 1 -[(2-бутинілокси)-етил]-3,4диметоксибензолу (сполука 599) У колбі об'ємом 50мл, що містить термометр, магніт для перемішування, лійку і з'єднаній із системою інертного газу, готували суспензію ЗОмл сухого ТГФ і 1,5г (0,063моля) NaH (cca 90%) До суспензії крапельне додавали розчин 4,0г (0,021 13C-NMR5(ppm) 3 54 (CH3-C=), 30 37 (NH-CH2-C=), 74 72 and 79 77(C=C) 101 73 (OCH2O), 107 72 108 02(C-4C-7), 121 70(C-6), 128 26(C5) 148 01 (C-5a) 150 49(C-7a), 166 37 (CONH) 3 27 (CH3-O) 29 11 (CH2-C=), 76 77 and 78 07(C=C), 124 29 (C3), 126 90, 127 82 перекриття трьох сигналів 128 08 129 07 131 51 (C-4a) 132 32(C-2) 134 37(C-8a) 166 07 (CO) 29 62 (-CH2-C=) 71-80 (H-C=C) 79 43 (H-C=C) 124 59 125 29, 125 29 126 41 127 14, 128 28 130 06(C-8a) 130 85 (C-2) 133 34(C-1) 133 59(C-4a) 16914 (CO) 3 50 (CH3-C=) 30 24 (CH2-C=) 74 47 and 79 81 (C=C) 124 59 125 19 124 62 125 09, 125 37 126 39, 127 10, 128 26 13011 (C-8a) 130 75 (C-2) 135 64 and 133 75(C-1,C-4a), 169 03 (CO) 13C-NMR5(ppm) 3 12(CH3-C=) 27 16(NCH2-C=) 73 82 (CH3-C=), 79 06 (CH2-C=), 123 48 (C-3C-6), 131 64(C-1 C2), 134 87(C-4 C-5) 167 01 (CO) моля) а-метилвератри-спирту у 21 мл сухого ТГФ при кімнатній температурі Суміш нагрівали при ВІДЛИВІ протягом 1 години, охолоджували до кімнатної температури, додавали 4,1г (0,0315 моль) 1-бромо-2-бутину, потім продовжували нагрівання За реакцією слідувала TIC (елюент гексан- ЕЮАс 4 1) Реакцію закінчували приблизно через 3-4 години 21 49864 22 До охолодженої мутної суспензії додавали 1Н-ЯМР (200 МГц, CDCI3)d 50мл ефіру, суміш фільтрували на Целіті, фільт1 46 (ЗН, d, J=6 5 Гц, СН-СНз), 1 85 (ЗН, t, рат промивали дистильованою водою, висушуваJ=2 3Гц, =С-СН3), ли на сульфаті магнію і випарювали Залишкове 3 83 і 4 01 (2Н, АВХз JAB = 1 5 0ГЦ, JAX = масло очищували колоночною хроматографією JBX=2 ЗГЦ, =С-СН2О), 1 (елюент гексан-ЕЮ Ас 4 1,R = 0 37) 3 87 І 3 89 (сума 6Н, s кожний ОСН3) Вихід 2,3Г (9,8ММОЛЬ), 46 9% 4 55 (2Н, q, J=6 5Гц, Аг-СНО), Чистоту продукту перевіряли аналізом GC 6 80-6 89 (ЗН, т, ароматичний) 13 (СР 9000, CP-SIL-5CB, 60м х 0 53глм, 5мл/хв N2, С-ЯМР (50МГц, CDCI 3 )d FID, 250°C)tR=12 Охв, >99% 3 61 (=С-СНЗ), 23 76 (СН-СНз), 55 87 (ОСНЗ), 55 96 (С-СН2), Підтвердження структури Елементарний аналіз (С14Н17О3, 233 29) 75 36 (=С-СН2), 76 40 (Аг-СН-СН3), 81 91 (=ССНЗ), 109 06(С-2), підраховано С% 72 08, Н% 7 35 виявлено С% 69 70, Н% 7 21 110 86(С-5), 118 94(С-6), 135 30 (С-1), 148 52(С-3), 149 19(С-4) IR (CHCI )VCM 2976, 2855, 2837, 1605, 1595, 1514, 1465, 1419, Аналогічно тому, як описано у Прикладі 4 0, ми 1371, 1353, 1311, 1260, 1164, 1141,1086, 1027, 864 одержали наступні сполуки 1 3 І сполука Мр(С°) IR v ( c m ') 1H-NMR5(ppm) 13C-NMR5(ppm) 1 93(3H,t,J=2 3Hz, C=C 1-нафти лметил 241279 бутиніловий ефір масло 3044, 3 0 0 1 , 2945, 2920, 2854, 1598, 1509, 1356, 1166, 1086, 1067 1-[1-(24 2- бутинілокси)масло 292 етил]нафталін 3052, 2977, 2 9 2 1 , 2856, 1596, 1509, 1444, 1 3 7 1 , 1095, 1078 1-[1-(24 3- бутинілокси)пропіл]454 нафталін ОЛІЯ 1-[2-метил1(24 4- бутинілокси)472 пропіл]нафталін ОЛІЯ 3058, 2962, 2876, 1509, 3048, 2932, 2S56, 1460, 1062 3000, 2923, 1598, 1105, 3051, 2959, 2922, 2871, 1598, 1509, 1466, 1064 СНз) 4 22 (2H q 3 6 (С^С-СНз), 57 71 (О-СНзJ=2 1HzO-CH2-C=C) C^C), 69 72 C10H7-CH2-O), 5 06(2H s C10H7-CH2-O), 75 10 (O-CH2-C=C), 82 76 (O7 45(1 H t J=8Hz), 7 53 СНз-С^С), 124 03 12510 (3H, m), 125 72 126 19, 126 85 128 43 7 84(1H,d J=8 1Hz), 7 88 128 72 131 79(C-8a), 133 06, (3H, m) 7 88 133 70 (1Hd,J=7 7Hz)8 19(1H, d, J=8 2 Hz) 1 67(3H d J=6 5Hz, CH3CH), 1 87(3H,r J=2 3Hz=CCH3), 2 96 and 4 15 (summa 2H ABX,JAB=15 0 3 64 (С^С-СНз), 22 96 (CH3Hz JAX=JBX=2 3 H Z OCH2- CH), 56 37 (O-CH2-C=C), 74 29 (СНз-СН), 75 36 and 82 14 CvC) 5 40(1 H (C^C), 123 26(C-8), 123 52, q,J=6 5Hz C10H7-CH-O), 125 50 125 85 127 92, 128 83 7 51 (3H m) 7 61 130 78(C-8a), 133 88(C-4a) (1H,d J=6 8Hz) 138 42(C-1) 7 79(1Hd J=8 1Hz) 7 89 (1H dd, J=7 9 1 8 Hz) 8 22(1Hd J=8 1 Hz) 1 02(3H, t,J=7 4Hz CH33 59(C=C-CH3) 10 62(СНзCH2) 1 89(3H t J=2 3Hz CH2) ЗО 27 (СНз-СНз) 56 54 С^С-СНз) 2 03 (2H (О-СН2-С=С) 75 50(О-СН2тСНз-СНз) 3 95 and 4 17 С^С) 80 08 і 81 96 (ОСН- на(summa 2H ABXJ A B =15 0 фтил і О-СН2-С=С) 123 43 (СHz, JAX=JBX=2 3 H Z OCH28), 124 40 125 31 125 36 C=C) 5 15(1HtJ=6 4Hz 125 73, 127 91 128 79 131 19 C10H7-CH-O), 7 53 (3H m) (С-8а), 1 33 88 (С-4а) 7 59(1H, d), 7 81 (1H,d), 137 12(С-1) 7 89(3H, m) 8 27(1 H, d) 0 87 and 1 16 (summa 6H, d each, J = 6Hz, CH(CH3)2), 1 88(3H, t,J=2 3Hz, C^C3 57 (С^С-СНз), 19 87 and CH3), 2 31(1H, m, 18 77(СН(СН3)2), 34 20 CH(CH3)2) 3 89 and 4 14 (СН(СН3)2), 56 7 (ОСН2) 75 67 (2H summa ABX3 JAB(С=С-СНз),81 77 (С^С-СНз), 15Hz JAX=JBX= 2 3Hz, 123 84(С-8), 125 15, 125 31 OCH2), 4 92(1H,d J = 6Hz, 125 39 125 60 127 91 (С-4), CH-O), 7 53(4H,m), 128 76(С-5) 131 74(С-8а) 7 83(1Hd J=8Hz), 133 87(С-4а) 136 56 (С-1) 7 91(1Hdd J=7 2Hz) 8 30(1Hd J=7 6Hz) 23 І сполука Мр(С°) 1-[(1-метил )(24 5пропшілокси)389 метил]нафталін ОЛІЯ 2-[1-(24 6- пропшілокси)256 етил]нафталін ОЛІЯ 2-[1-(24 7- бутинілокси)етил]293 нафталін ОЛІЯ 5-[(бут-2Ішлокси)метил] 1 3бензодюксол ОЛІЯ 4 8441 5-[2-метил-1(24 9бутинілокси)484 пропіл]-1,3бензодюксоль ОЛІЯ 5-[(бут-2ІНІЛОКСИ) 410 554 циклогексилметил]-1,3бензодюксоль 5-[(бут-2ІНІЛОКСИ)411555 феніл-метил]1,3 ОЛІЯ ОЛІЯ 49864 IR v ( c m ') 1H-NMR5(ppm) 24 Продовження таблиці 13C-NMR5(ppm) 1 5 1 ( 3 H d J=6Hz) СНз, 2 5 6 ( 1 H d J=2Hz), 22 1 СНз 64 25 OCH 68 99 CH 4 30(H qxd CH 73 34 aryl-CH 2 83 71 CH-C 3306, 3049, 2990, 293, J=6 2Hz)OCH 4 91 and 124 11 C-8 127 1 7 C - 2 2866, 1599, 1510, 5 34 (2H 125 74 C-3 126 18 C-6 1441, 1374, 1327, AB J A B =15Hz)OCH2 7 46 126 92 C-7 4 128 47 C-4 1099, 1064 (1H,dd,J=7 8Hz) 7 54(3H 128 75 C-5 131 88 C-8a m) 7 86(2H m, 8 18(1H, 133 20 C-4a, 133 77 C-1 mxd J=6Hz) ароматичний 1 58(3H,d,J=6 5Hz, СНзC H ) 2 44(1Ht, J=2 4Hz) 23 66 (СНз-СН), 55 55 (O-CH 2 3307, 3000, 2979, C H 3 92(1H,dd J=2 4 C^C), 74 07 and 76 80 (CH-O 2929, 2857, 1603, 15 7 H z ) O C H a 1505,1442, 1373, CCH) 79 98, (CCH), 124 11 (CC = C 4 13(1H dd,J=2 4 1311, 1270, 1215, 6), 125 60 (C-7), 125 90, 15 7Hz), OCH b 1087, 1055, 8 6 0 , 8 2 1 , 126 15, 127 68 127 85, 128 5 C = C 4 84(1H, q,J=6 5Hz, 633 133 16 133 21,139 75 (C-1) C10H7 CH-O), 7 50(3H, m), 7 77(1H,s), 7 85(3H, m) 1 57(3H d J=6 5Hz, CH33 64 (С^С-СНз), 23 78 (СНзCH) 1 8 7 ( 3 H t J = 2 3Hz, СНз-С), З 90 and 4 08(1- СН) 56 23 (O-CH 2 -C=C) 75 28 (С^С-СНз), 76 72 (СН-СНз), 3051, 2977, 2920, 1H, A3X3, J=15,2 3Hz 82 10 (С^С-СНз), 124 14 (С-6) 2854, 1602, 1444, ОСНаь-С^С), 1084 4 79(1H,q,J=6 5, C10H7-CH- 125 42 125 78 126 05 127 64 127 80 128 40 33 07 (С-4), O) 7 49 (3H, m) 133 19С-8), 140 14(С-2) 7 77(1H,bs,H-1), 7 85(3H,m) 1 87(3H t J=2 3Hz Me) 3 52 (Me) 57 29 (О-СН2-С=) 4 1 0 ( 2 H q J=2 3HzO-CH 2 2997, 2946, 2 9 2 1 , 71 15(О-СН 2 -Аг) 82 54(СН 3 2888, 2376, 1609, C=) 4 47(2H s О-СН2-АГ) С=), 100 9С-2, 107 95, 1503, 1 4 9 1 , 1445, 5 94 (2H s O-CH2-O), 6 76 108 71 (С-4 7), 121 66 (С-6) 1251, 1099, 1070, ( 1 H d J=8HzH-7), 131 39(С-5) 147 15, 1042, 937, 865, 810 6 8 1 ( 1 H d d J=815Hz,H147 66(СЗа, С-7а) 6),686(1H,J=1,5HzH-4) 0 63 and 0 94 (summa 6H,d each J=6 8Hz, CH(CH 3 ) 2 ), 1 76(3H,t,J=2 3Hz C^CCH3), 1 81(1H,m, 3 58(С=С-СНз) 18 93 and CH(CH 3 ) 2 ), 3 69 and 3 94 19 30((СН(СН 3 ) 2 ),34 42 (summa 2H (СН(СН 3 ) 2 ), 56 20 (ОСН 2 ), 2958, 2 9 2 1 , 2874, A B X 3 , J A B = 1 5 1HZ, 75 48 (С=С-СН 3 ),81 66(С=С1608, 1502, 1486, JAX-JBX-2 3 H Z СН 3 ),86 25(СН-О), 100 85 1 4 4 1 , 1 0 7 6 , 1 0 4 1 , 9 4 0 OCH ),3 8 6 ( 1 H d J=7 8Hz 2 (ОСН 2 О), 107 44, 107 63(С-4, CH-O) 5 87 (2H AB 7), 121 29 (С-6), 134 48(0-5), OCH 2 O), 6 6 2 ( 1 H d d J=7 9, 146 88 and 147 63(C-3a, 7а) 1 6Hz, 6-H) 6 68(1H,d,J=7 9Hz7-H) 6 7 1 ( 1 H d J=1 6Hz 4-H) 0 84-1 31 (6H m) 1 503 64(С=С-СН 3 )25 93 and 26 05 1 77 (4H m) 1 83 (3H t (С-2' С-61) 26 52 (С-3) 29 25 J=2 3Hz =С-СНз) and 29 86 (С-3' С-51) 43 97 (С2920 2877, 2 8 5 1 , 2 08(1 H m H-1), 3 76 and '), 56 19(ОСН 2 ) 75 5 7 ( С = С 1610, 1502, 1485, 4 01 ( A B X 3 , J A B = 1 5 H Z СНз) 81 64(С=С-СНз) 85 45 1441, 1357, 1243, JAX-JBX-2 3HZ(СН-О) 100 8 8 ( О С Н 2 О ) 1 1 3 2 , 1 0 6 4 , 1 0 4 0 , 9 4 2 OCH 2 ),3 98(1Hd,J=8 3Hz 107 47 and 107 64 (С-4 С-7) CH-O) 5 97 (2H 121 31 (С-6), 134 48 (С-5), s,OCH 2 O) 6 65-6 78(3H, 146 91 and 147 69 (С-За С-7а) m) 1 89(3H, t,J=2 3 H z - C - 3 69 (С^С-СНз) 56 34 (ОСН2), 2993, 2887, 2859, 1605, 1502, 1486, CH 3 ),4 12(2H,q J=2 3Hz, 75 12 (С=С-СН 3 ),81,23 (С=С1442, 1357, 1239, СНз), 82 56 (СН-О) 100 99 OCH 2 ), 5 56(1H,s,CH1037, 937 (ОСН 2 О), 107 78 and 107 95 O),5 93 (2H, s OCH 2 O), 25 (2-бутинілокси-метил)4 123,4493 диметоксибензол Олія 2,6-дихлоро 4 13- 1-(2-бутині503 локси-метил) ОЛІЯ 1-(2бутинілокси4 14- 1,2,3,4498 тетрапдронафталін ОЛІЯ 4 15- 1-(2-бутині479 локси)-шдан ОЛІЯ бензол 2-[(2-бутині 4 16- локси)510 метил]-1 4 ОЛІЯ бензодюксан 2-(бутині локси-метил)-2,3дипдробензофуран 26 (C-4, C-7), 120 98 (C-6), 127 01 (C-2' C-61), 127 50 (C-41) 128 36 (C-31, C-51), 35 54 (C-5') 141 62(C-1') 147 05 and 47 83 (C-3a, C-7a) 3 45 (С^С-СНз) 55 67 and 1 84(ЗН t J=2 3Hz C=C55 71 (CH3O) 57 31 (OCH2C=C3025 3000 2956 2937 СНз) 3 83 and 3 85 ) 71 22aryl-CH2) 75 0 (C^C2921 2855 2339 1607 (summa 6Н СН3О), 4 08 1595 1512 1466 CH3) 82 42 (С^С-СНз) 110 76 (2H,q,J=2 3Hz ОСН2С=С) 1443 1420 1158 (C-2) 111 23(C-5) 120 54(C4 48(2Н, s aryl-CH2) 6 771140 1070 11028 6) 130 05(C-1) 148 58 (C-4), 6 88(ЗН т , aryl) 148 88 (C-3) 3 64(=C-CH3),58 68 (OCH21 87(3H,tJ=2 3Hz,=C2931,2918 2881,2849, C=)66 15(C6H4CI2-O-CH2), CH3),4 21(2Hz, J=2 3Hz, 2241 1584, 1563, 74 94 (OCH2-C=) 82 81 (=CОСН2-С=), 4 83(2H,s, 1473 1356 1198, CH3), 128 33 (C-3, C-5), 129 96 СбН4СІ2-О-СН2), 1157,1091, 7 17(1H,dd, J=91 6 7Hz), (C-4), 133 17 (C-2, C-6), 136 97 1073,787,769 (C-1) 7 31(2H,m) 3 45(C=C-CH3), 55 67 and 1 84(3H U=2 3Hz, C=C55 71(CH3O), 57 31 (OCH2C=CСНз), З 83 and 3 85 2998 2941 2860 1604 (summa 6H CH3O), 4 08 ), 71 22(aryl-CH2) 75 0 (C=CCH3), 82 42(С=С-СНз) 110 76 1489 1440, 1070 (2H, q, J=2 3Hz (C-2), 111 23 (C-5) 120 54 (C1044 OCH2C=C-), 4 48(2H s aryl-CH2), 6 77-6 88(3H m 6), 130 05 (C-1), 48 58 (C-4) 148 88 (C-3) aryl) 1 91(3H,t,J=2 3HzC=CCH3),2 15(1H, dddd J=13 2 8 4, 4 8, 3 8Hz, 2H) 2 37(1 H dddd J=15 8 3 52(C=C-CH3),30 11(C-2) 3073, 3000, 2938, 4 6 5,6 5Hz, 2-H), 2 83(1H 32 25(C-3), 56 14(OCH2) 75 45 ddd, J=15 8 8 4 4 8 H z 3 (С^С-СНз) 81 68(C-1) 2924, 2854, 2243, H),312(1H ddd,J=1572, 1711, 1667, 1608, 82 15(C=C-CH3), 124 80 8 4, 3-H), 1461, 1332, 1097, 125 16(C-5 6) 126 11 4 21(2H,q J=2 3Hz, 1063, 1018 128 36(C-4 7), 14210 OCH2),5 14(1H, dd, J=6 5, 144 14(C-3a,7a) 3 7Hz1-H), 7 23(1H,m) 7 28(2H, m),7 45(1Hd J=7 Hz) 49864 6 74-6 86 (ЗН, т ) , 7 257 39 (5Н, т ) бензодюксоль ОЛІЯ 1 87(3H,rJ=2 4Hz 3 70 3 57(H3C-C=) 59 43 (O-CH2and 3 80(2H, C=), 65 58(CH-CH2-C) 68 12(CABX,JAB=10 1Hz 2996, 2921, 2358, JAX=JBX=5 0HZ CH-CH2-O) 3), 71 96 (C-2), 74 54 (CH2-C=) 2222 1594, 1492, 4 05(1Hdd J=7 6 11 8Hz 83 22 (H3C-C=), 117 12, 117 40 1466, 1269 1097, H-3(J), 4 20(2H d J=2 3Hz (C-5andC-8), 121 37 121 56 1043 O-CH2-C=), 4 28-4 41 (2H, (C-6 and C-7), 143 07, 143 21 (C-4a, C-8a) m, H-3aH-2a) 6 81-6 92 (4H m C6H4) 2 65(1H,tJ=5 4Hz, OH), 2 97 and 3 25 (summa 2H 3598, 3478 (broad), ABX J AB =15 6Hz JAX=9 4 3080, 3040, 2996, 31 18(C-3), 64 77 (CH2-OH), Hz, JBx=7 5HZ H-3), 3 79 2952, 2871, 1611, 83 02 (C-2), 109 36(C-7), (2H, m, CH2-OH), 4 90(1 H 1598, 1481, 1462, 120 54 (C-5), 124 97 (C-6), m H-2), 6 79 1232, 1092, 1050, 126 48(C-3a), 127 95 (C-4), (1H,d,J=8 0Hz),6 87 1012, 1004, 954,899, 159 08(C-7a) (1H,td,J=7 5, 0 8 Hz), 7 11 865 (1Hd J=7 8Hz), 7 16(td, J=7 2 0 5Hz) Сполука 4 18330 4 19331 Mp(C°) IR ( c m ') [а] 3-(-)-1-[1-(2-бутинілокси)-етил]-нафталін ОЛІЯ як 4 2 292 (-)78°(с=1 МеОН) Р(+)-1-[1-(2-бутинілокси)-етил]-нафталін ОЛІЯ як 4 2 292 (+) 155°(с=1, хлороформ 27 49864 28 Продовження таблиці [а] Сполука 4 20456 Мр(С°) IR ( c m ') 3-(-)-2-[1-(2-бутинілокси)-етил]-нафталш ОЛІЯ як 4 7 293 (-) 190 8° (с=1 0 хлороформ ОЛІЯ як 4 7 293 (-) 199 0° (с=1 17, хлороформ ОЛІЯ як 4 6 256 (-) 224 4° (с=1 18, хлороформ 28-29 як 4 6 256 (+) 228° (с=1 хлороформ 4 21Р-(+)-2-[1-(2-бутинілокси)-етил]-нафталш 455 4 223-(-)-2-[1-(2-пропінілокси)-етил]-нафталш 474 4 23Р-(+)-2-[1-(2-пропінілокси)-етил]-нафталш 475 5 Ароматичні ПОХІДНІ алкіл-алкіл-алкініл-амшу Загальна процедура Амін розчиняли в сухому бензолі, додавали алкініл бромід і перемішували суміш при кімнатній Сполука 51251 Мр(С°) І\І-а-диметил-г\І2-пропініл-Ьнафтилметиламш 51-53 IR (cm ') 3173, 5053, 2970,2941, 2837, 2788, 1600, 1444, 1433, 1371, 1334 1295, 1227, 1123, 1074, 1011, 969, 952, 935, 900, 863, 827, 754, 734, 713, 557, 482 6 Арил алкінілові ефіри Загальна процедура А) Підхожий фенол розчиняли в сухому ДМФ і додавали до розчину сухої К2СО3 і до підхожого галогеніду алкінілу Реакційну суміш нагрівали до 60°С і перемішували при цій температурі протягом 3-6 годин ДМФ далі дистилювали у вакуумі, відбирали залишок у суміші хлороформу і дистильованої води Фази розділяли, водяну фазу ДВІЧІ екстрагували з хлороформом, об'єднані органічні фази промивали послідовно водою і насиченим розчином хлориду натрію, висушували на MgSC^ і випарювали Грубий продукт очищували хроматографією Б) РпзР розчиняли в сухому бензолі в інертній атмосфері і добавляли до розчину ВІДПОВІДНИЙ спирт і потім фенол Суміш охолоджували до 010°С і повільно, малими порціями додавали DEAD (діетил-азодикарбоксилат), підтримуючи температуру нижче 10°С Реакційну суміш перемішували протягом 10-24 годин Результат осаджений РпзРО відфільтровували, фільтрат промивали водою, висушували й випарювали Залишок хроматографували Сполука 61547 1-(3-бутинілокси 4-нітро-бензол температурі Далі, її розбавляли водою й ефіром, фази розділяли, водяну фазу ДВІЧІ екстрагували ефіром, об'єднані органічні фази ДВІЧІ промивали водою і висушували на 1H-NMR5(ppm) 1 455(ЗН, d,CH-Me), 2 271(1Н, s CCH), 2 360 (ЗН s NMe), 3 253-3 302 and 3 487-3 530 (2Н СН2), 3 708-3 757 ( І Н т С Н М е ) , 7 260-7 834 (7Н т ароматичний 13C-NMR5(ppm) В) 0,01 молю фенолу розчиняли в 7мл сухого ацетонітрилу і охолоджували до -4°С в 25 атмосфері аргону Далі до розчину додавали 1 968г (0 0129 молю) DBU, підтримуючи температуру нижче -4°С До розчину додавали 1 8г МІДІ (II) і паралельно готували трифторацетат іншого реактанту 0 0115 молю алкініл-спирту розчиняли в 7мл ацетонатрилу й охолоджували розчин до -5 °С, під атмосферою аргону До розчину додавали 1 968г (0 0129 молю) DBU, при підтримці температури нижче -5 °С До суміші крапельне добавляли 1 6г (0 0115 молю) трифторацетатного ангідриду, підтримуючи температуру нижче 2°С Отриману суміш перемішували при 0°С протягом ЗО хв Отриманий у такий спосіб розчин трифторацетату крапельне додавали до першого розчину, підтримуючи температуру нижче 0°С і, перемішували суміш при 0°С протягом 5 годин Після реакції слідувала TLC Наприкінці реакції ацетонітрил дистилювали у вакуумі Залишок перемішували із сумішшю 150мл бензолу і 50мл води Органічну фазу промивали послідовно IN пдрохлорною кислотою, IN гідроксидом натрію, водою і насиченим розчином хлориду натрію, потім висушували й випарювали Продукт очищували хроматографією Мр(С°) 1R (cm ') Q9 QA 3287, 3111, 3085,3075, 2964, 2947, 2920, 1609, 1596 1510 1466, 1344 1333 1263, 1179 1110, 1019, 856, 846, 753, 669 653 1H-NMR5(ppm) 2 07(1H,t,J=2 6Hz C=C-H) 2 73 (2H, td J=6 8 2 6Hz CH2C=C) 4 18(2HtJ=6 8Hz, OCH2), 6 97 and 8 18 (summa 4H dm, J=9Hz C6H4) 13C-NMR5(ppm) 1937(C=C-CH2) 66 60 (C=CH) 70 38 (OCH2) 79 62(C=CH) 114 51 (C-2 C-6), 125 89(C-3 C-5), 141 73(C-4) 163 40(C-1) 29 Сполука 6 2- 143-пєнтинілокси)540 4-нітро-бензол 6 3377 6 4418 2,3-дипдро,2,2диметил-7-(3бутинілокси)бензофуран 2,3-дипдро-2,2диметил-7-(3пентинілокси)бензофуран 49864 Мр(С°) 77-78 78-80 58-59 5 1R (cm ') 3277, 3071, 3043,2970 2923, 2889, 2858,2119, 2022, 1874, 1795, 1714, 1656, 1624, 1611, 1591 1492, 1470, 1440, 1492, 1396, 1385, 1371, 1302, 1283, 1244, 1201, 1172, 1128, 1077, 999,972, 946, 887, 838, 780, 753, 720, 682, 663, 635, 600, 546, 502, 458 7,2572 1-ацето-нафтоноксим-(2бутиніл)-ефір 3,4-диметоксиацетофенонокси т-(2-бутиніл)ефір 1 512(6H,s,diMe), 2 033(1H,t,CH), 2 710(2H,m-CH 2 C), 3 027(2H,s,CH 2 -ar) 4 206(2H t, O-CH2), 6 739-6 815(3H,m, ароматичний 2977, 2963, 2942,2918, 1 510(6H,sdiMe) 2880, 2849, 1621, 1591, 1 800(3H, t Me) 1492, 1468, 1389, 1369 2 627-2 672(2H m 1329, 1305, 1286, 1245, CH 2 C) 3 023(2H s 1203, 1174, 1135, 1115, CH 2 -ar),4 150(2Ht O1080, 1065, 966,947, 8 8 1 , CH 2 ) 6 751-6 784 (3H 860, 8 4 1 , 779, 751, 718, m, ароматичний 634, 598, 532, 499 Загальна процедура Оксим переводили в ефір оксиму класичним способом, шляхом реагування його з алкініл бро 7,1571 1H-NMR5(ppm) Продовження таблиці 13C-NMR5(ppm) 3 57 (С^С-СНз), 19 61 1 78(3H,t,J=2 3Hz, (C=C-CH 2 ) 67 26 3067, 3048, 2963,2917, С^С-СНз) 2 66(2Н, 2886, 1923 1607, 1594, (OCH 2 ), 74 27 (C=Cm,CH 2 C=C),4 1 2 ( 2 H t 1512, 1467, 1403, 1339, CH3), 77 84 (С^С-СНз), J=7 OHz ОСН 2 ), 6 95 1260, 1178, 1110,866, 856, 114 49(C-2, C-6), and 8 18 (summa4H, 753, 694, 648, 628, 522, 506 125 85(C-3C-5), 141 59 dm, J=9Hz, C 6 H 4 ) (C-4), 163 59(C-1) 7 АЛКІНІЛ-ОКСИМ ефіри сполука ЗО 19 12(CH 2 -C),27 88 (diMe) 42 93 (C-3), 66 79(C-2), 69 61(0CH 2 ) 79 96 (CCH), 87 06 (CC), 113 31 (C-6), 117 86(C-5), 119 99 (C4), 128 36(C-9), 142 62 (C-7), 147 52(C-8) 3 471 (Me), 19 6 3 ( C H 2 C), 28 18(diMe) 43 26 (C-3), 67 54 (C-2), 74 82 (CC-Mc) 77 32 (O-CH 2 ) 87 26(CC) 113 21 (C-6) 117 87(C-5), 120 2 5 ( C 4) 128 48(C-9) 143 12(C-7), 145 00(C-8) мідом у диметил формаміді, у присутності карбонату калію (Див спосіб А при одержанні ефірів нафтилу) Грубий продукт у кожному випадку очищували колоночною хроматографією Мр(С°) IR (cm ') Олія 2990,2919, 2853,2230, 1604, 1591, 1459, 1436, 1363, 1353, 1309, 1252, 1034, 1017, 1002,912 85 3080, 3003, 2963, 2929, 2869, 2840, 2237, 1595, 1577, 1518, 1447, 1417, 1337, 1311, 1278, 1249, 1234, 1176, 1153, 1030, 937, 879, 804, 768, 634, 621 Результати активності Приклад 1 Дослідження синергічної активності на домашній мусі (Musca domestica) після поверхневого нанесення У двох рівнобіжних експериментах 10 жіночих осіб домашньої мухи, у ВІЦІ 2-4 днів, обробляли з бічного боку їхньої грудної частини 0 2 т л тест 1H-NMR5(ppm) 13C-NMR5(ppm) 3 80(CH 3 -C=), 17 51 (CH3-C=N) 62 25 (OCH 2 ), 75 33 (CH 2 -C=), 1 94(3H,t,J=2 3Hz, СНз82 75 (СНЗ-СЕЕ), 125 15, C=), 2 4 1 ( 3 H s , СНз125 46(C-6,C-7), 125 96 C=N), 4 8 4 ( 2 H , q, (C-3), 126 01 (C-3), J=2 3Hz, O-CH2), 7 46126 49 (C-2), 128 40 (C7 57(4H m) 7 87(2H, 5), 129 10 (C-4), m),8 15(1H,m) 130 85(C-1), 133 86 (C4a), 135 27(C-8a), 157 41 (CH 3 -C=N) 3 77(CH 3 -C=), 12 76 1 8 7 ( 3 H t J = 2 3Hz, CH3(CH 3 -C=N) 55 86 C=), 2 23(3H, s, CH3(CH3O), 62 23 (O-CH2), C=N), 3 88 and 3 90 75 27 (CH 2 -C=), 82 53 (CH3O), 4 75 (2H,q, (СН 3 -С=), 108 8(С-5), J=2 3Hz, O-CH2), 110 51 (C-2), 119 28(C6 83(1H,d J=8 4Hz), 6) 129 18(C-1), 148 78 715(1H,dd J = 8 4 2 H z ) (C-3), 150 14 (C-4), 155 0 7 29(1Hd,J=2Hz) (CH 3 -C=N) розчину, за допомогою мікропіпетки Hamilton MicroLab P Крім фіксованої синергічної дози в ЮООнг/муху тварин обробляли карбофураном у дозі 20нг/муху У якості розчинника був використаний целлосолв Селекцію й підрахунок мух проводили під впливом СО 2 Після обробки мух містили у пластикові чашки, покриті тюлем Смертність після 24 годин відображували в % Результати, продемонстровані в т а б л нижче 31 32 49864 карбофуран+синер речов (нг/муху) 20 + 0 20-1000 смертність Матеріал алкінілові ефіри, аміди, ІМІДИ 3 0 0 3 0 0 53 47 17 27 46 42 0 0 1 0 1 10 0 0 0 0 1 1 0 0 0 0 2 0 0 0 0 2 5 0 72 32 97 63 100 100 95 72 45 75 68 58 62 72 70 47 27 58 90 48 50 75 70 47 251 2 37 547 540 377 418 0 0 0 0 47 60 57 63 0 0 53 55 501 502 523 535 541 542 арил-алкіл-алкінілові ефіри 279 256 441 484 493 599 503 292 291 454 472 479 330 331 455 456 389 554 555 539 474 510 498 475 ароматичні ПОХІДНІ алкіл-алкіл-алкінмл-аміну ефіри арил алкініл ефіри аралкіл-алдоксим, кетоксим-алкініл 571 572 Приклад 2 Дослідження синергічної активності на черв'яку насінної коробочки бавовни (Hehcoverpa armigera) після поверхневого нанесення Обробку проводили подібним способом, як описано у Прикладі 1, але як тест-тварини були оброблені личинки стадії L2 черв'яка насінної коробочки бавовни (Hehcoverpa armigera) Значення даних доза-смертність LDso (нг/личинку) після 24 годин визначали пробіт-аналізом Жодна із синергічних речовин не діяла у використаній дозі ЮООнг/личинку Відношення синергічної речовини було підраховано як коефіцієнт значень LDso карбофурану, уведеного єдино й із синергічною речовиною Експерименти були проведені в 2-4 повтореннях Відношення синергічних речовин продемонстровано в таблиці нижче Матеріали алкініл ефіри, аміди 501, 502, 525, 535, 541, 442, 537 арил-алкіл алкіл-алкінілові ефіри 279, 256, 441, 484, 493, 503, 292, 293, 454, 510, 475, 498, 479 472, 331, 455, 456, 389, 554, 555, 539, 474, 330 599 ароматичні ПОХІДНІ алкіл-алкіл-алкініл-аміну 251 відношення синергічної реч >5 >5 >5 33 49864 34 Продовження таблиці Матеріали відношення синергічної реч Ефіри аїл-алкініл 540, 377, 413 алкініл-оксим ефіри 571 572 >5 >5 Приклад З Дослідження синергічної активності на домашній мусі (Musca domestica) і черв'яку насінної коробочки бавовни (Hehcoverpa armigera) після поверхневого нанесення Синергічні активності матеріалів N 279 і 599 цього винаходу для різних активних інгредієнтів визначали на домашній мусі (Musca domestica) і черв'яку насінної коробочки бавовни (Hehcoverpa armigera), використовуючи способи обробки, як описано в біологічних Прикладах 1 і 2 Для активних інгредієнтів ISO дані звичайні назви (див Посібник із Пестицидів (Pesticide Manual 1994) Отримані відношення синергічних речовин надані нижче 279 активний інгредієнт Карбофуран Бендюкарб Ізопрокарб Фенобукарб Аміно карб Тюдикарб Метоміл Піримікарб Дюксакарб Пропоксур Імідаклопрід Піндан Азінфосметил Хлорпірифос Есбюл перметрин Тетраметрин Musca domestica 599 Hehcoverpa armigera відношення синергічних речовин >20 > 10 >20 > 10 >40 >40 >40 >20 >20 >40 > 10 >20 > 10 > 10 >20 >20 >5 >5 >5 >5 >5 Hehcoverpa armigera відношення синергічних речовин Musca domesuca > 10 > 10 >20 >40 >5 > 10 >5 >5 >5 > 10 > 10 >5 >5 Приклад 4 Вплив активного інгредієнта відношення синергічних речовин до синергічної активності Обробку проводили, як описано у Прикладі 1, використовуючи мікродозатор Hamilton MicroLab Р У двох рівнобіжних експериментах 10 жіночих осіб домашньої мухи, у ВІЦІ 2-3 днів, обробляли з бічного боку їхньої грудної частини 0 2 т л тестрозчину Крім фіксованої синергічної дози в 1000 >20 >20 >20 >20 >20 400-200-80нг/муху, їх обробляли постійним карбофураном у дозі 20нг/муху Селекцію й підрахунок мух проводили під впливом СОг Після обробки мух містили у пластикові чашки, покриті тюлем Після 24 годин визначали % смертності У залежності від результатів, експерименти повторювали 2-4 рази Результати продемонстровані в таблиці нижче доза синергічної речовини (нг/муху) матеріали 0 200 80 400 1000 80 90 94 65 60 63 95 80 95 100 93 75 77 100 смертність після 24 годин (%) 501 441 493 503 454 455 599 0 0 0 0 0 0 0 60 62 75 37 40 25 65 Приклад 5 Дослідження синергічної активності на попудомашніх мух (Musca domestica) Таблиця нижче демонструє синергічні активності матеріалів цього винаходу для різних інгреді 75 67 88 50 45 48 90 ляціях стійких ЄНТІВ на двох стійких штамах домашньої мухи (INSEL, IX) Дослідження було проведено, як описано в біологічному Прикладі 1 Значення LDso відПрикладі 2 ношення синергічних речовин визначали, як дано у Обробка штам INSEL LD50 (нг/муху) SR Карбофуран 15375 -279 29 530 метоміл 475 + 279 46 10 піримікарб >100000 + 279 696 145 алдикарб 695 + 279 172 4 бендюкарб 100000 + 279 150 667 ізопрокарб >100000 + 279 983 102 есбюл 10653 + 279 794 13 Приклад 6 Дослідження синергічної активності на попелицях вівса (Rhopalosiphum padi) Рослини вівса висотою 5 - 8см, поміщені у пластикові чашки заражали видами попелиці Rhopalosiphum padi різного віку Поміщених попелиць підраховували перед обробкою, потім рослини оброблювали розпиленням із використанням ручного розпилювача 1мл розчину для розпилення, крім уведення фіксованої дози (ЗО ррт) синергічної речовини Таблиця нижче демонструє синергічні активності матеріалів цього винаходу для різних інгредієнтів на двох стійких штамах домашньої мухи (INSEL, IX) Був приготовлений емульгований концентрат, 100г/л, сполуки No 279 цього винаходу способами, відомими практиці формулювання, із додаванням розчинника і поверхневоактивних матеріалів Тест-розчини, використані для розпилення, були приготовлені з цього концентрату і з препаратів на ринку шляхом розведення Смертність попелиць визначали через 24 години після обробки 279 карбофуран бромопропілат 4760 5 115 4 134 47 Приклад 8 Синергізм акарицид ного ефекту, досліджуваний на двоплямистих павутинних кліщах (Tetranychus urticae) З першої пари листів однотижневої рослини бобу вирізували диски листів діаметром 225мм, що були оброблені шляхом їхнього занурення (5 хв) у тест-розчин, що складається з активного інгредієнта і синергічної речовини у визначених концентраціях Для приготування концентрованих розчинів необхідної концентрації додавали 10% ацетону в якості спів-розчинника і 0 , 1 % Tween-80 у якості детергенту Висушені диски листів укладали на вологу поверхню й інфікували 10 підростаючими жіночими кліщами на лист Після 48 годин підраховували смертність, використовуючи мікроскоп і щітку Експеримент проводили 4 рази Середні дані результатів показані в таблиці нижче смертність % 95 95 95 Приклад 7 Дослідження впливу на ПЛІДНІСТЬ, на домашній Обробка тільки активними інгредієнтами SR мусі (Musca domestica) Групи, що складалися із з'явившихся знову 50 чоловічих і 50 жіночих мух, годували протягом 48 годин гранульованим цукром, що містив 500 ррт матеріалу No 441 і 484 цього винаходу, ВІДПОВІДНО, вирощували яйця, відкладені протягом наступних 10 днів Ефект зниження ПЛІДНОСТІ виражали як КІЛЬКІСТЬ мух, що вилупилися, в обробленій і необробленій групах Експерименти повторювали 4 рази обробка ефект зниження плодовитості 441 87% 484 90% Результати показані нижче Обробка карбофуран 1 ррт карбофуран 1 ррт +279 піримор2 ррт піримор2 ррт+ 279 імідаклопрід 0 1 ррт імідаклопрід 0 1 р р т - 2 7 9 штам IX LD50 (нг/муху) >100000 94 851 109 >100000 3552 2104 507 100000 746 >100000 2145 31 62 0 13 18 6 39 28 Концентрація 125 смертність % 8 44 90 250 500 18 81 ЗО 90 37 49864 38 Продовження таблиці обробка активними Інгредієнтами в комбінаціях 16+16 29 75 279 + карбофуран 279 + бромопропілат 80 90 Приклад 9 Ефективність польових випробувань проти колорадського жука (Leptmotarsa decemlmeata) Готували концентрований емульгований розчин у концентрації 100г/л сполуки No 279 цього винаходу способами, використовуваними в практиці формулювання, додаючи розчинник і поверхнево-активні матеріали Додавали композицію Чінуфур 40 FW, що містить 400г/л карбофурану, обробка доза (л/акр) необроблених чшуфур40 FW чшуфур40 FW чшуфур40 FW+279 0,1 0,2 0,1 + 2 , 0 карбофуран карбофуран+ МВ-599 феназахін феназахін + РВО феназахін + МВ-599 тебуфенпірад тебуфенпірад + РВО тебуфенпірад+МВ 599 відношення синергічна 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 акарицид/ речовина 0 1 2 4 0 0 1 1 1 1 0 0 1 1 1 1 Приклад 11 Синергічна активність проти попелиці гороху (Acyrthosiphon pisun) Синергічну активність сполуки No 599 тестували проти попелиці гороху (Acyrthosiphon pisun) при польових умовах на малих ділянках землі (10м2) Наносили об'єм розчину Обробка Піримікарб п і ри м і карб+ М В-599 Фіпроніл 250+250 100 разом із фіксованою дозою в 2л/га сполуки No 279 при дослідженні на полі малого розміру проти колорадського жука (Leptmotarsa decemlmeata) Розпилення проводили розпилювачем із мотором (Maruyama), розпилюючи 300л/га розчину для розпилення Обробки повторювали 4 рази, на ДІЛЯНЦІ землі 25м Вплив обробок оцінювали на другий день шляхом підрахунку жуків, що вижили, на рослинах Результати показані в таблиці нижче відношення карбофуран 279 Приклад 10 Синергічна активність сполуки Nr 599 Синергічну активність сполуки Nr 599 із різними специфічними акарицидами досліджували проти двоплямистого павутинного кліща (Tetranychus обробка концентрація (ррт) 62-62 125+125 Смертність 80 100 100 31+31 1 1 1 0 0 5 КІЛЬКІСТЬ жуків особина/рослина перед оброб після оброб 23,6 28,0 18,4 6,1 32,0 6,8 21,3 0,4 urticae) способами, описаними в Прикладі 8 Значення LCso і LC95, обчислені з відношення концентрація-смертність, показані в таблиці нижче Синергічна активність проти двоплямистого павутинного кліща (Tetranychus urticae) експозиція (години) 24 24 24 24 3 24 24 3 24 3 24 3 24 3 24 LC 5 0 LC 9 5 (мг/л) 163 9 799 9 55 5 286 8 33 5 93 7 27 5 67 0 > 1000 41 9 801 3 326 7 > 1000 20 4 371 8 68 1 280 2 31 3 174 8 > 1000 63 4 > 1000 1159 1081 35 7 1180 61 8 658 7 22 3 141 8 синерпч ВІДНОШ SR50 SR95 ЗО 49 60 > 31 21 > 15 1 3 >9 1 8 > 16 28 28 85 11 9 22 46 >85 >70 для розпилення 300л/га, використовуючи моторний розпилювач (Maruyama) Ефективність виражали середнім числом попелиці/лист до і два дні після обробки, ВІДПОВІДНО (Henderson and Tilton J Econ Entomol , 48 157,1995) Результати показані в таблиці нижче доза акт шгр /га 250 80 80 + 80 240 Е(%) 93 8 86 3 95 5 94 6 39 Карбофуран+М В-599 Тріазамат тріазамат+МВ-599 Імідаклоприд імідаклоприд+МВ-599 Приклад 12 Порівняльні дослідження з відомими ВІДПОВІДНИМИ синергічними речовинами Значення LD50 ВІДПОВІДНИХ сполук визначали в 4 повтореннях на мухах, оброблених карбофураном і ЮООнг відомої синергічної речовини, і відношення синергічних речовин SR50 40 49864 120+ 120 160 110 110+ 110 50 33 + 33 120 120+ 120 фіпроніл+МВ-599 Карбофуран 95 7 99 1 98 0 100 0 96 8 97 7 98 4 100 0 підраховували відношення SRso щодо контрольного карбофурану Ці відношення SRso порівнювали з такими ж нових сполук, отриманих нами Наші сполуки були активніше в кожному випадку 1 АЛКІНІЛОВІ ефіри ВІДОМІ 2-пропініл-нафтил-карбоксилат 4,11 ВІДПОВІДНО до винаходу 502 6,28 2 (Арил-алкіл), алкіл-алкінілові ефіри ВІДОМ Відношення сінергичних речовин (2, 6-діхлорфеніл) метил 2 пропшіловий ефір 20,92 SR50 ВІДОМ SR50 відношення сінергичних речовин SR50 1-нафтилметил 2-пропілшовий ефір 5 58 SR50 SR50 ВІДПОВІДНО до винаходу 25,70 ВІДОМ 2-[(2-пропілшокси) метил]-1 ,4бензодюксан 5 58 ВІДОМ відношення сінергичних речовин 503 441 ВІДОМ відношення сінергичних речовин винаходу 21,16 5-[(2-пропшіл)-метіл]-1 3бензодюксоль 10,60 відношення сінергичних речовин ВІДПОВІДНО До (2-пропшілоксиметил)-3,4діметоксибензол 6 58 ВІДПОВІДНО До 279 винаходу 28 7 ВІДПОВІДНО до винаходу 510 18 32 ВІДПОВІДНО до винаходу 493 32 84 З Арил алкінілові ефіри ВІДОМ відношення сінергичних речовин SR50 2 , 3-д ипд ро-2, 2-д и метил-7-(2пропшілокси) бензофцран 18 ВІДПОВІДНО до винаходу 418 20 5 4 АЛКІНІЛ-ОКСИМОВІ ефіри ВІДОМІ відомий нафтил алкініловии ефір 1-нафтил 2-пропарпловий ефір 1 -нафтил 3-бутиніловий ефір 2-нафтил 2-бутиніловий ефір 2-нафтил 3-пентиніловий ефір ВІДПОВІДНО до винаходу відношення синергічних речовин 6 52 7 95 7 72 9 97 41 42 49864 Приклади для формулювання Торгові назви додаткових матеріалів дані в лапках, після чого йдуть назви виробників 1 Одержання порошків А) 158г сильно роздрібненого перліту, 20г карбофурану і 20г сполуки 279 змішували в гомогенізаторі, до цієї суміші додавали 2г ефіру жирних кислот і спирту ПОЛІГЛІКОЛЮ ("G-3920" ІСІ) і гомогенізували суміш Порошкову суміш роздрібнювали в ежекторному млині і додавали до неї 5г октил-фенол-полігліколь ефіру (ЕО = 20) ("Triton Х-165" Rohm & Haas) і 2г алкіл-сульфосукцинату ("Aerosol- 13" Ціанамід) Отриманий продукт є зволоженою порошковою сумішшю (WP) Б) 10г сполуки 279 і 10г карбофурану розбавляли 2г етанолу Розчин змішували з 5г лігнінсульфонату кальцію ("Borrespeseca", Borregard), 5г ноніл-фенол-полігліколь ефіру ("Arkopal N-200" Hoechst) і 70г карбонату кальцію в порошковому гомогенізаторі Отриманий продукт роздрібнювали у млині аІріпе-100 typ Середній розмір часток склав 1-2 т м Ця композиція може бути використана для одержання мікросуспензій В) Суміш Зг Діазинону, Зг сполуки 441 і 0 Зг ефіру жирних кислот і спирту ПОЛІГЛІКОЛЮ ("G-3920" ІСІ) поміщували в апарат для гомогенізування в суміш 1 0г синтетичної силікової кислоти (Aerosil 200) і 191г тальку (dmax = 15-30тм), рН останнього був попередньо доведений до рН = 7 0 за допомогою калій- і натрій-фосфатного буферів При подальшому перемішуванні додавали 1 г д ю ктилсульфосукцинату ("Aerosol OTB" Cyanamid) і 1 г ефіру жирних кислот і спирту ПОЛІГЛІКОЛЮ ("Genapol LRD" Hoechst) і, нарешті, суміш роздрібнювали до середнього розміру часток 2 0 т м Отриманий продукт є легко летучим порошковим препаратом 2 Одержання концентратів емульсій А) Суміш 5г піримікарбу і 5г сполуки 493 розчиняли в суміші 20г ксилену і 40г пропанолу До цього розчину додавали суміш 4г етоксильованого алкіл-фенолу + лінійну сіль алкіл-арилсульфонату кальцію ("Geronol FF/U" Geronazzo) і 6 г етоксильованого аміну + жирна кислота + лінійна сіль алкіл-арил-сульфонат лужний метал ("Geronol MS" Geronazzo) Після повного розчинення додавали 20г води Одержували прозорий розчин, для якого характерно те, що при розве денні водою він формує емульсію з діаметром крапель 0 8-1 5 т м Б) Суміш 5г хіналфосу і 10г сполуки 484 і суміш 7г етоксильованого (ЕО =13) пропоксильованого (РО = 21) ноніл фенолу, 2г лінійної кальцієвої солі додецилбензолсульфонікової кислоти і 12 г РОЕ-(20)-сорбітан-моноолеату розчиняли в суміші 28 6-28 бмл пропіленгліколю і соснової жирної кислоти і 23 8мл соняшникового масла, 9 5мл етанолу і 95мл аліфатичного пдровуглецю с 45% нафталіновою константою Отриманий у такий спосіб матеріал може бути, переважно, використаний для одержання мікроемульсій В) Суміш 0 02-0 02 частин по масі активного інгредієнта і синергічної речовини розчиняли в 10 частинах по масі пропанолу, до отриманого розчину добавляли 99 96 частин по масі позбавленої запаху нафти і перемішували суміш до одержання гомогенного розчину Отриманий у такий спосіб дисперсійний препарат може прямо бути використаний у застосуванні до ULV П Дотримуються способу, описаного в прикладі А), із різницею, що в якості синергічного активного інгредієнта використовують 10г сполуки 279 3 Одержання гранулятів У механічному грануляторі змішували 300г карбофурану, 300г сполуки 418, 1500г полікарбоксилату лужної солі ("Sorphol", Toho), 500г додецилбензолсульфонікової кислоти («Marion TP 370» Huls), 500г бурякового цукру і 7200г каолініту Отриману в такий спосіб суміш змішували з 8300мл води, використовуючи міксер із високою силою різання (v = 10м/с) Наприкінці суміш висушували розпиленням Розподіл розміру часток продукту складає 0 1-0 4мм 4 Одержання аерозолів В апараті 1001, забезпеченому перемішувачем, змішували 1кг бюапетрину, 0 5кг сполуки 441, 0,1кг aerosil-air 972, 0,1кг етиленглікольмоносаліцилату, 15кг позбавленої запаху нафти і 50 кг пропанолу Після розчинення нею заповнювали циліндри з 33 3 кг рідкого газу пропан-бутан (25-75) 5 Одержання парів У 60мл етанолу розчиняють 5г S-бюалетрину, 5г сполуки 279 і 1г лимонного ароматизатору Розчином заповнюють випарник при температурі 50°С ДП «Український інститут промислової власності» (Укрпатент) вул Сім'ї Хохлових, 15, м Київ, 04119, Україна ( 0 4 4 ) 4 5 6 - 2 0 - 90 ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)216-32-71
ДивитисяДодаткова інформація
Назва патенту англійськоюPesticide combinations, method of its production, compositions on its base and parasites elimination method
Автори англійськоюBertok Bela, PAP LASZLO
Назва патенту російськоюПестицидные соединения, способ их получения, композиции на их основе и способ уничтожения паразитов
Автори російськоюБерток Бела, Пап Ласло
МПК / Мітки
МПК: A01N 33/22, C07C 43/166, A01N 43/32, C07C 233/65, C07D 307/80, C07D 319/00, C07C 43/178, A01N 31/04, C07C 251/40, C07C 231/00, C07C 211/30, C07C 43/215, C07D 231/12, A01N 31/16, C07C 251/48, A01N 35/10, A01N 31/06, A01N 43/16, C07C 43/196, C07C 249/00, C07C 43/188, A01N 43/12, A01N 37/18, A01N 37/32, C07C 43/176, A01N 31/14, C07C 41/00, C07D 307/79, C07D 317/54, A01N 43/30, C07C 205/00, A01N 33/04
Мітки: спосіб, композиції, основі, одержання, паразитів, пестицидні, знищення, сполуки
Код посилання
<a href="https://ua.patents.su/21-49864-pesticidni-spoluki-sposib-kh-oderzhannya-kompozici-na-kh-osnovi-ta-sposib-znishhennya-parazitiv.html" target="_blank" rel="follow" title="База патентів України">Пестицидні сполуки, спосіб їх одержання, композиції на їх основі та спосіб знищення паразитів</a>
Попередній патент: Пристрій для уловлювання платиноїдів при каталітичному окисленні аміаку
Наступний патент: Голка для ін’єкцій
Випадковий патент: Трубчастий абсорбер