Аматоксинові кон’югати з покращеними зв’язками
Номер патенту: 110370
Опубліковано: 25.12.2015
Автори: Андерль Ян, Сімон Вернер, Мюллер Крістоф, Луц Крістіан
Формула / Реферат
1. Аматоксиновий кон'югат формули І:

де:
R1=Η або ОН;
R2=Η або ОН;
R3=NH2 або OH;
R4=ОН або ОС1-6-алкіл і
R5=L-T; де L являє собою лінкер; а Т являє собою мішеньзв'язуючий фрагмент.
2. Аматоксиновий кон'югат за п. 1, де лінкер приєднаний до мішеньзв'язуючого фрагмента через фрагмент сечовини.
3. Аматоксиновий кон'югат за п. 1 або п. 2, де мішеньзв'язуючий фрагмент приєднаний до лінкера L через аміногрупу, присутню в мішеньзв'язуючому фрагменті, де вказана аміногрупа утворює частину вказаного фрагмента сечовини.
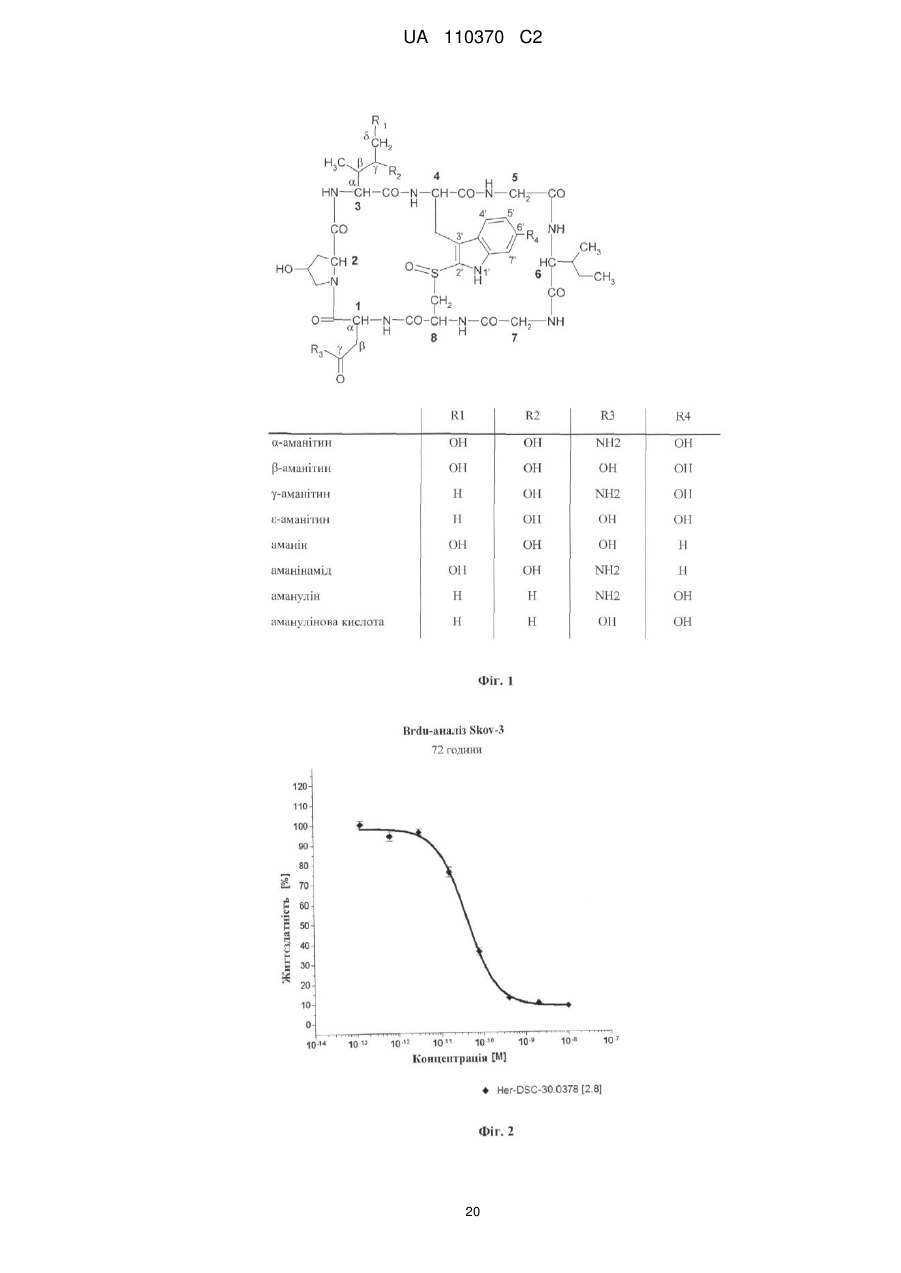
4. Аматоксиновий кон'югат за будь-яким з пп. 1-3, де лінкер має довжину від 1 до 8 атомів, конкретно від 1 до 6, більш конкретно від 1 до 4 і найбільш конкретно від 2 до 4 атомів.
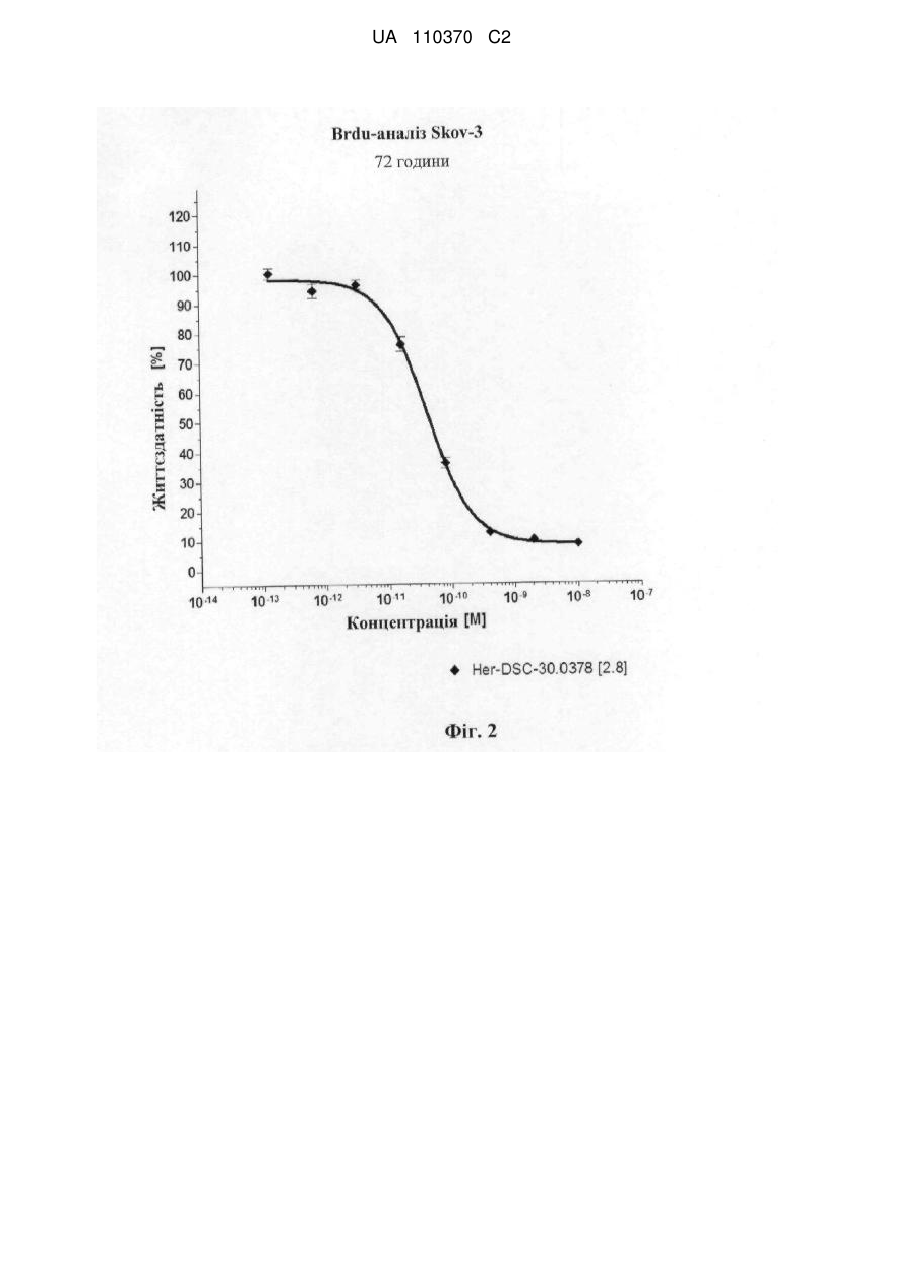
5. Аматоксиновий кон'югат за будь-яким з пп. 1-4, де лінкер L являє собою алкіленову, гетероалкіленову, алкеніленову, гетероалкеніленову, алкініленову, гетероалкініленову, циклоалкіленову, гетероциклоалкіленову, ариленову, гетероариленову, аралкіленову або гетероаралкіленову групу, необов'язково заміщену.
6. Аматоксиновий кон'югат за будь-яким з пп. 1-5, де лінкер L містить фрагмент, вибраний з одного з наступних фрагментів: дисульфідний, ефірний, амінний, естерний, карбоксамідний, уретановий і сечовинний фрагменти.
7. Аматоксиновий кон'югат за будь-яким з пп. 1-6, де мішеньзв'язуючий фрагмент специфічно зв'язується з епітопом, який присутній на пухлинній клітині, зокрема, де мішеньзв'язуючий фрагмент специфічно зв'язується з епітопом молекули адгезії епітеліальних клітин (ЕрСАМ).
8. Аматоксиновий кон'югат за будь-яким з пп. 1-7, де мішеньзв'язуючий фрагмент вибраний з групи, що містить:
(і) антитіло або його антигензв'язуючу ділянку;
(іі) подібний антитілу білок та
(ііі) аптамер нуклеїнової кислоти.
9. Аматоксиновий кон'югат за п. 8, де мішеньзв'язуючий фрагмент являє собою антитіло або його антигензв'язуючу ділянку, вибрані з діатіла, тетратіла, нанотіла, химерного антитіла, деімунізованого антитіла, гуманізованого антитіла й антитіла людини.
10. Аматоксиновий кон'югат за п. 8 або п. 9, де антигензв'язуюча ділянка вибрана з групи, що включає Fab, F(ab')2, Fd, Fv, одноланцюговий Fv та з'єднані за допомогою дисульфідного містка Fv (dsFv).
11. Аматоксиновий кон'югат за будь-яким з пп. 1-10 для застосування як лікарського препарату.
12. Аматоксиновий кон'югат за будь-яким з пп. 1-11 для застосування при лікуванні раку у пацієнта, де пухлина вибрана з групи, що включає рак підшлункової залози, холангіокарциному, рак молочної залози, рак прямої та ободової кишки, рак легені, рак передміхурової залози, рак яєчника, рак шлунка, рак нирки, злоякісну меланому, лейкоз та лімфосаркому.
13. Фармацевтична композиція, що включає аматоксиновий кон'югат за будь-яким з пп. 1-10 та додатково включає один або декілька фармацевтично прийнятних розріджувачів, носіїв, наповнювачів, заповнювачів, зв'язуючих речовин, змащувальних засобів, засобів, що забезпечують сипкість, розпушувачів, адсорбентів та/або консервантів.
14. Кон'югаційна молекула аматоксину формули І, де R1-R4 визначені в п. 1 і де R5=L-X; де L являє собою лінкер; а X являє собою групу, що відходить, яка може бути заміщена нуклеофільною групою мішеньзв'язуючого фрагмента.
15. Кон'югаційна молекула аматоксину за п. 14, де X являє собою групу, що відходить, яка може бути заміщена первинним аміном.
16. Кон'югаційна молекула аматоксину за п. 14 або п. 15, де X вибраний з: -'бутилокси, -сукцинімідилокси, -1-О-сукцинімідилокси-3-сульфонату (-норборнен-2,3-дикарбоксимід-1-ил), -1-фталімідоїлокси, -1-бензотриазолілокси, -1-(7-аза-бензотриазоліл)окси) та -N-імідазоліл.
17. Спосіб синтезу аматоксинового кон'югату за будь-яким з пп. 1-12, що включає етап, на якому здійснюють реакцію кон'югаційної молекули аматоксину за будь-яким з пп. 14-16 з мішеньзв'язуючим фрагментом, що містить нуклеофільну групу.
18. Спосіб за п. 17, при якому зазначена нуклеофільна група являє собою первинний амін.
19. Спосіб лікування раку у пацієнта, що включає етап, на якому зазначеному пацієнту вводять аматоксиновий кон'югат за будь-яким з пп. 1-11 або фармацевтичну композицію за п. 13.
20. Спосіб за п. 19, при якому зазначена пухлина вибрана з групи, що включає рак підшлункової залози, холангіокарциному, рак молочної залози, рак прямої та ободової кишок, рак легені, рак передміхурової залози, рак яєчника, рак шлунка, рак нирки, злоякісну меланому, лейкоз та лімфосаркому.
Текст
Реферат: Даний винахід належить до протипухлинної терапії. В одному аспекті даний винахід належить до кон'югатів аматоксину та мішеньзв'язуючого фрагмента, наприклад, антитіла, з'єднаних за допомогою певних зв'язків, які є ефективними при лікуванні раку. В іншому аспекті даний винахід належить до фармацевтичних композицій, що включають такі кон'югати. UA 110370 C2 (12) UA 110370 C2 UA 110370 C2 5 10 15 20 25 30 35 40 45 50 55 60 ГАЛУЗЬ ВИНАХОДУ [001] Даний винахід відноситься до протипухлинної терапії. В одному аспекті даний винахід відноситься до кон'югатів аматоксину та мішень-зв'язуючого фрагмента, наприклад, антитіла, з'єднаних за допомогою певних зв'язків, які ефективні при лікуванні раку. В додатковому аспекті даний винахід відноситься до фармацевтичних композицій, які включають такі кон'югати. ПЕРЕДУМОВИ ВИНАХОДУ [002] Аматоксини представляють собою циклічні пептиди, що складаються з 8 амінокислот. Вони можуть бути виділені з грибів Amanita phalloides або одержані штучно. Аматоксини, зокрема, інгібують ДНК-залежну РНК-полімерaзу II клітин ссавців і внаслідок цього також транскрипцію та біосинтез білка уражених клітин. Інгібування транскрипції в клітині викликає припинення росту та проліферації. Хоча природа зв'язку не є ковалентною, комплекс між аманітином та РНК-полімеразою ІІ є дуже міцним (KD=3 нM). Дисоціація аманітину з ферменту є дуже повільним процесом, що таким чином робить відновлення ураженої клітини малоймовірним. Якщо інгібування транскрипції триває надто довго, тоді клітина зазнає запрограмованої смерті (апоптозу). [003] Застосування аматоксинів в якості цитотоксичних фрагментів для терапії пухлин уже досліджували в 1981 році зшиванням антитіла з Thy 1.2 з α-аманітином, за допомогою лінкера, прикріпленого до індольного кільця Trp (амінокислота 4; дивись фігуру 1), шляхом діазотування (Davis & Preston, Science 1981, 213, 1385-1388). Davis та Preston позначили сайт приєднання як положення 7". Morris та Venton також продемонстрували, що заміна за положенням 7" дає похідну, яка зберігає цитотоксичну активність (Morris & Venton, Int. J. Peptide Protein Res. 1983, 21 419-430). [004] У патентній заявці EP 1859811 A1 (опублікованій 28 листопада 2007 року) описані кон'югати, у яких γ C-атом амінокислоти 1 аматоксину β-аманітину був безпосередньо зв'язаний, тобто без лінкерної структури, з альбуміном або з моноклональним антитілом HEA125, OKT3 або PA-1. Крім того, показана інгібіторна дія таких кон'югатів на проліферацію клітин пухлини молочних залоз (MCF-7), клітин лімфоми Беркіта (Raji) та клітин T-лімфоми (Jurkat). Запропоновано застосування лінкерів, включаючи лінкери, які містять такі елементи, як амідний, естерний, ефірний, тіоефірний, дисульфідний, сечовинний, тіосечовингий, вуглеводний фрагменти та подібні, але такі конструкти фактично не показані, та не запропоновані більш докладні дані, такі як сайти приєднання на аматоксинах. [005] У патентних заявках WO 2010/115629 та WO 2010/115630 (обидві опубліковані 14 жовтня 2010 року) описані кон'югати, де антитіла, такі як антитіла проти EpCAM, наприклад гуманізоване антитіло huHEA125, з'єднані з аматоксинами через (i) γ C-атом амінокислоти 1 аматоксину, (ii) 6" C-атом амінокислоти 4 аматоксину або (iii) через δ C-атом амінокислоти 3 аматоксину, та в кожному випадку або безпосередньо, або через лінкер між антитілом та аматоксинами. Запропоновані лінкери містять такі елементи, як амідний, естерний, ефірний, тіоефірний, дисульфідний, сечовинний, тіосечовинний, вуглеводний фрагменти і т. п. Крім того, показана інгібіторна дія цих кон'югатів на проліферацію клітин пухлини молочної залози (клітинна лінія MCF-7), карциноми підшлункової залози (клітинна лінія Capan-1), раку ободової та прямої кишки (клітинна лінія Colo205) та холангіокарциноми (клітинна лінія OZ). [006] Відомо, що аматоксини є відносно нетоксичними, коли зшиті з носіями великих біомолекул, такими як молекули антитіл, а також, що вони проявляють свою цитотоксичну активність тільки після того, як носій біомолекули відщепиться. З урахуванням токсичності аматоксинів, зокрема для клітин печінки, винятково важливе значення має те, що аматоксинові кон'югати для націленої протипухлинної терапії залишаються високо стійкими після введення в плазму, а також, що вивільнення аматоксину відбувається після інтерналізації в цільові клітини. В даному контексті незначні покращення стабільності кон'югатів можуть мати тяжкі наслідки для "терапевтичного вікна" та безпеки аматоксинових кон'югатів для терапевтичних підходів. МЕТА ДАНОГО ВИНАХОДУ [007] Таким чином, у даному рівні техніки існувала велика потреба у аматоксинових кон'югатах з мішень-зв'язуючим фрагментом, які були б стійкими в плазмі таким чином, що шкідливі побічні ефекти на нецільові клітини були б зведені до мінімуму. КОРОТКИЙ ОПИС ДАНОГО ВИНАХОДУ [008] Даний винахід заснований на несподіваному спостереженні, що націлюючі фрагменти можна з'єднати з аматоксинами через лінкери у додаткових сайта приєднання на амінокислоті 4 триптофані, тобто положеннях 1'-N, не впливаючи на взаємодію таких аматоксинів з їх мішенню, ДНК-залежною РНК-полімеразою ІІ клітин ссавців. [009] Таким чином, даний винахід стосується кон'югата, який містить мішень-зв'язуючий фрагмент, зв'язаний через лінкер L з аматоксином, або аналогом аматоксину, де лінкер L 1 UA 110370 C2 зв'язаний з аматоксином через 1’-N атом амінокислоти 4. [0010] В одному аспекті даний винахід стосується аматоксинового кон'югату формули І, R1 R2 HN O O H N O HN + HO N R4 H N R5 O O O O N H N O S O O NH N H R3 5 10 15 20 25 30 35 40 Формула І, де: R1=H або OH; R2=H або OH; R3=NH2 або OH; R4=OH або OC1-6алкіл і R5=L-T; де L являє собою лінкер; і T являє собою мішень-зв'язуючий фрагмент. [0011] У наступному аспекті даний винахід відноситься до фармацевтичної композиції, що містить кон'югат за даним винаходом. [0012] В іншому аспекті даний винахід відноситься до кон'югаційної молекули аматоксину формули І, де R1-R4 визначені вище; і де R5=L-X; де L являє собою лінкер; і X являє собою групу, що відходить, яка може бути заміщена нуклеофільною групою мішень-зв'язуючого фрагмента, зокрема первинного аміну. [0013] В ще одному аспекті даний винахід відноситься до способу синтезу кон'югату даного винаходу, що включає етап, на якому проводять реакцію кон'югаційної молекули аматоксину даного винаходу з мішень-зв'язуючим фрагментом, що містить нуклеофільну групу, зокрема первинний амін. КОРОТКИЙ ОПИС ГРАФІЧНИХ МАТЕРІАЛІВ [0014] На Фіг. 1 показані структурні формули різних аматоксинів. Числа жирним шрифтом (18) позначають стандартну нумерацію восьми амінокислот, які утворюють аматоксин. Також показані стандартні позначення атомів в амінокислотах 1, 3 та 4 (грецькі літери α-γ, грецькі літери α -δ та числа від 1" до 7", відповідно). [0015] На Фіг. 2 показана цитотоксична активність Her-DSC-30.0378 [2.8] щодо лінії HER2позитивних пухлинних клітин in vitro в аналізі BrdU після інкубації впродовж 72 годин. ДЕТАЛЬНИЙ ОПИС ДАНОГО ВИНАХОДУ [0016] Перш ніж даний винахід буде докладно описаний нижче, треба відзначити, що даний винахід не обмежений конкретним способом, протоколами та реагентами, описаними в даному документі, оскільки їх можна змінювати. Слід також розуміти, що термінологія, яку використали в даному документі, наявна тільки з метою описати конкретні варіанти здійснення, та не призначена обмежувати обсяг даного винаходу, який буде обмежуватися тільки прикладеною формулою винаходу. Якщо не зазначено інше, всі технічні та наукові терміни, використані в даному документі, мають такі самі значення, які зазвичай зрозумілі фахівцеві в даній галузі. [0017] Терміни, які використані в даному документі, переважно визначені як описано в "Багатомовному словнику біотехнологічних термінів: (Рекомендації IUPAC)", Leuenberger, H.G.W, Nagel, B. and Kolbl, H. eds. (1995), Helvetica Chimica Acta, CH-4010 Basel, Switzerland). [0018] В усьому даному описі та формулі винаходу, яка надана далі, крім випадків, якщо за контекстом вимагається інше, слово "містити" та варіації, такі як "містить" та "що містить", слід розуміти як такі, що передбачають включення заданого цілого числа або етапу або групи цілих чисел або етапів, але не виключення будь-якого іншого цілого числа або етапу або групи цілих чисел або етапів. [0019] В тексті даного опису процитовано декілька документів. Кожний з документів, 2 UA 110370 C2 5 10 15 20 25 30 35 40 45 50 55 60 процитованих в даному документі (включаючи всі патенти, заявки на патенти, наукові публікації, нормативи виробників, інструкції, записи послідовностей з номером доступу в GenBank і т. д.) або вище, або нижче, таким чином включені за допомогою посилань в їх повному об'ємі, наскільки це можливо за відповідним патентним законом. Нічого з даного документу не варто розцінювати як визнання того, що даний винахід не дає права датувати таке розкриття більш раннім числом відповідно до більш раннього винаходу. [0020] Далі описується даний винахід. В наведених нижче абзацах різні аспекти даного винаходу визначені більш детально. Кожний аспект, визначений таким чином, можна поєднати з будь-яким іншим аспектом або аспектами, крім випадків, коли чітко вказане протилежне. Зокрема, будь-яку рису, вказану як переважну або корисну, можна поєднати з будь-якою іншою рисою або рисами, вказаними як переважні або корисні. [0021] Таким чином, даний винахід стосується кон'югата, який містить мішень-зв'язуючий фрагмент, зв'язаний через лінкер L з аматоксином, або аналогом аматоксину, де лінкер L зв'язаний з аматоксином через 1’-N атом амінокислоти 4. [0022] В контексті даного винаходу вираз "кон'югат" відноситься до молекули, включаючи щонайменше дві різні молекули, зв'язані ковалентним зв'язком. [0023] Вираз "мішень-зв'язуючий фрагмент", як використовується у даному документі, відноситься до будь-якої молекули або частини молекули, яка може специфічно зв'язуватися з молекулою-мішенню або епітопом-мішенню. Переважні мішень-зв'язуючі фрагменти в контексті даної заявки представляють собою (i) антитіла або їх антиген-зв'язуючі ділянки, (ii) подібні антитілам білки та (iii) аптамери нуклеїнових кислот. Придатні для застосування в даному винаході "мішень-зв'язуючі фрагменти", як правило, мають молекулярну масу 40000 Да (40 кДа) або більше. [0024] В контексті даного винаходу вважають, що перша сполука (наприклад, антитіло) "специфічно зв'язується" з другою сполукою (наприклад, антигеном, таким як білок-мішень), якщо вона має константу дисоціації KD до зазначеної другої сполуки 100 мкM або менше, переважно 50 мкМ або менше, переважно 30 мкМ або менше, переважно 20 мкМ або менше, переважно 10 мкМ або менше, переважно 5 мкМ або менше, більш переважно 1 мкМ або менше, більш переважно 900 нМ або менше, більш переважно 800 нМ або менше, більш переважно 700 нМ або менше, більш переважно 600 нМ або менше, більш переважно 500 нМ або менше, більш переважно 400 нМ або менше, більш переважно 300 нМ або менше, більш переважно 200 нМ або менше, ще більш переважно 100 нМ або менше, ще більш переважно 90 нМ або менше, ще більш переважно 80 нМ або менше, ще більш переважно 70 нМ або менше, ще більш переважно 60 нМ або менше, ще більш переважно 50 нМ або менше, ще більш переважно 40 нМ або менше, ще більш переважно 30 нМ або менше, ще більш переважно 20 нМ або менше та ще більш переважно 10 нМ або менше. [0025] В контексті даної заявки вирази "молекула-мішень" та "епітоп-мішень", відповідно, стосуються антигена та епітопа антигена, відповідно, що специфічно зв'язаний мішеньзв'язуючим фрагментом. Переважно молекулою-мішенню є асоційований з пухлиною антиген, зокрема антиген або епітоп, що присутній на поверхні пухлинних клітин одного або декількох типів у підвищеній концентрації та/або у відмінній просторовій конфігурації в порівнянні з поверхнею клітин, які не є пухлинними. Переважно вказаний антиген або епітоп присутній на поверхні пухлинних клітин одного або декількох типів, але не на поверхні клітин, які не є пухлинними. В конкретних варіантах здійснення мішень-зв'язуючий фрагмент специфічно зв'язується з епітопом HER-2/neu або молекулою адгезії епітеліальних клітин (EpCAM). В інших варіантах здійснення вказаний антиген або епітоп переважно експресується на клітинах, задіяних в аутоімунних захворюваннях. В таких конкретних варіантах здійснення мішеньзв'язуючий фрагмент специфічно зв'язується з епітопом рецептора IL-6 (IL-6R). [0026] Вираз "антитіло або його антиген-зв'язуюча ділянка", як використовується у даному документі, відноситься до молекул імуноглобуліну та імунологічно активних частин молекул імуноглобуліну, тобто молекул, які містять антиген-зв'язуючий сайт, який імуноспецифічно зв'язує антиген. Також включено білки, подібні імуноглобуліну, які вибирають завдяки технікам, включаючи, наприклад, фаговий дисплей специфічного зв'язування з молекулою-мішенню, наприклад з білком-мішенню Her-2/neu або EpCAM. Молекули імуноглобуліну даного винаходу можуть бути будь-якого типу (наприклад, IgG, IgE, IgM, IgD, IgA та IgY), класу (наприклад, IgG1, IgG2, IgG3, IgG4, IgA1 та IgA2) або підкласу молекули імуноглобуліну. "Антитіла та їх антигензв'язуючі ділянки", придатні для застосування за даним винаходом, включають, без обмежень, поліклональні, моноклональні, моновалентні, біспецифічні, гетерокон'югатні, мультиспецифічні, людські, гуманізовані (зокрема прищеплені на CDR), деімунізовані або хімерні антитіла, одноланцюгові антитіла (наприклад, scFv), Fab-ділянки, F(ab")2-ділянки, ділянки, отримані за 3 UA 110370 C2 5 10 15 20 25 30 35 40 45 50 55 60 допомогою бібліотеки експресії Fab, діатіла або тетратіла (Holliger P. et al., 1993), нанотіла, антиідіотипові (анти-Id) антитіла (включаючи, наприклад, анти-Id антитіла до антитіл даного винаходу) та епітоп-зв'язуючі ділянки будь-чого з вищенаведеного. [0027] В деяких варіантах здійснення антиген-зв'язуючі ділянки являють собою людські антиген-зв'язуючі ділянки антитіла за даним винаходом та включають, без обмежень, Fab, Fab" і F(ab")2, Fd, одноланцюгові Fv (scFv), одноланцюгові антитіла, з'єднані дисульфідними містками Fv (dsFv) та ділянки, які містять або VL-, або VH-домен. Антиген-зв'язуючі ділянки антитіл, включаючи одноланцюгові антитіла, можуть включати варіабельний домен(и) сам по собі або в комбінації з усім або ділянкою з наступного: "шарнірна" область, CL, CH1, CH2 та CH3 домени. Також в даний винахід включені антиген-зв'язуючі ділянки, що також включають будь-яку комбінацію варіабельного домену(ів) з "шарнірною" областю, CL, CH1, CH2 та CH3 доменами. [0028] Антитіла, придатні для використання в даному винаході, можна одержувати з будьякої тварини, включаючи птахів та ссавців. Переважно, антитіла одержують з людини, гризуна (наприклад, миші, щура, морської свинки або кроля), курки, свині, вівці, кози, верблюда, корови, коня, віслюка, кота або собаки. Особливо переважно, щоб антитіла були одержані від людини або мишей. Як використовується у даному документі, "антитіла людини" включають антитіла, що мають послідовність амінокислот імуноглобуліну людини, та включають антитіла, вибрані з бібліотек імуноглобулінів людини або від тварин, трансгенних стосовно одного або декількох імуноглобулінів людини, та що не експресують ендогенні імуноглобуліни, як описано, наприклад, в патенті США № 5939598, Kucherlapati & Jakobovits. [0029] Вираз "подібний антитілу білок" відноситься до білка, який сконструйовано (наприклад, шляхом мутагенезу петель) для специфічного зв'язування з молекулою-мішенню. Як правило, такий подібний антитілу білок містить щонайменше одну варіабельну пептидну петлю, прикріплену з обох кінців до каркасу білка. Таке подвійне структурне обмеження суттєво підвищує зв'язувальну афінність подібного антитілу білка до рівнів, порівнюваних з рівнями антитіла. Довжина варіабельної пептидної петлі складає, як правило, від 10 до 20 амінокислот. Каркасним білком може бути будь-який білок, що має хороші властивості розчинності. Переважно, каркасний білок являє собою малий глобулярний білок. Подібні антитілам білки включають, без обмеження, афітіла, антикаліни та сконструйовані білки з анкіриновим повтором (для огляду дивись: Binz зі співавт, 2005). Подібні антитілам білки можуть бути отримані з великих бібліотек мутантів, наприклад, розділені методом пенінга завдяки великим бібліотекам фагового дисплея, та можуть бути виділені аналогічно нормальним антитілам. Також подібні антитілам зв'язуючі білки можуть бути одержані шляхом комбінаторного мутагенезу поверхневих залишків глобулярних білків. [0030] Вираз "аптамер нуклеїнової кислоти" відноситься до молекули нуклеїнової кислоти, що сконструйована за допомогою повторюваних циклів селекції in vitro або SELEX (систематичної еволюції лігандів експоненціальним збагаченням) для зв'язування з молекулоюмішенню (для огляду дивись: Brody and Gold, 2000). Аптамер нуклеїнової кислоти може бути молекулою ДНК або РНК. Аптамери можуть містити модифікації, наприклад, модифіковані нуклеотиди, такі як 2’-фторзаміщені піримідини. [0031] Як застосовується у даному документі, "аналог" сполуки є структурно спорідненим, але не ідентичним сполуці, та проявляє щонайменше одну активність сполуки. Сполука, з якою порівнюють аналог, відома як "вихідна" сполука. Вищезгадані активності включають, без обмежень, наступне: активність зв'язування з іншою сполукою; активність інгібування, наприклад, активність інгібування ферменту; токсичну дію; активність активізації, наприклад, активність активізації ферменту. Не вимагається, щоб аналог проявляв таку активність в тій же мірі, що вихідна сполука. Сполуку розглядають як аналог в контексті даної заявки, якщо вона проявляє відповідну активність у розмірі щонайменше 1 % (більш переважно щонайменше 5 %, більш переважно щонайменше 10 %, більш переважно щонайменше 20 %, більш переважно щонайменше 30 %, більш переважно щонайменше 40 % та більш переважно щонайменше 50 %) від активності вихідної сполуки. Таким чином, "аналог аматоксину", як використовується в даному документі, відноситься до сполуки, яка по своїй структурі є спорідненою до будь-якого з α-аманітину, β-аманітину, γ-аманітину, ε-аманітину, аманіну, аманінаміду, амануліну та аманулінової кислоти, як показано на фіг. 1, та яка проявляє щонайменше 1 % (більш переважно щонайменше 5 %, більш переважно щонайменше 10 %, більш переважно щонайменше 20 %, більш переважно щонайменше 30 %, більш переважно щонайменше 40 % та більш переважно щонайменше 50 %) активністі інгібування щодо РНК-полімерaзи II ссавців у порівнянні щонайменше з одним з α-аманітину, β-аманітину, γ-аманітину, ε-аманітину, аманіну, аманінаміду, амануліну та аманулінової кислоти. "Аналог аматоксину", придатний для застосування в даному винаході, може проявляти навіть більшу активність інгібування стосовно 4 UA 110370 C2 5 10 15 20 25 30 35 40 45 50 55 60 РНК-полімерaзи II ссавців, ніж будь-який з α-аманітину, β-аманітину, γ-аманітину, ε-аманітину, аманіну, аманінаміду, амануліну або аманулінової кислоти. Інгібіторну активність можна виміряти шляхом виявлення концентрації, при якій відбувається 50 % інгібування (величина IC50). Активність інгібування щодо РНК-полімерaзи II ссавців можна визначити опосередковано шляхом вимірювання активності інгібування клітинної проліферації. Придатний аналіз для вимірювання інгібування клітинної проліферації описаний в прикладах. [0032] "Напівсинтетичний аналог" відноситься до аналога, який одержали шляхом хімічного синтезу із застосуванням сполук з природних джерел (наприклад, рослинних матеріалів, культур бактерій або культур клітин) в якості вихідних матеріалів. Як правило, "напівсинтетичний аналог" даного винаходу синтезували, виходячи зі сполуки, виділеної з гриба родини Аманітових. На відміну від цього, "синтетичний аналог" відноситься до аналога, синтезованого шляхом так званого повного синтезу з малих (як правило, нафтохімічних) складових. Як правило, такий повний синтез проводять без допомоги біологічних процесів. [0033] Як застосовується у даному документі, "кон'югат аптамера" відноситься до кон'югату токсину з мішень-зв'язуючим фрагментом, в якому мішень-зв'язуючий фрагмент представляє собою аптамер нуклеїнової кислоти згідно вищенаведеного варіанту (iii). [0034] "Лінкер" в контексті даного винаходу відноситься до молекули, яка з'єднує два компоненти, при цьому кожний прикріплений до одного кінця лінкера, та яка збільшує відстань між двома компонентами та послаблює просторовий взаємний вплив цих компонентів, у даному випадку, наприклад, мішень-зв'язуючого фрагмента та аматоксину. За відсутності лінкера безпосередній зв'язок аматоксину з мішень-зв'язуючим фрагментом може зменшити здатність аматоксину взаємодіяти з РНК-полімерaзою II. В конкретних варіантах здійснення лінкер має безперервні ланцюги з довжиною від 1 до 30 атомів (наприклад, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 або 30 атомів; отже, в контексті даного винаходу вираз "від…до" застосовують так, щоб визначені межі були включені) в його скелеті, тобто довжину лінкера визначають як найкоротше з'єднання, вимірюване числом атомів або зв'язків між фрагментом аматоксину та мішень-зв'язуючим фрагментом, де одна сторона скелета лінкера вступає в реакцію з аматоксином, а інша сторона - з мішень-зв'язуючим фрагментом. В контексті даного винаходу лінкер переважно являє собою C1-20-алкіленову, C1-20гетероалкіленову, C2-20-алкеніленову, C2-20-гетероалкеніленову, C2-20-алкініленову, C2-20гетероалкініленову, циклоалкіленову, гетероциклоалкіленову, ариленову, гетероариленову, аралкіленову або гетероаралкіленову групу, необов'язково заміщену. Лінкер може включати один або декілька структурних елементів, таких як карбоксамідний, естерний, ефірний, тіоефірний, дисульфідний, сечовинний, тіосечовинний, вуглеводний фрагменти і т. п. Лінкер також може містити комбінації з двох або більше таких структурних елементів. Кожний з таких структурних елементів може бути присутнім в лінкері більше одного разу, наприклад, двічі, три рази, чотири рази, п'ять разів або шість разів. В деяких варіантах здійснення лінкер може містити дисульфідний зв'язок. Зрозуміло, що лінкер має бути приєднаним до аматоксину та до мішень-зв'язуючого фрагмента або за один етап, або за два, або більше послідовних етапів. У зв'язку з цим лінкер буде нести дві групи, переважно на проксимальному та дистальному кінці, і може (i) утворювати ковалентний зв'язок з групою, присутньою у одного з компонентів, що має бути приєднаним, переважно з активованою групою на аматоксині або з мішень-зв'язуючим пептидом, або (ii) є або може бути активованим для утворення ковалентного зв'язку з групою на аматоксині. Таким чином, переважним є те, щоб хімічні групи знаходились на дистальному та проксимальному кінці лінкера, що є результатом такої реакції зв'язування, як наприклад естерний, ефірний, уретановий, пептидний зв'язок і т.д. [0035] В контексті даного винаходу вираз "аматоксин" включає всі циклічні пептиди, що складаються з 8 амінокислот, які виділені з роду Аманіта та описані Wieland, T. та Faulstich H. (Wieland T, Faulstich H., CRC Crit Rev Biochem. 1978 Dec;5(3): 185-260), та крім того включає всі його хімічні похідні, додатково всі його напівсинтетичні аналоги, додатково всі його синтетичні аналоги, складені зі складових згідно основної структури природних сполук (циклічних, 8 амінокислот), додатково всі синтетичні або напівсинтетичні аналоги, що містять негідроксильовані амінокислоти замість гідроксильованих амінокислот, додатково всі синтетичні або напівсинтетичні аналоги, у яких фрагмент сульфоксиду тіоефіру заміщений сульфідом, сульфоном або атомами, відмінними від сірки, наприклад, атомом вуглецю, як в карбо-аналогу аманітину, в кожному випадку, де будь-яка така похідна або аналог є функціонально активним щодо інгібування РНК-полімерaзи II ссавців. [0036] Функціонально аматоксини визначені як пептиди або депсипептиди, які інгібують РНКполімерaзу II ссавців. Переважними є аматоксини з функціональною групою (наприклад, карбоксильною групою, аміногрупою, гідроксигрупою, тіоловою або тіол-захоплюючою групою), 5 UA 110370 C2 5 10 15 що може вступати в реакцію з лінкерними молекулами або мішень-зв'язуючими фрагментами, як визначено вище. Аматоксинами, особливо придатними для кон'югатів даного винаходу, є αаманітин, β-аманітин, γ-аманітин, ε-аманітин, аманін, аманінамід, аманулін та аманулінова кислота, як показано на фіг. 1, а також їх солі, хімічні похідні, напівсинтетичні аналоги та синтетичні аналоги. Особливо переважними аматоксинами для застосування в даному винаході є α-аманітин, β-аманітин та аманінамід. [0037] Як використовується у даному документі, "хімічна похідна" (або коротше "похідна") сполуки відноситься до зразку, який має хімічну структуру подібну до сполуки, крім того містить щонайменше одну не присутню в сполуці хімічну групу та/або позбавлений щонайменше однієї хімічної групи, що присутня в сполуці. Сполука, з якою порівнюють похідну, відома як "вихідна" сполука. Як правило, "похідну" можна отримати з вихідної сполуки за один або декілька етапів хімічних реакцій. [0038] В конкретних варіантах здійснення даного винаходу аматоксин вибраний з αаманітину, β-аманітину, γ-аманітину, ε-аманітину, аманіну, аманінаміду, амануліну або аманулінової кислоти або з їх солей, або аналогів. [0039] В одному аспекті даний винахід стосується аматоксинового кон'югата формули І, R1 R2 HN O O H N O HN + HO N R4 H N R5 O O O O N H N O S O N H O NH R3 20 25 30 35 40 45 Формула І, де: R1=H або OH; R2=H або OH; R3=NH2 або OH; R4=OH або OC1-6-алкіл і R5=L-T; де L являє собою лінкер; а T являє собою мішень-зв'язуючий фрагмент. [0040] В окремому варіанті здійснення аматоксиновий кон'югат формули І являє собою похідну α-аманітину (R1=OH; R2=OH і R3=NH2). [0041] В окремому варіанті здійснення R4 являє собою O-Me. [0042] В окремому варіанті здійснення лінкер приєднаний до мішень-зв'язуючого фрагмента через фрагмент сечовини. [0043] В контексті даного винаходу вираз "приєднаний до мішень-зв'язуючого фрагмента через фрагмент сечовини" відноситься до з'єднання між лінкером та мішень-зв'язуючим фрагментом, де мішень-зв'язуючий фрагмент безпосередньо приєднаний до лінкера через групу -NH-C(О)-NH-. [0044] В конкретних варіантах здійснення даного винаходу мішень-зв'язуючий фрагмент приєднаний до лінкера L через аміногрупу, присутню в мішень-зв'язуючому фрагменті, де вказана аміногрупа утворює частину вказаного фрагмента сечовини. [0045] В окремих варіантах здійснення лінкер має довжину від 1 до 8 атомів, конкретно від 1 до 6, більш конкретно від 1 до 4 і найбільш конкретно від 2 до 4 атомів. Отже, етиленовий лінкер має довжину лінкера 2 атоми, пропіленовий лінкер - 3 атоми, та бутиленовий лінкер - 4 атоми. [0046] В окремих варіантах здійснення даного винаходу лінкер L містить одну або декілька груп, зокрема одну, дві або три групи, вибрані з наступного переліку: алкіленова, алкеніленова, алкініленова, циклоалкіленова, гетероалкіленова, гетероалкеніленова, гетероалкініленова, гетероциклоалкіленова, ариленова, гетероариленова, аралкіленова та гетероаралкіленова група, де кожна група може бути необов'язково заміщеною. [0047] Вираз "алкілен" відноситься до двовалентних насичених вуглеводневих групам з прямим ланцюгом, що мають від 1 до 20 атомів вуглецю, включаючи групи, що мають від 1 до 10 атомів вуглецю. У деяких варіантах здійснення алкіленові групи можуть бути нижчими алкіленовими групами. Вираз "нижчий алкілен" відноситься до алкіленових груп, що мають від 1 6 UA 110370 C2 5 10 15 20 25 30 35 40 45 50 55 60 до 6 атомів вуглецю, та у деяких варіантах здійснення - від 1 до 5 або від 1до 4 атомів вуглецю. Приклади алкіленових груп включають, без обмеження, метиленову (-CH2-), етиленову (-CH2CH2-), н-пропіленову, н-бутиленову, н-пентиленову і н-гексиленову. [0048] Вираз "алкенілен" відноситься до двовалентних груп з прямим ланцюгом, які мають від 2 до 20 атомів вуглецю, де щонайменше один зі зв'язків вуглець-вуглець є подвійним зв'язком, тоді як інші зв'язки можуть бути одинарними зв'язками або також подвійними зв'язками. Вираз "алкінілен" в даному документі відноситься до груп, що мають від 2 до 20 атомів вуглецю, де щонайменше один зі зв'язків вуглець-вуглець є потрійним зв'язком, тоді як інші зв'язки можуть бути одинарними, подвійними або також потрійними зв'язками. Приклади алкеніленових груп включають етенілен (-CH=CH-), 1-пропенілен, 2-пропенілен, 1-бутенілен, 2бутенілен, 3-бутенілен і т. п. Приклади алкініленових груп включають етинілен, 1-пропінілен, 2пропінілен і т. д. [0049] Як використовується у даному документі, вираз "циклоалкілен" призначений для позначення двовалентного кільця, що є частиною будь-якої стійкої моноциклічної або поліциклічної системи, де таке кільце має від 3 до 12 атомів вуглецю, але без жодного гетероатома, та де таке кільце повністю насичене, а вираз "циклоалкенілен" призначений для позначення двовалентного кільця, що являється частиною будь-якої стійкої моноциклічної або поліциклічної системи, де таке кільце має від 3 до 12 атомів вуглецю, але без жодного гетероатома, та де таке кільце щонайменше частково ненасичене (але за виключенням будьякого ариленового кільця). Приклади циклоалкіленів включають, без обмеження, циклопропілен, циклобутилен, циклопентилен, циклогексилен та циклогептилен. Приклади циклоалкеніленів включають, без обмеження, циклопентенілен та циклогексенілен. [0050] Як використовується у даному документі, вирази "гетероциклоалкілен" та "гетероциклоалкенілен" призначені для позначення двовалентного кільця, що є частиною будьякої стійкої моноциклічної або поліциклічної кільцевої системи, де таке кільце має від 3 до приблизно 12 атомів, та де таке кільце складається з атомів вуглецю та щонайменше одного гетероатома, зокрема щонайменше одного гетероатома, незалежно вибраного з групи, що включає N, O та S, при цьому гетероциклоалкілен відноситься до такого кільця, яке є повністю насиченим, та гетероциклоалкенілен відноситься до кільця, яке щонайменше є частково ненасиченим (але за виключенням будь-якого ариленового або гетероариленового кільця). [0051] Вираз "арилен" призначений для позначення двовалентного кільця або кільцевої системи, що є частиною будь-якої стійкої моноциклічної або поліциклічної системи, де таке кільце або кільцева система має від 3 до 20 атомів вуглецю, але не має гетероатома, чиє кільце або кільцева система складається з ароматичного фрагмента, як визначено "4n+2" правилом πелектронів, включаючи фенілен. [0052] Як використовується у даному документі, вираз "гетероарилен" відноситься до двовалентного кільця або кільцевої системи, що є частиною будь-якої стійкої моно- або поліциклічної системи, де таке кільце або кільцева система має від 3 до 20 атомів, чиє кільце або кільцева система складається з ароматичного фрагмента, як визначено "4n+2" правилом πелектронів, та містить атоми вуглецю та один або декілька гетероатомів азоту, сірки та/або кисню. [0053] В контексті даного винаходу вираз "заміщений" призначений для позначення того, що один або декілька атомів водню, присутніх в скелеті лінкера, заміщені на вибір вказаною групою (групами), за умови, що нормальна валентність позначеного атома або відповідного атома групи, яка заміщена, не перевищує заданого значення, та що заміщення приводить до стійкої сполуки. Вираз "необов'язково заміщений" призначений для позначення, що лінкер є або незаміщеним або заміщеним, як визначено в даному документі, одним або декількома замісниками, як визначено в даному документі. Якщо замісником є кетогрупа (або оксо, тобто =О), тіо- або іміногрупа або подібна, тоді два атоми водню з атомів на лінкерному скелеті є заміщеними. Ілюстративні замісники включають, наприклад, алкіл, алкеніл, алкініл, циклоалкіл, гетероциклоалкіл, арил, гетероарил, аралкіл, гетероаралкіл, ацил, ароїл, гетероароїл, карбоксил, алкоксі, арилоксі, ацилоксі, ароїлоксі, гетероароїлоксі, алкоксикарбоніл, галоген, (тіо)естер, ціано, фосфорил, аміно, іміно, (тіо)амідо, сульфгідрил, алкілтіо, ацилтіо, сульфоніл, сульфат, сульфонат, сульфамоїл, сульфонамідо, нітро, азидо, галогеналкіл, у тому числі перфторалкіл (такий як трифторметил), галогеналкоксі, алкілсульфаніл, алкілсульфініл, алкілсульфоніл, алкілсульфонаміно, арилсульфоноаміно, фосфорил, фосфат, фосфонат, фосфінат, алкілкарбоксі, алкілкарбоксіамід, оксо, гідроксі, меркапто, аміно (необов'язково моноабо дизаміщений, наприклад, алкілом арилом або гетероарилом), іміно, карбоксамід, карбамоїл (необов'язково моно- або дизаміщений, наприклад, алкілом, арилом або гетероарилом), амідино, аміносульфоніл, ациламіно, ароїламіно, (тіо)уреїдо, арил(тіо)уреїдо, алкіл(тіо)уреїдо, 7 UA 110370 C2 5 10 15 20 25 30 35 40 45 50 55 60 циклоалкіл(тіо)уреїдо, арилоксі, аралкоксі або -O(CH2)n-OH, -O(CH2)n-NH2, -O(CH2)nCOOH, (CH2)nCOOH, -C(O)O(CH2)nR, -(CH2)nN(H)C(O)OR або -N(R)S(O)2R, де n дорівнює 1-4, а R незалежно обраний з водню, -алкілу, -алкенілу, -алкінілу, -циклоалкілу, -циклоалкенілу, -(Cзв'язаний-гетероциклоалкілу), -(C-зв'язаний-гетероциклоалкенілу), -арилу і -гетероарилу, причому можливо багато ступенів заміщення. Фахівцю в даній галузі буде зрозуміло, що замісники, такі як гетероциклоалкіл, арил, гетероарил, алкіл і т. п., або функціональні групи, такі як -OH, -NHR і т. д., самі по собі можуть бути заміщені, якщо це доцільно. Також фахівцю в даній галузі буде зрозуміло, що заміщені фрагменти самі по собі можуть бути також заміщені, коли це доцільно. [0054] В окремих варіантах здійснення даного винаходу, де лінкер L містить m груп, обраних з наступного переліку: алкіленова, алкеніленова, алкініленова, циклоалкіленова, гетероалкіленова, гетероалкеніленова, гетероалкініленова, гетероциклоалкіленова, ариленова, гетероариленова, аралкіленова і гетероаралкіленова група, де кожна група може бути необов'язково заміщена, лінкер додатково містить n фрагментів, незалежно обраних з наступних фрагментів: дисульфідного (-S-S-), ефірного (-O-), тіоефірного (-S-), амінного (-NH-), естерного (-O-C(=O)- або -C(=O)-O-), карбоксамідного (-NH-C(=O)- або -C(=O)-NH-), уретанового (-NH-C(=O)-O- або -O-C(=O)-NH-) та сечовинного (-NH-C(=O)-NH-) фрагментів, де m=n+1. В окремих варіантах здійснення m дорівнює 2, а n дорівнює 1, або m дорівнює 3, а n дорівнює 2. В окремих варіантах здійснення лінкер містить 2 або 3 незаміщені алкіленові групи та 1 або 2, відповідно, дисульфідних, ефірних, тіоефірних, амінних, естерних, карбоксамідних, уретанових або сечовинних фрагментів, що зв'язують незаміщені алкіленові групи. [0055] В конкретних варіантах здійснення даного винаходу мішень-зв'язуючий фрагмент специфічно зв'язується з епітопом, який присутній на пухлинній клітині. [0056] В конкретних варіантах здійснення даного винаходу мішень-зв'язуючий фрагмент специфічно зв'язується з епітопом Her-2/neu або молекулою адгезії епітеліальних клітин (EpCAM). [0057] В окремих варіантах здійснення даного винаходу мішень-зв'язуючий фрагмент обирають з групи, що включає антитіло або його антиген-зв'язуючу ділянку, подібний антитілу білок та аптамер нуклеїнової кислоти. [0058] В конкретних варіантах здійснення даного винаходу антитіло або його антигензв'язуюча ділянка вибрані з діатіла, тетратіла, нанотіла, химерного антитіла, деімунізованого антитіла, гуманізованого антитіла або антитіла людини. [0059] В окремих варіантах здійснення даного винаходу антиген-зв'язуючу ділянка вибрана з групи, що включає Fab, F(ab’)2, Fd, Fv, одноланцюговий Fv та з'єднані за допомогою дисульфідного містка Fv (dsFv). [0060] В окремих варіантах здійснення антитіло являє собою герцептин або HEA125, або ділянку антитіла, що містить антиген-зв'язуючу ділянку герцептину або HEA125. [0061] В окремих варіантах здійснення більш ніж одна молекула аматоксину зшита з одним мішень-зв'язуючим фрагментом. Підвищення числа молекул аматоксина на кон'югат також буде підвищувати токсичність. Таким чином, в окремому варіанті здійснення співвідношення мішеньзв'язуючих фрагментів й аматоксину складає від 1 мішень-зв'язуючого фрагмента на 2-15 молекул аматоксину, зокрема 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 або 15. З метою розрахунку співвідношення у випадку димерів антитіл, таких як IgG, димер розглядають як один мішеньзв'язуючий фрагмент. [0062] В окремих варіантах здійснення даного винаходу кон'югат призначений для застосування в якості лікарського препарату. [0063] В окремих варіантах здійснення даного винаходу кон'югат призначений для застосування при лікуванні раку у пацієнта, де рак вибрано з групи, що включає рак підшлункової залози, холангіокарциному, рак молочної залози, рак прямої і ободової кишки, рак легені, рак передміхурової залози, рак яєчника, рак шлунка, рак нирки, злоякісну меланому, лейкоз та лімфосаркому. [0064] В ще одному іншому аспекті даний винахід відноситься до способу лікування раку у пацієнта, де рак вибрано з групи, що включає рак підшлункової залози, холангіокарциному, рак молочної залози, рак прямої і ободової кишки, рак легені, рак передміхурової залози, рак яєчника, рак шлунка, рак нирки, злоякісну меланому, лейкоз та лімфосаркому, що включає етап, на якому вводять кон'югат за даним винаходом пацієнту, який цього потребує. [0065] Як використовується у даному документі, "пацієнт" означає будь-якого ссавця або птаха, що може отримати користь від лікування за допомогою кон'югатів токсину з мішеньзв'язуючим фрагментом, описаних в даному документі. Переважно "пацієнт" вибраний з групи, що включає лабораторних тварин (наприклад, мишей або щурів), домашніх тварин (включаючи, 8 UA 110370 C2 5 10 15 20 25 30 35 40 45 50 55 60 наприклад, морську свинку, кроля, курку, свиню, вівцю, козу, верблюда, корову, коня, віслюка, кота або собаку) або приматів, а також людей. Особливо переважним є, щоб "пацієнтом" була людина. [0066] Як застосовується у даному документі, "лікувати", "курс лікування" або "лікування" захворювання або розладу означає виконання одного або декількох з наступного: (a) послаблення тяжкості розладу; (b) обмеження або попередження прогресування симптомів, характерних для розладу(ів), що підлягає лікуванню; (c) затримку наростання симптомів, характерних для розладу(ів), що підлягає лікуванню; (d) обмеження або попередження повторного прояву розладу(ів) у пацієнтів, які раніше мали розлад(и), та (e) обмеження або попередження повторного прояву симптомів у пацієнтів, у яких раніше були клінічні прояви розладу(ів). [0067] Як використовується у даному документі, лікування може включати введення кон'югату або фармацевтичної композиції за даним винаходом пацієнту, при цьому "прийом" включає введення in vivo, а також введення безпосередньо в тканину ex vivo, наприклад, за допомоги венозних трансплантатів. [0068] В окремих варіантах здійснення застосовують терапевтично ефективну кількість кон'югату за даним винаходом. [0069] "Терапевтично ефективна кількість" являє собою кількість терапевтичного засобу достатню для досягнення наміченої мети. Ефективна кількість даного терапевтичного засобу буде змінюватися в залежності від факторів, таких як природа засобу, спосіб введення, розмір та вид тварини, що отримує терапевтичний засіб, та мета введення. Ефективна кількість у кожному окремому випадку може бути встановлена емпірично фахівцем у даній галузі згідно загальновизнаних способів в даній галузі техніки. [0070] У наступному аспекті даний винахід відноситься до фармацевтичної композиції, що містить кон'югат за даним винаходом, додатково містить один або декілька фармацевтично прийнятних розріджувачів, носіїв, наповнювачів, заповнювачів, зв'язуючих речовин, змащувальних засобів, засобів, що забезпечують плинність, розпушувачів, адсорбентів та/або консервантів. [0071] "Фармацевтично прийнятний" означає схвалений контролюючим органом федерального уряду або уряду держави або занесений до списку Фармакопеї США або іншої загальноприйнятої фармакопеї для застосування у тварин та більш конкретно у людей. [0072] В окремих варіантах здійснення фармацевтичну композицію застосовують у вигляді лікарського препарату, який вводять системно. Такий охоплює парентеральні препарати, які включають серед інших препарати для ін'єкцій та інфузій. Препарати для ін'єкцій складені або у вигляді ампул, або так званих готових для застосування препаратів для ін'єкцій, наприклад, готових для застосування шприців або одноразових шприців, та за виключенням цього у вигляді флаконів з пробками що проколюються для багаторазового забору. Введення препаратів для ін'єкцій може бути у вигляді підшкірного (s.c), внутрішньом'язового (i.m.), внутрішньовенного (i.v.) або внутрішньошкірного (i.e.) використання. Зокрема, можливо отримувати відповідно придатні ін'єкційні склади у вигляді суспензії кристалів, розчинів, систем у вигляді наночастинок або колоїднодисперсних систем, таких як, наприклад, гідрозолі. [0073] Склади для ін'єкцій також можна отримати у вигляді концентратів, які можуть бути розчинені або дисперговані у водних ізотонічних розріджувачах. Інфузію також можна отримати у вигляді ізотонічних розчинів, жирових емульсій, ліпосомальних складів та мікроемульсій. Подібно препаратам для ін'єкцій склади для інфузій також можна отримати у вигляді концентратів для розведення. Склади для ін'єкцій також можна використати у вигляді безперервних інфузій як при стаціонарному, так і при амбулаторному лікуванні, наприклад, за допомогою міні-насосів. [0074] До парентеральних лікарських складів можна додавати, наприклад, альбумін, плазму, речовину для збільшення об'єму, поверхнево-активні речовини, органічні розріджувачі, речовини, які впливають на pH, комплексоутворюючі речовини або полімерні речовини, зокрема в якості речовин, які впливають на адсорбцію кон'югатів токсину з мішень-зв'язуючим фрагментом даного винаходу білками або полімерами, або їх можна також додавати з метою зменшення адсорбції кон'югатів токсину з мішень-зв'язуючим фрагментом даного винаходу матеріалами, подібними до інструментів для ін'єкцій або пакувальних матеріалів, наприклад, пластиком або склом. [0075] Кон'югати токсину з мішень-зв'язуючим фрагментом даного винаходу можуть бути зв'язані з мікроносіями або наночастинками в парентеральних препаратах, подібних, наприклад, тонкодисперсним частинкам, на основі полі(мет)акрилатів, полілактатів, полігліколатів, поліамінокислот або поліефіруретанів. Парентеральні склади також можуть бути модифіковані 9 UA 110370 C2 5 10 15 20 25 30 35 40 45 як депо-препарати, наприклад, основані на "принципу багатократної дози", якщо кон'югати токсину з мішень-зв'язуючим фрагментом даного винаходу введені в тонкодисперсну, дисперговану та суспендовану форму, відповідно, або як суспензія кристалів в лікарському препараті або основані на "принципу однократної дози", якщо кон'югат токсину з мішеньзв'язуючим фрагментом даного винаходу включений в склад, наприклад, в таблетку або стержень, який потім вживлюють. Такі імплантати або лікарські депо-препарати пролонгованої дії в складах однократної дози та багатократної дози часто складаються з так званих полімерів, які піддаються біологічному розкладанню, таких як, наприклад, поліестери молочної кислоти та гліколевої кислоти, поліефіруретани, поліамінокислоти, полі(мет)акрилати або полісахариди. [0076] Допоміжні засоби та носії, які додають під час отримання фармацевтичних композицій за даним винаходом, складених у формі парентеральних препаратів, переважно являють собою aqua sterilisata (стерилізована вода), речовини, які впливають на значення рН, такі як, наприклад, органічні або неорганічні кислоти або основи, а також їх солі, буферні речовини для корекції значень рН, речовини для ізотонізації, такі як, наприклад, хлорид натрію, гідрокарбонат натрію, глюкоза та фруктоза, тенсиди та поверхнево-активні речовини, відповідно, та емульгатори, такі як, наприклад, неповні естери жирних кислот і поліоксіетиленсорбітанів (наприклад, Tween®) або, наприклад, естери жирних кислот і поліоксіетиленів (наприклад, Cremophor®), жирні олії, такі як, наприклад, арахісова олія, соєва олія або рицинова олія, синтетичні естери жирних кислот, такі як, наприклад, етилолеат, ізопропілміристат і нейтральна олія (наприклад, Miglyol®), а також полімерні допоміжні речовини, такі як, наприклад, желатин, декстран, полівінілпіролідон, добавки, які підвищують розчинність органічних розчинників, таких як, наприклад, пропіленгліколь, етанол, N, N-диметилацетамід, пропіленгліколь або комплексоутворюючі речовини, такі як, наприклад, цитрат та сечовина, консерванти, такі як, наприклад, гідроксипропіловий естер та метиловий естер бензойної кислоти, бензиловий спирт, антиоксиданти, такі як, наприклад, сульфіт натрію, та стабілізатори, такі як, наприклад, EDTA. [0077] При складанні фармацевтичних композицій даного винаходу у вигляді суспензій в переважному варіанті здійснення додають загусники для попередження осадження кон'югатів токсину з мішень-зв'язуючим фрагментом або тензиди та поліелектроліти для забезпечення ресуспендованості осадів, та/або комплексоутворюючі засоби, такі як, наприклад, EDTA. Також можна забезпечити комплекси активного інгредієнту з різноманітними полімерами. Прикладами таких полімерів є поліетиленгліколь, полістирол, карбоксиметилцелюлоза, Pluronics® або поліетиленгліколевий естер жирної кислоти та сорбіту. Кон'югати токсину і мішень-зв'язуючого фрагмента даного винаходу також можуть бути включені в рідкі склади у вигляді сполук включення, наприклад, з циклодекстринами. В окремих варіантах здійснення диспергуючі засоби можна додавати в якості додаткових допоміжних засобів. Для одержання ліофілізатів можна застосовувати засоби для утворення каркасу, такі як маніт, декстран, сахароза, альбумін людини, лактоза, PVP або різновиди желатину. [0078] В додатковому аспекті даний винахід направлений на спосіб лікування раку підшлункової залози, холангіокарциноми, раку молочної залози, раку прямої і ободової кишки, раку легені, раку передміхурової залози, раку яєчника, раку шлунка, раку нирки, злоякісної меланоми, лейкозу або лімфосаркоми у пацієнта, який потребує цього, який включає введення пацієнту ефективної кількості кон'югату або фармацевтичної композиції даного винаходу. [0079] У іншому аспекті даний винахід відноситься до кон'югаційної молекули аматоксину, яка містить групу Х, що відходить, зв'язану з лінкером L, з'єднаним з аматоксином або аналогом аматоксину, де лінкер L зв'язаний з аматоксином через 1’-N атом амінокислоти 4. [0080] У деяких варіантах здійснення такого аспекту даний винахід стосується кон'югаційної молекули аматоксину формули І, 10 UA 110370 C2 5 10 15 20 25 30 35 40 Формула І, де: R1=H або OH; R2=H або OH; R3=NH2 або OH; R4=OH або OC1-6-алкіл і R5=L-X; де L являє собою лінкер; а X являє собою групу, що відходить, яку можна замістити нуклеофільною групою мішень-зв'язуючого фрагмента. [0081] В окремому варіанті здійснення нуклеофільною групою є первинний амін. [0082] В окремому варіанті здійснення кон'югаційна молекула аматоксину формули І являє собою похідну α-аманітину (R1=OH; R2=OH і R3=NH2). [0083] В окремому варіанті здійснення R4 являє собою O-Me. [0084] В окремих варіантах здійснення лінкер має довжину від 1 до 8 атомів, конкретно від 1 до 6, більш конкретно від 1 до 4 і найбільш конкретно від 2 до 4 атомів. [0085] У деяких варіантах здійснення лінкер L являє собою алкіленову, гетероалкіленову, алкеніленову, гетероалкеніленову, алкініленову, гетероалкініленову, циклоалкіленову, гетероциклоалкіленову, ариленову, гетероариленову, аралкіленову або гетероаралкіленову групу, необов'язково заміщену. [0086] У деяких варіантах здійснення лінкер L містить фрагмент, обраний з одного з наступних фрагментів: дисульфідний, ефірний, амінний, естерний, карбоксамідний, уретановий і сечовинний фрагменти. [0087] У певних варіантах здійснення функціональна група X вибрана з: tбутилоксі, сукцинімідилоксі, 1-О-сукцинімідилокси-3-сульфонату (сульфо-NHS), О-(4-нітрофенілоксі), О-(3нітрофенілоксі), О-(2,4-динітрофенілоксі), О-(2,4-дихлор-6-нітрофенілоксі), пентафторфенілоксі, пентахлорфенілоксі, О-(2,4,5-трихлорфенілоксі), О-(3,4-дигідро-3-гідрокси-4-оксо-1,2,3бензотриазин-3-ілу), О-(ендо-1-гідрокси-5-норборнен-2,3-дикарбоксимід-1-ілу), 1фталімідоїлоксі, 1-бензотриазолілоксі, 1-(7-аза-бензотриазоліл)оксі та N-імідазолілу. [0088] В ще одному аспекті даний винахід відноситься до способу синтезу аматоксинового кон'югату даного винаходу, що включає етап проведення реакції кон'югаційної молекули аматоксину даного винаходу з мішень-зв'язуючим фрагментом, що містить нуклеофільну групу, зокрема первинний амін. [0089] В ще одному аспекті даний винахід відноситься до способу синтезу кон'югаційної молекули аматоксину даного винаходу, який включає етап (і) проведення реакції аматоксину з лінкерної молекулою Y-L-X, де Y являє собою фрагмент, який може вступати в реакцію з 1'-N атомом амінокислоти 4 аматоксину, та де X являє собою групу, що відходить, яка може бути заміщена нуклеофільною групою мішень-зв'язуючого фрагмента, зокрема первинним аміном. [0090] В ще одному аспекті даний винахід відноситься до способу синтезу кон'югаційної молекули аматоксину даного винаходу, який включає етап (і) проведення реакції аматоксину з лінкерної молекулою Y-L-Z, де Y являє собою фрагмент, який може вступати в реакцію з 1'-N атомом амінокислоти 4 аматоксину, та де Z являє собою фрагмент, який може бути перетворений на групу, що відходить, яка може бути заміщена нуклеофільною групою мішеньзв'язуючого фрагмента, зокрема первинним аміном. 11 UA 110370 C2 5 10 15 [0091] У деяких варіантах здійснення проводять реакцію аматоксину з лінкерною молекулою Y-L-X або Y-L-Z, відповідно, де Y обраний з групи, яка включає: O-Tos (O-Tos = тозилат); I; Br і O-Tf (O-Tf = трифлат). У деяких таких варіантах здійснення аматоксин оброблюють Y-L-X або YL-Z, відповідно, у присутності основи, зокрема KOtBu, LiOH або NaH, у розчиннику, зокрема у полярному, апротонному розчиннику, такому як DMF, DMSO або NMP. [0092] У деяких варіантах здійснення група Z являє собою захищену первинну аміногрупу, зокрема NH-C(=O)OtBu. У окремих таких варіантах здійснення з захищеної первинної аміногрупи видаляють захисну групу та потім активують за допомогою похідної карбонової кислоти, такої як дигідроксисукцинімідокарбонат (DSC). [0093] В іншому аспекті даний винахід відноситься до молекули анатоксин-лінкер формули І, де R1-R4 визначені вище; і де R5=L-Z; де L являє собою лінкер; і де Z являє собою фрагмент, який можна перетворити на групу X, що відходить, яка може бути заміщена нуклеофільною групою мішень-зв'язуючого фрагмента, зокрема первинним аміном. ПРИКЛАДИ Нижче даний винахід пояснюється більш детально за допомогою необмежуючих прикладів. Приклад 1 Синтез аманітинів з N1’ лінкером 1.1 Одержання N1’-6-аміногексил-6’-O-метил-α-аманітину (HDP 30.0378) 20 25 30 [0094] Розчиняли 4,86 мг (5,21 мкмоль) O-метил-α-аманітину в 500 мкл безводного DMSO. В атмосфері аргону додавали 11,68 мг (41,67 мкмоль) Boc-аміногексилброміду та 100 мкл 52,1 мM розчину калію t-бутаноляту в DMSO. Додавали додаткові порції t-бутаноляту калію у якості 5,21 мМ маточного розчину: 50 мкл через 1,5 години; 50 мкл через 4години та 50 мкл через 6 годин. Через 19 годин додавали 100 мкл t-бутаноляту калію та 11,96 мг (41,67 мкмоль) Bocаміногексилброміду. Через 21 годину при кімнатній температурі реакційну суміш гасили за допомогою 104 мкл 100 мM розчину оцтової кислоти в DMSO. Неочищений продукт очищали на колонці LaPrep-ВЕРХ: Kromasil 100-C18, 10 мкм, 250 × 20 мм, з метанолом/водою (0,05 % TFA), потік: 26,0 мл/хв., виявлення при λ = 295 нм. Розчинник A: 95 % води: 5 % метанолу, 0,05 % трифтороцтової кислоти. Розчинник B: 10 % води: 90 % метанолу, 0,05 % трифтороцтової кислоти. Градієнт: 0-5 хв. 100 % A; 5-20 хв. 0 % A; 20-25 хв. 0 % A; 25-27 хв. 100 % A; 27-35 хв. 100 % A; фракцію з часом утримання 19,2-20,9 хв. збирали та випарювали розчинники до одержання твердої речовини. + 4,81мг (81 %) HDP 30.0368; MS: 1133 (M+H ). 35 [0095] Розчиняли 4,75 мг (4,19 мкмоль) HDP 30.0368 в 200 мкл трифтороцтової кислоти та 12 UA 110370 C2 5 10 15 20 перемішували впродовж 2 хвилин. Реакційну суміш випарювали насухо при температурі навколишнього середовища та спільно випарювали з 1000 мкл толуолу та 10000 мкл ацетонітрилу. Неочищений продукт очищали на колонці LaPrep-ВЕРХ: Kromasil 100-C18, 10 мкм, 250 × 20 мм, з метанолом/водою (0,05 % TFA), потік: 26,0 мл/хв., виявлення при λ = 295 нм. Розчинник A: 95 % води: 5 % метанолу, 0,05 % трифтороцтової кислоти. Розчинник B: 10 % води: 90 % метанолу, 0,05 % трифтороцтової кислоти. Градієнт: 0-5 хв. 100 % A; 5-20 хв. 0 % A; 20-25 хв. 0 % A; 25-27 хв. 100 % A; 27-35 хв. 100 % A; фракцію з часом утримання 14,9-15,5 хв. збирали та випарювали розчинники та ліофілізували до одержання порошку. + [0096] 1,54 мг (32 %) HDP 30.0378; MS: 1033 (M+H ). 1.2 Одержання N1’-8-амінооктил-6’-O-метил-α-аманітину (HDP 30.0516) [0097] Розчиняли 12,43 мг (13,32 мкмоль) O-метил-α-метиламанітину в 750 мкл безводного DMSO. Додавали 40,00 мг (129,76 мкмоль) N-Boc-8-амінобромактану та 120 мкл 0,1 M розчину LiOH у DMSO/воді 1:1. Реакційну суміш перемішували при кімнатній температурі в атмосфері аргону. Через 18 годин додавали додаткові 80 мкл LiOH з наступним додаванням 40 мкл через 36 годин, 50 мкл через 39 годин і 80 мкл через 44 години. DMSO і воду видаляли у високому вакуумі та залишок очищали на колонці LaPrep-ВЕРХ: Kromasil 100-C18, 10 мкм, 250 × 20 мм, з метанолом/водою (0,05 % TFA), потік: 10,0 мл/хв., виявлення при λ = 230 нм. Розчинник A: 95 % води: 5 % метанолу, 0,05 % трифтороцтової кислоти. Розчинник B: 10 % води: 90 % метанолу, 0,05 % трифтороцтової кислоти. Градієнт: 0-5 хв. 80 % A; 5-10 хв. 50 % A; 10-20 хв. 30 % A; 2050 хв. 20 % A; фракцію з часом утримання 37,0 хв. збирали та випарювали розчинники у вакуумі. + [0098] 3,96 мг (26 %) HDP 30.0496 у вигляді білого порошку. MS: 1160 (M+H ). 25 30 [0099] Розчиняли 3,96 мг (3,41 мкмоль) HDP 30.0496 в 300 мкл трифтороцтової кислоти та перемішували впродовж 2,5 хв. при кімнатній температурі. Реакційну суміш розбавляли 1000 мкл толуолу та випарювали насухо при температурі навколишнього середовища. Залишок спільно випарювали двічі з тим же об'ємом толуолу. Залишок очищали на колонці LaPrep-ВЕРХ: Kromasil 100-C18, 10 мкм, 250 × 20 мм, з метанолом/водою (0,05 % TFA), потік: 10,0 мл/хв., виявлення при λ = 230 нм. Розчинник A: 95 % води: 5 % метанолу, 0,05 % трифтороцтової кислоти. Розчинник B: 10 % води: 90 % метанолу, 0,05 % трифтороцтової кислоти. Градієнт: 0-5 хв. 80 % A; 5-10 хв. 50 % A; 10-20 хв. 30 % A; 20-50 хв. 20 % A; фракцію з часом утримання 21,0 13 UA 110370 C2 хв. збирали та випарювали розчинники у вакуумі. + [00100] 2,66 мг (74 %) HDP 30.0516 у вигляді білого порошку. MS: 1060 (M+H ); 1083 + (M+Na ). 1.3 Одержання N1’-6-амінобутил-6’-O-метил-α-аманітину HDP 30.0592 5 10 15 20 25 [00101] Розчиняли 11,88 мг (12,74 мкмоль) O-метил-α-аманітину в 500 мкл безводного DMSO. В атмосфері аргону додавали 20,00 мг (79,32 мкмоль) Boc-амінобутилброміду та 83,4 мкл 0,25 мM розчину t-бутаноляту калію. У ході реакційного періоду кожен час додавали додаткові порції 20,00 мг (79,32 мкмоль) Boc-амінобутилброміду та 83,4 мкл t-бутаноляту калію. Через 8 годин реакційну суміш гасили за допомогою 100 мкл оцтової кислоти. Неочищений продукт очищали на колонці LaPrep-ВЕРХ: Phenomenex Luna C18, 10 мкм, 250 × 20 мм, з метанолом/водою, потік: 15,0 мл/хв., виявлення при λ = 290 нм. Розчинник A: 100 % води. Розчинник B: 100 % метанолу. Градієнт: 0 хв. 95 % A; 0-5 хв. 50 % A; 5-10 хв. 30 % A; 10-20 хв. 20 % A; 20-45 хв. 5 % A. Фракцію з часом утримання 16,5 хв. збирали та випарювали розчинники. + [00102] 5,10 мг (36 %) HDP 30.0587; MS: 1104,5 (M+H ). [00103] Розчиняли 5,10 мг (4,61 мкмоль) HDP 30.0587 в 1000 мкл трифтороцтової кислоти та перемішували впродовж 2 хв. Реакційну суміш випарювали насухо при температурі навколишнього середовища та сушили у вакуумі. Неочищений продукт очищали на колонці LaPrep-ВЕРХ: колонці: Phenomenex Luna C18, 10 мкм, 250 × 20 мм, з метанолом/водою, потік: 15,0 мл/хв., виявлення при λ = 290 нм. Розчинник A: 95 % води: 5 % метанолу, 0,05 % трифтороцтової кислоти. Розчинник B: 5 % води: 95 % метанолу, 0,05 % трифтороцтової кислоти. Градієнт: 0 хв. 100 % A; 0-5 хв. 50 % A; 5-10 хв. 30 % A; 10-20 хв. 20 % A; 20-45 хв. 0 % A. Фракцію з часом утримання 10,0 хв. збирали та випарювали розчинники. + [00104] 3,48 мг (75 %) HDP 30.0592 білий порошок MS: 1004,4 (M+H ). 1.4 Одержання N1’-6-амінопентил-6’-O-метил-α-аманітину HDP 30.0644 14 UA 110370 C2 5 10 15 20 25 [00105] Розчиняли 8,40 мг (9,00 мкмоль) O-метил-α-метиламанітину в 400 мкл безводного DMSO. Додавали 29,00 мг (108,94 мкмоль) N-Boc-5-амінобромпентану та 14,20 мкл 1 M розчину LiOH у воді. Реакційну суміш перемішували при кімнатній температурі в атмосфері аргону. Через 4 години додавали додаткові 7,10 мкл LiOH. Через 6 годин реакційну суміш гасили за допомогою 100 мкл оцтової кислоти, а DMSO і воду видаляли у високому вакуумі. Залишок очищали на колонці LaPrep-ВЕРХ: Kromasil 100-C18, 10 мкм, 250 × 20 мм, з метанолом/водою Kromasil 100-C18, 10 мкм, 250 × 20 мм, з метанолом/водою, потік: 10,0 мл/хв., виявлення при λ = 290 нм. Розчинник A: 95 % води: 5 % метанолу. Розчинник B: 5 % води: 95 % метанолу. Градієнт: 0-5 хв. 80 % A; 5-10 хв. 50 % A; 10-20 хв. 30 % A; 20-50 хв. 20 % A. Фракцію з часом утримання 30 хв. збирали та випарювали розчинники у вакуумі. + [00106] HDP 30.0636 одержували у вигляді білого порошку. MS: 1118,5 (M+H ). Продукт застосовували на наступному етапі. [00107] Розчиняли HDP 30.0636 в 400 мкл трифтороцтової кислоти та перемішували впродовж 5 хв. при кімнатній температурі. Реакційну суміш розбавляли 1000 мкл толуолу та випарювали насухо при температурі навколишнього середовища. Твердий залишок спільно випарювали з тим самим об'ємом толуолу (2х) та очищали на колонці LaPrep-ВЕРХ: Kromasil 100-C18, 10 мкм, 250 × 20 мм, з метанолом/водою (0,05 % TFA), потік: 10,0 мл/хв., виявлення при λ = 290 нм. Розчинник A: 95 % води: 5 % метанолу, 0,05 % трифтороцтової кислоти. Розчинник B: 10 % води: 90 % метанолу, 0,05 % трифтороцтової кислоти. Градієнт: 0-5 хв. 80 % A; 5-10 хв. 50 % A; 10-20 хв. 30 % A; 20-50 хв. 20 % A. Фракцію з часом утримання 18,0 хв. збирали та випарювали розчинники у вакуумі. + [00108] 0,51 мг білого порошку (загальний вихід 6 %) HDP 30.0644. MS: 1018,4 (M+H ). 1.5 Одержання N1-t-бутилпропіоніл-6-O-метил-α-аманітину HDP 30.0678 15 UA 110370 C2 5 10 15 20 25 30 35 [00109] Розчиняли 7,04 мг (7,55 мкмоль) O-метил-α-метиламанітину в 500 мкл безводного DMSO. Додавали 14,10 мкл 1 M розчину LiOH у воді. Реакційну суміш перемішували при кімнатній температурі в атмосфері аргону протягом 5 хв. і додавали 20 мкл t-бутилового естеру 1-хлорпропіонової кислоти. Через 1 годину додавали додаткові 20,00 мкл LiOH і 20 мкл tбутилового естеру 1-хлорпропіонової кислоти. Через 2 години реакційну суміш гасили за допомогою 100 мкл оцтової кислоти. DMSO і воду видаляли у високому вакуумі та залишок очищали на колонці LaPrep-ВЕРХ: Kromasil 100-C18, 10 мкм, 250 × 20 мм, з метанолом/водою, потік: 10,0 мл/хв., виявлення при λ = 290 нм. Розчинник A: 95 % води: 5 % метанолу. Розчинник B: 5 % води: 95 % метанолу. Градієнт: 0-5 хв. 80 % A; 5-10 хв. 50 % A; 10-20 хв. 30 % A; 20-50 хв. 20 % A. Фракцію з часом утримання 26,0 хв. збирали та випарювали розчинники у вакуумі. + [00110] HDP 30.0677 отримували у вигляді білої твердої речовини. MS: 1047,4 (M+H ). Залишок застосовували на наступному етапі. [00111] Розчиняли HDP 30.0677 в 500 мкл трифтороцтової кислоти та перемішували впродовж 4 хв. при кімнатній температурі. Реакційну суміш випарювали насухо при температурі навколишнього середовища. Залишок спільно випарювали двічі з 5 мл толуолу. Білий залишок очищали на колонці LaPrep-ВЕРХ: Kromasil 100-C18, 10 мкм, 250 × 20 мм, з метанолом/водою (0,05 % TFA), потік: 10,0 мл/хв., виявлення при λ = 290 нм. Розчинник A: 95 % води: 5 % метанолу, 0,05 % трифтороцтової кислоти. Розчинник B: 10 % води: 90 % метанолу, 0,05 % трифтороцтової кислоти. Градієнт: 0-5 хв. 80 % A; 5-10 хв. 50 % A; 10-20 хв. 30 % A; 20-50 хв. 20 % A. Фракцію з часом утримання 18,0 хв. збирали та випарювали розчинники у вакуумі. + [00112] 1,90 мг (25 %) HDP 30.0678 білий порошок. MS: 991,3 (M+H ). 1.6 Одержання N1’-4-Boc-амінометилбензил-6’-O-метил-α-аманітину HDP 30.0683 [00113] Розчиняли 8,90 мг (9,54 мкмоль) O-метил-α-метиламанітину в 500 мкл безводного DMSO. Додавали 21,4 мкл 1 M розчину LiOH у воді. Реакційну суміш перемішували при кімнатній температурі в атмосфері аргону впродовж 10 хв. і додавали 20,00 мг (78,40 мкмоль) 4Вос-амінобензилхлориду. Через 18 годин реакційну суміш гасили за допомогою 100 мкл оцтової кислоти. DMSO і воду видаляли у високому вакуумі та залишок очищали на колонці LaPrepВЕРХ: Kromasil 100-C18, 10 мкм, 250 × 20 мм, з метанолом/водою Kromasil 100-C18, 10 мкм, 250 × 20 мм, з метанолом/водою, потік: 10,0 мл/хв., виявлення при λ = 290 нм. Розчинник A: 95 % води: 5 % метанолу. Розчинник B: 5 % води: 95 % метанолу. Градієнт: 0-5 хв. 80 % A; 5-10 хв. 50 % A; 10-20 хв. 30 % A; 20-50 хв. 20 % A. Фракцію з часом утримання 34,0 хв. збирали та випарювали розчинники у вакуумі з одержанням HDP 30.0680 у вигляді білого залишку. MS: + 1152,5 (M+H ). Продукт застосовували на наступному етапі. 16 UA 110370 C2 5 10 [00114] Розчиняли HDP 30.0680 в 500 мкл трифтороцтової кислоти та перемішували впродовж 10 хвилин при кімнатній температурі, та випарювали насухо при температурі навколишнього середовища. Залишок спільно випарювали двічі з 4 мл толуолу. Білий порошок очищали на колонці LaPrep-ВЕРХ: Kromasil 100-C18, 10 мкм, 250 × 20 мм, з метанолом/водою (0,05 % TFA), потік: 10,0 мл/хв., виявлення при λ = 290 нм. Розчинник A: 95 % води: 5 % метанолу, 0,05 % трифтороцтової кислоти. Розчинник B: 10 % води: 90 % метанолу, 0,05 % трифтороцтової кислоти. Градієнт: 0-5 хв. 80 % A; 5-10 хв. 50 % A; 10-20 хв. 30 % A; 20-50 хв. 20 % A. Фракцію з часом утримання 18,4 хв. збирали та випарювали розчинники у вакуумі. + [00115] 3,15 мг (31 %) HDP 30.0683 у вигляді білого порошку. MS: 1052,4 (M+H ). Приклад 2 Синтез аматоксинового кон'югату Синтез кон'югату HDP 30.0378, Her-DSC-30.0378 [2.8] 15 20 25 30 35 [00116] Розчиняли 1,0 мг HDP 30.0378 в 100 мкл безводного диметилформаміду (DMF). В атмосфері аргону та перемішуючи при кімнатній температурі, одночасно додали 10,4 мкл розчину дигідроксисукцинімідкарбонату (DSC) в DMF (2,56 мг в 100 мкл DMF) та 2,1 мкл триетиламіну. Реакційну суміш перемішували при кімнатній температурі. Через 12 годин додавали 30 мл холодного діетилового ефіру. Збирали осад, промивали кілька раз діетиловим ефіром та сушили у вакуумі. Тверду речовину, що залишилася, помістили в 200 мкл DMF = розчин A. Розчиняли 12,0 мг герцептину в 4,0 мл фосфатного буферного розчину (PBS, pH=7,4) = розчин B. Об'єднували розчин A та розчин B. Розчин герцептину з аманітин-лінкером збовтували при 4 °C впродовж 14 годин та розділяли шляхом гель-фільтраційної хроматографії на Sephadex G-25 (колонка XK-16; 2 мл/хв.). Колонку G-25 попередньо промивали 500 мл розчинів PBS, pH=7,4. Фракцію кон'югату Her-DSC-30.0378 визначали за УФ-поглинанням. Концентрацію білка визначали за допомогою RotiQuant-аналізу (Carl Roth; Німеччина). Навантаження герцептину аманітином визначали шляхом визначення УФ поглинання при A=280 нм та A=310 нм. Розрахували навантаження токсину 2,8 молекул аманітину на кожну молекулу герцептину. Приклад 3 Цитотоксичність Her-DSC-30.0378 [2.8] щодо лінії HER2-позитивних пухлинних клітин in vitro [00117] Цитотоксичну активність Her-DSC-30.0378 [2.8] оцінювали з використанням лінії HER2-позитивних пухлинних клітин SK-OV-3 (яєчник) і за допомогою аналізу із включенням хемілюмінісцентного BrdU (Roche Diagnostics) in vitro. Життєздатність клітин визначали через 72 17 UA 110370 C2 5 години інкубації з різними концентраціями Her-DSC-30.0378 [2.8] при 37 °C та 5 % CО2 шляхом кількісне вимірювання фіксованих та пермеабілізованих клітин з антитілом до BrdU-HRP на планшет-рідері BМG Labtech Optima. Значення EC50 кривої залежності доза-відповідь розраховували за допомогою програмного забеспечення Graphpad Prism 4.0. EC 50 для Her-DSC30.0378 [2.8] з клітинами SK-OV-3 складала 4,1 × 10-11 M. (див. фігуру 2). ФОРМУЛА ВИНАХОДУ 1. Аматоксиновий кон'югат формули І: R1 O R2 H N O O O N H HN HN O N N R4 H R5 N HO O S+ O O NH N H O O R3 10 15 20 25 30 35 40 , Формула І де: R1=Η або ОН; R2=Η або ОН; R3=NH2 або OH; R4=ОН або ОС1-6-алкіл і R5=L-T; де L являє собою лінкер; а Т являє собою мішеньзв'язуючий фрагмент. 2. Аматоксиновий кон'югат за п. 1, де лінкер приєднаний до мішеньзв'язуючого фрагмента через фрагмент сечовини. 3. Аматоксиновий кон'югат за п. 1 або п. 2, де мішеньзв'язуючий фрагмент приєднаний до лінкера L через аміногрупу, присутню в мішеньзв'язуючому фрагменті, де вказана аміногрупа утворює частину вказаного фрагмента сечовини. 4. Аматоксиновий кон'югат за будь-яким з пп. 1-3, де лінкер має довжину від 1 до 8 атомів, конкретно від 1 до 6, більш конкретно від 1 до 4 і найбільш конкретно від 2 до 4 атомів. 5. Аматоксиновий кон'югат за будь-яким з пп. 1-4, де лінкер L являє собою алкіленову, гетероалкіленову, алкеніленову, гетероалкеніленову, алкініленову, гетероалкініленову, циклоалкіленову, гетероциклоалкіленову, ариленову, гетероариленову, аралкіленову або гетероаралкіленову групу, необов'язково заміщену. 6. Аматоксиновий кон'югат за будь-яким з пп. 1-5, де лінкер L містить фрагмент, вибраний з одного з наступних фрагментів: дисульфідний, ефірний, амінний, естерний, карбоксамідний, уретановий і сечовинний фрагменти. 7. Аматоксиновий кон'югат за будь-яким з пп. 1-6, де мішеньзв'язуючий фрагмент специфічно зв'язується з епітопом, який присутній на пухлинній клітині, зокрема, де мішеньзв'язуючий фрагмент специфічно зв'язується з епітопом молекули адгезії епітеліальних клітин (ЕрСАМ). 8. Аматоксиновий кон'югат за будь-яким з пп. 1-7, де мішеньзв'язуючий фрагмент вибраний з групи, що містить: (і) антитіло або його антигензв'язуючу ділянку; (іі) подібний антитілу білок та (ііі) аптамер нуклеїнової кислоти. 9. Аматоксиновий кон'югат за п. 8, де мішеньзв'язуючий фрагмент являє собою антитіло або його антигензв'язуючу ділянку, вибрані з діатіла, тетратіла, нанотіла, химерного антитіла, деімунізованого антитіла, гуманізованого антитіла й антитіла людини. 18 UA 110370 C2 5 10 15 20 25 30 10. Аматоксиновий кон'югат за п. 8 або п. 9, де антигензв'язуюча ділянка вибрана з групи, що включає Fab, F(ab')2, Fd, Fv, одноланцюговий Fv та з'єднані за допомогою дисульфідного містка Fv (dsFv). 11. Аматоксиновий кон'югат за будь-яким з пп. 1-10 для застосування як лікарського препарату. 12. Аматоксиновий кон'югат за будь-яким з пп. 1-11 для застосування при лікуванні раку у пацієнта, де пухлина вибрана з групи, що включає рак підшлункової залози, холангіокарциному, рак молочної залози, рак прямої та ободової кишки, рак легені, рак передміхурової залози, рак яєчника, рак шлунка, рак нирки, злоякісну меланому, лейкоз та лімфосаркому. 13. Фармацевтична композиція, що включає аматоксиновий кон'югат за будь-яким з пп. 1-10 та додатково включає один або декілька фармацевтично прийнятних розріджувачів, носіїв, наповнювачів, заповнювачів, зв'язуючих речовин, змащувальних засобів, засобів, що забезпечують сипкість, розпушувачів, адсорбентів та/або консервантів. 14. Кон'югаційна молекула аматоксину формули І, де R1-R4 визначені в п. 1 і де R5=L-X; де L являє собою лінкер; а X являє собою групу, що відходить, яка може бути заміщена нуклеофільною групою мішеньзв'язуючого фрагмента. 15. Кон'югаційна молекула аматоксину за п. 14, де X являє собою групу, що відходить, яка може бути заміщена первинним аміном. 16. Кон'югаційна молекула аматоксину за п. 14 або п. 15, де X вибраний з: -'бутилокси, сукцинімідилокси, -1-О-сукцинімідилокси-3-сульфонату (-норборнен-2,3-дикарбоксимід-1-ил), -1фталімідоїлокси, -1-бензотриазолілокси, -1-(7-аза-бензотриазоліл)окси) та -N-імідазоліл. 17. Спосіб синтезу аматоксинового кон'югату за будь-яким з пп. 1-12, що включає етап, на якому здійснюють реакцію кон'югаційної молекули аматоксину за будь-яким з пп. 14-16 з мішеньзв'язуючим фрагментом, що містить нуклеофільну групу. 18. Спосіб за п. 17, при якому зазначена нуклеофільна група являє собою первинний амін. 19. Спосіб лікування раку у пацієнта, що включає етап, на якому зазначеному пацієнту вводять аматоксиновий кон'югат за будь-яким з пп. 1-11 або фармацевтичну композицію за п. 13. 20. Спосіб за п. 19, при якому зазначена пухлина вибрана з групи, що включає рак підшлункової залози, холангіокарциному, рак молочної залози, рак прямої та ободової кишок, рак легені, рак передміхурової залози, рак яєчника, рак шлунка, рак нирки, злоякісну меланому, лейкоз та лімфосаркому. 19 UA 110370 C2 20 UA 110370 C2 Комп’ютерна верстка Л. Бурлак Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 21
ДивитисяДодаткова інформація
Автори англійськоюSimon, Werner, Lutz, Christian, Muller, Christoph, Anderl, Jan
Автори російськоюСимон Вернер, Луц Кристиан, Мюллер Кристоф, Андэрль Ян
МПК / Мітки
МПК: A61K 47/48, A61P 35/00
Мітки: кон'югати, аматоксинові, зв'язками, покращеними
Код посилання
<a href="https://ua.patents.su/23-110370-amatoksinovi-konyugati-z-pokrashhenimi-zvyazkami.html" target="_blank" rel="follow" title="База патентів України">Аматоксинові кон’югати з покращеними зв’язками</a>
Попередній патент: Парова турбіна та спосіб створення пікової потужності на енергоблоках теплових електростанцій
Наступний патент: Автоматична зброя
Випадковий патент: Спосіб виробництва горілки