5-алкінілпіримідини
Номер патенту: 110471
Опубліковано: 12.01.2016
Автори: Шнайдер Зігфрід, Кесслер Дірк, ван дер Вен Ларс, Вунберг Тобіас
Формула / Реферат
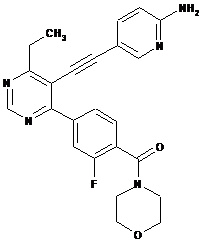
1. Сполуки загальної формули (1)
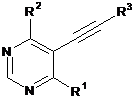 , (1)
, (1)
в якій
R3 означає піридил, необов'язково заміщений одним або більшим числом однакових або різних радикалів, вибраних з метилу, етилу, аміно, метиламіно, етиламіно; і
R1 означає феніл або піридил, необов'язково заміщений одним або більшим числом однакових або різних R5; і
R2 означає С1-С4-алкіл; і
кожний R5 означає групу, вибрану з Rm і Rn; і
кожний Rm незалежно один від одного означає водень або групу, вибрану з С1-С6-алкілу, 2-6-членного гетероалкілу, С1-С6-галогеналкілу, С3-С10-циклоалкілу, С4-С16-циклоалкілалкілу, С6-С10-арилу, С7-С16-арилалкілу, 5-12-членного гетероарилу, 6-18-членного гетероарилалкілу, 3-14-членного гегероциклоалкілу і 4-14-членного гетероциклоалкілалкілу, і Rm необов'язково заміщений одним або більшим числом однакових або різних Rn і/або Ro4,
кожний Rn означає придатну групу і незалежно один від одного вибраний з групи, що включає =O, -ORo, C1-С3-галогеналкілоксигрупу, -OCF3, -OCHF2, =S, -SRo, =NRo, =NORo, =NNRoRo1, =NN(Rs)C(O)NRoRo1, -NRoRo1, -ONRoRo1, -N(ORo)Ro1, -N(Rs)NRoRo1, галоген, -CF3, -CN, -NC, -OCN, -SCN, -NO, -NO2, =N2, -N3, -S(O)Ro, -S(O)ORo, -S(O)2Ro, -S(O)2ORo, -S(O)NRoRo1, -S(O)2NRoRo1, -OS(O)Ro, -OS(O)2Ro, -OS(O)2ORo, -OS(O)NRoRo1, -OS(O)2NRoRo1, -C(O)Ro, -C(O)ORo, -C(O)SRo, -C(O)NRoRo1, -C(O)N(Rs)NRoRo1, -C(O)N(Rs)ORo, -C(NRs)NRoRo1, -C(NOH)Ro, -C(NOH)NRoRo1, -OC(O)Ro, -OC(O)ORo, -OC(O)SRo, -OC(O)NRoRo1, -OC(NRs)NRoRo1, -SC(O)Ro, -SC(O)ORo, -SC(O)NRoRo1, -SC(NRs)NRoRo1, -N(Rs)C(O)Ro, -N[C(O)Ro][C(O)Ro1], -N(ORs)C(O)Ro, -N(Rs)C(NRs1)Ro, -N(Rs)N(Rs1)C(O)Ro, -N[C(O)Ro2]NRoRo1, -N(Rs)C(S)Ro, -N(Rs)S(O)Ro, -N(Rs)S(O)ORo, -N(Rs)S(O)2Ro, -N[S(O)2Ro][S(O)2Ro1], -N(Rs)S(O)2ORo, -N(Rs)S(O)2NRoRo1, -N(Rs)[S(O)2]2Ro, -N(Rs)C(O)ORo, -N(Rs)C(O)SRo, -N(Rs)C(O)NRoRo1, -N(Rs)C(O)NRs1NRoRo1, -N(Rs)N(Rs1)C(O)NRoRo1, -N(Rs)C(S)NRoRo1, -[N(Rs)C(O)]2Ro, -N(Rs)[C(O)]2Ro, -N{[C(O)]2Ro}{[C(O)]2Ro1}, -N(Rs)[C(O)]2ORo, -N(Rs)[C(O)]2NRoRo1, -N{[C(O)]2ORo}{[C(O)]2ORo1},-N{[C(O)]2NRoRo1}{[C(O)]2NRo2Ro3}, -[N(Rs)C(O)]2ORo, -N(Rs)C(NRs1)ORo, -N(Rs)C(NOH)Ro, -N(Rs)C(NRs1)SRo, -N(Rs)C(NRs1)NRoRo1 і -N-C(Rs)NRoRo1, і
кожний Ro, Ro1, Ro2 і Ro3 незалежно один від одного означає водень або групу, вибрану з C1-С6-алкілу, 2-6-членного гетероалкілу, C1-С6-галогеналкілу, C3-С10-циклоалкілу, C4-С16-циклоалкілалкілу, C6-С10-арилу, C7-С16-арилалкілу, 5-12-членного гетероарилу, 6-18-членного гетероарилалкілу, 3-14-членного гетероциклоалкілу і 4-14-членного гетероциклоалкілалкілу, де Ro разом з Ro1 і/або Rs, і/або Rc1, і/або Rc2, і/або Rc3 або Rc2 разом з Rc3 можуть утворювати 3-8-членний моно- або біциклічний гетероциклоалкільний залишок з загальним атомом С, N, О або S, або де Ro разом з Ro1 можуть утворювати 3-14-членний спіроциклічний гетероциклоалкільний залишок з загальним атомом С, N, О або S, і де Ro, Ro1, Ro2 і Ro3 необов'язково незалежно заміщені одним або більшим числом однакових або різних Rp і/або Rq4, і
кожний Rp означає придатну групу і незалежно один від одного вибраний з -O, -OR4, C1-С3-галогеналкілоксигрупу, -OCF3, -OCHF2, =S, -SRq, =NRq, =NORq, =NNRqRq1, =NN(Rs)C(O)NRqRq1, -NRqRq1, -ONRqRq1, -N(Rs)NRqRq1, галоген, -CF3, -CN, -NC, -OCN, -SCN, -NO, -NO2, =N2, -N3, -S(O)Rq, -S(O)ORq, -S(O)2Rq, -S(O)2ORq, -S(O)NRqRq1, -S(O)2NRqRq1, -OS(O)Rq, -OS(O)2Rq, -OS(O)2ORq, -OS(O)NRqRq1, -OS(O)2NRqRq1, -C(O)Rq, -C(O)ORq, -C(O)SRq, -C(O)NRqRq1, -C(O)N(Rs)NRqRq1, -C(O)N(Rs)ORq, -C(NRs)NRqRq1, -C(NOH)Rq, -C(NOH)NRqRq1, -OC(O)Rq, -OC(O)ORq, -OC(O)SRq, -OC(O)NRqRq1, -OC(NRs)NRqRq1, -SC(O)Rq, -SC(O)ORq, -SC(O)NRqRq1, -SC(NRs)NRqRq1, -N(Rs)C(O)Rq, -N[C(O)Rq][C(O)Rq1], -N(ORs)C(O)Rq, -N(Rs)C(Rs1)Rq, -N(Rs)N(Rs1)C(O)Rq, -N[C(O)Rq2]NRqRq1, -N(Rs)C(S)Rq, -N(Rs)S(O)Rq, -N(Rs)S(O)ORq, -N(Rs)S(O)2Rq, -N[S(O)2Rq][S(O)2Rq1], -N(Rs)S(O)2ORq, -N(Rs)S(O)2NRqRq1, -N(Rs)[S(O)2]2Rq, -N(Rs)C(O)ORq, -N(Rs)C(O)SRq, -N(Rs)C(O)NRqRq1, -N(Rs)C(O)NRs1NRqRq1, -N(Rs)N(Rs1)C(O)NRqRq1, -N(Rs)C(S)NRq1, -[N(Rs)C(O)][N(Rg1)C(O)]Rq, -N(Rs)[C(O)]2Rq, -N{[C(O)]2Rq}{[C(O)]2Rq1}, -N(Rs)[C(O)]2ORq, -N(Rs)[C(O)]2NRqRq1, -N{[C(O)]2ORq}{[C(O)]2ORq1}, -N{[C(O)]2NRqRq1}{[C(O)]2NRq2Rq3},-[N(Rs)C(O)][N(Rs1)C(O)]ORq, -N(Rs)C(NRs1)ORq, -N(Rs)C(NOH)Rq, -N(Rs)C(NRs1)SRq, -N(Rs)C(NRs1)NRqRq1, -N(Rs)C(=N-CN)NRqRq1 і -N=C(Rs)NRqRq1, і
кожний Rq, Rq1, Rq2, Rq3 i Rq4 незалежно один від одного означає водень або групу, вибрану з C1-С6-алкілу, 2-6-членного гетероалкілу, C1-С6-галогеналкілу, C3-С10-циклоалкілу, C4-С16-циклоалкілалкілу, C6-С10-арилу, C7-С16-арилалкілу, 5-12-членного гетероарилу, 6-18-членного гетероарилалкілу, 3-14-членного гетероциклоалкілу і 4-14-членного гетероциклоалкілалкілу, де Rq разом з Rq1 і/або Rq2, і/або Rq3, і/або Rs можуть утворювати 3-8-членний гетероциклоалкільний залишок з загальним атомом С, N, О або S, де Rq, Rq1, Rq2, Rq3 і Rq4 необов'язково незалежно заміщені одним або більшим числом однакових або різних Rr і/або Rs4, і
кожний Rr означає придатну групу і в кожному випадку незалежно один від одного вибраний з групи, що включає =O, -ORs, C1-С3-галогеналкілоксигрупу, -OCF3, -OCHF2, =S, -SRs, =NRs, =NORs, =NNRsRs1, =NN(Rt)C(O)NRsRs1, -NRsRs1, -ONRsRs1, -N(Rh)NRsRs1, галоген, -CF3, -CN, -NC, -OCN, -SCN, -NO, -NO2, =N2, -N3, -S(O)Rs, -S(O)ORs, -S(O)2Rs, -S(O)2ORs, -S(O)NRsRs1, -S(O)2NRsRs1, -OS(O)Rs, -OS(O)2Rs, -OS(O)2ORs, -OS(O)NRsRs1, -OS(O)2NRsRs1, -C(O)Rs, -C(O)ORs, -C(O)SRs, -C(O)NRsRs1, -C(O)N(Rt)NRsRs1, -C(O)N(Rt)ORs, -C(NRt)NRsRs1, -C(NOH)Rs, -C(NOH)NRsRs1, -OC(O)Rs, -OC(O)ORs, -OC(O)SRs, -OC(O)NRsRs1, -OC(NRt)NRsRs1, -SC(O)Rs, -SC(O)ORs, -SC(O)NRsRs1, -SC(NRt)NRsRs1, -N(Rt)C(O)Rs, -N[C(O)Rs][C(O)Rs1], -N(ORt)C(O)Rs, -N(Rt)C(NRt1)Rs, -N(Rt)N(Rt1)C(O)Rs, -N[C(O)Rg2]NRsRs1, -N(Rt)C(S)Rs, -N(Rt)S(O)Rs, -N(Rt)S(O)ORs, -N(Rt)S(O)2Rs, -N[S(O)2Rs][S(O)2Rs1], -N(Rt)S(O)2ORs, -N(Rt)S(O)2NRsRs1, -N(Rt)[S(O)2]2Rs, -N(Rt)C(O)ORs, -N(Rt)C(O)SRs, -N(Rt)C(O)NRsRs1, -N(Rt)C(O)NRt1NRsRs1, -N(Rt)N(Rt1)C(O)NRsRs1, -N(Rt)C(S)NRsRs1, -[N(Rt)C(O)][N(Rh1)C(O)]Rs, -N(Rt)[C(O)]2Rs, -N{[C(O)]2Rs}{[C(O)]2Rs1}, -N(Rt)[С(О)]2ОRs, -N(Rt)[C(O)]2NRsRs1, -N{[C(O)]2ORs}{[C(O)]2ORs1}, -N{[C(O)]2NRsRs1}{[C(O)]2NRs2Rs3}, -[N(Rt)С(О)][N(Rt1)C(O)]ORs, -N(Rt)C(NRt1)ORs, -N(Rt)C(NOH)Rs, -N(Rt)C(NRt1)SRs, -N(Rt)C(NRt1)NRsRs1, -N(Rt)C(=N-CN)NRsRs1 і -N=C(Rt)NRsRs1; і
кожний Rs, Rs1, Rs2, Rs3 і Rs4 незалежно один від одного означає водень або групу, вибрану з C1-С6-алкілу, 2-6-членного гетероалкілу, C1-С6-галогеналкілу, C3-С10-циклоалкілу, C4-С16-циклоалкілалкілу, C6-С10-арилу, C7-С16-арилалкілу, 5-12-членного гетероарилу, 6-18-членного гетероарилалкілу, 3-14-членного гетероциклоалкілу і 4-14-членного гетероциклоалкілалкілу, де Rs разом з Rs1 і/або Rs2, і/або Rs3, і/або Rt можуть утворювати 3-8-членний гетероциклоалкільний залишок з загальним атомом С, N, О або S, Rs, Rs1, Rs2, Rs3 i Rs4 необов'язково незалежно заміщені одним або більшим числом однакових або різних Rt2; і
кожний Rt, Rt1 і Rt2 незалежно один від одного вибраний з водню, C1-С6-алкілу, 2-6-членного гетероалкілу, C1-С6-галогеналкілу, C3-С10-циклоалкілу, C4-С16-циклоалкілалкілу, C6-С10-арилу, C7-С16-арилалкілу, 5-12-членного гетероарилу, 6-18-членного гетероарилалкілу, 3-14-членного гетероциклоалкілу і 4-14-членного гетероциклоалкілалкілу, де Rt разом з Rt1 можуть утворювати 3-8-членний гетероциклоалкільний залишок з загальним атомом С, N, О або S, і
необов'язково в формі їх таутомерів, рацематів, енантіомерів, діастереоізомерів і їх сумішей і необов'язково їх фармакологічно прийнятних солей.
2. Сполуки за п. 1, в яких R2 означає -СН3 або -С2Н5.
3. Сполуки за п. 1 або 2, в яких R5 означає групу, вибрану з Rm, Rn; і
кожний Rm незалежно один від одного означає водень або групу, вибрану з -C1-С4-алкілу C4-С6-циклоалкілу, метоксіетилу, циклопропілметилу, фенілу, нафтилу, бензилу, 5-6-членного гетероарилу, 4-6-членного гетероциклоалкілу, де Rm необов'язково незалежно заміщений одним або більшим числом однакових або різних Rn і/або Ro4, і
кожний Rn означає придатну групу і незалежно один від одного вибраний з =O, -ОН, -ОСН3, -ОС2Н5, -OCF3, -OCHF2, -SCH3, =NOH, =NOCH3, -NRoRo1, -F, -Cl, -Br, -CF3, -CN, -NO2, -N3, -S(O)Ro, -S(O)2Ro, -C(O)Ro, -C(O)ORo, -C(O)NRoRo1, -OC(O)Ro, -OC(O)ORo, -OC(O)NRoRo1, -N(Rs)C(O)Ro, -N(Rs)S(O)Ro, -N(Rs)S(O)2Ro, -N(Rs)S(O)2NRoRo1, -N(Rs)C(O)ORo, -N(Rs)C(O)NRoRo1, і
кожний Ro, Ro1 і Ro4 незалежно один від одного означає водень або групу, вибрану з C1-С4-алкілу, 2-6-членного гетероалкілу, C3-С6-циклоалкілу, C4-С10-циклоалкілалкілу, фенілу, бензилу, 5-6-членного гетероарилу, C4-С6-гетероциклоалкілу, де Ro разом з Ro1 і/або Rs можуть утворювати 3-8-членний гетероциклоалкільний залишок з загальним атомом С, N, О або S, де Ro, Ro1 і Ro4 необов'язково незалежно заміщені одним або більшим числом однакових або різних Rp і/або Rq4, і
кожний Rp означає придатну групу і незалежно один від одного вибраний з =O, -ОН, метоксигрупи, етоксигрупи, ізопропоксигрупи, -OCF3, -OCHF2, -SCH3, аміногрупи, метиламіногрупи, диметиламіногрупи, етиламіногрупи, ізопропіламіногрупи, морфоліну, піперидину, піролідину, піперазину, N-метилпіперазину, ацетилу, метилсульфонілу, етилсульфонілу, ізопропілсульфонілу, метоксикарбонілу, етоксикарбонілу, -F, -Сl, -Вr, -CF3, -CN, -S(O)2C2H5, -S(O)2CH3, і
кожний Rq4 означає придатну групу і незалежно один від одного вибраний з С1-С4-алкілу, 4-6-членного гетероалкілу, С4-С6-циклоалкілу, С4-С7-циклоалкілалкілу, фенілу, бензилу, 5-6-членного гетероарилу, 6-8-членного гетероарилалкілу, 4-6-членного гетероциклоалкілу і 4-7-членного гетероциклоалкілалкілу, і
кожний Rs незалежно один від одного означає водень або групу, вибрану з С1-С4-алкілу, 2-6-членного гетероалкілу, С3-С8-циклоалкілу, С4-С10-циклоалкілалкілу, фенілу, бензилу, 5-6-членного гетероарилу, 6-12-членного гетероарилалкілу, 3-8-членного гетероциклоалкілу і 4-10-членного гетероциклоалкілалкілу.
4. Сполуки за будь-яким з пп. 1-3, в яких кожний Rq1 означає придатну групу і незалежно один від одного вибраний з метилу, етилу, 1-пропілу, 2-пропілу, 1-бутилу, трет-бутилу, оксетанілу, тетрагідрофуранілу, тетрагідропіранілу, циклобутилу, циклопентилу, циклогексилу, циклопропілметилу, метоксіетилу, фенілу, бензилу, піридилу, піримідинілу, піридазинілу, імідазолілу, піразолілу, тіазолілу.
5. Сполуки за будь-яким з пп. 1-4, в яких R5 означає групу, вибрану з Rn, і кожний Rn означає придатну групу і незалежно один від одного вибраний з метоксигрупи, етоксигрупи, -F, -Сl, C(O)Ro, -C(О)NRoRo1, і
кожний Ro і Ro1 незалежно один від одного означає водень або групу, вибрану з метилу, етилу, проп-2-ілу, проп-1-ілу, метоксіетилу, циклопропілу, циклобутилу, циклопентилу, циклогексилу, циклопропілметилу, морфоліну, піперидину, піролідину, піперазину, або де Ro і Ro1 утворюють циклічний амін, вибраний з морфоліну, піперазину, гомоморфоліну, гомопіперазину, піперидину, піролідину, де Ro і Ro1 необов'язково незалежно заміщені одним або більшим числом однакових або різних Rp і/або Rq4, і
кожний Rp означає придатну групу і незалежно один від одного вибраний з =O, -OH, метоксигрупи, етоксигрупи, ізопропоксигрупи, аміногрупи, метиламіногрупи, диметиламіногрупи, етиламіногрупи, ізопропіламіногрупи, ацетилу, метилсульфонілу, етилсульфонілу, ізопропілсульфонілу, метоксикарбонілу, етоксикарбонілу, -F, -Сl, -Br, CF3, -CN, і
кожний Rq4 означає придатну групу і незалежно один від одного вибраний з метилу, етилу, 1-пропілу, 2-пропілу, 1-бутилу, 2-бутилу, трет-бутилу, морфолінілу, піперидинілу, піролідинілу, піперазипілу, N-метилпіперазинілу, оксетанілу, тетрагідрофуранілу, тетрагідропіранілу, тстрагідротіофенілу, 1,1-діоксотетрагідротіофенілу, циклопропілу, циклобутилу, циклопентилу, циклогексилу, циклопропілметилу, метоксіетилу, фенілу, бензилу, піридилу, піримідинілу, піридазинілу, імідазолілу, піразолілу, тіазолілу.
6. Сполуки за будь-яким з пп. 1-5, в яких R1 означає піридил і де R5 вибраний з метилу, етилу, н-пропілу, ізопропілу, циклопропілу, метоксигрупи, -СF3.
7. Сполуки за будь-яким з пп. 1-6, в яких R1 означає феніл і де R5 вибраний з R5, і
кожний Rn означає придатну групу і незалежно один від одного вибраний з метилу, метоксигрупи, етоксигрупи, -F, -Сl, C(O)Ro, -C(O)NRoRo, і
кожний Ro і Ro1 незалежно один від одного означає водень або групу, необов'язково заміщену одним або більшим числом однакових або різних Rp і/або Rq4, вибраних з метилу, етилу, проп-2-ілу, проп-1-ілу, метоксіетилу, циклопропілу, циклобутилу, циклопентилу, циклогексилу, циклопропілметилу, морфоліну, піперидину, піролідину, піперазину, або де Ro і Ro1 утворюють циклічний амін, вибраний з морфоліну, піперазину, гомоморфоліну, гомопіперазину, піперидину, піролідину, необов'язково заміщеного одним або більшим числом однакових або різних Rp і/або Rq4, і
кожний Rp означає придатну групу і незалежно один від одного вибраний з =O, -ОН, метоксигрупи, етоксигрупи, ізопропоксигрупи, аміногрупи, метиламіногрупи, диметиламіногрупи, етиламіногрупи, ізопропіламіногрупи, ацетилу, метилсульфонілу, етилсульфонілу, ізопропілсульфонілу, метоксикарбонілу, етоксикарбонілу, -F, -Сl, -Br, -CF3, -CN, і
кожний Rq4 означає придатну групу і незалежно один від одного вибраний з метилу, етилу, 1-пропілу, 2-пропілу, 1-бутилу, 2-бутилу, трет-бутилу, морфолінілу, піперидинілу, піролідинілу, піперазинілу, N-метилпіперазинілу, оксетанілу, тетрагідрофуранілу, тетрагідропіранілу, тетрагідротіофенілу, 1,1-діоксотетрагідротіофенілу, циклопропілу, циклобутилу, циклопентилу, циклогексилу, циклопропілметилу, метоксіетилу, фенілу, бензилу, піридину, піримідинілу, піридазинілу, імідазолілу, піразолілу, тіазолілу.
8. Сполука за будь-яким з пп. 1-7, вибрана з групи, що включає
№
Структура
№
Структура
D-8

D-13

D-15
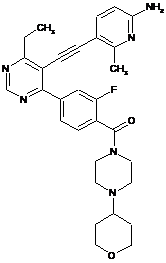
D-20
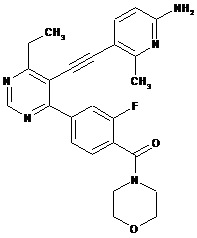
D-21

D-28

D-29
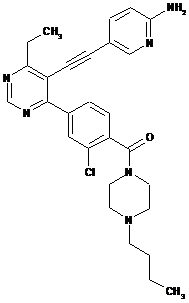
D-31
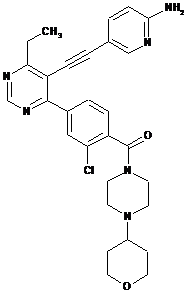
D-38

D-42

D-45

D-58

D-63

D-64

D-70

D-78

D-83

D-84
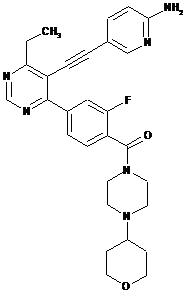
D-95

D-96

D-106

D-121

D-122

D-151
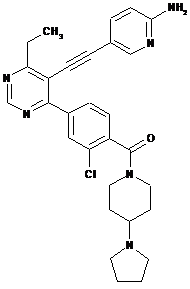
D-79
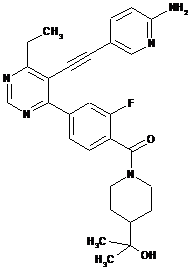
D-236

D-237

D-239
9. Сполуки або їх фармакологічно ефективні солі за будь-яким з пп. 1-8 як лікарські засоби.
10. Сполуки або їх фармакологічно ефективні солі за будь-яким з пп. 1-8, призначені для приготування лікарського засобу, що має антипроліферативну активність.
11. Фармацевтичний препарат, що містить як активну речовину одну або більшу кількість сполук загальної формули (1) за будь-яким з пп. 1-8 або їх фармакологічно ефективних солей, необов'язково в комбінації зі звичайними інертними наповнювачами і/або носіями.
12. Сполуки загальної формули (1) за будь-яким з пп. 1-8, призначені для застосування для лікування і/або попередження раку, інфекцій, запальних і аутоімунних захворювань.
13. Застосування сполук загальної формули (1) за будь-яким з пп. 1-8 для приготування лікарського засобу, призначеного для лікування і/або попередження раку, інфекцій, запальних і аутоімунних захворювань.
14. Фармацевтичний препарат, що містить сполуку загальної формули (1) за будь-яким з пп. 1-8 і щонайменше одну іншу цитостатично або цитотоксично активну речовину, відмінну від формули (1), необов'язково у формі їх таутомерів, рацематів, енантіомерів, діастереоізомерів і їх сумішей, а також необов'язково їх фармакологічно прийнятних солей.
Текст
Реферат: 1 3 Даний винахід належить до сполук загальної формули (1), де значення R -R визначені в пункті 1 формули винаходу, які застосовні для лікування захворювань, що характеризуються надмірною або аномальною проліферацією клітин, і до їх застосування для приготування лікарського засобу, що має зазначені вище характеристики. UA 110471 C2 (12) UA 110471 C2 R 2 R 3 N N R 1 (1) UA 110471 C2 Даний винахід належить до нових 5-алкінілпірімідінів загальної формули (1) 2 R R 3 N 1 R N 5 10 15 20 25 30 35 40 (1), 1 3 в якій групи R - R мають значення, зазначені у формулі винаходу та описі, до їх ізомерів, способів отримання цих алкінілпіримідинів і до їх застосування в якості лікарських засобів. Рівень техніки Раніше показано, що цілий ряд протеїнкіназ є придатними молекулами-мішенями для терапевтичного втручання при різних показаннях, наприклад, при раку і запальних і аутоімунних захворюваннях. Оскільки більша частина генів, що беруть участь в розвитку раку, ідентифікованих до теперішнього часу, кодує кінази, ці ферменти є привабливими молекуламимішенями для лікування, зокрема, раку. Шляхи фосфатіділінозіт-3-кінази (PI3K) активуються в широкому спектрі типів раку людини. Це може відбуватися внаслідок мутації PI3K, що призводить до активації кінази, або непрямим чином шляхом інактивації фосфатази і гомолога тензіну (PTEN), що є супресором. В обох випадках індукується активація каскаду передачі сигналів, що стимулює перетворення клітин in vitro та in vivo. У каскаді передачі сигналів основну роль відіграють ферменти сімейства PI3K і кіназа mTOR. Сімейство PI3K включає 15 ліпідкіназ, що мають різні специфічності по відношенню до субстратів, характеристиками експресії та режимами регулювання. Вони відіграють важливу роль у численних клітинних процесах, таких як, наприклад, процеси росту і диференціації клітин, в регулюванні цитоскелетних змін і регулюванні процесів внутрішньоклітинного переносу. За специфічністю in vitro по відношенню до деяких фосфоінозітних субстратів кінази PI3 можна розділити на різні категорії. Мішенню впливу рапаміцину у ссавців (mTOR) є серин / треонінкіназа, що відноситься до ліпідкіназ сімейства кіназ PI3. Вона існує у вигляді двох комплексів, mTORC1 і mTORC2, які різним чином регулюються, мають різну специфічність по відношенню до субстратів і по-різному сприйнятливі до рапаміцину. mTOR відіграє центральну роль у контролюванні основних шляхів зростання і життєздатності клітин і це викликало інтерес до отримання інгібіторів mTOR, які зв'язуються з ділянкою АТФ (аденозинтрифосфат), і тому їх мішенями є і mTORC2, і mTORC1. Тому інгібування шляху PI3K, особливо опосередковане за допомогою PI3K і mTOR, виявилося привабливою мішенню для лікування раку. 5-Алкінілпіримідини описані, наприклад, в WO 2006044823 в якості сполук, що інгібують протеїнкінази. Детальний опис винаходу Згідно винаходу неочікувано було встановлено, що сполуки загальної формули (1), в якій 1 4 групи R -R мають наведені нижче значення, діють в якості інгібіторів кіназ. Зокрема, сполуки, пропоновані в даному винаході, застосовні в якості інгібіторів кіназ PI3K і mTOR. Таким чином, сполуки, пропоновані в даному винаході, можна застосовувати, наприклад, для лікування захворювань, пов'язаних з активністю кіназ і характеризуються надмірною або аномальною проліферацією клітин, таких як, наприклад, рак. Даний винахід належить до сполук загальної формули (1) 3 2 R R N N 45 1 R (1), в якій 3 R вибраний з групи, що включає 3-8-членний гетероциклоалкіл, C 6-C10-арил і 5-12-членний 4 гетероарил, необов’язково заміщений одним або більше однакових або різних R ; і 1 R вибраний з групи, що включає C6-C10-арил і 5-12-членний гетероарил, необов’язково 5 заміщений одним або більше однакових або різних R ; і 2 R вибраний з групи, що включає водень, C1-C4-алкіл, C3-C8-циклоалкіл, 3-8-членний v v v1 v гетероалкіл, 3-8-членний гетероциклоалкіл, –OR , –NR R , -SR , –CF3, –CN, NC і –NO2, і 1 UA 110471 C2 4 5 10 15 20 25 30 35 40 45 50 55 60 a b кожний R вибраний з R і R ; і a кожний R незалежно один від одного означає водень або вибраний з групи, що включає C 1C6-алкіл, 2-6-членний гетероалкіл, C1-C6-галогеналкіл, C3-C10-циклоалкіл, C4-C16циклоалкілалкіл, C6-C10-арил, C7-C16-арилалкіл, 5-12-членний гетероарил, 6-18-членний a гетероарилалкіл, 3-14-членний гетероциклоалкіл і 4-14-членний гетероциклоалкілалкіл, R b c4 необов’язково заміщений одним або більше однакових або різних R і/або R , b кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що c c c c включає =O, -OR , C1-C3-галогеналкілоксигрупу, –OCF3, -OCHF2, =S, –SR , =NR , =NOR , c c1 g c c1 c c1 c c1 c c1 g c c1 =NNR R , =NN(R )C(O)NR R , –NR R , –ONR R , –N(OR )R , –N(R )NR R , галоген, -CF3, c c c c CN, –NC, –OCN, –SCN, –NO, –NO2, =N2, –N3, –S(O)R , –S(O)OR , -S(O)2R , -S(O)2OR , – c c1 c c1 c c c c c1 c c1 S(O)NR R , –S(O)2NR R , –OS(O)R , –OS(O)2R , -OS(O)2OR , -OS(O)NR R , –OS(O)2NR R , – c c c c c1 g c c1 g c g c c1 C(O)R , –C(O)OR , –C(O)SR , -C(O)NR R , -C(O)N(R )NR R , –C(O)N(R )OR , –C(NR )NR R , – c c c1 c c c c c1 g c c1 C(NOH)R , -C(NOH)NR R , -OC(O)R , –OC(O)OR , –OC(O)SR , –OC(O)NR R , -OC(NR )NR R , c c c c1 g c c1 g c c c1 –SC(O)R , -SC(O)OR , –SC(O)NR R , –SC(NR )NR R , -N(R )C(O)R , –N[C(O)R ][C(O)R ], g c g g1 c g g1 c c2 c c1 g c N(OR )C(O)R , –N(R )C(NR )R , -N(R )N(R )C(O)R , –N[C(O)R ]NR R , -N(R )C(S)R , – g c g c g c c c1 g c N(R )S(O)R , -N(R )S(O)OR , –N(R )S(O)2R , –N[S(O)2R ][S(O)2R ], -N(R )S(O)2OR , g c c1 g c g c g c g c c1 N(R )S(O)2NR R , –N(R )[S(O)2]2R , –N(R )C(O)OR , -N(R )C(O)SR , -N(R )C(O)NR R , – g g1 c c1 g g1 c c1 g c c1 g c N(R )C(O)NR NR R , –N(R )N(R )C(O)NR R , -N(R )C(S)NR R , –[N(R )C(O)]2R , – g c c c1 g c g c c1 N(R )[C(O)]2R , –N{[C(O)]2R }{[C(O)]2R }, -N(R )[C(O)]2OR , –N(R )[C(O)]2NR R , – c c1 c c1 c2 c3 g c N{[C(O)]2OR }{[C(O)]2OR }, –N{[C(O)]2NR R }{[C(O)]2NR R }, -[N(R )C(O)]2OR , – g g1 c g c g g1 c g g1 c c1 g N(R )C(NR )OR , –N(R )C(NOH)R , –N(R )C(NR )SR , -N(R )C(NR )NR R , -N(R )C(=Nc c1 g c c1 CN)NR R і -N=C(R )NR R ; і c c1 c2 c3 c4 кожний R , R , R , R і R незалежно один від одного означає водень або вибраний з групи, що включає C1-C6-алкіл, 2-6-членний гетероалкіл, C1-C6-галогеналкіл, C3-C10-циклоалкіл, C4-C16-циклоалкілалкіл, C6-C10-арил, C7-C16-арилалкіл, 5-12-членний гетероарил, 6-18-членний c c1, гетероарилалкіл, 3-14-членний гетероциклоалкіл і 4-14-членний гетероциклоалкілалкіл, R , R c2 c3 c4 d R , R і R необов’язково незалежно заміщені одним або більше однакових або різних R і/або e4 c g c1 c2 c3 c2 c3 R , де R разом з R і/або R і/або R і/або R або R разом з R можуть утворювати 3-8членний гетероциклоалкільний залишок із загальним атомом C, N, O або S, і d кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що e e e e включає =O, -OR , C1-C3-галогеналкілоксигрупу, -OCF3, -OCHF2, =S, -SR , =NR , =NOR , e e1 g2 e e1 e e1 e e1 g2 e e1 =NNR R , =NN(R )C(O)NR R , -NR R , –ONR R , –N(R )NR R , галоген, -CF3, –CN, -NC, e e e e e e1 OCN, –SCN, -NO, -NO2, =N2, –N3, –S(O)R , –S(O)OR , –S(O)2R , –S(O)2OR , -S(O)NR R , – e e1 e e e e e1 e e1 e S(O)2NR R , –OS(O)R , –OS(O)2R , -OS(O)2OR , –OS(O)NR R , -OS(O)2NR R , –C(O)R , – e e e e1 g2 e e1 g2 e g2 e e1 C(O)OR , –C(O)SR , –C(O)NR R , -C(O)N(R )NR R , -C(O)N(R )OR , –C(NR )NR R , – e e e1 e e e e e1 C(NOH)R , –C(NOH)NR R , –OC(O)R , -OC(O)OR , –OC(O)SR , –OC(O)NR R , – g2 e e1 e e e e1 g2 e e1 g2 e OC(NR )NR R , –SC(O)R , -SC(O)OR , -SC(O)NR R , –SC(NR )NR R , -N(R )C(O)R , – e e1 g2 e g2 g3 e g2 g3 e e2 e e1 N[C(O)R ][C(O)R ] , -N(OR )C(O)R , -N(R )C(NR )R , –N(R )N(R )C(O)R , -N[C(O)R ]NR R , g2 e g2 e g2 e g2 e e e1 N(R )C(S)R , -N(R )S(O)R , –N(R )S(O)OR –N(R )S(O)2R , –N[S(O)2R ][S(O)2R ], g2 e g2 e e1 g2 e g2 e g2 e N(R )S(O)2OR , -N(R )S(O)2NR R , –N(R )[S(O)2]2R , –N(R )C(O)OR , -N(R )C(O)SR , g2 e e1 g2 g3 e e1 g2 g3 e e1 g2 e e1 N(R )C(O)NR R , –N(R )C(O)NR NR R , -N(R )N(R )C(O)NR R , -N(R )C(S)NR R , g2 g3 e g2 e e e1 g2 e [N(R )C(O)][N(R )C(O)]R , –N(R )[C(O)]2R , -N{[C(O)]2R }{[C(O)]2R }, -N(R )[C(O)]2OR , g2 e e1 e e e e1 e2 e3 N(R )[C(O)]2NR R , –N{[C(O)]2OR }{[C(O)]2OR }, -N{[C(O)]2NR R }{[C(O)]2NR R }, g3 g3 e g2 g3 e g2 e g2 g3 e [N(R )C(O)][N(R )C(O)]OR , –N(R )C(NR )OR , –N(R )C(NOH)R , -N(R )C(NR )SR , g2 g3 e e1 g2 e e1 g2 e e1 N(R )C(NR )NR R , -N(R )C(=N-CN)NR R і -N=C(R )NR R ; e e1 e2 e3 e4 кожний R , R , R , R і R незалежно один від одного означає водень або вибраний з групи, що включає C1-C6-алкіл, 2-6-членний гетероалкіл, C1-C6-галогеналкіл, C3-C10-циклоалкіл, C4-C16-циклоалкілалкіл, C6-C10-арил, C7-C16-арилалкіл, 5-12-членний гетероарил, 6-18-членний e гетероарилалкіл, 3-14-членний гетероциклоалкіл і 4-14-членний гетероциклоалкілалкіл, де R g2 e1 e2 e3 e2 e3 разом з R і/або R і/або R і/або R або R разом з R можуть утворити 3-8-членний e e1 e2 e3 e4 гетероциклоалкільний залишок із загальним атомом C, N, O або S, і де R , R , R , R і R f g6 необов’язково незалежно заміщені одним або більше однакових або різних R і/або R , і f кожний R означає підходящу групу і в кожному випадку незалежно один від одного g g вибраний з групи, що включає =O, –OR , C1-C3-галогеналкілоксигрупу, –OCF3, -OCHF2, =S, –SR , g4 g4 g4 g5 h g4 g5 g4 g5 g4 g5 h g4 g5 =NR , =NOR , =NNR R , =NN(R )C(O)NR R , –NR R , –ONR R , –N(R )NR R , галоген, – g4 g4 g4 g4 CF3, -CN, –NC, –OCN, –SCN, –NO, -NO2, =N2, –N3, –S(O)R , -S(O)OR , –S(O)2R , -S(O)2OR , – g4 g5 g4 g5 g4 g4 g4 g4 g5 S(O)NR R , –S(O)2NR R , –OS(O)R , -OS(O)2R , –OS(O)2OR , -OS(O)NR R , – g4 g5 g4 g4 g4 g4 g5 h g4 g5 OS(O)2NR R , –C(O)R , –C(O)OR , -C(O)SR , –C(O)NR R , -C(O)N(R )NR R , – h g4 h g4 g5 g4 g4 g5 g4 g4 C(O)N(R )OR , –C(NR )NR R , -C(NOH)R , –C(NOH)NR R , -OC(O)R , -OC(O)OR , – g4 4g g5 h g4 g5 g4 g4 g4 g5 OC(O)SR , -OC(O)NR R , –OC(NR )NR R , –SC(O)R , -SC(O)OR , –SC(O)NR R , 2 UA 110471 C2 h 5 10 15 20 25 30 35 40 45 50 55 60 g4 g5 h g4 g4 h g4 h h1 g4 SC(NR )NR R , –N(R )C(O)R , –N[C(O)R ]2 , -N(OR )C(O)R , -N(R )C(NR )R , – h h1 g4 g6 g4 g5 h g4 h g4 h g4 N(R )N(R )C(O)R , -N[C(O)R ]NR R , -N(R )C(S)R , -N(R )S(O)R , –N(R )S(O)OR , – h g4 g4 g5 h g4 h g4 g5 h g4 N(R )S(O)2R , –N[S(O)2R ][S(O)2R ], -N(R )S(O)2OR , –N(R )S(O)2NR R , –N(R )[S(O)2]2R , – h g4 h g4 h g4 g5 h h1 g4 g5 N(R )C(O)OR , -N(R )C(O)SR , -N(R )C(O)NR R , –N(R )C(O)NR NR R , – h h1 g4 g5 h g4 g5 h h1 g4 h g4 N(R )N(R )C(O)NR R , -N(R )C(S)NR R , -[N(R )C(O)][N(R )C(O)]R , –N(R )[C(O)]2R , – g4 g5 h g4 h g4 g5 g4 g4 N{[C(O)]2R }{[C(O)]2R }, -N(R )[C(O)]2OR , -N(R )[C(O)]2NR R , –N{[C(O)]2OR }{[C(O)]2OR }, – g4 g5 g4 g5 h h1 g4 h h1 g4 N{[C(O)]2NR R }{[C(O)]2NR R }, -[N(R )C(O)][N(R )C(O)]OR , –N(R )C(NR )OR , – h g4 h h1 g4 h h1 g4 g5 h g4 g5 N(R )C(NOH)R , –N(R )C(NR )SR , -N(R )C(NR )NR R , -N(R )C(=N-CN)NR R і h g4 g5 N=C(R )NR R ; і g g1 g2 g3 g4 g5 g6 кожний R , R , R , R , R , R і R незалежно один від одного означає водень або вибраний з групи, що включає C1-C6-алкіл, 2-6-членний гетероалкіл, C1-C6-галогеналкіл, C3-C10циклоалкіл, C4-C16-циклоалкілалкіл, C6-C10-арил, C7-C16-арилалкіл, 5-12-членний гетероарил, 618-членний гетероарилалкіл, 3-14-членний гетероциклоалкіл і 4-14-членний g g1 h гетероциклоалкілалкіл, де R разом з R і/або R можуть утворити 3-8-членний циклоалкільний g g1 або 3-8-членний гетероциклоалкільний залишок з загальним атомом C, N, O або S,і де R , R , g2 g3 g4 g5 g6 R , R , R , R і R необов’язково незалежно заміщені одним або більше однакових або різних h2 R ;і h h1 h2 кожний R , R і R незалежно один від одного вибраний з групи, що включає водень, C 1-C6алкіл, 2-6-членний гетероалкіл, C1-C6-галогеналкіл, C3-C10-циклоалкіл, C4-C16-циклоалкілалкіл, C6-C10-арил, C7-C16-арилалкіл, 5-12-членний гетероарил, 6-18-членний гетероарилалкіл, 3-14h h1 членний гетероциклоалкіл і 4-14-членний гетероциклоалкілалкіл, де R разом з R можуть утворити 3-8-членний циклоалкільний або 3-8-членний гетероциклоалкільний залишок з загальним атомом C, N, O або S, і 5 m n кожний R вибраний з R і R ; і m кожний R незалежно один від одного означає водень або вибраний з групи, що включає C 1C6-алкіл, 2-6-членний гетероалкіл, C1-C6-галогеналкіл, C3-C10-циклоалкіл, C4-C16циклоалкілалкіл, C6-C10-арил, C7-C16-арилалкіл, 5-12-членний гетероарил, 6-18-членний m гетероарилалкіл, 3-14-членний гетероциклоалкіл і 4-14-членний гетероциклоалкілалкіл, і R n o4 необов’язково заміщений одним або більше однакових або різних R і/або R , n кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що o o o o включає =O, -OR , C1-C3-галогеналкілоксигрупу, –OCF3, -OCHF2, =S, –SR , =NR , =NOR , o o1 s o o1 o o1 o o1 o o1 o o1 =NNR R , =NN(R )C(O)NR R , –NR R , –ONR R , –N(OR )R , –N(Rs)NR R , галоген, -CF3, o o o o CN, –NC, –OCN, -SCN, –NO, –NO2, =N2, –N3, –S(O)R , –S(O)OR , -S(O)2R , -S(O)2OR , – o o1 o o1 o o o o o1 o o1 S(O)NR R , –S(O)2NR R , –OS(O)R , -OS(O)2R , -OS(O)2OR , -OS(O)NR R , –OS(O)2NR R , – o o o o o1 s o o1 s o s o o1 C(O)R , –C(O)OR , –C(O)SR , -C(O)NR R , -C(O)N(R )NR R , –C(O)N(R )OR , –C(NR )NR R , – o o o1 o o o o o1 s o o1 C(NOH)R , -C(NOH)NR R , -OC(O)R , –OC(O)OR , -OC(O)SR , –OC(O)NR R , -OC(NR )NR R , o o o o1 s o o1 s o o o1 –SC(O)R , -SC(O)OR , –SC(O)NR R , –SC(NR )NR R , -N(R )C(O)R , –N[C(O)R ][C(O)R ], s o s s1 o s s1 o o2 o o1 s o N(OR )C(O)R , –N(R )C(NR ) R , -N(R )N(R )C(O)R , -N[C(O)R ]NR R , -N(R )C(S) R , – s o s o s o o o1 s o N(R )S(O)R , -N(R )S(O)OR , –N(R )S(O)2R , –N[S(O)2R ][S(O)2R ], -N(R )S(O)2OR , s o o1 s o s o s o s o o1 N(R )S(O)2NR R , –N(R )[S(O)2]2R , –N(R )C(O)OR , -N(R )C(O)SR , -N(R )C(O)NR R , s s1 o o1 s s1 o o1 s o o1 s o N(R )C(O)NR NR R , –N(R )N(R )C(O)NR R , -N(R )C(S)NR R , –[N(R )C(O)]2R , – s o o o1 s o s o o1 N(R )[C(O)]2R , -N{[C(O)]2R }{[C(O)]2R }, -N(R )[C(O)]2OR , –N(R )[C(O)]2NR R , – o o1 o o1 o2 o3 s o N{[C(O)]2OR }{[C(O)]2OR }, -N{[C(O)]2NR R }{[C(O)]2NR R }, -[N(R )C(O)]2OR , – s s1 o s o s s1 o s s1 o o1 s o o1 N(R )C(NR )OR , –N(R )C(NOH)R , –N(R )C(NR )SR , -N(R )C(NR )NR R і -N=C(R )NR R і o o1 o2 o3 кожний R , R , R і R незалежно один від одного означає водень або вибраний з групи, що включає C1-C6-алкіл, 2-6-членний гетероалкіл, C1-C6-галогеналкіл, C3-C10-циклоалкіл, C4-C16циклоалкілалкіл, C6-C10-арил, C7-C16-арилалкіл, 5-12-членний гетероарил, 6-18-членний o гетероарилалкіл, 3-14-членний гетероциклоалкіл і 4-14-членний гетероциклоалкілалкіл, де R s c1 c2 c3 c2 c3 разом з R і/або R і/або R і/або R або R разом з R можуть утворити 3-8-членний o o1 o2 o3 гетероциклоалкільний залишок з загальним атомом C, N, O або S, і де R , R , R і R p q4 необов’язково незалежно заміщені одним або більше однакових або різних R і/або R , і p кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що q q q q включає =O, -OR , C1-C3-галогеналкілоксигрупу, –OCF3, -OCHF2, =S, –SR , =NR , =NOR , q q1 s q q1 q q1 q q1 s q q1 =NNR R , =NN(R )C(O)NR R , –NR R , –ONR R , –N(R )NR R , галоген, –CF3, –CN, -NC, q q q q q q1 OCN, –SCN, –NO, –NO2, =N2, –N3, –S(O)R , –S(O)OR , –S(O)2R , –S(O)2OR , -S(O)NR R , – q q1 q q q q q1 q q1 q S(O)2NR R , –OS(O)R , –OS(O)2R , -OS(O)2OR , –OS(O)NR R , -OS(O)2NR R , –C(O)R , – q q q q1 s q q1 s q s q q1 C(O)OR , –C(O)SR , –C(O)NR R , -C(O)N(R )NR R , -C(O)N(R )OR , –C(NR )NR R , –C(NOH) q q q1 q q q q q1 s q q1 R , –C(NOH)NR R , –OC(O) R , -OC(O)OR , -OC(O)SR , –OC(O)NR R , –OC(NR )NR R , – q q q q1 s q q1 s q q q1 SC(O) R , -SC(O)OR , -SC(O)NR R , –SC(NR )NR R , -N(R )C(O)R , –N[C(O)R ][C(O) R ] , s q s s1 q s s1 q q2 q q1 s q N(OR )C(O)R , -N(R )C(R )R , –N(R )N(R )C(O)R , -N[C(O)R ]NR R , -N(R )C(S)R , 3 UA 110471 C2 s 5 10 15 20 25 30 35 40 45 50 55 60 q s q s q q q1 s q N(R )S(O)R , –N(R )S(O)OR , –N(R )S(O)2R , –N[S(O)2R ][S(O)2R ], -N(R )S(O)2OR , s q q1 s q s q s q s q q1 N(R )S(O)2NR R , –N(R )[S(O)2]2R , –N(R )C(O)OR , -N(R )C(O)SR , -N(R )C(O)NR R , s s1 q q1 s s1 q q1 s q1 s g1 q N(R )C(O)NR NR R , -N(R )N(R )C(O)NR R , -N(R )C(S)NR , -[N(R )C(O)][N(R )C(O)] R , s q q q1 s q s q q1 N(R )[C(O)]2R , -N{[C(O)]2R }{[C(O)]2R }, -N(R )[C(O)]2OR , –N(R )[C(O)]2NR R , q q1 q q1 q2 q3 s s1 q N{[C(O)]2OR }{[C(O)]2OR }, -N{[C(O)]2NR R }{[C(O)]2NR R }, -[N(R )C(O)][N(R )C(O)]OR , s s1 q s q s s1 q s s1 q q1 s N(R )C(NR )OR , –N(R )C(NOH) R , -N(R )C(NR )SR , -N(R )C(NR )NR R , -N(R )C(=Nq q1 s q q1 CN)NR R і -N=C(R )NR R , і q q1 q2 q3 q4 кожний R , R , R , R і R незалежно один від одного означає водень або вибраний з групи, що включає C1-C6-алкіл, 2-6-членний гетероалкіл, C1-C6-галогеналкіл, C3-C10-циклоалкіл, C4-C16-циклоалкілалкіл, C6-C10-арил, C7-C16-арилалкіл, 5-12-членний гетероарил, 6-18-членний q гетероарилалкіл, 3-14-членний гетероциклоалкіл і 4-14-членний гетероциклоалкілалкіл, де R q1 q2 q3 s разом з R і/або R і/або R і/або R можуть утворити 3-8-членний гетероциклоалкільний q q1 q2 q3 q4 залишок з загальним атомом C, N, O або S, де R , R , R , R і R необов’язково незалежно r s4 заміщені одним або більше однакових або різних R і/або R , і r кожний R означає підходящу групу і в кожному випадку незалежно один від одного s s вибраний з групи, що включає =O, –OR , C1-C3-галогеналкілоксигрупу, –OCF3, -OCHF2, =S, –SR , s s s s1 t s s1 s s1 s s1 h s s1 =NR , =NOR , =NNR R , =NN(R )C(O)NR R , –NR R , –ONR R , –N(R )NR R , галоген, –CF3, s s s s CN, –NC, –OCN, –SCN, –NO, –NO2, =N2, –N3, –S(O)R , -S(O)OR , –S(O)2R , -S(O)2OR , – s s1 s s1 s s s s s1 s s1 S(O)NR R , –S(O)2NR R , –OS(O)R , -OS(O)2R , -OS(O)2OR , -OS(O)NR R , –OS(O)2NR R , – s s s s s1 t s s1 t s t s s1 C(O) R , –C(O)OR , -C(O)SR , –C(O)NR R , -C(O)N(R )NR R , –C(O)N(R )OR , –C(NR )NR R , s s s1 s s s s s1 t s s1 C(NOH) R , –C(NOH)NR R , -OC(O) R , –OC(O)OR , –OC(O)SR , -OC(O)NR R , –OC(NR )NR R , s s s s1 t s s1 t s s s1 –SC(O)R , -SC(O)OR , –SC(O)NR R , -SC(NR )NR R , –N(R )C(O) R , -N[C(O)R ][C(O)R ] , t s t t1 s t t1 s g2 s s1 t s N(OR )C(O)R , -N(R )C(NR )R , –N(R )N(R )C(O)R , –N[C(O)R ]NR R , -N(R )C(S)R , t s t s t s s s1 t s N(R )S(O)R , –N(R )S(O)OR , -N(R )S(O)2R , –N[S(O)2R ][S(O)2R ], -N(R )S(O)2OR , – t s s1 t s t s t s t s s1 N(R )S(O)2NR R , -N(R )[S(O)2]2R , –N(R )C(O)OR , -N(R )C(O)SR , -N(R )C(O)NR R , – t t1 s s1 t t1 s s1 t s s1 t h1 s N(R )C(O)NR NR R , -N(R )N(R )C(O)NR R , -N(R )C(S)NR R , –[N(R )C(O)][N(R )C(O)]R , – t s s s1 t s t s s1 N(R )[C(O)]2R , -N{[C(O)]2R }{[C(O)]2R }, -N(R )[C(O)]2OR , –N(R )[C(O)]2NR R , – s s1 s s1 s2 s3 t t1 s N{[C(O)]2OR }{[C(O)]2OR }, -N{[C(O)]2NR R }{[C(O)]2NR R }, -[N(R )C(O)][N(R )C(O)]OR , – t t1 s t s t t1 s t t1 s s1 t s s1 N(R )C(NR )OR , –N(R )C(NOH)R , -N(R )C(NR )SR , -N(R )C(NR )NR R і -N=C(R )NR R ; і s s1 s2 s3 s4 кожний R , R , R , R і R незалежно один від одного означає водень або вибраний з групи, що включає C1-C6-алкіл, 2-6-членний гетероалкіл, C1-C6-галогеналкіл, C3-C10-циклоалкіл, C4-C16циклоалкілалкіл, C6-C10-арил, C7-C16-арилалкіл, 5-12-членний гетероарил, 6-18-членний s гетероарилалкіл, 3-14-членний гетероциклоалкіл і 4-14-членний гетероциклоалкілалкіл, де R s1 s2 s3 t разом з R і/або R і/або R і/або R можуть утворити 3-8-членний гетероциклоалкільний s s1 s2 s3 s4 залишок з загальним атомом C, N, O або S, R , R , R , R і R необов’язково незалежно t2 заміщені одним або більше однакових або різних R ; і t t1 t2 кожний R , R і R незалежно один від одного вибраний з групи, що включає водень, C 1-C6алкіл, 2-6-членний гетероалкіл, C1-C6-галогеналкіл, C3-C10-циклоалкіл, C4-C16-циклоалкілалкіл, C6-C10-арил, C7-C16-арилалкіл, 5-12-членний гетероарил, 6-18-членний гетероарилалкіл, 3-14t t1 членний гетероциклоалкіл і 4-14-членний гетероциклоалкілалкіл, де R разом з R можуть утворити 3-8-членний гетероциклоалкільний залишок з загальним атомом C, N, O або S, і v v1 кожний R і R незалежно один від одного вибраний з групи, що включає водень, C 1-C6v v1 алкіл, 2-6-членний гетероалкіл, C1-C6-галогеналкіл, де R разом з R можуть утворити 3-8членний гетероциклоалкільний залишок з загальним атомом C, N, O або S, необов’язково у формі їх проліків, таутомерів, рацематів, енантіомерів, діастереоізомерів, проліків і їх сумішей і необов’язково їх фармакологічно прийнятних солей. 2 В бажаному варіанті здійснення R вибраний з групи, що включає C3-C8-циклоалкіл, 3-8v v v1 членний гетероалкіл, 3-8-членний гетероциклоалкіл, –OR , –NR R , –CF3, –CN, -NC і –NO2. 2 В іншому бажаному варіанті здійснення R означає -C1-C4-алкіл. 2 В іншому бажаному варіанті здійснення R означає -CH3 або -C2H5. 1 В іншому бажаному варіанті здійснення R означає феніл або піридил, необов’язково 5 заміщений одним або більше однакових або різних R . 5 m n В іншому бажаному варіанті здійснення R вибраний з R , R ; і m кожний R незалежно один від одного означає водень або вибраний з групи, що включає C1C4-алкіл, C4-C6-циклоалкіл, метоксиетил, циклопропілметил, феніл, нафтил, бензил, 5-6m членний гетероарил, 4-6-членний гетероциклоалкіл, де R необов’язково незалежно заміщений n o4 одним або більше однакових або різних R і/або R , і n кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що o o1 включає =O, -OH, -OCH3, -OC2H5, –OCF3, -OCHF2, –SCH3, =NOH, =NOCH3, -NR R , -F, -Cl, -Br, o o o o o o1 o o CF3, -CN,–NO2, –N3, -S(O)R , -S(O)2R , –C(O)R , –C(O)OR , -C(O)NR R , -OC(O)R , –OC(O)OR , – 4 UA 110471 C2 o 5 10 15 20 25 30 35 40 45 50 55 60 o1 s o s o s o s o o1 s o OC(O)NR R , -N(R )C(O)R , -N(R )S(O)R ,–N(R )S(O)2R , -N(R )S(O)2NR R , –N(R )C(O)OR , s o o1 N(R )C(O)NR R , і o o1 o4 кожний R , R і R незалежно один від одного означає водень або вибраний з групи, що включає C1-C4-алкіл, 2-6-членний гетероалкіл, C3-C6-циклоалкіл, C4-C10-циклоалкілалкіл, феніл, o o1 s бензил, 5-6-членний гетероарил, C4-C6-гетероциклоалкіл, де R разом з R або R можуть o утворити 3-8-членний гетероциклоалкільний залишок з загальним атомом C, N, O або S, де R , o1 o4 p q4 R і R необов’язково незалежно заміщені одним або більше однакових або різних R і/або R , і p кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що включає =O, -OH, метоксигрупу, етоксигрупу, ізопропоксигрупу, –OCF3, - OCHF2, –SCH3, аміногрупу, метиламіногрупу, диметиламіногрупу, етиламіногрупу, ізопропіламіногрупу, морфолін, піперидин, піролідин, піперазин, N-метилпіперазин, ацетил, метилсульфоніл, етилсульфоніл, ізопропілсульфоніл, метоксикарбоніл, етоксикарбоніл, -F, -Cl, -Br, –CF3, –CN, – S(O)2C2H5, –S(O)2CH3, і q4 кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що включає C1-C4-алкіл, 4-6-членний гетероалкіл, C4-C6-циклоалкіл, C4-C7-циклоалкілалкіл, феніл, бензил, 5-6-членний гетероарил, 6-8-членний гетероарилалкіл, 4-6-членний гетероциклоалкіл і 4-7-членний гетероциклоалкілалкіл, і s кожний R незалежно один від одного означає водень або вибраний з групи, що включає C 1C4-алкіл, 2-6-членний гетероалкіл, C3-C8-циклоалкіл, C4-C10-циклоалкілалкіл, феніл, бензил, 5-6членний гетероарил, 6-12-членний гетероарилалкіл, 3-8-членний гетероциклоалкіл і 4-10членний гетероциклоалкілалкіл. q4 В іншому бажаному варіанті здійснення R означає підходящу групу і незалежно один від одного вибраний з групи, що включає метил, етил, 1-пропіл, 2-пропіл, 1-бутил, трет-бутил, оксетаніл, тетрагідрофураніл, тетрагідропіраніл, циклобутил, циклопентил, циклогексил, циклопропілметил, метоксиетил, феніл, бензил, піридил, піримідиніл, піридазиніл, імідазоліл, піразоліл, тіазоліл. 5 n В іншому бажаному варіанті здійснення R вибраний з R , і n кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що o o o1 включає метоксигрупу, етоксигрупу, -F, -Cl, –C(O)R , -C(O)NR R , і o o1 кожний R і R незалежно один від одного означає водень або вибраний з групи, що включає метил, етил, проп-2-іл, проп-1-іл, метоксиетил, циклопропіл, циклобутил, циклопентил, o o1 циклогексил, циклопропілметил, морфолін, піперидин, піролідин, піперазин, або де R і R утворюють циклічний амін, вибраний з групи, що включає морфолін, піперазин, гомоморфолін, o o1 гомопіперазин, піперидин, піролідин, де R і R необов’язково незалежно заміщені одним або p q4 більше однакових або різних R і/або R , і p кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що включає =O, -OH, метоксигрупу, етоксигрупу, ізопропоксигрупу, аміногрупу, метиламіногрупу, диметиламіногрупу, етиламіногрупу, ізопропіламіногрупу, ацетил, метилсульфоніл, етилсульфоніл, ізопропілсульфоніл, метоксикарбоніл, етоксикарбоніл, -F, -Cl, -Br, –CF3, –CN, і q4 кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що включає метил, етил, 1-пропіл, 2-пропіл, 1-бутил, 2-бутил, трет-бутил, морфолініл, піперидиніл, піролідиніл, піперазиніл, N-метилпіперазиніл, оксетаніл, тетрагідрофураніл, тетрагідропіраніл, тетрагідротиофеніл, 1,1-діоксотетрагидротиофеніл, циклопропіл, циклобутил, циклопентил, циклогексил, циклопропілметил, метоксиетил, феніл, бензил, піридил, піримідиніл, піридазиніл, імідазоліл, піразоліл, тіазоліл. 1 5 В іншому бажаному варіанті здійснення R означає піридил, і R вибраний з групи, що включає метил, етил, н-пропіл, ізопропіл, циклопропіл, метоксигрупу, -CF3. 1 5 n В іншому бажаному варіанті здійснення R означає феніл і R вибраний з R , і n кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що o o o1 включає метил, метоксигрупу, етоксигрупу, -F, -Cl, –C(O)R , -C(O)NR R , і o o1 кожний R і R незалежно один від одного означає водень або групу, необов’язково p q4 заміщену одним або більше однакових або різних R і/або R , вибраних з групи, що включає метил, етил, проп-2-іл, проп-1-іл, метоксиетил, циклопропіл, циклобутил, циклопентил, o o1 циклогексил, циклопропілметил, морфолін, піперидин, піролідин, піперазин, або де R і R утворюють циклічний амін, вибраний з групи, що включає морфолін, піперазин, гомоморфолін, гомопіперазин, піперидин, піролідин, необов’язково заміщений одним або більше однакових або p q4 різних R і/або R , і p кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що включає =O, -OH, метоксигрупу, етоксигрупу, ізопропоксигрупу, аміногрупу, метиламіногрупу, 5 UA 110471 C2 5 10 15 20 25 30 35 40 45 50 диметиламіногрупу, етиламіногрупу, ізопропіламіногрупу, ацетил, метилсульфоніл, етилсульфоніл, ізопропілсульфоніл, метоксикарбоніл, етоксикарбоніл, -F, -Cl, -Br, –CF3, –CN, і q4 кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що включає метил, етил, 1-пропіл, 2-пропіл, 1-бутил, 2-бутил, трет-бутил, морфолініл, піперидиніл, піролідиніл, піперазиніл, N-метилпіперазиніл, оксетанил, тетрагідрофураніл, тетрагідропіраніл, тетрагидротіофеніл, 1,1-диоксотетрагидротіофеніл, циклопропіл, циклобутил, циклопентил, циклогексил, циклопропілметил, метоксиетил, феніл, бензил, піридил, піримідиніл, піридазиніл, імідазоліл, піразоліл, тіазоліл. 3 В іншому бажаному варіанті здійснення R означає феніл або піридил, необов’язково 4 заміщений одним або більше однакових або різних R . 4 a b a В іншому бажаному варіанті здійснення R вибраний з R , R і R , заміщену одним або b c більше однакових або різних R і/або R ; і a кожний R незалежно один від одного вибраний з водню, метилу, етилу, і b кожний R означає підходящу групу і незалежно один від одного вибраний з групи, що включає -OCH3, -NH2, -NHCH3, -NHC2H5, -F, -Cl, -Br, -CF3, -CN. 3 В іншому бажаному варіанті здійснення R означає піридил, необов’язково заміщений одним 4 або більше однакових або різних R . 3 4 В іншому бажаному варіанті здійснення R означає піридил і R вибраний з групи, що включає метил, етил, аміногрупу, метиламіногрупу, етиламіногрупу. Сполуки або їх фармакологічно ефективні солі, пропоновані в даному винаході, можна застосовувати в якості лікарських засобів. Сполуки або їх фармакологічно ефективні солі, пропоновані в даному винаході, можна застосовувати для приготування лікарського засобу, що має антипроліферативну активність. Даний винахід також належить до фармацевтичних препаратів, що містять в якості активної речовини одну або більшу кількість сполук загальної формули (1), запропонованих в даному винаході або їх фармакологічно ефективних солей, необов'язково в комбінації зі звичайними інертними наповнювачами і / або носіями. Даний винахід також належить до сполук формули (1), призначеним для застосування для лікування і / або попередження раку, інфекцій, запальних і аутоімунних захворювань. Даний винахід також належить до застосування сполук загальної формули (1), запропонованих в даному винаході, для приготування лікарського засобу, призначеного для лікування і / або попередження раку, інфекцій, запальних і аутоімунних захворювань. Даний винахід також належить до фармацевтичних препаратів, що містять сполуку загальної формули (1), запропоновану в даному винаході, і щонайменше одну іншу цитостатичну або цитотоксичну активну речовину, що відрізняється від формули (1), необов'язково у формі таутомерів, рацематів, енантіомерів, діастереоізомерів і їх сумішей, а також необов'язково їх фармакологічно прийнятних солей. Визначення При використанні у цьому винаході використовуються такі визначення, якщо не вказано інше. Алкільні замісники в кожному випадку означають насичені, ненасичені, що мають лінійній або розгалужений ланцюг аліфатичні вуглеводневі групи (алкільні групи) i це визначення включає і насичені алкільні групи, і ненасичені алкенільні і алкінільні групи. Алкенільні замісники в кожному випадку означають які мають лінійній або розгалужений ланцюг ненасичені алкільні групи, які містять щонайменше один подвійний зв'язок. Алкінільні замісники в кожному випадку означають які мають лінійній або розгалужений ланцюг ненасичені алкільні групи, які містять щонайменше один потрійний зв'язок. Термін гетероалкіл означає групи, які можна утворити з алкілу, визначеного вище в даному винаході в самому широкому значенні, шляхом заміщення в вуглеводневих ланцюгах однієї або більшої кількості груп-CH3 незалежно один від одного групами-OH,-SH або-NH2, однієї або більшого кількості груп-CH2-незалежно один від одного групами-O-,-S-або-NH-, однієї або більшої кількості груп H C групою N , 55 6 UA 110471 C2 5 10 15 20 25 30 35 40 45 50 55 60 однієї або більшої кількості груп = CH-групою = N-, однієї або більшої кількості груп = CH2 групою = NH або однієї або більшої кількості груп ≡ CH групою ≡ N, причому в одному гетероалкілі може міститися не більше 3 гетероатомів і між двома атомами кисню і між двома атомами сірки, або між атомом кисню і атомом сірки повинен знаходитися щонайменше один атом вуглецю і група в цілому повинна бути хімічно стабільна. Безпосереднім результатом непрямого визначення / утворення похідного алкілу є те, що гетероалкіл утворений з підгруп насичених вуглеводневих ланцюгів, що містять гетероатом (и), аналогічним чином - гетероалкеніл і гетероалкініл, і їх можна додатково розділити на що містять лінійний ланцюг (нерозгалужені) i розгалужені. Якщо передбачається, що гетероалкіл є заміщеним, то він може бути моно-або полізаміщеним по всьому що містить атоми водних атомам кисню, сірки, азоту і/або атомам вуглецю незалежно один від одного. Сам гетероалкіл, як замісник, може бути приєднаний до молекули через атом вуглецю і через гетероатом. В якості прикладу перераховані наступні типові сполуки: діметіламінометіл; діметіламіноетіл (1-діметіламіноетіл; 2-діметіламіноетіл); діметіламінопропіл (1-діметіламінопропіл, 2діметіламінопропіл, 3-діметіламінопропіл); діетіламінометіл; діетіламіноетіл (1-діетіламіноетіл, 2-діетіламіноетіл); діетіламінопропіл (1-діетіламінопропіл, 2-діетіламінопропіл, 3діетіламінопропіл); діізопропіламіноетіл (1-діізопропіламіноетіл, 2-діізопропіламіноетіл); біс-2метоксіетіламіногрупу; [2-(діметіламіноетіл) етиламіно] метил; 3-[2-(діметіламіноетіл) етиламіно]пропіл; гідроксиметил; 2-гідроксіетіл; 3-гідроксіпропіл; метоксігрупа; етоксігрупа; пропоксігрупа; метоксіметіл; 2-метоксіетіл і т.п. Галогеналкіл означає алкільні групи, в яких один або більшу кількість атомів водню замінені на атоми галогенів. Галогеналкіл включає і насичені алкільні групи, і ненасичені алкенільні і алкінільні групи, такі як, наприклад, -CF3, -CHF2, -CH2F, -CF2CF3, -CHFCF3, -CH2CF3, -CF2CH3, CHFCH3, -CF2CF2CF3, -CF2CH2CH3, -CF=CF2, -CCl=CH2, -CBr=CH2, -CI=CH2, -C≡C-CF3, CHFCH2CH3 і -CHFCH2CF3. Галоген означає атоми фтору, хлору, брому і / або йоду. C1-C3-Галогеноксигрупа означає C1-C3-галогеналкіл-O-. Циклоалкіл означає моно-або біциклічні кільце або спіроциклічне кільце, в якому кільцева система може являти собою насичене кільце, але може являти собою і ненасичене неароматичне кільце, яке також може необов'язково містити подвійні зв'язки, такі як, наприклад, циклопропіл, циклопропеніл, циклобутил, циклобутеніл, циклопентил, ціклопентеніл, циклогексил, ціклогексеніл, норборніл і норборненіл. Циклоалкілалкіл включає нециклічну алкільну групу, в якій атом водних, пов'язаний з атомом вуглецю, зазвичай з кінцевим атомом C, замінений на ціклоалкільну групу. Арил означає моноциклічні або біциклічні ароматичні кільця, містять 6-10 атомів вуглецю, такі як, наприклад, феніл і нафтил. Арилалкіл включає нециклічну алкільну групу, в якій атом водню, пов'язаний з атомом вуглецю, зазвичай з кінцевим атомом C, замінений на арильну групу. Гетероаріл означає моно-або біциклічні ароматичні кільця, які замість одного або більшої кількості атомів вуглецю містять один або більшу кількість однакових або різних гетероатомів, таких як, наприклад, атоми азоту, сірки або кисню. Приклади включають фуріл, тієніл, піроліл, оксазол, тіазоліл, ізоксазол, ізотіазоліл, піразол, імідазол, триазолам, тетразолію, оксадіазоліл, тіадіазол, піріділ, піримідил, пірідазініл, піразініл і тріазініл. Прикладами біциклічних гетероарільних груп є індол, ізоіндолу, бензофурил, бензотіеніл, бензоксазоліл, бензотіазол, бензізоксазола, бензізотіазоліл, бензімідазолів, бензопіразоліл, індазоліл, ізохіноліну, хінолініл, хіноксалініл, ціннолініл, фталазініл, хіназолін і бензотріазініл, індолізініл, оксазолопіріділ, імідазопіріділ, нафтірідініл, індолініл, ізохроманіл, кульгання, тетрагідроізохінолініл, ізоіндолініл, ізобензотетрагідрофуріл, ізобензотетрагідротіеніл, ізобензотіеніл, бензоксазоліл, пірідопіріділ, бензотетрагідрофуріл, бензотетрагідротіеніл, пуринів, бензодіоксоліл, тріазініл, феноксазініл, фенотіазініл, птерідініл, бензотіазол, імідазопіріділ, імідазотіазоліл, дігідробензізоксазініл, бензізоксазініл, бензоксазініл, дігідробензізотіазініл, бензопіраніл, бензотіопіраніл, кумарини, ізокумарініл, хромонов, хроманоніл, піріділ-N-оксид, тетрагідрохінолініл, дигідрохінолін, дігідрохіноліноніл, дігідроізохіноліноніл, дігідрокумарініл, дігідроізокумарініл, ізоіндоліноніл, бензодіоксаніл, бензоксазоліноніл, піроліл-N-оксид, піримідиніл-N-оксид, пірідазініл-N-оксид, піразініл-N-оксид, хінолін-N-оксид, індол-N-оксид, індолініл-N-оксид, ізохіноліл-N-оксид, хіназолін-N-оксид, хіноксалініл-N-оксид, фталазініл-N-оксид, імідазол-N-оксид, ізоксазол-Nоксид, оксазол-N-оксид, тіазоліл-N-оксид, індолізініл-N-оксид, індазоліл-N-оксид, бензотіазол-Nоксид, бензімідазоліл-N-оксид, піроліл-N-оксид, оксадіазоліл-N-оксид, тіадіазол-N-оксид, триазолам-N-оксид, тетразолію-N-оксид, бензотіопіраніл-S-оксид і бензотіопіраніл-S,S-діоксид. Гетероарілалкіл включає нециклічну алкільну групу, в якій атом водню, пов'язаний з атомом 7 UA 110471 C2 5 10 15 20 25 30 35 40 45 50 55 60 вуглецю, зазвичай з кінцевим атомом C, замінений на гетероарильну групу. Гетероциклоалкіл означає насичені або ненасичені неароматичні моно-, біциклічні, спіроциклічні або місткові біциклічні кільця, містять 3-14 атомів вуглецю, які замість одного або більшої кількості атомів вуглецю містять гетероатоми, такі як атоми азоту, кисню або сірки. Прикладами таких гетероціклоалкільних груп є тетрагідрофурил, піролідиніл, піролініл, імідазолідініл, імідазоліну, піразолідініл, піразолініл, піперідініл, піперазиніл, індолініл, ізоіндолініл, морфоліну, тіоморфолініл, гомоморфолініл, гомопіперідініл, гомопіперазініл, гомотіоморфолініл, тіоморфолініл-S-оксид, тіоморфолініл-S,S-діоксид, тетрагідропіраніл, тетрагідротіеніл, гомотіоморфолініл-S,S-діоксид, оксазолідіноніл, дігідропіразоліл, дігідропіроліл, дігідропіразініл, дігідропіріділ, дігідропірімідініл, дігідрофуріл, дігідропіраніл, тетрагідротіеніл-S-оксид, тетрагідротіеніл-S,S-діоксид, гомотіоморфолініл-S-оксид, 2-окса-5азабіцикло [2.2.1] гептан, 8-окса-3-азабіцикло [3.2.1] октан, 3,8-діазабіцікло [3.2.1] октан, 2,5діазабіцікло [2.2.1] гептан, 3,8-діазабіцікло [3.2.1] октан, 3,9-діазабіцікло [4.2.1] Нона і 2,6діазабіцікло [3.2.2] Нона, 3,9-діазаспіро [5.5] ундекан, 2,9-діазаспіро [5.5] ундекан, 2,8-діазаспіро [4.5] декан, 1,8-діазаспіро [4.5] декан, 3-азаспіро [5.5] ундекан, 1,5-діоксо-9-азаспіро [5.5] ундекан, 2-окса-9-азаспіро [5.5] ундекан, 3-окса-9-азаспіро [5.5] ундекан, 8-азаспіро [4.5] декан, 2-окса-8-азаспіро [4.5] декан, 1,4-діоксо-8-азаспіро [4.5] декан, 3-азаспіро [5.6] додекан, 3,9діазаспіро [5.6] додекан, 9-окса-3-азаспіро [5.6] додекан і 1,3,8-тріазаспіро [4.5] декан. Гетероциклоалкілалкіл означає нециклічну алкільну групу, в якій атом водню, пов'язаний з атомом вуглецю, зазвичай з кінцевим атомом C, замінений на гетероциклоалкільну групу. Наведені нижче приклади ілюструють даний винахід, не накладаючи обмеження на його обсяг. Загальна методика 1 (GP1): Йодування піримідинів або піридинів Розчин піримідину або пірідіну (1,0 екв.) у оцтовій кислоті охолоджують до 0 °C і однією порцією додають NIS (1,0 екв.). Реакційну суміш перемішують при КТ до завершення перетворення вихідної речовини (2-6 год). Суміш виливають в охолоджену льодом воду і обробляють сумішшю 5 % Na2S2O3 і 10 % NaHCO3. Осад відфільтровують, ретельно промивають водою і сушать у вакуумі при 40 °C. Неочищений продукт можна використовувати без додаткового очищення або додатково очистити за допомогою хроматографії на силікагелі в градієнтному режимі з використанням суміші CH2Cl2/MeOH. Загальна методика 2 (GP2): Реакція Соногашира Методика 1: Галогенід (1,0 екв.) розчиняють у ДМФ або ТГФ і додають 0,1 екв. що містить Pd каталізатора (наприклад, PdCl2(PPh3)2 або Pd (PPh3)4) i CuI (0,1 екв.). Потім додають триетиламін (10,0 екв.) I на закінчення алкін (1,5 екв.) I реакційну суміш перемішують при 65 °C. За протіканням реакції стежать за допомогою РХ-МС. Якщо через 4 год йодид піддався перетворенню не повністю, то невеликими порціями додають додаткову кількість алкіну. Продукт осаджується з реакційної суміші (і його відфільтровують і при необхідності перекристалізовують) і/або після видалення розчинника його очищають за допомогою препаративної ОФ-ВЕРХ або за допомогою хроматографії на силікагелі. Методика 2: Галогенід (1,0 екв.) розчиняють у ДМСО і додають Pd (PPh 3)4 (0,1 екв.) I CuI (0,1 екв.). Потім додають діізопропіламін (0,9 екв.) I на закінчення алкін (1,2 екв.). Реакційну суміш поміщають на попередньо нагріту Елекртирні плитку і перемішують при 80 °C. За протіканням реакції стежать за допомогою РХ-МС. Якщо через 4 год галогенід піддався перетворенню не повністю, то невеликими порціями додають додаткову кількість алкіну. Продукт осаджується з реакційної суміші (і його відфільтровують і при необхідності перекристалізовують) і/або після видалення розчинника його очищають за допомогою препаративної ОФ-ВЕРХ або за допомогою флешхроматографії на силікагелі. Загальна методика 3 (GP3): Десилілування алкінів ТМС-алкін (1,0 екв.) розчиняють у MeOH, однією порцією додають K2CO3 (0,5 екв.) i реакційну суміш перемішують при кімнатній температурі до завершення перетворення (3-16 год). Розчинник видаляють у вакуумі, неочищений продукт розчиняють у етилацетаті і органічну фазу екстрагують водою. Органічну фазу сушать, фільтрують і розчинник видаляють у вакуумі. Продукт використовують без додаткового очищення або очищають за допомогою хроматографії на силікагелі з використанням суміші ДХМ / MeOH або (цикло) гексан / етилацетат. Загальна методика 4 (GP4): Комбінація за Судзукі 4-Хлорпіримідин (1,0 екв.) розчиняють у суміші ДМЕ / вода (20:1 об. / Об.), додають боронову кислоту (1,3 екв.), K2CO3 (2,0 екв.) I Pd (PPh3)4 (0,2 екв.) i реакційну суміш перемішують при кип'ятінні зі зворотним холодильником протягом 4 год. у випадку, якщо 8 UA 110471 C2 5 10 15 20 25 30 35 40 45 перетворення вихідної речовини не завершено, додають додаткові кількості боронової кислоти і що містить Pd каталізатора і реакцію проводять при кип'ятінні зі зворотним холодильником протягом ночі. Після охолодження до КТ додають воду. Осад відфільтровують. У випадку, якщо продукт не осаджується, його екстрагують діетиловим ефіром, органічну фазу сушать, фільтрують і розчинник видаляють при зниженому тиску. Отриманий продукт можна використовувати без додаткового очищення або очистити за допомогою хроматографії. Загальна методика 8 (GP8): Омилення складних ефірів Складний ефір переносять у ТГФ або діоксан, додають 1,1-1,5 екв. 1 н. розчину NaOH і суміш кип'ятять із зворотним холодильником, поки дані про протікання реакції не вкажуть на повне перетворення вихідної речовини. Продукт осаджується з реакційної суміші і його використовують без стадій додаткового очищення або його можна додатково очистити за допомогою хроматографії. Загальна методика 9 (GP9): Одержання аміду з використанням амінів Суміш 0,21 моля вихідної речовини, 0,31 моля TBTU (O-(бензотриазол-1-іл)-N,N,N′,N′тетраметилуронійтетрафторборат) або ГАТУ (O-(7-азабензотриазол-1-іл)-N,N,N,Nтетраметилуронійгексафторфосфат) і 0,42 моля основи Хюніга у 2 мл ДМСО або ТГФ, або NMP перемішують протягом 5 хв. Додають 0,31 моля аміну і отриману суміш перемішують при КТ протягом ночі. Очищення проводять за допомогою препаративної ОФ-ВЕРХ і після випарювання розчинника отримують шуканий продукт. Загальна методика 10 (GP10): Отримання аміду з використанням хлорангідридів кислоти До суміші 0,13 моля вихідної речовини і 67 мкл основи Хюніга у 2 мл ТГФ додають 0,26 моля хлорангідридів кислоти. Реакційну суміш перемішують при КТ протягом ночі. Розчинник випарюють і залишок переносять у 1 мл ДМСО. Нерозчинну речовину відфільтровують і отриманий розчин очищають за допомогою препаративної ОФ-ВЕРХ і після випарювання розчинника отримують шуканий продукт. Загальна методика 11 (GP11): Отримання сечовини з використанням ізоціанатів До суміші 0,16 моля вихідної речовини і 64,4 мкл основи Хюніга у 2 мл ТГФ додають 0,49 моля ізоціанату. Реакційну суміш перемішують при КТ протягом ночі. Розчинник випарюють і залишок переносять у 1 мл ДМСО. Нерозчинну речовину відфільтровують і отриманий розчин очищають за допомогою препаративної ОФ-ВЕРХ і після випарювання розчинника отримують шуканий продукт. Загальна методика 12 (GP12): Отримання сечовини шляхом попередньої активації аміну Суміш 0,34 моля аміну і 0,34 моля N,N'-карбонілдіімідазола і 0,34 моля 1,8-діазабіцікло [5.4.0] ундец-7-ена перемішують при КТ протягом 10 хв. Потім однією порцією додають 0,32 моля вихідної речовини. Реакційну суміш нагрівають у мікрохвильовій печі при 100 °C протягом 1 год. Розчинник випарюють і залишок переносять у 1 мл ДМСО. Нерозчинну речовину відфільтровують і отриманий розчин очищають за допомогою препаративної ОФ-ВЕРХ і отримують шуканий продукт. Загальна методика 13 (GP13): Отримання аміду з використанням вугільних кислот Суміш 0,62 моля вугільної кислоти, 0,93 моля TBTU і 1,2 моля основи Хюніга у 2 мл ДМСО перемішують протягом 5 хв. Потім додають 0,31 моля вихідної речовини і отриману суміш перемішують при КТ протягом ночі. Очищення проводять за допомогою препаративної ОФВЕРХ і після випарювання розчинника отримують шуканий продукт. Проміжні продукти A A-1a) 6-Метил-3H-піримідин-4-он N N H 50 O 100 г (0,70 моля) 4-гідрокси-2-меркапто-6-метилпіримідина і 300 г нікелю Ренея суспендують у воді (1000 мл) i суспензію нагрівають і перемішують при кип'ятінні зі зворотним холодильником протягом ночі. Повноту перетворення реєструють за допомогою ТШХ (10 % MeOH у ДХМ). Каталізатор відфільтровують через целіт і фільтрат випарюють і отримують неочищений продукт у вигляді блідо-зеленої твердої речовини. Продукт використовують без додаткового очищення на наступній стадії. A-1b) 5-Йод-6-метил-3H-піримідин-4-он 9 UA 110471 C2 I N N H 5 O При перемішуванні до розчину 70 г (0,64 моля) 4-гідрокси-6-метилпіримідина у оцтовій кислоті при КТ протягом 15 хв порціями додають 127 г (0,56 моля) NIS. Реакційну суміш перемішують при КТ протягом 30 год до витрачення всієї вихідної речовини. Реакційну суміш розбавляють водою і твердий продукт фільтрують і промивають розчином тіосульфату натрію для видалення надлишку йоду. Після сушіння одержують потрібний продукт у вигляді блідокоричневої твердої речовини (90 г; 60%), яку використовують без додаткового очищення. A-1) 4-Хлор-5-йод-6-метилпіримідин I N 10 15 N Cl Суспензію 90 г (0,38 моля) 4-гідрокси-5-йод-6-метилпіримідина у 600 мл POCl3 нагрівають при 90 °C протягом 1 год. Реакційну суміш концентрують при зниженому тиску і залишок виливають на подрібнений лід. Осаджену тверду речовину збирають фільтруванням і промивають водою. Після сушіння одержують потрібний продукт у вигляді твердої речовини (90 г; 93 %). A-2a) 6-Етил-3H-піримідин-4-он N N H 20 25 O 90 г (0,58 моля) 4-гідрокси-2-меркапто-6-етилпіримідина і 270 г нікелю Ренея суспендують у воді (1000 мл). Суспензію нагрівають і перемішують при кип'ятінні зі зворотним холодильником протягом ночі. Повноту перетворення реєструють за допомогою ТШХ (10 % MeOH у ДХМ). Каталізатор відфільтровують через целіт і фільтрат випарюють і отримують неочищений продукт у вигляді блідо-зеленої твердої речовини (70,0 г; 98 %). Продукт використовують без додаткового очищення на наступній стадії. A-2b) 6-Етил-5-йод-3H-піримідин-4-он I N N H 30 O При перемішуванні до розчину 70 г (0,56 моля) 4-гідрокси-6-етилпіримідина у оцтовій кислоті при КТ протягом 15 хв порціями додають 127 г (0,56 моля) NIS. Реакційну суміш перемішують при КТ протягом 30 год до витрачення всієї вихідної речовини. Реакційну суміш розбавляють водою і твердий продукт фільтрують і промивають розчином тіосульфату натрію для видалення надлишку йоду. Після сушіння одержують потрібний продукт у вигляді твердої речовини (90 г; 64 %), яку використовують без додаткового очищення. A-2c) 4-Хлор-5-йод-6-етилпіримідин I N 35 N Cl Суспензію 90 г (0,36 моля) 4-гідрокси-5-йод-6-етилпіримідину в 600 мл POCl3 нагрівають при 10 UA 110471 C2 90 °C протягом 1 год. Реакційну суміш концентрують при зниженому тиску і залишок виливають на подрібнений лід. Осаджену тверду речовину збирають фільтруванням і промивають водою. Після сушіння одержують потрібний продукт у вигляді твердої речовини (65 г; 67 %). A-2) 5-Йод-3-трифторметилпіридин-2-іламін 5 CF3 NH2 10 N I Шукану сполуку синтезують за загальною методикою GP1 з використанням у якості вихідних речовин 5,0 г (31 моль) 3-тріфторпіридин-2-іламіна і 6,9 г (31 моль) NIS. Вихід після осадження з реакційної суміші: 6,78 г (76 %). A-3) 6-Трифторметил-5-йодпіридин-2-іламін NH2 I N CF3 15 Шукану сполуку синтезують за загальною методикою GP1 з використанням у якості вихідних речовин 4,8 г (30 моль) 6-тріфторметилпіридин-2-іламіна і 6,7 г (30 моль) NIS. Вихід після осадження з реакційної суміші і виділення додаткової кількості продукту з маточного розчину за допомогою хроматографії на силікагелі: 5,73 г (67 %). A-4) 5-Йод-6-метилпіридин-2-іламін NH2 I 20 25 N Шукану сполуку синтезують за загальною методикою GP1 з використанням у якості вихідних речовин 2,7 г (25 моль) 6-метилпіридин-2-іламіна і 5,6 г (25 моль) NIS. В ході реакції утворюється невелика кількість відповідного біс-йодпіридину (РХ-МС). Реакційну суміш виливають на лід, після цього осаджується біс-йодований продукт. Матковий розчин обробляють сумішшю 5 % Na2S2O3 і 10 % NaHCO3 і потім нейтралізують шляхом додавання 4 н. розчину NaOH. Осаджений продукт збирають фільтруванням і промивають водою. Вихід: 4,95 г (85 %). A-5) 6-Етил-5-йодпіридин-2-іламін NH2 I 30 N Шукану сполуку синтезують за загальною методикою GP1 з використанням у якості вихідних речовин 10,0 г (83 моля) 6-етілпірідін-2-іламіна і 18,4 г (83 моля) NIS. Вихід після осадження з реакційної суміші: 18,0 г (89 %). A-6) 5-Йод-4-метилпіридин-2-іламін NH2 N I 35 Шукану сполуку синтезують за загальною методикою GP1 з використанням у якості вихідних речовин 2,0 г (18 моль) 4-метилпіридин-2-іламіна і 4,2 г (18 моль) NIS. Вихід після осадження з реакційної суміші: 3,6 г (83 %). A-7) 4-Етил-5-йодпіридин-2-іламін 11 UA 110471 C2 NH2 5 N I Шукану сполуку синтезують за загальною методикою GP1 з використанням у якості вихідних речовин 5,0 г (41 моль) 4-етілпірідін-2-іламіну і 9,2 г (41 моль) NIS. Вихід після осадження з реакційної суміші і виділення додаткової кількості продукту з маточного розчину за допомогою хроматографії на силікагелі: 10,3 г (100 %). A-8) 4-Трифторметил-5-йодпіридин-2-іламін NH2 CF3 N I 10 Шукану сполуку синтезують за загальною методикою GP1 з використанням у якості вихідних речовин 20,0 г (123 моля) 4-тріфторметилпіридин-2-іламіна і 27,8 г (123 моля) NIS. Вихід після осадження з реакційної суміші і виділення додаткової кількості продукту з маточного розчину за допомогою хроматографії на силікагелі: 20,3 г (57 %). A-9) 3-Фтор-5-йодпіридин-2-іламін F NH2 N I 15 Шукану сполуку синтезують за загальною методикою GP1 з використанням у якості вихідних речовин 200 мг (1,78 моля) 3-фторпіридин-2-іламіна і 401 мг (1,78 моля) NIS. Вихід після осадження з реакційної суміші: 380 мг (90 %). A-10) 2-Метил-5-триметилсиланілетинілпіридин N Si 20 25 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 2,0 г (11,6 моля) 5-бромпіридин-2-іламіна і 2,3 мл (16,3 моля) 1-тріметілсілілетіну і з використанням 68 мг (0,36 моля) CuI, 305 мг (1,2 моля) трифенілфосфіна, 213 мг (0,30 моля) PdCl2(PPh3)2 і 18 мл (127 моль) триетиламіну у 18 мл сухого ТГФ. Для обробки реакційну суміш розбавляють етилацетатом, органічну фазу екстрагують водою і розсолом. Продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші гексан / етилацетат. Вихід: 1,5 г (68 %). A-11) 5-Триметилсиланілетинілпіридин-2-іламін NH2 N Si 30 35 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 5,0 г (28,9 моля) 5-бромпіридин-2-іламіна і 5,7 мл (40,5 моля) 1-триметилсилілетіна і з використанням 168 мг (0,88 моля) CuI, 758 мг (2,9 моля) трифенілфосфіна, 533 мг (0,76 моля) PdCl2(PPh3)2 і 40 мл (288 моль) триетиламіну у 40 мл сухого ТГФ. Для обробки реакційну суміш розбавляють етилацетатом і невеликою кількістю циклогексану, органічну фазу екстрагують водою і розсолом. Продукт очищають за допомогою хроматографії на силікагелі з використанням суміші гексан / етилацетат (10/1 об. / Об.). Вихід: 5,0 г (91 %). A-12) Метил-(5-триметилсиланілетинілпіридин-2-іл)-амін 12 UA 110471 C2 H N N Si 5 10 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 4,3 г (23,0 моля) 5-бром-2-метиламінопіридина і 4,5 мл (32,2 моля) 1триметилсилілетіна і з використанням 134 мг (0,71 моля) CuI, 601 мг (2,3 моля) трифенілфосфіна, 420 мг (0,60 моля) PdCl2(PPh3)2 і 32 мл (101 моль) триетіламін у 40 мл сухого ТГФ. Для обробки реакційну суміш розбавляють етилацетатом і невеликою кількістю циклогексану, органічну фазу екстрагують водою і розсолом. Продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші гексан / етилацетат. Вихід: 4,0 г (85 %). A-13) Етил-(5-триметилсиланілетинілпіридин-2-іл)-амін H N N Si 15 20 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 909 мг (4,5 моля) 5-бром-2-етиламінопіридина і 0,89 мл (6,3 моля) 1-тріметілсілілетіну і з використанням 26 мг (0,13 моля) CuI, 118 мг (0,45 моля) трифенілфосфіну, 82 мг (0,12 моля) PdCl2(PPh3)2 і 6,3 мл (45,0 моля) триетиламіну у 7 мл сухого ТГФ. Для обробки реакційну суміш розбавляють етилацетатом і невеликою кількістю циклогексану, органічну фазу екстрагують водою і розсолом. Продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші гексан / етилацетат. Вихід: 980 мг (99 %). A-14) 4-Трифторметил-5-триметилсиланілетинілпіридин-2-іламін NH2 CF3 N Si 25 30 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 12,8 г (44 моля) 4-трифторметил-5-йодпіридин-2-іламіна і 8,8 мл (62 моля) 1триметилсилілетіна і з використанням 844 мг (4,4 моля) CuI, 3,1 г (4,4 моля) PdCl 2(PPh3)2 і 62 мл (443 моля) триетиламіну у 80 мл сухого ТГФ. Для обробки розчинник видаляють при зниженому тиску, неочищений продукт переносять у етилацетат і органічну фазу екстрагують водою. Продукт двічі очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші ДХМ / MeOH. Вихід: 5,85 г (51 %). A-15) 6-Трифторметил-5-триметилсиланілетинілпіридин-2-іламін NH2 N CF3 Si 35 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 5,7 г (20 моль) 6-трифторметил-5-йодпіридин-2-іламіна і 3,9 мл (28 моль) 1триметілсілілетіна і з використанням 379 мг (2,0 моля) CuI, 1,4 г (2,0 моля) PdCl 2(PPh3)2 і 28 мл (199 моль) триетиламіну у 30 мл сухого ТГФ. Для обробки розчинник видаляють при зниженому тиску, неочищений продукт переносять у етилацетат і органічну фазу екстрагують водою. Продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з 13 UA 110471 C2 використанням суміші ДХМ / MeOH. Вихід: 2,83 г (55 %). A-16) 4-Метил-5-триметилсиланілетинілпіридин-2-іламін NH2 N Si 5 10 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 3,3 г (14,1 моля) 4-метил-5-йодпіридин-2-іламіна і 2,8 мл (19,7 моля) 1триметилсилілетіна і з використанням 81 мг (1,4 моля) CuI, 296 мг (0,42 моля) PdCl 2(PPh3)2, 370 мг (1,4 моля) трифенілфосфіна і 20 мл (141 моль) триетиламіну у 25 мл сухого ТГФ. Після охолодження до КТ суміш фільтрують і продукт виділяють з фільтрату за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші ДХМ / MeOH. Вихід: 2,75 г (95 %). A-17) 6-Метил-5-триметилсиланілетинілпіридин-2-іламін NH2 N Si 15 20 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 5,0 г (21,4 моля) 6-метил-5-йодпіридин-2-іламіна і 4,5 мл (32 моля) 1-триметілсілілетіна і з використанням 407 мг (2,1 моля) CuI, 2,0 г (2,1 моля) Pd (PPh 3)4 і 30 мл (214 моль) триетиламіну у 40 мл сухого ДМФ. Для обробки розчинник видаляють при зниженому тиску і продукт двічі очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші ДХМ / MeOH. Вихід: 4,2 г (96 %). A-18) 4-Етил-5-триметилсиланілетинілпіридин-2-іламін NH2 N Si 25 30 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 10,3 г (41,6 моля) 4-етил-5-йодпіридин-2-іламіна і 8,2 мл (58,2 моля) 1триметилсилілетіна і з використанням 792 мг (4,2 моля) CuI, 2,9 г (4,2 моля) PdCl 2(PPh3)2 і 58 мл (416 моль) триетиламіну у 140 мл сухого ТГФ. Для обробки розчинник видаляють при зниженому тиску, неочищений продукт переносять у етилацетат і органічну фазу екстрагують водою. Продукт двічі очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші циклогексан / етилацетат. Вихід: 9,08 г (100 %). A-19) 6-Етил-5-триметилсиланілетинілпіридин-2-іламін NH2 N Si 35 40 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 18 г (72,6 моля) 6-етил-5-йодпіридин-2-іламіна і 14,4 мл (102 моля) 1триметилсилілетіна і з використанням 1,38 г (7,3 моля) CuI, 5,1 г (7,3 моля) PdCl2 (PPh3) 2 і 101 мл (726 моль) триетиламіну у 100 мл сухого ТГФ. Для обробки розчинник видаляють при зниженому тиску, неочищений продукт переносять у етилацетат і органічну фазу екстрагують водою. Продукт двічі очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші циклогексан / етилацетат. Вихід: 12,73 г (80 %). 14 UA 110471 C2 A-20) 5-Триметилсиланілетинілпіридин-3-ол OH N Si 5 10 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 2,0 г (11,6 моля) 5-бром-3-гідроксіпірідіна і 2,3 мл (16,2 моля) 1-триметилсилілетіна і з використанням 66 мг (0,3 моля) CuI, 303 мг (1,2 моля) трифенілфосфіна, 243 мг (0,3 моля) PdCl2(PPh3)2 і 19 мл (139 моль) триетиламіну у 20 мл сухого ТГФ. Для обробки реакційну суміш розбавляють етилацетатом і невеликою кількістю циклогексану, органічну фазу екстрагують водою і розсолом. Продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші ДХМ / MeOH. Вихід: 2,0 г (91 %). A-21) 5-Триметилсиланілетинілпіридин-3-іламін NH2 N Si 15 20 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 2,0 г (11,6 моля) 5-бромпіридин-3-іламіна і 2,3 мл (16,2 моля) 1-триметилсилілетіна і з використанням 66 мг (0,3 моля) CuI, 303 мг (1,2 моля) трифенілфосфіна, 243 мг (0,3 моля) PdCl2(PPh3)2 і 19 мл (139 моль) триетиламіну у 20 мл сухого ТГФ. Для обробки реакційну суміш розбавляють етилацетатом і невеликою кількістю циклогексану, органічну фазу екстрагують водою і розсолом. Продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші ДХМ / MeOH. Продукт осідає на колонці і потім його екстрагують з силікагелю чистим MeOH. Вихід: 2,0 г (91 %). A-22) 5-Триметилсиланілетиніл-1H-піразоло[3,4-b]піридин N NH N Si 25 30 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 1,0 г (5,1 моля) 5-бром-1H-піразоло[4,5-b]пірідіну і 1,0 мл (7,1 моля) 1триметилсилілетіна і з використанням 29 мг (0,15 моля) CuI, 133 мг (0,51 моля) трифенілфосфіна, 106 мг (0,15 моля) PdCl2 (PPh3) 2 і 8,4 мл (60,6 моля) триетиламіну у 8 мл сухого ТГФ. Утворений осад відфільтровують і продукт очищають за допомогою ОФ-ВЕРХ у градієнтному режимі з використанням суміші АЦН/H 2O. Вихід: 542 мг (50 %). A-23) 5-Триметилсиланілетиніл-1H-піроло[2,3-b]піридин NH N Si 35 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 3,0 г (15,2 моля) 5-бром-1H-піроло[2,3-b]пірідіну і 3,0 мл (21,3 моля) 1триметилсилілетіну і з використанням 87 мг (0,46 моля) CuI, 400 мг (1,5 моля) трифенілфосфіну, 15 UA 110471 C2 312 мг (0,46 моля) PdCl2(PPh3)2 і 25,4 мл (182 моля) триетиламіну в 25 мл сухого ТГФ. Утворений осад відфільтровують і продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші ДХМ / MeOH. Вихід: 3,05 г (94 %). A-24) 6-Триметилсиланілетиніл-3H-імідазо[4,5-b]піридин 5 N NH N Si 10 Шукану сполуку синтезують за загальною методикою GP2 з використанням у якості вихідних речовин 1,2 г (6,1 моля) 5-бром-3H-імідазо [4,5-b] пірідіну і 1,2 мл (8,4 моля) 1триметилсилілетіна і з використанням 34 мг (0,18 моля) CuI, 159 мг (0,61 моля) трифенілфосфіна, 128 мг (0,18 моля) PdCl2(PPh3)2 і 10,1 мл (72,7 моля) триетиламіну у 10 мл сухого ТГФ. Утворений осад відфільтровують і продукт очищають за допомогою ОФ-ВЕРХ у градієнтному режимі з використанням суміші АЦН/H 2O. Вихід: 606 мг (46 %). A-25) 5-Етиніл-2-метилпіридин x HCl N 15 20 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 2,2 г (12 моль) 2-метил-5-триметилсиланілетинілпіридину і 0,80 г (5,8 моля) K 2CO3 у 13 мл MeOH. Неочищений продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші циклогексан / етилацетат. Продукт екстрагують з органічної фази 1 н. розчином HCl і після ліофілізації виділяють у вигляді гідрохлориду. Вихід: 1,3 г (73 %). A-26) 5-Етинілпіридин-2-іламін NH2 N 25 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 5,5 г (29 моль) 5-триметилсиланілетинілпіридин-2-іламіна і 2,0 г (14 моль) K2CO3 у 30 мл MeOH. Продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші гексан / етилацетат. Вихід: 2,9 г (85 %). A-27) (5-Етинілпіридин-2-іл)-метиламін 30 H N N 35 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 1,5 г (7,3 моля) метил-(5-триметилсиланилетинилпіридин-2-іл)-аміна і 507 мг (3,7 моля) K2CO3 у 10 мл MeOH. Вихід після хроматографії на силікагелі: 698 мг (56 %). A-28) (5-Етинілпіридин-2-іл)-етиламін H N N 40 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 980 мг (4,5 моля) ТМС-алкіну і 310 мг (2,3 моля) K2CO3 у 6 мл MeOH. Вихід після хроматографії на силікагелі: 388 мг (59 %). A-29) 5-Етиніл-4-трифторметилпіридин-2-іламін 16 UA 110471 C2 NH2 CF3 N 5 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 5,9 г (22,6 моля) і 1,56 г (11,3 моля) K2CO3 у 50 мл MeOH. Продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші ДХМ / MeOH. Вихід: 2,97 г (71 %). A-30) 5-Етиніл-6-трифторметилпіридин-2-іламін NH2 N CF3 10 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 2,82 г (11,0 моля) і 757 мг (5,5 моля) K2CO3 у 25 мл MeOH. Продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші циклогексан / етилацетат. Вихід: 0,9 г (44 %). A-31) 5-Етиніл-4-метилпіридин-2-іламін NH2 N 15 20 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 1,8 г (8,8 моля) 4-метил-5-триметилсиланилетинилпіридин-2-іламіна і 609 мг (4,4 моля) K2CO3 в 315 мл MeOH. Продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші ДХМ / MeOH. Вихід: 1,0 г (86 %). A-32) 5-Етиніл-6-метилпіридин-2-іламін NH2 N 25 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 4,3 г (21,0 моля) 6-метил-5-триметилсиланилетинилпіридин-2-іламіна і 1,5 г (10,5 моля) K2CO3 у 30 мл MeOH. Продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші ДХМ / MeOH. Вихід: 3,6 г. A-33) 4-Етил-5-етинілпіридин-2-іламін NH2 N 30 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 3,3 г (15 моль) 4-етил-5-триметилсиланилетинилпіридин-2-іламіна і 1,04 г (7,5 моля) K2CO3 у 30 мл MeOH. Продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші ДХМ / MeOH. Вихід: 1,78 г (81 %). A-34) 6-Етил-5-етинілпіридин-2-іламін 35 NH2 N Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 12,23 г (56 моль) 6-етил-5-триметилсиланілетинілпіридин-2-іламіна і 3,87 г (28 моль) 17 UA 110471 C2 K2CO3 у 120 мл MeOH. Продукт очищають за допомогою хроматографії на силікагелі у градієнтному режимі з використанням суміші ДХМ / MeOH. Вихід: 4,5 г (85 %). A-35) 5-Етинілпіридин-3-ол OH N 5 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 2,0 г (10,5 моля) ТМС-алкіну і 722 мг (5,2 моля) K2CO3 у 10 мл MeOH. Вихід після хроматографії на силікагелі: 804 мг (49 %). A-36) 5-Етинілпіридин-3-іламін 10 NH2 x HCl N 15 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 2,0 г (11 моль) ТМС-алкіну і 722 мг (5,2 моля) K2CO3 у 10 мл MeOH. Вихід після хроматографії на силікагелі і осадження з суміші діоксану/HCl: 1,2 г (74 %). A-37) 5-Етиніл-1H-піразоло[3,4-b]піридин N NH N 20 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 542 мг (2,5 моля) ТМС-алкіну і 174 мг (1,3 моля) K2CO3 у 6 мл MeOH. Вихід після екстракціі: 330 мг (92 %). A-38) 5-Етиніл-1H-піроло[2,3-b]піридин NH N 25 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 3,1 г (14 моль) ТМС-алкіну і 983 мг (7,1 моля) K2CO3 у 15 мл MeOH. Вихід після хроматографії на силікагелі: 1,2 г (61 %). A-39) 6-Етиніл-3H-імідазо[4,5-b]піридин N NH N 30 Шукану сполуку синтезують за загальною методикою GP3 з використанням у якості вихідних речовин 706 мг (3,3 моля) ТМС-алкіну і 227 мг (1,6 моля) K2CO3 у 6 мл MeOH. Вихід після екстракціі: 491 мг (94 %). A-40) 4-Хлор-6-метил-5-піридин-3-ілетинілпіримідин 18 UA 110471 C2 N N 5 Cl N Шукану сполуку синтезують за загальною методикою GP2 з використанням в якості вихідної речовини 250 мг (1,0 моля) 4-хлор-5-йод-6-метилпіримідина і з використанням 123 мг (1,2 моля) 3-етинілпіридина, 18 мг (0,10 моля) CuI, 34 мг (0,05 моля) біс-(трифенілфосфін) паладій (II) хлориду, 0,5 мл триетиламіну у 2 мл ДМФ. Реакційну суміш перемішують при 60 °C протягом 3 г. Після видалення розчинника при зниженому тиску продукт очищають за допомогою ОФ-ВЕРХ. Вихід: 25 мг (11 %). A-41) 5-(6-Амінопіридин-3-ілетиніл)-4-хлор-6-метилпіримідин NH2 N N 10 15 Cl N Шукану сполуку можна синтезувати за загальною методикою GP2 з використанням у якості вихідних речовин 30 г (0,11 моля) 4-хлор-5-йод-6-метилпіримідина (A-1) i 26,4 г (0,22 моля) 5 етинілпіридин-2-іламіна (A-36) i з використанням 2,1 г (11 моль) йодиду міді і 7,9 г (11 моль) біс (трифенілфосфін) палладійхлорида і триетиламіну у 600 мл ТГФ. Після обробки і хроматографії (діоксид кремнію, елюент: 5 % MeOH у ДХМ) отримують 13 г (45 %) шуканого продукту. A-42) 4-Хлор-6-етил-5-(6-метилпіридин-3-ілетиніл)піримідин N N 20 25 Cl N Шукану сполуку синтезують за загальною методикою GP2 з використанням в якості вихідної речовини 250 мг (1,0 моля) 4-хлор-6-етил-5-йодпіримідин і з використанням 121,5 мг (1,2 моля) 5-етиніл-2-метилпіримідина, 18 мг (0,10 моля) CuI, 34 мг (0,05 моля) біс-(трифенілфосфін) паладій (II) хлориду, 0,5 мл триетиламіну у 2 мл ДМФ. Реакційну суміш перемішують при 60 °C протягом 3 г. Після видалення розчинника при зниженому тиску продукт очищають за допомогою ОФ-ВЕРХ. Вихід: 25 мг (11 %). A-43) 5-(6-Амінопіридин-3-ілетиніл)-4-хлор-6-етилпіримідин NH2 N N N 30 Cl При перемішуванні до розчину 60 г (0,22 моля) 4-хлор-5-йод-6-етилпіримідина (A-2) у 1200 мл ТГФ у атмосфері аргону додають 4,2 г (22 моля) CuI і 15,7 г (22 моля) біс (трифенілфосфін) паладійхлорида. Реакційну суміш продувають аргоном протягом 30 хв. Додають 15,7 г (0,22 моля) 5-етинілпіридин-2-іламіна (A-36) i триетиламін і реакційну суміш нагрівають при 60 °C протягом 4 год. Після обробки і хроматографії (діоксид кремнію, елюент: 5 % MeOH у ДХМ) отримують 26 г (45 %) шуканого продукту. A-44) 5-(6-Аміно-2-метилпіридин-3-ілетиніл)-4-хлор-6-етилпіримідин 35 19 UA 110471 C2 NH2 N N N 5 10 Cl Шукану сполуку синтезують за загальною методикою GP2 з використанням в якості вихідної речовини 6,0 г (22,3 моля) 4-хлор-6-етил-5-йодпіримідина і з використанням 3,5 г (26,8 моля) 5етиніл-6-метилпіридин-2-іламіна, 213 мг (1,1 моля) CuI, 1,57 г (2,2 моля) біс-(трифенілфосфін) паладій (II) хлориду, 15 мл (112 моль) триетиламіну у 100 мл ДМЕ. Реакційну суміш перемішують при КТ протягом ночі. Після видалення розчинника при зниженому тиску залишок переносять у воду і етилацетат і водну фазу двічі екстрагують етилацетатом. Об'єднані органічні фази сушать над MgSO4, фільтрують через діоксид кремнію і розчинник видаляють при зниженому тиску. Вихід: 2,9 г (64 %). A-45) [5-(4-Хлор-6-етилпіримідин-5-ілетиніл)-піридин-2-іл]-метиламін H N N N 15 20 Cl N Шукану сполуку синтезують за загальною методикою GP2 з використанням в якості вихідної речовини 0,89 г (2,6 моля) 4-хлор-6-етил-5-йодпіримідина і з використанням 0,48 г (3,65 моля) (5-етинілпіридин-2-іл)-метиламіна, 40 мг (0,21 моля) CuI, 180 мг (0,26 моля) біс(трифенілфосфін) паладій (II) хлориду, 3,6 мл (26,1 моля) триетиламіну у 5,5 мл ТГФ. Реакційну суміш перемішують при 65 °C протягом ночі. Після видалення розчинника при зниженому тиску залишок переносять у воду і етилацетат і водну фазу двічі екстрагують етилацетатом. Об'єднані органічні фази сушать над MgSO4, фільтрують через діоксид кремнію і розчинник видаляють при зниженому тиску. Вихід: 320 мг (46 %). A-46) [5-(4-Хлор-6-етилпіримідин-5-ілетиніл)-піридин-2-іл]-етиламін H N N N 25 Cl N Шукану сполуку синтезують за загальною методикою GP2 з використанням в якості вихідної речовини 4-хлор-6-етил-5-йодпіримідина і з використанням (5-етинілпіридин-2-іл) етиламіну (A28), CuI, біс-(трифенілфосфін) паладій (II) хлориду, триетиламіну у ТГФ. Після обробки отримують шукане з'єднання з хорошим виходом і прийнятною чистотою. H2) 4-Бром-2,6-дифторбензойна кислота F F O ДАЛ, CO2, ТГФ Br 30 35 F OH Br H1 F H2 До розчину діізопропіламіна (32 г, 0,31 моля) у ТГФ (170 мл) по краплях додають n-BuLi (116 мл, 0,30 моля), підтримуючи внутрішню температуру нижче -65 °C. Суміш перемішують при -50 °C протягом 1 год і отримують розчин ДАВ. До розчину сполуки H1 (50 г, 0,26 моля) у ТГФ (170 мл) додають ДАВ, підтримуючи внутрішню температуру нижче -65 °C, потім перемішують протягом 1,5 год і при -65 °C через суміш пропускають CO2, потім 1 н. розчином HCl значення 20 UA 110471 C2 pH доводять до 2 ~ 3 і суміш екстрагують за допомогою EtOAc (3 500 мл). Органічний шар сушать над Na2SO4, концентрують у вакуумі і отримують сполуку H2 (39,0 г, 63,4 %). H3) Метиловий ефір 4-бром-2,6-дифторбензойної кислоти F O F OH Br 10 15 20 H2SO4, MeOH O Br F F H3 H2 5 До суспензії сполуки H2 (52,5 г, 0,23 моля) у MeOH (320 мл) повільно додають H 2SO4 (98 %). Реакційну суміш кип'ятять із зворотним холодильником до тих пір, поки ТШХ не показує, що вихідна речовина повністю витрачена. Розчинник видаляють і отриманий залишок піддають розподілу між NaHCO3 і EtOAc. Органічний шар сушать над безводним Na 2SO4 і концентрують у вакуумі і отримують продукт H3 (50,0 г, 90,0 %). A-47) Метиловий ефір 2,6-дифтор-4-(4,4,5,5-тетраметил-[1,3,2]діоксаборолан-2-іл)-бензойної кислоти Суспензію сполуки H3 (50,0 г, 0,20 моля), біс (пінаколято) дібора (53,3 г, 0,21 моля), Pd(dppf)Cl2 (15,0 г, 0,02 моля) i KOAc (61,5 г, 0,6 моля) в діоксані (400 мл) швидко нагрівають до 70 °C і витримують протягом 2 год. Діоксан випарюють у вакуумі і отриманий залишок промивають за допомогою ПЕ. Зібраний органічний розчин концентрують у вакуумі. Неочищений продукт кристалізують з ПЕ і отримують сполуку A-47 (52,76 г, 89,0 %). H5) 4-Бром-2-хлор-6-фторбензойна кислота F F O ДАЛ, CO2, ТГФ Br Cl 30 OH Br H4 25 O Cl H5 До розчину діізопропіламіна (2,4 г, 24 моля) у ТГФ (40 мл) при -78 °C по краплях додають nBuLi (8,8 мл, 22 моля). Суміш перемішують при -78 °C протягом 1 год і потім їй дають нагрітися до 0 °C. Отриманий розчин при -78 °C переносять у розчин сполуки H4 (4,16 г, 20 моль) у ТГФ (60 мл) i перемішують протягом 1 год. Потім через розчин пропускають сухий CO 2 протягом ще 1 год. Реакцію зупиняють 1 н. розчином HCl (50 мл) при 0 °C і отриманий розчин екстрагують за допомогою EtOAc (2 50 мл). Органічні шари промивають насиченим водним розчином NaHCO3 і розсолом, сушать і концентрують, і отримують неочищений продукт H5 (ізомер, 5 г, неочищений) у вигляді коричневого масла, яке безпосередньо використовують на наступній стадії. H6) Метиловий ефір 4-бром-2-хлор-6-фторбензойної кислоти 21 UA 110471 C2 F O F O MeI, ДМФ, Na CO3 2 O OH Br Br Cl H6 H5 5 10 Cl До суміші сполуки H5 (20 г, 80 моль) i K2CO3 (13,2 г, 96 моль) у ДМФ (200 мл) додають метилйодид (23 г, 160 моль). Суміш перемішують при температурі навколишнього середовища протягом 2 год., виливають у воду (600 мл) i екстрагують за допомогою ДХМ (2 200 мл). Об'єднані органічні шари промивають водою, розсолом, сушать і концентрують при зниженому тиску і отримують коричневе масло, яке очищають за допомогою хроматографії на силікагелі (ПЕ: EtOAc = 100:1), і отримують сполуку H6 (ізомер, 8 г, 49 % за 2 стадії) у вигляді світложовтого масла. A-48) Метиловий ефір 2-хлор 6-фтор-4-(4,4,5,5-тетраметил-[1,3,2]діоксаборолан-2-іл)бензойної кислоти F F O O B B O O O O O O Br O Cl O Pd(dppf)Cl , KOAc, диоксан 2 Cl B H6 15 20 Суміш сполуки H6 (18 г, 68 моль), біс (пінаколято) дібора (17,3 г, 68 моль), Pd(dppf)Cl 2 (2,5 г, 3,4 моля) i KOAc (20 г, 0,2 моля) в діоксані (300 мл) нагрівають при 80 °C протягом 2 год і концентрують досуха при зниженому тиску. Отриманий залишок очищають за допомогою хроматографії на силікагелі (ПЕ: EtOAc = 150:1) i отримують неочищений продукт у вигляді прозорого масла, яке потім перекристалізовують з гексану, і отримують сполуку A-48 (5,5 г, 35,7 %) у вигляді білої твердої речовини. H8) Метиловий ефір 2,6-дихлорбензойної кислоти Cl Cl O OH Cl CH3I, K2CO3, ДМФ 30 O КТ, 2 ч Cl H8 H7 25 O До розчину сполуки H7 (50 г, 0,26 моля) i K2CO3 (53,8 г, 0,39 моля) у ДМФ (200 мл) додають метилйодид (75,9 г, 0,52 моля). Суміш перемішують при температурі навколишнього середовища протягом 2 год., виливають у воду (500 мл) i екстрагують етилацетатом (2500 мл). Об'єднані ефірні шари промивають водою, розсолом, сушать, фільтрують і концентрують при зниженому тиску і отримують сполуку H8 (45 г, 83 %) у вигляді жовтого масла, Rf = 0,8 (петролейний ефір: етилацетат = 10:1). A-49A) Метиловий ефір 2,6-дихлор-4-(4,4,5,5-тетраметил-[1,3,2]діоксаборолан-2-іл)бензойної кислоти 22 UA 110471 C2 5 10 Біс (пінаколято) дибор [Pin2B2] (44,8 г, 176 моль), 4,4'-ді-трет-бутил-[2,2']біпіридиніл (120 мг, 0,44 моля) i [Ir(COD)(OMe)]2 (147 мг, 0,22 моля) додають до розчину сполуки H8 (45 г, 0,22 моля) у гептані (500 мл). Жовта реакційна суміш протягом першої хвилини стає трав'янисто-зеленою і потім цегляно-червоною. Реакційну суміш кип'ятять із зворотним холодильником протягом 18 год і потім піддають розподілу між етилацетатом і водою. Органічні екстракти об'єднують, сушать над Na2SO4 і концентрують при зниженому тиску. Твердий залишок очищають за допомогою хроматографії на силікагелі (ПЕ: EtOAc = 50:1, детектування за допомогою індикатора бору) i отримують шукане сполуку (A-49A) у вигляді білої твердої речовини (41,0 г, 53 %). Rf = 0,4 (петролейний ефір: етилацетат = 20:1). H10) Метиловий ефір 4-бром-2-трифторметилбензойної кислоти 15 20 Розчин сполуки H9 (25,0 г, 94 моля) у суміші HCl-MeOH (250 мл) кип'ятять із зворотним холодильником протягом ночі. ТШХ показує, що вихідна речовина повністю витрачена. MeOH випарюють у вакуумі. Отриманий залишок піддають розподілу між насиченим розчином NaHCO 3 і EtOAc. Органічний шар сушать над безводним Na2SO4 і концентрують у вакуумі і отримують продукт H10 (23,5 г; 90,0 %). A-49B) Метиловий ефір 2-трифторметил-4-(4,4,5,5-тетраметил-[1,3,2]діоксаборолан-2-ил)бензойної кислоти 25 23 UA 110471 C2 5 Суспензію сполуки H10 (23,5 г, 83,3 моля), біс (пінаколято) дибору (21 г, 83,3 моля), Pd(dppf)Cl2 (6 г, 8,3 моля) i KOAc (24 г, 25 моль) у ДМФ (400 мл) швидко нагрівають до 80 °C і витримують протягом 2 год. Розчинник випарюють у вакуумі. Отриманий залишок розчиняють у ПЕ, фільтрують і фільтрат збирають. Отриманий фільтрат концентрують у вакуумі і отримують неочищений продукт, який кристалізують з петролейного ефіру і отримують сполуку A-49B (10,8 г; 40 %). H12) Метиловий ефір 4-бром-2-трифторметоксибензойної кислоти 10 15 20 25 Суспензію сполуки H11 (30,0 г, 0,11 моля) у суміші 4 M MeOH-HCl (500 мл) кип'ятять із зворотним холодильником протягом ночі. MeOH випарюють у вакуумі. Отриманий залишок піддають розподілу між насиченим розчином Na2CO3 і EtOAc. Органічний шар сушать над безводним Na2SO4 і концентрують у вакуумі і отримують продукт H12 (24,0 г; 77 %). A-49C) Метиловий ефір 2-трифторметокси-4-(4,4,5,5-тетраметил-[1,3,2]діоксаборолан-2-іл)бензойної кислоти Суспензію сполуки H12 (24 г, 0,08 моля), біс (пінаколято) дибору (20,4 г, 0,08 моля), Pd(dppf)Cl2 (1,0 г) i KOAc (15,68 г, 0,16 моля) в діоксані (400 мл) швидко нагрівають до 80 °C і витримують протягом 2 год. Розчинник випарюють у вакуумі і отриманий залишок розчиняють у петролейному ефірі, фільтрують і фільтрат збирають. Отриманий фільтрат концентрують у вакуумі і отримують неочищений продукт, який кристалізують з петролейного ефіру і отримують сполуку A-49C (15,0 г; 63,2 %). A-50) Метиловий ефір 4-[5-(6-аміно-2-метилпіридин-3-ілетиніл)-6-етилпіримідин-4-іл]-2фторбензойної кислоти NH2 N N F N O O 30 Шукану сполуку синтезують за методикою, аналогічною загальною методикою GP4, з використанням в якості вихідної речовини 3,9 г (14,3 моля) і з використанням 3,7 г (18,6 моля) 3фтор-4-метоксикарбонілфенілборонової кислоти, 502 г (0,71 моля) біс-(трифенілфосфін) паладій (II) хлориду, 10,7 мл (21,5 моля) 2 M водного розчину Cs 2CO3 і 10 мл EtOH у 100 мл 24 UA 110471 C2 5 ДМЕ. Реакційну суміш перемішують при 80 °C протягом ночі. Реакційну суміш фільтрують через целіт і розчинник видаляють при зниженому тиску. Неочищений продукт розтирають з водою і етилацетатом. Фази розділяють і водну фазу двічі екстрагують етилацетатом. Об'єднані органічні шари сушать над Mg2SO4 і розчинник випарюють при зниженому тиску. Неочищена речовину перемішують з циклогексаном і відфільтровують. Після сушіння одержують 4,0 г (72 %) шуканого продукту у вигляді твердої речовини, яку використовують на наступній стадії без додаткового очищення. A-51) 4-[5-(6-Аміно-2-метилпіридин-3-ілетиніл)-6-етилпіримідин-4-іл]-2-фторбензойна кислота 10 NH2 N N F N O 15 OH Шукану сполуку синтезують за загальною методикою GP8 з використанням в якості вихідної речовини 4,0 г (10,3 моля) метилового ефіру кислоти і з використанням 1,29 г (30,7 моля) LiOH у 40 мл води і 200 мл ТГФ. Реакційну суміш перемішують при 50 °C протягом ночі. Розчинник видаляють при зниженому тиску і залишок переносять у воду. Додають 1 M водний розчин HCl до встановлення pH 5. Осаджений продукт відфільтровують і промивають за допомогою АЦН. Після сушіння одержують 1,3 г (32 %) шуканого продукту у вигляді твердої речовини. A-52) 5-[5-(6-Амінопіридин-3-ілетиніл)-6-етилпіримідин-4-іл]-піридин-2-карбонова кислота NH2 N N N N O 20 25 30 OH Шукану сполуку синтезують за методикою, аналогічною загальною методикою GP4, з використанням в якості вихідної речовини 1,2 г (4,63 моля) 4-хлор-6-етил-5-(6-амінопіридин-3ілетиніл)-піримідину і з використанням 1,0 г (5,6 моля) 4-метоксікарбоніл-3-піридилборонової кислоти, 163 мг (0,23 моля) біс-(трифенілфосфін) паладій (II) хлориду, 7,0 мл (13,9 моля) 2 M водного розчину Cs2CO3 і 2 мл MeOH у 10 мл ДМЕ. Реакційну суміш перемішують при 80 °C протягом ночі. Реакційну суміш виливають у воду і промивають за допомогою ДХМ. До водної фази додають 1 M водний розчин HCl до встановлення pH 5. Осаджений продукт відфільтровують і промивають водою і метанолом. Після сушіння одержують 290 мг (13 %) шуканого продукту у вигляді твердої речовини, яку використовують на наступній стадії без додаткового очищення. A-72) Метиловий ефір 4-[5-(6-амінопіридин-3-ілетиніл)-6-етилпіримідин-4-іл]-2фторбензойної кислоти NH2 N N F N O O 25 UA 110471 C2 5 10 Шукану сполуку синтезують за методикою, аналогічною загальною методикою GP4, з використанням в якості вихідної речовини 15 г (58,06 моля) 4-хлор-6-етил-5-(6-амінопіридин-3ілетиніл)-піримідину і з використанням 13,8 г (69,6 моля) 3-фтор-4метоксикарбонілфенілборонової кислоти, 1,51 г (2,15 моля) біс-(трифенілфосфін) паладій (II) хлориду, 43,5 мл (87,0 моля) 2 M водного розчину Cs 2CO3 і 20 мл EtOH у 200 мл ДМЕ. Реакційну суміш перемішують при 80 °C протягом ночі. Реакційну суміш фільтрують через целіт і розчинник видаляють при зниженому тиску. Неочищений продукт розтирають з водою і обробляють ультразвуком протягом 30 хв. Осаджений продукт відфільтровують, промивають за допомогою АЦН і невеликою кількістю MeOH. Після сушіння одержують 14,8 г (68 %) шуканого продукту у вигляді твердої речовини. A-73) 4-[5-(6-Амінопіридин-3-ілетиніл)-6-етилпіримідин-4-іл]-2-фторбензойна кислота NH2 N N F N O OH 15 20 Шукану сполуку синтезують за загальною методикою GP8 з використанням в якості вихідної речовини 17,8 г (47,3 моля) метилового ефіру кислоти і з використанням 3,97 г (94,6 моля) LiOH у 30 мл води і 300 мл ТГФ. Реакційну суміш перемішують при КТ протягом ночі. Розчинник видаляють при зниженому тиску і залишок переносять у воду. Додають 1 M водний розчин HCl до встановлення pH 5. Осаджений продукт відфільтровують і промивають за допомогою АЦН. Після сушіння одержують 17,1 г (85 %) шуканого продукту у вигляді твердої речовини. A-74) Метиловий ефір 4-[5-(6-амінопіридин-3-ілетиніл)-6-етилпіримідин-4-іл]-бензойної кислоти NH2 N N N O O 25 30 Шукану сполуку синтезують за загальною методикою GP4 з використанням в якості вихідної речовини 2,0 г (7,73 моля) 4-хлор-6-етил-5-(6-амінопіридин-3-ілетиніл)-піримідину і з використанням 2,1 г (11,6 моля) 4-метоксикарбонілфенілборонової кислоти, 271,3 мг (0,39 моля) біс-(трифенілфосфін) паладій (II) хлориду, 5,7 мл (11,5 моля) 2 M водного розчину Cs 2CO3 і 2 мл EtOH у 5 мл ДМЕ. Реакційну суміш перемішують в мікрохвильовій печі при 130 °C протягом 1 год Реакційну суміш суспендують у MeOH і осаджений продукт відфільтровують і промивають за допомогою MeOH. Після сушіння одержують 2,25 г (81 %) шуканого продукту у вигляді твердої речовини. A-75) 4-[5-(6-Амінопіридин-3-ілетиніл)-6-етилпіримідин-4-іл]-бензойна кислота NH2 N N N O OH 26 UA 110471 C2 5 Шукану сполуку синтезують за загальною методикою GP8 з використанням в якості вихідної речовини 2,25 г (6,28 моля) метилового ефіру кислоти і з використанням 1,32 г (31,4 моля) LiOH у 5 мл води і 50 мл ТГФ. Реакційну суміш перемішують при 50 °C протягом ночі. Розчинник видаляють при зниженому тиску і залишок переносять у воду. Додають 1 M водний розчин HCl до встановлення pH 5. Осаджений продукт відфільтровують і переносять у воду. Після сушіння виморожуванням отримують 2,3 г неочищеного продукту, який використовують на наступній стадії без додаткового очищення. A-76) Метиловий ефір 4-[5-(6-амінопіридин-3-ілетиніл)-6-етилпіримідин-4-іл]-2хлорбензойної кислоти 10 NH2 N N Cl N O O 15 20 Шукану сполуку синтезують за загальною методикою GP4 з використанням в якості вихідної речовини 4,0 г (15,5 моля) 4-хлор-6-етил-5-(6-амінопіридин-3-ілетиніл)-піримідину і з використанням 4,3 г (20,1 моля) 3-хлор-4-метоксикарбонілфенілборонової кислоти, 543 мг (0,77 моля) біс-(трифенілфосфін) паладій (II) хлориду, 11,6 мл (23,2 моля) 2 M водного розчину Cs2CO3 і 10 мл EtOH у 100 мл ДМЕ. Реакційну суміш перемішують при 80 °C протягом ночі. Розчинник видаляють при зниженому тиску і залишок переносять у воду і етилацетат. Водну фазу двічі екстрагують етилацетатом. Об'єднані органічні шари сушать над MgSO 4, фільтрують через целіт і розчинник видаляють при зниженому тиску. Після сушіння одержують 3,3 г (54 %) шуканого продукту. A-77) 4-[5-(6-Амінопіридин-3-ілетиніл)-6-етилпіримідин-4-іл]-2-хлорбензойна кислота NH2 N N Cl N O 25 30 OH Шукану сполуку синтезують за загальною методикою GP8 з використанням в якості вихідної речовини 3,3 г (8,4 моля) метилового ефіру кислоти і з використанням 1,06 г (25,2 моля) LiOH у 20 мл води і 100 мл ТГФ. Реакційну суміш перемішують при 50 °C протягом ночі. Розчинник видаляють при зниженому тиску і залишок переносять у воду. Додають 1 M водний розчин HCl до встановлення pH 5-6. Осаджений продукт відфільтровують і промивають водою і MeOH. Після сушіння одержують 2,5 г (89 %) шуканого продукту у вигляді твердої речовини. A-78) Метиловий ефір 4-[5-(6-амінопіридин-3-ілетиніл)-6-метилпіримідин-4-іл]бензойної кислоти NH2 N N N O O 27 UA 110471 C2 5 Шукану сполуку синтезують за загальною методикою GP4 з використанням в якості вихідної речовини 2,0 г (8,2 моля) 4-хлор-6-метил-5-(6-амінопіридин-3-ілетиніл)-піримідину і з використанням 2,2 г (12,3 моля) 4-метоксикарбонілфенілборонової кислоти, 240 мг (1,5 моля) 287 мг (0,41 моля) біс-(трифенілфосфін) паладій (II) хлориду, 6,1 мл (12,3 моля) 2 M водного розчину Cs2CO3 і 2 мл EtOH у 5 мл ДМЕ. Реакційну суміш перемішують в мікрохвильовій печі при 130 °C протягом 1 год. Реакційну суміш суспендують у MeOH і осаджений продукт відфільтровують і промивають за допомогою MeOH. Після сушіння одержують 2,2 г (77 %) шуканого продукту у вигляді твердої речовини. A-79) 4-[5-(6-Амінопіридин-3-ілетиніл)-6-метилпіримідин-4-іл]-бензойна кислота NH2 N N N O 10 15 OH Шукану сполуку синтезують за загальною методикою GP8 з використанням в якості вихідної речовини 2,2 г (6,3 моля) метилового ефіру кислоти і з використанням 1,33 г (31,6 моля) LiOH у 5 мл води і 50 мл ТГФ. Реакційну суміш перемішують при 50 °C протягом ночі. Розчинник видаляють при зниженому тиску і залишок переносять у воду. Додають 1 M водний розчин HCl до встановлення pH 5. Осаджений продукт відфільтровують і переносять у воду. Після сушіння виморожуванням отримують 2,7 г неочищеного продукту, який використовують на наступній стадії без додаткового очищення. A-80) Метиловий ефір 4-[5-(6-амінопіридин-3-ілетиніл)-6-метилпіримідин-4-іл]-2хлорбензойної кислоти NH2 N N Cl N O 20 25 30 O Шукану сполуку синтезують за загальною методикою GP4 з використанням в якості вихідної речовини 10 г (40,9 моля) 4-хлор-6-метил-5-(6-амінопіридин-3-ілетиніл)-піримідину і з використанням 10,5 г (49,0 моля) 2-хлор-4-метоксикарбонілфенілборонової кислоти, 1,43 г (2,04 моля) біс-(трифенілфосфін) паладій (II) хлориду, 61,3 мл (122 моля) 2 M водного розчину Cs2CO3 і 50 мл EtOH у 500 мл ДМЕ. Реакційну суміш перемішують при 80 °C протягом 3 год. Реакційну суміш фільтрують через целіт і розчинник видаляють при зниженому тиску. Додають воду і осаджений продукт відфільтровують і промивають за допомогою АЦН і MeOH. Після сушіння одержують 13,8 г неочищеного продукту, який використовують на наступній стадії без додаткового очищення. A-81) 4-[5-(6-Амінопіридин-3-ілетиніл)-6-метилпіримідин-4-іл]-2-хлорбензойна кислота NH2 N N Cl N O O Шукану сполуку синтезують за загальною методикою GP8 з використанням в якості вихідної речовини 13,8 г (36,4 моля) метилового ефіру кислоти і з використанням 7,64 г (182 моля) LiOH у 200 мл води і 400 мл ТГФ. Реакційну суміш перемішують при 50 °C протягом ночі. Розчинник 28
ДивитисяДодаткова інформація
Назва патенту англійською5-alkynyl-pyrimidines
Автори англійськоюSchneider, Siegfried, Kessler, Dirk, van der Veen, Lars, Wunberg, Tobias
Автори російськоюШнайдер Зигфрид, Кесслер Дирк, ван дер Вен Ларс, Вунберг Тобиас
МПК / Мітки
МПК: C07D 401/06, C07D 401/14, C07D 471/04, C07D 239/26, A61K 31/506, C07D 413/14, C07D 409/14, A61P 35/00, A61K 31/606, C07D 405/14, C07D 487/08
Мітки: 5-алкінілпіримідини
Код посилання
<a href="https://ua.patents.su/232-110471-5-alkinilpirimidini.html" target="_blank" rel="follow" title="База патентів України">5-алкінілпіримідини</a>
Попередній патент: Антидот антикоагулянта
Випадковий патент: Спосіб діагностики гострої ниркової недостатності у дітей при тяжкому сепсисі та септичному шоку












