Мікроінкапсульовані інсектицидні композиції
Формула / Реферат
1. Пестицидна композиція, яка містить:
фосфорорганічний пестицид; і
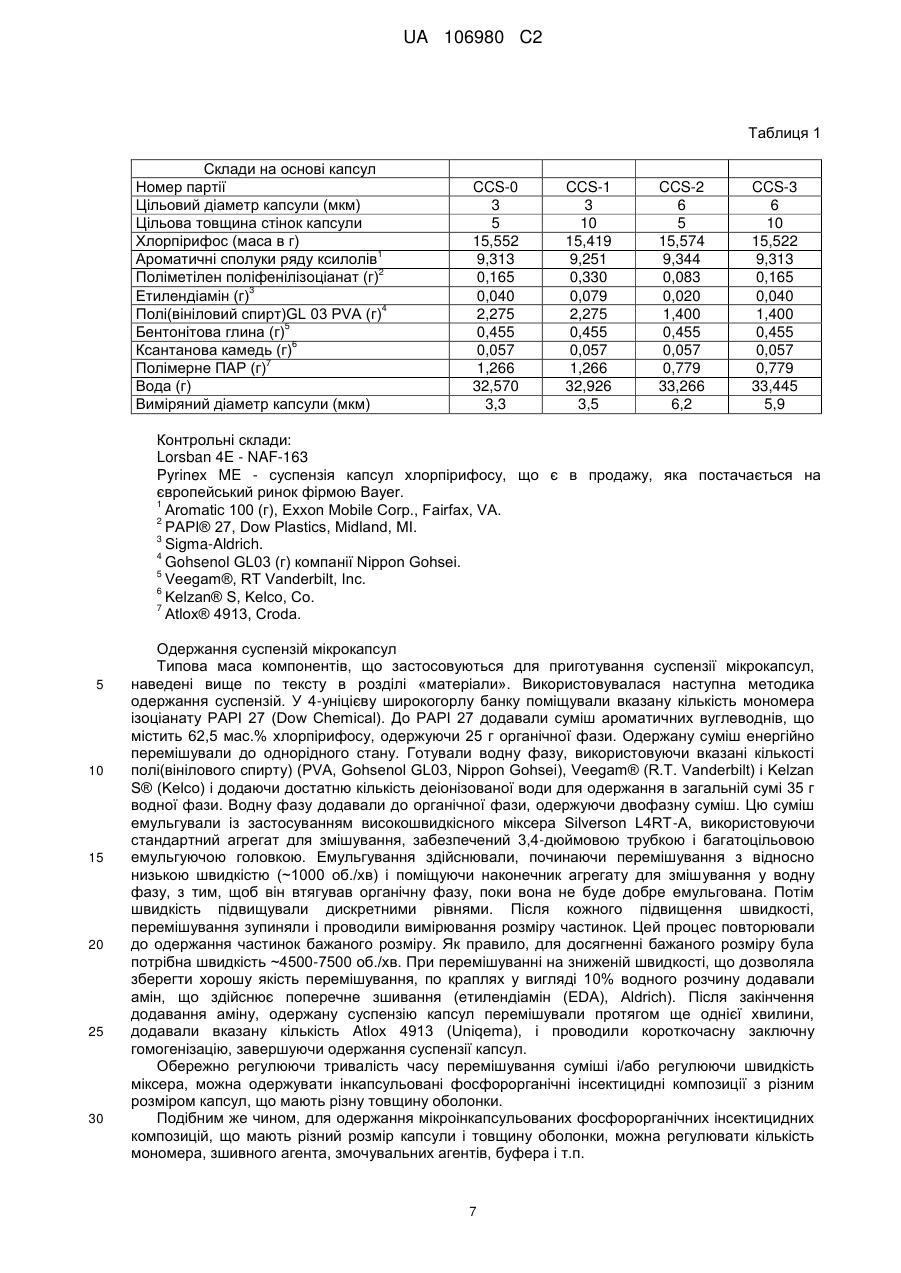
полімер, який утворює стінку капсули, яка щонайменше частково інкапсулює фосфорорганічний пестицид, утворюючи мікрокапсулу, де стінка має середню товщину від приблизно 5 нм до приблизно 25 нм, де вказана мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон,
де фосфорорганічний пестицид являє собою хлорпірифос, і
мікрокапсула містить від приблизно 15 мас. % до приблизно 35 мас. % хлорпірифосу,
де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення.
2. Пестицидна композиція за п. 1, де стінка капсули має середню товщину від приблизно 8 нм до приблизно 12 нм, де вказана мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення.
3. Пестицидна композиція за п. 1, де стінка капсули утворена міжфазною поліконденсацією:
щонайменше одного маслорозчинного мономера, вибраного з групи, яка складається з: діізоціанатів, поліізоціанатів, хлорангідридів двоосновних кислот, хлорангідридів багатоосновних кислот, сульфонілхлоридів і хлорформіатів; і
щонайменше одного водорозчинного мономера, вибраного з групи, яка складається з: діамінів, поліамінів, водорозчинних діолів і водорозчинних поліолів.
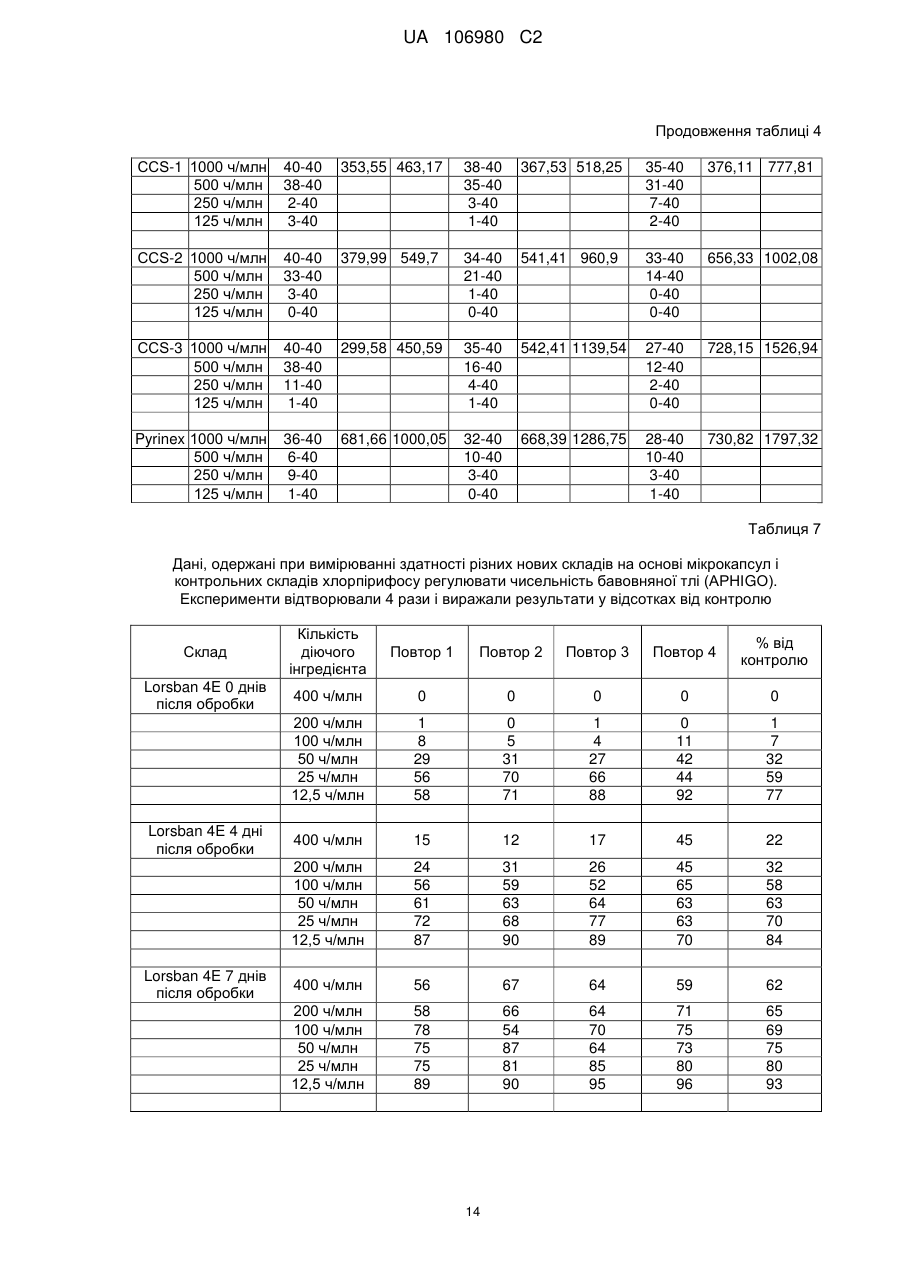
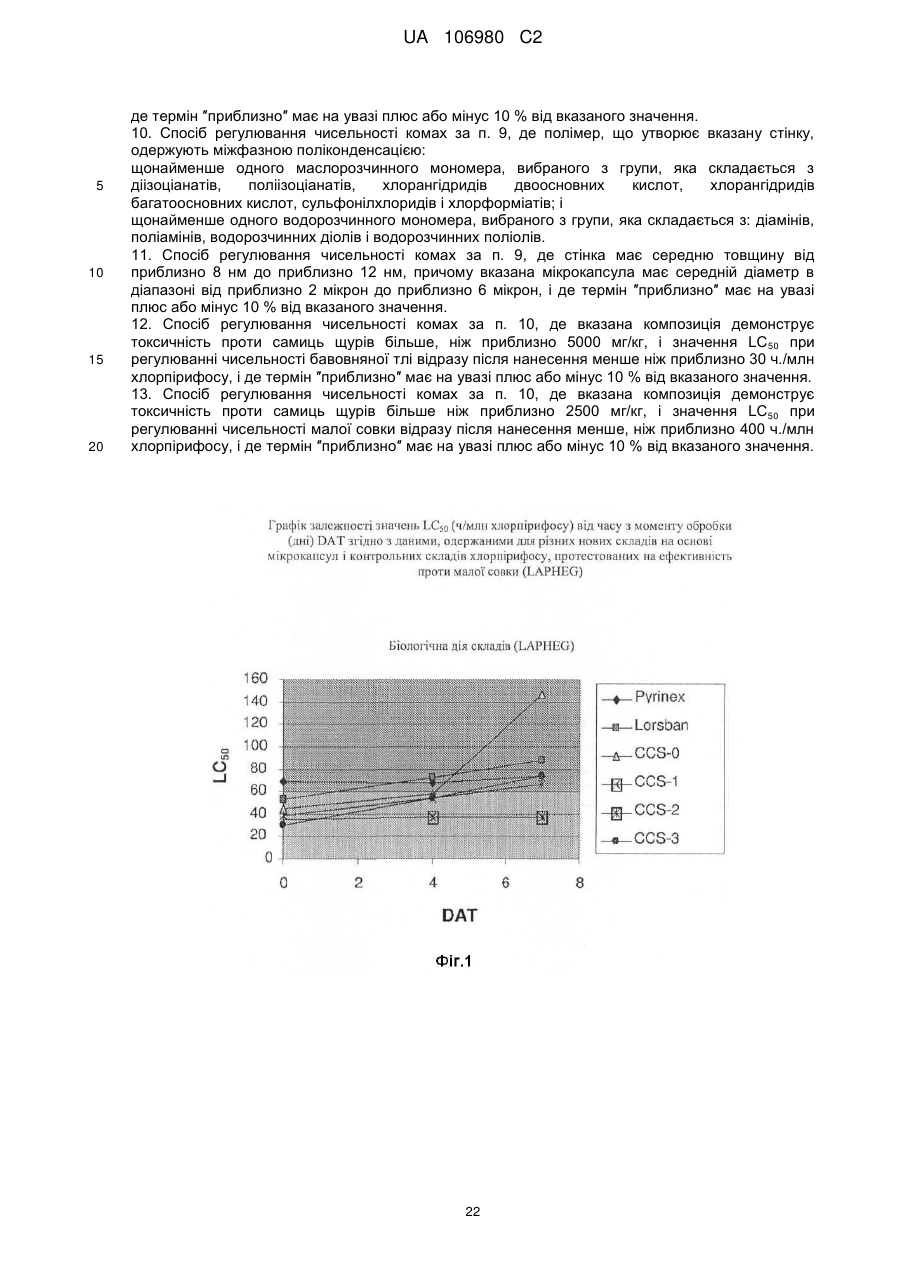
4. Пестицидна композиція за п. 3, де вказана композиція демонструє токсичність проти самиць щурів більше ніж приблизно 5000 мг/кг, і LC50 при регулюванні чисельності бавовняної тлі відразу після внесення менше ніж приблизно 30 ч./млн. хлорпірифосу, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення.
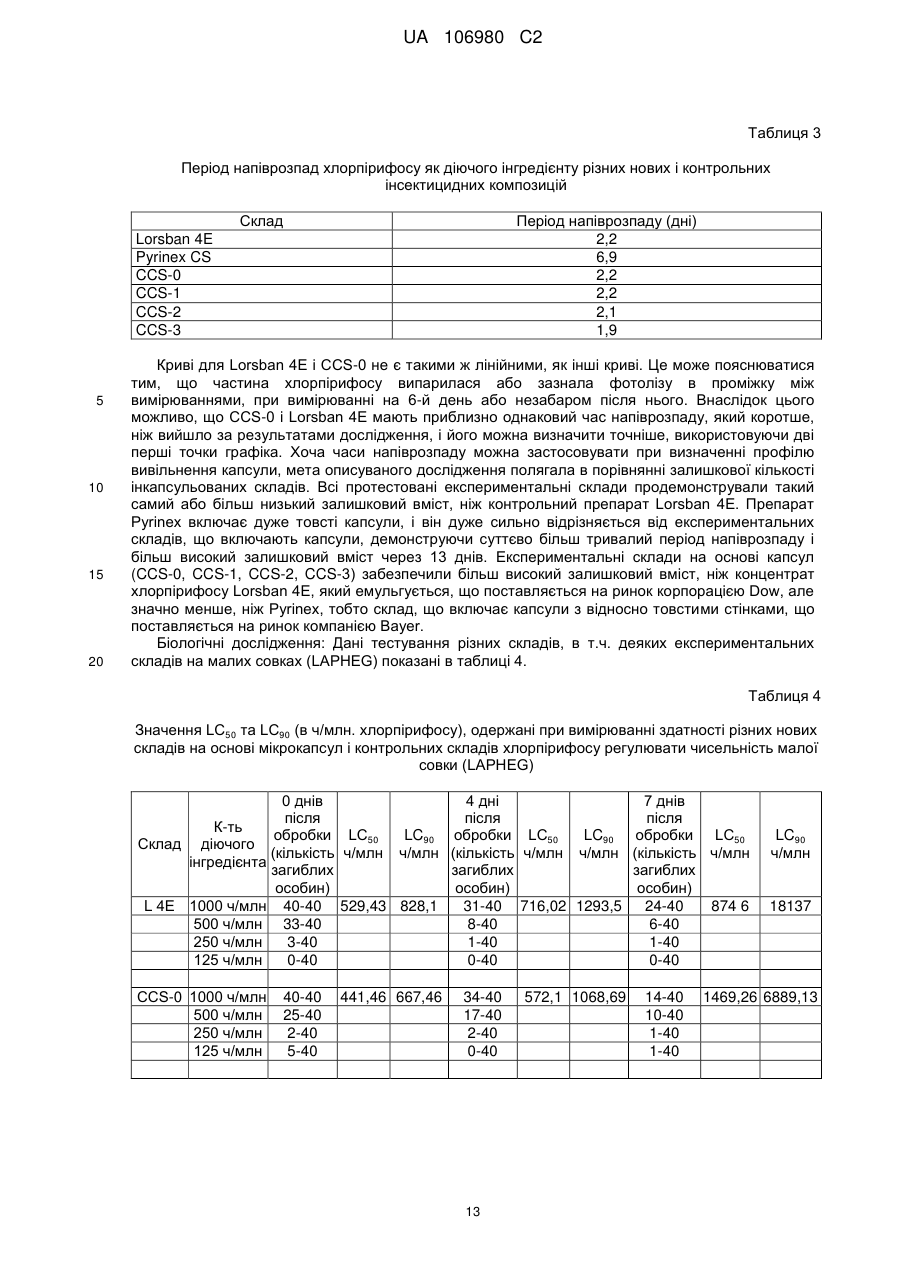
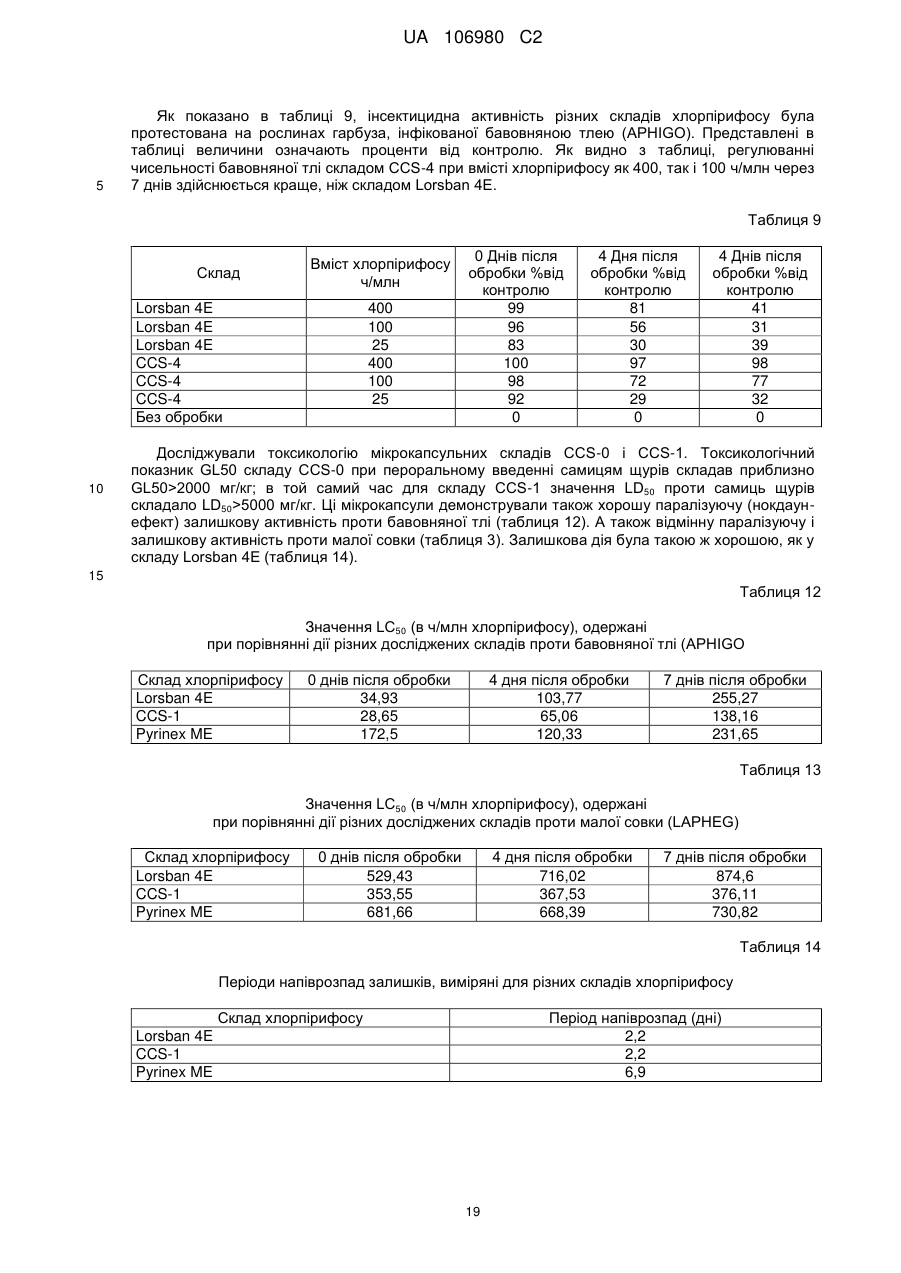
5. Пестицидна композиція за п. 3, де вказана композиція демонструє токсичність проти самиць щурів більше, ніж приблизно 2500 мг/кг, і LC50 при регулюванні чисельності малої совки відразу після внесення менше ніж приблизно 400 ч./млн. хлорпірифосу, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення.
6. Спосіб одержання мікрокапсул, що включає стадії:
одержання фосфорорганічного інсектициду і щонайменше одного мономера;
змішування фосфорорганічного інсектициду і щонайменше одного мономера; і
формування мікрокапсул, де мономер утворює полімер, з якого формується стінка, причому ця стінка щонайменше частково оточує порцію інсектициду, утворюючи вказану мікрокапсулу, де стінка має середню товщину від приблизно 5 нм до приблизно 25 нм, і вказана мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон,
де фосфорорганічний пестицид являє собою хлорпірифос, і
мікрокапсула містить від приблизно 15 мас. % до приблизно 35 мас. % хлорпірифосу,
де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення.
7. Спосіб одержання мікрокапсул за п. 6, де полімер одержують міжфазною поліконденсацією щонайменше одного маслорозчинного мономера, вибраного з групи, яка складається з діізоціанатів, поліізоціанатів, хлорангідридів двоосновних кислот, хлорангідридів багатоосновних кислот, сульфонілхлоридів і хлорформіатів; і
щонайменше одного водорозчинного мономера, вибраного з групи, яка складається з: діамінів, поліамінів, водорозчинних діолів і водорозчинних поліолів.
8. Спосіб одержання мікрокапсул за п. 7, де стінка капсули має середню товщину від приблизно 8 нм до приблизно 12 нм, причому вказана мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення.
9. Спосіб регулювання чисельності комах, що включає стадії: одержання інсектицидної композиції, що складається з мікрокапсул, де мікрокапсули містять:
фосфорорганічний інсектицид; і
полімер, де полімер утворює стінку, яка щонайменше частково інкапсулює фосфорорганічний пестицид з утворенням мікрокапсули, причому стінка має середню товщину від приблизно 5 нм до приблизно 25 нм, і середній діаметр вказаної мікрокапсули знаходиться в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон; і
нанесення вказаного інкапсульованого інсектициду на популяцію комах або на ділянку, розташовану в безпосередній близькості від популяції комах,
де фосфорорганічний пестицид являє собою хлорпірифос, і
мікрокапсула містить від приблизно 15 мас. % до приблизно 35 мас. % хлорпірифосу,
де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення.
10. Спосіб регулювання чисельності комах за п. 9, де полімер, що утворює вказану стінку, одержують міжфазною поліконденсацією:
щонайменше одного маслорозчинного мономера, вибраного з групи, яка складається з діізоціанатів, поліізоціанатів, хлорангідридів двоосновних кислот, хлорангідридів багатоосновних кислот, сульфонілхлоридів і хлорформіатів; і
щонайменше одного водорозчинного мономера, вибраного з групи, яка складається з: діамінів, поліамінів, водорозчинних діолів і водорозчинних поліолів.
11. Спосіб регулювання чисельності комах за п. 9, де стінка має середню товщину від приблизно 8 нм до приблизно 12 нм, причому вказана мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення.
12. Спосіб регулювання чисельності комах за п. 10, де вказана композиція демонструє токсичність проти самиць щурів більше, ніж приблизно 5000 мг/кг, і значення LC50 при регулюванні чисельності бавовняної тлі відразу після нанесення менше ніж приблизно 30 ч./млн. хлорпірифосу, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення.
13. Спосіб регулювання чисельності комах за п. 10, де вказана композиція демонструє токсичність проти самиць щурів більше ніж приблизно 2500 мг/кг, і значення LC50 при регулюванні чисельності малої совки відразу після нанесення менше, ніж приблизно 400 ч./млн. хлорпірифосу, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення.
Текст
Реферат: У винаході розроблені різні мікроінкапсульовані інсектицидні композиції, призначені для регулювання чисельності шкідників, наприклад тлі і малої совки. Ці композиції демонструють відмінну паралізуючу дію (нокдаун-ефект) проти як гризучих, так і не гризучих шкідників, причому значення токсичності проти самиць щурів LD50 знаходяться в діапазоні приблизно 2500 мг/кг. Деякі з цих композицій включають стінки з полімеру, одержаного, наприклад, при міжфазній поліконденсації водорозчинного мономера і нерозчинного у воді мономера, яка щонайменше частково оточує фосфорорганічний інсектицид. У деяких аспектах винаходу фосфорорганічна сполука, що знаходиться в мікрокапсулі, являє собою хлорпірифос. Діаметр мікрокапсули знаходиться в діапазоні від приблизно 2 до приблизно 25 мікрон, і товщина стінки складає від приблизно 5 до приблизно 25 нанометрів. UA 106980 C2 (12) UA 106980 C2 UA 106980 C2 5 10 15 20 25 30 35 40 45 50 55 60 Перехресні посилання на споріднені заявки Дана заявка претендує на пріоритет попередньої заявки на патент США з порядковим номером 61/157339, поданої 4 березня 2009 року, яка безпосередньо включена в дану заявку за допомогою посилання. Галузь техніки, якої стосується винахід Різні аспекти і варіанти здійснення даного винаходу в основному належать до композицій мікроінкапсульованих пестицидів, які мають корисні біологічні, комерційні і/або екологічні властивості. Передумови винаходу Регулювання чисельності комах відіграє важливу роль в сучасному сільському господарстві, зберіганні харчових продуктів і гігієні. У даний час значну роль в регулюванні чисельності комах грають інкапсульовані інсектицидні композиції, які є безпечними і ефективними. Властивості інкапсульованих інсектицидних композицій, що застосовуються, включають високу початкову токсичність проти цільових шкідників, легкість застосування, стабільність, низьку токсичність проти інших тварин в районі 2500 мг/кг і значний час дії на навколишнє середовище. Вважалося, що деякі з цих властивостей знаходяться в суперечності одна з одною, і розробка інсектицидних композицій, що застосовуються, часто включає створення складів з характеристиками, які відображають баланс між цими властивостями. Приймаючи до уваги велику користь і значущість інкапсульованих інсектицидів, існує насущна і постійна потреба в нових інсектицидних композиціях, які демонструють сприятливі фізичні, хімічні, біологічні і екологічні властивості. Різні аспекти і варіанти здійснення винаходу, розкриті в даній заявці, прагнуть задовольнити цю потребу. Суть винаходу Один з аспектів даного винаходу належить до пестицидної композиції, що містить фосфорорганічний пестицид, і полімер; де полімер утворює стінку капсули, яка щонайменше частково інкапсулює фосфорорганічний пестицид, формуючи мікрокапсулу, причому стінка має середню товщину від приблизно 5 нм до приблизно 25 нм, і вказана мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до при приблизно 6 мікрон. В одному з варіантів здійснення стінка мікрокапсули має середню товщину від приблизно 8 нм до приблизно 12 нм, причому вказана мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон. В одному з варіантів здійснення мікрокапсула містить щонайменше один пестицид, вибраний з групи фосфорорганічних пестицидів, а саме з групи, яка включає: ацефат, азинфосметил, хлорфенвінфос, хлоретоксифос, хлорпірифос-метил, діазинон, диметоат, дисульфотон, етопрофос, фенітротіон, фентіон, фенаміфос, фостіазат, малатіон, метамідофос, метидатіон, ометоат, оксидеметон-метил, паратіон, паратіон-метил, форат, фосмет, профенофос і трихлорфон. В іншому варіанті здійснення мікрокапсула включає фосфорорганічний пестицид хлорпірифос. У ще одному варіанті здійснення, мікрокапсула містить щонайменше від приблизно 15 мас.% до приблизно 35 мас.% хлорпірифосу. В одному з варіантів здійснення мікрокапсула формується при міжфазній конденсації, в якій бере участь щонайменше один маслорозчинний мономер, вибраний, наприклад, з групи, яка складається з: діізоціанатів, поліізоціанатів, хлорангідридів двоосновних кислот, хлорангідридів багатоосновних кислот, сульфонілхлоридів і хлорформіатів; і щонайменше один водорозчинний мономер, вибраний з групи, яка складається, наприклад, з: діамінів, поліамінів, водорозчинних діолів і водорозчинних поліолів. В одному з варіантів здійснення, мікрокапсули за даним винаходом демонструють значення токсичності відносно самиць щурів вище, ніж приблизно 5000 мг/кг, і значення LC 50 при регулюванні чисельності бавовняної тлі (APHIGO) відразу після нанесення менше ніж приблизно 30 ч/млн хлорпірифосу. У ще одному варіанті здійснення, мікрокапсули за даним винаходом демонструють значення токсичності відносно самиць щурів вище, ніж приблизно 2500 мг/кг, і значення LC50 при регулюванні чисельності малої совки (LAPHEG) відразу після нанесення менше ніж приблизно 400 ч/млн хлорпірифосу. Інший аспект даного винаходу належить до способу одержання мікрокапсул з інсектицидними властивостями, що включає стадії одержання фосфорорганічного інсектициду і щонайменше одного мономера; змішування фосфорорганічного інсектициду і щонайменше одного мономера; і формування мікрокапсул, причому мономер перетворюється на полімер, а саме полімер, що створює стінку, де ця стінка хоча б частково охоплює порцію інсектициду, формуючи мікрокапсулу, причому стінка має середню товщину від приблизно 5 нм до приблизно 25 нм, і мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон. В одному з варіантів здійснення, полімер, що створює щонайменше 1 UA 106980 C2 5 10 15 20 25 30 35 40 45 50 55 частину стінки мікрокапсули, одержують міжфазною поліконденсацією щонайменше одного маслорозчинного мономера, вибраного з групи, яка включає: діізоціанати, поліізоціанати, хлорангідриди двоосновних кислот, хлорангідриди багатоосновних кислот, сульфонілхлориди і хлорформіати; і щонайменше одного водорозчинного мономера, вибраного з групи, яка включає: діаміни, поліаміни, водорозчинні діоли і водорозчинні поліоли. В одному з варіантів здійснення мікрокапсула з інсектицидними властивостями утворена полімером, який хоча б частково оточує фосфорорганічний інсектицид, наприклад, хлорпірифос. Полімер утворює стінку капсули, яка щонайменше частково оточує порцію хлорпірифосу, причому ця стінка має середню товщину від приблизно 8 нм до приблизно 12 нм, в той час як мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон. В одному з варіантів здійснення мікрокапсула містить не менше приблизно 10 мас.% хлорпірифосу. У ще одному варіанті здійснення полімерна стінка мікрокапсули щонайменше частково оточує щонайменше один фосфорорганічний пестицид, вибраний з групи, яка включає: ацефат, азинфос-метил, хлорфенвінфос, хлоретоксифос, хлорпірифос-метил, діазинон, диметоат, дисульфотон, етопрофос, фенітротіон, фентіон, фенаміфос, фостіазат, малатіон, метамідофос, метидатіон, ометоат, оксидеметон-метил, паратіон, паратіон-метил, форат, фосмет, профенофос, трихлорфон і т.п. Ще один аспект даного винаходу належить до способу регулювання чисельності комах, що включає стадії: одержання частинок інсектицидної композиції, де вказані частинки включають фосфорорганічний інсектицид і полімер, причому полімер утворює стінку капсули, яка хоча б частково інкапсулює фосфорорганічний пестицид з утворенням мікрокапсули, де стінка мікрокапсули має середню товщину від приблизно 5 нм до приблизно 25 нм, і мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон; і нанесення вказаного інкапсульованого інсектициду на поверхню, наприклад, листя, стебла або стовбура рослини. Один з варіантів здійснення даного винаходу являє собою спосіб регулювання чисельності комах, який включає стадії: формування мікрокапсул з інсектицидними властивостями, де мікрокапсула включає стінку, сформовану шляхом міжфазної поліконденсації щонайменше одного маслорозчинного мономера, вибраного з групи, яка складається з діізоціанатів, поліізоціанатів, хлорангідридів двоосновних кислот, хлорангідридів багатоосновних кислот, сульфонілхлоридів і хлорформіатів; і щонайменше одного водорозчинного мономера, вибраного з групи, яка складається з: діамінів, поліамінів, водорозчинних діолів і водорозчинних поліолів; і щонайменше один фосфорорганічний інсектицид, який вибраний з групи, яка складається з: ацефату, азинфос-метилу, хлорфенвінфосу, хлоретоксифосу, хлорпірифосметилу, діазинону, диметоату, дисульфотону, етопрофосу, фенітротіону, фентіону, фенаміфосу, фостіазату, малатіону, метамідофосу, метидатіону, ометоату, оксидеметонметилу, паратіону, паратіон-метилу, форату, фосмету, профенофосу і трихлорфону, де стінка з полімерного компонента щонайменше частково оточує порцію інсектициду з утворенням мікрокапсули. В одному з варіантів здійснення мікрокапсула включає від приблизно 15 мас.% до приблизно 35 мас.% хлорпірифосу. В одному з варіантів здійснення, мікрокапсула, що застосовується для регулювання чисельності комах, має стінку зі середньою товщиною від приблизно 8 нм до приблизно 12 нм, причому середній діаметр вказаної мікрокапсули знаходиться в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон. Ще один варіант здійснення винаходу являє собою мікроінкапсульований фосфорорганічний інсектицид, що застосовується для контролю за чисельністю комах, зі значенням токсичності відносно самиць щурів більше ніж приблизно 5000 мг/кг і LC 50 при регулюванні чисельності комах, наприклад, бавовняної тлі, відразу після нанесення менше ніж приблизно 30 ч/млн хлорпірифосу. У ще одному варіанті здійснення мікрокапсули мають значення токсичності для самиць щурів більше ніж приблизно 2500 мг/кг і LC 50 для регулювання чисельності комах, наприклад, малої совки відразу після нанесення менше ніж приблизно 400 ч/млн хлорпірифосу. Інші відмітні ознаки і переваги даного винаходу будуть викладені нижче по тексту в докладному описі винаходу, і частково вони будуть легко зрозумілі фахівцеві в даній галузі техніки з цього опису або виявлені при практичній реалізації винаходу, описаного в даній заявці, включаючи докладний опис, що іде далі, формулу винаходу, а також прикладені креслення. Потрібно розуміти, що як наведений вище по тексту загальний опис, так і наведений нижче по тексту докладний опис варіантів здійснення даного винаходу, призначені для надання загальних відомостей або основ для розуміння природи і характерних рис заявленого винаходу. Супроводжуючий ілюстративний матеріал включений для більш глибокого розуміння винаходу, входить до складу даного опису і становить його частину. Креслення ілюструють різні варіанти 2 UA 106980 C2 5 10 15 20 25 30 35 40 45 50 55 60 здійснення винаходу і в сукупності з описом служать для пояснення принципів і особливостей втілення даного винаходу. Короткий опис ілюстративного матеріалу На фіг. 1 зображена залежність значень LC50 (в частинах на мільйон ч/млн) хлорпірифосу від DAT (часу в днях після нанесення) для різних інсектицидних композицій при тестуванні їх ефективності проти малої совки (LAPHEG). На фіг. 2 зображена залежність значень LC50 (в ч/млн хлорпірифосу) від DAT для різних мікрокапсульних і контрольних складів хлорпірифосу при тестуванні їх ефективності проти бавовняної тлі (APHIGO). Докладний опис винаходу З метою сприяння розумінню основних принципів даного винаходу, далі по тексту будуть описані переважні варіанти здійснення винаходу, і для їх опису будуть використовуватися конкретні формулювання. Проте, потрібно розуміти, що ці формулювання не передбачають накладення обмежень на обсяг винаходу, і в цей обсяг включені такі зміни, модифікації і подальші додатки принципів даного винаходу, які зазвичай згадуються фахівцеві в тій галузі техніки, якої стосується винахід. В одному з варіантів здійснення, винахід належить до мікроінкапсульованої пестицидної композиції, яка містить щонайменше один пестицид, призначений для знищення або контролю чисельності щонайменше одного шкідника рослин. У деяких композиціях цей пестицид являє собою або щонайменше містить хоча б один фосфорорганічний пестицид. Застосовні фосфорорганічні пестициди містять, не обмежуючись цим, наступні сполуки і їх різні похідні: ацефат, азинфос-метил, хлорфенвінфос, хлоретоксифос, хлорпірифос-метил, діазинон, диметоат, дисульфотон, етопрофос, фенітротіон, фентіон, фенаміфос, фостіазат, малатіон, метамідофос, метидатіон, ометоат, оксидеметон-метил, паратіон, паратіон-метил, форат, фосмет, профенофос, трихлорфон і т. п. Оболонка мікрокапсули може бути утворена полімером, який повністю або частково покриває ядро капсули, збагачене пестицидом. Оболонка мікрокапсули може складатися зі стінки, де стінка виготовлена з полімеру. Деякі придатні полімери, які можуть застосовуватися для створення стінки мікрокапсули, містять щонайменше один тип мономера, молекули якого зв'язуються одна з одною з утворенням полімеру. В одному з варіантів здійснення, полімерна стінка утворюється в результаті міжфазної поліконденсації одного мономера, який переважно розчинний у воді, і іншому мономера, який переважно нерозчинний у воді. Придатні переважно нерозчинні у воді мономери, які можуть застосовуватися для формування стінки мікрокапсули, включають, не обмежуючись перерахованими, такі сполуки, як діізоціанати, поліізоціанати, хлорангідриди двоосновних кислот, хлорангідриди багатоосновних кислот, сульфонілхлориди, хлорформіати і т. п. Прийнятні переважно розчинні у воді мономери, які можуть застосовуватися для формування стінки мікрокапсули, включають, не обмежуючись цим, такі сполуки, як діаміни, поліаміни, водорозчинні діоли і водорозчинні поліоли. Стінка, що є щонайменше частиною оболонки деяких мікрокапсул, має середню товщину від приблизно 5 нм до приблизно 25 нм, причому мікрокапсула може також мати середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон. У деяких варіантах здійснення, стінка мікрокапсули має середню товщину від приблизно 8 до приблизно 12 нм, де вказані мікрокапсули мають середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон. У даній заявці під терміном «приблизно» розуміється плюс або мінус десять процентів від вказаного значення або діапазону значень. Наприклад, «приблизно» 12 включає значення, що знаходяться в діапазоні від 10,8 до 13,2; фраза «приблизно 10 мас.%» належить до складів, які включають від 9 до 11 мас.%; і т.п. Мікрокапсули за різними аспектами і варіантами здійснення даного винаходу демонструють хороші показники токсичності проти популяцій цільових комах і значення LD 50 проти самиць щурів, в діапазоні, що перевищує приблизно 2500 мг/кг. В одній серії варіантів здійснення, мікрокапсули мають значення LD50 для самиць щурів в діапазоні більше ніж приблизно 5000 мг/кг, причому, як правило, ці величини виражають у вигляді відносини кількості пестициду в складі до маси тіла тестового ссавця. У ще одному варіанті здійснення, ці мікрокапсули демонструють значення LD50, виміряні для самиць щурів, порядку приблизно 2500 мг діючих інсектициди. Крім того мікрокапсули ефективні для знищення, пригнічення або налякування шкідників. Деякі варіанти здійснення добре підходять для обробки або регулювання чисельності популяції комах при контакті з комахами. Наприклад, одна композиція включає приблизно 25 мас.% хлорпірифосу і має значення LC50 проти бавовняної тлі (APHIGO) приблизно 30 ч/млн хлорпірифосу, при нанесенні препарату мікрокапсул на популяцію комах або на ділянку, розташовану поруч з популяцією комах. 3 UA 106980 C2 5 10 15 20 25 30 35 40 45 50 55 60 У ще одному варіанті здійснення, мікрокапсули за даним винаходом застосовні для обробки гризучих комах, наприклад, малої совки (LAPHEG). В одному з варіантів здійснення, склад містить приблизно 25 мас.% хлорпірифосу і має значення LC50 для регулювання чисельності малої совки відразу після нанесення приблизно 450 ч/млн, або менш приблизно 400 ч/млн хлорпірифосу, якщо мікроінкапсульований препарат наносять на ділянку рослини, розташовану поруч з популяцією комах. У наступному варіанті здійснення, склад містить приблизно 25 мас.% хлорпірифосу і має значення LC50 проти бавовняної тлі (APHIGO) приблизно 50 ч/млн, при нанесенні препарату мікрокапсул на рослини, рахуючи за підсумковою кількістю, або менше 30 ч/млн хлорпірифосу. У ще одному варіанті здійснення, мікрокапсули застосовні для обробки гризучих комах, наприклад, малої совки (LAPHEG). В одному з варіантів здійснення, склад містить приблизно 20 мас.% хлорпірифосу і має таку ж ефективність регулювання чисельності малої совки відразу після нанесення, як і Lorsban®, при застосуванні в кількості, що відповідає 185-1000 ч/млн хлорпірифосу. Цей самий склад більш ефективний при регулюванні чисельності малої совки, ніж Lorsban®, через п'ять днів після нанесення. Інший аспект даного винаходу належить до способу одержання мікрокапсул з інсектицидними властивостями. В одному з варіантів здійснення, цей спосіб включає стадію одержання інсектициду, наприклад, фосфорорганічного інсектициду, і щонайменше однієї сполуки, яку можна використовувати для формування покриття, яке принаймні частково покриває інсектицид, формуючи хоча б частковий бар'єр між інсектицидом і навколишнім середовищем. В одному з варіантів здійснення, це покриття, оболонку або принаймні компоненти стінки мікрокапсули формують з мономера, який можна ввести в реакцію з аналогічним або іншим мономером з утворенням полімеру, з якого формується стінка мікрокапсули. Додаткові стадії можуть включати змішування інсектициду і компонентів, що утворює стінку, і взаємодію хоча б деяких з цих компонентів з утворенням структури стінки, яка щонайменше частково покриває, оточує, або ізолює інсектицид в частині мікрокапсули. В одному з варіантів здійснення, інсектицид, що застосовується для формування мікрокапсул за даним винаходом, являє собою фосфорорганічну сполуку, наприклад, одну з таких сполук, як: ацефат, азинфос-метил, хлорфенвінфос, хлоретоксифос, хлорпірифос-метил, діазинон, диметоат, дисульфотон, етопрофос, фенітротіон, фентіон, фенаміфос, фостіазат, малатіон, метамідофос, метидатіон, ометоат, оксидеметон-метил, паратіон, паратіон-метил, форат, фосмет, профенофос, трихлорфон і т. п. В одному з варіантів здійснення інсектицид являє собою хлорпірифос. В одному з варіантів здійснення полімер, що містить щонайменше частину стінки мікрокапсули, формують шляхом міжфазної поліконденсації щонайменше одного маслорозчинного мономера, вибраного з групи, яка включає діізоціанати, поліізоціанати, хлорангідриди двоосновних кислот, хлорангідриди багатоосновних кислот, сульфонілхлориди і хлорформіати; і щонайменше одного водорозчинного мономера, вибраного з групи, яка включає: діаміни, поліаміни, водорозчинні діоли і водорозчинні поліоли. В одному з варіантів здійснення, мікрокапсула з інсектицидними властивостями утворена полімером, який хоча б частково оточує фосфорорганічний інсектицид, наприклад, хлорпірифос. Цей полімер утворює стінку, яка хоча б частково оточує порцію хлорпірифосу, і ця стінка має середню товщину від приблизно 8 нм до приблизно 12 нм. В іншому варіанті здійснення, ця стінка має середню товщину від приблизно 5 до приблизно 25 нм. В одному з варіантів здійснення мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон. Ще один аспект даного винаходу належить до способу регулювання чисельності комах, що включає стадії: одержання частинок інсектицидної композиції, де вказані частинки включають фосфорорганічний інсектицид і полімер, причому полімер утворює стінку капсули, яка щонайменше частково інкапсулює фосфорорганічний пестицид з утворенням мікрокапсули, де стінка мікрокапсули має середню товщину від приблизно 5 нм до приблизно 25 нм, і сама мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон; і нанесення вказаного інкапсульованого інсектициду на поверхню, наприклад, листя, стебла або стовбура рослини. Один з варіантів здійснення належить до способу регулювання чисельності комах, який включає стадії: формування мікрокапсули з інсектицидними властивостями, де ця мікрокапсула включає стінку, утворену при міжфазній поліконденсації щонайменше одного маслорозчинного мономера, вибраного з групи, яка складається з діізоціанатів, поліізоціанатів, хлорангідридів двоосновних кислот, хлорангідридів багатоосновних кислот, сульфонілхлоридів і хлорформіатів; і щонайменше одного водорозчинного мономера, вибраного з групи, яка складається з: діамінів, поліамінів, водорозчинних діолів і водорозчинних поліолів; і щонайменше один 4 UA 106980 C2 5 10 15 20 25 30 35 40 45 50 55 60 фосфорорганічний інсектицид, вибраний з групи, яка складається з: ацефату, азинфос-метилу, хлорфенвінфосу, хлоретоксифосу, хлорпірифос-метилу, діазинону, диметоату, дисульфотону, етопрофосу, фенітротіону, фентіону, фенаміфосу, фостіазату, малатіону, метамідофосу, метидатіону, ометоату, оксидеметон-метилу, паратіону, паратіон-метилу, форату, фосмету, профенофосу, трихлорфону і т.п., причому полімерна стінка хоча б частково оточує порцію інсектициду, утворюючи мікрокапсулу. В одному з варіантів здійснення, мікрокапсула містить щонайменше приблизно 10 мас.% хлорпірифосу. В одному з варіантів здійснення, мікрокапсула, що застосовується для регулювання чисельності комах, має стінку, середня товщина якої складає від приблизно 8 нм до приблизно 12 нм, причому середній діаметр вказаної мікрокапсули знаходиться в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон. У наступному варіанті здійснення винахід належить до мікроінкапсульованого фосфорорганічного інсектициду, що застосовується для регулювання чисельності комах, який має значення токсичності проти самиць щурів, що перевищує приблизно 5000 мг/кг, і значення LC50 відразу після застосування при контролі чисельності комах, наприклад, бавовняної тлі (APHIGO) менше ніж приблизно 30 ч/млн хлорпірифосу. У ще одному варіанті здійснення, мікрокапсули мають значення токсичності проти самиць щурів, що перевищує приблизно 2500 мг/кг, і значення LC50 відразу після застосування при контролі чисельності комах, наприклад, малої совки (LAPHEG) менше ніж приблизно 400 ч/млн хлорпірифосу. Один з дуже успішних підходів, застосованих виробниками пестицидів для створення інсектицидних композицій, які демонструють збалансованість корисних властивостей, полягав в інкапсулюванні інсектицидних сполук із застосуванням матеріалів, які виявляють низьку токсичність або взагалі не виявляють токсичності по відношенню до цільової популяції комах і/або які є більш стійкими, і/або з якими простіше поводитися, ніж з самим інсектицидом. Ці інкапсульовані композиції, як правило, демонструють щонайменше одну додаткову бажану властивість в порівнянні з не інкапсульованим інсектицидом. Важливе значення мають композиції на основі частинок, в т.ч. мікрокапсул, які містять щонайменше одну сполуку, токсичну по відношенню хоча б до одного з видів комах, зокрема, до видів комах, які служать переносником захворювань тварин і людини, або створюють загрозу для комерційно значущих видів рослин. Сполуки, що виявляють токсичність по відношенню до комах, включають, не обмежуючись цим, фосфорорганічні сполуки, наприклад, ацефат, азинфос-метил, хлорфенвінфос, хлоретоксифос, хлорпірифос-метил, діазинон, диметоат, дисульфотон, етопрофос, фенітротіон, фентіон, фенаміфос, фостіазат, малатіон, метамідофос, метидатіон, ометоат, оксидеметон-метил, паратіон, паратіон-метил, форат, фосмет, профенофос, трихлорфон і т.п. Іншим класом молекул, що мають інсектицидні властивості, є хлорорганічні сполуки, і в їх число входять такі речовини, як гептахлор, дихлордифенілтрихлоретан, дикофол, ендосульфан, хлордан, мірекс і пентахлорфенол. Іншим класом інсектицидів і репелентів комах є піретроїди, тобто аналоги природних сполук, що зустрічаються в ромашці Pyrethrum, і в їх число входять, наприклад, алетерин, біфентрин, циперметрин, дельтаметрин, перметрини, пралетрин, ресметрин, сумітрин, тетраметрин, тралометрин, трансфлурин і іміпротрин. Ще один клас інсектицидів утворює сполуки, подібні до природної сполуки нікотин, і, крім нікотину, цей клас інсектицидів і репелентів комах включає наступні сполуки: ацетаміприд, клотіанідин, імідаклоприд, нітенпірам, тіаклоприд і тіаметоксам. Способи і сполуки, які придатні для формування частинок, включають будь-який спосіб, який може застосовуватися для формування оболонки, шару, покриття або стінок. Як правило, діючий інгредієнт в таких частинках в основному розташований всередині стінки, хоча для формування частинок повне покриття діючого інгредієнту не є суворо необхідним; склади включають частинки, в яких щонайменше частина діючого інгредієнту стикається зі стінкою або навіть знаходиться за межами хоча б частини стінки. Один з способів формування частинок, який включає повне або часткове формування стінки, функція якої полягає в повному або частковому відділенні інсектициду від маси розчинника або навколишнього середовища, полягає в міжфазній поліконденсації мономерів. Кажучи коротко, суміш мономерів піддають конденсації з метою формування полімерної стінки в присутності щонайменше одного інсектициду. Стінка, що містить полімер, в основному формує зовнішній кордон частинки; інсектицид може бути в основному сконцентрований в частинці, обмеженій безперервною або переривчастою стінкою, яка формує зовнішні контури частинки. Мономери, які можуть застосовуватися для формування частинок способом міжфазної поліконденсації, можуть включати в основному маслорозчинний мономер або групу таких мономерів, і водорозчинний мономер або групу таких водорозчинних мономерів. Маслорозчинні мономери включають, наприклад, сполуки, вибрані з групи, в яку входять: діізоціанати, 5 UA 106980 C2 5 10 15 20 25 30 35 40 45 поліізоціанати, хлорангідриди двоосновних кислот, хлорангідриди багатоосновних кислот, сульфонілхлориди, хлорформіати і т.п. Водорозчинні мономери включають, наприклад, сполуки, вибрані з групи, в яку входять: діаміни, поліаміни, водорозчинні діоли і водорозчинні поліоли. Для одержання інсектициду або репеленту комах з бажаними характеристиками, необхідно добитися, щоб препарат мав широкий набір різних властивостей. Ці властивості включають токсичність по відношенню до комах або, принаймні, відлякувальну дію на цільових комахах або обмеження їх розвитку і/або здатності до розмноження. Інша бажана властивість включає низьку токсичність або, в ідеальному випадку, відсутність токсичності відносно інших тварин, наприклад, ссавців, зокрема, людей, або відносно рослин, або нецільових, зокрема, корисних видів комах. Іншою бажаною властивістю є передбачуваний і, в більшості випадків, тривалий період двократного зменшення ефективності (період напіврозпаду) проти цільових шкідників. Пестицидні композиції, які зберігають ефективність проти популяції цільових шкідників протягом тривалого періоду часу, можна застосовувати з метою контролю над цільовими шкідниками не так часто або в менших вихідних кількостях, що дозволяє економити трудовитрати, енергію і матеріали. З іншого боку, склади, що мають тривалі періоди напіврозпаду, наприклад, період напіврозпаду яких значно перевищує тривалість сезону росту даної культури, або часу максимального зараження цільовими шкідниками, можуть, в деяких ситуаціях, вважатися джерелом небезпеки для навколишнього середовища. Ще однією бажаною властивістю є передбачуваний і, в більшості випадків, тривалий час перебування інсектициду на рослині, що захищається. Нанесення пестицидних композицій, що демонструють тривалий час перебування на рослині, може призвести до зниження витрат, оскільки протягом сезону росту або періоду очікуваного зараження необхідна менша кількість нанесення. Хоча можна перерахувати ідеальні властивості ідеального інсектициду, через відмінності в способах застосування ідеальних пестицидів не існує. Тому мета полягає в створенні пестициду з певними властивостями, який за необхідності можна застосовувати в різних конкретних умовах. У даній заявці розкриті мікроінкапсульовані пестициди в формі частинок, що мають таку товщину стінки і такий розмір, які сприяють їх застосуванню в різних умовах. Несподівано виявилося, що ці варіанти здійснення включають інсектицидні композиції, з таким розміром частинок і такою товщиною стінки, які дозволяють цим частинкам демонструвати високу вихідну активність з позбавлення рухомості комах (нокдаун-ефект, параліч комах), включаючи контактну активність проти цільових комах, значення токсичності LD50 проти самиць щурів порядку 2500 мг/кг і, в деяких випадках, більш високий або переважний залишковий вміст препарату на рослинах. Далі буде наведений докладний опис варіантів здійснення даного винаходу, приклади яких проілюстровані прикладеними кресленнями. У всіх випадках, коли це можливо, на кресленнях і в таблицях буде використана одна і та ж нумерація, для посилань на одні і ті ж або подібні сполуки, композиції, пристрої і т.п. ПРИКЛАДИ Фахівцеві в даній галузі техніки повинно бути очевидно, що в даний винахід можна внести різні модифікації і варіанти, не відступаючи від суті і не виходячи за межі обсягу винаходу. Таким чином, розуміється, що даний винахід охоплює ці модифікації і варіанти, за умови, що вони входять в обсяг прикладеної формули винаходу і її еквівалентів. Матеріали і методики У таблиці 1 підсумовувані хімічні і фізичні властивості деяких нових і деяких контрольних складів, що містять хлорпірифос і мікрокапсули. Ці капсули одержували міжфазною конденсацією, приклад здійснення якої описаний в типовій методиці. 50 6 UA 106980 C2 Таблиця 1 Склади на основі капсул Номер партії Цільовий діаметр капсули (мкм) Цільова товщина стінок капсули Хлорпірифос (маса в г) 1 Ароматичні сполуки ряду ксилолів 2 Поліметілен поліфенілізоціанат (г) 3 Етилендіамін (г) 4 Полі(вініловий спирт)GL 03 PVA (г) 5 Бентонітова глина (г) 6 Ксантанова камедь (г) 7 Полімерне ПАР (г) Вода (г) Виміряний діаметр капсули (мкм) CCS-0 3 5 15,552 9,313 0,165 0,040 2,275 0,455 0,057 1,266 32,570 3,3 CCS-1 3 10 15,419 9,251 0,330 0,079 2,275 0,455 0,057 1,266 32,926 3,5 CCS-2 6 5 15,574 9,344 0,083 0,020 1,400 0,455 0,057 0,779 33,266 6,2 CCS-3 6 10 15,522 9,313 0,165 0,040 1,400 0,455 0,057 0,779 33,445 5,9 Контрольні склади: Lorsban 4E - NAF-163 Pyrinex ME - суспензія капсул хлорпірифосу, що є в продажу, яка постачається на європейський ринок фірмою Bayer. 1 Aromatic 100 (г), Exxon Mobile Corp., Fairfax, VA. 2 PAPI® 27, Dow Plastics, Midland, MI. 3 Sigma-Aldrich. 4 Gohsenol GL03 (г) компанії Nippon Gohsei. 5 Veegam®, RT Vanderbilt, Inc. 6 Kelzan® S, Kelco, Co. 7 Atlox® 4913, Croda. 5 10 15 20 25 30 Одержання суспензій мікрокапсул Типова маса компонентів, що застосовуються для приготування суспензії мікрокапсул, наведені вище по тексту в розділі «матеріали». Використовувалася наступна методика одержання суспензій. У 4-уніцієву широкогорлу банку поміщували вказану кількість мономера ізоціанату PAPI 27 (Dow Chemical). До PAPI 27 додавали суміш ароматичних вуглеводнів, що містить 62,5 мас.% хлорпірифосу, одержуючи 25 г органічної фази. Одержану суміш енергійно перемішували до однорідного стану. Готували водну фазу, використовуючи вказані кількості полі(вінілового спирту) (PVA, Gohsenol GL03, Nippon Gohsei), Veegam® (R.T. Vanderbilt) і Kelzan S® (Kelco) і додаючи достатню кількість деіонізованої води для одержання в загальній сумі 35 г водної фази. Водну фазу додавали до органічної фази, одержуючи двофазну суміш. Цю суміш емульгували із застосуванням високошвидкісного міксера Silverson L4RT-A, використовуючи стандартний агрегат для змішування, забезпечений 3,4-дюймовою трубкою і багатоцільовою емульгуючою головкою. Емульгування здійснювали, починаючи перемішування з відносно низькою швидкістю (~1000 об./хв) і поміщуючи наконечник агрегату для змішування у водну фазу, з тим, щоб він втягував органічну фазу, поки вона не буде добре емульгована. Потім швидкість підвищували дискретними рівнями. Після кожного підвищення швидкості, перемішування зупиняли і проводили вимірювання розміру частинок. Цей процес повторювали до одержання частинок бажаного розміру. Як правило, для досягненні бажаного розміру була потрібна швидкість ~4500-7500 об./хв. При перемішуванні на зниженій швидкості, що дозволяла зберегти хорошу якість перемішування, по краплях у вигляді 10% водного розчину додавали амін, що здійснює поперечне зшивання (етилендіамін (EDA), Aldrich). Після закінчення додавання аміну, одержану суспензію капсул перемішували протягом ще однієї хвилини, додавали вказану кількість Atlox 4913 (Uniqema), і проводили короткочасну заключну гомогенізацію, завершуючи одержання суспензії капсул. Обережно регулюючи тривалість часу перемішування суміші і/або регулюючи швидкість міксера, можна одержувати інкапсульовані фосфорорганічні інсектицидні композиції з різним розміром капсул, що мають різну товщину оболонки. Подібним же чином, для одержання мікроінкапсульованих фосфорорганічних інсектицидних композицій, що мають різний розмір капсули і товщину оболонки, можна регулювати кількість мономера, зшивного агента, змочувальних агентів, буфера і т.п. 7 UA 106980 C2 5 10 15 20 25 30 35 Вимірювання розміру частинок в суспензіях мікрокапсул Розподіл розмірів частинок в суспензіях капсул визначали з використанням приладу для визначення розмірів частинок з розсіювання світла Malvern Mastersizer 2000, обладнаного вузлом для роботи із зразками малого об'єму, застосовуючи програму версії 5.12. Перед вимірюваннями зразки добре струшували або перемішували для гарантії гомогенності. Розподіл середніх значень об'єму (VMD) для кожного складу наведений вище по тексту в розділі «матеріали». Обчислення товщини стінки капсули Розрахунок кількості компонентів стінки капсули, необхідних для одержання стінки шуканої товщини, основувався на геометричній формулі, що виражає об'єм сфери через величину її радіуса. При певних припущеннях про морфологію ядра і оболонки, з урахуванням того, що ядро складається з нерозчинних у воді компонентів, які не входять до складу стінки (хлорпірифосу, розчинника), і оболонка складається з здатних до полімеризації матеріалів (масло- і водорозчинних мономерів), можна одержати рівняння (1), яке зв'язує відношення об'єму ядра (VC) до суми об'ємів ядра і оболонки (VS) з відповідними радіусами, де rS означає радіус капсули, включаючи оболонку, і I S означає товщину оболонки. Розв’язуючи рівняння (1) для об'єму оболонки, одержуємо: Виражаючи відповідні об'єми через маси (m i) і густину (di) (mS/dS=VS і mC/dC=VC, де підрядкові коефіцієнти S або С належать до оболонки або ядра відповідно) і розв’язуючи одержане рівняння для маси оболонки, одержуємо: Порівнюючи рівняння (2) і (3), можна бачити, що вплив співвідношення густини d S/dC полягає в появі постійного коректуючого коефіцієнта, якщо для обчислення кількості компонентів стінки, необхідних для одержання капсули з бажаним розміром і товщиною стінки, використовувати масу. Якщо співвідношення густини для ряду капсул залишається постійним, як у випадку даного дослідження, де у всіх препаратах використовуються одні і ті самі матеріали ядра і оболонки, видалення члена, що відображає співвідношення густини, вплине тільки на абсолютні значення товщини стінок, а не на їх відносну різницю. Оскільки першорядне значення має відносна різниця, для спрощення розрахунків застосовували наближення, в якому прибраний множник, що описує співвідношення густини, одержуючи рівняння (4) 40 45 Здійснюючи підстановки, а саме m C=mO-mOSM, mS=mO+(fWSM/OSM)mOSM-mC і fWSM/OSM=mWSM/mOSM (співвідношення маси водорозчинного мономера і маслорозчинного мономера), де m O означає масу масляних компонентів (хлорпірифос, розчинник, маслорозчинний мономер), m OSM означає масу маслорозчинного мономера, і m WSM означає масу водорозчинного мономера, і розв’язуючи рівняння для m WSM, одержуємо: 8 UA 106980 C2 5 10 15 20 25 30 35 40 45 50 Для визначення m OSM в розрахунку як вихідна умова використовується загальна кількість mWSM. У даному дослідженні водорозчинний мономер використовувався в еквівалентному масовому співвідношенні 1:1 до маслорозчинного мономера при одержанні всіх препаратів суспензій капсул. Біологічні дослідження для визначення активності проти типових поширених видів комахшкідників Pyrinex CS® є зареєстрованою торговою маркою Bayer Corporation. Цей продукт являє собою інкапсульовану форму хлорпірифосу. Продукт, застосований як контроль в описаному нижче експерименті, був зроблений Makhteshim Chemical Works, Be'er Sheva, Israel. Згідно зі специфікацією з безпеки матеріалів, випущеною постачальником, Pyrinex CS має пероральну токсичність, причому значення LD50>20000 мг/кг. Lorsban 4E являє собою концентрат хлорпірифосу, який емульгується, що поставляється на ринок Dow Agro Sciences, Indianapolis, Indiana, USA. Згідно зі специфікацією з безпеки матеріалів, яку можна отримати у постачальника, Lorsban 4E має значення LD 50 для самиць щурів, рівне приблизне 300 мг/кг. Lorsban і Pyrinex CS вибрані як контроль для більшості тестів, оскільки ці склади є представниками двох протилежного типу складів, що включають хлорпірифос. Lorsban є концентратом, який емульгується, що характеризується прекрасною паралізуючою активністю (нокдаун-ефектом) і значенням LD50 проти самиць щурів приблизно 300 мг/кг, тоді як Pyrinex має значення LD50 проти самиць щурів порядку приблизно 20000 мг/кг і слабку паралізуючу активність. Дані про токсичність Lorsban і Pyrinex взяті із специфікацій з безпеки матеріалів виробників цих двох складів. Активність проти малої совки (LAPHEG): Рослини в стадії росту 4-5 даного листка обприскували із застосуванням самохідного обприскувача, налаштованого таким чином, щоб подавати розчин в кількості 200 л/га через насадку Teejet 8003 EVS при тиску 40 фунт/кв.дюйм. Для одержання даних на момент початку експерименту, рослинам давали висохти, після чого відбирали зразки тканини листя. Для тестів на кількість препарату, що залишився, рослини витримували в теплиці при 80-100F і відносній вологості 70-80%. З листя обприсканих рослин вирізали диски 33 см і поміщували по одному листовому диску в кожну ямку 32-ямкового планшета для біологічних аналізів, на дні яких був тонкий шар агар-агару. 5 личинок малої совки на другій стадії росту поміщували в центр кожного листового диска і закривали планшет пластиковою кришкою. Личинок утримували в камері штучного клімату при 25C/відносний вологості 40%. Підраховували смертність личинок через 24 години після зараження паразитами листових дисків, причому личинку вважали мертвою, якщо вона не могла рухатися, коли її стимулювали дотиком. Дані аналізували, застосовуючи пробіт-трансформацію log дози для визначення значень LC50 і LC90 і їх 95% довірчих рівнів. Активність проти бавовняної тлі (APHIGO). Сіянці гарбуза заражали бавовняною тлею, вміщуючи на сім’ядолі невеликі шматочки листя гарбуза, інфікованого тлею з лабораторної колонії (Aphis Gossypii). Перед обробкою тлі давали розповсюдитися по листі протягом 24 годин. Рослини гарбуза обприскували тестованим розчином, використовуючи ручний розпилювач Devilbis. Рослини обприскували до стікання. Результати контрольних дослідів підраховували через 24 години шляхом випадкового вибору одного листка на кожній рослині і підрахунку живої тлі, що є на ньому. Дані аналізували, застосовуючи пробіт-трансформацію log дози для визначення значень LC50 і LC90 і їх 95% довірчих рівнів. Для визначення ефективності регулювання чисельності комах залишковими кількостями препаратів, обприскували неінфіковані рослини гарбуза і витримували в теплиці при 80-90F/відносна вологість 70-80%. Через певний час рослини інфікували за описаною вище методикою і підраховували результати через 24 години. Типові методики, які застосовувалися для вимірювання залишкової ефективності різних тестованих складів Методика: Розводили склади, до досягнення концентрації 1 кг хлорпірифосу/200 л об'єму розпалюваного препарату і розпилювали на 12 рослин на стадії 2-3 листка (сім’ядолі). Рослини 9 UA 106980 C2 5 10 15 20 25 30 35 40 45 50 55 60 переносили в теплицю (80-90F/відносна вологість 70-80%) і розміщували таким чином, щоб витрата при обприскуванні складала 200 л/га, тобто 1 кг дійсн. інгредієнта/га. Відбір зразків: У групи оброблених рослин на 0, 3, 7 і 14 день після обробки видаляли в загальній сумі по три сім’ядолі (несправжніх листка). Листя зважували, поміщували в 1-унцієву скляну посудину, в яку додавали 10 мл ацетонітрилу. Посудину закривали кришкою і струшували на вібростолі протягом 45 хвилин, таким чином, щоб ацетонітрил під час струшування покривав увесь листок. Зразок ацтонітрилу пропускали через шприц з фільтром з політетрафторетилену з розміром пор 0,45 мкм, в пляшечку для РХ і піддавали аналізу. Аналіз: Для вимірювання концентрації хлорпірифосу в екстракті застосовували РХ/МС. Визначення концентрації зразків не було потрібне. Методики, які застосовувалися для вимірювання токсичності різних складів проти самиць щурів Методика тесту для 2000 мг/кг Мета цього дослідження полягала у визначенні потенціалу тестованих сполук надавати летальну дію при фіксованому дозуванні. Вихідну дозу, рівну 2000 мг/кг, вводили одній жіночій особині тварини. Якщо перша тварина виживала після введення дози, тестовану сполуку послідовно вводили ще 4 самицям, вводячи дозу в загальній сумі п'яти тваринам. Методика тесту для 5000 мг/кг Трьом іншим тваринам послідовно вводили 5000 мг/кг. Якщо перша особина виживала після введення дози, тестовану речовину послідовно вводили двом іншим самицям щурів. Якщо всі тварини виживали, тестування припиняли і вважали, що значення LD50 перевищує 5000 мг/кг. Тварини, використані для тестування Для цього дослідження використовували щурів, маса яких на початку дослідження складала 113,0-143,2 г. Препарати вводили щурам, починаючи з віку приблизно двох місяців, і через 2-3 тижні проводили розтин тварин. Лінія тварин і обґрунтування її використання Для експериментів використовували самиць щурів F344/DuCrl, оскільки вони добре підходять для дослідження гострої пероральної токсичності, для них доступні історичні дані і є надійний комерційний постачальник. Тестових тварин одержували у Charles River Laboratories Inc. (Raleigh, North Carolina). Вік тварин на початку дослідження становив 8-11 тижнів. Фізичний стан і аклімація тварин Всіх тварин при надходженні в лабораторію (повністю акредитовану Міжнародною Асоціацією з Атестації і Акредитації Утримання Лабораторних Тварин - AAALAC International) піддавали огляду, який проводив лабораторний ветеринар або кваліфікований фахівець з токсикології тварин під безпосереднім спостереженням лабораторного ветеринара, з метою визначення загального стану здоров'я і придатності для цілей дослідження. Утримання тварин Тварин селили в клітки з нержавіючої сталі по дві-три особини на клітку в кімнатах, розрахованих на підтримання необхідних умов (температури, вологості і світлового циклу), і перед початком дослідження адаптували до лабораторних умов протягом щонайменше одного тижня. Тварин селили в клітки з нержавіючої сталі по одній особині на клітку. Відносну вологість підтримували в діапазоні 40-70%. Середню температуру в кімнаті підтримували на рівні 22±1C (при максимальному допустимому відхиленні ±3C). У всіх кімнатах з тваринами встановлювали світловий цикл 12 годин світло/темрява, при включенні світла о 6:00 ранку і вимкненні світла у 18: 00 вечора. Повітря в кімнаті оновлювалося приблизно 12-15 разів на годину. Підлоги в клітках являли собою сітку з металевого дроту, яка була покрита зверху всмоктувальним папером. Клітки були забезпечені ручними годівницями і системою подачі води клапанного типу, що активується натисканням. Рандомізація і ідентифікація Щурів випадковим чином розподіляли за експериментальними групами, використовуючи комп'ютерну програму. Ідентифікацію тварин здійснювали за допомогою кодового числа, що передається імплантованим під шкіру транспондером (BioMedic Data Systems, Seaford, Delaware). Їжа і вода Тваринам давали корм LabDietâ Certified Rodent Diet #5002 (PMI Nutrition International, St.Louis, Missouri) в формі гранул. Їжа і водопровідна вода давалися без обмежень. Для підтвердження того, що раціон харчування забезпечує достатнє надходження поживних речовин і кількісного визначення вмісту окремих небажаних домішок, PMI Nutrition International здійснювали аналіз корму. Міський департамент водопостачання періодично проводив аналіз питної води, яку відбирали з муніципальних джерел, з метою визначення хімічних параметрів і 10 UA 106980 C2 5 10 15 20 25 30 35 40 45 50 55 біологічних забруднень. Крім того, через певні проміжки часу незалежні експертні служби здійснювали вибіркові аналізи для виявлення хімічних забруднень. Ні в їжі, ні у воді не були виявлені будь-які небажані домішки, які могли б несприятливим чином вплинути на результати дослідження або їх інтерпретацію. Благополуччя тварин Згідно з правилами департаменту США про благополуччя сільськогосподарських тварин, 9 CFR, підрозділ А, частини 1-4, благополуччя тварин і проведення дій, необхідних для здійснення описаних досліджень, були розглянуті і схвалені Інституціональним Комітетом з Утримання і Використання Тварин (IACUC). IACUC встановив, що запропоновані дії знаходяться у повній відповідності до згаданих Остаточних Правил. Схваленими IACUC діями з утримання і використання тварин, які потрібно було застосовувати при описаному дослідженні, були Acute Tox 01, DCO 01 і Animal ID 01. Розрахунок доз Індивідуальні дози розраховували на основі вихідної маси тіла тварин (натщесерце). Всі дози вводили в одиницях об'єму, з урахуванням питомої ваги. Введення препаратів Введення препаратів окремим тваринам проводили послідовно. Часовий інтервал між введеннями визначали виходячи з часу початку, тривалості і тяжкості ознак отруєння. Введення дози наступній тварині відкладали до появи обґрунтованої впевненості у виживанні тварини, що отримала попередню дозу. Всі тварини отримували дози через пероральний зонд, в якому використовувалася голка для примусового харчування з нержавіючої сталі з шароподібним наконечником, сполучена з відповідним шприцом. Максимальний об'єм, що вводиться за один раз, залежав від розмірів тварини. Цей об'єм не перевищував 10 мл/кг. Щоденний огляд Як правило, тварин оглядали в їх клітках, і огляд був призначений для виявлення значних клінічних аномалій, які явно помітні при швидкому огляді, а також для спостереження за загальним станом здоров'я тварин. Під час огляду тварин не брали в руки, якщо не вважали це необхідним. Значні відхилення, які можна було виявити під час огляду, включали, не обмежуючись цим: знижену/підвищену активність, патологічні циклічні дії, видавання звуків, нескоординовані/уповільнені рухи, тілесні ушкодження, нервово-м’язові функції (судоми, фасцикуляції, тремор, конвульсії), зміну дихання, синяву/блідість шкіри і слизових оболонок, важкі ураження очей (розрив), зміну консистенції фекальної маси і кількості фекалій/сечі. Крім того, визначали захворюваність, смертність і можливість приймати їжу і воду хоча б два рази на день. Детальні клінічні огляди Детальний клінічний огляд (DCO) проводили для всіх щурів до введення тестованих продуктів з метою порівняння з результатами оглядів, що реєструються протягом дослідження. У день введення препаратів тварин піддавали огляду мінімум два рази. DCO здійснювали кожний день (включаючи вихідні і святкові дні) протягом всього дослідження. Ручний огляд і огляд у відкритому просторі включав ретельні вивчення параметрів фізичного стану згідно з встановленим форматом. Для підрахунку результатів DCOs реєстрували тільки ті дані, які відрізнялися від звичайно очікуваних. Огляд проводився на основі довідника, причому цей довідник містив більшість звичайних фізичних і неврологічних відхилень, що спостерігаються при дослідженні токсичності. Оскільки в довіднику були наведені не всі можливі симптоми, допускався також опис у вільній формі. Патологія Тваринам, які піддавались розтину, будучи живими, проводили анестезію вдиханням діоксиду вуглецю, розкривали і фіксували їм трахеї і умертвляли обезголовлюванням. Повний розтин всіх тварин проводився ветеринарним патологоанатомом при сприянні групи кваліфікованих помічників. Розтин включав дослідження зовнішніх частин тканин і всіх отворів. Очі обстежували in situ накладенням змоченої скляної пластинки на всі рогові оболонки. Розкривали порожнину черепа і оглядали мозок, гіпофіз і сусідні тканини шийного відділу. Знімали шкіру з тушки, розкривали грудну і черевину порожнину і оглядали внутрішні органи. Потім всі тканини і тушки викидали. Статистична обробка результатів Обчислювали середні значення і стандартні відхилення маси тіла тварин. Після закінчення введення кожної дози, відомості про короткочасні і довготривалі наслідки (результати) вводили в програму OECD 425 AOT. Коли досягалися умови зупинки, обчислювали LC 50 і 95% довірчі інтервали. 60 11 UA 106980 C2 5 Приклад 1 Результати і обговорення Вихідні дані з залишкової кількості інсектициду на бавовнику для різних контрольних і експериментальних складів наведені в таблиці 2. Ці дані аналізували в Minitab, передбачаючи, що розпад препаратів відбувається за рівнянням першого порядку і підбираючи криву залежності логарифма середньої залишкової кількості препарату від часу (в днях). Таблиця 2 Дані з залишкової кількості інсектициду, одержані в тестах нових мікрокапсул і контрольних складів Вихідна маса листка Склад Lorsban 4E Pyrinex CS CCS-0 CCS-1 CCS-2 CCS-3 Конц. дійсн. інгр. 1 2 Lorsban 4E Pyrinex CS CCS-0 CCS-1 CCS-2 CCS-3 2 3 44,1 мас.% 0,621 0,475 0,591 51 48 32 410,6 505,3 270,7 457,9 250 г/л 20,1 мас.% 19,9 мас.% 20,4 мас.% 20,3 мас.% 0,672 0,446 0,728 0,461 0,534 65 53 66 59 68 60 29 102 75 79 92 74 62 39 98 638,5 400,9 378,0 450,4 509,0 616,1 615,3 573,2 477,7 715,8 0,509 0,661 0,873 0,655 0,668 0,571 0,853 0,557 0,67 0,548 Конц. дійсн. інгр. Lorsban 4E Pyrinex CS CCS-0 CCS-1 CCS-2 CCS-3 10 1 Аналіз через 6 днів 2 525,4 170,0 915,6 559,7 720,8 3 Середн. 1 684,5 829,6 425,8 423,0 917,6 Залишок мг/кг 3 1 2 3 1 2 3 Середн. 44,1 мас.% 0,999 1,008 1,259 1,1 1,4 1,2 11,0 13,9 9,5 11,5 250 г/л 20,1 мас.% 19,9 мас.% 20,4 мас.% 20,3 мас.% 1,244 1,157 1,356 1,496 1,007 22 0,6 6,8 1,5 2,1 30 0,7 6,1 2,6 3,8 34 1,3 5,9 2,3 3,7 168,8 248,6 273,3 4,4 6,2 11,2 61,4 58,0 43,5 12,6 23,7 15,4 14,8 32,1 36,7 1 2 1,303 1,351 1,108 1,186 1,419 1,207 1,121 1,051 1,096 1,183 Аналіз через 13 днів Маса листка Склад Залишок мг/кг 3 Маса листка Склад Вихідний аналіз CPF Конц. дійсн. інгр. Залишок мг/кг 2 3 1 2 3 1 2 3 Середн. 1,021 1,027 0,7 0,5 1 4,8 4,9 9,7 6,5 1,09 1,261 1,029 1,264 1,603 1,09 1,343 1,297 1,168 1,41 1,245 1,334 1,296 1,305 1,13 11,9 0,8 1,5 1 0,8 16,8 1,2 1,1 0,6 0,9 26,8 1,2 1,1 0,8 0,7 1 44,1 мас.% 1,45 250 г/л 20,1 мас.% 19,9 мас.% 20,4 мас.% 20,3 мас.% 230,2 7,3 54,3 17,2 27,9 109,2 133,2 215,3 7,8 9,5 9,0 9,4 10,1 8,5 7,4 4,6 6,1 6,8 6,4 6,2 152,6 8,8 9,3 6,1 6,5 Період напіврозпаду хлорпірифосу в даних експериментах обчислювали виходячи з нахилу підігнаних ліній (-0,693/нахил); дані, одержані для різних контрольних і експериментальних складів, що включають хлорпірифос, показані в таблиці 3. Дані за періодом напіврозпаду виражені в днях. 12 UA 106980 C2 Таблиця 3 Період напіврозпад хлорпірифосу як діючого інгредієнту різних нових і контрольних інсектицидних композицій Склад Період напіврозпаду (дні) 2,2 6,9 2,2 2,2 2,1 1,9 Lorsban 4E Pyrinex CS CCS-0 CCS-1 CCS-2 CCS-3 5 10 15 20 Криві для Lorsban 4E і CCS-0 не є такими ж лінійними, як інші криві. Це може пояснюватися тим, що частина хлорпірифосу випарилася або зазнала фотолізу в проміжку між вимірюваннями, при вимірюванні на 6-й день або незабаром після нього. Внаслідок цього можливо, що CCS-0 і Lorsban 4E мають приблизно однаковий час напіврозпаду, який коротше, ніж вийшло за результатами дослідження, і його можна визначити точніше, використовуючи дві перші точки графіка. Хоча часи напіврозпаду можна застосовувати при визначенні профілю вивільнення капсули, мета описуваного дослідження полягала в порівнянні залишкової кількості інкапсульованих складів. Всі протестовані експериментальні склади продемонстрували такий самий або більш низький залишковий вміст, ніж контрольний препарат Lorsban 4E. Препарат Pyrinex включає дуже товсті капсули, і він дуже сильно відрізняється від експериментальних складів, що включають капсули, демонструючи суттєво більш тривалий період напіврозпаду і більш високий залишковий вміст через 13 днів. Експериментальні склади на основі капсул (CCS-0, CCS-1, CCS-2, CCS-3) забезпечили більш високий залишковий вміст, ніж концентрат хлорпірифосу Lorsban 4E, який емульгується, що поставляється на ринок корпорацією Dow, але значно менше, ніж Pyrinex, тобто склад, що включає капсули з відносно товстими стінками, що поставляється на ринок компанією Bayer. Біологічні дослідження: Дані тестування різних складів, в т.ч. деяких експериментальних складів на малих совках (LAPHEG) показані в таблиці 4. Таблиця 4 Значення LC50 та LС90 (в ч/млн. хлорпірифосу), одержані при вимірюванні здатності різних нових складів на основі мікрокапсул і контрольних складів хлорпірифосу регулювати чисельність малої совки (LАРНЕG) 0 днів 4 дні 7 днів після після після К-ть обробки LС50 LC90 обробки LС50 LC90 обробки LС50 Склад діючого (кількість ч/млн ч/млн (кількість ч/млн ч/млн (кількість ч/млн інгредієнта загиблих загиблих загиблих особин) особин) особин) L 4Е 1000 ч/млн 40-40 529,43 828,1 31-40 716,02 1293,5 24-40 874 6 500 ч/млн 33-40 8-40 6-40 250 ч/млн 3-40 1-40 1-40 125 ч/млн 0-40 0-40 0-40 ССS-0 1000 ч/млн 500 ч/млн 250 ч/млн 125 ч/млн 40-40 25-40 2-40 5-40 441,46 667,46 34-40 17-40 2-40 0-40 13 572,1 1068,69 14-40 10-40 1-40 1-40 LC90 ч/млн 18137 1469,26 6889,13 UA 106980 C2 Продовження таблиці 4 ССS-1 1000 ч/млн 500 ч/млн 250 ч/млн 125 ч/млн 40-40 38-40 2-40 3-40 353,55 463,17 38-40 35-40 3-40 1-40 367,53 518,25 35-40 31-40 7-40 2-40 376,11 777,81 ССS-2 1000 ч/млн 500 ч/млн 250 ч/млн 125 ч/млн 40-40 33-40 3-40 0-40 379,99 549,7 34-40 21-40 1-40 0-40 541,41 960,9 33-40 14-40 0-40 0-40 656,33 1002,08 ССS-3 1000 ч/млн 500 ч/млн 250 ч/млн 125 ч/млн 40-40 38-40 11-40 1-40 299,58 450,59 35-40 16-40 4-40 1-40 542,41 1139,54 27-40 12-40 2-40 0-40 728,15 1526,94 Pyrinex 1000 ч/млн 500 ч/млн 250 ч/млн 125 ч/млн 36-40 6-40 9-40 1-40 681,66 1000,05 32-40 10-40 3-40 0-40 668,39 1286,75 28-40 10-40 3-40 1-40 730,82 1797,32 Таблиця 7 Дані, одержані при вимірюванні здатності різних нових складів на основі мікрокапсул і контрольних складів хлорпірифосу регулювати чисельність бавовняної тлі (АРНІGО). Експерименти відтворювали 4 рази і виражали результати у відсотках від контролю Склад Кількість діючого інгредієнта Повтор 1 Повтор 2 Повтор 3 Повтор 4 % від контролю Lorsban 4E 0 днів після обробки 400 ч/млн 0 0 0 0 0 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн 1 8 29 56 58 0 5 31 70 71 1 4 27 66 88 0 11 42 44 92 1 7 32 59 77 400 ч/млн 15 12 17 45 22 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн 24 56 61 72 87 31 59 63 68 90 26 52 64 77 89 45 65 63 63 70 32 58 63 70 84 400 ч/млн 56 67 64 59 62 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн 58 78 75 75 89 66 54 87 81 90 64 70 64 85 95 71 75 73 80 96 65 69 75 80 93 Lorsban 4E 4 дні після обробки Lorsban 4E 7 днів після обробки 14 UA 106980 C2 Продовження таблиці 7 Pyrinex 0 днів після обробки 13 41 61 71 91 90 45 76 74 87 85 44 55 65 81 88 39 59 88 94 92 42 63 75 88 89 400 ч/млн 42 53 44 41 45 49 59 89 83 91 55 71 84 88 82 61 65 72 81 85 50 52 70 71 87 54 62 79 81 86 400 ч/млн 35 29 31 24 30 47 63 83 81 95 55 58 81 90 80 51 57 80 92 85 46 71 77 86 83 50 62 80 87 86 400 ч/млн 0 0 0 0 0 0 3 29 49 51 0 6 36 41 43 0 1 20 45 56 0 5 19 39 65 0 4 26 44 54 400 ч/млн 6 1 3 7 4 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн ССS-0 7 днів після обробки 8 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн ССS-0 0 днів після обробки 14 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн ССS-0 0 днів після обробки 12 200 ч/млн 100 ч/млн 50 ч/млн 25 12,5 Pyrinex 7 днів після обробки 18 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн Pyrinex 4 дні після обробки 400 ч/млн 20 32 45 42 54 26 39 48 54 50 31 49 41 58 62 16 42 51 61 68 23 41 46 54 59 400 ч/млн 21 35 26 24 27 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн 33 41 52 61 68 41 38 55 62 71 35 47 58 59 65 29 50 61 65 72 35 44 57 62 69 15 UA 106980 C2 Продовження таблиці 7 ССS-1 0 днів після обробки 0 0 7 17 51 71 0 1 30 58 81 0 4 34 49 76 0 1 19 63 65 0 3 25 55 73 400 ч/млн 1 0 1 0 1 14 36 47 68 87 24 49 56 74 77 26 51 63 65 61 19 45 66 72 74 21 45 58 70 75 400 ч/млн 25 30 21 28 26 35 55 66 78 86 32 49 57 83 79 29 51 60 81 72 38 53 55 88 85 34 52 60 83 81 400 ч/млн 0 0 0 0 0 0 2 56 71 80 0 4 33 75 84 0 8 31 64 77 0 14 44 60 86 0 7 41 68 82 400 ч/млн 5 3 4 12 6 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн ССS-2 7 днів після обробки 0 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн ССS-2 4 дні після обробки 0 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн ССS-2 0 днів після обробки 0 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн ССS-1 7 днів після обробки 0 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн ССS-1 4 дні після обробки 400 ч/млн 39 51 70 73 84 44 48 64 85 78 36 57 61 66 81 40 52 76 79 75 40 52 68 76 80 400 ч/млн 22 25 31 27 26 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн 46 71 75 84 91 51 63 71 72 87 55 58 67 81 83 58 62 70 75 89 53 64 71 78 88 16 UA 106980 C2 Продовження таблиці 7 ССS-3 0 днів після обробки 0 0 0 0 0 15 76 85 0 1 22 71 93 0 5 31 59 90 0 2 25 33 87 0 2 23 60 89 400 ч/млн 6 3 5 2 4 31 43 54 72 84 36 49 61 66 86 27 51 55 69 75 12 56 64 63 89 27 50 59 68 84 400 ч/млн 31 20 24 27 26 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн 5 0 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн ССS-3 7 днів після обробки 0 200 ч/млн 100 ч/млн 50 ч/млн 25 ч/млн 12,5 ч/млн ССS-3 4 днів після обробки 400 ч/млн 51 61 63 77 81 49 58 76 75 84 43 74 59 69 77 38 69 67 71 87 45 66 66 73 82 Дані тестування складів на бавовняній тлі показані в таблиці 7. Зведення значень LC50, визначених для LAPHEG, наведене нижче в таблиці 5. Данні реєстрували відразу після обробки, а також через 4 і 7 днів після обробки складами. Таблиця 5 Значення LC50 (в ч/млн), одержані при вимірюванні здатності різних нових складів на основі мікрокапсул і контрольних складів хлорпірифосу регулювати чисельність малої совки (LAPHEG). Значення LC50 при регулюванні чисельності малої совки (LAPHEG) Склади Pyrinex ME Lorsban 4E CCS-0 CCS-1 CCS-2 CCS-3 10 15 20 0 день 681,66 529,43 441,46 353,55 379,99 299,58 4 день 668,39 716,02 572,1 367,53 541,41 542,41 7 день 730,82 874,6 1469,26 376,11 656,33 728,15 Ці дані представлені в графічному вигляді на фіг. 1. Lorsban 4E не так активний в момент обробки, як експериментальні склади на основі мікрокапсул, і його активність продовжує зменшуватися згодом. Активність Pyrinex практично не змінюється з плином часу, причому склад демонструє ще меншу вихідну активність, ніж Lorsban 4E. Значення для складу на основі мікрокапсул CCS-0 (3 мікрони, 5 нм) раптово зростають після 4 DAT, навіть не дивлячись на те, що цей склад демонструє більш високу активність, ніж Lorsban 4E в 0 і 4 днів після обробки. Представлені дані показують, що склади хлорпірифосу на основі мікрокапсул CCS-1 і CCS-2 більш активні, ніж контрольний концентрат, що емульгується. Склад CCS-1 (розмір частинок 3 мікрони, товщина стінки 10 нм) продемонстрував відмінну початкову активність проти таких комах, як LAPHEG, причому ця активність зберігалася протягом всіх 7 днів тесту. Склади CCS-2 (розмір частинок 6 мікрон, товщина стінки 5 нм) і CCS-3 (6 мікрон, 10 нм) показали схожу зміну активності згодом, причому, як і у випадку 3-мікронних капсул, більш висока вихідна активність була виявлена у капсул з більш товстими стінками. Ці результати здаються правдоподібними, оскільки в цьому тесті здійснювалася оцінка токсичності хлорпірифосу проти гризучих шкідників. 17 UA 106980 C2 Таблиця 6 Визначення інсектицидної активності різних складів хлорпірифосу при тестуванні на рослинах перця, інфікованих малою совкою (LAPHEG) № експерименту 13 14 15 16 17 18 19 20 21 5 10 Склад Lorsban 4E Lorsban 4E Lorsban 4E Lorsban 4E CCS-4 CCS-4 CCS-4 CCS-4 без обробки К-ть хлорпірифосу ч/млн 1000 500 250 125 1000 500 250 125 0 день % від контролю 100 100 100 100 100 100 100 100 0 2 день % від контролю 100 100 92 75 100 100 100 63 0 5 день % від контролю 100 29 13 0 100 100 75 17 0 8 день % від контролю 13 0 0 0 100 21 0 0 0 Будь-яке інкапсулювання хлорпірифосу, яке уповільнює його випарування, повинно забезпечити більш тривалу дію, доти, поки капсула вивільняє діючу речовину, при поїданні її личинкою. Більш висока вихідна активність експериментальних капсул передбачає наявність значної втрати хлорпірифосу при розпиленні складу Lorsban 4E, за той час, поки рослини залишають висихати до відбору зразків. У той самий час менша активність складу Pyrinex дозволяє передбачити, що хлорпірифос в цих капсулах не має таку ж біодоступність, як хлорпірифос в капсулах експериментальних складів. Одержані дані з біологічної активності проти не гризучих шкідників, а саме бавовняної тлі (APHIGO), показані в таблиці 7. Значення LD50, обчислені з цих даних, показані в таблиці 8. Таблиця 8 Значення LC50 (ч/млн), одержані внаслідок вимірювання здатності різних нових складів на основі мікрокапсул і контрольних складів хлорпірифосу регулювати чисельність бавовняної тлі (APHIGO). Дані реєстрували відразу після обробки, а також через 4 і 7 днів після обробки складами Склади CCS-0 CCS-1 CCS-2 CCS-3 Pyrinex ME Lorsban 4E 15 20 25 Обчислені значення LC50 (ч/млн) 0 день 4 день 20,54 40,30 28,65 65,06 39,98 101,12 34,51 76,61 172,50 120,33 34,93 103,77 7 день 95,71 138,16 209,7 185,64 231,65 255,27 І фіг. 2 являє собою графік залежності цих значень LC 50 від часу після обробки (DAT). Боротьба з тлею є досить складною задачею для більшості складів на основі капсул, оскільки основним шляхом дії інсектициду на цих шкідників є контакт з хлорпірифосом, а не попадання його в травний тракт. На початку даного дослідження тлю безпосередньо обприскували складами, чекаючи, що інкапсульовані композиції не будуть так само активні, як емульговані концентрати. Несподівано виявилося, що відразу після обробки експериментальні склади на основі капсул забезпечують рівну або кращу ефективність в порівнянні з Lorsban 4E, при кращій ефективності з плином часу. Ряд досліджених складів від кращого до гіршого виглядав таким чином: CCS-0>CCS-1>CCS-3>CCS-2=L4E. Капсули розміром 3 мікрони перевершували мікрокапсули розміром 6 мікрон, і мікрокапсули з більш тонкими стінками були ефективніші мікрокапсул з більш товстими стінками. Pyrinex в цьому тесті показав низьку ефективність, як і можна було чекати для складу на основі звичайних капсул. Несподіваний результат полягав в тому, що склади на основі мікрокапсул CCS-0, CCS-1, CCS-2, CCS-3 продемонстрували прекрасну ефективність проти такого не гризучого шкідника, як бавовняна тля. 18 UA 106980 C2 5 Як показано в таблиці 9, інсектицидна активність різних складів хлорпірифосу була протестована на рослинах гарбуза, інфікованої бавовняною тлею (APHIGO). Представлені в таблиці величини означають проценти від контролю. Як видно з таблиці, регулюванні чисельності бавовняної тлі складом CCS-4 при вмісті хлорпірифосу як 400, так і 100 ч/млн через 7 днів здійснюється краще, ніж складом Lorsban 4E. Таблиця 9 Склад Вміст хлорпірифосу ч/млн Lorsban 4E Lorsban 4E Lorsban 4E CCS-4 CCS-4 CCS-4 Без обробки 10 400 100 25 400 100 25 0 Днів після обробки %від контролю 99 96 83 100 98 92 0 4 Дня після обробки %від контролю 81 56 30 97 72 29 0 4 Днів після обробки %від контролю 41 31 39 98 77 32 0 Досліджували токсикологію мікрокапсульних складів CCS-0 і CCS-1. Токсикологічний показник GL50 складу CCS-0 при пероральному введенні самицям щурів складав приблизно GL50>2000 мг/кг; в той самий час для складу CCS-1 значення LD50 проти самиць щурів складало LD50>5000 мг/кг. Ці мікрокапсули демонстрували також хорошу паралізуючу (нокдаунефект) залишкову активність проти бавовняної тлі (таблиця 12). А також відмінну паралізуючу і залишкову активність проти малої совки (таблиця 3). Залишкова дія була такою ж хорошою, як у складу Lorsban 4E (таблиця 14). 15 Таблиця 12 Значення LC50 (в ч/млн хлорпірифосу), одержані при порівнянні дії різних досліджених складів проти бавовняної тлі (APHIGO Склад хлорпірифосу Lorsban 4E CCS-1 Pyrinex ME 0 днів після обробки 34,93 28,65 172,5 4 дня після обробки 103,77 65,06 120,33 7 днів після обробки 255,27 138,16 231,65 Таблиця 13 Значення LC50 (в ч/млн хлорпірифосу), одержані при порівнянні дії різних досліджених складів проти малої совки (LAPHEG) Склад хлорпірифосу Lorsban 4E CCS-1 Pyrinex ME 0 днів після обробки 529,43 353,55 681,66 4 дня після обробки 716,02 367,53 668,39 7 днів після обробки 874,6 376,11 730,82 Таблиця 14 Періоди напіврозпад залишків, виміряні для різних складів хлорпірифосу Склад хлорпірифосу Період напіврозпад (дні) 2,2 2,2 6,9 Lorsban 4E CCS-1 Pyrinex ME 19 UA 106980 C2 5 Приклад 2 Результати токсикологічних досліджень Смертність Всі тварини вижили внаслідок 14-денного періоду спостереження. Дані за смертністю, одержані при тестуванні токсичності CCS-1 на самицях щурів, представлені в таблиці 10. Таблиця 10 Результати дослідження гострої пероральної токсичності нових мікрокапсул CCS-1 для щурів F344/DUCRL (за методикою підвищення-зниження). Смертність Доза (мг/кг) 2000 5000 10 15 20 25 30 Кількість тварин/дозу 5 3 Кількість померлих тварин 0 0 Прибл. спост. час смерті Смертельних випадків відмічено не було. Клінічні огляди Здійснювали ретельні огляди окремих тварин і клінічні огляди щурів, що одержували вказані дози складу. У одного з п'яти щурів, що одержували дозу 2000 мг/кг, на 9-й день тестування спостерігалося забруднення пахової ділянки сечею. У інших чотирьох тварин протягом всього дослідження не було зафіксовано клінічних порушень. У двох з трьох тварин, що одержували 5000 мг/кг, спостерігалося забруднення навколо очей і забруднення пахової ділянки сечею, яке закінчилося на 4-й день дослідження. Третя тварина не мала клінічних ознак відхилень протягом всього дослідження. Маса тіла Реєстрували дані про середню і індивідуальну масу тіла тварин. По відношенню до вихідної маси тіла, два щури, які одержували дозу 5000 мг/кг, втратили масу на 2-й день тестування, але набрали масу в інший час дослідження. Всі інші тварини, що одержували 2000 або 5000 мг/кг, набирали масу тіла протягом всього дослідження. Відчутні вияви патології були відсутні. Висновки з токсикологічних досліджень В умовах проведеного дослідження, значення LD50 при гострому пероральному отруєнні самиць щурів Fisher 344 для препарату CCS-1 складали приблизно більше 5000 мг/кг. Див. таблицю 11. Склади хлорпірифосу на основі мікрокапсул, розкриті в даному винаході, мали значення токсичності LD50 для самиць щурів вище ніж приблизно 2500, і високу паралізуючу активність проти двох поширених видів шкідників рослин. Не обмежуючись будь-якою теорією або конкретним поясненням, ці результати узгоджуються з тим, що мікрокапсули мають найбільш вигідний розмір і товщину стінки. Приймаючи до уваги, що можна одержати широкий діапазон можливих розмірів і товщину стінок мікрокапсул, можна вважати успіхом, що були одержані композиції за даним винаходом, які демонструють такі сприятливі біологічні характеристики. Таблиця 11 Дані з пероральної токсичності, одержані при порівнянні дії різних складів хлорпірифосу на щурах Склад хлорпірифосу LD50 (мг/кг) 300 >5000 Lorsban 4E CCS-1 35 40 Хоча даний винахід був детально викладений і проілюстрований за допомогою креслень і попереднього опису, цей матеріал потрібно вважати ілюстративним і таким, що не носить обмежуючого характеру, розуміючи, що були продемонстровані і описані тільки переважні варіанти здійснення винаходу, і що бажане одержання патентного захисту для всіх змін і модифікацій, які відповідають суті винаходу. Рівним чином, хоча даний винахід був проілюстрований із залученням конкретних прикладів, теоретичних аргументів, розрахунків і ілюстрацій, ці ілюстрації і супроводжуюче їх обговорення не треба тлумачити, як обмеження обсягу винаходу. Всі згадані в даній заявці патенти, заявки на патенти, а також згадувані тексти, наукові праці, публікації і т.д., включені в заявку у всій їх повноті за допомогою посилань. 20 UA 106980 C2 ФОРМУЛА ВИНАХОДУ 5 10 15 20 25 30 35 40 45 50 55 60 1. Пестицидна композиція, яка містить: фосфорорганічний пестицид; і полімер, який утворює стінку капсули, яка щонайменше частково інкапсулює фосфорорганічний пестицид, утворюючи мікрокапсулу, де стінка має середню товщину від приблизно 5 нм до приблизно 25 нм, де вказана мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон, де фосфорорганічний пестицид являє собою хлорпірифос, і мікрокапсула містить від приблизно 15 мас. % до приблизно 35 мас. % хлорпірифосу, де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення. 2. Пестицидна композиція за п. 1, де стінка капсули має середню товщину від приблизно 8 нм до приблизно 12 нм, де вказана мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення. 3. Пестицидна композиція за п. 1, де стінка капсули утворена міжфазною поліконденсацією: щонайменше одного маслорозчинного мономера, вибраного з групи, яка складається з: діізоціанатів, поліізоціанатів, хлорангідридів двоосновних кислот, хлорангідридів багатоосновних кислот, сульфонілхлоридів і хлорформіатів; і щонайменше одного водорозчинного мономера, вибраного з групи, яка складається з: діамінів, поліамінів, водорозчинних діолів і водорозчинних поліолів. 4. Пестицидна композиція за п. 3, де вказана композиція демонструє токсичність проти самиць щурів більше ніж приблизно 5000 мг/кг, і LC50 при регулюванні чисельності бавовняної тлі відразу після внесення менше ніж приблизно 30 ч./млн хлорпірифосу, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення. 5. Пестицидна композиція за п. 3, де вказана композиція демонструє токсичність проти самиць щурів більше, ніж приблизно 2500 мг/кг, і LC50 при регулюванні чисельності малої совки відразу після внесення менше ніж приблизно 400 ч./млн хлорпірифосу, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення. 6. Спосіб одержання мікрокапсул, що включає стадії: одержання фосфорорганічного інсектициду і щонайменше одного мономера; змішування фосфорорганічного інсектициду і щонайменше одного мономера; і формування мікрокапсул, де мономер утворює полімер, з якого формується стінка, причому ця стінка щонайменше частково оточує порцію інсектициду, утворюючи вказану мікрокапсулу, де стінка має середню товщину від приблизно 5 нм до приблизно 25 нм, і вказана мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон, де фосфорорганічний пестицид являє собою хлорпірифос, і мікрокапсула містить від приблизно 15 мас. % до приблизно 35 мас. % хлорпірифосу, де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення. 7. Спосіб одержання мікрокапсул за п. 6, де полімер одержують міжфазною поліконденсацією щонайменше одного маслорозчинного мономера, вибраного з групи, яка складається з діізоціанатів, поліізоціанатів, хлорангідридів двоосновних кислот, хлорангідридів багатоосновних кислот, сульфонілхлоридів і хлорформіатів; і щонайменше одного водорозчинного мономера, вибраного з групи, яка складається з: діамінів, поліамінів, водорозчинних діолів і водорозчинних поліолів. 8. Спосіб одержання мікрокапсул за п. 7, де стінка капсули має середню товщину від приблизно 8 нм до приблизно 12 нм, причому вказана мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення. 9. Спосіб регулювання чисельності комах, що включає стадії: одержання інсектицидної композиції, що складається з мікрокапсул, де мікрокапсули містять: фосфорорганічний інсектицид; і полімер, де полімер утворює стінку, яка щонайменше частково інкапсулює фосфорорганічний пестицид з утворенням мікрокапсули, причому стінка має середню товщину від приблизно 5 нм до приблизно 25 нм, і середній діаметр вказаної мікрокапсули знаходиться в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон; і нанесення вказаного інкапсульованого інсектициду на популяцію комах або на ділянку, розташовану в безпосередній близькості від популяції комах, де фосфорорганічний пестицид являє собою хлорпірифос, і мікрокапсула містить від приблизно 15 мас. % до приблизно 35 мас. % хлорпірифосу, 21 UA 106980 C2 5 10 15 20 де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення. 10. Спосіб регулювання чисельності комах за п. 9, де полімер, що утворює вказану стінку, одержують міжфазною поліконденсацією: щонайменше одного маслорозчинного мономера, вибраного з групи, яка складається з діізоціанатів, поліізоціанатів, хлорангідридів двоосновних кислот, хлорангідридів багатоосновних кислот, сульфонілхлоридів і хлорформіатів; і щонайменше одного водорозчинного мономера, вибраного з групи, яка складається з: діамінів, поліамінів, водорозчинних діолів і водорозчинних поліолів. 11. Спосіб регулювання чисельності комах за п. 9, де стінка має середню товщину від приблизно 8 нм до приблизно 12 нм, причому вказана мікрокапсула має середній діаметр в діапазоні від приблизно 2 мікрон до приблизно 6 мікрон, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення. 12. Спосіб регулювання чисельності комах за п. 10, де вказана композиція демонструє токсичність проти самиць щурів більше, ніж приблизно 5000 мг/кг, і значення LC 50 при регулюванні чисельності бавовняної тлі відразу після нанесення менше ніж приблизно 30 ч./млн хлорпірифосу, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення. 13. Спосіб регулювання чисельності комах за п. 10, де вказана композиція демонструє токсичність проти самиць щурів більше ніж приблизно 2500 мг/кг, і значення LC50 при регулюванні чисельності малої совки відразу після нанесення менше, ніж приблизно 400 ч./млн хлорпірифосу, і де термін ″приблизно″ має на увазі плюс або мінус 10 % від вказаного значення. 22 UA 106980 C2 Комп’ютерна верстка М. Шамоніна Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 23
ДивитисяДодаткова інформація
Автори англійськоюWilson, Stephen, Boucher, Raymond
Автори російськоюУилсон Стефен
МПК / Мітки
МПК: A01N 57/00, A01N 25/28, A01N 57/16, A01P 7/00
Мітки: композиції, інсектицидні, мікроінкапсульовані
Код посилання
<a href="https://ua.patents.su/25-106980-mikroinkapsulovani-insekticidni-kompozici.html" target="_blank" rel="follow" title="База патентів України">Мікроінкапсульовані інсектицидні композиції</a>
Попередній патент: Система обробки для нагріву їжі, спосіб приготування, висушування або консервації харчового об’єкта та спосіб обробки харчового об’єкта
Наступний патент: Мікроінкапсульований інсектицид з підвищеною залишковою активністю
Випадковий патент: Ущільнення сальникового типу для обертового вала