Піридазинова сполука, її застосування, агент та спосіб контролювання захворювання рослин, а також проміжна сполука
Формула / Реферат
1. Піридазинова сполука формули (1):
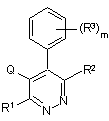 , (1)
, (1)
де
R1 представляє атом хлору, атом брому, С1-С4 алкільну групу або С1-С4 алкоксигрупу,
R2 представляє С1-С4 алкільну групу,
R3 представляє атом галогену, нітрогрупу, ціаногрупу, С1-С4 алкільну групу, необов'язково заміщену принаймні одним атомом галогену, С1-С4 алкоксигрупу, необов'язково заміщену принаймні одним атомом галогену або С1-С4 алкілтіогрупу, необов'язково заміщену принаймні одним атомом галогену,
m представляє ціле число 0 - 5, і коли m є ціле число 2 або більше, R3 є разом однаковими або різними,
Q представляє 6-членну ароматичну гетероциклічну групу, що має принаймні один атом азоту як атом кільця, і ця ароматична гетероциклічна група необов'язково заміщена принаймні одним замісником, що вибраний з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи, необов'язково заміщені принаймні одним атомом галогену, і С1-С4 алкоксигрупи, необов'язково заміщені принаймні одним атомом галогену.
2. Піридазинова сполука за п. 1, де у формулі (1) Q є ароматична гетероциклічна група, що вибрана з групи, яка містить піридильну групу, піридазинільну групу, піримідинільну групу і піразинільну групу, і ця ароматична гетероциклічна група необов'язково заміщена принаймні одним замісником, що вибраний з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи, необов'язково заміщені принаймні одним атомом галогену, і С1-С4 алкоксигрупи, необов'язково заміщені принаймні одним атомом галогену.
3. Піридазинова сполука за п. 1, де у формулі (1) Q є ароматична гетероциклічна група, що вибрана з групи, яка містить 2-піридильну групу, 3-піридазинільну групу, 2-піримідинільну групу, 4-піримідинільну групу і 2-піразинільну групу, і ця ароматична гетероциклічна група необов'язково заміщена принаймні одним замісником, що вибраний з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи, необов'язково заміщені принаймні одним атомом галогену, і С1-С4 алкоксигрупи, необов'язково заміщені принаймні одним атомом галогену.
4. Піридазинова сполука за п. 1, де у формулі (1) Q є ароматична гетероциклічна група, що вибрана з групи, яка містить 2-піридильну групу, 2-піримідинільну групу і 4-піримідинільну групу, і ця ароматична гетероциклічна група необов'язково заміщена принаймні одним замісником, що вибраний з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи, необов'язково заміщені принаймні одним атомом галогену, і С1-С4 алкоксигрупи, необов'язково заміщені принаймні одним атомом галогену.
5. Піридазинова сполука за п. 1, де у формулі (1) Q є 2-піридильна група, і ця піридильна група необов'язково заміщена принаймні одним замісником, що вибраний з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи, необов'язково заміщені принаймні одним атомом галогену, і С1-С4 алкоксигрупи, необов'язково заміщені принаймні одним атомом галогену.
6. Піридазинова сполука за п. 1, де у формулі (1) m є 1 або 2.
7. Піридазинова сполука за п. 1, де у формулі (1) R1 є атом хлору, атом брому або метильна група і R2 є метильна група.
8. Агент для контролювання захворювання рослини, що містить як активний інгредієнт піридазинову сполуку за п. 1.
9. Спосіб контролювання захворювання рослини, що включає стадію нанесення ефективної кількості піридазинової сполуки за п. 1 на рослини або ґрунти, на яких вирощують рослину.
10. Застосування піридазинової сполуки за п. 1 для контролювання захворювань рослин.
11. Сполука формули (2):
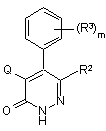 , (2)
, (2)
де
R2 представляє С1-С4 алкільну групу,
R3 представляє атом галогену, нітрогрупу, ціаногрупу, С1-С4 алкільну групу, необов'язково заміщену принаймні одним атомом галогену, С1-С4 алкоксигрупу, необов'язково заміщену принаймні одним атомом галогену, або С1-С4 алкілтіогрупу, необов'язково заміщену принаймні одним атомом галогену,
m представляє ціле число 0 - 5, і коли m є ціле число 2 або більше, R3 є разом однаковими або різними,
Q представляє 6-членну ароматичну гетероциклічну групу, що має принаймні один атом азоту як атом кільця, і ця ароматична гетероциклічна група необов'язково заміщена принаймні одним замісником, що вибраний з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи, необов'язково заміщені принаймні одним атомом галогену, і С1-С4 алкоксигрупи, необов'язково заміщені принаймні одним атомом галогену.
Текст
1. Піридазинова сполука формули (1): 2 (19) 1 3 90360 обов'язково заміщені принаймні одним атомом галогену, і С1-С4 алкоксигрупи, необов'язково заміщені принаймні одним атомом галогену. 6. Піридазинова сполука за п.1, де у формулі (1) m є 1 або 2. 7. Піридазинова сполука за п.1, де у формулі (1) R1 є атом хлору, атом брому або метильна група і R2 є метильна група. 8. Агент для контролювання захворювання рослини, що містить як активний інгредієнт піридазинову сполуку за п.1. 9. Спосіб контролювання захворювання рослини, що включає стадію нанесення ефективної кількості піридазинової сполуки за п.1 на рослини або ґрунти, на яких вирощують рослину. 10. Застосування піридазинової сполуки за п.1 для контролювання захворювань рослин. 11. Сполука формули (2): (R3) m Q O 4 де R2 представляє С1-С4 алкільну групу, R3 представляє атом галогену, нітрогрупу, ціаногрупу, С1-С4 алкільну групу, необов'язково заміщену принаймні одним атомом галогену, С1-С4 алкоксигрупу, необов'язково заміщену принаймні одним атомом галогену, або С1-С4 алкілтіогрупу, необов'язково заміщену принаймні одним атомом галогену, m представляє ціле число 0 - 5, і коли m є ціле число 2 або більше, R3 є разом однаковими або різними, Q представляє 6-членну ароматичну гетероциклічну групу, що має принаймні один атом азоту як атом кільця, і ця ароматична гетероциклічна група необов'язково заміщена принаймні одним замісником, що вибраний з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи, необов'язково заміщені принаймні одним атомом галогену, і С1-С4 алкоксигрупи, необов'язково заміщені принаймні одним атомом галогену. R2 N H N , (2) Представлений винахід стосується піридазинової сполуки, її застосування і проміжної сполуки для її одержання. Умовно, розробляються сільськогосподарські фунгіциди і було знайдено ряд сполук, що мають фунгіцидну активність. Однак, ці сполуки в деяких випадках не є достатньо ефективними при контролюванні захворювань рослин, і розробляються нові сполуки здатні ефективно контролювати захворювання рослин. Винахідники інтенсивно шукали сполуку, що має відмінну активність з контролю захворювань рослин, і результатом цих досліджень стало створення піридазинової сполуки наступної формули (1), що має відмінну здатність контролювати захворювання рослин, що і призвело до створення представленого винаходу Тобто, представлений винахід є таким як описано в наступних пунктах [1]-[11] [1] Піридазинова сполука формули (1): (1) (де, 1 R представляє атом хлору, атом брому, С1С4 алкільну групу або С1-С4 алкоксигрупу, R2 представляє С1-С4 алкільну групу, R3 представляє атом галогену, нітрогрупу, ціаногрупу, С1-С4 алкільну групу необов'язково заміщену принаймні одним атомом галогену, С1-С4 алкоксигрупу необов'язково заміщену принаймні одним атомом галогену або С1-С4 алкілтіогрупу необов'язково заміщену принаймні одним атомом галогену, m представляє ціле число 0-5, і коли m є ціле число 2 або більше, R3e разом однаковими або різними, Q представляє 6-членну ароматичну гетероциклічну групу, що має принаймні один атом азоту, як атом кільця, і ароматичну гетероциклічну групу необов'язково заміщену принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену.). (тут далі, описується як сполука представленого винаходу.). [2] Піридазинова сполука згідно з [1], де у формулі (1), Q є ароматична гетероциклічна група, що вибирають з групи, яка містить піридильну групу, піридазинільну групу, піримідинільну групу і піразинільну групу, і ароматична гетероциклічна група необов'язково заміщена принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену. [3] Піридазинова сполука згідно з [1], де у формулі (1), Q є ароматична гетероциклічна група, що вибирають з групи, яка містить 2-піридильну групу, 3-піридазинільну групу, 2-піримідинільну групу, 4-піримідинільну групу і 2-піразинільну групу, і ароматична гетероциклічна група необов'яз 5 90360 ково заміщена принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену. [4] Піридазинова сполука згідно з [1], де у формулі (1), Q є ароматична гетероциклічна група, що вибирають з групи, яка містить 2-піридильну групу, 2-піримідинільну групу і 4-піримідинільну групу, і ароматична гетероциклічна група необов'язково заміщена принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену. [5] Піридазинова сполука згідно з [1], де у формулі (1), Q є 2-піридильна група, і піридильна група необов'язково заміщена принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену. [6] Піридазинова сполука згідно з будь-яким одним з [1] - [5], де у формулі (1), m є 1 або 2. [7] Піридазинова сполука згідно з будь-яким одним з [1] - [6], де у формулі (1), R1 є атом хлору, атом брому або метильна група і R2 є метильна група. [8] Агент для контролю захворювання рослини, що містить піридазинову сполуку, як описано з будь-якого одному з [1] - [7], як активний інгредієнт. [9] Спосіб контролю захворювання рослини, що включає стадію нанесення ефективної кількості піридазинової сполуки, як описано з будь-якого одному з [1] - [7], на рослини або ґрунт, на якому ростуть рослини. [10] Застосування піридазинової сполуки, як описано з будь-якого одному з [1] - [7], для контролю захворювань рослин. [11] Сполука формули (2) (2) (де, R2 представляє С1-С4 алкільну групу, R3 представляє атом галогену, нітрогрупу, ціаногрупу, С1-С4 алкільну групу необов'язково заміщену принаймні одним атомом галогену, С1-С4 алкоксигрупу необов'язково заміщену принаймні одним атомом галогену або С1-С4 алкілтіогрупу необов'язково заміщену принаймні одним атомом галогену, m представляє ціле число 0 - 5, і коли m є ціле число 2 або більше, R3e разом однаковими або різними, 6 Q представляє 6-членну ароматичну гетероциклічну групу, що має принаймні один атом азоту, як атом кільця, і ароматичну гетероциклічну групу необов'язково заміщену принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену.). Далі описуються замісники на сполуках представленого винаходу. В представленому винаході, як R1, R2, R3 і Q згадуються наступні групи. Прикладами С1-С4 алкоксигрупи представленої R1 є метоксигрупа і етоксигрупа. Прикладами С1-С4 алкільної групи представленої R2 є метильна група і етильна група. Прикладами С1-С4 алкільної групи необов'язково заміщеної принаймні одним атомом галогену представленої R3 є метильна група, етильна група, ізопропільна група, трет-бутильна група, трифторметильна група, дифторметильна група і фторметильна група. Прикладами С1-С4 алкоксигрупи необов'язково заміщеної принаймні одним атомом галогену представленої R3 є метоксигрупа, етоксигрупа, ізопропоксигрупа, трифторметоксигрупа, дифторметоксигрупа, фторметоксигрупа, хлордифторметоксигрупа, бромдифторметоксигрупа, 1,1,2,2тетрафторетоксигрупа і 2,2,2-трифторетоксигрупа. Прикладами С1-С4 алкілтіогрупи необов'язково заміщеної принаймні одним атомом галогену представленої R3 є метилтіогрупа, етилтіогрупа, трифторметилтіогрупа і 1,1,2,2тетрафторетилтіогрупа. Атомом галогену представленим R3 є атом фтору, атом хлору, атом брому і атом йоду. Прикладами 6-членної ароматичної гетероциклічної групи, що має принаймні один атом азоту, як атом кільця, є піридильна група, піридазинільна група, піримідинільна група і піразинільна група. Ілюстрацією втілення сполуки представленого винаходу є сполука, в якій з'єднані атом сусідній до атому азоту, як атом кільця, 6-членної ароматичної гетероциклічної групи представленої Q і атом вуглецю піридазинового кільця у формулі (1). Прикладами 6-членної ароматичної гетероциклічної групи, що має принаймні один атом азоту, як атом кільця, представленої Q в цьому втіленні є 2піридильна група, 3-піридазинільна група, 2піримідинільна група, 4-піримідинільна групу і 2піразинільна група. 6-членна ароматична гетероциклічна група, що має принаймні один атом азоту, як атом кільця, представлена Q необов'язково заміщена принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів (атом фтору, атом хлору, атом брому і атом йоду), нітрогрупу, ціаногрупу, С1-С4алкільні групи необов'язково заміщені принаймні одним атомом галогену (наприклад, метильна група, етильна група, трифторметильна група, дифторметильна група і фторметильна група) і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену (наприклад, метоксигрупа, етоксигрупа, трифторметоксигрупа, диф 7 торметоксигрупа і фторметоксигрупа). Такою 6членною ароматично гетероциклічною групою, що має принаймні один атом азоту, як атом кільця, наприклад, згадують наступні групи. 2-піридильні групи необов'язково заміщені принаймні одним замісником з групи, що містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену, такі як 2-піридильну групу, 3-метил-2піридильну групу, 3-хлор-2-піридильну групу, 3фтор-2-піридильну групу, 3-трифторметил-2піридильну групу, 3-метокси-2-піридильну групу, 3нітро-2-піридильну групу, 3-ціано-2-піридильну групу, 5-метил-2-піридильну групу, 5-хлор-2піридильну групу, 5-фтор-2-піридильну групу, 5трифторметил-2-піридильну групу, 5-метокси-2піридильну групу, 4-метил-2-піридильну групу, 4хлор-2-піридильну групу, 4-фтор-2-піридильну групу, 4-трифторметил-2-піридильну групу, 4метокси-2-піридильну групу, 6-метил-2-піридильну групу, 6-хлор-2-піридильну групу, 6-фтор-2піридильну групу, 6-трифторметил-2-піридильну групу, 6-метокси-2-піридильну групу, 3,5-диметил2-піридильну групу, 3,5-дихлор-2-піридильну групу, 3,5-дифтор-2-піридильну групу, 3,6-диметил-2піридильну групу, 3,6-дихлор-2-піридильну групу, 3,6-дифтор-2-піридильну групу, 6-хлор-3трифторметил-2-піридильну групу, 6-хлор-5трифторметил-2-піридильну групу, 3-хлор-5трифторметил-2-піридильну групу, 3-хлор-5метокси-2-піридильну групу, 3-нітро-5-метокси-2піридильну групу, 3-ціано-5-метокси-2-піридильну групу, 5-метокси-3-метил-2-піридильну групу, 3хлор-5-нітро-2-піридильну групу, 3,5,6-трихлор-2піридильну групу, 3,5,6-трифтор-2-піридил групу і т.і.; 3-піридазинільні групи необов'язково заміщені принаймні одним замісником з групи, що містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену, такі як 3-піридазинільну групу, 4-метил-3піридазинільну групу, 4-трифторметил-3піридазинільну групу, 4-ціано-3-піридазинільну групу, 4-нітро-3-піридазинільну групу, 4-метокси-3піридазинільну групу, 4-хлор-3-піридазинільну групу і т.і.; 2-піримідинільні групи необов'язково заміщені принаймні одним замісником з групи, що містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену, такі як 2-піримщинільну групу, 5-метил-2піримідинільну групу, 5-метокси-2-піримідинільну групу, 5-хлор-2-піримідинільну групу, 5-фтор-2піримідинільну групу, 5-нітро-2-піримідинільну групу, 5-ціано-2-піримідинільну групу, 5трифторметил-2-піримідинільну групу, 4,6диметил-2-піримідинільну групу, 4,6-диметокси-2піримідинільну групу, 4,6-біс(трифторметил)-2піримідинільну групу, 4-метокси-6-метил-2 90360 8 піримідинільну групу, 4-метил-2-піримідинільну групу, 4-метокси-2-піримідинільну групу, 4-хлор-2піримідинільну групу, 4-фтор-2-піримідинільну групу і т.і.; 4-піримідинільні групи необов'язково заміщені принаймні одним замісником з групи, що містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену, такі як 4-піримідинільну групу, 5-метил-4піримідинільну групу, 5-метокси-4-піримідинільну групу, 5-нітро-4-піримідинільну групу, 5-ціано-4піримідинільну групу, 5-трифторметил-4піримідинільну групу, 5-хлор-4-піримідинільну групу, 5-фтор-4-піримідинільну групу, 2,5-диметил-4піримідинільну групу, 2-метил-4-піримідинільну групу, 2-метокси-4-піримідинільну групу, 2-хлор-4піримідинільну групу, 5-хлор-6-метил-4піримідинільну групу, 5-хлор-2-метил-4піримідинільну групу, 5-фтор-6-метил-4піримідинільну групу, 5-фтор-2-метил-4піримідинільну групу, 2-хлор-6-метил-4піримідинільну групу і т.і.; 2-піразинільні групи необов'язково заміщені принаймні одним замісником з групи, що містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену, такі як 2-піразинільну групу, 3-метил-2піразинільну групу, 3-метокси-2-піразинільну групу, 3-трифторметилметил-2-піразинільну групу, 3ціано-2-піразинільну групу, 3-нітро-2-піразинільну групу, 3-хлор-2-піразинільну групу і т.і.. Прикладами фенільної групи заміщеної (R3)m є фенільна група; 4-метилфенільна група, 3метилфенільна група, 2-метилфенільна група, 4етилфенільна група, 4-ізопропілфенільна група, 4трет-бутилфенільна група, 4(трифторметил)фенільна група, 3(трифторметил)фенільна група, 4-хлорфенільна група, 3-хлорфенільна група, 2-хлорфенільна група, 4-фторфенільна група, 3-фторфенільна група, 2-фторфенільна група, 4-метоксифенільна група, 3-метоксифенільна група, 4-етоксифенільна група, 4-(трифторметокси)фенільна група, 4нітрофенільна група, 4-ціанофенільна група, 4(метилтіо)фенільна група і 4(трифторметилтіо)фенільна група в якій m є 1; і 2,4-диметилфенільна група, 2,5-диметилфенільна група, 3,4-диметилфенільна група, 2,4дихлорфенільна група, 2,5-дихлорфенільна група, 3,4-дихлорфенільна група, 2,3-дифторфенільна група, 2,4-дифторфенільна група, 2,5дифторфенільна група, 3,4-дифторфенільна група, 3,5-дифторфенільна група, 4-хлор-2фторфенільна група, 2,4-диметоксифенільна група і 3,4-диметоксифенільна група, в якій m є 2. Як втілення сполуки представленого винаходу, наприклад, серед сполук представленого винаходу згадуються наступні піридазинові сполуки. Піридазинові сполуки, де R1 є атом хлору або атом брому, у формулі (1); 9 Піридазинові сполуки, де R1 є С1-С4 алкільна група, у формулі (1); Піридазинові сполуки, де R1 є С1-С4 алкоксигрупа, у формулі (1); 1 2 Піридазинові сполуки, де R є атом хлору і R є метильна група, у формулі (1); Піридазинові сполуки, де R1 є метокси група і 2 R є метильна група, у формулі (1); Піридазинові сполуки, де R1 є метильна група і 2 R є метильна група, у формулі (1); Піридазинові сполуки, де R3 є С1-С4 алкільна група необов'язково заміщена принаймні одним атомом галогену, С1-С4 алкоксигрупа необов'язково заміщена принаймні одним атомом галогену, або атом галогену, у формулі (1); Піридазинові сполуки, де R3 є С1-С4 алкільна група або атом галогену, у формулі (1); Піридазинові сполуки, де R3 є метильна група, трифторметильна група, атом хлору, атом фтору або метоксигрупа, у формулі (1); Піридазинові сполуки, де R3 є метильна група, атом хлору або атом фтору, у формулі (1); Піридазинові сполуки, де m є 1 або 2, у формулі (1); Піридазинові сполуки, де m є 1, у формулі (1); Піридазинові сполуки, де гл є 2, у формулі (1); Піридазинові сполуки, де m є 1 і R3 є замісником в 4-положенні бензольного кільця, у формулі (1); Піридазинові сполуки, де m є 1, R3 є атом галогену, С1-С4 алкільна група необов'язково заміщена атомом галогену, або С1-С4 алкоксигрупа необов'язково заміщена принаймні одним атомом галогену, і R3 є замісником в 4-положенні бензольного кільця, у формулі (1); Піридазинові сполуки, де m є 1, R3 є атом галогену або С1-С4 алкільна група необов'язково заміщена принаймні одним атомом галогену, і R3 є замісником в 4-положенні бензольного кільця, у формулі (1); 3 Піридазинові сполуки, де m є 1, R є атом га3 логену або С1-С4 алкільна група, і R є замісником в 4-положенні бензольного кільця, у формулі (1); Піридазинові сполуки, де m є 1, R3 є метильна група, трифторметильна група, атом хлору, атом фтору або метоксигрупа, і R3 є замісником в 4положенні бензольного кільця, у формулі (1); Піридазинові сполуки, де m є 1, R3 є метильна група, атом хлору або атом фтору, і R3 є замісником в 4-положенні бензольного кільця, у формулі (1); Піридазинові сполуки, де Q є ароматична гетероциклічна група, що вибирають з групи, яка містить піридильну групу, піридазинільну групу, піримідинільну групу і піразинільну групу, і ароматична гетероциклічна група необов'язково заміщена принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену, у формулі (1); Піридазинові сполуки, де Q є ароматична гетероциклічна група, що вибирають з групи, яка містить 2-піридильну групу, 3-піридазинільну групу, 90360 10 2-піримідинільну групу, 4-піримідинільну групу і 2піразинільну групу, і ароматична гетероциклічна група необов'язково заміщена принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену, у формулі (1); Піридазинові сполуки, де Q є ароматична гетероциклічна група, що вибирають з групи, яка містить 2-піридильну групу, 2-піримідинільну групу і 4-піримідинільну групу, і ароматична гетероциклічна група необов'язково заміщена принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену, у формулі (1), Піридазинові сполуки, де Q є 2-піридильна група, і 2-піридильна група необов'язково заміщена принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену, у формулі (1), Піридазинові сполуки, де Q є 2-піридильна група, і 3-положення 2-піридильної групи є заміщеним атомом галогену, нітрогрупою, ціаногрупою, С1-С4 алкільною групою необов'язково заміщеною принаймні одним атомом галогену або С1С4 алкоксигрупою необов'язково заміщеною принаймні одним атомом галогену, у формулі (1); Піридазинові сполуки, де Q є 2-піридильна група, і 3-положення 2-піридильної групи є заміщеним атомом галогену або С1-С4 алкільною групою необов'язково заміщеною принаймні одним атомом галогену, у формулі (1); Піридазинові сполуки, де Q є 2-піридильна група, і 3-положення 2-піридильної групи є заміщеним атомом галогену, нітрогрупою, ціаногрупою, метильною групою, трифторметильною групою або метоксигрупою, і інші положення 2піридильної групи є необов'язково заміщеними принаймні одним замісником з групи, що містить атоми галогенів, нітрогрупу, ціаногрупу, метильну групу, трифторметильну групу і метоксигрупу, у формулі (1); Піридазинові сполуки, де Q є 2-піридильна група, 3-положення 2-піридильної групи є заміщеним атомом галогену або метильною групою, і інші положення 2-піридильної групи є необов'язково заміщеними принаймні одним замісником з групи, що містить атоми галогенів, нітрогрупу, ціаногрупу, метальну групу, трифторметильну групу і метоксигрупу, у формулі (1); Піридазинові сполуки, де Q є 2-піримідинільна група, і 2-піримідинільна група необов'язково заміщена принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1 11 С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену, у формулі (1); Піридазинові сполуки, де Q є 4-піримідинільна група, і 4-піримідинільна група необов'язково заміщена принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену, у формулі (1); Піридазинові сполуки, де Q є 4-піримідинільна група, і 5-положення 4-піримідинільної групи є заміщеним атомом галогену, нітрогрупою, ціаногрупою, С1-С4 алюльною групою необов'язково заміщеною принаймні одним атомом галогену або С1С4 алкоксигрупою необов'язково заміщеною принаймні одним атомом галогену, у формулі (1); Піридазинові сполуки, де Q є 4-піримідинільна група, і 5-положення 4-піримідинільної групи є заміщеним атомом галогену або С1-С4 алкільною групою необов'язково заміщеною принаймні одним атомом галогену, у формулі (1); Піридазинові сполуки, де Q є 4-піримідинільна група, 5-положення 4-піримідинільної групи є заміщеним атомом галогену, нітрогрупою, ціаногрупою, метальною групою, трифторметильною групою або метоксигрупою, і інші положення 4піримідинільноі групи є необов'язково заміщеними принаймні одним замісником з групи, що містить атоми галогенів, нітрогрупу, ціаногрупу, метильну групу, трифторметильну групу і метоксигрупу, у формулі (1); Піридазинові сполуки, де Q є 4-піримідинільна група, 5-положення 4-піримідинільної групи є заміщеним атомом галогену або метальною групою, і інші положення 4-піримідинільної групи є необов'язково заміщеними принаймні одним замісником з групи, що містить атоми галогенів, нітрогрупу, ціаногрупу, метильну групу, трифторметильну групу і метоксигрупу, у формулі (1). Далі описується спосіб одержання сполуки представленого винаходу. Сполуку представленого винаходу можна одержати наступним шляхом, наприклад, (Спосіб одержання 1), (Спосіб одержання 2), (Спосіб одержання 3) або (Спосіб одержання 4). (Спосіб одержання 1) Сполуки формули (1-1), де R1 є атом хлору або атом брому, з ряду сполук представленого винаходу, можна одержати шляхом взаємодії сполуки формули (2) з галогенувальним агентом. 2 (де, R представляє С1-С4 алкільну групу, R3 представляє атом галогену, нітрогрупу, ціаногрупу, С1-С4 алкільну групу необов'язково заміщену принаймні одним атомом галогену, С1-С4 алкоксигрупу необов'язково заміщену принаймні одним атомом галогену або С1-С4 алкілтіогрупу 90360 12 необов'язково заміщену принаймні одним атомом галогену, m представляє ціле число 0-5, і коли m є ціле число 2 або більше, R3 є разом однаковими або різними, Q представляє 6-членну ароматичну гетероциклічну групу, що має принаймні один атом азоту, як атом кільця, і ароматичну гетероциклічну групу необов'язково заміщену принаймні одним замісником, що вибирають з групи, яка містить атоми галогенів, нітрогрупу, ціаногрупу, С1-С4 алкільні групи необов'язково заміщені принаймні одним атомом галогену і С1-С4 алкоксигрупи необов'язково заміщені принаймні одним атомом галогену. R11 представляє атом хлору або атом брому.). Реакцію проводять у відсутності або присутності розчинника. Прикладами використовуваного в реакції розчинника є вуглеводні, такі як толуол, ксилен і т.і., галогеновані вуглеводні, такі як хлорбензол, дихлорбензол і т.і., і їх суміші. Прикладами використовуваного в реакції галогенувального агента є хлорувальні агенти, такі як оксихлорид фосфору, пентахлорид фосфору і т.і., і бромувальні агенти, такі як оксибромід фосфору, пентабромід фосфору і т.і., також використовуються суміші хлорувальних агентів або бромувальних агентів. Кількість галогенувального агента використовуваного в реакції зазвичай становить від 1 до 100моль на 1моль сполуки формули (2). Температура реакцію зазвичай знаходиться в інтервалі від 20 до 120°С, і час реакції зазвичай знаходиться в інтервалі від 0,1 до 24 годин. Після завершення реакції, наприклад, реакційну суміш концентрують, до одержаного залишку додають воду або водний бікарбонат натрію і потім екстрагують органічним розчинником, і органічний шар піддають переробці, такій як сушіння, концентрування і т.і., виділяючи таким чином сполуку формули (1-1). Виділену сполуку формули (11) також можна ще очистити за допомогою хроматографії, перекристалізації і т.і.. (Спосіб одержання 2) Сполуки формули (1-2), де R1 є С1-С4 алкоксигрупа, з ряду сполук представленого винаходу, можна одержати, наприклад, шляхом взаємодії сполуки формули (1-1) з алкоголятом формули: NaR12 (де, R12 представляє С1-С4 алкоксигрупу) (де, R11, R2, R3, m, Q і R12 мають ті ж самі значення як описано вище.). Реакцію зазвичай проводять в розчиннику. Використовуваними в реакції розчинника є спирти представлені R12 Η , етери, такі як тетрагідрофуран, 1,2-диметоксиетан і т.і., і їх суміші. 13 90360 14 Кількість алкоголяту використовуваного в реакції зазвичай становить від 1 до 20моль на 1моль сполуки формули (1-1). Температура реакцію зазвичай знаходиться в інтервалі від 0 до 120°С, і час реакції зазвичай знаходиться в інтервалі від 1 до 72 годин. Після завершення реакції, наприклад, лор реакційної суміші додають воду і потім екстрагують органічним розчинником, і органічний шар піддають переробці, такій як сушіння, концентрування і т.і., таким чином, можна виділити сполуку формули (1-2) Виділену сполуку формули (1-2) також можна в подальшому очистити за допомогою хроматографії, перекристалізації і т.і.. (Спосіб одержання 3) Сполуки формули (1-3), де R1 є С1-С4 алкільна група, з ряду сполук представленого винаходу, можна одержати за допомогою наступної методики. (де, R2, R3, m і Q мають ті ж самі значення як описано вище, і R13 представляє С1-С4 алкільну групу.). Далі описуються процес (1-а). Сполуку формули (4) можна одержати шляхом взаємодії сполуки формули (3) з гідразином. Реакцію зазвичай проводять в розчиннику. Прикладами використовуваного в реакції розчинника є спирти, такі як метанол, етанол, пропанол, ізопропанол і т.і., етери, такі як тетрагідрофуран, 1,2-диметоксиетан і т.і., і їх суміші. Кількість використовуваного в реакції гідразину зазвичай становить від 1 до 5моль на 1моль сполуки формули (3). Гідразин використовуваний в реакції також може бути гідратом. Температура реакцію зазвичай знаходиться в інтервалі від 0 до 80°С, і час реакції зазвичай знаходиться в інтервалі від 1 до 24 годин. Після завершення реакції, реакційну суміш піддають переробці, такій як концентрування і т.і., таким чином можна виділити сполуку формули (4). Реакційну суміш також можна використати як є в наступному процесі (І-b). Далі описуються процес (І-b). Сполуку представленого винаходу можна одержати шляхом взаємодії сполуки формули (4) з окислювальним агентом. Реакцію зазвичай проводять в розчиннику. Прикладами окислювального агента використовуваного в реакції є оксид платини (РtO2) і оксид олова (РbО2). Прикладами використовуваного в реакції розчинника є спирти, такі як метанол, етанол, пропанол, ізопропанол і т.і., етери, такі як тетрагідрофуран, 1,2-диметоксиетан і т.і., вода, і їх суміші. Кількість окислювального агента використовуваного в реакції зазвичай становить від 1 до 5моль на 1моль сполуки формули (4). Температура реакцію зазвичай знаходиться в інтервалі від 40 до 80°С, і час реакції зазвичай знаходиться в інтервалі від 1 до 48 годин. Після завершення реакції, наприклад, реакційну суміш фільтрують, і одержаний фільтрат піддають переробці, такій як концентрування і т.і., таким чином можна виділити сполуку представленого винаходу. Виділену сполуку представленого винаходу також можна в подальшому очистити за допомогою операцій, таких як хроматографія, перекристалізація і т і.. (Спосіб одержання 4) Сполуки формули (1-3), де R1 є С1-С4 алкільна група, з ряду сполук представленого винаходу, можна одержати шляхом взаємодії сполуки формули (5) з основою. (де, R13, R2, R3, m і Q мають ті ж самі значення як описано вище.). Реакцію зазвичай проводять в розчиннику. Прикладами використовуваного в реакції розчинника є спирти, такі як метанол, етанол, пропанол, ізопропанол, трет-бутанол і т.і., етери, такі як тетрагідрофуран, 1,2-диметоксиетан і т.і., і їх суміші. Прикладами основи використовуваної в реакції є гідроксиди лужних металів, такі як гідроксид калію, гідроксид натрію і т.і.. Кількість основи використовуваної в реакції зазвичай становить від 1 до 2моль на 1моль сполуки формули (5). Температура реакцію зазвичай знаходиться в інтервалі від 0 до 100°С, і час реакції зазвичай знаходиться в інтервалі від 0,1 до 8 годин. Після завершення реакції, наприклад, реакційну суміш змішують з водою, проводять екстрагування органічним розчинником і органічний шар піддають переробці, такій як сушіння, концентрування і т.і., таким чином можна виділити сполуку представленого винаходу. Виділену сполуку представленого винаходу також можна в подальшому очистити за допомогою хроматографії, перекристалізації і т і.. Далі розкривається спосіб одержання проміжної сполуки представленого винаходу як референсний спосіб одержання. 15 (Референсний Спосіб одержання 1) Сполуку формули (2) можна одержати, наприклад, взаємодією сполуки формули (13) з гідразином. (де, R2, R3, m і Q мають ті ж самі значення як описано вище.). Реакцію зазвичай проводять в розчиннику. Прикладами використовуваного в реакції розчинника є спирти, такі як метанол, етанол, пропанол, ізопропанол, бутанол і т.і, етери, такі як тетрагідрофуран, 1,2-диметоксиетан і т.і., і їх суміші. Кількість гідразину використовуваного в реакції зазвичай становить від 1 до 5моль на 1моль сполуки формули (13). Гідразин використовуваний в реакції також може бути гідратом. Температура реакцію зазвичай знаходиться в інтервалі від 0 до 120°С, і час реакції зазвичай знаходиться в інтервалі від 0,2 до 24 годин. Після завершення реакції, проводять обробку, таку як охолодження реакційної суміші з осадженням твердої речовини, яку потім фільтрують, або концентрування реакційної суміші, і т.і., таким чином виділяють сполуку формули (2). Виділену сполуку формули (2) також можна в подальшому очистити за допомогою хроматографії, перекристалізації і т.і.. (Референсний Спосіб одержання 2) Сполуку формули (13) можна одержати, наприклад, згідно з наступною схемою. (де, R2, R3, m і Q мають ті ж самі значення як описано вище.). Спосіб одержання зображений на приведеній вище схемі складається із стадії (іі-а), стадії (ii-b) і стадії (іі-с). Реакцію стадії (іі-а) проводять, наприклад, зміщуючи сполуку формули (14); сполуку формули (15) або її сіль (наприклад, гідрохлорид і т.і.); нециклічний третинний амін, такий як триетиламін, діізопропілетиламін і т.і.; і розчинник. Прикладами використовуваного в реакції розчинника є нітрили, такі як ацетонітрил, пропіонітрил і т.і., етери, такі як тетрагідрофуран, 1,2 90360 16 диметоксиетан і т.і., аміди, такі як Ν,Νдиметилформамід (DMF) і т.і., ароматичні вуглеводні, такі як толуол, ксилен і т.і., і їх суміші. Кількість сполуки формули (15) і нециклічного третинного аміну використовуваного в реакції зазвичай знаходиться у співвідношенні 0,8 до 3моль на 1моль сполуки формули (14). Температура реакцію зазвичай знаходиться в інтервалі від 0 до 50°С, і час реакції зазвичай знаходиться в інтервалі від 1 до 48 годин. Після завершення реакції, наприклад, реакційну суміш змішують з водою, проводять екстракцію органічним розчинником, і органічний шар піддають переробці, такій як сушіння, концентрування і т.і., таким чином виділяють естер формули (16). Після завершення реакції, реакційну суміш також можна використати як ε на наступній стадії (іі-b). Реакцію стадії (іі-b) проводять, наприклад, змішуванням сполуки формули (16); принаймні одного циклічного аміну, що вибирають з групи, яка містить 1,8-діазабіцикло[5.4.0]ундец-7-ен (DBU), 1,5-діазабіцикло[4.3.0]нон-5-ен (DBN) і 1,4діазабіцикло[2.2.2]октан; і, якщо необхідно, розчинника. Прикладами використовуваного в реакції розчинника є нітрили, такі як ацетонітрил, пропіонітрил і т.і., етери, такі як тетрагідрофуран, 1,2диметоксиетан і т.і., аміди, такі як Ν,Νдиметилформамід (DMF) і т.і., ароматичні вуглеводні, такі як толуол, ксилен і т.і., і їх суміші. Кількість циклічного аміну використовуваного у винаході зазвичай становить від 1 до 5моль на 1моль сполуки формули (16). Температура реакцію зазвичай знаходиться в інтервалі від 0 до 50°С, і час реакції зазвичай знаходиться в інтервалі від 1 до 8 годин Після завершення реакції, наприклад, реакційну суміш змішують з водою, проводять екстракцію органічним розчинником, і органічний шар піддають переробці, такій як сушіння, концентрування і т.і., таким чином виділяють сполуку формули (17). Далі, після завершення реакції, реакційну суміш також можна використати як є на наступній стадії (іі-с). Реакцію стадії (іі-с) проводять, наприклад, залишаючи сполуку формули (17) для контакту з киснем. Реакцію зазвичай проводять в розчиннику. Прикладами використовуваного в реакції розчинника є нітрили, такі як ацетонітрил, пропіонітрил і т.і., етери, такі як тетрагідрофуран, 1,2диметоксиетан і т.і., аміди, такі як Ν,Νдиметилформамід (DMF) і т і., ароматичны вуглеводні, такі як толуол, ксилен і т.і., і їх суміші. Киснем використовуваним в реакції може бути кисень сам по собі або газ, що містить кисень, такий як повітря і т.і.. Контактування сполуки формули (17) і кисню проводять, наприклад, барботуючи кисень в розчин сполуки формули (17), або інтенсивно перемішуючи розчин сполуки формули (17) в атмосфері кисню. Температура реакцію зазвичай знаходиться в інтервалі від 0 до 150°С, і час реакції зазвичай знаходиться в інтервалі від 1 до 24 годин. 17 Після завершення реакції, реакційну суміш змішують з розведеною хлорводневою кислотою, проводять екстракцію органічним розчинником, і органічний шар піддають переробці, такій як сушіння, концентрування і т.і., таким чином виділяють сполуку формули (13). Виділену сполуку формули (13) також можна в подальшому очистити за допомогою хроматографії, перекристалізації і т.і. (Референсний Спосіб одержання 3) Сполуку формули (14) можна одержати, наприклад, шляхом взаємодії сполуки формули (18) з бромом. (де, R2, R3 і m мають ті ж самі значення як описано вище.). Реакцію зазвичай проводять в розчиннику. Прикладами використовуваного в реакції розчинника є оцтова кислота. Кількість використовуваного брому зазвичай знаходиться у співвідношення 0,8 до 1,3моль на 1моль сполуки формули (18). Температура реакцію зазвичай знаходиться в інтервалі від -10 до 40°С, і час реакції зазвичай знаходиться в інтервалі від 0,1 до 24 годин. Реакцію можна проводити, наприклад, в присутності каталітичної кількості бромводневої кислоти. Після завершення реакції, наприклад, реакційну суміш концентрують або до реакційної суміші додають воду і екстрагують органічним розчинником, і органічний шар промивають водним розчином гідрокарбонату натрію і водою, і піддають подальшій обробці, такій як сушіння, концентрування і т.і., таким чином виділяють сполуку формули (14). Виділену сполуку формули (14) також можна в подальшому очистити за допомогою хроматографії, перекристалізації і т.і.. (Референсний Спосіб одержання 4) Сполуку формули (3) можна одержати, наприклад, з сполуки формули (22) і сполуки формули (23), згідно з наступною схемою. (де, R13, R2, R3, m, R5 i n мають ті ж самі значення як описано вище.). Стадія (iv-a) 90360 18 Сполуку формули (21) можна одержати шляхом взаємодії сполуки формули (23) і сполуки формули (22). Реакцію проводять в присутності або відсутності розчинника. Використовуваними в реакції розчинника є вуглеводні, такі як толуол, ксилен і т і.. Кількість використовуваної у винаході сполуки формули (23) зазвичай знаходиться в діапазоні від 0,8 до 1,3моль на 1моль сполуки формули (22). Температура реакцію зазвичай знаходиться в інтервалі від 0 до 50°С, і час реакції зазвичай знаходиться в інтервалі від 1 до 48 годин. Після завершення реакції, зазвичай, реакційну суміш концентрують, і зазвичай, залишок використовують як є в реакцію стадії (iv-b). Стадія (iv-b) Сполуку формули (3) можна одержати шляхом взаємодії сполуки формули (21) з кислотою. Реакцію зазвичай проводять в присутності води і розчинника. Прикладами використовуваного в реакції розчинника є спирти, такі як метанол, етанол і т.і., етери, такі як тетрагідрофуран, 1,4-діоксан і т.і,, і їх суміші. Реакцію зазвичай проводять при рН приблизно 2. Прикладами використовуваної кислоти є хлорводнева кислота. Температура реакцію зазвичай знаходиться в інтервалі від 0 до 30°С, і час реакції зазвичай знаходиться в інтервалі від 1 до 48 годин. Після завершення реакції, наприклад, до реакційної суміші додають водний розчин гідрокарбонату натрію, проводять екстракцію органічним розчинником, і органічний шар концентрують, таким чином виділяють сполуку формули (3). Виділену сполуку формули (3) також можна в подальшому очистити перекристалізацією, хроматографією і т.і.. Сполуку формули (22) можна одержати, наприклад, згідно з методикою описаною в J. Org. Chem., 32, pp.213-214 (1967). Сполуку формули (23) можна одержати, наприклад, згідно з методикою описаною в J. Med. Chem., 29, pp.924-939 (1986). (Референсний Спосіб одержання 5) Сполуку формули (5) можна одержати шляхом взаємодії сполуки формули (24) і сполуки формули (25) в присутності кислоти. (де, R13, R2, R3, m і Q мають ті ж самі значення як описано вище.). Реакцію зазвичай проводять в присутності розчинника Прикладами використовуваного в реакції розчинника є ароматичну вуглеводні, такі як толуол, ксилен і т.і.. Прикладами кислоти використовуваної в реакції є органічні сульфонові кислоти, такі як птолуолсульфонова кислота і т.і.. 19 90360 20 Кількість сполуки формули (25) використовуваної в реакції зазвичай знаходиться у співвідношенні від 0,8 до 1,3моль на 1моль сполуки формули (24). Кількість кислоти використовуваної в реакції зазвичай знаходиться у співвідношенні від 0,001 до 0,05моль на 1моль сполуки формули (24). Температура реакцію зазвичай знаходиться в інтервалі від 20 до 120°С, і час реакції зазвичай знаходиться в інтервалі від 1 до 8 годин. Реакцію проводять зазвичай при дегідратуванні використовуючи насадку Діна-Старка. Після завершення реакції, наприклад, (1) реакційну суміш концентрують як є, або (2) реакційну суміш змішують з водним розчином гідрокарбонату натрію, проводять екстракцію органічним розчинником, і органічний шар піддають переробці, такій як сушіння, концентрування і т.і., таким чином виділяють сполуку формули (5). Виділену сполуку формули (5) також можна в подальшому очистити за допомогою операцій, таких як хроматографія, перекристалізації і т.і.. (Референсний Спосіб одержання 6) Сполуку формули (24) можна одержати шляхом взаємодії сполуки формули (26) з гідразином. (де, R2, R3 і m мають ті ж самі значення як описано вище.). Реакцію проводять в присутності розчинника. Прикладами використовуваного в реакції розчинника є спирти, такі як етанол і т.і.. Кількість гідразину використовуваного в реакції зазвичай знаходиться у співвідношенні від 0,8 до 1,3моль на 1моль сполуки формули (26). Гідразин використовуваного в реакції також може бути гідратом. Температура реакцію зазвичай знаходиться в інтервалі від 0 до 80°С, і час реакції зазвичай знаходиться в інтервалі від 1 до 48 годин. Після завершення реакції, реакційну суміш піддають переробці, такій як концентрування і т.і., таким чином виділяють сполуку формули (24) Виділену сполуку формули (24) також можна в подальшому очистити за допомогою хроматографії, перекристалізації і т.і.. Як сполуку формули (26), можна використовувати комерційно доступні сполуки, або сполуки одержані згідно з, наприклад, використовуючи методику описану в J. Org. Chem., 43, pp.2933-2935 (1978) або Synthesis, pp.403-404, (1977). Як сполуку формули (25), можна використати сполуки одержані згідно з, наприклад, методиками описаними в J. Med. Chem., 29, pp.924-939 (1986); J. Med. Chem , 6, pp.205-207 (1963); J. Org. Chem., 43, pp.2286-2288(1978). (Референсний Спосіб одержання 7) Сполуку формули (2) також можна одержати, наприклад, шляхом взаємодії сполуки формули (27) і сполуки формули (24). (де, R2, R3, m і Q мають ті ж самі значення як описано вище, R представляє метильну групу або етильну групу.). Реакцію проводять зазвичай в розчиннику в присутності основи. Прикладами використовуваного в реакції розчинника є етери, такі як метанол, етанол, третбутанол, тетрагідрофуран, 1,2-диметоксиетан, 1,4діоксан і т.і., ароматичні вуглеводні, такі як толуол, ксилен і т.і., аміди, такі як N,Nдиметилформамід(DМР) і т.і., нітрили такі якацетонітрил, пропіонітрил і т.і., і їх суміші. Прикладами основи використовуваної в реакції є метоксид натрію, етоксид натрію, третбутоксид калію, гідрид натрію, 1,8діазабіцикло[5.4.0]ундец-7-ен (DBU), 1,5діазабіцикло[4.3.0]нон-5-ен (DBN), 1,4діазабіцикло[2.2.2]октан і т.і.. Кількість сполуки формули (24) і основи використовуваної в реакції зазвичай знаходиться у співвідношенні від 0,8 до 2моль на 1моль сполуки формули (27). Температура реакцію зазвичай знаходиться в інтервалі від 20 до 120°С, і час реакції зазвичай знаходиться в інтервалі від 1 до 24 годин. Після завершення реакції, (1) до реакційної суміші додають воду, і якщо необхідно, до неї додають кислоту, потім, суміш охолоджують з осадженням твердої речовини, яку потім фільтрують, або (2) реакційну суміш екстрагують органічним розчинником і органічний шар піддають обробці, такій як концентрування і т.і., таким чином виділяють сполуку формули (2). Виділену сполуку формули (2) також можна в подальшому очистити за допомогою хроматографії, перекристалізації і т.і.. Далі показані специфічні приклади сполук представленого винаходу. Піридазин формули (1-а): (1a) 21 90360 Піридазин формули (1-b): (1b) Піридазин формули (1-c): (1c) У формулі (1-а), формулі (1-b) або формулі (1c), (R3)m і Q представляє одну з комбінацій замісників показаних в (Таблиця 1) - (Таблиця 4). (за умови, що в колонці (R3)m в таблицях, символ "-" означає, що m є 0). Таблиця 1 (R3)m 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ Q 2-піридил 3-метил-2-піридил 3-хлор-2-піридил 3-фтор-2-піридил 3-трифторметил-2-піридил 3-метокси-2-піридил 5-метил-2-піридил 5-хлор-2-піридил 5-фтор-2-піридил 5-трифторметил-2-піридил 5-метокси-2-піридил 4-метил-2-піридил 4-хлор-2-піридил 4-фтор-2-піридил 4-трифторметил-2-піридил 4-метокси-2-піридил 6-метил-2-піридил 6-хлор-2-піридил 6-фтор-2-піридил 6-трифторметил-2-піридил 6-метокси-2-піридил 3,5-диметил-2-піридил 3,5-дихлор-2-піридил 3,5-дифтор-2-піридил 3,6-диметил-2-піридил 3,6-дихлор-2-піридил 3,6-дифтор-2-піридил 6-хлор-3-трифторметил-2-піридил 6-хлор-5-трифторметил-2-піридил Таблиця 2 (R3)m 4-СІ 4-СІ 4-СІ 4-СН3 4-F 4-ОСН3 Q 3-хлор-5-трифторметил-2-піридил 3,5,6-трихлор-2-піридил 3,5,6-трифтор-2-піридил 3-метил-2-піридил 3-метил-2-піридил 3-метил-2-піридил 22 4-CF3 3-СІ 3,4-СІ2 2-F, 4-CI 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 3-метил-2-піридил 3-метил-2-піридил 3-метил-2-піридил 3-метил-2-піридил 3-метил-2-піридил 2-піримідиніл 5-метил-2-піримідиніл 5-метокси-2-піримідиніл 5-хлор-2-піримідиніл 5-фтор-2-піримідиніл 4,6-диметил-2-піримідиніл 4,6-біс(трифторметил)-2-піримідиніл 4-метил-2-піримідиніл 4-метокси-2-піримідиніл 4-хлор-2-піримідиніл 4-фтор-2-піримідиніл 4-піримідиніл 5-метил-4-піримідиніл 5-метокси-4-піримідиніл 5-хлор-4-піримідиніл 5-фтор-4-піримідиніл 2,5-диметил-4-піримідиніл 2-метил-4-піримщиніл Таблиця 3 (R3)m 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ Q 2-метокси-4-піримідиніл 2-хлор-4-піримідиніл 5-хлор-6-метил-4-піримідиніл 5-хлор-2-метил-4-піримідиніл 5-фтор-6-метил-4-піримідиніл 5-фтор-2-метил-4-піримідиніл 2-хлор-6-метил-4-піримідиніл 3-піридазиніл 4-метил-3-піридазиніл 4-хлор-2-піридазиніл 2-піразиніл 3-метил-2-піразиніл 3-хлор-2-піразиніл Таблиця 4 (R3)m 4-СН3 4-F 4-ОСН3 4-CF3 3-СІ 3,4-СІ2 2-F, 4-CI 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ Q 3-хлор-2-піридил 3-хлор-2-піридил 3-хлор-2-піридил 3-хлор-2-піридил 3-хлор-2-піридил 3-хлор-2-піридил 3-хлор-2-піридил 3-хлор-2-піридил 3-нітро-2-піридил 3-ціано-2-піридил 3-хлор-5-метокси-2-піридил 3-нітро-5-метокси-2-піридил 3-ціано-5-метокси-2-піридил 5-метокси-3-метил-2-піридил 3-хлор-5-нітро-2-піридил 4-метокси-6-метил-2-піримідиніл 4,6-диметокси-2-піримідиніл 5-нітро-4-піримідиніл 23 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СН3 4-F 4-ОСН3 4-CF3 3-СІ 3,4-СІ2 2-F, 4-CI 4-СН3 4-F 4-ОСН3 4-CF3 3-СІ 3,4-СІ2 2-F, 4-CI 4-СН3 4-F 4-ОСН3 4-CF3 3-СІ 3,4-СІ2 2-F, 4-CI 4-СН3 4-F 4-ОСН3 4-CF3 3-СІ 3,4-СІ2 2-F.4-CI 4-СН3 4-F 4-ОСН3 4-CF3 3-СІ 3,4-СІ2 2-F, 4-CI 90360 24 Сполука наступної формули (13-а) 5-ціано-4-піримідиніл 5-трифторметил-4-піримідиніл 4-трифторметил-3-піридазиніл 4-ціано-3-піридазиніл 4-нітро-2-піридазиніл 4-метокси-3-піридазиніл 3-трифторметил-2-піразиніл 3-ціано-2-піразиніл 3-нітро-2-піразиніл 3-метокси-2-піразиніл 3-фтор-2-піридил 3-фтор-2-піридил 3-фтор-2-піридил 3-фтор-2-піридил 3-фтор-2-піридил 3-фтор-2-піридил 3-фтор-2-піридил 3-фтор-2-піридил 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил (13a) Сполука наступної формули (16-а) (16a) Сполука наступної формули (17-а) (17a) Сполука наступної формули (3-а) (3a) Сполука наступної формули (4-а) (4a) Сполука наступної формули (5-а) (5a) Сполука наступної формули (21-а) (21a) Специфічні приклади одержаних проміжних сполук сполуки представленого винаходу показані далі. Сполука наступної формули (2-а) (2a) У формулі (2-а), формулі (13-а), формулі (16а), формулі (17-а), формулі (3-а), формулі (4-а), 3 формулі (5-а) і формулі (21-а), (R )m і Q представляють одну з комбінації замісників показаних в (Таблиця 5) - (Таблиця 8). (за умови, що в колонці (R3)m в таблицях, символ "-" означає, що m є 0) 25 90360 Таблиця 5 (R3)m 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ Q 2-піридил 3-метил-2-піридил 3-хлор-2-піридил 3-фтор-2-піридил 3-трифторметил-2-піридил 3-метокси-2-піридил 5-метил-2-піридил 5-хлор-2-піридил 5-фтор-2-піридил 5-трифторметил-2-піридил 5-метокси-2-піридил 4-метил-2-піридил 4-хлор-2-піридил 4-фтор-2-піридил 4-трифторметил-2-піридил 4-метокси-2-піридил 6-метил-2-піридил 6-хлор-2-піридил 6-фтор-2-піридил 6-трифторметил-2-піридил 6-метокси-2-піридил 3,5-диметил-2-піридил 3,5-дихлор-2-піридил 3,5-дифтор-2-піридил 3,6-диметил-2-піридил 3,6-дихлор-2-піридил 3,6-дифтор-2-піридил 6-хлор-3-трифторметил-2-піридил 6-хлор-5-трифторметил-2-піридил Таблиця 6 (R3)m 4-СІ 4-СІ 4-СІ 4-СН3 4-F 4-ОСН3 4-CF3 3-СІ 3,4-СІ2 2-F, 4-CI 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ Q 3-хлор-5-трифторметил-2-піридил 3,5,6-трихлор-2-шридил 3,5,6-трифтор-2-піридил 3-метил-2-піридил 3-метил-2-піридил 3-метил-2-піридил 3-метил-2-піридил 3-метил-2-піридил 3-метил-2-піридил 3-метил-2-піридил 3-метил-2-піридил 2-піримідиніл 5-метил-2-піримідиніл 5-метокси-2-піримідиніл 5-хлор-2-піримідиніл 5-фтор-2-піримідиніл 4,6-диметил-2-піримідиніл 4,6-біс(трифторметил)-2-піримідиніл 4-метил-2-піримідиніл 4-метокси-2-піримідиніл 4-хлор-2-піримідиніл 4-фтор-2-піримідиніл 4-піримідиніл 5-метил-4-піримідиніл 5-метокси-4-піримідиніл 26 4-СІ 4-СІ 4-СІ 4-СІ 5-хлор-4-піримідиніл 5-фтор-4-піримідиніл 2,5-диметил-4-піримідиніл 2-метил-4-піримідиніл Таблиця 7 (R3)m 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ Q 2-метокси-4-піримідиніл 2-хлор-4-піримідиніл 5-хлор-6-метил-4-піримідиніл 5-хлор-2-метил-4-піримідиніл 5-фтор-6-метил-4-піримідиніл 5-фтор-2-метил-4-піримідиніл 2-хлор-6-метил-4-піримідиніл 3-піридазиніл 4-метил-3-піридазиніл 4-хлор-2-піридазиніл 2-піразиніл 3-метил-2-шразиніл 3-хлор-2-піразиніл Таблиця 8 (R3)m 4-СН3 4-F 4-ОСН3 4-CF3 3-СІ 3,4-Cl2 2-F, 4-CI 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СІ 4-СН3 4-F 4-ОСН3 4-CF3 3-СІ 3,4-СІ2 2-F, 4-CI Q 3-хлор-2-піридил 3-хлор-2-піридил 3-хлор-2-піридил 3-хлор-2-піридил 3-хлор-2-піридил 3-хлор-2-піридил 3-хлор-2-піридил 3-хлор-2-піридил 3-нітро-2-піридил 3-ціано-2-піридил 3-хлор-5-метокси-2-піридил 3-нітро-5-метокси-2-піридил 3-ціано-5-метокси-2-піридил 5-метокси-3-метил-2-піридил 3-хлор-5-нітро-2-піридил 4-метокси-6-метил-2-піримідиніл 4,6-диметокси-2-піримідиніл 5-нітро-4-піримідиніл 5-ціано-4-піримідиніл 5-трифторметил-4-піримідиніл 4-трифторметил-3-піридазиніл 4-ціано-3-піридазиніл 4-нітро-2-піридазиніл 4-метокси-3-піридазиніл 3-трифторметил-2-піразиніл 3-ціано-2-піразиніл 3-нітро-2-піразиніл 3-метокси-2-піразиніл 3-фтор-2-піридил 3-фтор-2-піридил 3-фтор-2-піридил 3-фтор-2-піридил 3-фтор-2-піридил 3-фтор-2-піридил 3-фтор-2-піридил 3-фтор-2-піридил 27 4-СНз 4-F 4-ОСН3 4-CF3 3-СІ 3,4-СІ2 2-F, 4-CI 4-СН3 4-F 4-ОСН3 4-CF3 3-СІ 3,4-СІ2 2-F, 4-CI 4-СН3 4-F 4-ОСН3 4-CF3 3-СІ 3,4-СІ2 2-F, 4-CI 4-СН3 4-F 4-ОСН3 4-CF3 3-СІ 3,4-СІ2 2-F, 4-CI 90360 28 Таблиця 9 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дифтор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 3,5-дихлор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 5-хлор-3-фтор-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил 3-хлор-5-метокси-2-піридил Q 2-піридил 3-метил-2-піридил 3-хлор-2-піридил 3-фтор-2-піридил 3-трифторметил-2-піридил 3-метокси-2-піридил 5-метил-2-піридил 5-хлор-2-піридил 5-фтор-2-піридил 5-трифторметил-2-піридил 5-метокси-2-піридил 4-метил-2-піридил 4-хлор-2-піридил 4-фтор-2-піридил 4-трифторметил-2-піридил 4-метокси-2-піридил 6-метил-2-піридил 6-хлор-2-піридил 6-фтор-2-піридил 6-трифторметил-2-піридил 6-метокси-2-піридил 3,5-диметил-2-піридил 3,5-дихлор-2-піридил 3,5-дифтор-2-піридил 3,6-диметил-2-піридил 3,6-дихлор-2-піридил 3,6-дифтор-2-піридил 6-хлор-3-трифторметил-2-піридил 6-хлор-5-трифторметил-2-піридил Таблиця 10 Сполука наступної формули (15-а), (15a) Сполука наступної формули (27-а), (27a) Сполука наступної формули (27-b), (27-b) Сполука наступної формули (23-а), (23-а) Сполука наступної формули (25-а), (25-а) У формулі (15-а), формулі (27-а), формулі (27b), формулі (23-а) і формулі (25-а), Q представляє один із замісників показаний в (Таблиця 9) - (Таблиця 11) Q 3-хлор-5-трифторметил-2-піридил 3,5,6-трихлор-2-піридил 3,5,6-трифтор-2-піридил 2-піримідиніл 5-метил-2-піримідиніл 5-метокси-2-піримідиніл 5-фтор-2-піримідиніл 5-фтор-2-піримщиніл 4,6-диметил-2-піримідиніл 4,6-біс(трифторметил)-2-піримідиніл 4-метил-2-піримідиніл 4-метокси-2-піримідиніл 4-хлор-2-піримідиніл 4-фтор-2-піримідиніл 4-піримідиніл 5-метил-4-піримідиніл 5-метокси-4-піримідиніл 5-хлор-4-піримідиніл 5-фтор-4-піримідиніл 2,5-диметил-4-піримідиніл 2-метил-4-піримідиніл 2-метокси-4-піримідиніл 2-хлор-4-піримідиніл 5-хлор-6-метил-4-піримідиніл 5-хлор-2-метил-4-піримідиніл 5-фтор-6-метил-4-піримідиніл 29 90360 5-фтор-2-метил-4-піримідиніл 2-хлор-6-метил-4-піримідиніл 3-піридазиніл Таблиця 11 Q 4-метил-3-піридазиніл 4-хлор-2-піридазиніл 2-піразиніл 3-метил-2-піразиніл 3-хлор-2-піразиніл 3-нітро-2-піридил 3-ціано-2-піридил 3-хлор-5-метокси-2-піридил 3-нітро-5-метокси-2-піридил 3-ціано-5-метокси-2-піридил 5-метокси-3-метил-2-піридил 3-хлор-5-нітро-2-піридил 4-метокси-6-метил-2-піримідиніл 4,6-диметокси-2-піримідиніл 5-нітро-4-піримідиніл 5-ціано-4-піримідиніл 5-трифторметил-4-піримідиніл 4-трифторметил-3-піридазиніл 4-ціано-3-піридазиніл 4-нітро-2-піридазиніл 4-метокси-3-піридазиніл 3-трифторметил-2-піразиніл 3-ціано-2-піразиніл 3-нітро-2-піразиніл 3-метокси-2-піразиніл Прикладами захворювань рослин на які сполука представленого винаходу проявляє контролюючу дію є наступні захворювання. Рис: Magnaporthe grisea, Cochliobolus miyabeanus, Rhizoctonia solani; Пшениця та ячмінь: Erysiphe graminis, Fusarium graminarum, F. avenacerum, F Culmorum, Puccinia striiformis, P. graminis, P. recondita, P. hordei, Typhula sp., Micronectriella nivalis, Ustilago tritici, U. Nuda, Tilletia caries, Pseudocercosporella herpotrichoides, Rhynchosporium secalis, Septoria tritici, Leptosphaeria nodorum; Цитрус: Diaporthe citri, Elsinoe fawcetti, Penicillium digitatum, P. Italicum; Яблуко: Monilinia mali, Valsa ceratosperma, Podosphaera leucotricha, Altemana alternata apple pathotype, Venturia inaequalis; Груша: Venturia nashicola, V. Pirina, Alternaria alternata Japanese pear pathotype, Gymnosporangium haraeanum; Персик: Monilinia fructicola, Cladosporium carpophilum, Phomopsis sp.; Виноград: Elsinoe ampelina, Glomerella cingulata, Uncinula necator, Phakopsora ampelopsidis, Guignardia bidwellii, Plasmopara viticola; Хурма: Gloeosporium kaki, Cercospora kaki, Mycosphaerella nawae; Гарбузові: Colletotrichu mlagenarium, Sphaerotheca fuliginea, Mycosphaerella melonis, 30 Fusarium oxysporum, Pseudoperonospora cubensis, Phytophthora sp.; Pythium sp.; Томати: Alternaria solani, Cladosporium fulvum, Phytophthora infestans; Баклажан: Phomopsis vexans, Erysiphe cichoracearum; Крестоцвітні овочі: Alternaria japonica, Cercosporella brassicae; Зелена цибуля: Puccinia allii; Соя: Cercospora kikuchii, Elsinoe glycines, Diaporthe phaseolorum var. sojae, Phakopsora pachyrhizi; Фасоль: Colletotrichu mlindemthianum; Арахіс: Cercospora personata, Cercospora arachidicola; Горох: Erysiphe pisi; Картопля: Alternaria solani, Phytophthora infestans; Полуниця: Sphaerotheca humuli; Чай: Exobasidium reticulatum, Elsinoe leucospila; Тютюн: Alternaria longipes, Erysiphe cichoracearum, Colletotrichum tabacum, Peronospora tabacina; Phytophthora nicotianae; Цукровий буряк: Cercospora beticola; Рожа: Diplocarpon rosae, Sphaerotheca pannosa; Хризантеми: Septoria chrysanthemi-indici; Puccinia horiana; Різні зернові: Botrytis cinerea, стеблова гниль Sclerotinia sclerotiorum; Редька: Alternaria brassicicola; Дерн: Sclerotinia homeocarpa, Rhizoctonia solani. При нанесенні сполуки представленого винаходу як вона є на рослини або ґрунт проявляється фунгіцидна дія. Однак, зазвичай використовується композиція, що містить сполуку представленого винаходу і носій. Тобто, для одержання фунгіциду представленого винаходу, змішують сполуку представленого винаходу і твердий носій і/або рідкий носій, і якщо необхідно, до рецептури додають поверхнево-активну речовину і інші допоміжні речовини, і суміш формулюють у концентрат, що емульсифікується, змочуваний порошок, гранули, що диспергуються у воді, текучий агент, дуст, гранули і т.і.. Ці рецептури містять сполуку представленого винаходу зазвичай в кількості від 0,1-90ваг.%. Прикладами твердого носія для використання в рецептурі є тонкі порошки або гранульовані матеріали, що включають мінеральні речовини, такі як каолін, аттапульгіт, бентоніт, монтмориллоніт, кислу глину, пірофілліт, тальк, діатомова земля, кальцит і т.і, природні органічні матеріали, такі як висівки зернових, порошок шкарлупи грецького горіха і т.і., синтетичні органічні матеріали, такі як сечовина і т.і., солі, такі як карбонат кальцію, сульфат амонію і т.і., синтетичні неорганічні матеріали, такі як синтетичний гідратований оксид кремнію і т.і., і прикладами рідкого носія є ароматичні вуглеводні, такі як ксилен, алкілбензол, метилнафталін і т і., спирти, такі як 2-пропанол, етиленгліколь, пропіленгліколь, целюлоза і т.і., кетони, такі як ацетон, циклогексанон, ізофорон і т.і., рослинні 31 олії, такі як соєва олія, олія з насіння бавовнику і т.і., аліфатичні вуглеводні, естери, диметилсульфоксид, ацетонітрил і вода. Прикладами поверхнево-активної речовини є аніонні поверхнево-активні речовини, такі як солі алкілсульфатів, солі алкіларилсульфонової кислоти, солі діалкілсульфосукцинової кислоти, солі поліоксиетиленалкіларилового етеру фосфату, солі лігнінсульфонової кислоти, поліконденсат нафталінсульфонат-формальдегід і т.і., і неіонні поверхнево-активна речовини, такі як поліоксиетиленалкіларилові етери, блокспівполімери поліоксиетиленалкілу поліоксипропілену, жирні естери сорбіту і т.і.. Прикладами інших допоміжних речовин для рецептури є водорозчинні полімери, такі як полівініловий спирт, полівінілпіролідон і т.і., гуміарабік, алгінова кислота і її солі, полісахариди, такі як CMC (карбоксиметилцелолоза), ксантанова камедь і т.і., неорганічні речовини, такі як силікат алюмінію магнію, золь глинозему і т.і., консерванти, фарбники і стабілізатори, такі як РАР (кислий ізопропілфосфат), ВНТ і т.і. Шляхом обробки тіла рослини фунгіцидом представленого винаходу, рослину можна захистити від захворювань рослин. Шляхом обробки ґрунту фунгіцидом представленого винаходу, рослину, що росте, на ґрунті можна захистити від захворювань рослин. Тобто, фунгіцид представленого винаходу використовується в способі контролювання захворювання рослин, що включає стадію нанесення зазвичай ефективної кількості фунгіциду представленого винаходу на рослину або ґрунт, на якому вирощується рослина. Коли фунгіцид представленого винаходу використовується для лікування тіла рослини або коли фунгіцид представленого винаходу використовується для обробки ґрунту, його використовувана кількість може змінюватись в залежності від виду рослини, виду захворювання, часу розвитку захворювання, форми рецептури, періоду обробки, погодних умов і т.і., і зазвичай становить 1-5000г, переважно 5-1000г з розрахунку на сполуку представленого винаходу на 10000м2. Концентрат, що емульсифікується, змочуваний порошок, текучий агент і т.і. зазвичай розводять водою і розпилюють під час обробки. В цьому випадку, концентрація сполуки представленого винаходу знаходиться зазвичай в інтервалі від 0,0001 до 3ваг.%, переважно 0,0005-1ваг.%. Дуст, гранули і т.і. зазвичай використовують для обробки без розведення. Фунгіцид представленого винаходу також може бути використаний для протруювання насіння. Протруювання є, наприклад, способом, в якому насіння рослин занурюють у фунгіцид представленого винаходу, де концентрація сполуки представленого винаходу регулюються в межах 1-1000м.ч., способом, в якому фунгіцидом представленого винаходу, де концентрація сполуки представленого винаходу регулюються в межах 1-1000м.ч., обприскують або обмазують насіння рослин, і способом, в якому фунгіцид представленого винаходу сформульований у дуст наносять на насіння рослин. 90360 32 Спосіб контролювання захворювання рослини представленого винаходу зазвичай здійснюють шляхом обробки рослини або фунту, на якому росте рослина і на якому в перспективі утворюється захворювання, ефективною кількістю фунгіциду представленого винаходу. Фунгіцид представленого винаходу зазвичай використовується як фунгіцид для сільському господарстві і садівництві, а саме, як фунгіцид для контролювання захворювань рослин на зораних полях, рисових полях, фруктових полях, чайних полях, пасовиськах, торф'яниках і т.і.. Фунгіцид представленого винаходу також може бути використаний разом з іншим фунгіцидом, інсектицидами, акарицидом, нематоцидом, гербіцидом, регулятором росту рослин і/або добривом. Прикладами активних інгредієнтів таких фунгіцидів є фунгіциди азольного типу, такі як пропіоконазол, протіоконазол, триадіименол, прохлораз, пенконазол, тебуконазол, флузилазол, диніконазол, бромуконазол, епоксиконазол, дифеноконазол, ципроконазол, метконазол, трифлумізол, тетраконазол, міклобутаніл, фенбуконазол, гексаконазол, флухінконазол, тритиконазол, бітертанол, імізаліл і флутриафол і т.і; фунгіциди типу киклічних амінів, такі як фенпропіморф, тридеморф, фенпродипін і т.і., фунгіциди бензімідазольного типу, такі як карбендазим, беноміл, тіабенздазол, тіофанат-метил і т.і.; процимідон; ципродиніл; піриметаніл; діетофенкарб; тіурам; флуазинам; манкозеб; іпродіон; вінклозолін; хлорталоніл; каптан, мепаніпірим; фенпіклоніл; флудіоксоніл; дихлофлуанід; фолпет; клероксим-метил; азоксистробін; трифлоксистробін; пікоксистробін; піраклостробін; N-метил-а-метоксиіміно-2-((2,5диметилфенокси)метил)фенілацетамід; спіроксамін; хіноксифен; фенгексамід, фамоксадон; фенамідон; іпровалікарб; бентіавалікарб; циазофамід; боскалід; метрафенон і циклуфєнамід. Представлений винахід далі описується детально за допомогою прикладів одержання, прикладів рецептур і прикладів тестування і т.і. нижче, але представлений винахід не обмежується цими прикладами. Спочатку показані приклади одержання сполук представленого винаходу. Приклад одержання 1 Змішували 0,24г 5-(4-хлорфеніл)-6-метил-4-(2піридил)-2Н-піридазин-3-ону і 3г оксихлориду фосфору. Суміш перемішували протягом 1 години на масляній бані при 110°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розді 33 ляли. Органічний шар промивали розсолом, і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску одержуючи 0,25г 3-хлор-5-(4-хлорфеніл)-6-метил-4-(2піридил)піридазину (тут далі, описується як сполука (1) представленого винаходу.). Сполука (1) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,55 (3Н, с), 7,00 (2Н, д, J=8,6Гц), 7,06 (1Η, д, J=7,8Гц), 7,25 (2Н, д, J=8,6Гц), 7,17-7,25 (1Η, м), 7,61 (1Η, дт, J=1,8, 7,8Гц), 8,56 (1Η, д, J=4,2Гц) Приклад одержання 2 Змішували 0,34г 5-(4-хлорфеніл)-6-метил-4-(3метил-2-піридил)-2Н-піридазин-3-ону і 3,6г оксихлориду фосфору. Суміш перемішували 2 години на масляній бані при 120°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розділяли Органічний шар промивали розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 0,33г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,21г 3-хлор-5-(4хлорфеніл)-6-метил-4-(3-метил-2піридил)піридазину (тут далі, описується як сполука (2) представленого винаходу.). Сполука (2) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,98 (3Н, с), 2,56 (3Н, с), 7,04 (2Н, ш д, J=8,8Гц), 7,15 (1Η, м), 7,23 (2Н, д, J=8,8Гц), 7,43 (1Η, д, J=7,8Гц), 8,42 (1Η, д, J=3,6Гц) Приклад одержання 3 Змішували 0,20г 5-(4-хлорфеніл)-6-метил-4-(5метил-2-піридил)-2Н-піридазин-3-ону і 3,2г оксихлориду фосфору. Суміш перемішували протягом 2 годин на масляній бані при 120°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розділяли. Органічний шар промивали розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 0,20г одер 90360 34 жаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,18г 3-хлор-5-(4хлорфеніл)-6-метил-4-(5-метил-2піридил)піридазину (тут далі, описується як сполука (3) представленого винаходу.). Сполука (3) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,32 (3Н, с), 2,53 (3Н, с), 6,94 (1Η, д, J=7,8Гц), 7,00 (2Н, д, J=8,4Гц), 7,25 (2Н, д, J=8,4Гц), 7,40 (1Η, д, J=7,8Гц), 8,38 (1Η, с) Приклад одержання 4 Змішували 6мг 5-(4-хлорфеніл)-6-метил-4-(6метил-2-піридил)-2Н-піридазин-3-ону і 2г оксихлориду фосфору. Суміш перемішували протягом 4 годин на масляній бані при 130°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розділяли. Органічний шар промивали розсолом, і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску, одержуючи 4мг 3-хлор-5-(4-хлорфеніл)-6-метил-4-(6-метил-2піридил)піридазину (тут далі, описується як сполука (4) представленого винаходу.) Сполука (4) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,47 (3Н, с), 2,53 (3Н, с), 6,89 (1Η, д, J=7,8Гц), 7,01 (2Н, д, J=8,4Гц), 7,05 (1Η, д, J=7,8Гц), 7,25 (2Н, д, J=8,4Гц), 7,50 (1Η, т, J=7,8Гц) Приклад одержання 5 Змішували 0,64г 5-(4-хлорфеніл)-4-(3-хлор-2піридил)-6-метил-2Н-піридазин-3-ону і 15г оксихлориду фосфору. Суміш перемішували протягом 6 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розділяли. Органічний шар промивали розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 0,67г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,50г 35 90360 36 3-хлор-5-(4-хлорфеніл)-4-(3-хлор-2-піридил)-6метилпіридазину (тут далі, описується як сполука (5) представленого винаходу). Сполука (5) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,56 (3Н, с), 7,08 (2Н, д, J=8,8Гц), 7,20-7,25 (3Η), 7,66 (1Η, дд, J=8,3, 1,5Гц), 8,47 (1Η, дд, J=4,6,1,5Гц) Приклад одержання б описується як сполука (7) представленого винаходу.). Сполука (7) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,55 (3Н, с), 7,05 (2Н, д, J=8,6Гц), 7,22 (2Н, ш), 7,41-7,44 (1Η, м), 7,93 (1Η, дд, J=8,3, 1,0Гц), 8,80 (1Η, дд, J=4,9,1,0Гц) Приклад одержання 8 Змішували 0,64г 5-(4-хлорфеніл)-6-метил-4-(2піримідиніл)-2Н-піридазин-3-ону і 10,4г оксихлориду фосфору. Суміш перемішували протягом 2 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і додавали охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розділяли. Органічний шар промивали розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 0,56г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,49г 3-хлор-5-(4-хлорфеніл)-6-метил4-(2-піримідиніл)піридазину (тут далі, описується як сполука (6) представленого винаходу (6).) Сполука (6) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,57 (3Н, с), 7,06 (2Н, д, J=8,8Гц), 7,21 (1Η, т, J=4,9Гц), 7,26 (2Н, д, J=8,8Гц), 8,70 (1Η, д, J=4,9Гц) Приклад одержання 7 Змішували 0,35г сполуки (5) представленого винаходу, 1,92г метоксиду натрію (28% розчин метанолу) і 6мл безводного метанолу, потім, суміш перемішували протягом 2 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, додавали льодяну воду, і екстрагували етилацетатом. Органічний шар промивали двічі розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску, одержуючи 0,34г 5-(4-хлорфеніл)-4-(3-хлор-2піридил)-3-метокси-6-метилпіридазину (тут далі, описується як сполука (8) представленого винаходу.) Сполука (8) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,46 (3Н, с), 4,10 (3Н, с), 7,08 (2 Н), 7,1-7,3 (3Η), 7,62 (1Н), 8,42 (1Н) Приклад одержання 9 Змішували 0,69г 5-(4-хлорфеніл)-6-метил-4-(3трифторметил-2-піридил)-2Н-піридазин-3-ону і 6,3г оксихлориду фосфору. Суміш перемішували протягом 2 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розділяли. Органічний шар промивали розсолом, і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 0,50г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,11г 3-хлор-5-(4-хлорфеніл)-6-метил-4-(3трифторметил-2-піридил)піридазину (тут далі, 0,48г гідриду натрію (55% дисперсія в маслі) додавали до 5мл Ν,Ν-диметилформаміду. До цієї суміші в атмосфері азоту прикапували 1,76г діетилмалонату, і суміш перемішували при кімнатній температурі протягом 30 хвилин. До цієї суміші додавали 1,05г сполуки (5) представленого винаходу і суміш перемішували при 100°С протягом 16 годин і при 120°С протягом 9,5 годин. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, додавали льодяну воду, і екстрагували етилацетатом. Органічний шар промивали три рази розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 1,45г одержаного залишку піддавали колонковій хроматографії на силікагелі одержуючи 0,23г твердої речовини. Цю тверду речовину піддавали тонкошаровій хроматографії на силікагелі одержуючи 0,15г проміжної сполуки. Змішували одержану проміжну сполуку і 3мл концентрованої хлорводневої кислоти. Суміш перемішували протягом 30 хвилин на масляній бані при 100°С. Реакційну суміш залишали охолоджуватись 37 до кімнатної температури, потім, додавали суміш льоду і 10% водного розчину гідроксиду натрію і суміш екстрагували етилацетатом. Органічний шар двічі промивали розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 0,07г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,05г 5-(4-хлорфеніл)-4-(3-хлор-2піридил)-3,6-диметилпіридазину (тут далі, описується як сполука (9) представленого винаходу.). Сполука (9) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,44 (3Н, с), 2,54 (3Н, с), 7,05 (2Н, ш), 7,15-7,3 (3Η),7,63 (1Η, дд, J=8,0, 1,5Гц), 8,47 (1Η, дд, J=4,6, 1,5Гц) Приклад одержання 10 Змішували 0,24г 5-(4-хлорфеніл)-4-(3-хлор-5метокси-2-піридил)-6-метил-2Н-піридазин-3-ону і 6г оксихлориду фосфору. Суміш перемішували протягом 2 годин на масляній бані при 110°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розділяли. Органічний шар промивали розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 0,12г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,07г 3-хлор-5(4-хлорфеніл)-4-(3-хлор-5-метокси-2-піридил)-6метилпіридазину (тут далі, описується як сполука (10) представленого винаходу.). Сполука (10) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,55 (3Н, с), 3,86 (3Н, с), 7,07 (2Н, д, J=8,8Гц), 7,15 (1Η, д, J=2,7Гц), 7,27 (2Н, д, J=8,8Гц), 8,15 (1Η, д, J=2,7Гц) Приклад одержання 11 Змішували 0,66г 5-(4-хлорфеніл)-4-(3,5дихлор-2-піридил)-6-метил-2Н-піридазин-3-ону і 6г оксихлориду фосфору. Суміш перемішували протягом 2 годин на масляній бані при 110°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розділяли. Органічний шар промивали розсолом і сушили над безводним сульфатом 90360 38 магнію, потім, концентрували при пониженому тиску. 0,67г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,47г 3-хлор-5-(4-хлорфеніл)-4-(3,5-дихлор-2-піридил)-6метилпіридазину (тут далі, описується як сполука (11) представленого винаходу.). Сполука (11) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,56 (3Н, с), 7,06 (2Н, д, J=7,8Гц), 7,29 (2Н, д, J=7,8Гц), 7,69 (1Η, с), 8,42 (1Η, с) Приклад одержання 12 Змішували 0,57г 5-(4-хлорфеніл)-4-(3-хлор-2піразиніл)-6-метил-2Н-піридазин-3-ону і 6г оксихлориду фосфору. Суміш перемішували протягом 2 годин на масляній бані при 110°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розділяли. Органічний шар промивали розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 0,60г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,49г 3-хлор-5-(4хлорфеніл)-4-(3-хлор-2-піразиніл)-6метилпіридазин (тут далі, описується як сполука (12) представленого винаходу.). Сполука (12) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,58 (3Н, с), 7,08 (2Н, ш), 7,29 (2Н, д, J=8,6Гц), 8,34 (1Η, д, J=2,4Гц), 8,48 (1Η, д, J=2,4Гц) Приклад одержання 13 Змішували 0,30г 5-(4-хлорфеніл)-4-(6-хлор-4метил-3-піридазиніл)-6-метил-2Н-піридазин-3-ону і 5г оксихлориду фосфору. Суміш перемішували протягом 1,5 годин на масляній бані при 110°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розділяли. Органічний шар промивали розсолом, і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 0,31г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 026г 3-хлор-5 39 (4-хлорфеніл)-4-(6-хлор-4-метил-3-піридазиніл)-6метилпіридазину (тут далі, описується як сполука (13) представленого винаходу(13).). Сполука (13) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,04 (3Н, с), 2,59 (3Н, с), 6,9-7,2 (2Н, ш), 7,25-7,35 (3Η) Приклад одержання 14 Змішували 0,3г 5-(4-хлорфеніл)-4-(5-хлор-3фтор-2-піридил)-6-метил-2Н-піридазин-3-ону і 10г оксихлориду фосфору . Суміш перемішували протягом 1,5 годин на масляній бані при 110°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розділяли Органічний шар промивали розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 0,3г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,22г 3-хлор-5-(4хлорфеніл)-4-(5-хлор-3-фтор-2-піридил)-6метилпіридазину (тут далі, описується як сполука (14) представленого винаходу.). Сполука (14) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,56 (3Н, с), 7,03 (2Н, д, J=8,5Гц), 7,29 (2Н, д, J=8,5Гц), 7,41 (1Η, дд, J=8,5, 2,0Гц), 8,37 (1Η, дд, J=2,0, 1,0Гц) Приклад одержання 15 Змішували 0,14г 5-(4-хлорфеніл)-4-(3,5дифтор-2-піридил)-6-метил-2Н-піридазин-3-ону і 5г оксихлориду фосфору. Суміш перемішували протягом 1,5 годин на масляній бані при 120°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розділяли. Органічний шар промивали розсолом, і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 0,14г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,08г 3-хлор-5-(4хлорфеніл)-4-(3,5-дифтор-2-піридил)-6метилпіридазин (тут далі, описується як сполука (15) представленого винаходу.). Сполука (15) представленого винаходу 90360 40 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,56 (3Н, с), 7,02 (2Н, д, J=8,8Гц), 7,16 (1Η, м), 7,29 (2Н, д, J=8,8Гц), 8,31 (1Η, д, J=2,2Гц) Приклад одержання 16 0,63г 5-(4-хлорфеніл)-4-(3-фтор-2-піридил)-6метил-2Н-піридазин-3-ону і 7,2г оксихлориду фосфору. Суміш перемішували протягом 1,5 годин на масляній бані при 120°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, концентрували при пониженому тиску. До одержаного залишку додавали етилацетат і охолоджений льодом водний бікарбонат натрію. Суміш перемішували протягом приблизно 5 хвилин при кімнатній температурі, потім, рідини розділяли. Органічний шар промивали розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 0,64г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,51г 3-хлор-5-(4хлорфеніл)-4-(3-фтор-2-піридил)-6метилпіридазину (тут далі, описується як сполука (16) представленого винаходу.). Сполука (16) представленого винаходу 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,56 (3Н, с), 7,04 (2Н, д, J=8,8Гц), 7,2-7,4 (4Η), 8,39 (1Η, м), Далі, приведені приклади одержання проміжної сполуки представленого винаходу, як допоміжні для Прикладів одержання. Допоміжний Приклад одержання 1 Суміш 10,12г 4'-хлорпропіофенону, 0,1мл бромводневої кислоти (48% водний розчин) і 60мл оцтової кислоти охолоджували до 0°С в атмосфері азоту. По краплям до суміші додавали 3,1мл брому, потім, суміш залишали нагріватись до кімнатної температури і перемішували протягом 1 години. Реакційну суміш концентрували при пониженому тиску одержуючи 14,34г 2-бром-4'хлорпропіофенону. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,90 (3Н, д, J=6,5Гц), 5,22 (1Η, к, J=6,5Гц), 7,46 (2Н, д, J=8,7Гц), 7,97 (2Н, д, J=8,7Гц) Допоміжний Приклад одержання 2 До суміші 1,05г 2-бром-4'-хлорпропіофенону, 0,74г 2-піридилоцтовоі кислоти·гідрохлорид і 20мл ацетонітрилу додавали 1,07г триетиламіну. Суміш перемішували протягом ночі при кімнатній температурі. Після цього, суміш охолоджували до 0°С, і 41 до неї прикапували 2,58г DBU, і суміш перемішували протягом 2 годин при тій же самій температурі. Потім, суміш перемішували протягом 5 годин при кімнатній температурі барботуючи повітря крізь реакційну суміш. До реакційної суміші додавали 8мл 1,2моль/л хлорводневої кислоти і екстрагували етилацетатом. Органічний шар двічі промивали розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 1,14г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,79г 4-(4-хлорфеніл)-5-гідрокси-5метил-3-(2-піридил)-2(5Н)-фуранону. 1 Н-ЯМР (СDСI3, ТМС) δ(м.ч.): 1,68 (3Н, с), 5,52 (1Η, ш), 7,28 (2Н, д, J=8,8Гц), 7,25-7,31 (1Η, м), 7,41 (2Н, д, J=8,8Гц), 7,55 (1Η, д, J=7,8Гц), 7,75 (1Η, дт, J=1,7, 7,8Гц), 8,51 (1Η, д, J=3,9Гц) Допоміжний Приклад одержання 3 Суміш 0,67г 4-(4-хлорфеніл)-5-гідрокси-5метил-3-(2-піридил)-2(5Н)-фуранону, 0,25г моногідрату гідразину і 8мл 1-бутанолу перемішували протягом 5 годин на масляній бані при 110°С. Реакційну суміш охолоджували до 0°С. Твердий осад збирали фільтруванням. Одержану тверду речовину промивали сумішшю гексану і тбутилметилового етеру, і сушили при пониженому тиску, одержуючи 0,32г 5-(4-хлорфеніл)-6-метил-4(2-піридил)-2Н-піридазин-3-ону. 1 Н-ЯМР (CDCI3 +ДMCO-d6, ТМС) δ(м.ч.): 2,11 (3Н, с), 7,01 (2Н, д, J=8,3Гц), 7,08-7,13 (1Η, м), 7,22 (2Н, д, J=8,3Гц), 7,2-7,25 (1Η, м), 7,57 (1Η, дт, J=1,7, 7,7Гц), 8,45 (1Η, д, J=4,9Гц) Допоміжний Приклад одержання 4 21,90г сполуки формули (26-і) розчиняли в 100мл етанолу і по краплям до цього розчину в атмосфері азоту при охолодженні льодом додавали розчин одержаний розчиненням 6,00г моногідрату гідразину в 20мл етанолу. Суміш перемішували протягом 1 години при тій же самій температурі і перемішували протягом 2 годин при кімнатній температурі, потім, залишали стояти протягом ночі. До реакційної суміш додавали 80мл хлороформу, суміш фільтрували і одержаний фільтрат концентрували при пониженому тиску, одержуючи 23,52г сполуки формули (24-і). 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,05 (3Н, с), 6,09 (2Н, ш с), 7,38 (2Н, д, J=8Гц), 7,81 (2Н, д, J=8Гц) Допоміжний Приклад одержання 5 90360 42 До суміші 10,72г 2,3-лутидину і 150мл тетрагідрофурану при кімнатній температурі додавали 63мл н-бутилітію (1,6моль/л гексановий розчин). До суміші при -70°С прикапували суміш 11,81г діетилкарбонату і 50мл безводного тетрагідрофурану. Суміш нагрівали до кімнатної температури. Реакційну суміш додавали до охолодженого льодом водного розчину хлориду амонію і екстрагували трет-бутилметиловим етером. Органічний шар промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 16,16г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 6,31г етил (3-метил-2-піридил)ацетату. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,25 (3Н, т, J=7,2Гц), 2,31(3 Η, с), 3,87 (2Н, с), 4,18(2Н, к, J=7,2Гц), 7,10 (1Η, м), 7,47(1Η, дд, J=1,2, 7,7Гц), 8,39(1Η, дд, J=1,2, 4,9Гц) Наступні сполуки одержували згідно з Допоміжним Прикладом одержання 5. Етил (5-метил-2-піридил)ацетат 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,26 (3Η, т, J=7,2Гц), 2,32 (3 Η, с), 3,80(2Н, с), 4,18 (2Н, κ, J=7,2Гц), 7,19 (1Η, д, J=7,8Гц), 7,46 (1Η, дд, J=2,2, 7,8Гц), 8,38 (1Η, д, J=2,2Гц) Етил (6-метил-2-піридил)ацетат 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,26 (3Н, т, J=7,3Гц), 2,54 (3Η, с), 3,81 (2Н, с), 4,18 (2Н, к, J=7,3Гц), 7,04 (1Η, д, J=7,8Гц), 7,09 (1Η, д, J=7,8Гц), 7,54 (1Η, т, J=7,8Гц) Допоміжний Приклад одержання 6 Змішували 1,97г сполуки формули (24-і), 1,65г етил 2-піридилацетату, 3,40г етоксиду натрію (20% етанольний розчин) і 35мл етанолу. Суміш перемішували протягом 5 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші послідовно додавали лід і 8,3мл 1,2моль/л хлорводневої кислоти, і екстрагували етилацетатом. Органічний шар промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 2,52г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,70г 5-(4-хлорфеніл)-6-метил-4-(2піридил)-2Н-піридазин-3-ону. Наступні сполуки одержували згідно з Допоміжним Прикладом одержання 6. 5-(4-хлорфеніл)-6-метил-4-(3-метил-2піридил)-2Н-піридазин-3-он 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,12 (3Н, с), 2,13 (3Н, с), 7,06 (1Η, м), 7,1-7,3 (4Η, м), 7,39 (1Η, д, J=7,8Гц), 8,34 (1Η, д, J=3,7Гц), 11,61 (1Η, ш с) 5-(4-хлорфеніл)-6-метил-4-(5-метил-2піридил)-2Н-піридазин-3-он 43 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,10 (3Н, с), 2,26 (3Н, с), 7,0-7,05 (2Н, м), 7,13 (2Н, д, J=7,2Гц), 7,207,25 (2Н, м), 7,38 (1Η, д, J=7,2Гц), 8,29 (1Η, с) 5-(4-хлорфеніл)-6-метил-4-(6-метил-2піридил)-2Н-піридазин-3-он 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,11 (3Н, с), 2,36 (3Н, с), 6,96 (1Η, д, J=7,8Гц), 7,03 (2Н, д, J=8,3Гц), 7,10 (1Η, д, J=7,8Гц), 7,23 (2Н, д, J=8,3Гц),7 ,48 (1Η, т, J=7,8Гц) Допоміжний Приклад одержання 7 8,73г гідриду натрію (55% дисперсія в маслі) суспендували в 100мл 1,4-діоксану. До цієї суспензії, в атмосфері азоту протягом 1 години при 60°С прикапували 32,03г діетилмалонату. Суміш перемішували при цій же самій температурі протягом 0,5 годин, потім, до суміші додавали 8,26г хлориду міді (І). Після цього, до суміші при 80°С прикапували розчин одержаний розчиненням 12,23г 2,3-дихлорпіридину в 50мл 1,4-діоксану. Суміш перемішували протягом 22,5 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної' температури і до реакційної суміші додавали 15мл концентрованої хлорводневої кислоти. До суміші додавали воду і етилацетат і суміш фільтрували крізь целіт. Фільтрат рідини розділяли Органічний шар промивали насиченим розсолом, сушили над безводним сульфатом магнію і концентрували при пониженому тиску. 46,65г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 3,90г діетил (3-хлор-2піридил)малонат. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,29 (6Н, т, J=7,1Гц), 4,29 (4Η, к, J=7,1Гц), 5,22 (1Η, с), 7,23 (1Η, дд, J=8,1, 4,6Гц),7,71 (1Η, дд, J=4,6, 1,5Гц), 8,49 (1Η, дд, J=4,6, 1,5Гц) Допоміжний Приклад одержання 8 Змішували 3,70г діетил (3-хлор-2піридил)малонату і 15мл диметилсульфоксиду. До суміші додавали 0,95г хлориду натрію і 0,49г води. Суміш перемішували протягом приблизно 20 хвилин при внутрішній температурі 135 - 150°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, додавали до реакційної суміші воду і екстрагували етилацетатом. Після відокремлення рідини, органічний шар двічі промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску одержуючи 2,57г етил (3-хлор-2піридил)ацетату. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,27 (3Н, т, J=7,1Гц), 4,02 (2Н, с), 4,21 (2Н, к, J=7,1Гц), 7,19 (1Η, дд, J=8,0, 4,6Гц), 7,69 (1Η, д, J=8,0Гц), 8,47 (1Η, д, J=4,6Гц) Допоміжний Приклад одержання 9 90360 44 Змішували 1,97г сполуки формули (24-і), 2,22г етил (3-хлор-2-піридил)ацетату, 4,08г етоксиду натрію (20% етанольний розчин) і 35мл етанолу. Суміш перемішували протягом 2 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші послідовно додавали лід і 6мл 1,71моль/л хлорводневої кислоти. Одержану тверду речовину збирали фільтруванням. Тверду речовину промивали послідовно водою (чотири рази), холодним етанолом (двічі) і холодним трет-бутилметиловим етером (один раз), потім, сушили, одержуючи 1,48г 5-(4хлорфеніл)-4-(3-хлор-2-піридил)-6-метил-2Нпіридазин-3-ону. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,13 (3Н, с), 7,10 (2Н, ш), 7,14 (1Η, дд, J=8,0, 4,6Гц), 7,23 (2Н, д, J=8,8Гц), 7,61 (1Η, дд, J=8,0, 1,5Гц), 8,41 (1Η, дд, J=4,6, 1,5Гц) Допоміжний Приклад одержання 10 4,80г гідрид натрію (55% дисперсія в маслі) суспендували в 50мл Ν,Ν-диметилформаміду. До суспензії протягом приблизно 0,5 годин при кімнатній температурі в атмосфері азоту прикапували 17,60г діетилмалонату. Суміш перемішували ще протягом 0,5 годин при тій же самій температурі, потім, до суміші додавали 5,73г 2-хлорпіримідин Суміш перемішували протягом 3 годин при 100°С. Реакційну суміш залишали охолоджуватись до кімнатної температури. До реакційної суміші додавали льодяну воду, екстрагували етилацетатом. Органічний шар три рази промивали насиченим розсолом, сушили над безводним сульфатом магнію і концентрували при пониженому тиску. 18,84г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 5,09г діетил (2піримідиніл)малонату. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,29 (6Н, т, J=7,1Гц), 4,29 (4Η, к, J=7,1Гц), 5,11 (1Η, с), 7,26 (1Η, т, J=5,1Гц), 8,75 (1Η, д, J=5,1Гц) Допоміжний Приклад одержання 11 Змішували 4,76г діетил (2піримідиніл)малонату і 20мл диметилсульфоксиду. До суміші додавали 1,40г хлориду натрію і 0,72г води. Суміш перемішували протягом приблизно 20 хвилин при внутрішній температурі 140-145°С, і протягом приблизно 20 хвилин при внутрішній температурі 145-148°С. Суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної' суміші додавали воду і екстрагували 45 етилацетатом. Органічний шар промивали двічі насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску одержуючи 2,12г етил (2піримідиніл)ацетат. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,27 (3Н, т, J=7,3Гц), 4,04 (2Н, с), 4,22 (2Н, к, J=7,3Гц), 7,21 (1Η, т, J=5,1Гц), 8,72 (2Н, д, J=5,1Гц) Допоміжний Приклад одержання 12 Змішували 1,97г сполуки формули (24-і), 1,84г етил (2-піримідиніл)ацетату, 4,08г етоксиду натрію (20% етанольний розчин) і 35мл етанолу. Суміш перемішували протягом 6 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури, до реакційної суміші послідовно додавали лід і 6мл 1,71моль/л хлорводневої кислоти і екстрагували етилацетатом Органічний шар промивали насиченим розсолом, сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. Одержану тверду речовину збирали фільтруванням, і тверду речовину сушили при пониженому тиску, одержуючи 1,63г 5-(4-хлорфеніл)6-метил-4-(2-піримідиніл)-2Н-піридазин-3-ону. 1 Н-ЯМР (CDCI3 +ДМСО-d6, ТМС) δ(м.ч.): 2,13 (3Н, с), 7,07 (2Н, д, J=8,8Гц), 7,13 (1Η, т, J=5,1Гц), 7,23 (2Н, д, J=8,8Гц), 8,66 (2Н, д, J=5,1Гц), 12,00 (1Η, ш с) Допоміжний Приклад одержання 13 8,73г гідриду натрію (55% дисперсія в маслі) суспендували в 100мл 1,4-діоксану. До суспензії протягом приблизно 1 години при 60°С в атмосфері азоту прикапували 32,03г діетилмалонату. Суміш перемішували ще 0,5 годин при тій же самій температурі, потім, до суміш додавали 8,26г хлориду міді (І). Після цього, до суміші прикапували розчин одержаний розчиненням 15,00г 2-хлор-3(трифторметил)піридину в 50мл 1,4-діоксану при 80°С. Суміш перемішували протягом 16 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури і до реакційної суміші додавали 15мл концентрованої хлорводневої кислоти. До суміші додавали воду і етилацетат і суміш фільтрували крізь целіт Фільтрат рідини розділяли. Органічний шар промивали насиченим розсолом, сушили над безводним сульфатом магнію і концентрували при пониженому тиску. 51,14г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 6,90г діетил (3-трифторметил-2піридил)малонату. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,27 (6Η, т, J=7,1Гц), 4,27 (4Η, к, J=7,1Гц), 5,21 (1Η, с), 7,40 (1Η, дд, J=8,0, 4,9Гц), 7,99 (1Η, д, J=8,0Гц), 8,80 (1Η, д, J=4,9Гц) 90360 46 Допоміжний Приклад одержання 14 Змішували 6,10г діетил (3-трифторметил-2піридил)малонату і 20мл диметилсульфоксиду. До суміші додавали 1,40г хлориду натрію і 0,72г води. Суміш перемішували протягом приблизно 20 хвилин при внутрішній температурі 132-145°С Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші додавали воду і екстрагували етилацетатом. Органічний шар промивали двічі насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску, одержуючи 4,64г етил (3-трифторметил-2-піридил)ацетату. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,25 (3Н, т, J=7,1Гц), 4,06 (2Н, с), 4,20 (2Н, к, J=7,1Гц), 7,35 (1Η, дд, J=8,0, 4,9Гц), 7,97 (1Η, д, J=8,0Гц), 8,75 (1Η, д, J=4,9Гц) Допоміжний Приклад одержання 15 Змішували 1,97г сполуки формули (24-і), 2,33г етил (3-трифторметил-2-піридил)ацетату, 3,40г етоксиду натрію (20% етанольний розчин) і 35мл етанолу. Суміш перемішували протягом 5 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші послідовно додавали лід і 8,3мл 1,2моль/л хлорводневої кислоти і екстрагували етилацетатом. Органічний шар промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 2,93г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,92г 5-(4хлорфеніл)-6-метил-4-(3-трифторметил-2піридил)-2Н-піридазин-3-ону. 1 Н-ЯМР (CDCI3 +ДMCO-d6 одна крапля, ТМС) б(м.ч): 2,13 (3Н, с), 7,06 (2Н, ш), 7,20 (2Н, ш д), 7,30-7,35 (1Η), 7,87 (1Η, д), 8,75 (1Η, д) Допоміжний Приклад одержання 16 Суміш 4,56г 2,3,5-трихлорпіридину, 8,80г діетилмалонату, 30мл диметилсульфоксиду і 17,9г карбонату цезію перемішували протягом 8 годин при 110°С в атмосфері азоту. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до неї додавали льодяну воду і екстрагували етилацетатом. Органічний шар двічі промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 7,45г одержаного залишку піддавали колонковій хроматографії на силікагелі, 47 одержуючи 7,08г діетил (3,5-дихлор-2піридил)малонату. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,28 (6Н, т, J=7,1Гц), 4,28 (4Η, κ, J=7,1Гц), 5,16 (1Η, с), 7,74 (1Η, д, J=2,2Гц), 8,45 (1Η, д, J=2,2Гц) Допоміжний Приклад одержання 17 Змішували 6,75г діетил (3,5-дихлор-2піридил)малонату і 20мл диметилсульфоксиду. До суміші додавали 1,57г хлориду натрію і 0,79г води. Суміш перемішували протягом приблизно 40 хвилин при внутрішній температурі 135-150°С. Суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші додавали воду і екстрагували етилацетатом. Органічний шар промивали двічі насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску, одержуючи 4,76г етил (3,5-дихлор-2-піридил)ацетату. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,25 (3Н, т, J=7,1Гц), 3,98 (2Н, с), 4,18 (2Н, к, J=7,1Гц), 7,72 (1Η, д, J=2,2Гц), 8,42 (1Η, д, J=2,2Гц) Допоміжний Приклад одержання 18 Змішували 3,74г сполуки формули (24-і), 4,47г етил (3,5-дихлор-2-піридил)ацетату, 6,46г етоксиду натрію (20% етанольний розчин) і 50мл етанолу. Суміш перемішували протягом 2 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші додавали лід і 10мл 1,71моль/л хлорводневої кислоти. Тверду речовину збирали фільтруванням. Тверду речовину послідовно промивали водою (чотири рази), холодним етанолом (двічі) і холодним третбутилметиловим етером (один раз), потім, сушили одержуючи 3,51г твердої речовини. До цієї твердої речовини додавали 50мл бутанолу і суміш перемішували протягом 20 хвилин на масляній бані при 120°С, потім охолоджували. Тверду речовину збирали фільтруванням і промивали сумішшю третбутилметиловий етер і гексан, одержуючи 2,71г 5(4-хлорфеніл)-4-(3,5-дихлор-2-піридил)-6-метил2Н-піридазин-3-ону. 1 Н-ЯМР (CDCI3 +ДМСО-d6 одна капля, ТМС) δ(м.ч.): 2,12 (3Н, с), 7,08 (2Н, ш), 7,26 (2Н, д, J=8,8Гц), 7,64 (1Η, д, J=2,0Гц), 8,37 (1Η, д, J=2,0Гц), 12,18 (1Η, ш с), Допоміжний Приклад одержання 19 Суміш 3,73г 2,3-дихлорпіразину, 8,80г діетилмалонату, 30мл диметилсульфоксиду і 17,9г карбонату цезію перемішували протягом 8 годин при 110°С в атмосфері азоту. Реакційну суміш зали 90360 48 шали охолоджуватись до кімнатної температури, потім, до неї додавали льодяну воду і екстрагували етилацетатом. Органічний шар двічі промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 3,67г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 2,69г діетил (3-хлор-2піразиніл)малонату. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,27 (6Н, т, J=7,2Гц), 4,30 (4Η, κ, J=7,2Гц), 5,20 (1Η, с), 8,36 (1Η, д, J=2,6Гц), 8,50 (1Η, д, J=2,6Гц) Допоміжний Приклад одержання 20 Змішували 2,42г діетил (3-хлор-2піразиніл)малонату і 15мл диметилсульфоксиду До суміші додавали 0,62г хлориду натрію і 0,32г води. Суміш перемішували протягом приблизно 35 хвилин при внутрішній температурі 127-153°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші додавали воду і екстрагували етилацетатом. Органічний шар двічі промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску, одержуючи 1,53г етил (3-хлор-2-піразиніл)ацетат 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,27 (3Н, т, J=7,1Гц), 4,09 (2Н, с), 4,22 (2Н, к, J=7,1Гц), 8,31 (1Η, д, J=2,4Гц), 8,47 (1Η, д, J=2,4Гц) Допоміжний Приклад одержання 21 Змішували 1,32г сполуки формули (24-і), 1,35г етил (3-хлор-2-піразил)ацетату, 2,29г етоксиду натрію (20% етанольний розчин) і 20мл етанолу. Суміш перемішували протягом 2 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші послідовно додавали лід і 3,5мл 1,71моль/л хлорводневої кислоти. Тверду речовину збирали фільтруванням. Тверду речовину послідовно промивали водою (чотири рази), холодним етанолом (двічі) і холодним третбутилметиловим етером (один раз), потім, сушили одержуючи 1,18г 5-(4-хлорфеніл)-4-(3-хлор-2піразил)-6-метил-2Н-піридазин-3-ону. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,15 (3Н, с), 7,08 (2Н, ш д, J=8,2Гц), 7,26 (2Н, д, J=8,2Гц), 8,26 (1Η, д, J=2,4Гц), 8,42 (1Η, д, J=2,4Гц) Допоміжний Приклад одержання 22 Суміш 4,29г 3,6-дихлор-4-метилпіридазинц, 8,80г діетилмалонату, 25мл диметилсульфоксиду і 17,9г карбонату цезію перемішували протягом 4 49 годин при 110°С в атмосфері азоту. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до неї додавали льодяну воду і екстрагували етилацетатом. Органічний шар двічі промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 7,08г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 1,95г діетил (6-хлор-4-метил-3піридазиніл)малонату. 1 Н-ЯМР (CDCI3, ТМС) δ(м ч.): 1,30 (6Н, т, J=7,2Гц), 2,32 (3Η, с), 4,28 (4Η, κ, J=7,2Гц), 5,17 (1Η, с), 7,36 (1Η, с) Допоміжний Приклад одержання 23 Змішували 1,81г діетил (6-хлор-4-метил-3піридазиніл)малонату і 15мл диметилсульфоксиду. До суміші додавали 0,45г хлориду натрію і 0,23г води. Суміш перемішували протягом приблизно 40 хвилин при внутрішній температурі 125150°С Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші додавали воду і екстрагували етилацетатом. Органічний шар двічі промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 1,05г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,91г етил (6-хлор-4-метил-3-піридазиніл)ацетату. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,27 (3Н, т, J=7,2Гц), 2,34 (3Η, с), 4,07 (2Н, с), 4,20 (2Н, κ, J=7,2Гц), 7,33 (1Η, с) Допоміжний Приклад одержання 24 Змішували 0,69г сполуки формули (24-і), 0,75г етил (б-хлор-4-метил-3-піридазиніл)ацетату, 1,19г етоксиду натрію (20% етанольний розчин) і 10мл етанолу Суміш перемішували протягом 2 годин при кип'ятінні із зворотнім холодильником Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, послідовно додавали лід і 2,4мл 1,2моль/л хлорводневої кислоти і воду. До реакційної суміші додавали воду і екстрагували етилацетатом. Органічний шар промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 1,06г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,37г 5-(4-хлорфеніл)-4-(6-хлор-4-метил-3-піридазиніл)6-метил-2Н-піридазин-3-ону. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,15 (3Н, с), 2,22 (3Н, с), 6,75-6,9 (2Н, ш), 7,28 (1Η, с), 7,2-7,4 (2Н, ш), 11,63 (1Η, ш с) Допоміжний Приклад одержання 25 90360 50 Суміш 3,85г 5-хлор-2,3-дифторпіридину, 8,80г діетилмалонату, 25мл диметилсульфоксиду і 17,9г карбонату цезію перемішували протягом 4,5 годин при 110°С в атмосфері азоту. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до неї додавали льодяну воду і екстрагували етилацетатом. Органічний шар двічі промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску, одержуючи 5,83г діетил (5хлор-3-фтор-2-піридил)малонату. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,29 (6Н, т, J=7,1Гц), 4,28 (4Η, κ, J=7,1Гц), 5,03 (1Η, с), 7,49 (1Η, дд, J=9,0, 2,0Гц), 8,39 (1Η, д, J=2,0Гц) Допоміжний Приклад одержання 26 Змішували 5,83г діетил (5-хлор-3-фтор-2піридил)малонату і 25мл диметилсульфоксиду. До суміші додавали 1,29г хлориду натрію і 0,72г води. Суміш перемішували протягом приблизно 40 хвилин при внутрішній температурі 135-142°С Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші додавали воду і екстрагували етилацетатом. Органічний шар двічі промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 4,03г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 3,16г етил (5-хлор3-фтор-2-піридил)ацетату. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,26 (3Н, т, J=7,1Гц), 3,92 (2Н, с), 4,21 (2Н, к, J=7,1Гц),7,46 (1Η, дд, J=8,8, 2,0Гц), 8,36 (1Η, д, J=2,0Гц) Допоміжний Приклад одержання 27 Змішували 0,88г сполуки формули (24-і), 1,24г етил (5-хлор-3-фтор-2-піридил)ацетату, 1,71г етоксиду натрію (20% етанольний розчин) і 15мл етанолу. Суміш перемішували протягом 2 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші послідовно додавали лід і 1,7моль/л хлорводневої кислоти і воду, і екстрагували етилацетатом. Органічний шар промивали насиченим розсолом, і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 1,43г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 0,40г 5-(4-хлорфеніл)-4-(5-хлор-3фтор-2-піридил)-6-метил-2Н-піридазин-3-ону. 51 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч ): 2,13 (3Н, с), 6,957,15 (2Н, ш), 7,28 (2Н, д, J=8,8Гц), 7,35 (1Η, дд, J=8,6, 2,0Гц), 8,33 (1Η) Допоміжний Приклад одержання 28 Змішували 0,36г сполуки формули (24-і), 0,37г етил (3,5-дифтор-2-піридил)ацетату, 0,63г етоксиду натрію (20% етанольний розчин) і 10мл етанолу. Суміш перемішували протягом 2 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші послідовно додавали лід і 1,0мл 1,2моль/л хлорводневої кислоти і екстрагували етилацетатом. Органічний шар промивали насиченим розсолом, і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 0,54г одержаного залишку піддавали колонковій хроматографії на силікагелі (градієнт гексан-етилацетат), одержуючи 0,14г 5-(4-хлорфеніл)-4-(3,5-дифтор-2-піридил)-6-метил2Н-піридазин-3-ону. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,13 (3Н, с), 6,957,15 (2Н, ш), 7,10 (2Н, д, J=7,8Гц), 8,26 (1Η, д, J=2,4Гц), 10,94 (1Η, ш) Допоміжний Приклад одержання 29 Суміш 3,95г 2,3-дифторпіридину, 13,2г діетилмалонату, 38мл диметилсульфоксиду і 26,85г карбонату цезію перемішували протягом 3 годин при 100°С в атмосфері азоту. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до неї додавали льодяну воду і екстрагували етилацетатом Органічний шар промивали насиченим розсолом двічі і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 12,18г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 6,38г діетил (3-фтор-2піридил)малонату. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,28 (6Н, т, J=7,2Гц), 4,28 (4Η, κ, J=7,2Гц), 5,08 (1Η, с), 7,30 (1Η, м), 7,43 (1Η, м), 8,41 (1Η) Допоміжний Приклад одержання 30 Змішували 5,10г діетил (3-фтор-2піридил)малонату і 25мл диметилсульфоксиду До суміші додавали 1,29г хлориду натрію і 0,72г води. Суміш перемішували протягом приблизно 40 хвилин при внутрішній температурі 145-152°С. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші додавали воду і екстрагували етилацетатом. Органічний шар двічі промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, 90360 52 концентрували при пониженому тиску, одержуючи 2,99г етил (3-фтор-2-піридил)ацетату. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 1,26 (3Н, т, J=7,2Гц), 3,92 (2Н, с), 4,19 (2Н, к, J=7,2Гц), 7,23 (1Η, м), 7,39 (1Η, м), 8,38 (1Η, м) Допоміжний Приклад одержання 31 Змішували 1,97г сполуки формули (24-і), 1,83г етил (3-фтор-2-піридил)ацетату, 4,08г етоксиду натрію (20% етанольний розчин) і 25мл етанолу. Суміш перемішували протягом 2 годин при кип'ятінні із зворотнім холодильником. Реакційну суміш залишали охолоджуватись до кімнатної температури, потім, до реакційної суміші послідовно додавали лід і 8мл 1,2моль/л хлорводневої кислоти і екстрагували етилацетатом Органічний шар промивали насиченим розсолом і сушили над безводним сульфатом магнію, потім, концентрували при пониженому тиску. 2,62г одержаного залишку піддавали колонковій хроматографії на силікагелі, одержуючи 1,32г 5-(4-хлорфеніл)-4-(3-фтор-2піридил)-6-метил-2Н-піридазин-3-ону. 1 Н-ЯМР (CDCI3, ТМС) δ(м.ч.): 2,13 (3Н, с), 6,957,15 (2Н, ш), 7,15-7,35 (4Η), 8,34 (1Η, м), 10,91 (1Η, ш с) Далі приведені приклади рецептур. Тут частки є ваговими. Приклад рецептури 1 50 частин кожної із сполук (1)-(16) представленого винаходу, 3 частини лігнінсульфонату кальцію, 2 частини лаурилсульфату магнію і 45 частин синтетичного гідратованого оксиду кремнію розмелювали і змішували разом одержуючи змочувані порошки. Приклад рецептури 2 Змішували 20 частин кожної із сполук (1)-(16) представленого винаходу і 1,5 частин триолеату сорбіту з 28,5 частинами водного розчину, що містить 2 частини полівінілового спирту і добре розмелювали використовуючи вологе розмелювання, потім, до суміші додавали 40 частин водного розчину, що містить 0,05 частин ксантанової смоли і 0,1 частину силікату алюмінію магнію, і також, додавали 10 частин пропіленгліколю і змішували при перемішуванні одержуючи рецептури, що течуть. Приклад рецептури 3 2 частини кожної із сполук (1)-(16) представленого винаходу, 88 частин каоліну і 10 частин тальку розмелювали і змішували разом одержуючи дуети. Приклад рецептури 4 5 частин кожної із сполук (1)-(16) представленого винаходу, 14 частин поліоксиетиленстирилфенілового етеру, 6 частин додецилбензолсульфонату кальцію і 75 частин ксилену змішували разом одержуючи концентрати, що емульсифікуються. Приклад рецептури 5 2 частини кожної із сполук (1)-(16) представленого винаходу, 1 частину синтетичного гідрато 53 90360 ваного оксиду кремнію, 2 частини лігнінсульфонату калцыю, 30 частин бентоніту і 65 частин каоліну розмелювали і змішували разом, потім, додавали воду і добре вимішували, гранулювали і сушили, одержуючи гранули. Приклад рецептури 6 Змішували 10 частин кожної із сполук (1)-(16) представленого винаходу, 35 частин білого графіту, що містить 50ваг.% сульфатамонієвої солі поліоксиетиленалкілового етеру і 55 частин води і добре подрібнювали використовуючи вологе подрібнення, одержуючи рецептури. Далі в прикладах тестування буде показана ефективність сполуки представленого винаходу для контролю захворювань рослин. Приклад тестування 1 Пластиковий горщик наповнювали піщаним суглинком, висівали японську редьку (сорт: WASE 40 днів) і вирощували в теплиці 5 днів. Рецептури сполук (1)-(3), (5), (6), (9)-(12) і (14)-(16) представленого винаходу одержані згідно з Прикладом рецептури 6 розводили водою одержуючи концентрацію 500м.ч.. Одержані розведені рідини розпилювали на стебла і листя так щоб вони були достатньо добре прилипали до поверхні листя згаданої вище редьки. Після розпилення, рослини сушили на повітрі і інокулювали спори Alternaha brassicicola. Потім редьку тримали протягом ночі при 23°С у вологому середовищі, і потім залишали стояти протягом 3 днів у теплиці, а потім, перевіряли контролюючу дію. Як результат, площі пошкодження на редьці обробленій сполуками (1)-(3), (5), (6), (9)-(12) і (14)-(16) представленого винаходу було 30% або менше порівняно із площею пошкодження на необроблених зразках. Приклад тестування 2 Пластиковий горщик наповнювали піщаним суглинком, висівали огірки (сорт SAGAMI HANJIRO) і вирощували у теплиці 10 днів. Рецептури сполук (1)-(3), (5)-(16) представленого винаходу одержані згідно з Прикладом рецептури 6 розводили водою одержуючи концентрацію 500м.ч.. Одержані розведені рідини розпилювали на стебла і листя так щоб вони були достатньо добре прилипали до поверхні листя згаданих вище огірків. Після розпилення, рослини сушили на повітрі, і PDA середовище, що містить пори Botrytis cinema поміщали на поверхню сім'ядоль огірка. Потім огірок залишали на 5 днів при 12°С у вологому середовищі, потім, Комп’ютерна верстка Т. Чепелева 54 візуально оцінювали площу плями захворювання рослини. Як результат, площі пошкодження на огірку обробленому сполуками (1)-(3), (5)-(16) представленого винаходу було 50% або менше порівняно із площею пошкодження на необроблених зразках. Приклад тестування 3 Пластиковий горщик наповнювали піщаним суглинком, висівали рис (сорт: NIHONBARE) і вирощували у теплиці протягом 20 днів. Рецептури сполук (1)-(3), (5)-(16) представленого винаходу одержані згідно з Прикладом рецептури 6 розводили водою одержуючи концентрацію 200м.ч.. Одержані розведені рідини розпилювали на стебла і листя так щоб вони були достатньо добре прилипали до поверхні листя згаданого вище рису. Після розпилення, рослини сушили на повітрі. Культивований на висівках міцелій Rhizoctonia solani поміщали навколо низу стебла рису і залишали на 6 днів при 28°С у вологому середовищі. Після цього, перевіряли контролюючу дію. Як результат, площі пошкодження на рисі обробленому сполуками (1)-(3), (5)-(16) представленого винаходу було 50% або менше порівняно із площею пошкодження на необроблених зразках. Приклад тестування 4 Пластиковий горщик наповнювали піщаним суглинком, висівали огірки (сорт: SAGAMI HANJIRO) і вирощували в теплиці протягом 12 днів. Рецептури сполук (1)-(3), (5)-(7), (9)-(12) і (14)-(16) представленого винаходу одержані згідно з Прикладом рецептури 6 розводили водою одержуючи концентрацію 200м.ч.. Одержані розведені рідини розпилювали на стебла і листя так щоб вони були достатньо добре прилипали до поверхні листя згаданих вище огірків. Після розпилення, рослини сушили на повітрі і інокулювали спори Sphaerotheca fuliginea. Потім огірок залишали на 12 днів при 23°С, а потім, перевіряли контролюючу дію. Як результат, площі пошкодження на огірку обробленому сполуками (1)-(3), (5)-(7), (9)-(12) і (14)-(16) представленого винаходу були 10% або менше порівняно із площею пошкодження на необроблених зразках. Промислова придатність Використовуючи сполуки представленого винаходу можна контролювати захворювання рослин. Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюPyridazine compound, use thereof, agent and method for plant disease control, and intermediate
Автори англійськоюManabe Akio
Назва патенту російськоюПиридазинова соединение, его применение, агент и способ контролирования заболевания растений, а также промежуточное соединение
Автори російськоюМанабе Акио
МПК / Мітки
МПК: A61P 3/00, A01N 43/58, C07D 403/04, C07D 401/04
Мітки: рослин, піридазинова, контролювання, захворювання, спосіб, проміжна, застосування, агент, також, сполука
Код посилання
<a href="https://ua.patents.su/27-90360-piridazinova-spoluka-zastosuvannya-agent-ta-sposib-kontrolyuvannya-zakhvoryuvannya-roslin-a-takozh-promizhna-spoluka.html" target="_blank" rel="follow" title="База патентів України">Піридазинова сполука, її застосування, агент та спосіб контролювання захворювання рослин, а також проміжна сполука</a>
Попередній патент: Добавка до цементних сумішей
Наступний патент: Спосіб створення пікової потужності на енергоблоках теплових електростанцій та енергоблок теплової електростанції для його здійснення
Випадковий патент: Установка відвантаження вапна































