Спосіб екстракційно-фотометричного визначення кобальту
Номер патенту: 20973
Опубліковано: 07.10.1997
Автори: Студеняк Ярослав Іванович, Базель Ярослав Рудольфович, Кушнір Лариса Миколаївна, Зимомря Іван Іванович, Толмачев Андрій Олексійович
Формула / Реферат
Спосіб екстракційно-фотометричного визначення кобальту, який передбачає зв'язування кобальту в іонний асоціат з роданід-іонами і органічною основою у водно-органічному середовищі, екстракцію комплексу толуолом 1 наступне фотометрування екстрактів, який відрізняється тим, що в якості органічної основи використовують ціаніновий барвник 6-нітродиметиліндокарбоціанін, зв'язування в комплексну сполуку проводять в присутності 8-16 об. % диметил-формаміду при концентрації роданід-іонів і барвника 1,5-2,5 М і (1,0-1,6) • 10-4 M відповідно, в середовищах з рН = 4 -10.
Текст
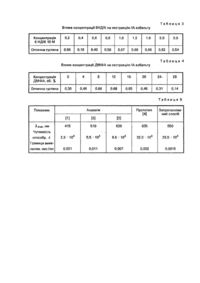
Винахід відноситься до аналітичної хімії, а саме до способів екстракційно-фотометричного визначення кобальту, і може бути використаний для аналізу різноманітних матеріалів з низьким вмістом кобальту. Для фотометричного визначення кобальту найбільш часто використовуть сполуки, що містять функціональну групу: ; 1-нітрозо-2-нафтол: 2-нітрозо-1-нафтол; 1-нітрозо-2-оксі-3,6нафталіндисульфокисло-ту [Пятницкий И.В., Сухан В.В. Аналитическая химия кобальта. М., Наука, 1975,253 с]. Найбільш чутливим та селективним реактивом є 1-нітрозо-2-нафтол (кобальтон). Комплекс цього реактиву з кобальтом має оранжеве забарвлення, молярний коефіцієнт поглинання при l mах = 415 нм складає 2,9-104. Для екстрагування комплексу частіше використовують хлороформ або ССl4. Недоліком способу є недостатньо висока чутливість та вибірковість. Визначенню кобальту заважають багато елементів, в їх числі Cu, Fe, Ni та ін. Крім цього, реакція проходить досить повільно (необхідно витримувати розчини 20-30 хв). Більш чутливим реактивом на кобальт є 1-(2-пірідiлазо)-резорцин. Молярний коефіцієнт світлопоглинання комплексу при l mах = 510 нм рівний 5,5-104 [Иванов В.М. Гетероциклические азотсодержащие азосо-единения. М., Наука, 1982, 270 с]. До. недоліків способу слід віднести вузьк! межі оптимальної кислотності комплексоутворення та екстракції (рН 8-9), а також невисоку вибірковість. Визначенню кобальта заважають ряд елементів, що утворюють з 1-(2-пiріділазо)-резорцином комплекси, i елементи, які гідролізують при рН >8 (Ni, Fe, Cu, Sn та Ін.). Відомий також метод екстракційно-фотометричного визначення кобальту, що базується на екстрації кобальту у вигляді Іонного асоціату (ІА) з роданід-іонами І малахітовим зеленим [Журн. аналит. химии. 1973, Т.28, N= 10, с. 1999-2003]. ІА утворюється у водній фазі при рНопт = 9-11 І екстрагується сумішшю ССІд І циклогексано-ну (7:1). При l mах = 630 нм молярний коефіцієнт світлопоглинання складає e = 8,6 • 104. Недоліком методу є: невисока вибірковість, низька стійкість барвника при стоянні у водному та органічному середовищах, значне вилучення простої солі барвника. Найбільш близьким по технологічній сутності та досягаємим результатам є спосіб екстракційнофотометричного визначення кобальту, що базується на утворенні та. екстракції іонного асоціату кобальту з роданід-іонами І бістриметинціаніном [Авт.св. СССР № 1606932, опублик. 1990]. ІА, що утворюється у водному середовищі при концентрації роданід-Іонів та барвника 0,2-0,4 М і (0,4-0,6) • 10~4 М відповідно екстрагується сумішшю толуолу з цикло-гексаноном в співвідношенні 3:2. При lmах = 635 нм молярний коефіцієнт поглинання e = 32,0*104. Недоліком способу є низька вибірковість. В рекомендованих авторами умовах разом Із кобальтом вилучаються елементи, що утворюють стійкі роданідні комплекси - цинк, ртуть, паладій, олово, золото, мідь, кадмій, титан, молібден, вольфрам та ін. Крім цього, сумішшю толуолу з циклогексано-ном в значній мірі екстрагується і проста (роданідна) сіль барвника, що безперечно погіршує метрологічні характеристики методики. Складність синтезу бістриметинціаніну та його низький вихід [Журн. орг. химии, 1987, т. 23, Ns 10, с. 2212-2215], що рівнозначно високій вартості, є несприятливими факторами, які обмежують практичне застосування способу для серійного аналізу. Завдання винаходу - підвищення вибірковості, чутливості і точності аналізу. Поставлене завдання вирішується завдяки тому, що запропонований спосіб екстраційно-фотомеричного визначення кобальту передбачає зв'язування кобальту в іонний асоціат з роданід-іонами І органічною основою у водно-органічному середовищі, екстраціютолуолом і наступне фотометрування екстрактів, і який відрізняється тим, що згідно винаходу використовують органічну основу - ціаніновий барвник 6нІтродиметиліндокарбоціанІн, а зв'язування Со в комплексну сполуку проводять в присутності 8-16 об.% диметил-формаміду при концентрації роданід-Іонів та барвника 1,5-2,5 М І (1,0-1,6)• 10-4 М відповідно, в середовищах з рН 4-10. Структурна формула барвника: Барвник синтезується досить легко І з хорошим виходом (80-90%), конденсацією 6-нітрозаміщеної основи Фішера з альдегідом Фшшера, які легко одержати із промислово доступної основи Фішера [Чукаев Ю.М., Прильянговская Н.М. 2-Метиленин-долиевые основания. Синтез и свойства // Итоги науки и техники. М., ВИНИТИ, 1990, т. 14, 127 с]. Водні розчини барвника стійкі більше 1 місяця і володіють інтенсивним забарвленням. Рівновага екстрації ІА кобальту встановлюється за 30 с, забарвлення екстрактів не змінюється протягом 4 годин. Світлопоглинання забарвлених екстрактів підлягає закону Бера вдіапазоні концентрацій кобальту 0,001-1,2 мкг/мл. Визначенню кобальту запропонованим способом не заважають 10-10 кратні кількості лужних, лужноземельних елементів, а також Мп (II), At, Cd, Cr (III), Ni, Fe (II), Ga, 10-50 кратні кількості золота, міді, срібла маскуються тіосульфатом та тіосечовиною. Нижче приводяться експериментальні дані (табл. 1-4), які доказують суттєвість концентрацій Іонів водню (рН), роданіду натрію, барвника 6НДІК та диметилформаміду. Дослідження проводили таким чином. В градуйовані побірки з притертими пробками вносять 9,43 мкг кобальту, добавляють 0,1-1,0 мл 10 М розчину роданіду натрію. 0,1-1,5 мл диметилформаміду, 0,1-1,5 мл 10 М розчину барвника 6НДІК і ацетатноамонійним буферним розчином доводять об'єм до 5 мл. Приливають рівний об'єм толуолу І екстрагують ЗО сек. Органічний шар відокремлюють, центрифугують І вимірюють оптичну густину (А) в 0,1 см кюветах на фото-електроколориметрі КФК 2М при l еф = 540 нм відносно екстракту контрольного досліду (без кобальту). Дані, приведені в табл. 1-4 свідчать, що чутливість визначення кобальту згідно даного способу, максимальна в широкому інтервалі рН 4-10, при концентрації роданіду натрію, барвника 6НДІК та диметилформаміду 1,5-2,5 М; (1,0-1,6)-104 М I 8-16 об.% відповідно. Важливість присутності у водній фазі до-норно-активного розчинника диметил-формаміду зумовлена тим, що кобальт вилучається основними барвниками у вигляді координаційно-ненасичених комплексів [Co(NCS)3H2O]-R+. Такого типу комплекси слабо екстрагуються Інертними розчинниками, тому молярний коефіцієнт світлопоглинання ІА не високий. При екстрації активними розчинниками, вилучення ІА стає неселективним, крім цього, такими розчинниками значно вилучаються прості солі барвника І різниця оптичних густин екстрактів ІА і простої солі (без кобальту) невелика. Донорно-активний розчинник ДМФА витісняє (блокує) молекулу води Із внутрішньої координаційної сфери, а також сприяє утворенню координаційно-насичених комплексів типу [Co(SCN)4]2-, тому в присутності ДМФА ІА кількісно вилучаються Інертними розчинниками, і, як результат -різко зростає чутливість методу. Крім ДМФА, можна використовувати також диметилсульфоксид, метилформамід, гексаме-тилфосфортриамід; проте по ряду критеріїв кращим є ДМФА. В даному випадку екстрація ІА кобальту максимальна і найменше екстрагується проста сіль барвника, і зв'язку з чим чутливість методу максимальна. Молярний коефіцієнт світлопоглинання при l mах = 550 нм рівний e = 26,5 • 104. Запропонований нами спосіб екстракційнофотометричного визначення кобальту по вибірковості перевершує всі найбільш чутливі методи, а високий молярний коефіцієнт світлопоглинання при низьких значеннях с компл/ е реактиву та хорошій відтворюваності дозволяє також стверджувати, що даний спосіб перевершує по чутливості всі відомі методи (табл.5). Все це дозволяє використовувати даний спосіб для визначення мікрокількостей кобальту в складних і різноманітних об'єктах (сплави, високочисті речовини, напівпровідникові матеріали). Приклад, Визначення кобальту в стандартному зразку нікелевого сплаву НП. Склад сплаву, %: Со (0,023); SI (0,22); Mn (0,0046); Pb (0,0059) Bi (0,0087); Sb (0,0045); Zn (0,0061); Sb (0,0047); Al (0,038); Ni; Cu. Наважку 0,5 г нікелевого сплаву розчиняли в 5 мл HNO3 (1:1) При нагріванні, доливали 1 мл H2SO4 (конц.) і упарювали до появи білих парів. Залишок розчиняли в бідистильованій воді, переводили в мірну колбу І доводили об'єм до 100 мл бідистилятом. Відбирали аліквоту (1 мл) в градуйовані пробірки з притертими пробками, добавляли 0,5 мл 1 М розчину тіосечовини, 1 мл 10 М розчину NaSCN, 0,5 мл ДМФА, 0,6 • 10-3 М розчину 6НДІК і доводили ацетатно-аміачним буферним розчином з рН 5 об'єм до 5 мл. Приливали 5 мл толуолу І перемішували суміш 30 сек. Екстракт відділяли, центрифугували, після чого вимірювали оптичну густину на фото-електроколориметрі КФК-2М при А l еф= 540 нм в 0,1 см кюветах відносно екстракту контрольного розчину. Кількість кобальту знаходили по калібрувальному графіку, побудованому аналогічно, або методом добавок. Знайдено 0,024% кобальту, відносне стандартне відхилення S2 = 0,026 (n = 5; Р = 0,95). Винахід може бути використаний для аналізу матеріалів з низьким вмістом кобальту в заводських та науково-дослідних лабораторіях.
ДивитисяДодаткова інформація
Автори англійськоюBasel Yaroslav Rudolfovych, Kyshnir Larysa Mykolaivna, Studeniak Yaroslav Ivanovych, Zymomria Ivan Ivanovych, Tolmachov Andrii Oleksiiovych
Автори російськоюБазель Ярослав Рудольфович, Кушнир Лариса Николаевна, Студеняк Ярослав Иванович, Зымомря Иван Иванович, Толмачев Андрей Алексеевич
МПК / Мітки
МПК: G01N 31/22
Мітки: екстракційно-фотометричного, спосіб, кобальту, визначення
Код посилання
<a href="https://ua.patents.su/3-20973-sposib-ekstrakcijjno-fotometrichnogo-viznachennya-kobaltu.html" target="_blank" rel="follow" title="База патентів України">Спосіб екстракційно-фотометричного визначення кобальту</a>
Попередній патент: Пристрій для знищення комах
Наступний патент: Відстійник
Випадковий патент: Спосіб лікування гнійно-фібринозного перитоніту у хворих з гострими хірургічними захворюваннями