Солі та кристалічні форми 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-с]хінолін-1-іл)феніл]пропіонітрилу
Номер патенту: 98473
Опубліковано: 25.05.2012
Автори: Штовассер Франк, Гарад Судхакар Девідасрао, Бенцігер Маркус
Формула / Реферат
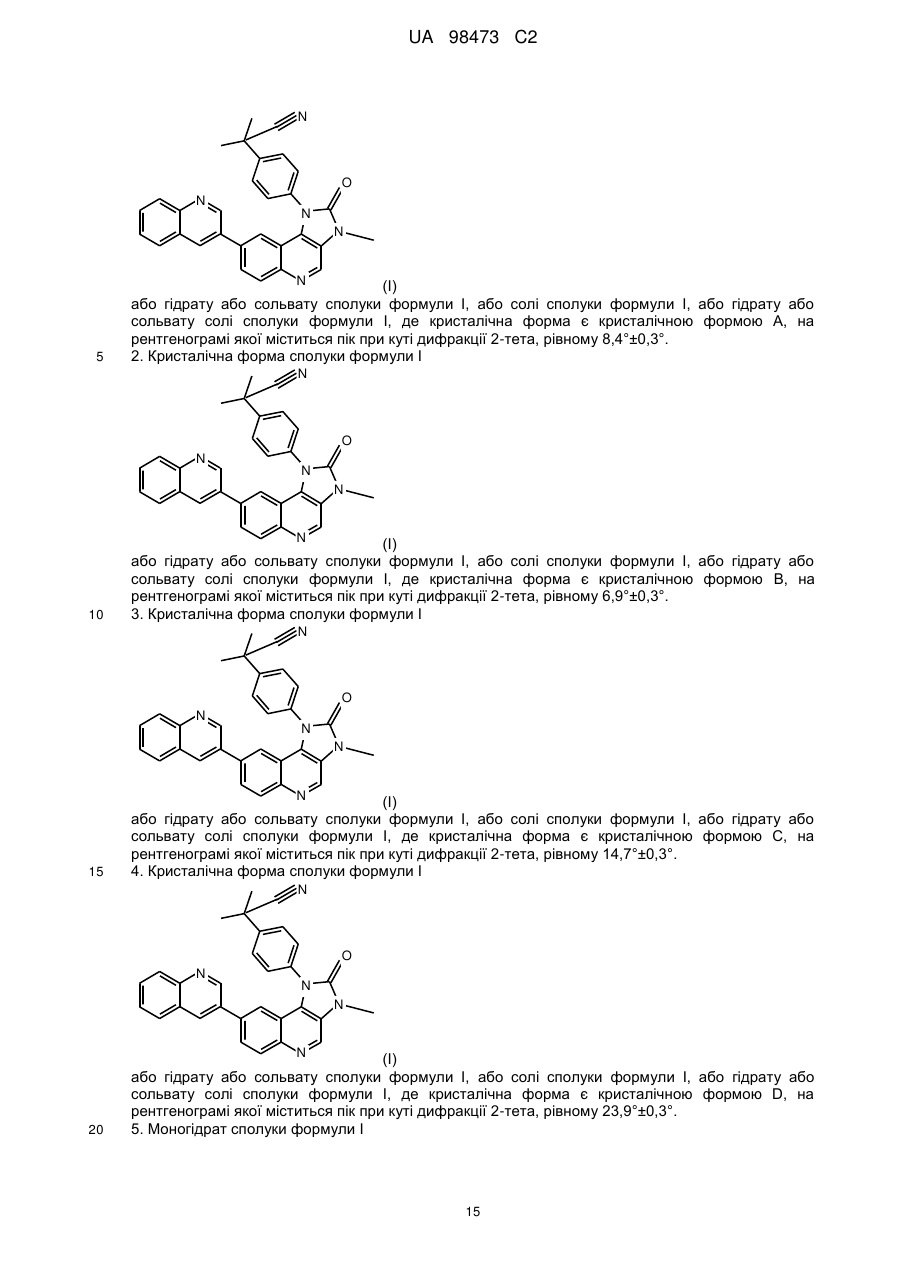
1. Кристалічна форма сполуки формули І
 (І)
(І)
або гідрату або сольвату сполуки формули І, або солі сполуки формули І, або гідрату або сольвату солі сполуки формули І, де кристалічна форма є кристалічною формою А, на рентгенограмі якої міститься пік при куті дифракції 2-тета, рівному 8,4°±0,3°.
2. Кристалічна форма сполуки формули І
 (І)
(І)
або гідрату або сольвату сполуки формули І, або солі сполуки формули І, або гідрату або сольвату солі сполуки формули І, де кристалічна форма є кристалічною формою В, на рентгенограмі якої міститься пік при куті дифракції 2-тета, рівному 6,9°±0,3°.
3. Кристалічна форма сполуки формули І
 (І)
(І)
або гідрату або сольвату сполуки формули І, або солі сполуки формули І, або гідрату або сольвату солі сполуки формули І, де кристалічна форма є кристалічною формою С, на рентгенограмі якої міститься пік при куті дифракції 2-тета, рівному 14,7°±0,3°.
4. Кристалічна форма сполуки формули І
 (І)
(І)
або гідрату або сольвату сполуки формули І, або солі сполуки формули І, або гідрату або сольвату солі сполуки формули І, де кристалічна форма є кристалічною формою D, на рентгенограмі якої міститься пік при куті дифракції 2-тета, рівному 23,9°±0,3°.
5. Моногідрат сполуки формули І
 (І)
(І)
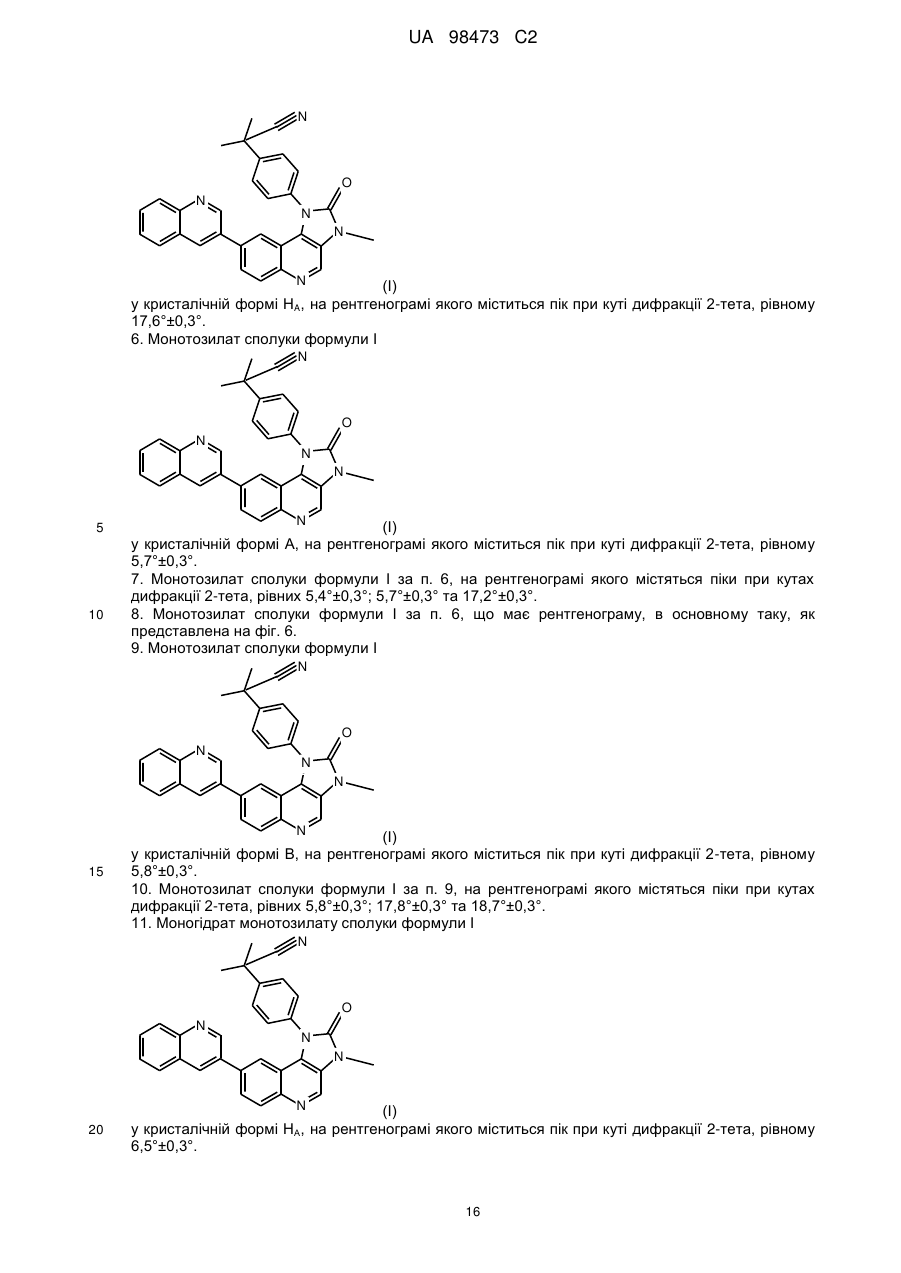
у кристалічній формі НA, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 17,6°±0,3°.
6. Монотозилат сполуки формули І
 (І)
(І)
у кристалічній формі А, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 5,7°±0,3°.
7. Монотозилат сполуки формули І за п. 6, на рентгенограмі якого містяться піки при кутах дифракції 2-тета, рівних 5,4°±0,3°; 5,7°±0,3° та 17,2°±0,3°.
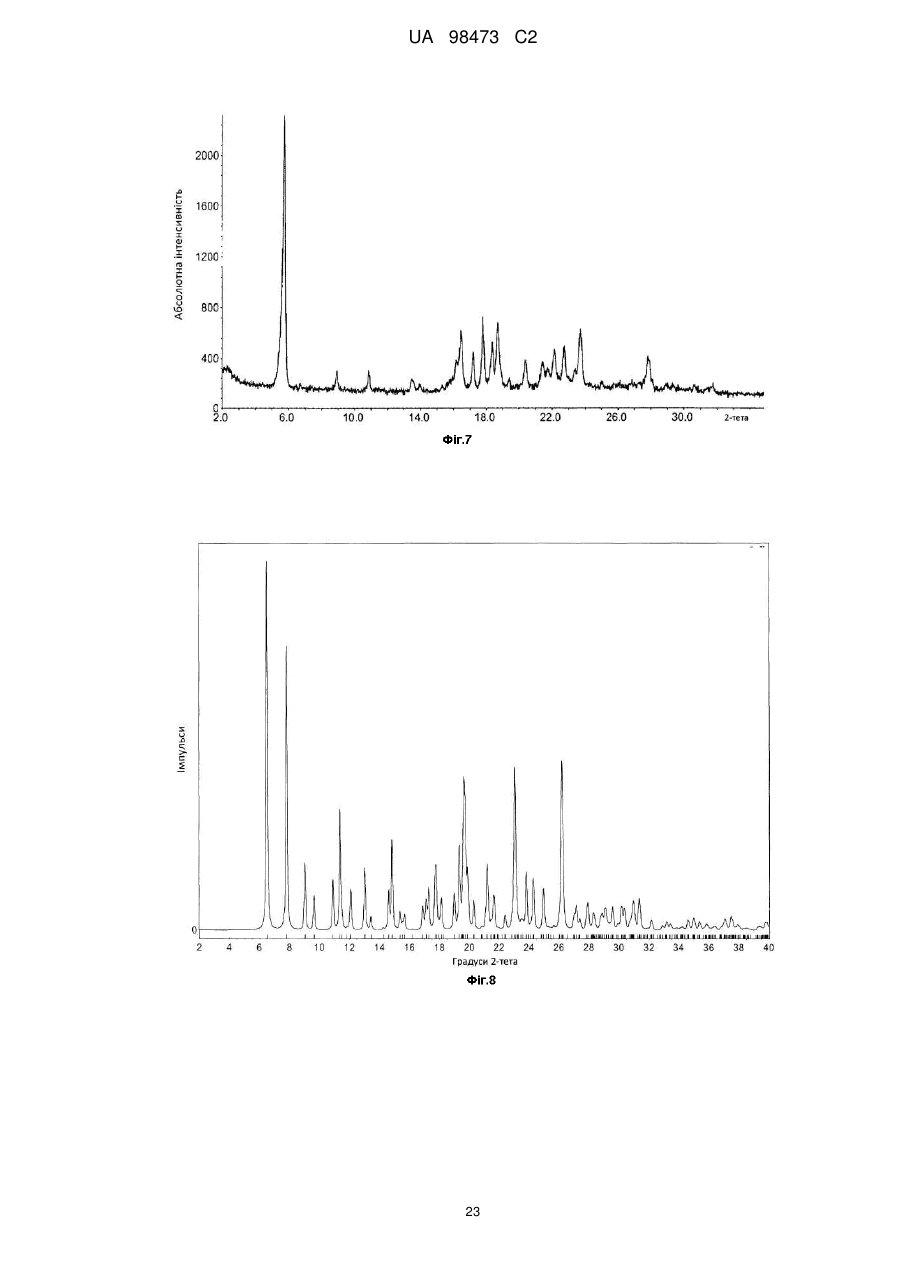
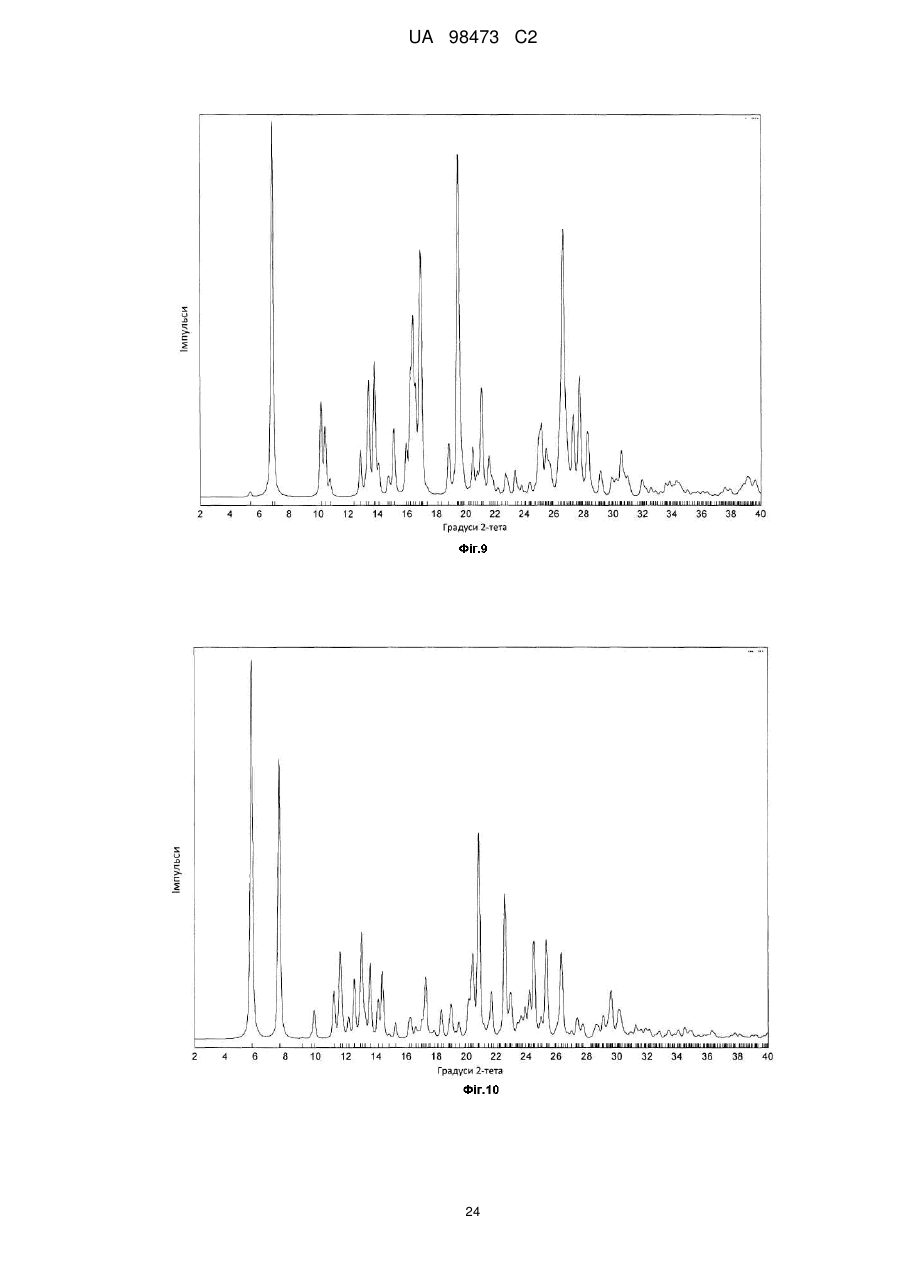
8. Монотозилат сполуки формули І за п. 6, що має рентгенограму, в основному таку, як представлена на фіг. 6.
9. Монотозилат сполуки формули І
 (І)
(І)
у кристалічній формі В, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 5,8°±0,3°.
10. Монотозилат сполуки формули І за п. 9, на рентгенограмі якого містяться піки при кутах дифракції 2-тета, рівних 5,8°±0,3°; 17,8°±0,3° та 18,7°±0,3°.
11. Моногідрат монотозилату сполуки формули І
 (І)
(І)
у кристалічній формі НА, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 6,5°±0,3°.
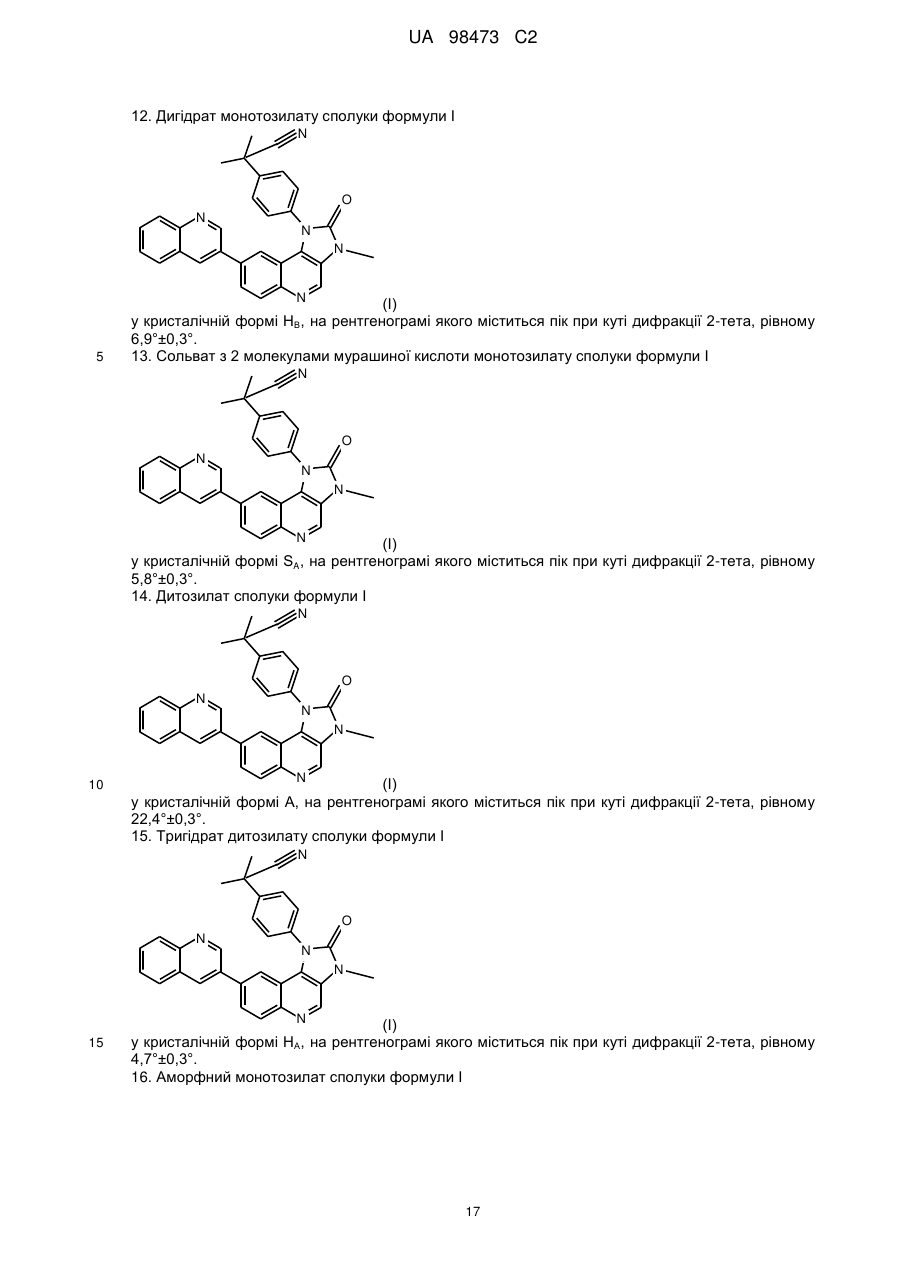
12. Дигідрат монотозилату сполуки формули І
 (І)
(І)
у кристалічній формі НВ, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 6,9°±0,3°.
13. Сольват з 2 молекулами мурашиної кислоти монотозилату сполуки формули І
 (І)
(І)
у кристалічній формі SA, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 5,8°±0,3°.
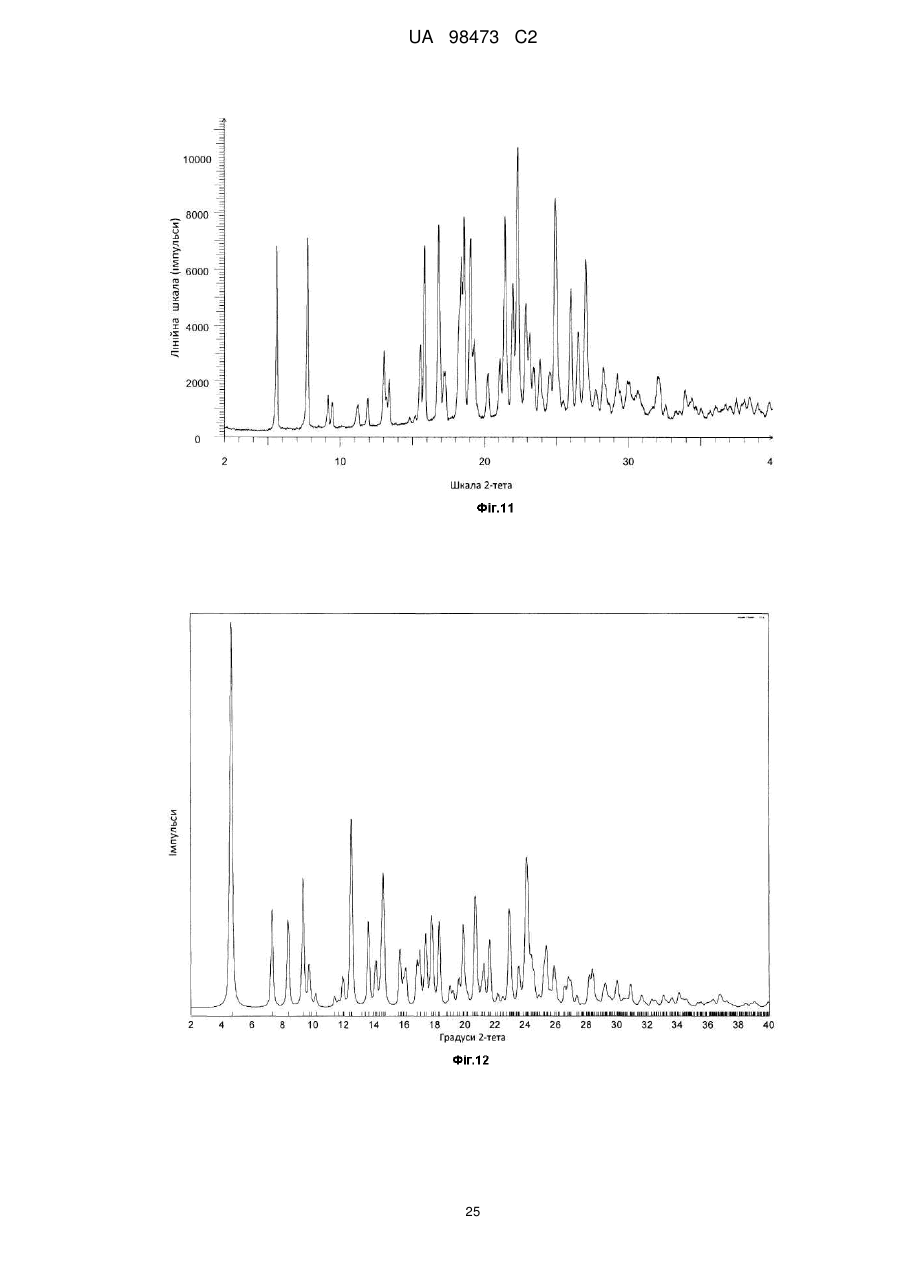
14. Дитозилат сполуки формули І
 (І)
(І)
у кристалічній формі А, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 22,4°±0,3°.
15. Тригідрат дитозилату сполуки формули І
 (І)
(І)
у кристалічній формі НА, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 4,7°±0,3°.
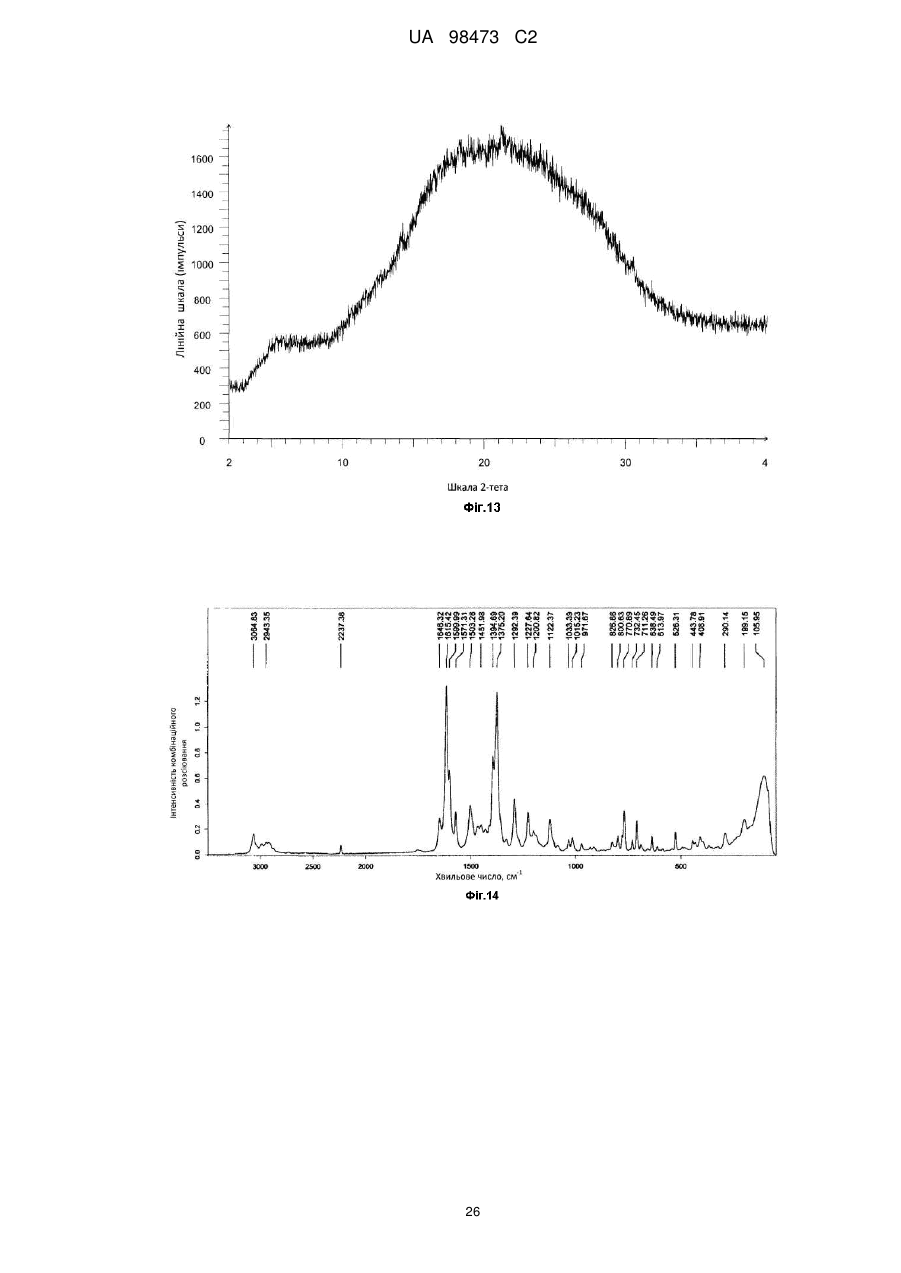
16. Аморфний монотозилат сполуки формули І
 (І).
(І).
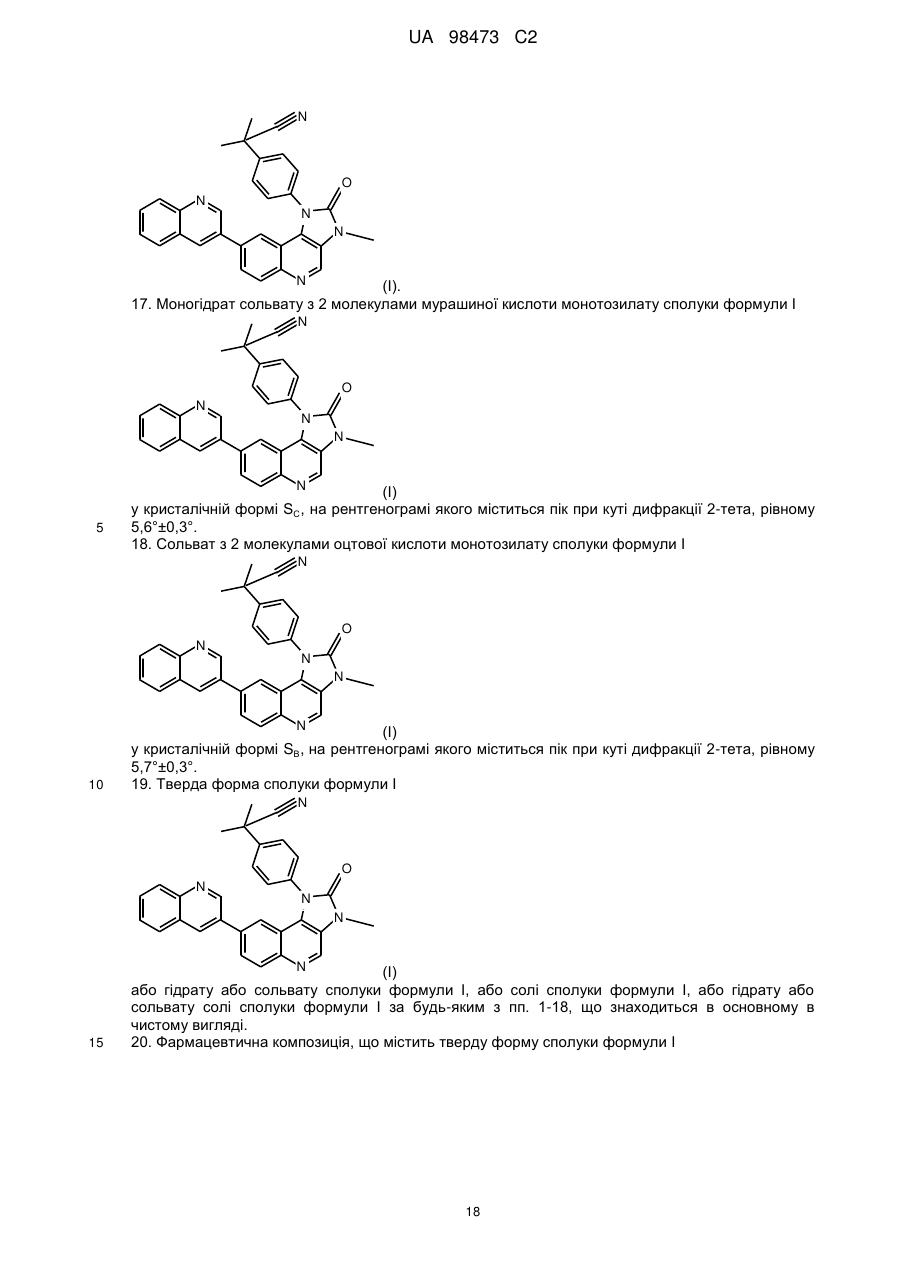
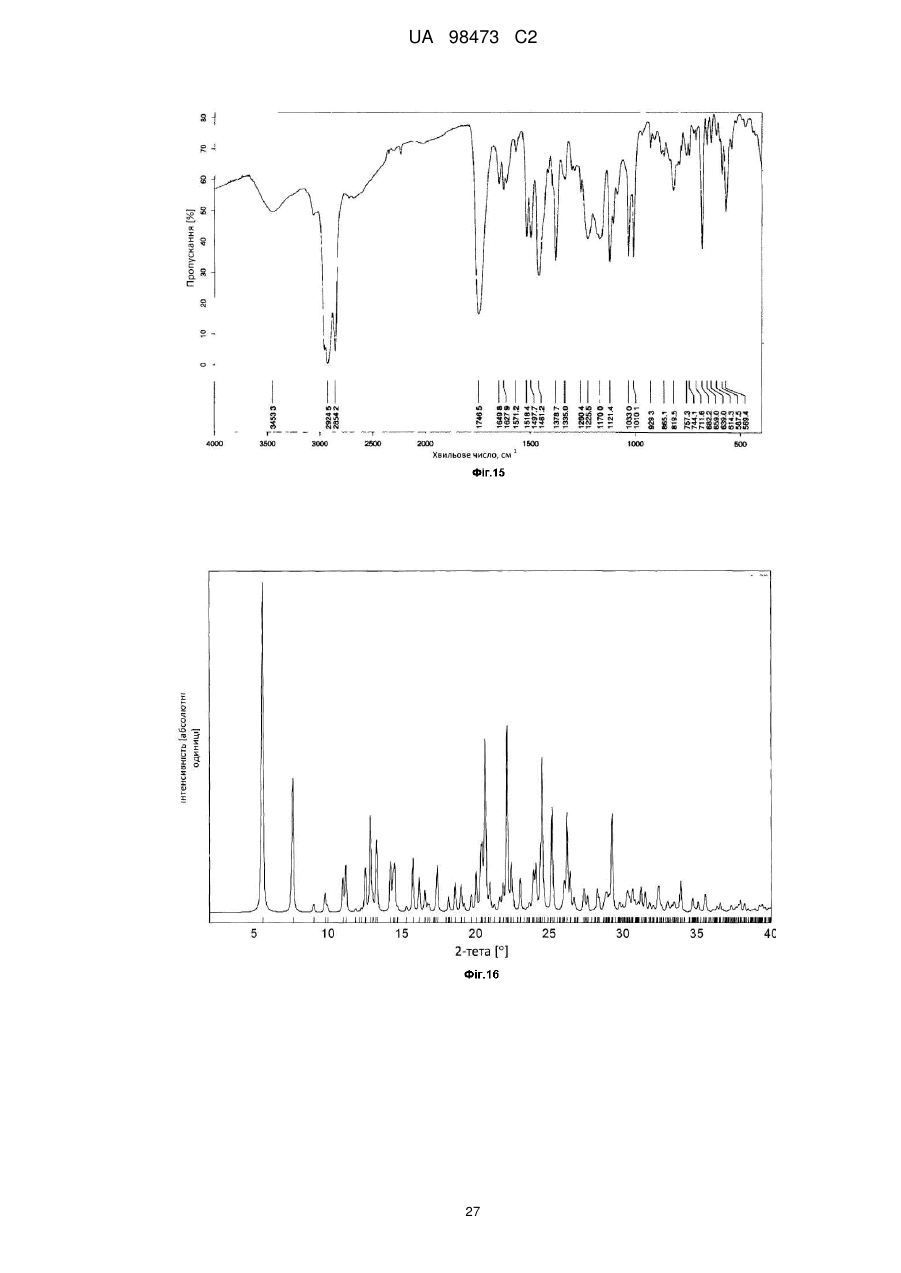
17. Моногідрат сольвату з 2 молекулами мурашиної кислоти монотозилату сполуки формули І
 (І)
(І)
у кристалічній формі SС, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 5,6°±0,3°.
18. Сольват з 2 молекулами оцтової кислоти монотозилату сполуки формули І
 (І)
(І)
у кристалічній формі SВ, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 5,7°±0,3°.
19. Тверда форма сполуки формули І
 (І)
(І)
або гідрату або сольвату сполуки формули І, або солі сполуки формули І, або гідрату або сольвату солі сполуки формули І за будь-яким з пп. 1-18, що знаходиться в основному в чистому вигляді.
20. Фармацевтична композиція, що містить тверду форму сполуки формули І
 (І)
(І)
або її гідратів або сольватів, її солей та гідратів або сольватів її солей за будь-яким з пп. 1-18 і необов'язково щонайменше один фармацевтично прийнятний носій.
21. Застосування твердої форми сполуки формули І
 (І)
(І)
її гідратів або сольватів, її солей і гідратів або сольватів її солей за будь-яким з пп. 1-18 для виготовлення терапевтичного засобу, призначеного для лікування проліферативного захворювання, вибраного із групи, що включає доброякісну або злоякісну пухлину, карциному головного мозку, нирок, печінки, надниркової залози, сечового міхура, молочної залози, шлунка, пухлини шлунка, яєчників, ободової кишки, прямої кишки, передміхурової залози, підшлункової залози, легенів, піхви або щитовидної залози, саркому, гліобластому, множинну мієлому або рак шлунково-кишкового тракту, переважно - карциному ободової кишки або колоректальну аденому, або пухлину голови та шиї, гіперпроліферацію епідермісу, псоріаз, гіперплазію передміхурової залози, неоплазію, неоплазію епітеліального характеру, лімфому, карциному молочної залози або лейкозу, а також захворювань, що включають синдром Коудена, хворобу Лерміта-Дудоса та синдром Банаяна-Зонана, або захворювань, у яких шлях РІ3К/РКВ є аберантно активованим.
22. Спосіб лікування захворювання, вибраного з групи, що включає доброякісну або злоякісну пухлину, карциному головного мозку, нирок, печінки, надниркової залози, сечового міхура, молочної залози, шлунка, пухлини шлунка, яєчників, ободової кишки, прямої кишки, передміхурової залози, підшлункової залози, легенів, піхви або щитовидної залози, саркому, гліобластому, множинну мієлому або рак шлунково-кишкового тракту, переважно - карциному ободової кишки або колоректальну аденому, або пухлину голови та шиї, гіперпроліферацію епідермісу, псоріаз, гіперплазію передміхурової залози, неоплазію, неоплазію епітеліального характеру, лімфому, карциному молочної залози або лейкоз, а також захворювання, вибраного з синдрому Коудена, хвороби Лерміта-Дудоса та синдрому Банаяна-Зонана, або захворювань, у яких шлях РІ3К/РКВ є аберантно активованим, у теплокровної тварини, що цього потребує, у якому тварині вводять кристалічну форму сполуки формули І
 (І)
(І)
її гідратів або сольватів, її солей або гідратів або сольватів її солей за будь-яким з пп. 1-18 у кількості, яка є терапевтично ефективною для боротьби з відповідним захворюванням.
Текст
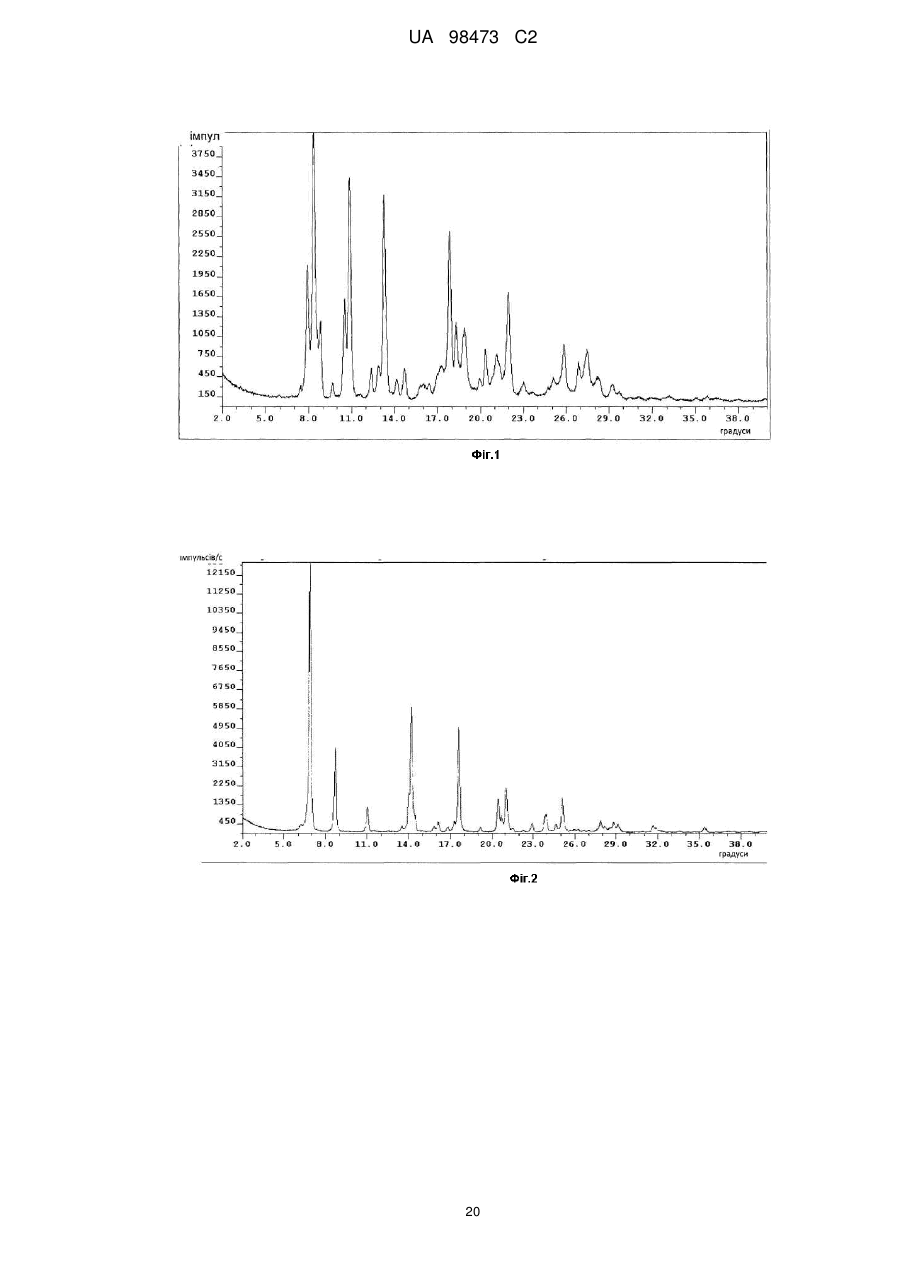
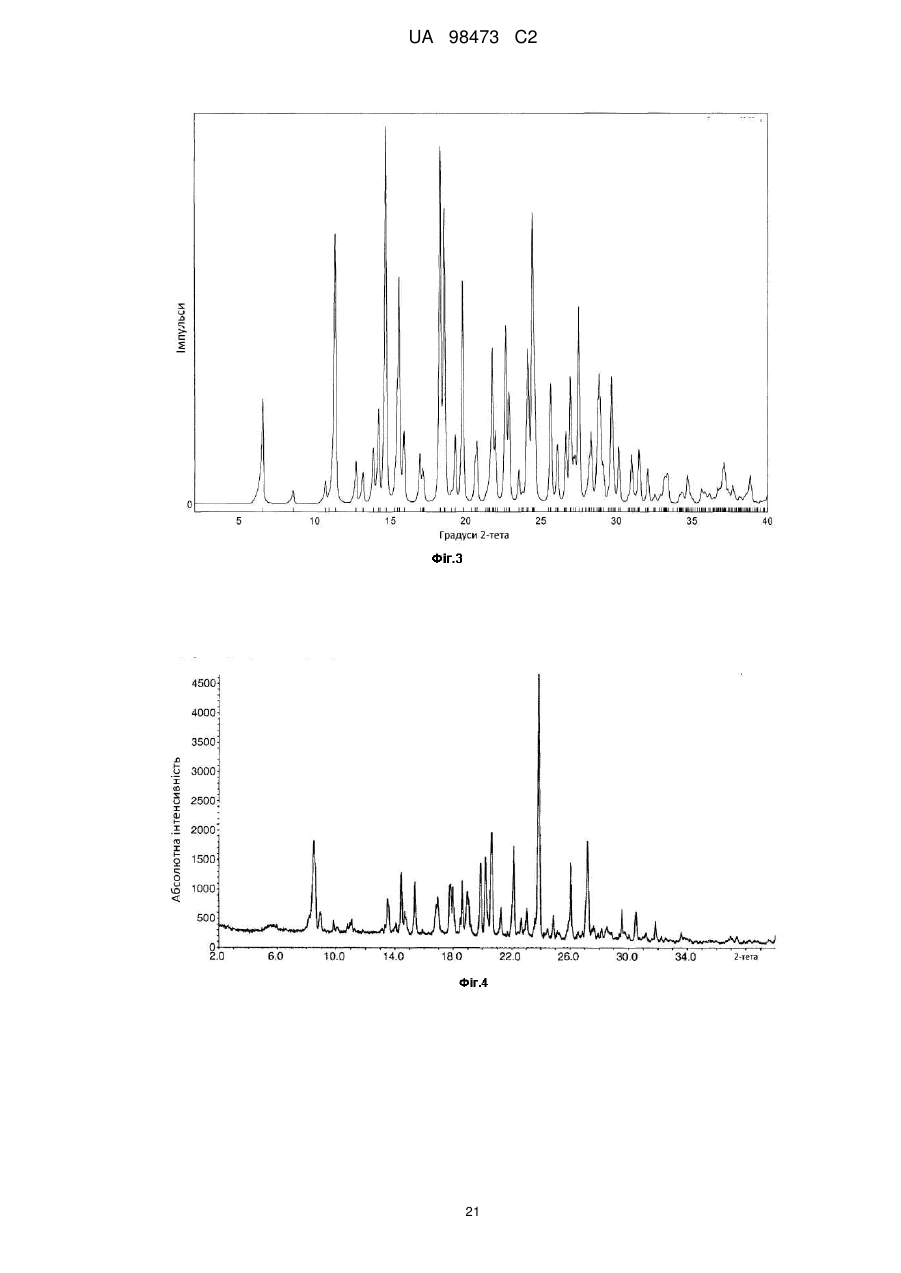
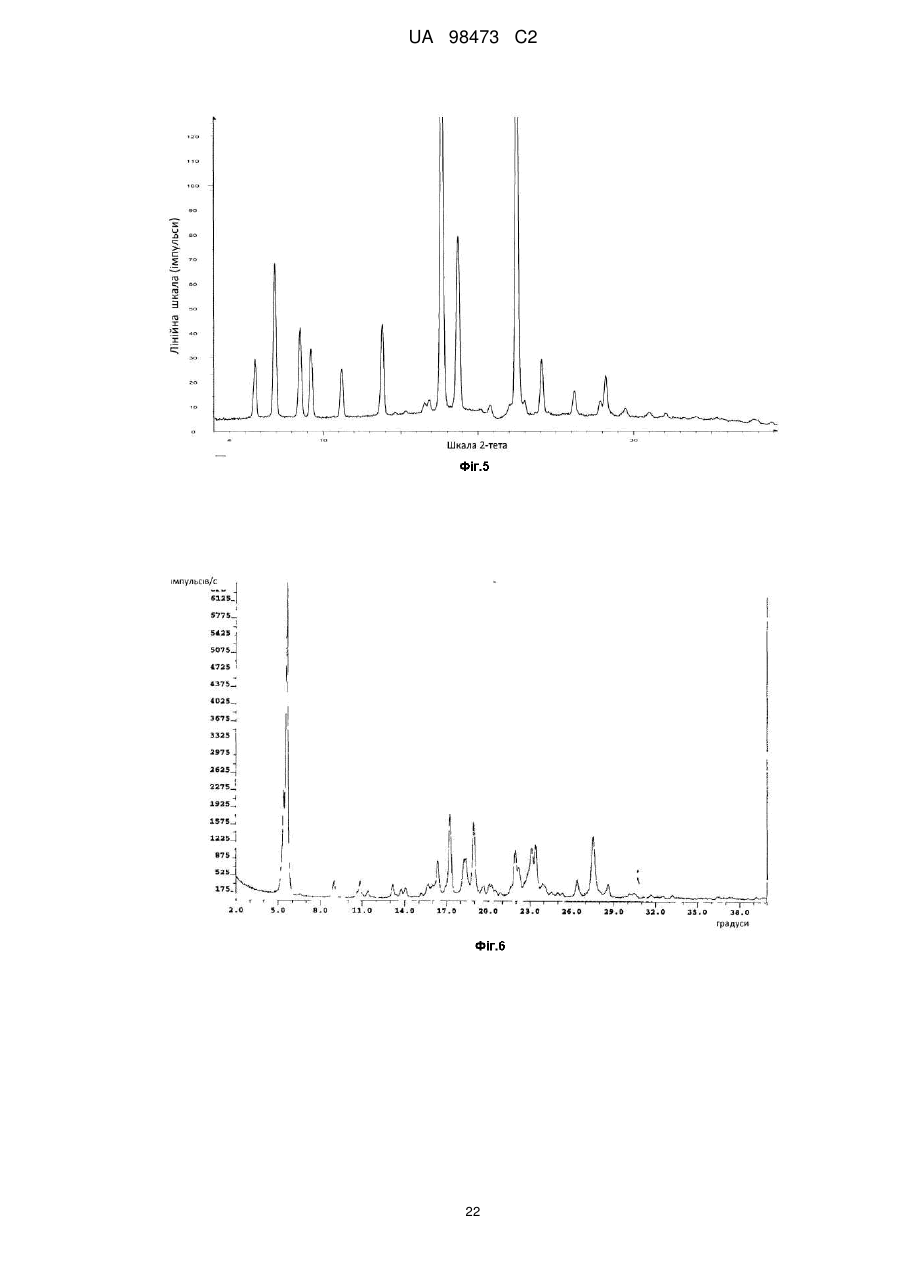
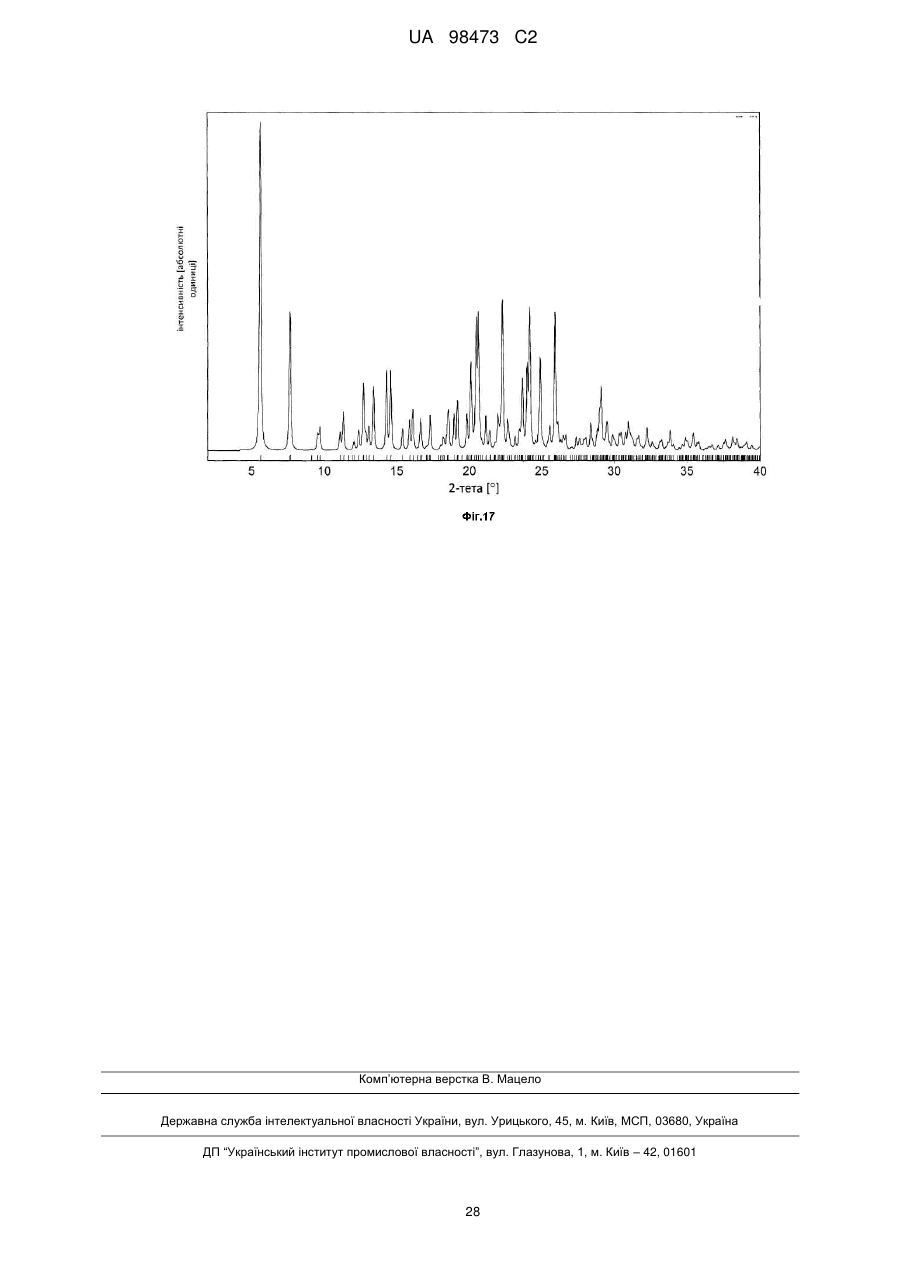
Реферат: У заявці описані кристалічні форми 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-с]хінолін-1-іл)феніл]пропіонітрилу, його гідратів і сольватів, його солей і гідратів і сольватів його солей, способи їх одержання, фармацевтичні композиції, що містять ці кристалічні форми, та їх застосування в діагностичних методиках або, переважно, для терапевтичного лікування теплокровних тварин, переважно - людей, а також їх застосування як проміжного продукту для виготовлення фармацевтичних препаратів, призначених для застосування в діагностичних методиках або, переважно, для терапевтичного лікування теплокровних тварин, переважно - людей. N O N N N N UA 98473 C2 (12) UA 98473 C2 UA 98473 C2 5 10 15 20 25 30 Даний винахід стосується особливих твердих, переважно - кристалічних або аморфних, більш переважно - кристалічних форм 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу (сполука I, див. нижче), до його гідратів і сольватів, його солей і гідратів і сольватів його солей, деяких способів їх одержання, фармацевтичних композицій, що містять ці тверді форми, та до їх застосування у діагностичних методиках або, переважно, для терапевтичного лікування теплокровних тварин, переважно людей, і до їх застосування як проміжного продукту для виготовлення фармацевтичних препаратів, призначених для застосування в діагностичних методиках або, переважно, для терапевтичного лікування теплокровних тварин, переважно - людей. Рівень техніки 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]пропіонітрил, інгібування ним активності ліпідкіназ, таких як PI3-кіназа та/або представників сімейства протеїнкіназ, родинних PI3-кіназі (які також називають PIKK, що включають DNA-PK, ATM, ATR, hSMG-1 та mTOR), таких як ДНК-протеїнкіназа, його одержання і його застосування, особливо як протипухлинного засобу, описані в WO2006/122806. У цій публікації сполуки наведені як приклад у вільній формі (див, наприклад, приклад 7) та у вигляді солі з 4толуолсульфоновою кислотою в стехіометричному співвідношенні 1:1. Синтез 2-метил-2-[4-(3метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу також описаний в експериментальній частині в прикладі 1. Відповідно до винаходу несподівано було встановлено, що за деяких умов можна виявити нові особливі кристалічні форми 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу, його гідратів і сольватів, його солей і гідратів або сольватів його солей, які описані нижче в даному винаході і які є корисними для застосування в різних випадках і мають корисні характеристики. Вони мають нові фізичні характеристики, які можуть привести до значних розходжень у деяких фармацевтичних характеристиках і які можна використати для лікарської речовини та виготовлення терапевтичного продукту, наприклад, для розчинення лікарських речовин та/або полегшення шляхів виготовлення/очищення. Детальний опис винаходу Даний винахід більш детально описаний нижче з використанням креслень та інших засобів. Даний винахід переважно стосується, в основному, чистих кристалічних форм 2-метил-2-[4(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу формули I (сполука I), N O N N N 35 40 45 50 N гідрату або сольвату сполуки формули I, або солі сполуки формули I, або гідрату або сольвату солі сполуки формули I. Опис графічних матеріалів На рентгенограмах, розглянутих нижче, кути дифракції 2-тета відкладені по горизонтальній осі (осі x), а інтенсивності (кількості імпульсів) - по вертикальній осі (осі y). ФІГ. 1 Форма A 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1іл)-феніл]-пропіонітрилу Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 8,4°, і вона має відносну інтенсивність рівну 100%. Виявлені ще 2 лінії, що мають відносні інтенсивності рівні більше 10%, розташовані при 7,9° та 10,5°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2-тета, рівних 7,9°, 8,4°, 10,5°, 10,9°, 13,3°, 17,9°, 22,0°. Дані порошкової рентгенограми отримані на приладі Scintag з використанням джерела випромінювання Cu K-альфа; крок 0,020 °, діапазон 2,00-40,00°, постійна швидкість сканування 0,50/хв (всі значення 2-тета 0,3). ФІГ. 2 Форма B 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1 1 UA 98473 C2 5 10 15 20 25 30 35 40 45 50 55 60 іл)-феніл]-пропіонітрилу Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 6,9°, і вона має відносну інтенсивність рівну 100%. Виявлені ще 2 лінії, що мають відносні інтенсивності рівні більше 10%, розташовані при 14,2° та 17,7°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2-тета, рівних 6,9°, 8,7°, 10,1°, 14,2°, 17,7°, 20,5°, 21,1°. Дані порошкової рентгенограми отримані на приладі Scintag з використанням джерела випромінювання Cu K-альфа; крок 0,020 °, діапазон 2,00-40,00°, постійна швидкість сканування 0,50/хв (всі значення 2-тета 0,3). ФІГ. 3 Модельна порошкова рентгенограма форми C 2-метил-2-[4-(3-метил-2-оксо-8-хінолін3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 14,7°, і вона має відносну інтенсивність рівну100%. Виявлені ще 2 лінії, що мають відносні інтенсивності рівні більше 10%, розташовані при 11,4° та 18,6°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2-тета, рівних 6,6°, 11,4°, 14,7°, 15,6°, 18,3°, 18,6°, 19,8°, 22,7°, 24,5° (всі значення 2-тета 0,3). ФІГ. 4 Форма D 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1іл)-феніл]-пропіонітрилу Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 23,9°, і вона має відносну інтенсивність рівну100%. Виявлені ще 2 лінії, що мають відносні інтенсивності рівні більше 10%, розташовані при 20,6° та 22,1°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2-тета, рівних 8,5°, 19,9°, 20,2°, 20,6°, 22,1°, 23,9°, 26,1°, 27,2°. Дані порошкової рентгенограми отримані на приладі STOE Stadi P Combi з використанням джерела випромінювання Cu K-альфа-1; щілина 4 мм/2 мм; зі зразком, поміщеним у каптонову плівку; Монохроматор: зріз кристалу германію в напрямку (111), випромінювання 1,54060 Å, генератор: 50 кВ, 30 мА, детектор: лінійний ФЗД (фазочутливий детектор)/регульований/на постійній частоті; діапазон 1: 2-тета (початок, кінець, крок) = 2,000, 39,980, 0,020; 390,00 с/крок (всі значення 2-тета +/- 0,3). ФІГ. 5 Форма HA моногідрату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 17,6°, і вона має відносну інтенсивність рівну100%. Виявлені ще 2 лінії, що мають відносні інтенсивності рівні більше 10%, розташовані при 18,8° та 22,5°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2-тета, рівних 5,6°, 6,9°, 8,5°, 9,2°, 13,8°, 17,6°, 18,8°, 22,5°, 24,0°. Дані порошкової рентгенограми отримані на приладі Bruker D8 Discover GADDS у режимі відбиття (всі значення 2-тета +/- 0,3). ФІГ. 6 Форма A монотозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 5,7°, і вона має відносну інтенсивність рівну100 %. Виявлені ще 2 лінії, що мають відносні інтенсивності рівні більше 10%, розташовані при 5,4° та 17,2°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2-тета, рівних 5,4°, 5,7°, 16,4°, 17,2°, 18,3°, 19,0°, 22,0°, 23,1°, 23,4°, 27,5°. Дані порошкової рентгенограми отримані на приладі Scintag з використанням джерела випромінювання Cu Kальфа; крок 0,020 °, діапазон 2,00-40,00°, постійна швидкість сканування 0,50/хв (всі значення 2тета 0,3). ФІГ. 7 Форма B монотозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 5,8°, і вона має відносну інтенсивність рівну100%. Виявлені ще 2 лінії, що мають відносні інтенсивності рівні більше 10%, розташовані при 17,8° та 18,7°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2-тета, рівних 5,8°, 16,4°, 17,2°, 17,8°, 18,4°, 18,7°, 22,1°, 22,7°, 23,7°. Дані порошкової рентгенограми отримані на приладі STOE Stadi P Combi з використанням джерела випромінювання Cu Kальфа-1; щілина 4 мм/2 мм; зі зразком, поміщеним у каптонову плівку; Монохроматор: зріз кристалу германію в напрямку (111), випромінювання 1,54060 Å, генератор: 50 кВ, 30 мА, детектор: лінійний ФЗД/регульований/на постійній частоті; діапазон 1: 2-тета (початок, кінець, крок) = 2,000, 39,980, 0,020; 390,00 с/крок (всі значення 2-тета +/- 0,3). ФІГ. 8 Модельна порошкова рентгенограма форми HA моногідрату монотозилату 2-метил-2[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу (розрахована за відповідною монокристалічною структурою) 2 UA 98473 C2 Кристалографічні характеристики моногідратумонотозилату сполуки I: Кристалографічна система Просторова група a, Å b, Å c, Å α, β, γ 3 V, Å -3 Dcalc, г.см Z 5 10 α, β, γ 3 V, Å -3 Dcalc, г.см Z 20 P21/c 9,790(3) 12,431(3) 27,209(8) 90, 92,560(16), 90 3308,0(16) 1,325 4 Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 6,5°, і вона має відносну інтенсивність рівну100%. Виявлені ще 4 лінії, що мають відносні інтенсивності рівні більше 50%, розташовані при 7,8°, 19,6°, 23,1° та 26,2°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2тета, рівних 6,5°, 7,8°, 9,0°, 11,4°, 14,9°, 19,3°, 19,6°, 23,1°, 26,2° (всі значення 2-тета 0,3). ФІГ. 9 Модельна порошкова рентгенограма форми HB дигідрату монотозилату 2-метил-2-[4(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу (розрахована за відповідною монокристалічною структурою) Кристалографічні характеристики дигідрату монотозилату сполуки I: Кристалографічна система Просторова група a, Å b, Å c, Å 15 Моноклінна Триклинна P-1 7,1921(2) 13,8439(3) 17,5657(4) 111,203(1), 90,980(1), 96,388(1) 1617,33(7) 1,318 2 Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 6,9°, і вона має відносну інтенсивність рівну100%. Виявлені ще 2 лінії, що мають відносні інтенсивності рівні більше 10%, розташовані при 19,5° та 26,6°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2-тета, рівних 6,9°, 10,2°, 13,4°, 13,8°, 16,4°, 16,9°, 19,5°, 21,1°, 26,6° (всі значення 2-тета 0,3). ФІГ. 10 Модельна порошкова рентгенограма форми SA сольвату з 2 молекулами мурашиної кислоти монотозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5c]хінолін-1-іл)-феніл]-пропіонітрилу (розрахована за відповідною монокристалічною структурою) Кристалографічні характеристики сольвату з мурашиною кислотою монотозилату сполуки I: Кристалографічна система Просторова група a, Å b, Å c, Å α, β, γ 3 V, Å -3 Dcalc, г.см Z Моноклінна P21/n 9,4104(3) 12,5101(5) 30,3995(11) 90, 92,183(2), 90 3576,2(2) 1,547 4 25 Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 5,8°, і вона має відносну інтенсивність рівну100%. Виявлені ще 2 лінії, що мають 3 UA 98473 C2 5 відносні інтенсивності рівні більше 10%, розташовані при 7,6° та 20,9°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2-тета, рівних 5,8°, 7,9°, 11,7°, 13,1°, 13,6°, 14,5°, 17,3°, 20,9°, 22,6°, 24,5° (всі значення 2-тета 0,3). ФІГ. 11 Форма A дитозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Кристалографічні характеристики дитозилату сполуки I: Кристалографічна система Просторова група a, Å b, Å c, Å α, β, γ 3 V, Å -3 Dcalc, г.см Z 10 15 20 3 V, Å -3 Dcalc, г.см Z 30 35 P21/n 10,3246(2) 12,0935(3) 31,5031(7) 90, 99,416(1), 90 3880,50(15) 1,159 4 Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 22,4°, і вона має відносну інтенсивність рівну100%. Виявлені ще 2 лінії, що мають відносні інтенсивності рівні більше 10%, розташовані при 21,5° та 25,0°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2-тета, рівних 5,6°, 7,7°, 15,8°, 16,8°, 18,6°, 19,1°, 21,5°, 22,4°, 25,0°. Дані порошкової рентгенограми отримані на приладі Bruker D8 Advance з використанням джерела випромінювання Cu K-альфа; крок 0,017°, час підрахунку 0,3 с, діапазон 2,00-40,00°, щілина зі змінним відхиленням 12 мм, детектор ФЗД VANTEC (всі значення 2-тета 0,3). ФІГ. 12 Модельна порошкова рентгенограма форми HA тригідрату дитозилату 2-метил-2-[4(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу (розрахована за відповідною монокристалічною структурою) Кристалографічні характеристики сполуки I дитозилату тригідрату: Кристалографічна система Просторова група a, Å b, Å c, Å α, β, γ 25 Моноклінна Моноклінна P21/n 9,120(3) 12,646(4) 37,827(12) 90, 95,565(16), 90 4342(2) 1,328 4 Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 4,7°, і вона має відносну інтенсивність рівну100%. Виявлені ще 2 лінії, що мають відносні інтенсивності рівні більше 10%, розташовані при 9,4° та 12,6°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2-тета, рівних 4,7°, 7,4°, 8,4°, 9,4°, 12,6°, 13,7°, 14,7°, 18,3°, 20,8°, 24,1° (всі значення 2-тета 0,3). ФІГ. 13 Аморфна форма монотозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Дані порошкової рентгенограми отримані на приладі Bruker D8 Advance з використанням джерела випромінювання Cu K-альфа; крок 0,017°, час підрахунку 0,3 с, діапазон 2,00-40,00°, щілина зі змінним відхиленням 12 мм, детектор ФЗД VANTEC. ФІГ. 14 Спектри комбінаційного розсіювання аморфної форми монотозилату 2-метил-2-[4-(3метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Спектр комбінаційного розсіювання зразка зняти на дисперсійному спектрометрі комбінаційного розсіювання з лазерним джерелом збудження при 1064 нм (Bruker RFS 100). -1 Суттєві смуги в спектрах охарактеризовані зворотними значеннями хвильових чисел (см ). ФІГ. 15 ІЧ Фур'є-спектри аморфної форми монотозилату 2-метил-2-[4-(3-метил-2-оксо-8 4 UA 98473 C2 5 10 15 20 хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Інфрачервоний спектр поглинання зразка отриманий з використанням інфрачервоного Фур'є-мікроскопу (Bruker Vertex 70). Суттєві смуги в спектрах охарактеризовані зворотними -1 значеннями хвильових чисел (см ). ФІГ. 16 Модельна порошкова рентгенограма форми SC сольвату з 2 молекулами мурашиної кислоти моногідрату монотозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу (розрахована за відповідною монокристалічною структурою) Кристалографічні характеристики сольвату з мурашиною кислотою моногідрату монотозилату сполуки I: Кристалографічна Моноклінна система Просторова група P21/n a, Å 9,304(3) b, Å 12,421(4) c, Å 31,500(10) α, β, γ 90, 91,571(18), 90 3 V, Å 3639(2) -3 Dcalc, г.см 1,372 Z 4 Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 5,6°, і вона має відносну інтенсивність рівну100%. Виявлені ще 2 лінії, що мають відносні інтенсивності рівні більше 10%, розташовані при 20,7° та 22,2°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2-тета, рівних 5,6°, 7,6°, 12,9°, 13,3°, 14,3°, 20,7°, 22,2°, 24,5°, 25,2°, 26,2°, 29,3 (всі значення 2-тета 0,3). ФІГ. 17 Модельна порошкова рентгенограма форми SB сольвату з 2 молекулами оцтової кислоти монотозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5c]хінолін-1-іл)-феніл]-пропіонітрилу (розрахована за відповідною монокристалічною структурою) Кристалографічні характеристики сольвату з оцтовою кислотою сполуки монотозилату I: Кристалографічна система Просторова група a, Å b, Å c, Å α, β, γ 3 V, Å -3 Dcalc, г.см Z 25 30 35 40 Моноклінна P21/n 9,590(2) 12,372(3) 31,220(8) 90, 91,487(11), 90 3702,9(15) 1,367 4 Найбільш інтенсивна лінія спостерігається на рентгенограмі при куті дифракції 2-тета, рівному 5,7°, і вона має відносну інтенсивність рівну100%. Виявлені ще 2 лінії, що мають відносні інтенсивності рівні більше 10%, розташовані при 7,7° та 22,3°. При повному описі ця форма характеризується дифракційними піками, розташованими при кутах дифракції 2-тета, рівних 5,7°, 7,7°, 12,7°, 13,4°, 14,3°, 14,6°, 20,1°, 20,5°, 20,7°, 22,3°, 23,7°, 24,0°, 24,2°, 24,9°, 26,0° (всі значення 2-тета 0,3). Термін "в основному чиста" у контексті даного винаходу означає, що не менше 90, переважно - не менше 95 і найбільш переважно - не менше 99 мас. % кристалів сполуки формули I, її гідратів або сольватів, її солей або гідратів або сольватів її солей знаходяться у зазначеній кристалічній формі, запропонованій в даному винаході. Термін "тверда форма" у контексті даного винаходу включає кристалічні форми та аморфні форми. Кращими твердими формами є кристалічні форми. У контексті твердження про те, що кристалічна форма сполуки формули I, її гідратів або сольватів, її солей або її гідратів або сольватів її солей має рентгенограму, в основному таку, як наведена на одному з креслень, термін "в основному" означає, що на діаграмі, наведеній на зазначеному кресленні, містяться щонайменше головні лінії, тобто які мають відносну інтенсивність рівну більше 20%, переважно - більше 30 % у порівнянні з найбільш інтенсивною 5 UA 98473 C2 5 10 15 20 25 30 35 40 45 50 55 60 лінією цієї діаграми. В одному кращому варіанті здійснення кристалічна форма сполуки формули I, її гідратів або сольватів, її солей або її гідратів або сольватів її солей має рентгенограму, в основному таку, як наведена на одному із креслень. Особливо висока перевага надається твердій, переважно - кристалічній формі сполуки формули I, її гідратів і сольватів, її солей і гідратів або сольватів її солей, які можна одержати, як це описано в прикладах. Однією з переваг можливості використання різних кристалічних форм сполуки формули I, її гідратів або сольватів, її солей або гідратів або сольватів її солей є те, що для різних кристалічних форм при кристалізації характерним є включення різних домішок, тобто домішка, що включається в кристалічну форму AA, необов'язково включається в кристалічну форму BB або в кристалічну форму CC. Інакше кажучи, послідовне одержання різних кристалічних форм тієї ж самої речовини приводить до поліпшення чистоти кінцевої одержаної речовини. Крім того, різні кристалічні форми мають різні фізичні характеристики, такі як температури плавлення, гігроскопічність, розчинність, сипкість або термодинамічна стабільність, і тому наявність різних кристалічних форм дозволяє вибрати форму, найбільш придатну для конкретного застосування або об'єкта, наприклад, для застосування як проміжного продукту в методиці виготовлення терапевтичного засобу або для застосування в різних формах введення, таких як таблетки, капсули, мазі або розчини. Тверді, переважно - кристалічні форми сполуки формули I, її гідратів або сольватів, її солей і гідратів або сольватів її солей мають цінні фармакологічні характеристики та можуть, наприклад, застосовуватися для лікування патологічних станів, які опосередковуються активацією ферментів PI3 кіназ, таких як проліферативні, запальні або алергійні патологічні стани або порушення, які зазвичай виникають у зв'язку із трансплантацією. Тверді, аморфні або кристалічні, переважно - кристалічні форми сполуки формули I, її гідратів або сольватів, її солей і гідратів або сольватів її солей переважно можна використати для лікування проліферативного захворювання, вибраного із групи, що включає доброякісну або злоякісну пухлину, карциному головного мозку, нирок, печінки, надниркової залози, сечового міхура, молочної залози, шлунка, пухлини шлунка, яєчників, ободової кишки, прямої кишки, передміхурової залози, підшлункової залози, легенів, піхви або щитовидної залози, саркоми, гліобластоми, множинну мієлому або рак шлунково-кишкового тракту, особливо карциному прямої кишки або колоректальну аденому або пухлину голови та шиї, гіперпроліферацію епідермісу, псоріаз, гіперплазію передміхурової залози, неоплазію, неоплазію епітеліального характеру, лімфоми, карциноми молочної залози або лейкоз. Інші захворювання включають синдром Коудена, хвороба Лерміта-Дудоса та синдром БанаянаЗонана та захворювання при яких аберантно активований шлях PI3K/PKB. Даний винахід переважно стосується форми A монотозилату 2-метил-2-[4-(3-метил-2-оксо-8хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу, призначеної для лікування одного з зазначених захворювань, відзначених у даному винаході, або для виготовлення фармакологічного засобу, призначеного для його лікування. Даний винахід також стосується способу лікування теплокровних тварин, що страждають від зазначених захворювань, у якому кількість твердої, переважно - кристалічної форми сполуки формули I, її гідратів або сольватів, її солей або гідратів або сольватів її солей, ефективну для боротьби з відповідним захворюванням, переважно - кількість, що має антипроліферативну ефективність, вводять теплокровним тваринам, що потребують такого лікування. Крім того, даний винахід стосується застосування твердих, переважно - кристалічних форм сполуки формули I, її гідратів або сольватів, її солей і гідратів або сольватів її солей для виготовлення фармацевтичних композицій, призначених для застосування з метою лікування організму людини або тварини, переважно - для лікування проліферативного захворювання, такого як доброякісна або злоякісна пухлина, карцинома головного мозку, нирок, печінки, надниркової залози, сечового міхура, молочної залози, шлунка, пухлини шлунка, яєчників, ободової кишки, прямої кишки, передміхурової залози, підшлункової залози, легенів, піхви або щитовидної залози, саркоми, гліобластоми, множинної мієломи або раку шлунково-кишкового тракту, особливо карциноми прямої кишки або колоректальної аденоми або пухлини голови та шиї, гіперпроліферації епідермісу, псоріазу, гіперплазії передміхурової залози, неоплазії, неоплазії епітеліального характеру, лімфоми, карциноми молочної залози або лейкозу. Тверді, переважно - кристалічні форми сполуки формули I, її гідратів або сольватів, її солей або гідратів або сольватів її солей, описані в даному винаході, можна використати для виготовлення стабільних фармацевтичних дозованих форм. Отже, даний винахід також стосується фармацевтичних препаратів, які містять кількість, переважно - терапевтично 6 UA 98473 C2 5 10 15 20 25 30 35 40 45 50 55 60 ефективну для попередження або лікування одного із захворювань, зазначених у даному винаході, кількість твердої, переважно - кристалічної форми сполуки формули I, її гідратів або сольватів, її солей або гідратів або сольватів її солей, разом з фармацевтично прийнятними носіями, які придатні для місцевого, ентерального, наприклад, перорального або ректального, або парентерального введення іякі можуть бути неорганічними або органічними та твердими або рідкими. Фармацевтичні препарати, запропоновані в даному винаході, які при необхідності можуть містити додаткові фармакологічно активні речовини, виготовляють відповідно до відомих технологій, наприклад, за допомогою звичайних технологій перемішування, гранулювання, нанесення покриттів, розчинення або ліофілізації, і вони містять приблизно від 1 до 100%, переважно - від приблизно від 1 до приблизно 20% активної речовини або речовин. Даний винахід також стосується способу виготовлення фармацевтичної композиції, що включає змішування твердої, переважно - кристалічної форми сполуки формули I, її гідратів або сольватів, її солей або гідратів або сольватів її солей, запропонованих у даному винаході, щонайменше з одним фармацевтично прийнятним носієм або розріджувачем. Термін "фармацевтична композиція" означає продукт, що включає активний інгредієнт (інгредієнти), фармацевтично прийнятні інертні наповнювачі, які утворюють носій, а також будьякий продукт, який прямо або побічно утворюється шляхом комбінування, комплексоутворення або агрегації будь-яких двох або більшого кількості інгредієнтів або шляхом дисоціації одного або більшої кількості інгредієнтів або внаслідок інших типів реакцій або взаємодій одного або більшої кількості інгредієнтів. Відповідно до цього, фармацевтичні композиції, запропоновані в даному винаході, включають будь-яку композицію, отриману змішуванням активного інгредієнта, додаткового активного інгредієнта (інгредієнтів) і фармацевтично прийнятних інертних наповнювачів. Термін "інертний наповнювач" означає компонент фармацевтичного продукту, що не є активним інгредієнтом, такий як наповнювач, розріджувач або носій. Інертні наповнювачі, які є придатними для виготовлення фармацевтичної композиції, переважно звичайно є безпечними, нетоксичними та не є біологічно або в іншому відношенні небажаними і є прийнятними для застосування у ветеринарії, а також у фармацевтиці. "Фармацевтично прийнятний інертний наповнювач" при використанні в даному описі та формулі винаходу включає один або більше, ніж один такий інертний наповнювач. "Терапевтично ефективна кількість" означає кількість сполуки, якої при введенні для лікування або попередження захворювання досить для такого лікування або попередження захворювання. "Терапевтично ефективна кількість" буде змінюватися залежно від сполуки, захворювання та його складності, а також віку, маси та т.п. пацієнта, якого піддають лікуванню. Даний винахід також стосується способу виготовлення твердих, переважно - кристалічних форм сполуки формули I, її гідратів або сольватів, її солей і гідратів або сольватів її солей. Тепер можна визначити точні умови за яких утворюються кристали, і на практиці існує цілий ряд придатних методик, включаючи умови кристалізації, описані в прикладах 3 - 17. Умови, що викликають кристалізацію, зазвичай включають використання відповідного розчинника, що викликає кристалізацію, такого як трет-бутилметиловий ефір (ТБМЕ), метанол, етанол, ізопропанол або вода або їх суміші. Зазвичай аморфну сполуку розчиняють у розчиннику при температурі не нижче 10°C. Розчин можна одержати розчиненням у розчиннику будь-якої одної або більшої кількості аморфних форм сполуки і її сольватів, таких як гідрати, метаноляти, етаноляти, ізопропаноляти або форміати. Потім кристали можна одержати з розчину, кристалізація відбувається при температурі приблизно від 0°C і до температури кипіння розчинника. Розчинення та кристалізацію можна виконати відповідно до різних звичайних методик. Наприклад, аморфну сполуку можна розчинити в розчиннику або суміші розчинників, у якій вона легкорозчинна при підвищеній температурі, але в якій вона лише помірно розчинна при більш низьких температурах. Після розчинення при підвищеній температурі виконують охолодження, під час якого очікувані кристали викристалізовуються з розчину. Стадію охолодження та нагрівання можна виконувати кілька разів, наприклад, щонайменше один раз, щонайменше 2 рази, щонайменше 3 рази, щонайменше 5 разів. Температури охолодження та нагрівання рівні, наприклад, не нижче 5°C, не нижче 10°C або не нижче 15°C. Низька температура циклів охолодження/нагрівання може, наприклад, бути нижче 15°C, нижче 10°C, нижче 5°C або нижче 0°C, тоді як висока температура може, наприклад, бути не нижче 15 °C, не нижче 20°C, не нижче 25°C або не нижче 30°C. Також можна використовувати змішані розчинники, що включають гарний розчинник, у якому сполука легко розчинна, переважно, у кількостях, що становлять не менш 1 мас. % при 30°C, і поганий розчинник, у якому вона помірно розчинна, переважно, у кількостях, що становлять не 7 UA 98473 C2 5 10 15 20 25 30 35 40 більш приблизно 0,01 мас. % при 30°C, за умови, що при зниженій температурі, звичайно не нижче приблизно 0°C, можлива кристалізація з суміші вибраних розчинників. Альтернативно, можна використати розходження в розчинності кристалів у різних розчинниках. Наприклад, аморфну сполуку можна розчинити в гарному розчиннику, у якому вона добре розчинна, такому як у якому вона розчинна в кількостях, що становлять не менше 1 мас. % приблизно при 30°C, а потім розчин змішати з поганим розчинником, у якому вона гірше розчинна, таким як у якому вона розчинна в кількостях, що становлять не більше приблизно 0,01 мас. % приблизно при 30°C. Таким чином, розчин сполуки в гарному розчиннику можна додати до поганого розчинника, звичайно при підтриманні температури вище приблизно 0°C, або поганий розчинник можна додати до розчину сполуки в гарному розчиннику, також звичайно при підтриманні температури вище приблизно 0°C. Приклади гарних розчинників можуть включати нижчі спирти, такі як метанол, етанол та ізопропанол, мурашину кислоту, оцтову кислоту або ацетон. Прикладом поганого розчинника є, наприклад, вода. Кристалізацію бажано, проводити при температурі в діапазоні від приблизно 0 до приблизно 40°C. В альтернативному варіанті здійснення способу, запропонованого в даному винаході, тверду аморфну сполуку суспендируют при температурі зазвичай не нижче приблизно 0°C у розчиннику, у якому вона не повністю розчинна, переважно, у якому воно лише помірно розчинна при цій температурі. Утворюється суспензія, у якій дисперговані частки твердої речовини, і вони залишаються не повністю розчиненими в розчиннику. Бажано, якщо тверді речовини підтримуються в стані суспензії шляхом змішування, наприклад, шляхом струшування або перемішування. Температуру суспензії зазвичай підтримують рівною приблизно 0°C або вище, щоб забезпечити перетворення вихідних твердих речовин у кристали. Аморфна тверда сполука, суспендована в підходящому розчиннику, може являти собою сольват, наприклад, гідрат, метанолят, етанолят, ацетат або форміат. Шляхом сушіння сольвату можна одержати аморфний порошок. Для стимулювання кристалізації до розчину бажано додати "затравку" кристалічної речовини. У кращому варіанті здійснення даного винаходу кристалічні форми формули I, її гідрати або сольвати, її солі та гідрати або сольвати її солей мають високу кристалічність. Кристалічна форма визначається в даному винаході, як така, що має "високу кристалічність" або що є "кристалографічно чистою", коли вона містить якнайбільше приблизно 0,5% (мас./мас.), наприклад, якнайбільше приблизно 0,1% (мас./мас.) іншої форми. Так, наприклад, "кристалографічно чиста форма AA" містить приблизно 0,5% (мас./мас.) або менше, наприклад, приблизно 0,1% (мас./мас.) або менше форми BB та/або іншої кристалічної форми. Що стосується вмісту аморфної форми, то "кристалографічно чиста" форма містить менше приблизно 5% аморфної форми або кількість аморфної форми є меншою межі виявлення (тобто містить кількість, яку не можна виявити) аморфної форми. Наведені нижче приклади ілюструють даний винахід, не обмежуючи його обсяг. Температури наведені в градусах Цельсія (°C). Приклади Приклад 1 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]пропіонітрил N O N N N 45 50 N У придатний скляний лабораторний реактор поміщають 45,0 г вихідного 2[4-(8-бром-3метил-2-оксо-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]2-метилпропіонітрилу разом з 2,25 г бістрифенілфосфінпаладійдихлориду в 445 мл N,N-диметилформаміду (ДМФ). Цю суміш нагрівають до 95 °C і потім додають розчин 22,2 г 3-хінолінборонової кислоти в суміші 225 мл 8 UA 98473 C2 5 10 15 ДМФ, 300 мл H2O та 60 г KHCO3. Цю суміш нагрівають протягом 2 год. при 95 °C. Потім додають 1080 мл H2O. Осаджується продукт, 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]пропіонітрил. Суміш охолоджують протягом 1,5 год. до 0 – 5 °C. Після перемішування при цій температурі протягом 2 год. неочищений продукт відфільтровують і промивають за допомогою 300 мл H 2O. Цей продукт сушать у вакуумі при 60 °C протягом 18 год. та одержують неочищений продукт. 40 г цього неочищеного продукту розчиняють в 200 мл мурашиної кислоти при 60 °C. Додають 8 г активованого вугілля та Smopex 234. Суміш перемішують при 60 °C протягом 1 год., вугілля відфільтровують, залишок промивають за допомогою 80 мл мурашиної кислоти та потім 175 мл мурашиної кислоти відганяють у вакуумі. Потім додають 320 мл метанолу та суміш кип'ятять зі зворотним холодильником протягом 3 год.. Очищений продукт осаджується з реакційної суміші. Суміш охолоджують до 0 – 5 °C протягом 1 год., потім перемішують 2 год. при цій температурі та на закінчення відфільтровують і промивають за допомогою 80 мл холодного метанолу. Цю процедуру перекристалізації повторюють ще раз. На закінчення двічі перекристалізовану речовину сушать у вакуумі при 60 °C та одержують очищений 2-метил-2-[4(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]пропіонітрил. Приклад 1a 5-бром-2-(2-нітровініламіно)-бензойна кислота OH Br O O + N N H 20 25 30 O Суспензію 25 г (16 ммолей) 2-аміно-5-бромбензойної кислоти (Fluka, Buchs, Switzerland) в H2O-HCl (37%) (10:1) перемішують протягом 8 год. і потім фільтрують (розчин A). 8,17 г (255 ммолей) нітрометану (Fluka, Buchs, Switzerland) додають протягом 10 хв до охолоджуваного в бані з льодом суміші 35 г льоду та 15,3 г (382 ммоля) NaOH. Після перемішування протягом 1 год. при 0 °C та 1 год. при КТ (кімнатна температура) розчин при 0 °C додають до 28 г льоду та 42 мл HCl (37%) (розчин B). Розчини A та B поєднують і реакційну суміш перемішують протягом 18 год. при КТ. Жовтий осад відфільтровують, промивають за допомогою H2O і сушать у вакуумі при 40°C та одержують очікувану сполуку. ЕР-МС (мас-спектроскопія з іонізацією + 1 елктророзпилюванням): 287, 289 (M + H) , Br; H ЯМР (ДМСО-d6 (ДМСО - диметилсульфоксид)): 13,7-14,6/br s (1H), 12,94/d (1H), 8,07/d (1H), 8,03/dd (1H), 7,83/dd (1H), 7,71/d (1H), 6,76/d (1H). Приклад 1b 6-бром-3-нітрохінолін-4-ол OH O + N Br O 35 40 N 29 г (101 ммоль) 5-бром-2-(2-нітровініламіно)-бензойної кислоти (приклад 1a) і 11,9 г (121 ммоль) ацетату калію в 129 мл (152 ммоля) оцтового ангідриду перемішують протягом 1,5 год. при 120 °C. Осад відфільтровують і промивають оцтовою кислотою, поки фільтрат не стане безбарвним, потім промивають за допомогою H2O і сушать у вакуумі та одержують очікувану + сполуку. ЕР-МС: 269, 271 (M + H) , Br; аналітична ВЕРХ (високоефективна рідинна хроматографія): tret= 2,70 хв (градієнтний режим 1). Приклад 1c 6-бром-4-хлор-3-нітрохінолін 45 9 UA 98473 C2 5 10 20 г (74,3 ммоля) 6-бром-3-нітрохінолін-4-олу (приклад 1b) в 150 мл (1,63 моля) POCl 3 перемішують протягом 45 хв при 120 °C. Суміш охолоджують до КТ і повільно виливають у суміш води з льодом. Осад відфільтровують, промивають охолодженою льодом водою та розчиняють в CH2Cl2. Органічну фазу промивають холодним розсолом і водну фазу відкидають. Після сушіння над MgSO4 органічний розчинник випарюють досуха та одержують очікувану 1 сполуку. H ЯМР (CDCl3): 9,20/s (1H), 8,54/d (1H), 8,04/d (1H), 7,96/dd (1H); аналітична ВЕРХ: tret= 4,32 хв (градієнтний режим 1). Приклад 1d 2-метил-2-(4-нітрофеніл)-пропіонітрил N O + N O 15 20 До 15 г (92,5 ммоля) (4-нітрофеніл)-ацетонітрилу (Fluka, Buchs, Switzerland), 1,64 мг (5,09 ммоля) тетрабутиламонійброміду (Fluka, Buchs, Switzerland) і 43,3 г (305 ммолей) йодметану в 125 мл CH2Cl2 додають 10 г (250 ммолей) NaOH в 125 мл води. Реакційну суміш перемішують протягом 20 год. при КТ. Потім органічний шар відокремлюють, сушать над MgSO 4 і випарюють досуха. Залишок розчиняють у диетиловому ефірі та обробляють деревним вугіллям протягом 30 хв, фільтрують через цеоліт і випарюють у вакуумі та одержують очікувану сполуку у вигляді блідо-жовтої твердої речовини. Аналітична ВЕРХ: tret= 3,60 хв (градієнтний режим 1). Приклад 1e (2-(4-амінофеніл)-2-метилпропіонітрил N 25 30 H2 N 16 г (84,1 ммоля) 2-метил-2-(4-нітрофеніл)-пропіонітрилу (приклад 1d) і 4,16 г Ni Ренея струшують в 160 мл суміші ТГФ (тетрагідрофуран)-MeOH (1:1) при тиску H2, рівному 1,1 бар, протягом 12 год. при КТ. Після завершення реакції каталізатор відфільтровують і фільтрат випарюють досуха. Залишок очищають за допомогою флеш-хроматографії на силікагелі (гексан-EtOAc від 3:1 до 1:2) і одержують очікувану сполуку у вигляді масла. ЕР-МС: 161 (M + + H) ; аналітична ВЕРХ: tret= 2,13 хв (градієнтний режим 1). Приклад 1f 2-[4-(6-бром-3-нітрохінолін-4-іламіно)-феніл]-2-метилпропіонітрил 35 10 UA 98473 C2 N NH O + N Br O N 5 10 18 г (62,6 ммоля) 6-Бром-4-хлор-3-нітрохіноліна (приклад 1c) і 11 г (68,9 ммоля) (2-(4амінофеніл)-2-метилпропіонітрилу (приклад 1e) розчиняють в 350 мл оцтової кислоти та перемішують протягом 2 год.. Потім додають воду і жовтий осад відфільтровують та промивають за допомогою H2O. Тверду речовину розчиняють у суміші EtOAc-ТГФ (1:1), промивають насиченим водним розчином NaHCO3 і сушать над MgSO4. Органічну фазу випарюють досуха та одержують очікувану сполуку у вигляді жовтої твердої речовини. ЕР-МС: + 411, 413 (M + H) , Br; аналітична ВЕРХ: tret= 3,69 хв (градієнтний режим 1). Приклад 1g 2-[4-(3-аміно-6-бромхінолін-4-іламіно)-феніл]-2-метилпропіонітрил N NH NH2 Br N 15 20 24 г (58,4 ммоля) 2-[4-(6-Бром-3-нітрохінолін-4-іламіно)-феніл]-2-метилпропіонітрил (приклад 1e) струшують в 300 мл суміші MeOH-ТГФ (1:1) при тиску H2, рівному 1,1 бар, у присутності 8,35 г Ni Ренея протягом 1 год.. Після завершення реакції каталізатор відфільтровують і фільтрат випарюють досуха та одержують очікувану сполуку у вигляді жовтого спіненої речовини. ЕР-МС: + 381, 383 (M + H) , Br; аналітична ВЕРХ: tret= 3,21 хв (градієнтний режим 1). Приклад 1h 2-[4-(8-бром-2-оксо-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-2-метилпропіонітрил N O N NH Br N 25 30 35 Розчин 5 г (13,1 ммоля) 2-[4-(3-аміно-6-бромхінолін-4-іламіно)-феніл]-2-метилпропіонітрилу (приклад 1g) і 1,59 г (15,7 ммоля) триетиламіну в 120 мл CH2Cl2 при 0°C у бані з льодом протягом 40 хв додають до розчину 2,85 г (14,4 ммоля) трихлорметилхлорформіату (Fluka, Buchs, Switzerland) в 80 мл CH2Cl2. Реакційну суміш перемішують протягом 20 хв при цій температурі потім реакцію зупиняють насиченим водним розчином NaHCO 3, перемішують протягом 5 хв та екстрагують за допомогою CH2Cl2. Органічний шар сушать над Na2SO4, фільтрують і випарюють у вакуумі та одержують неочищену очікувану сполуку у вигляді + коричнюватої твердої речовини. ЕР-МС: 407, 409 (M + H) , Br; аналітична ВЕРХ: tret= 3,05 хв (градієнтний режим 1). Приклад 1i 2-[4-(8-бром-3-метил-2-оксо-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-2-метилпропіонітрил 11 UA 98473 C2 N O N N Br N 5 10 15 20 25 30 35 40 45 50 До розчину 3,45 г (8,47 ммоля) 2-[4-(8-бром-2-оксо-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)феніл]-2-метилпропіонітрилу (приклад 1h), 1,8 г (12,7 ммоля) йодметану (Fluka, Buchs, Switzerland) і 273 мг (0,847 ммоля) тетрабутиламонійброміду (Fluka, Buchs, Switzerland) в 170 мл CH2Cl2 додають розчин 508 мг (12,7 ммоля) NaOH (Fluka, Buchs, Switzerland) в 85 мл H2O. Реакційну суміш перемішують протягом 2 днів і додають 900 мг (6,35 ммоля) йодметану та 254 мг (6,35 ммоля) NaOH в 5 мл H2O. Реакційну суміш перемішують протягом 1 дня при КТ . Потім реакцію зупиняють за допомогою H2O та екстрагують за допомогою CH2Cl2 (2). Органічний шар промивають розсолом, сушать над Na2SO4, фільтрують і випарюють у вакуумі та одержують + очікувану сполуку у вигляді бежевої твердої речовини. ЕР-МС: 421, 423 (M + H) , Br; аналітична ВЕРХ: tret= 3,15 хв (градієнтний режим 1). Приклад 2 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)феніл]пропіонітрил-п-толуолсульфонат 26,5 г 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)феніл]пропіонітрил разом з 55 мл мурашиної кислоти поміщають у скляний реактор. Цю суміш нагрівають до 60 °C та одержують прозорий розчин. Цей розчин фільтрують до одержання прозорого розчину та промивають за допомогою 36 мл мурашиної кислоти. Потім мурашину кислоту відганяють, поки об'єм розчину, що залишився, не стане рівним 55 мл. Потім при 50 °C додають розчин 11,3 г п-толуолсульфонової кислоти в 228 мл ацетону, а потім протягом 30 хв додатково додають 822 мл ацетону. З реакційної суміші осаджується сіль. Суміш охолоджують до 0 °C протягом 2 год., перемішують при цій температурі протягом 3 год., потім відфільтровують і промивають за допомогою 84 мл ацетону. Продукт сушать при 60 °C у вакуумі протягом 18 год. та одержують 29,8 г (82,4 %) 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]пропіонітрил-п-толуолсульфонату (кристалічна форма A). Кристалічні форми, запропоновані в даному винаході, синтезують відповідно до наведених нижче прикладів, які є ілюстративними та не обмежують обсяг даного винаходу. Приклад 3: Одержання форми A 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5c]хінолін-1-іл)-феніл]-пропіонітрилу Форму A сполуки I можна одержати в такий спосіб: 241 г вільної основи розчиняють в 2,4 л оцтової кислоти при 50 °C. Розчин фільтрують до одержання прозорого розчину, промивають за допомогою 250 мл оцтової кислоти та потім при 50 °C додають 7,2 л води. Починає осаджуватися вільна основа. Суміш охолоджують протягом 1 год. до 25 °C, потім фільтрують і промивають за допомогою 10 л H2O. Потім вільну основу сушать у вакуумі при 50 °C протягом ночі та одержують 204 г вільної основи. Приклад 4: Одержання форми B 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5c]хінолін-1-іл)-феніл]-пропіонітрилу 0,47 г вільної основи (сполука I) поміщають у реактор разом з 2 мл мурашиної кислоти. Суміш нагрівають до 60 °C та одержують прозорий розчин. Потім додають 5,2 мл метанолу. Суміш нагрівають при 65 °C протягом 2 год.. Сполука I починає осаджуватися (за цих умов мурашина кислота етерифікується у відповідний метиловий ефір). Суміш охолоджують до кімнатної температури та перемішують при кімнатній температурі протягом ще 2 год.. Потім осад відфільтровують, промивають за допомогою 2 мл метанолу та сушать у вакуумі при 60 °C протягом 17 год. та одержують форму B сполуки I. Приклад 5: Одержання форми C 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5c]хінолін-1-іл)-феніл]-пропіонітрилу Сполука I переходить в іншу поліморфну форму після приведення в рівновагу в різних розчинниках (експеримент з диспергування з використанням приблизно 20 мг зразка та 0,5 мл 12 UA 98473 C2 5 10 15 20 25 30 35 40 45 50 55 60 розчинника та приведенням у рівновагу при 25°C протягом 24 год. (з перемішуванням)). У метанолі, суміші метанол/вода, ДМФ, етанолі, етилацетаті та ТГФ можна виявити цю нову форму C. Сполуку I (0,94 г) додають до 14 мл етанолу і нагрівають до 62 °C. Потім додають 3 мл мурашиної кислоти і одержують прозорий розчин. Суміш перемішують 2 год. при 62 °C, при цьому починає осаджуватися вільна основа. Суміш охолоджують до кімнатної температури, перемішують при кімнатній температурі протягом 2,5 год. і потім відфільтровують. Потім осад на фільтрі промивають за допомогою 5 мл охолодженого льодом етанолу та після цього сушать у вакуумі при 60 °C протягом ночі і одержують форму C сполуки I. Альтернативно, сполуку I розчиняють у мурашиній кислоті при 60°C, фільтрують до одержання прозорого розчину та потім додають метанол. Після перемішування протягом 2 год. при 65°C, суміш охолоджують до кімнатної температури, сіль відфільтровують і промивають охолодженим льодом метанолом та одержують форму C сполуки I. Приклад 6: Одержання форми D 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5c]хінолін-1-іл)-феніл]-пропіонітрилу Сполука I переходить в іншу поліморфну форму після приведення в рівновагу в різних розчинниках (експеримент з диспергування з використанням приблизно 20 мг зразка та 0,5 мл розчинника та приведенням у рівновагу при 25°C протягом 24 год. (з перемішуванням)). В ізопропанолі як розчиннику можна виявити цю нову форму D. Приклад 7: Одержання форми HA моногідрату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Цю сполуку одержують після кристалізації шляхом повільного випарювання розчинника з розчину в ДМФ при кімнатній температурі. Приклад 8: Одержання форми A монотозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]пропіонітрил (сполука формули I) розчиняють в мурашиній кислоті при 56°C та отриманий розчин фільтрують до одержання прозорого розчину. Потім фільтрат концентрують і протягом 30 хв додають розчин п-толуолсульфонової кислоти (1,05 екв.) в ацетоні. Після додавання 25% і 50% об'єму в суміш вносять затравку для стимулювання кристалізації. Додають додаткову кількість ацетону і суспензію охолоджують до 0°C. Продукт, що закристалізувався (форма A сполуки I монотозилат) збирають центрифугуванням і сушать при°60 C у вакуумі. Приклад 9: Одержання форми B монотозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Фазове перетворення форми A, отриманої відповідно до прикладу 8, в іншу кристалічну форму, далі названу формою B, можна спостерігати при температурі вище 70°C (її також можна виявити при проведенні відповідної ДСК (диференціальна скануюча калориметрія)). За даними експериментів за допомогою ДСК це перетворення оборотне. Форма A і форма B є енантіомерами. Приклад 10: Одержання форми HA моногідрату монотозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Насичений розчин сполуки I дитозилату в суміші етанол/ацетон (1:1) можна використати в експерименті з повільним випарюванням розчинника при 25°C. Виявлено утворення монокристалів моногідрату монотозилату сполуки 1 (форма H A) і можна розрахувати структуру монокристалу. Приклад 11: Одержання форми HB дигідрату монотозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Шляхом проведення експерименту з приведення в рівновагу дитозилату сполуки I у воді (через 3 дні) при 25°C можна спостерігати утворення монокристалів. Можна визначити та розрахована структура кристала показала, що він являє собою дигідрат монотозилату сполуки I (форма HB). Приклад 12: Одержання форми SA сольвату з 2 молекулами мурашиної кислоти монотозилату 2-метил-2[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу 13 UA 98473 C2 5 10 15 20 25 30 35 40 45 Структуру монокристалу сполуки I монотозилат сольвату з 2 молекулами мурашиної кислоти визначали за допомогою рентгенографії (модифікація S A). Підходящі монокристали одержували шляхом приведення в рівновагу сполуки I монотозилат у суміші розчинників ацетон/мурашина кислота (1:1 (об./об.)) при 50°C після охолодження до кімнатної температури. Встановлено, що ця сіль має склад 1:1,7 (п-толуолсульфонат сполуки I/мурашина кислота). Хоча встановлено, що ця сіль має склад 1:1,7, оскільки одна молекула сольвату знаходиться в неупорядкованому стані, імовірна стехіометрія 1:2. Склади, що містять менше 2 молекул мурашиної кислоти виявлені з тієї причини, що молекули мурашиної кислоти можуть виходити зі структури. Приклад 13: Одержання форми A дитозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Якщо розчин сполуки I у мурашиній кислоті обробити ацетоновим розчином птолуолсульфонової кислоти (1,25 экв.), то після фільтрування монотозилату при кристалізації маткового розчину як другу порцію можна виділити дитозилат сполуки I. Дитозилат сполуки I характеризується початковими втратами при сушінні, рівними 0,4% (при нагріванні до 140°C). За допомогою ДСК виявляється плавлення приблизно при 262°C з ентальпією плавлення, рівною приблизно 93 Дж/г. Приклад 14: Одержання форми HA тригідрату дитозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу У насиченому розчині дитозилату сполуки I у суміші дихлорметан/метанол (1:1 (об./об.)) можна було виявити тригідрат дитозилату сполуки I (модифікація H A) і виявлені монокристали. Приклад 15: Одержання аморфного монотозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Аморфну речовину одержували шляхом розпилювального сушіння монотозилату сполуки I. За даними ДСК температура склування, Tg, дорівнює приблизно 128°C. Після перекристалізації приблизно при 175°C речовина плавилася приблизно при 279°C з ентальпією плавлення, рівною приблизно 65 Дж/г. Приклад 16: Одержання форми SC сольвату з 2 молекулами мурашиної кислоти моногідрату монотозилату 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)феніл]-пропіонітрилу Структуру монокристалу сольвату з 2 молекулами мурашиної кислоти моногідрату монотозилату сполуки I визначали за допомогою рентгенографії (модифікація S C). Підходящі монокристали одержували шляхом приведення в рівновагу монотозилату сполуки I у суміші розчинників метилізобутилкетон/мурашина кислота (1:1 (об./об.)) при 50°C після охолодження до кімнатної температури. Приклад 17: Одержання форми SB сольвату з 2 молекулами оцтової кислоти монотозилату 2-метил-2-[4(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-c]хінолін-1-іл)-феніл]-пропіонітрилу Структуру монокристалу сольвату з 2 молекулами оцтової кислоти монотозилату сполуки I визначали за допомогою рентгенографії (модифікація SC). Підходящі монокристали одержували шляхом приведення в рівновагу монотозилату сполуки I у суміші розчинників метилізобутилкетон/оцтова кислота (1:1 (об./об.)) при 50°C після охолодження до кімнатної температури. ФОРМУЛА ВИНАХОДУ 50 1. Кристалічна форма сполуки формули І 14 UA 98473 C2 N O N N N N 5 (І) або гідрату або сольвату сполуки формули І, або солі сполуки формули І, або гідрату або сольвату солі сполуки формули І, де кристалічна форма є кристалічною формою А, на рентгенограмі якої міститься пік при куті дифракції 2-тета, рівному 8,4°±0,3°. 2. Кристалічна форма сполуки формули І N O N N N N 10 (І) або гідрату або сольвату сполуки формули І, або солі сполуки формули І, або гідрату або сольвату солі сполуки формули І, де кристалічна форма є кристалічною формою В, на рентгенограмі якої міститься пік при куті дифракції 2-тета, рівному 6,9°±0,3°. 3. Кристалічна форма сполуки формули І N O N N N N 15 (І) або гідрату або сольвату сполуки формули І, або солі сполуки формули І, або гідрату або сольвату солі сполуки формули І, де кристалічна форма є кристалічною формою С, на рентгенограмі якої міститься пік при куті дифракції 2-тета, рівному 14,7°±0,3°. 4. Кристалічна форма сполуки формули І N O N N N N 20 (І) або гідрату або сольвату сполуки формули І, або солі сполуки формули І, або гідрату або сольвату солі сполуки формули І, де кристалічна форма є кристалічною формою D, на рентгенограмі якої міститься пік при куті дифракції 2-тета, рівному 23,9°±0,3°. 5. Моногідрат сполуки формули І 15 UA 98473 C2 N O N N N N (І) у кристалічній формі НA, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 17,6°±0,3°. 6. Монотозилат сполуки формули І N O N N N 5 10 N (І) у кристалічній формі А, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 5,7°±0,3°. 7. Монотозилат сполуки формули І за п. 6, на рентгенограмі якого містяться піки при кутах дифракції 2-тета, рівних 5,4°±0,3°; 5,7°±0,3° та 17,2°±0,3°. 8. Монотозилат сполуки формули І за п. 6, що має рентгенограму, в основному таку, як представлена на фіг. 6. 9. Монотозилат сполуки формули І N O N N N N 15 (І) у кристалічній формі В, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 5,8°±0,3°. 10. Монотозилат сполуки формули І за п. 9, на рентгенограмі якого містяться піки при кутах дифракції 2-тета, рівних 5,8°±0,3°; 17,8°±0,3° та 18,7°±0,3°. 11. Моногідрат монотозилату сполуки формули І N O N N N N 20 (І) у кристалічній формі НА, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 6,5°±0,3°. 16 UA 98473 C2 12. Дигідрат монотозилату сполуки формули І N O N N N N 5 (І) у кристалічній формі НВ, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 6,9°±0,3°. 13. Сольват з 2 молекулами мурашиної кислоти монотозилату сполуки формули І N O N N N N (І) у кристалічній формі SA, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 5,8°±0,3°. 14. Дитозилат сполуки формули І N O N N N 10 N (І) у кристалічній формі А, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 22,4°±0,3°. 15. Тригідрат дитозилату сполуки формули І N O N N N N 15 (І) у кристалічній формі НА, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 4,7°±0,3°. 16. Аморфний монотозилат сполуки формули І 17 UA 98473 C2 N O N N N N (І). 17. Моногідрат сольвату з 2 молекулами мурашиної кислоти монотозилату сполуки формули І N O N N N N 5 (І) у кристалічній формі SС, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 5,6°±0,3°. 18. Сольват з 2 молекулами оцтової кислоти монотозилату сполуки формули І N O N N N N 10 (І) у кристалічній формі SВ, на рентгенограмі якого міститься пік при куті дифракції 2-тета, рівному 5,7°±0,3°. 19. Тверда форма сполуки формули І N O N N N N 15 (І) або гідрату або сольвату сполуки формули І, або солі сполуки формули І, або гідрату або сольвату солі сполуки формули І за будь-яким з пп. 1-18, що знаходиться в основному в чистому вигляді. 20. Фармацевтична композиція, що містить тверду форму сполуки формули І 18 UA 98473 C2 N O N N N N (І) або її гідратів або сольватів, її солей та гідратів або сольватів її солей за будь-яким з пп. 1-18 і необов'язково щонайменше один фармацевтично прийнятний носій. 21. Застосування твердої форми сполуки формули І N O N N N 5 10 15 20 25 N (І) її гідратів або сольватів, її солей і гідратів або сольватів її солей за будь-яким з пп. 1-18 для виготовлення терапевтичного засобу, призначеного для лікування проліферативного захворювання, вибраного із групи, що включає доброякісну або злоякісну пухлину, карциному головного мозку, нирок, печінки, надниркової залози, сечового міхура, молочної залози, шлунка, пухлини шлунка, яєчників, ободової кишки, прямої кишки, передміхурової залози, підшлункової залози, легенів, піхви або щитовидної залози, саркому, гліобластому, множинну мієлому або рак шлунково-кишкового тракту, переважно - карциному ободової кишки або колоректальну аденому, або пухлину голови та шиї, гіперпроліферацію епідермісу, псоріаз, гіперплазію передміхурової залози, неоплазію, неоплазію епітеліального характеру, лімфому, карциному молочної залози або лейкозу, а також захворювань, що включають синдром Коудена, хворобу Лерміта-Дудоса та синдром Банаяна-Зонана, або захворювань, у яких шлях РІ3К/РКВ є аберантно активованим. 22. Спосіб лікування захворювання, вибраного з групи, що включає доброякісну або злоякісну пухлину, карциному головного мозку, нирок, печінки, надниркової залози, сечового міхура, молочної залози, шлунка, пухлини шлунка, яєчників, ободової кишки, прямої кишки, передміхурової залози, підшлункової залози, легенів, піхви або щитовидної залози, саркому, гліобластому, множинну мієлому або рак шлунково-кишкового тракту, переважно - карциному ободової кишки або колоректальну аденому, або пухлину голови та шиї, гіперпроліферацію епідермісу, псоріаз, гіперплазію передміхурової залози, неоплазію, неоплазію епітеліального характеру, лімфому, карциному молочної залози або лейкоз, а також захворювання, вибраного з синдрому Коудена, хвороби Лерміта-Дудоса та синдрому Банаяна-Зонана, або захворювань, у яких шлях РІ3К/РКВ є аберантно активованим, у теплокровної тварини, що цього потребує, у якому тварині вводять кристалічну форму сполуки формули І N O N N N N 30 (І) її гідратів або сольватів, її солей або гідратів або сольватів її солей за будь-яким з пп. 1-18 у кількості, яка є терапевтично ефективною для боротьби з відповідним захворюванням. 19 UA 98473 C2 20 UA 98473 C2 21 UA 98473 C2 22 UA 98473 C2 23 UA 98473 C2 24 UA 98473 C2 25 UA 98473 C2 26 UA 98473 C2 27 UA 98473 C2 Комп’ютерна верстка В. Мацело Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 28
ДивитисяДодаткова інформація
Назва патенту англійськоюSalts and crystal forms of 2-methyl-2-[4-(3-methyl-2-oxo-8-quinolin-3-yl-2,3-dihydro-imidazo[4,5-c]quinolin-1-yl)-phenyl]-propionitrile
Автори англійськоюStowasser, Frank, Banziger, Markus, Garad, Sudhakar Devidasrao
Назва патенту російськоюСоли и кристаллические формы 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрила
Автори російськоюШтовассер Франк, Бенцигер Маркус, Гарад Судхакар Девидасрао
МПК / Мітки
МПК: C07D 471/04, A61P 35/00, A61K 31/4745
Мітки: кристалічні, форми, 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-с]хінолін-1-іл)феніл]пропіонітрилу, солі
Код посилання
<a href="https://ua.patents.su/30-98473-soli-ta-kristalichni-formi-2-metil-2-4-3-metil-2-okso-8-khinolin-3-il-23-digidroimidazo45-skhinolin-1-ilfenilpropionitrilu.html" target="_blank" rel="follow" title="База патентів України">Солі та кристалічні форми 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-с]хінолін-1-іл)феніл]пропіонітрилу</a>
Попередній патент: Застосування агоніста рецептора epo людини для лікування інтолерантності до глюкози
Наступний патент: Спосіб сульфінілування похідної піразолу
Випадковий патент: Регулятор потужності нагрівачів (активного опору)