Інсектицидні сполуки
Номер патенту: 103540
Опубліковано: 25.10.2013
Автори: Корсі Камілла, Кассеір Жером Ів, Піттерна Томас, Майєнфіш Петер
Формула / Реферат
1. Сполука формули (І)
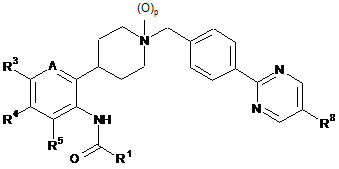 , (І)
, (І)
де
А означає CR2 або N;
p дорівнює 0 або 1;
R1 означає пірид-4-ил, що необов'язково містить один або два замісники, кожен з яких незалежно вибраний з галогену, С1-С3алкілу, С1-С3галоалкілу або С1-С3алкокси;
R2 означає водень, галоген, С1-С3галоалкіл або С1-С3галоалкокси;
R3 та R4 незалежно означають водень, галоген, ціано, С1-С8алкіл, С1-С8галоалкіл, С2-С8алкеніл, С2-С8галоалкеніл, С3-С8циклоалкіл, С3-С8галоциклоалкіл, С1-С8алкокси, С1-С8галоалкокси, С1-С8алкілтіо або С1-С8галоалкілтіо;
R5 означає водень або галоген;
R8 означає водень, галоген, ціано, С1-С8алкіл, С1-С8галоалкіл, С3-С8циклоалкіл, С2-С8алкеніл, С2-С8галоалкеніл, С2-С8алкініл, С1-С8алкокси чи С1-С8галоалкокси або сіль цих сполук.
2. Сполука за п. 1, де R1 означає пірид-4-ил, що необов'язково містить один або два замісники, кожен з яких незалежно вибраний з фтору, хлору, брому, метилу, дифторметилу, хлордифторметилу, трифторметилу чи метокси.
3. Сполука за п. 1 або 2, де R3 означає водень, галоген, ціано, С1-С6алкіл, С1-С6галоалкіл, С2-С6алкеніл, С3-С6циклоалкіл, С1-С6алкокси, С1-С6галоалкокси, С1-С6алкілтіо чи С1-С6галоалкілтіо.
4. Сполука за будь-яким з попередніх пунктів, де R4 означає водень, галоген, ціано, С1-С6алкіл, С1-С6галоалкіл, С2-С6алкеніл, С3-С6циклоалкіл, С1-С6алкокси, С1-С6галоалкокси, С1-С6алкілтіо чи С1-С6галоалкілтіо.
5. Сполука за будь-яким з попередніх пунктів, де R5 означає водень, фтор, хлор або бром.
6. Сполука за будь-яким з попередніх пунктів, де R8 означає водень, галоген, ціано, С1-С6алкіл, С1-С6галоалкіл, С3-С6циклоалкіл, С3-С6алкеніл, С2-С6галоалкеніл, С2-С6алкініл, С1-С6алкокси чи С1-С6галоалкокси.
7. Спосіб боротьби з комахами, акаридами, нематодами або молюсками, який полягає у нанесенні на шкідника, на місцезнаходження шкідника або на рослину, чутливу до атаки шкідника, достатньої для знищення комах, акарид, нематод або молюсків кількості сполуки формули (І), визначеної у будь-якому з пп. 1-6.
8. Інсектицидна, акарицидна, нематоцидна або молюскоцидна композиція, яка містить достатню для знищення комах, акарид, нематод або молюсків кількість сполуки формули (І), визначеної у будь-якому з пп. 1-6.
Текст
Реферат: 2 1 Сполука формули (І), де А означає CR або N; p дорівнює 0 або 1; R означає пірид-4-ил, необов'язково містить один або два замісники, кожен з яких незалежно вибраний з галогену, С 12 С3алкілу, С1-С3галоалкілу або С1-С3алкокси; R означає водень, галоген, С1-С3галоалкіл або С13 4 С3галоалкокси; R та R незалежно означають водень, галоген, ціано, С1-С8алкіл, С1С8галоалкіл, С2-С8алкеніл, С2-С8галоалкеніл, С3-С8циклоалкіл, С3-С8галоциклоалкіл, С15 С8алкокси, С1-С8галоалкокси, С1-С8алкілтіо або С1-С8галоалкілтіо; R означає водень або 8 галоген; R означає водень, галоген, ціано, С1-С8алкіл, С1-С8галоалкіл, С3-С8циклоалкіл, С2С8алкеніл, С2-С8галоалкеніл, С2-С8алкініл, С1-С8алкокси чи С1-С8галоалкокси або її сіль. Композиція на її основі та спосіб боротьби з комахами, акаридами, нематодами або молюсками. UA 103540 C2 (12) UA 103540 C2 (O)p N R 3 R 4 A N N NH R R 8 5 O R 1 (І) UA 103540 C2 5 Предметом цього винаходу є певні похідні піперидину, процеси їх отримання, інсектицидні, акарицидні, молюскоцидні та нематоцидні композиції, до складу яких вони входять, а також методи їх застосування для боротьби зі шкідниками - комахами, акаридами, молюсками (слимаками) та нематодами. Похідні піперидину з інсектицидними властивостями описані, наприклад, у публікації WO 2006/003494. Авторами цієї розробки було виявлено, що певні піперидини маю покращені інсектицидні властивості. Отже, цей винахід пропонує сполуку формули (I): ( O )p N R R 3 A 4 15 20 25 30 35 40 45 50 N NH R 10 N (I) R 8 5 O R 1 , де 2 A означає CR або N; p дорівнює 0 або 1; 1 R означає пірид-4-ил, як варіант - заміщуваний одним або двома заміщувачами, кожен з яких незалежно вибраний з галогену, C1-C3алкілу, C1-C3галоалкілу або C1-C3алкоксі; 2 R означає водень, галоген, C1-C3галоалкіл або C1-C3галоалкоксі; 3 4 R та R незалежно означають водень, галоген, ціано, C1-C8алкіл, C1-C8галоалкіл, C2C8алкеніл, C2-C8галоалкеніл, C3-C8циклоалкіл, C3-C8галоциклоалкіл, C1-C8алкоксі, C1C8галоалкоксі, C1-C8алкілтіо або C1-C8галоалкілтіо; 5 R означає водень або галоген; а 8 R означає водень, галоген, ціано, C1-C8алкіл, C1-C8галоалкіл, C3-C8циклоалкіл, C2C8алкеніл, C2-C8галоалкеніл, C2-C8алкініл, C1-C8алкоксі чи C1-C8галоалкоксі або сіль цих сполук. Сполуки формули (I) можуть існувати у вигляді різних геометричних або оптичних ізомерів або таутомерних форм. Цей винахід охоплює усі такі ізомери й таутомери та їх суміші у всіх пропорціях, а також ізомерні форми, такі як дейтеровані сполуки. Кожен алкільний фрагмент, самостійно чи у складi більшої групи (такої як алкоксі або алкілтіо), являє собою прямий або розгалужений ланцюг, наприклад, метил, етил, n-пропіл, ізопропіл, n-бутил, сек-бутил, ізо-бутил чи трет-бутил. Алкільні групи оптимально є алкільними групами C1-C6, оптимальніше - C1-C4, найоптимальніше - C1-C3. Алкенільні та алкінільні фрагменти можуть являти собою прямі або розгалужені ланцюги, а алкенільні фрагменти, залежно від обставин, можуть мати конфігурацію(E)- або (Z)-. Прикладами є вініл, аліл та пропаргіл. Алкенільні та алкінільні групи оптимально є алкенільними або алкінільними групами C2-C6, оптимальніше - C2-C4, найоптимальніше - C2-C3. Галоген означає фтор, хлор, бром чи йод. Галогеналкільні групи (самостійно чи у складi більшої групи, такої як галоалкоксі або галоалкілтіо) являють собою алкільні групи, заміщені одним чи кількома, однаковими чи різними атомами галогену, наприклад, -CF3, -CF2Cl, -CH2CF3 або -CH2CHF2. Галоалкеніл являє собою алкенільні групи, заміщені одним чи кількома, однаковими чи різними атомами галогену, наприклад, -CH=CF2 або -CCl=CClF. Галоалкенільні групи - це, відповідно, алкенільні групи, які заміщені одним чи кількома, однаковими чи різними атомами галогену, наприклад, -CH=CF2 або -CCl=CClF. Циклоалкільні групи можуть бути моноциклічними або біциклічними та - як варіант - бути заміщені однією чи кількома метильними групами. Циклоалкільні групи оптимально містять від 3 до 8 атомів вуглецю, оптимальніше - від 3 до 6 атомів вуглецю. Прикладами моноциклічних циклоалкільних груп є циклопропіл, 1-метилциклопропіл, 2-метилциклопропіл, циклобутил, циклопентил та циклогексил. Галоциклоалкільні групи - це циклоалкільні групи, які заміщені одним чи кількома, однаковими чи різними атомами галогену, та можуть - як варіант - бути заміщені однією чи кількома метильними групами. Прикладами моноциклічних галоциклоалкільних груп є 2,2дихлорциклопропіл, 2,2-дихлор-1-метилциклопропіл та 2-хлор-4-фтор-циклогексил. 1 2 3 4 5 8 Оптимальними групами та значеннями для R , R , R , R , R та R у будь-якому поєднанні є 1 UA 103540 C2 5 10 15 20 25 30 35 40 45 50 55 60 ті, що вказані нижче. 1 Оптимально R означає пірид-4-ил, як варіант - заміщений одним або двома заміщувачами, кожен з яких незалежно вибраний з фтору, хлору, брому, метилу, дифторметилу, 1 хлордифторметилу, трифторметилу або метоксі; оптимальніше R означає пірид-4-ил, як варіант - заміщений одним або двома заміщувачами, кожен з яких незалежно вибраний з 1 фтору, хлору або метилу; найоптимальніше R означає пірид-4-ил, заміщений одним або двома заміщувачами, кожен з яких незалежно вибраний з фтору або хлору. Оптимально один заміщувач займає позицію №2 у кільцi пірид-4-илу, а другий заміщувач - як варіант - займає 1 позицію № 5 або 6 у кільцi пірид-4-илу. Прикладами найоптимальніших груп R є 2-фторпірид-4ил, 2-хлорпірид-4-ил, 2,5-дихлорпірид-4-ил, а також 2,6-дихлорпірид-4-ил. 2 Оптимально R означає водень або галоген. 2 Оптимальніше R означає водень, фтор або хлор. 2 Ще оптимальніше R означає водень або фтор. 2 Найоптимальніше R означає водень. 3 Оптимально R означає водень, галоген, ціано, C1-C6алкіл, C1-C6галоалкіл, C2-C6алкеніл, C3C6циклоалкіл, C1-C6алкоксі, C1-C6галоалкоксі, C1-C6алкілтіо або C1-C6галоалкілтіо. 3 Оптимальніше R означає водень, фтор, хлор, бром, ціано, метил, ізо-пропіл, фторметил, дифторметил, трифторметил, гептафтор-ізо-пропіл, вініл, циклопропіл, метоксі, етоксі, дифторметоксі, трифторметоксі, 2,2,2-трифторетоксі або трифторметилтіо. 3 Ще оптимальніше R означає водень, фтор, хлор, бром, дифторметил, трифторметил, гептафтор-ізо-пропіл, вініл, циклопропіл, метоксі, дифторметоксі, трифторметоксі або 2,2,2трифторетоксі. 3 Навіть ще оптимальніше R означає водень, фтор, хлор, бром, трифторметил, циклопропіл або трифторметоксі. 3 Найоптимальніше R означає трифторметил. 4 Оптимально R означає водень, галоген, ціано, C1-C6алкіл, C1-C6галоалкіл, C2-C6алкеніл, C3C6циклоалкіл, C1-C6алкоксі, C1-C6галоалкоксі, C1-C6алкілтіо або C1-C6галоалкілтіо. 4 Оптимальніше R означає водень, фтор, хлор, бром, метил, ізо-пропіл, фторметил, дифторметил, трифторметил, гептафтор-ізо-пропіл, вініл, циклопропіл, метоксі, етоксі, дифторметоксі, трифторметоксі або 2,2,2-трифторетоксі. 4 Ще оптимальніше R означає водень, фтор, хлор, метил або трифторметил. 4 Найоптимальніше R означає водень. 5 Оптимально R означає водень, фтор, хлор або бром. 5 Оптимальніше R означає водень або фтор. 5 Найоптимальніше R означає водень. 8 Оптимально R означає водень, галоген, ціано, C1-C6алкіл, C1-C6галоалкіл, C3-C6циклоалкіл, C2-C6алкеніл, C2-C6галоалкеніл, C2-C6алкініл, C1-C6алкоксі або C1-C6галоалкоксі. 8 Оптимальніше R означає водень, фтор, хлор, бром, ціано, метил, трифторметил, циклопропіл, етиніл, метоксі або трифторметоксі. 8 Ще оптимальніше R означає водень, фтор, хлор, бром, трифторметил або трифторметоксі. 8 Навіть ще оптимальніше R означає фтор або хлор. 8 Найоптимальніше R означає хлор. 1 3 4 5 8 Одним з оптимальних варіантів здійснення є сполуки формули (Ia), у якій R , R , R , R та R 2 відповідають визначенню для сполуки формули (I), A означає CR , а p дорівнює 0. Переваги 1 2 3 4 5 8 щодо R , R , R , R , R та R ідентичні вказаним для сполуки формули (I). 1 3 4 5 8 Іншим оптимальним варіантом здійснення є сполуки формули (Ib), у якій R , R , R , R та R відповідають визначенню для сполуки формули (I), A означає N, а p дорівнює 0. Переваги щодо 1 3 4 5 8 R , R , R , R та R ідентичні вказаним для сполуки формули (I). 1 3 4 5 Ще одним оптимальним варіантом здійснення є сполуки формули (Ic), у якій R , R , R , R та 8 2 R відповідають визначенню для сполуки формули (I), A означає CR , а p дорівнює 1. Переваги 1 2 3 4 5 8 щодо R , R , R , R , R та R ідентичні вказаним для сполуки формули (I). 1 3 4 5 8 Оптимальним варіантом здійснення є сполуки формули (Id), у якій R , R , R , R та R відповідають визначенню для сполуки формули (I), A означає N, а p дорівнює 1. Переваги щодо 1 3 4 5 8 R , R , R , R та R ідентичні вказаним для сполуки формули (I). 1 3 4 5 8 Ще одним оптимальним варіантом здійснення є солі формули (Ie), у якій R , R , R , R та R 2 відповідають визначенню для сполуки формули (I), A означає CR , p дорівнює 0, а сіль утворюється шляхом обробки будь-якою кислотою з перелiчених нижче: соляної, оцтової, 2хлорбензойної, 2-гідроксібензойної, етансульфонової, 3-гідроксіпропан-1-сульфонової, метансульфонової, (4-метилфеніл)сульфонової (толуол-4-сульфонової кислоти), 3феноксіпропіонової, фосфорної, 2,3,4,5-тетрагідроксі-6-оксогексанової, тридеканової, 2 UA 103540 C2 1 5 10 2 3 4 5 8 трифтороцтової, глюкоронової або саліцилової кислоти. Переваги щодо R , R , R , R , R та R ідентичні вказаним для сполуки формули (I). Оптимально кислотою є оцтова або соляна кислота. 1 3 4 5 8 Оптимальним варіантом здійснення є солі формули (If), у якій R , R , R , R та R відповідають визначенню для сполуки формули (I), A означає N, p дорівнює 0, а сіль утворюється шляхом обробки кислотою згідно з визначенням для сполуки формули (Ie). 1 3 4 5 8 Переваги щодо R , R , R , R та R ідентичні вказаним для сполуки формули (I). Оптимально кислотою є оцтова або соляна кислота. Певні проміжні сполуки є новими і таким чином становлять ще один варіант цього винаходу. Однією з таких груп проміжних сполук є сполуки формули (II): NH 3 R N (II) 4 R NH 5 R 1 O R , 1 3 4 5 1 3 де R , R , R та R відповідають визначенню для сполуки формули (I). Переваги щодо R , R , 4 5 R та R ідентичні вказаним для сполуки формули (I). Іншою групою проміжних продуктів є сполуки формули (III): 11 R O N R 3 O N (III) R 4 NH R 15 20 5 O R 1 , 1 3 4 5 11 де R , R , R та R відповідають визначенню для сполуки формули (I), а R означає C1C6алкіл, такий як трет-бутил, C2-C6алкеніл, такий як аліл, або бензил, як варіант - заміщений одним-трьома заміщувачами, незалежно вибраними з галогену, C1-C6алкілу, C1-C6галоалкілу, 1 3 4 5 C1-C6алкоксі або C1-C6галоалкоксі. Переваги щодо R , R , R та R ідентичні вказаним для 11 сполуки формули (I). R оптимально означає трет-бутил. Ще іншою групою проміжних сполук є сполуки формули (IV): 11 R O N 3 R O N (IV) 4 R NH2 5 R 25 , 3 4 5 3 5 де R , R та R відповідають визначенню для сполуки формули (I), або R та R означають 4 11 водень, R означає фтор, хлор чи трифторметил, а R відповідає визначенню для сполуки 3 4 5 формули (III). Переваги щодо R , R та R ідентичні вказаним для сполуки формули (I). 11 Переваги щодо R ідентичні вказаним для сполуки формули (III). Ще однією групою проміжних сполук є сполуки формули (V): 3 UA 103540 C2 11 O N R 3 R O N (V) R 4 NH2 R 5 5 , 3 4 5 3 5 де R , R та R відповідають визначенню для сполуки формули (I), або R та R означають 4 11 водень, R означає фтор, хлор чи трифторметил, а R відповідає визначенню для сполуки 3 4 5 формули (III). Переваги щодо R , R та R ідентичні вказаним для сполуки формули (I). 11 Переваги щодо R ідентичні вказаним для сполуки формули (III). Наступною групою проміжних сполук є сполуки формули (VI): 11 R O N 3 R O N (VI) 4 R NO2 5 R 10 , 3 4 5 11 де R , R та R відповідають визначенню для сполуки формули (I), а R відповідає 3 4 5 визначенню для сполуки формули (III). Переваги щодо R , R та R ідентичні вказаним для 11 сполуки формули (I). Переваги щодо R ідентичні вказаним для сполуки формули (III). Ще однією групою проміжних сполук є сполуки формули (3): X N N 15 (3) R 8 , 8 де R відповідають визначенню для сполуки формули (I), а X означає хлор або бром. 8 Переваги щодо R ідентичні вказаним для сполуки формули (I). Оптимально X означає хлор. Ще однією групою проміжних сполук є сполуки формули (4): O H N N 20 25 (4) R 8 , 8 8 де R відповідає визначенню для сполуки формули (I). Переваги щодо R ідентичні вказаним для сполуки формули (I). Сполуки, що є предметом цього винаходу, можна отримати різними методами відповідно до опису в публікації WO 2006/003494. Наприклад, сполуки формули (I) можуть бути отримані згідно зі схемами 1, 2 та 3. 1 3 4 5 8 Таким чином, сполуку формули (1), де A, R , R , R , R та R відповідають визначенню для 1 3 4 5 сполуки формули (I), можна отримати зі сполуки формули (2), де A, R , R , R та R відповідають 8 визначенню для сполуки формули (I), шляхом реакції зі сполукою формули (3), де R відповідає визначенню для сполуки формули (I), а X означає заміщувану групу, таку як галогенід (наприклад, хлорид, бромід чи йодид) або сульфонат (наприклад, мезилат чи тозилат), у присутності основи, такої як третинний амін (наприклад, діізопропілетиламін чи триетиламін), в органічному розчиннику, такому як дихлорметан, ацетонітрил чи N, N-диметилформамід, за температури від 0 °C до 100 °C, зазвичай за кімнатної температури, як показано на схемі 1. 4 UA 103540 C2 Схема 1 NH R R 3 X A N 4 R N (3) NH 8 R 5 1 O R основа (2) N R R 3 A N 4 R 10 8 R 5 1 O 5 N NH (1) R Як варіант, сполуку формули (1), згідно з наведеним вище визначенням, можна отримати зі сполуки формули (2), згідно з наведеним вище визначенням, шляхом реакції з альдегідом 8 формули (4), де R відповідає визначенню для сполуки формули (I), у присутності відновлювальної речовини, такої як (триацетоксі)боргідрид натрію, ціаноборгідрид натрію чи боран і т.п., в органічному розчиннику, такому як тетрагідрофуран, метанол чи етанол, за температури від 0 °C до 100 °C, зазвичай за кімнатної температури, як показано на схемі 2. Схема 2 O NH R 3 H A N 4 R R N (4) NH 8 R 5 O 1 R відновлювальна речовина (2) N R 3 A N 4 R R 15 20 N NH 5 O 1 R R 8 (1) Сполуки формули (2) можна отримати згідно з описом у публікації WO 2006/003494. Приклади таких методів можна знайти у прикладах приготування. Сполуки формул (3) та (4) або є відомими сполуками, або можуть бути отримані за допомогою відомих фахівцю методів. Приклади таких методів можна знайти у прикладах отримання. Схема 3 5 UA 103540 C2 N R 3 A N окисник R 4 N NH R 8 R 5 O R 1 (1) O – N+ R R 3 A N 4 R 5 O 5 10 15 20 25 30 35 40 N NH R 1 8 R (5) N-оксиди формули (5) можна отримати шляхом окиснення сполуки формули (1) окисником, таким як пероксид водню чи 3-хлорпероксібензойна кислота, в органічному розчиннику, такому як дихлорметан, етанол, метанол чи вода або суміш розчинників, за температури від -78 °C до 100 °C, зазвичай за кімнатної температури, як показано на схемі 3. Сполука формули (I) має покращені пестицидні властивості. Наприклад, такі сполуки можуть мати підвищену інсектицидну активність та/або покращену світлостійкість. Сполуки формули (I) можна використовувати для боротьби з нашестями комах-шкідників, таких як Lepidoptera, Diptera, Hemiptera, Thysanoptera, Orthoptera, Dictyoptera, Coleoptera, Siphonaptera, Hymenoptera та Isoptera, а також з іншими безхребетними шкідниками, як наприклад акариди, нематоди та молюски. Надалі комахи, акариди, нематоди й молюски разом йменуються шкідниками. Шкідники, з якими можна боротися за допомогою сполук, що є предметом цього винаходу, включають шкідників, що мають відношення до сільського господарства (в це поняття входить вирощування культур для отримання харчових продуктів та волоконних продуктів), городництва та тваринництва, утримання домашніх тварин, лісництва і зберігання продуктів рослинного походження (таких як фрукти, зерно та деревина); шкідників, які мають відношення до пошкодження штучних споруд і переносу хвороб людини та тварин, а також надокучливих шкідників (таких як мухи). Приклади видів шкідників, з якими можна боротися за допомогою сполук формули (I), включають: Myzus persicae (тля), Aphis gossypii (тля), Aphis fabae (тля), Lygus spp. (клопи), Dysdercus spp. (клопи), Nilaparvata lugens (дельфацида), Nephotettixc incticeps (цикадка), Nezara spp. (щитники), Euschistus spp. (щитники), Leptocorisa spp. (щитники), Frankliniella occidentalis (трипс), Thrips spp. (трипс), Leptinotarsa decemlineata (колорадський жук), Anthonomus grandis (довгоносик бавовняний), Aonidiella spp. (кокцидові), Trialeurodes spp. (білокрилки), Bemisia tabaci (білокрилка), Ostrinia nubilalis (метелик кукурудзяний), Spodoptera littoralis (бавовняна совка), Heliothis virescens (тютюнова совка), Helicoverpa armigera (бавовняна совка), Helicoverpa zea (бавовняна совка), Sylepta derogata (бавовняна вогнівка), Pieris brassicae (капустяна білянка), Plutella xylostella (міль капустяна), Agrotis spp. (совки), Chilo suppressalis (жовта рисова вогнівка), Locusta migratoria (сарана), Chortiocetes terminifera (сарана), Diabrotica spp. (личинки, що пошкоджують коріння), Panonychus ulmi (червоний плодовий кліщ), Panonychus citri (червоний цитрусовий кліщ), Tetranychus urticae (павутинний звичайний кліщ), Tetranychus cinnabarinus (червоний павутинний кліщ), Phyllocoptruta oleivora (цитрусовий кліщ), Polyphagotarsonemus latus (оранжерейний прозорий кліщ), Brevipalpus spp. (плоскі кліщі), Boophilus microplus (південний кліщ), Dermacentor variabilis (іксодовий собачий кліщ), Ctenocephalides felis (блоха кошача), Liriomyza spp. (листовий мінер), Musca domestica (муха кімнатна), Aedes aegypti (комар), Anopheles spp. (комарі), Culex spp. (комарі), Lucillia spp. (м'ясні мухи), Blattella germanica (тарган), Periplaneta americana (тарган), Blatta orientalis (тарган), терміти сімейства Mastotermitidae (терміти дарвінів) (наприклад, Mastotermes spp.), Kalotermitidae (деревоїдні терміти) (наприклад, Neotermes spp.), Rhinotermitidae (носаті терміти) (наприклад, Coptotermes formosanus, Reticulitermes flavipes, R. speratu, R. virginicus, R. hesperus, і R. santonensis) та Termitidae (наприклад, Globitermes sulfureus), Solenopsis geminata (мураха 6 UA 103540 C2 5 10 15 20 25 30 35 40 45 50 55 60 вогняна), Monomorium pharaonis (фараонова мураха), Damalinia spp. і Linognathus spp. (пухоїди та воші), Meloidogyne spp. (галові нематоди), Globodera spp. та Heterodera spp. (цистоутворюючі нематоди), Pratylenchus spp. (галові нематоди), Rhodopholus spp. (бананові нематоди, які прогризають ходи), Tylenchulus spp.(цитрусові нематоди), Haemonchus contortus (гельмінт), Caenorhabditis elegans (оцтова нематода), Trichostrongylus spp. (нематоди шлунково-кишкового тракту) и Deroceras reticulatum (слимак). Таким чином, винахід пропонує метод боротьби з комахами, акаридами, нематодами або молюсками, який полягає у нанесенні достатньої для знищення комах, акарид, нематод або молюсків кількості сполуки формули (I) або композиції, до складу якої входять сполуки формули (І), на шкідника, місцезнаходження шкідника, переважно рослину, або на рослину, чутливу до атаки шкідника. Сполуки формули (I) переважно використовуються проти комах, акарид або нематод. Термін "рослина", як він використовується тут, включає саджанці, кущі та дерева. Під "сільськогосподарськими культурами" слід розуміти також культури, які були зроблені стійкими до гербіцидів або класів гербіцидів (наприклад, ALS-, GS-, EPSPS-, PPO- та HPPDінгібітори) за допомогою методів селекції або за допомогою генної інженерії. Прикладом сільськогосподарської культури, яку було зроблено стійкою до імідазолінонів, наприклад імазамоксу, за допомогою традиційних методів селекції, є суріпиця (канола) Clearfield®. Прикладами сільськогосподарських культур, які було зроблено стійкими до гербіцидів за допомогою методів генної інженерії є, наприклад, стійкі до гліфосату та глуфосинату різновиди кукурудзи, доступні в продажі під торговими назвами RoundupReady® та LibertyLink®. Під "сільськогосподарськими культурами" також слід розуміти культури, які були зроблені стійкими до комах-шкідників за допомогою методів генної інженерії, наприклад Bt-кукурудза (стійка до кукурудзяного метелика), Bt-бавовна (стійка до бавовняного довгоносика), а також Btкартопля (стійка до колорадського жука). Прикладами Bt-кукурудзи є гібриди кукурудзи Bt 176 від NK® (Syngenta Seeds). Прикладами трансгенних рослин, що містять один або більше генів, які визначають стійкість до інсектицидів і відсіч атаки одного або більше токсинів, є KnockOut® (кукурудза), Yield Gard® (кукурудза), NuCOTIN33B® (бавовна), Bollgard® (бавовна), NewLeaf® (картопля), NatureGard® та Protexcta®. Посіви цих рослин або їх насіннєвий матеріал можуть бути стійкими до гербіцидів і в той же час стійкими до поїдання комахами ("складені" трансгенні явища). Наприклад насінина може мати здатність продукувати інсектицидний білок Cry3 і в той же час бути стійкою до гліфозату. Під "сільськогосподарськими культурами" також слід розуміти культури, отримані за допомогою традиційних методів селекції або генної інженерії, які містять так звані вихідні властивості (output traits) (наприклад, покращена стійкість до зберігання, вища поживна цінність та покращений смак). Для обробки шкідника, місцезнаходження шкідника або рослини, чутливої до атаки шкідника, сполукою формули (I) у якості інсектициду, акарициду, нематоциду або молюскоциду зі сполуки формули (I) зазвичай утворюють композицію, у яку окрім сполуки формули (I) входять придатний розріджувач або носій та, як варіант, поверхнево-активна речовина (ПАР). ПАР - це хімічні речовини, здатні змінити характеристики граничного шару (наприклад, рідкий/твердий, рідкий/газоподібний або рідкий/рідкий граничний шар) шляхом зниження поверхневого натягу, тим самим приводячи до змін інших характеристик (наприклад, розсіювання, емульгування та змочування). Бажано, щоб усі композиції (як тверді, так і рідкі препаративні форми) складали за вагою від 0,0001 % до 95 %, ще краще від 1 % до 85 %, наприклад від 5 % до 60 %, сполуки формули (I). Композиція зазвичай використовується для боротьби зі шкідниками таким чином, щоб сполука формули (I) використовувалася у нормі від 0,1 г до 10 кг на гектар, краще - від 1 г до 6 кг на гектар, ще краще - від 1 г до 1 кг на гектар. При застосуванні сполуки формули (I) для протравлювання насіння норма її внесення складає від 0,0001 г до 10 г (наприклад, 0,001 г або 0,05 г), краще - від 0,005 г до 10 г, ще краще - від 0,005 г до 4 г на кілограм насіння. В іншому варіанті цей винахід пропонує інсектицидну, акарицидну, нематоцидну або молюскоцидну композицію, яка містить ефективну кількість сполуки формули (I) для боротьби зі шкідниками-комахами, акаридами, нематодами або молюсками, та придатний для неї носій або розріджувач. Переважно композиція є інсектицидною, акарицидною, нематоцидною або молюскоцидною. У ще одному варіанті цей винахід пропонує метод боротьби зі шкідниками в осередку їх скупчення, який полягає в обробці шкідників або осередку їх скупчення ефективною для боротьби з комахами, акаридами, нематодами чи молюсками кількістю композиції, що містить сполуку формули (I). Сполуки формули (I) переважно використовуються проти комах, акарид 7 UA 103540 C2 5 10 15 20 25 30 35 40 45 50 55 60 або нематод. Композиції можна вибирати з декількох типів препаративних форм, включаючи пилоподібні порошки (ПП), водорозчинні порошки (ВП), водорозчинні гранули (РГ), гранули, що диспергуються у воді (ВГ), порошки, що змочуються (ВП), гранули (ГР) (повільного або швидкого вивільнення), розчинні концентрати (РК), рідини, що змішуються з маслом (МР), рідини для ультрамалооб'ємного внесення (УР), концентрати, що емульгуються (КЕ), концентрати, що диспергуються (КД), емульсії (як типу "масло (олія) у воді" (ЕВ), так і типу "вода у маслі (олії)» (ЕМ)), мікроемульсії (МЕ), концентрати суспензій (КС), аерозолі, препаративні форми для утворення туману/диму, капсульні суспензії (СК) і препаративні форми для обробки насінин. Вибрана препаративна форма у будь-якому окремому випадку буде залежати від конкретної поставленої мети та фізичних, хімічних і біологічних характеристик сполуки формули (I). Пилоподібні порошки (ПП) можна приготувати шляхом змішування сполуки формули (I) з одним або більше твердих розріджувачів (наприклад, природні глини, каолін, пірофіліт, бентоніт, глинозем, монтморилоніт, діатоміт, крейда, діатомова земля, фосфати кальцію, карбонати кальцію й магнію, сірка, вапняк, тонкі порошки, тальк та інші органічні та неорганічні тверді носії) та механічного розтирання суміші до отримання тонкоподрібненого порошку. Водорозчинні порошки (ВП) можна приготувати шляхом змішування сполуки формули (I) з однією або більше водорозчинних неорганічних солей (таких як гідрокарбонат натрію, карбонат натрію або сульфат магнію) або однієї чи більше водорозчинних органічних порід (таких як полісахарид) та, як варіант, одним або більше змочуючих агентів, одним або більше диспергуючих агентів чи сумішшю згаданих агентів для покращення ступеню дисперсності/розчинності у воді. Далі суміш розтирають до отримання тонкоподрібненого порошку. Аналогічні композиції також можна гранулювати для отримання водорозчинних гранул (РГ). Порошки, що змочуються (ЗП), можна приготувати шляхом змішування сполуки формули (I) з одним або більше твердих розріджувачів чи носіїв, одним або більше змочуючих агентів та, краще, одним або більше диспергуючих агентів і, як варіант, одним або більше суспендуючих агентів для полегшення диспергування у рідинах. Далі суміш розтирають до отримання тонкоподрібненого порошку. Аналогічні композиції також можна гранулювати для отримання гранул, що диспергуються у воді (ВГ). Гранули (ГР) можна отримати або шляхом гранулювання суміші сполуки формули (I) та одного або більше порошкоподібних твердих розріджувачів або носіїв, або з попередньо утворених пустих гранул шляхом абсорбування сполуки формули (I) (або її розчину у придатному агенті) у пористому гранульованому матеріалі (такому як пемза, атапульгітова глина, фулерова земля, діатоміт, діатомова земля або перемолоті серцевини качанів кукурудзи) або шляхом абсорбування сполуки формули (I) (або її розчину у придатному агенті) у твердому заповнювачі (такому як піски, силікати, природні карбонати, сульфати або фосфати) та висушування за необхідності. Для сприяння абсорбуванню або адсорбуванню речовини широко використовуються такі агенти, як розчинники (такі як аліфатичні й ароматичні нафтові розчинники, спирти, ефіри, кетони та складні ефіри) й липкі речовини (такі як полівініл ацетати, полівінілові спирти, декстрини, види цукру і рослинні олії). В гранули також можуть бути включені одна або більше інших добавок (наприклад, емульгуючий агент, змочуючий агент або диспергуючий агент). Концентрати, що диспергуються (КД), можна приготувати шляхом розчинення сполуки формули (I) у воді або органічному розчиннику, такому як кетон, спирт або ефір гліколю. Ці розчини можуть містити поверхнево-активні речовини (наприклад, для покращення розчинення у воді або запобігання кристалізації у розпилювачі). Концентрати, що емульгуються (КЕ), або емульсії масло (олія) у воді (ЕВ) можна приготувати шляхом розчинення сполуки формули (I) в органічному розчиннику (що, як варіант, містить один або більше змочуючих агентів, один або більше емульгуючих агентів або суміш згаданих агентів). Придатні до використання у КЕ органічні розчинники включають ароматичні вуглеводні (такі як алкілбензоли або алкілнафталіни, представлені торговими марками SOLVESSO 100, SOLVESSO 150 та SOLVESSO 200; SOLVESSO є зареєстрованою торговою маркою), кетони (такі як циклогексанон або метилциклогексанон) і спирти (такі як бензиловий спирт, фурфуриловий спирт або бутанол), N-алкілпіролідони (такі як N-метилпіролідон або Nоктилпіролідон), диметиламіди або жирні кислоти (такі як C 8-C10 диметиламід жирної кислоти) або хлоровані вуглеводні. При додаванні води продукт КЕ може спонтанно емульгуватися для утворення емульсії зі значною стійкістю, щоб забезпечити нанесення аерозолю за допомогою відповідного обладнання. Приготування ЕВ включає отримання сполуки формули (I) або у 8 UA 103540 C2 5 10 15 20 25 30 35 40 45 50 55 60 вигляді рідини (якщо це не рідина кімнатної температури, її можна розтопити при помірній температурі, зазвичай нижче 70 °C), або у розчині (шляхом її розчинення у придатному розчиннику), а потім емульгування отриманої рідини або розчину у воді, яка містить одну або кілька ПАР, в умовах високого градієнта швидкості зсуву, для утворення емульсії. Придатні для застосування в ЕВ розчинники включають рослинні олії, хлоровані вуглеводні (такі як хлорбензоли), ароматичні розчинники (такі як алкілбензоли або алкілнафталіни) та інші належні органічні розчинники з низькою розчинністю у воді. Мікроемульсії (МЕ) можна приготувати шляхом змішування води із сумішшю одного або більше розчинників з одною або більше ПАР для спонтанного утворення препаративної форми термодинамічно стабільної ізотропної рідини. Сполука формули (I) початково присутня або у воді, або в суміші розчинника/ПАР. Придатні для застосування в МЕ розчинники включають розчинники, раніше описані для застосування у КЕ або вЕВ. МЕ може бути системою або типу "масло (олія) у воді", або типу "вода у маслі (олії)» (визначити, яка система присутня, можна шляхом вимірювання електропровідності) і може підходити для змішування водорозчинних або маслорозчинних пестицидів в аналогічній препаративній формі. МЕ підходить для розчинення у воді, залишаючись у вигляді мікроемульсії або утворюючи традиційну емульсію типу "масло (олія) у воді". Концентрати суспензій (КС) можуть бути як водними, так і не водними суспензіями тонкоподрібнених твердих часток сполуки формули (I). КС можна приготувати шляхом розмелу у шаровому млині твердої сполуки формули (I) у придатному середовищі, як варіант, з одним або кількома диспергуючими агентами, для виробництва суспензії тонкоподрібнених часток сполуки. В композицію можуть бути включені один або більше змочуючих агентів, а для зниження швидкості осідання часток можна також включити суспендуючий агент. Як варіант, сполуку формули (I) можна подрібнити у млині сухого подрібнення і додати у воду, що містить раніше описані агенти, для утворення потрібного кінцевого продукту. Аерозольні препаративні форми містять сполуку формули (I) і придатний газ-витіснювач (наприклад, n-бутан). Сполуку формули (I) можна також розчинити або диспергувати у придатній речовині (наприклад, воді або змішуваній з водою рідині, такій як n-пропанол) з метою отримання композицій для застосування у насосах з ручним приводом для обприскування при нормальному тискові. Сполуку формули (I) у сухій формі можна змішувати з піротехнічною сумішшю для утворення композиції, яка підходить для створення у замкнутому просторі диму, який містить сполуку. Капсульні суспензії (СК) можна приготувати у спосіб, аналогічний способу приготування препаративних форм ЕВ, але з додаванням етапу полімеризації для того, щоб отримати водну дисперсію масляних крапель, у якій кожна крапля поміщена у полімерну оболонку і містить сполуку формули (I) і, як варіант, їх носій чи розріджувач. Полімерна оболонка може утворюватися або шляхом реакції міжфазної поліконденсації, або за процедурою утворення комплексу донорно-акцепторного типу. Композиції можуть використовуватися для контрольованого вивільнення сполуки формули (I) та для обробки насінин. Сполуку формули (I) можна також виразити у полімерній матриці, яка біологічно розкладається, для забезпечення повільного контрольованого вивільнення сполуки. Композиція може включати одну або більше добавок для покращення її біологічних характеристик (наприклад, для покращення змочування, утримання або розподілу на поверхнях; стійкості до атмосферних опадів на оброблених поверхнях; або поглинання чи рухливості сполуки формули (I)). Такі добавки включають поверхнево-активні речовини, аерозольні добавки на основі масел (олій), наприклад окремих мінеральних масел або природних рослинних олій (таких як соєва олія і рапсова олія), та їх сумішей з іншими біостимулюючими присадками (інгредієнтами, які можуть сприяти дії сполуки формули (I) або змінювати її). Сполуку формули (I) можна також включити до складу для застосування у якості засобу обробки насіння, наприклад у вигляді порошкової композиції, включаючи порошок для сухої обробки насіння (ПС), водорозчинний порошок (ПР) порошок, що диспергується у воді, для обробки насіння суспензією (ВС), або у вигляді рідкої композиції, включаючи концентрат, що тече (ТН), розчин (РН) або капсульну суспензію (СК). Підготовка композицій ПС, ПР, ВС, ТН та РН дуже подібна до описаної вище підготовки відповідно композицій ПП, ВП, ЗП, КС та КД. У композиції для обробки насіння може бути включено агент для сприяння у прикріпленні композиції до насінини (наприклад, мінеральне масло або плівкоутворюючий захисний матеріал). Змочуючі агенти, диспергуючі агенти та емульгуючі агенти можуть бути поверхнево 9 UA 103540 C2 5 10 15 20 25 30 35 40 45 50 55 60 активними ПАР катіонного, аніонного, амфотерного або неіоногенного типу. Придатні ПАР катіонного типу включають четвертинні сполуки амонію (наприклад, цетилтриметил-амонію бромід), імідазолони та амінні солі. Придатні аніонні ПАР включають солі жирних кислот лужних металів, солі аліфатичних моноефірів сірчаної кислоти (наприклад, лаурилсульфат натрію), солі сульфонованих ароматичних сполук (наприклад, додецилбензолсульфонат натрію, додецилбензолсульфонат кальцію, бутилнафталінсульфонат та суміш ди-ізопропіл та три-ізопропілнафталінсульфонатів натрію), ефір сульфати, алкоголь ефір сульфати (наприклад, лаурет-3-сульфат натрію), ефіркарбоксилати (наприклад, лаурет-3-карбоксилат натрію), фосфатні ефіри (продукти реакції між одним або більше жирних спиртів і метафосфорною кислотою (переважно моноефіри) або фосфорний ангідрид (переважно диефіри), наприклад шляхом реакції між лауриловим спиртом і тетрафосфорною кислотою; на додаток усі ці продукти можуть бути етоксильовані), сульфосукцинамати, парафін або олефін-сульфонати, таурати і лігносульфонати. Придатні ПАР амфотерного типу включають бетаїни, пропіонати та гліцинати. Придатні ПАР неіоногенного типу включають продукти конденсації алкіленоксидів, таких як окис етилену, окис пропілену, окис бутилену та їх суміші з жирними спиртами (такими як олеїловий або цетиловий спирт) або з алкілфенолами (такими як октилфенол, нонілфенол та октилкрезол); ефіри, отримувані з жирних кислот з довгими ланцюгами та безводних гекситів; продукти конденсації вказаних неповних ефірів з оксидом етилену; блок-полімери (що містять окис етилену й окис пропілену); алканоламіди; прості ефіри (наприклад, ефіри жирних кислот поліетиленгліколю); амінооксиди (наприклад, лаурил диметил амін оксид); та лецитини. Придатними суспендуючими агентами є гідрофільні колоїди (такі як полісахариди, полівінілпіролідон або натрієва сіль карбоксіметилцелюлози) і набрякаючі глини (такі як бентоніт або атапульгіт). Сполука формули (I) може наноситися у будь-який відомий спосіб нанесення пестицидних сполук. Наприклад, його можна наносити, з допоміжними речовинами або без них, на шкідників та місцезнаходження шкідників (такі як зона проживання шкідників або рослину, яка зазнала нашестя шкідників) або на будь-яку частину рослини, у тому числі листя, стебла, гілки або корені, чи обробляти насіння перед посадкою, чи вносити в середовище, в якому вони ростуть або в якому будуть вирощуватися (таке як ґрунт навколо коренів, ґрунт загалом, в рисові чеки або в системи гідропоніки) безпосередньо або розприскувати, напилювати, протравлювати шляхом занурення, наносити у вигляді кремоподібної або пастоподібної композиції, наносити у вигляді пари або шляхом розподілу чи додавання композиції (такої як гранульована композиція або композиція, запакована у водорозчинний пакет) у ґрунт або водне середовище. Сполуку формули (I) можна також впорскувати у рослину або розприскувати на рослинність методом електродинамічного розпилення або за допомогою інших економічних способів або наносити за допомогою систем наземного або повітряного зрошування. Композиції для застосування у вигляді водних препаративних форм (водних розчинів або дисперсій) зазвичай постачаються у формі концентратів, що містять діючу речовину у значній пропорції; концентрат перед застосуванням розчиняють водою. Часто необхідно, щоб вказані концентрати, які можуть включати КД, КС, КЕ, ЕВ, МЕ, РГ, ВП, СП, ВГ і КС, добре зберігалися протягом тривалого періоду та мали здатність після такого зберігання розводитися з водою для утворення водних препаратів, які зберігають гомогенність протягом періоду, достатнього для їх нанесення за допомогою звичайного розпилювального обладнання. Такі водні препаративні форми можуть містити різну кількість сполуки формули (I) (наприклад, від 0,0001 % до 10 %, по вазі) залежно від їх цільового призначення. Сполука формули (I) може використовуватися у сумішах з добривами (зокрема, добривами, що містять азот, калій або фосфор). Придатними типами препаративних форм є гранули добрива. Суміші переважно містять до 25 % сполуки формули (I) за вагою. Таким чином, винахід надає композицію добрива, що містить добриво та сполуку формули (I). Композиції за цим винаходом можуть містити інші сполуки, які проявляють біологічну активність, зокрема поживні мікроелементи та сполуки, які проявляють фунгіцидну активність або мають властивості регуляторів росту рослин, гербіцидів, інсектицидів, нематоцидів або акарицидів. Сполука формули (I) може бути єдиною діючою речовиною композиції або, де це необхідно, може примішуватися до однієї або більше додаткових діючих речовин, таких як пестицид, фунгіцид, синергіст, гербіцид або регулятор росту рослин. Додаткова діюча речовина може мати композицію, яка проявляє ширший спектр активності або підвищену стійкість у місцях нанесення; спільно діяти або доповнювати дію (наприклад, шляхом збільшення швидкості 10 UA 103540 C2 5 10 15 20 25 30 35 40 45 50 55 60 впливу або подолання відштовхувальної здатності) сполуки формули (I); або сприяти у подоланні або запобіганні розвитку стійкості до окремих компонентів. Конкретна додаткова діюча речовина буде залежати від цільового використання композиції. Прикладами придатних пестицидів є: а) піретроїди, такі як перметрин, циперметрин, фенвалерат, есфенвалерат, дельтаметрин, цигалотрин (особливо лямбда-циклотрин), біфентрин, фенпропатрин, цифлутрин, тефлутрин, безпечні для риб піретроїди (наприклад етофенпрокс), натуральний піретрин, тетраметрин, sбіоалетрин, фенфлутрин, пралетрин або 5-бензил-3-фурилметил-(E)-(1R, 3S)-2,2-диметил-3-(2оксотіолан-3- іліденметил) циклопропанкарбоксилат; б) органічні фосфати, зокрема профенофос, сульпрофос, ацефат, метилпаратіон, азинфосметил, диметон-s-метил, гептенофос, тіометон, фенамифос, монокротофос, профенофос, триазофос, метамідофос, диметоат, фосфамідон, малатіон, хлорпірифос, фозалон, тербуфос, фенсульфотіон, фонофос, форат, фоксим, піриміфос-метил, піриміфос-етил, фенітротіон, фостіазат або діазинон; в) карбамати (у тому числі арилкарбамати), такі як пірімікарб, триазамат, клоетокарб, карбофуран, фуратіокарб, етнофенкарб, альдикарб, тіофурокс, карбосульфан, бендіокарб, фенобукарб, пропоксур, метоміл або оксаміл); г) бензоїлсечовини, такі як дифлубензурон, трифлумурон, гексафлумурон, флуфеноксурон або хлорфлуазурон; д) оловоорганічні сполуки, такі як цигексатин, фенбутатиноксид або азоциклотин; е) піразоли, такі як тебуфенпірад і фенпіроксимат; є) макроліди, такі як авермектини або мілбеміціни, наприклад абамектин, емамектин, бензоат, івермектин, мілбеміцин чи спіносад, спінеторам або азадірахтін; ж) гормони або феромони; з) хлорорганічні сполуки, такі як ендосульфан, гексахлорбензол, ДДТ, хлордан або диельдрин; и) амідини, такі як хлордимеформ або амітраз; i) фумігантні речовини, такі як хлорпікрин, дихлорпропан, метилбромід або метам; ї) неонікотиноїдні сполуки, такі як імідаклоприд, тіаклоприд, ацетаміприд, клотіанідин, нітенпірам, динотефуран або тіаметоксам; й) диацилгідразини, такі як тебуфенозид, хромафенозид або метоксіфенозид; к) дифенілові ефіри, такі як діофенолан або пірипроксифен; л) індоксакарб; м) хлорфенапір; н) піметрозин або пірифлуквіназон; о) спіротетрамат, спіродиклофен або спіромезифен; п) флубендіамід, хлорантраніліпрол або ціантраніліпрол; р) цієнопірафен чи цифлуметофен; або с) сульфоксафлор. Окрім перерахованих вище основних хімічних класів пестицидів до складу відповідних сумішей можуть входити й інші пестициди, які мають конкретне застосування. Наприклад, при захисті посівів рису можуть застосовуватися селективні інсектициди для конкретних рослин, наприклад інсектициди, специфічні до стеблових пильщиків (зокрема картап) або до стрибаючих комах (зокрема бупрофецин). Як варіант, до складу композицій можуть також входити інсектициди або акарициди, специфічні для контролю певних видів комах/стадій росту комахи (наприклад, акарицидні оволарвіциди, такі як хлофентезин, флубензімін; гексітіазокс або тетрадифон; акарицидні мотиліциди, такі як дикофол або пропаргіт; акарициди, такі як бромопропілат або хлорбензилат; або регулятори росту, такі як гідраметилнон, циромазин, метопрен, хлорфлуазирон або дифлубензурон). Прикладами фунгіцидних сполук, які можуть входити до складу композиції за винаходом, є (E)-N-метил-2-[2-(2,5-диметилфеноксіметил)феніл]-2-метоксі-іміноацетамід (SSF-129), 4-бром-2ціано-N, N-диметил-6-трифторметилбензімідазол-1-сульфонамід, -[N-(3-хлор-2,6-ксиліл)-2метоксіацетамідо]--бутиролактон, 4-хлор-2-ціано-N, N-диметил-5-p-толілімідазол-1сульфонамід (IKF-916, ціамідазосульфамід), 3-5-дихлор-N-(3-хлор-1-етил-1-метил-2оксопропіл)-4-метилбензамід (RH-7281, зоксамід), N-аліл-4,5,-диметил-2-триметилсилілтіофен3- карбоксамід (MON65500), N-(1-ціано-1,2-диметилпропіл)-2-(2,4-дихлорфеноксі)пропіонамід (AC382042), N-(2-метоксі-5-піридил)-циклопропан карбоксамід, ацібензолар (CGA245704), аланікарб, альдіморф, анілазін, азаконазол, азоксістробін, беналаксил, беноміл, білоксазол, бітертанол, бластіцидин С, бромуконазол, бупіримат, каптафол, каптан, карбендазим, хлоргідрат карбендазиму, карбоксин, карпропамід, карвон, CGA41396, CGA41397, хінометіонат, 11 UA 103540 C2 5 10 15 20 25 30 35 40 45 50 55 60 хлороталоніл, хлорозолінат, клозілакон, сполуки, що містять мідь, такі як оксіхлорид міді, оксіхонолят міді, сульфат міді, талат міді та бордоська рідина, цимоксаніл, ципроконазол, ципродиніл, дебакарб, 1,1'-діоксид ди-2-піридилдисульфіду, дихлорфлуанід, дихломезин, дихлоран, диетофенкарб, дифеноконазол, дифензокат, дифлуметорім, O, O-ди-ізо-пропіл-Sбензилтіофосфат, дімефлуазол, діметконазол, діметоморф, диметиримол, диніконазол, динокап, дитіанон, додецил диметил амонію хлорид, додеморф, додин, догуадин, едифенфос, епоксіконазол, етіримол, етил-(Z)-N-бензил-N-([метил(мeтил-тіoетилідeнaмінooкcікapбoніл)aмінo] тіо)-β-аланат, етридіазол, фамоксадон, фенамідон (RPA407213), фенрімол, фенбуконазол, фенфурам, фенгексамід (KBR2738), фенпіклоніл, фенпропідин, фенпропіморф, ацетат фентіну, гідроксид фентіну, фербам, ферімзон, флуазінам, флудіоксоніл, флуметовер, флуоримід, флуквінконазол, флузилазол, флутоланіл, флутріафол, фолпет, фуберидазол, фуралаксіл, фураметпір, гуазатин, гексаконазол, гідроксіізоксазол, гімексазол, імазаліл, імібенконазол, іміноктадин, іміноктадин триацетат, іпконазол, іпробенфос, іпродіон, іпровалікарб (SZX0722), ізопропанілбутилкарбамат, ізопротіолан, касугаміцин, крезоксим-метил, LY186054, LY211795, LY248908, манкозерб, манеб, мефеноксам, мепаніпірим, мепроніл, металаксил, метконазол, метирам, метирам-цинк, метоміностробін, міклобутаніл, неоазозін, диметилтіокарбамат нікелю, нітротал-ізо-пропіл, нуаримол, офурейс, ртутьорганічні сполуки, оксадиксил, оксасульфурон, оксолінова кислота, окспоконазол, оксікарбоксин, пефуразоат, пенконазол, пенцикурон, оксид феназину, фосетіл-алюміній, фосфорні кислоти, фталід, пікоксістробін (ZA1963), поліоксін D, полірам, пробеназол, прохлораз, процимідон, пропамокарб, пропіконазол, пропінеб, пропіонова кислота, піразофос, пірефенокс, піриметаніл, пірохілон, піроксіфур, піролнітрин, четвертинні амонієві сполуки, хінометіонат, квіноксіфен, квінтозен, сіпконазол (F-155), пентахлорфенат натрію, спіроксамін, стрептоміцин, сірка, тебуконазол, техлофталам, техназен, тетраконазол, тіабеназол, тіфлузамід, 2-(тіоціанометилтіо)бензотіазол, тіофанат-метил, тірам, тімібенконазол, толхлофос-метил, толілфлуанід, триадимефон, триазбутил, триазоксид, трициклазол, тридеморф, трифлоксістробін (CGA279202),трифорін, трифлумізол, тритіконазол, валідаміцин А, вапам, вінклозолін, зінеб та зірам. Сполуки формули (I) можна змішувати з ґрунтом, торфом та іншим кореневим середовищем для захисту рослин від грибкових захворювань, які вражають насіння, ґрунт або листя. Приклади придатних синергістів для застосування у композиціях включають бутоксид піпероніла, сезамекс, сафроксан та додецилімідазол. Придатні гербіциди і регулятори росту рослин для включення в композиції будуть залежати від цільового призначення та бажаного ефекту. Прикладом гербіциду, селективного до рису, який можна включити, є пропаніл. Прикладом регулятора росту рослин для застосування на бавовні є PIX . Деякі суміші можуть містити діючі речовини з суттєво відмінними фізичними, хімічними або біологічними характеристиками, завдяки яким їх нелегко використовувати в однаковому традиційному типі препаративної форми. За таких обставин можна приготувати інші типи препаративних форм. Наприклад, у випадку якщо одна діюча речовина є водорозчинним твердим тілом, а інша - нерозчинною у воді рідиною, все ж є можливість диспергувати кожну діючу речовину у аналогічній постійній водяній фазі шляхом диспергування твердої діючої речовини у вигляді суспензії (шляхом приготування, аналогічним приготуванню КС), в той же час диспергуючи рідку діючу речовину у вигляді емульсії (шляхом приготування, аналогічним приготуванню ЕВ). Отримана композиція є препаративною формою суспоемульсії (СЕ). Цей винахід ілюструється наведеними нижче прикладами. РХМС. Спектральні характеристики були отриманi за допомогою мас-спектрометра ZMD (виробництва компанії Micromass, Манчестер, Велика Британія) або ZQ (виробництва компанії Waters, Мілфорд, Массачусетс, США), обладнаного джерелом електророзпилення (ESI (іонізація розпиленням у електричному полі); температура джерела становить від 80 °C до 100 °C; температура десольвації - від 200 °C до 250 °C; різниця потенціалів на конусі - 30 В; швидкість потоку газу на конусі - 50 л/год., швидкість потоку газу для десольвації - від 400 до 600 л/год., діапазон маси - від 150 до 1000 а.о.м. (Da)) та колони 1100 HPLC виробництва Agilent: Gemini C18, розмір часток 3 мкм, 110 ангстрем, 30 × 3 мм (виробництва компанії Phenomenex, Торранс, Каліфорнія, США); температура колони - 60 °C; швидкість потоку 1,7 мл/хв; елюент A: H2O/HCOOH 100:0,05; елюент B: MeCN/MeOH/HCOOH 80:20:0,04; градієнт: 0 хв 5 % B; 2-2,8 хв 100 % B; 2,9-3 хв 5 % B; УФ-детектування: 200-500 нм, роздільна здатність 2 нм. Перед проведенням МС-аналізу потік розділяли після виходу з колони. RT означає тривалість відстоювання. Приклад 1 Цей приклад ілюструє отримання 2-хлор-N-(2-{1-[4-(5-хлор-піримідин-2-іл)-бензил] 12 UA 103540 C2 піперидин-4-іл}-4-трифторметилфеніл)-ізонікотинаміду (сполука A1 з таблиці A): N N F3C N NH Cl Cl O N 5 10 15 20 25 30 35 40 45 50 Етап A. Реактор ємністю 4,5 л наповнювали 2-бром-4-трифторметиланіліном (100 г), третбутиловим ефіром 4-(4,4,5,5-тетраметил-[1,3,2]діоксаборолан-2-іл)-3,6-дигідро-2H-піридин-1карбонової кислоти (124 г, отриманий згідно з описом у публікації WO 2006/003494) і 1,4діоксаном (2500 мл), після чого розчин дегазували аргоном протягом 30 хвилин. Додавали дихлор-біс(трифенілфосфін)паладій (5,6 г), і отриманий розчин перемішували протягом 30 хвилин за кімнатної температури в атмосфері аргону. Додавали дегазований розчин карбонату натрію (127 г) у воді (1200 мл), і суміш перемішували за температури 60 °C протягом 3 годин. Суміш охолоджували до кімнатної температури та екстрагували етилацетатом (3 × 300 мл). Об'єднані органічні шари промивали водою (3 × 400 мл) і розсолом, потім висушували над сульфатом натрію та випарювали під вакуумом. Залишок розчиняли у гептані (200 мл) й охолоджували до -70 °C, після чого залишали нагріватися до 0 °C. Тверду речовину збирали шляхом фільтрації та промивали холодним гептаном для отримання трет-бутилового ефіру 4(2-аміно-5-трифторметилфеніл)-піперидин-1-карбонової кислоти (128 г) у вигляді твердої речовини коричневого кольору. MS (ES+) 214/215; 243/244 (MH+-BOC); 287/288; 343 (MH+); 1H ЯМР (400 МГц, CDCl3) 1,5 (s, 9H), 2,4 (m, 2H), 3,65 (t, 2H), 4,05 (m, 2H), 5,8 (m, 1H), 6,7 (d, 1H), 7,2 (d, 1H), 7,3 (dd, 1H). Етап В. Отриману на етапі A сполуку (152 г) розчиняли в етанолі (2100 мл), і після дегазування додавали паладій на активованому вугіллі (10 % за вагою) (100 мг). Реакційну суміш перемішували за кімнатної температури в атмосфері водню протягом 30 годин. Фільтрація на Celite® давала темну тверду речовину, яку розчиняли у діетиловому ефірі (1000 мл). Фільтрація над Hyflo® та випарювання розчинника давали залишок жовтого кольору, який виділяли з петролейного ефіру (1000мл) для отримання трет-бутилового ефіру 4-(2-аміно5-трифторметилфеніл)-піперидин-1-карбонової кислоти (125 г) у вигляді твердої речовини білого кольору. M.p. 120 °C. MS (ES+) 330/331 (MH+-ізобутен+CH3CN); 1H ЯМР (400 МГц, CDCl3) 1,5 (s, 9H), 1,6 (m, 2H), 1,85 (m, 2H), 2,6 (m, 1H), 2,8 (m, 2H), 3,95 (br s, 2H), 4,3 8m, 2H), 6,7 (d, 1H), 7,3 (d, 2H). Етап C. До суспензії 2-хлор-ізонікотинової кислоти (56 г) у толуолі (1500 мл) та N, Nдиметилформаміду (0,5 мл) в атмосфері азоту за кімнатної температури по краплі додавали тіонілхлорид (81 мл), і суміш перемішували за температури 60 °C до розчинення всіх твердих речовин (3 години). Розчин випарювали під вакуумом, і залишок розчиняли в тетрагідрофурані (300 мл). Цей розчин по краплі додавали до розчину отриманого на етапі B продукту (103 г) в тетрагідрофурані (3000 мл) і N, N-діізопропілетиламіні (155 мл) за кімнатної температури. Реакційну суміш перемішували протягом 3 годин за кімнатної температури, гасили додаванням насиченого водного розчину бікарбонату натрію (1000 мл) і екстрагували етилацетатом (3 × 500 мл). Об'єднані органічні екстракти промивали водою (3 × 500 мл), потім розсолом (200 мл), висушували над сульфатом натрію та випарювали під вакуумом. Залишок розтирали з діетиловим ефіром, тверду речовину відділяли шляхом фільтрації та висушували під високим вакуумом для отримання трет-бутилового ефіру 4-{2-[(2-хлор-піридин-4-карбоніл)-аміно]-5трифторметил-феніл}-піперидин-1-карбонової кислоти (143 г) у вигляді порошку білого кольору. + + + MS (ES+) 384/386 (MH -BOC), 428/430 (MH -ізобутен), 484 / 486 (MH ); 1H ЯМР (400 МГц, CDCl3) 1,5 (s, 9H), 1,7 (m, 2H), 1,85 (m, 2H), 2,8 (m, 3H), 4,3 (m, 2H), 7,6 (m, 2H), 7,65 (d, 1H), 7,70 (d, 1H), 7,80 (s, 1H), 8,0 (s, 1H), 8,6 (d, 1H). Етап D. Розчин отриманого на етапі C продукту (140 г) у дихлорметані (1500 мл) обробляли трифтороцтовою кислотою (220 мл), і реакційну суміш перемішували за кімнатної температури в атмосфері азоту протягом 1 години. Потім реакційну суміш випарювали під вакуумом до утворення залишку, який виділяли з діетилового ефіру для отримання 2-хлор-N-(2-піперидин-4іл-4-трифторметил-феніл)-ізонікотинаміду у вигляді його трифторацетатної солі (тверда речовина білого кольору, 144 г). M.p. 248 °C. MS (ES+) 384/386 (MH+). Вільну основу отримували спочатку шляхом нейтралізації водним розчином гідроксиду натрію (1N) до pH 9, а 13 UA 103540 C2 5 10 15 потім екстрагуванням етилацетатом. Після видалення розчинника отримували тверду речовину жовтого кольору. M.p. 166 °C. Етап E. Отриманий на етапі D продукт (вільна основа, 38 г) змішували з 4-(5-хлор-піримідин2-іл)-бензальдегідом (препарат 1, 22 г) та розчиняли у тетрагідрофурані (500 мл). Розчин перемішували в атмосфері аргону й обробляли ціаноборгідридом натрію (33 г). Отриману суміш перемішували протягом 16 годин за кімнатної температури, гасили додаванням води, і суміш екстрагували етилацетатом. Органічний шар висушували над сульфатом натрію та випарювали під вакуумом для отримання ацетату 2-хлор-N-(2-{1-[4-(5-хлор-піримідин-2-іл)-бензил]піперидин-4-іл}-4-трифторметилфеніл)-ізонікотинаміду (сполука E1 з таблиці E) у вигляді твердої речовини бежевого кольору. Цю сіль розчиняли в етилацетаті, потім нейтралізували водним розчином гідроксиду натрію (2N) та промивали водою й розсолом. Об'єднані органічні шари висушували над сульфатом натрію, розчинник видаляли при зниженому тиску для отримання вказаної у заголовку сполуки у вигляді твердої речовини білого кольору. M.p. 202+ 203 °C. MS (ES+) 586/588 (MH ); 1H ЯМР (400 МГц, DMSO) 1,7 (m, 4H), 2,0 (m, 2H), 2,9 (m, 3H), 3,3 (s, 2H), 7,45 (d, 2H), 7,55 (d, 1H), 7,60 (d, 1H), 7,70 (s, 1H), 7,90 (d, 1H), 8,0 (s, 1H), 8,3 (d, 2H), 8,65 (d, 1H), 9,0 (s, 2H). Приклад 2 Цей приклад ілюструє отримання 2-хлор-N-(2-{1-[4-(5-фтор-піримідин-2-іл)-бензил]піперидин-4-іл}-4-трифторметилфеніл)-ізонікотинаміду (сполука A2 з таблиці A): N N F3C N NH F Cl O N 20 25 Вказану в заголовку сполуку отримували за процедурою, аналогічною описаним у прикладі 1, з використанням 4-(5-фтор-піримідин-2-іл)-бензальдегіду (препарат 2) на етапі E. M.p. 8990 °C. Так само виділяли сіль оцтової кислоти (сполука E2 з таблиці E). Приклад 3 Цей приклад ілюструє отримання 2-хлор-N-(2-{1-[4-(5-хлор-піримідин-2-іл)-бензил]піперидин-4-іл}-4-фторфеніл)-ізонікотинаміду (сполука A10 з таблиці A): N N F N NH Cl Cl O N 30 35 Суміш 2-хлор-N-(4-фтор-2-піперидин-4-іл-феніл)-ізонікотинаміду (333 мг) (отриманого за процедурами, аналогічними описаним у публікації WO 2006/003494) обробляли 4-(5-хлорпіримідин-2-іл)-бензальдегідом (препарат 1, 218 мг) і ціаноборгідридом натрію (316 мг) в тетрагідрофурані (50 мл) згідно з описом у прикладі 1, етап E, для отримання вказаної у заголовку сполуки (200 мг) у вигляді твердої речовини білого кольору. M.p. 176 °C. MS (ES+) 536/538 (MH+), 308/309 (M-ізопрен); 1H ЯМР (400 МГц, MeOD) 1,7(m, 4H), 2,1 (m, 2H), 2,8 (m, 1H), 3,1 (m, 2H), 3,6 (s, 2H), 7,0 (dt, 1H), 7,15 (dd, 1H), 7,30 (dd, 1H), 7,5 (d, 2H), 7,8 (d, 1H), 7,9 (s, 1H), 8,4 (d, 2H), 8,6 (d, 1H), 8,8 (s, 2H). Приклад 4 Цей приклад ілюструє отримання 2-хлор-N-(2-{1-[4-(5-хлор-піримідин-2-іл)-бензил]піперидин-4-іл}-5-трифторметоксіфеніл)-ізонікотинаміду (сполука A12 з таблиці A): 14 UA 103540 C2 N N N NH O CF3 Cl Cl O N 5 10 15 Вказану в заголовку сполуку готували згідно з процедурою, аналогічною описаним у прикладі 1, починаючи з 2-бром-5-трифторметоксі-аніліну, отримуваного наступним чином: Розчин 3-трифторметоксі-аніліну (1,77 г) у толуолі (20 мл) обробляли N-бромсукцинімідом (1,87 г) за кімнатної температури, реакційну суміш перемішували протягом 2 годин за кімнатної температури, гасили шляхом додавання води, і суміш екстрагували етилацетатом (3 × 50 мл). Об'єднані органічні екстракти промивали насиченим водним розчином бікарбонату натрію, висушували над сульфатом натрію та випарювали під вакуумом. Залишок очищували за допомогою хроматографії на силікагелі (елюент: циклогексан/етилацетат 95:5) для отримання 4-бром-3-трифторметоксі-аніліну (270 мг) і 2-бром-5-трифторметоксі-аніліну (1,45 г), які були охарактеризовані за допомогою мас-спектрів та спектрів ЯМР. 4-бром-3-трифторметоксі-анілін: MS (ES+) 256/258 (MH+); 1H ЯМР (400 МГц, CDCl3) 3,5 (brs, 2H), 6,5 (d, 1H), 6,7 (s, 1H), 7,3 (d, 1H). 2-бром-5-трифторметоксі-анілін: MS (ES+) 256/258 (MH+); 1H ЯМР (400 МГц, CDCl3) 4,2 (brs, 2H), 6,5 (d, 1H), 6,6 (s, 1H), 7,4 (d, 1H). Наведені нижче сполуки були отримані за процедурами, аналогічними описаним у прикладах 1-4: Таблиця A Сполуки формули (Ia) 2 R N 3 R N 4 R (Ia) N NH 8 R 5 R № сполук и A1 A2 A3 A4 A5 A6 A7 A8 R 1 2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-5-фторпірид-4-ил2,6-дихлорпірид-4-ил2,5-дихлорпірид-4-ил2-фтор-пірид4-ил2-хлор-пірид-4ил2-хлор-пірид-4ил R 2 1 R O R 3 R 4 R 5 R 8 H -CF3 H H Cl H -CF3 H H F H -CF3 H H H -CF3 H H -CF3 H M.p. ВЕРХ (RT) 202-203 °C 1,37 хв 586/588 1,29 хв 570/572 Cl 156-158 °C 1,38 хв 604/606 H Cl 169-170 °C 1,47 хв 620/622 H H Cl 147-148 °C 1,43 хв 620/622 -CF3 H H Cl 199-200 °C 1,35 хв 570/572 H -CF3 H H H 1,27 хв 552/554 H -CF3 F H Cl 200-205 °C 1,43 хв 604/606 15 89-90 °C МС (ES+) UA 103540 C2 Таблиця A Сполуки формули (Ia) 2 R N 3 R N 4 R (Ia) N NH 8 R 5 R № сполук и A9 A10 A11 A12 A13 A14 A15 A16 A17 A18 A19 A20 A21 A22 A23 A24 A25 A26 A27 A28 A29 R 1 2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-метоксіпірид-4-ил2-метоксіпірид-4-ил2-фтор-пірид4-ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2,6-дихлорпірид-4-ил2,5-дихлорпірид-4-ил2-хлор-5-фторпірид-4-ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2,5-дифторпірид-4-ил R 2 1 R O R 3 R 4 R 5 R 8 F F H H Cl H F H H Cl F -CF3 H H H H -OCF3 H CF3 H M.p. ВЕРХ (RT) 100-105 °C 1,30 хв 554/556 1,27 хв 536/538 Cl 105-110 °C 1,41 хв 604/606 H Cl 211-212 °C 1,39 хв 602/604 H H Cl 199-200 °C 1,42 хв 582/584 CF3 F H Cl 205-208 °C 1,41 хв 600/602 H CF3 F H Cl 173-176 °C 1,24 хв 588/590 H CF3 H H CF3 206-206 °C 1,42 хв 620/622 H CF3 H H циклопропіл 1,32 хв 592/594 H CF3 H H Br 199-199 °C 1,36 хв 630/632 CF3 H H H Cl 168-168 °C 1,33 хв 586/588 H CF3 H H CN 200-200 °C 1,29 хв 577/579 H CF3 H H етиніл 188-188 °C 1,31 хв 576/578 H CF3 H H CH3 1,26 хв 566/568 H CF3 F H Cl 198-202 °C 1,48 хв 638/640 H CF3 F H Cl 178-181 °C 1,44 хв 638/640 H CF3 F H Cl 192-194 °C 1,44 хв 622/624 H H CF3 H Cl 1,36 хв 586/588 H O-CF3 H H Cl 1,39 хв 602/604 H F F F Cl 205-207 °C 1,34 хв 572/574 H CF3 H H Cl 182-183 °C 1,33 хв 588/590 16 176 °C МС (ES+) UA 103540 C2 Таблиця A Сполуки формули (Ia) 2 R N 3 R N 4 R (Ia) N NH 8 R 5 R № сполук и A30 A31 A32 A33 A34 A35 A36 A37 A38 A39 A40 A41 A42 A43 A44 A45 A46 A47 A48 A49 A50 R 1 R 1 R O 2 2,6-дихлорF пірид-4-ил2-фтор-піридF 4-ил2-хлор-5-фторF пірид-4-ил2-метоксіF пірид-4-ил2,5-дихлорF пірид-4-ил2-хлор-пірид-4F ил2-хлор-пірид-4H ил2-хлор-пірид-4O-CF3 ил2-хлор-5-фторH пірид-4-ил2-хлор-5-фторH пірид-4-ил2-хлор-5-фторH пірид-4-ил2-хлор-5-фторH пірид-4-ил2-хлор-5-фторF пірид-4-ил2-хлор-5-фторF пірид-4-ил2,5-дихлорH пірид-4-ил2,5-дихлорH пірид-4-ил2,5-дихлорF пірид-4-ил2,5-дихлорH пірид-4-ил2,5-дихлорF пірид-4-ил2,5-дихлорH пірид-4-ил2,5-дифторH пірид-4-ил 5 R 4 R Cl H H Cl 121-125 °C 1,42 хв 604/606 Cl H H Cl 136-180 °C 1,28 хв 554/556 Cl H H Cl 124-126 °C 1,33 хв 588/590 Cl H H Cl 208-212 °C 1,30 хв 566/568 Cl H H Cl 188-191 °C Cl H H Cl 119-123 °C F F H Cl 1,27 хв 554/556 H H H Cl 74-74 °C 1,38 хв 602/604 CF3 F H F 195-198 °C 1,38 хв 606/608 F Cl H Cl 208-212 °C 1,38 хв 588/590 F Cl H F 191-194 °C 1,31 хв 572/574 CF3 H H F 128-130 °C 1,30 хв 588/590 CF3 H H F CF3 H H F Cl CF3 R 8 ВЕРХ (RT) 3 R M.p. 71-74 °C МС (ES+) 1,39 хв 606/608 Cl 128-132 °C 1,42 хв 622/624 H F 197-199 °C 1,34 хв 588/590 F H F 198-200 °C 1,42 хв 622/624 CF3 H H F F Cl H CF3 H CF3 F 1,39 хв 622/624 Cl 179-200 °C 1,41 хв 604/606 H Cl 98-103 °C 1,43 хв 638/640 H H F 179-183 °C 1,33 хв 604/606 Cl H F 177-178 °C 1,29 хв 556/558 17 74-76 °C UA 103540 C2 Таблиця A Сполуки формули (Ia) 2 R N 3 R N 4 R (Ia) N NH 8 R 5 R № сполук и A51 A52 A53 A54 A55 A56 A57 A58 A59 A60 5 R 1 2,5-дифторпірид-4-ил2,5-дифторпірид-4-ил2,5-дифторпірид-4-ил2,5-дифторпірид-4-ил2,5-дифторпірид-4-ил2,5-дифторпірид-4-ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил 1 R O 2 R H 3 R F Cl H Cl 188-189 °C 1,33 хв 572/574 H CF3 F H F 178-179 °C 1,35 хв 590 H CF3 F H Cl 181-182 °C 1,41 хв 606/608 F CF3 H H F 144-145 °C 1,32 хв 590 F CF3 H H Cl 151-152 °C 1,38 хв 606/608 H CF3 H H F 193-194 °C 1,29 хв 572 H F Cl H F 176-177 °C 1,28 хв 554/556 H F Cl H Cl 189-190 °C 1,33 хв 570/572 H CF3 F H F 163-166 °C 1,35 хв 588/590 F CF3 H H F R 5 R 8 ВЕРХ (RT) 4 R M.p. 94-96 °C 1,33 хв МС (ES+) 588/590 Приклад 5 Цей приклад ілюструє отримання 2-хлор-N-{1'-[4-(5-хлор-піримідин-2-іл)-бензил]-6трифторметил-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл}-ізонікотинаміду (сполука B1 з таблиці B): N F3C N N N NH Cl Cl O N 10 Етап A. Розчин 3-аміно-2-хлор-6-трифторметил-піридину (0,890 г), трет-бутилового ефіру 4(4,4,5,5-тетраметил-[1,3,2]діоксаборолан-2-іл)-3,6-дигідро-2H-піридин-1-карбонової кислоти (1,4 г) (отриманого згідно з описом у публікації WO 2006/003494) і тетракіс(трифенілфосфін)паладію (0,200 г) у 1,2-диметоксіетані (45 мл) обробляли водним розчином фосфату калію (1,1 M) (1,92 г). Реакційну суміш перемішували за температури 80 °C протягом 3 годин. Шляхом екстракції водним розчином з етилацетатом отримували осад, який очищали за допомогою хроматографії на силікагелі (елюент: гексан/етилацетат 1:1) для отримання трет-бутилового ефіру 3-аміно-6-трифторметил-3',6'-дигідро-2'H-[2,4']біпіридиніл-1' 18 UA 103540 C2 5 10 15 20 25 30 35 40 45 карбонової кислоти (1,5 г) у вигляді твердої речовини білого кольору. MS (ES+) 288 (M-ізопрен); 1H ЯМР (400 МГц, CDCl3) 1,50 (s, 9H), 2,61 (m, 2H), 3,67 (t, 2H), 4,10 (m, 2H), 4,21 (s, 2H), 6,11 (s, 1H), 7,03 (d, 1H), 7,33 (d, 1H). Етап В. Отриманий на етапі A продукт (1 г) розчиняли в етанолі (40 мл), і після дегазування додавали паладій на активованому вугіллі (10 % за вагою) (100 мг). Реакційну суміш перемішували за кімнатної температури в атмосфері водню протягом 2 днів. Фільтрація на Celite® давала трет-бутиловий ефір 3-аміно-6-трифторметил-3',4',5',6'-тетрагідро-2'H[2,4']біпіридиніл-1'-карбонової кислоти (1 г) у вигляді твердої речовини білого кольору. MS (ES+) 290/292 (M-ізопрен); 1H ЯМР (400 МГц, CDCl3) 1,48(s, 9H), 1,85 (m, 4H), 2,77 (m, 1H), 2,88 (m, 2H), 3,97 (s, 2H), 4,24 (m, 2H), 6,97 (d, 1H), 7,32 (d, 1H). Етап C. Розчин отриманого на етапі C продукту (1 г) у толуолі (40 мл) обробляли N, Nдіізопропілетиламіном (1,05 мл), а потім 2-хлор-ізонікотиноїл хлоридом. 2-хлор-ізонікотиноїл хлорид отримували з 2-хлорізонікотинової кислоти (0,496 г) та оксалілхлориду (0,346 мл) у дихлорметані (40 мл). Реакційну суміш перемішували за кімнатної температури протягом 2 годин, виливали у насичений водний розчин бікарбонату натрію, екстрагували етилацетатом, промивали водою, висушували над сульфатом натрію, а потім випарювали під вакуумом. Залишок очищували за допомогою хроматографії на силікагелі (елюент: гексан/етилацетат 1:1) для отримання трет-бутилового ефіру 3-[(2-хлор-піридин-4-карбоніл)-аміно]-6-трифторметил3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (1,1 г). MS (ES+) 485/487 (MH+), 429/431 (M-ізопрен); 1H ЯМР (400 МГц, CDCl3) 1,47 (s, 9H), 1,79 (m, 2H), 1,96 (m, 2H), 2,88 (m, 2H), 2,95 (m, 1H), 4,25 (m, 2H), 7,61 (d, 1H), 7,66 (m, 1H), 7,79 (s, 1H), 8,05 (s, 1H), 8,32 (d, 1H), 8,64 (d, 1H). Етап D. Розчин отриманої на етапі C сполуки (300 г) у дихлорметані (15 мл) обробляли трифтороцтовою кислотою (1,2 мл) за кімнатної температури протягом 1 години. Шляхом випарювання розчинника та висушування твердої речовини під високим вакуумом отримували трифторацетат 2-хлор-N-(6-трифторметил-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл)ізонікотинаміду. Вільну основу отримували шляхом розподілу між етилацетатом і насиченим водним розчином бікарбонату натрію. Етап E. Отриманий на етапі D продукт (вільна основа, 288 мг) змішували з 4-(5-хлорпіримідин-2-іл)-бензальдегідом (препарат 1, 165 мг) і розчиняли у тетрагідрофурані (20 мл). Розчин перемішували в атмосфері аргону й обробляли ціаноборгідридом натрію (475 мг). Реакційну суміш перемішували протягом 16 годин за кімнатної температури та гасили шляхом додавання води. Сіль оцтової кислоти (сполука F1 з таблиці F) виділяли шляхом екстрагування етилацетатом, висушування над сульфатом натрію та випарювання розчинників. Вільну основу отримували шляхом розподілу між етилацетатом і насиченим водним розчином бікарбонату натрію. Органічний шар висушували над сульфатом натрію та випарювали під вакуумом до утворення залишку, який очищали за допомогою хроматографії на силікагелі (елюент: етилацетат/циклогексан 4:6) для отримання вказаної у заголовку сполуки у вигляді твердої + речовини жовтого кольору (120 мг). M.p. 98 °C. MS (ES+) 587 / 589 (MH ); 1H ЯМР (400 МГц, CDCl3) 1,7 (m, 2H), 2,1 (m, 4H), 2,7 (m, 1H), 3,0 (m, 2H), 3,6 (s, 2H), 7,4 (d, 2H), 7,5 (d, 2H), 7,55 (m, 1H), 7,60 (d, 1H), 7,70 (s, 1H), 7,8 (br s, 1H), 8,3 (d, 2H), 8,4 (m, 1H), 8,6 (d, 12H), 8,7 (s, 2H). Приклад 6 Цей приклад ілюструє отримання 2-хлор-N-{1'-[4-(5-фтор-піримідин-2-іл)-бензил]-6трифторметил-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл}-ізонікотинаміду (сполука B2 з таблиці B): N F3C N N N NH F Cl O N 50 Вказану в заголовку сполуку готували за процедурою, аналогічною описаним у прикладі 5, з використанням 4-(5-фтор-піримідин-2-іл)-бензальдегіду (препарат 2) на етапі E. M.p. 82-83 °C. Так само виділяли сіль оцтової кислоти (сполука F2 з таблиці F). Приклад 7 Цей приклад ілюструє отримання 2-хлор-N-{1'-[4-(5-хлор-піримідин-2-іл)-бензил]-6 19 UA 103540 C2 дифторметоксі-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл}-ізонікотинаміду таблиці B): (сполука B6 з N F N O N F N NH Cl Cl O N 5 10 15 20 25 30 Вказану в заголовку сполуку отримували з 2-бром-6-дифторметоксі-піридин-3-іл-аміну, дотримуючись описаних у прикладі 5 процедур. 2-бром-6-дифторметоксі-піридин-3-іл-амін був отриманий наступним чином: Етап A. 2-гідроксі-5-нітропіридин (5 г) обробляли хлордифторацетатом натрію (11,5 г) у кип'ячому ацетонітрилі (186 мл) протягом 2 днів. Розчинник випарювали, залишок виливали в етилацетат, промивали розсолом, висушували над сульфатом натрію, а потім випарювали під вакуумом. За допомогою хроматографії на силікагелі (елюент: гексан/етилацетат 1:1) отримували 2-дифторметоксі-5-нітро-піридин (1 г) та 1-дифторметил-5-нітро-1H-піридин-2-он (90 мг). 2-дифторметоксі-5-нітропіридин: MS (ES+) 191 (MH+); 1H ЯМР (400 МГц, CDCl 3) 7,05 (d, 1H), 7,51 (t, 1H), 8,53 (dd, 1H), 9,09 (d, 1H). 1-дифторметил-5-нітро-1H-піридин-2-он: MS (ES+) 191 (MH+); 1H ЯМР (400 МГц, CDCl3) 6,65 (d, 1H), 7,63 (t, 1H), 8,14 (dd, 1H), 8,73 (d, 1H). Етап В. Отриманий на етапі А 2-дифторметоксі-5-нітропіридин (1,6 г) обробляли протягом 20 хвилин залізом (5 г) та концентрованою соляною кислотою (0,23 мл) в етанолі (15 мл) та воді (2,5 мл) за температури 80 °C. Шляхом фільтрації над Celite® та випарювання розчинника отримували 6-дифторметоксі-піридин-3-іл-амін (1,4 г) у вигляді твердої речовини помаранчевого кольору. 1H ЯМР (400 МГц, CDCl3) 3,51 (br s, 2H), 6,89 (d, 1H), 7,23 (d, 1H), 7,44 (dd, 1H), 7,80 (d, 1H). Етап C. Отриманий на етапі В 6-дифторметоксі-піридин-3-іл-амін (1,36 г) обробляли Nбромсукцинімідом (1,51 г) в ацетонітрилі протягом 10 хвилин. Розчин виливали у воду, екстрагували етилацетатом, органічний шар висушували над сульфатом натрію та випарювали під вакуумом. За допомогою хроматографії на силікагелі (елюент: циклогексан/етилацетат 7:3) отримували 2-бром-6-дифторметоксі-піридин-3-іл-амін у вигляді олії червоного кольору. 1H ЯМР (400 МГц, CDCl3) 3,95 (br s, 2H), 6,72 (d, 1H), 7,07 (d, 1H), 7,24 (dd, 1H). Приклад 8 Цей приклад ілюструє отримання 2-хлор-N-{1'-[4-(5-хлор-піримідин-2-іл)-бензил]-4-фтор-6трифторметил-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл}-ізонікотинаміду (сполука B7 з таблиці B): N F3C N N N NH F Cl Cl O N 35 40 Етап A. Розчин отриманої на етапі В прикладу 5 сполуки (10,35 г) та N-хлорсукциніміду(4,4 г) у N-метилпіролідиноні (150 мл) перемішували за кімнатної температури протягом 2,5 годин. Реакційну суміш виливали у воду та кілька разів екстрагували етилацетатом. Об'єднані органічні шари промивали розсолом, висушували над сульфатом натрію та випарювали під вакуумом. За допомогою хроматографії на силікагелі (елюент: гексан/етилацетат 1:1) отримували трет-бутиловий ефір 3-аміно-4-хлор-6-трифторметил-3',4',5',6'-тетрагідро-2'H[2,4']біпіридиніл-1'-карбонової кислоти (9,6 г) у вигляді піни. MS (ES+) 380/382 (MH+), 324/326 (M-ізопрен); 1H ЯМР (400 МГц, CDCl3) 1,48 (s, 9H), 1,85 (m, 4H), 2,82 (m, 3H), 4,24 (m, 2H), 4,41 (br s, 2H), 7,46 (s, 1H). Етап В. Розчин отриманої на етапі А сполуки (7,6 г) і трифтороцтової кислоти (61,7 мл) у дихлорметані (380 мл) нагрівали до температури 55 °C. За цієї температури протягом 30 хвилин 20 UA 103540 C2 5 10 15 20 25 30 поволі додавали водний розчин пероксиду водню (30 % за вагою) (23 мл). Реакційну суміш витримували за даної температури протягом наступних 2 годин. Реакційну суміш виливали у воду та кілька разів екстрагували дихлорметаном. Об'єднані органічні екстракти промивали розсолом, висушували над сульфатом натрію та випарювали під вакуумом. Залишок повторно розчиняли у дихлорметані (200 мл). Потім додавали ди-трет-бутилдикарбонат (5,4 г) та N, Nдіізопропілетиламін (14,2 мл), і реакційну суміш перемішували за кімнатної температури протягом 16 годин. Реакційну суміш гасили шляхом додавання води й екстрагували дихлорметаном. Об'єднані органічні екстракти промивали розсолом, висушували над сульфатом натрію та випарювали під вакуумом. За допомогою хроматографії на силікагелі (елюент: гексан/етилацетат 5:1) отримували трет-бутиловий ефір 4-хлор-3-нітро-6трифторметил-3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (4,9 г) у вигляді піни. MS (ES+) 410/412 (MH+), 354/356 (M-ізопрен); 1H ЯМР (400 МГц, CDCl3) 1,48 (s, 9H), 1,77 (m, 2H), 1,95 (m, 2H), 2,85 (m, 3H), 4,26 (m, 2H), 7,74 (s, 1H). Етап C. Розчин отриманої на етапі В сполуки (1,2 г) та висушений розпиленням фторид калію (339 мг) у диметилсульфоксиді (57 мл) перемішували за температури 80 °C протягом 1 години. Реакційну суміш виливали у воду та кілька разів екстрагували етилацетатом. Об'єднані органічні екстракти промивали розсолом, висушували над сульфатом натрію та випарювали під вакуумом. За допомогою хроматографії на силікагелі (елюент: гексан/етилацетат 5:1) отримували трет-бутиловий ефір 4-фтор-3-нітро-6-трифторметил3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (0,7 г) у вигляді піни. MS (ES+) 338/339 (M-ізопрен); 1H ЯМР (400 МГц, CDCl3) 1,48 (s, 9H), 1,79 (m, 2H), 1,94 (m, 2H), 2,79 (m, 2H), 2,99 (m, 1H), 4,26 (m, 2H), 7,51 (d, 1H). Етап D. Отриману на етапі С сполуку (1,8 г) розчиняли в етанолі (48 мл), і після дегазування додавали паладій на активованому вугіллі (10 % за вагою) (500 мг). Реакційну суміш перемішували за кімнатної температури в атмосфері водню протягом 1 дня. Фільтрація на Celite® давала трет-бутиловий ефір 3-аміно-4-фтор-6-трифторметил-3',4',5',6'-тетрагідро-2'H[2,4']біпіридиніл-1'-карбонової кислоти (1,6 г) у вигляді твердої речовини білого кольору. MS (ES+) 364/365 (MH+), 308/309 (M-ізопрен); 1H ЯМР (400 МГц, CDCl3) 1,48(s, 9H), 1,85 (m, 4H), 2,86 (m, 3H), 3,90 (br s, 2H), 4,25 (m, 2H), 7,22 (d, 1H). Далі отриману на етапі D сполуку обробляли за описаними у прикладі 5 (етапи C-E) процедурами для отримання вказаної у заголовку сполуки. Приклад 9 Цей приклад ілюструє отримання 2-хлор-N-{5,6-дихлор-1'-[4-(5-хлор-піримідин-2-ил)-бензил]1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл}-ізонікотинаміду (сполука B8 з таблиці B): N Cl N N Cl N NH F Cl O N 35 40 45 50 Вказану в заголовку сполуку отримували з трет-бутилового ефіру 3-аміно-5,6-дихлор3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти за процедурами, аналогічними описаним у прикладі 5, етапи C-E. Трет-бутиловий ефір 3-аміно-5,6-дихлор-3',4',5',6'-тетрагідро2'H-[2,4']біпіридиніл-1'-карбонової кислоти отримували наступним чином: Етап A. Дегазований розчин 2,5-дихлор-3-амінопіридину (40,75 г), трет-бутилового ефіру 4(4,4,5,5-тетраметил-[1,3,2]діоксаборолан-2-іл)-3,6-дигідро-2H-піридин-1-карбонової кислоти (77,25 г) (отриманого згідно з описом у публікації WO 2006/003494) та біс(трифенілфосфін)паладію(II) хлориду (8,76 г) у діоксані (1500 мл) обробляли дегазованим розчином карбонату натрію (79 г) у воді (800 мл). Реакційну суміш нагрівали до кипіння протягом 16 годин, охолоджували до кімнатної температури, і розчинник випарювали під вакуумом. Залишок розподіляли між етилацетатом і водою, а водний шар тричі екстрагували етилацетатом. Об'єднані органічні екстракти висушували над сульфатом натрію та випарювали під вакуумом. За допомогою хроматографії на силікагелі (елюент: гексан/етилацетат 8:2) отримували трет-бутиловий ефір 3-аміно-5-фтор-3',6'-дигідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (60 г) у вигляді твердої речовини жовтого кольору. MS (ES+) 310/311 (MH+), 254 / 256 (MH+-ізобутен). 21 UA 103540 C2 5 10 15 Етап В. Отриману на етапі А проміжну сполуку тетрагідропіридину (54 г) гідрогенізували в метанолі (4000 мл) за температури 80 °C та тиску 100 бар воднем у присутності 1,1'-біс(ди-ізопропілфосфіно)фероцен(1,5-циклооктадієн)родію(I) тетрафторборату (358 мг) протягом 20 годин для отримання трет-бутилового ефіру 3-аміно-5-хлор-3',4',5',6'-тетрагідро-2'H[2,4']біпіридиніл-1'-карбонової кислоти (44 г). MS (ES+) 312/314 (MH+). Етап C. Отриманий на етапі B продукт (43 г) розчиняли у N-метилпіролідоні (600 мл) і обробляли N-хлорсукцинімідом (19 г) за кімнатної температури протягом 20 годин. Потім реакційну суміш розводили діетиловим ефіром і кілька разів промивали водою. Водний шар екстрагували етилацетатом, а об'єднані органічні екстракти висушували над сульфатом натрію. Розчинник видаляли під вакуумом, а залишок очищали за допомогою хроматографії на силікагелі (елюент: дихлорметан) для отримання трет-бутилового ефіру 3-аміно-5,6-дихлор3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (43 г) у вигляді твердої речовини. MS (ES+) 312/314 (MH+). Як варіант, трет-бутиловий ефір 3-аміно-5,6-дихлор-3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл1'-карбонової кислоти можна отримати згідно з описом, наведеним у публікації WO 2006/003494, використовуючи реакцію Негіші між 2,5-дихлор-3-амінопіридином і трет-бутиловим ефіром 4йод-піперидин-1-карбонової кислоти. Наведені нижче сполуки були отримані за процедурами, аналогічними описаним у прикладах 5-9: 20 Таблиця B Сполуки формули (Ib) N 3 R N N 4 R (Ib) N NH 8 R 5 R № сполуки B1 B2 B3 B4 B5 B6 B7 B8 B9 B10 B11 B12 R 1 2-хлор-пірид-4ил2-хлор-пірид-4ил5-хлор-2-фторпірид-4-ил2-хлор-5-фторпірид-4-ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2-хлор-пірид-4ил2,5-дифторпірид-4-ил O -CF3 H H Cl 97-98 °C 1,34 хв 587/589 -CF3 H H F 89-90 °C 1,28 хв 571/573 -CF3 H H Cl 1,37 хв 605/607 -CF3 H H Cl -CF3 H H H -OCHF2 H H Cl -CF3 H F Cl 1,39 хв 605/607 Cl Cl H Cl 197 °C 1,35 хв 589/591 CF3 H H циклопропіл 1,33 хв 593/595 CF3 H H Br CF3 H H CH3 CF3 H H Cl 22 R 8 МС (ES+) R R 5 ВЕРХ (RT) 4 R 3 1 R M.p. 214-216 °C 1,38 хв 605/607 1,27 хв 553/555 182-188 °C 1,34 хв 585/587 180-180 °C 1,36 хв 631/633 1,25 хв 567/569 188-189 °C 1,34 хв 589/591 UA 103540 C2 Таблиця B Сполуки формули (Ib) N 3 R N N 4 R (Ib) N NH 8 R 5 R № сполуки B13 B14 B15 B16 B17 B18 B19 B20 B21 B22 B23 B24 B25 B26 R 1 O 3 МС (ES+) R 5 R CF3 H H F 197-201 °C 1,38 хв 589/591 O-CHF2 H H Cl 169-172 °C 1,36 хв 603/605 O-CHF2 H H F 165-168 °C 1,30 хв 587/589 CF3 H H F 197-198 °C 1,31 хв CF3 H H F 160-163 °C 1,35 хв 605/607 CF3 H H Cl Cl Cl H F 222-223 °C 1,34 хв 573/575 O-CHF2 H H F 173-174 °C 1,25 хв O-CHF2 H H Cl 170-171 °C 1,31 хв 587/589 Cl Cl H Cl 232-237 °C 1,38 хв 589/591 Cl Cl H F 225-229 °C 1,36 хв 589/591 O-CHF2 H H Cl O-CHF2 H H F 204-206 °C 1,31 хв 603/605 Cl Cl H F 128-131 °C 1,30 хв 571/573 R 8 ВЕРХ (RT) 4 R 2-хлор-5-фторпірид-4-ил2-хлор-5-фторпірид-4-ил2-хлор-5-фторпірид-4-ил2,5-дифторпірид-4-ил2,5-дихлорпірид-4-ил2,5-дихлорпірид-4-ил2,5-дифторпірид-4-ил2,5-дифторпірид-4-ил2,5-дифторпірид-4-ил2,5-дифторпірид-4-ил2-хлор-5-фторпірид-4-ил2,5-дихлорпірид-4-ил2,5-дихлорпірид-4-ил2-хлор-пірид-4ил 1 R M.p. 93-96 °C 79-83 °C 573 1,41 хв 621/623 571 1,36 хв 619/621 Приклад 10 Цей приклад ілюструє отримання 2-хлор-N-(2-{1-[4-(5-хлор-піримідин-2-ил)-бензил]-1-оксіпіперидин-4-іл}-4-трифторметилфеніл)-ізонікотинаміду (сполука С1 з таблиці С): O + N N F3C N NH Cl Cl O N 5 Розчин 2-хлор-N-(2-{1-[4-(5-хлор-піримідин-2-ил)-бензил]-1-оксі-піперидин-4-іл}-4трифторметилфеніл)-ізонікотинаміду (270 мг, приклад 1) у дихлорметані (12 мл) обробляли 3 23 UA 103540 C2 5 хлорпероксібензойною кислотою (92 мг) за кімнатної температури. Розчин перемішували за кімнатної температури протягом 16 годин, і шляхом фільтрації збирали осад. Отриману тверду речовину промивали діетиловим ефіром і висушували під високим вакуумом для отримання вказаної у заголовку сполуки у вигляді порошку білого кольору. M.p. 193-194 °C. MS (ES+) 603/605 (MH+). Наведені нижче сполуки були отримані за процедурами, аналогічними описаним у прикладі 10: Таблиця C Сполука формули(Ic) O R R + 2 N 3 N (Ic) R 4 R № сполуки C1 C2 C3 C4 C5 C6 C7 C8 C9 C10 C11 C12 C13 C14 C15 C16 C17 10 R N NH R 8 5 O 1 2-хлор-пірид-4-ил2-хлор-пірид-4-ил2-хлор-5-фтор-пірид4-ил2-хлор-пірид-4-ил2-хлор-пірид-4-ил2-хлор-пірид-4-ил2-фтор-пірид-4-ил2-метоксі-пірид-4-ил2,6-дихлор-пірид-4ил2,5-дихлор-пірид-4ил2-хлор-5-фтор-пірид4-ил2,6-дихлор-пірид-4ил2-фтор-пірид-4-ил2-хлор-5-фтор-пірид4-ил2-метоксі-пірид-4-ил2-хлор-пірид-4-ил2,5-дихлор-пірид-4ил R R 1 2 R 3 R 4 R 5 R 8 M.p. H H -CF3 -CF3 H H H H Cl F 193-194 °C 178-179 °C H -CF3 H H Cl 198-199 °C H F F H H -CF3 -F -CF3 CF3 CF3 F H H F F H H H H H Cl Cl Cl Cl Cl 196-197 °C 183-184 °C 207-209 °C 193-196 °C 183-186 °C H CF3 F H Cl 193-196 °C H CF3 F H Cl 188-192 °C H CF3 F H Cl 184-187 °C F Cl H H Cl 194-197 °C F Cl H H Cl >220 °C F Cl H H Cl 191-195 °C F F Cl Cl H H H H Cl Cl 183-187 °C 199-205 °C F Cl H H Cl 208-211 °C Приклад 11 Цей приклад ілюструє отримання 2-хлор-N-{1'-[4-(5-хлор-піримідин-2-іл)-бензил]-6-метил1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл}-ізонікотинаміду (сполука D1 з таблиці D): 24 UA 103540 C2 O + N N N F3C N H N Cl Cl O N 5 10 Розчин 2-хлор-N-{1'-[4-(5-хлор-піримідин-2-іл)-бензил]-6-метил-1',2',3',4',5',6'-гексагідро[2,4']біпіридиніл-3-іл}-ізонікотинаміду (188 мг, приклад 5) у дихлорметані (8 мл) обробляли 3хлорпероксібензойною кислотою (65 мг) за кімнатної температури. Розчин перемішували за кімнатної температури всю ніч, і шляхом фільтрації збирали осад. Отриману тверду речовину промивали діетиловим ефіром і висушували під високим вакуумом для отримання вказаної у заголовку сполуки (170 мг) у вигляді порошку білого кольору. M.p. 177 °C. MS (ES+) 603/605 (MH+). Наведені нижче сполуки були отримані за процедурами, аналогічними описаним у прикладі 11: Таблиця D Сполуки формули (Id) O + N R 3 N N (Id) R 4 R № сполуки D1 D2 D3 D4 D5 15 N NH R 8 5 1 R O 1 R 2-хлор-пірид-4-ил2-хлор-пірид-4-ил5-хлор-2-фтор-пірид-4-ил2-хлор-5-фтор-пірид-4-ил2-хлор-пірид-4-ил 3 R -CF3 -CF3 -CF3 -CF3 -CF3 R H H H H H 4 R H H H H F 5 R Cl F Cl Cl Cl 8 M.p. 177 °C 201 °C 183-185 °C 173-175 °C 222-224 °C Отримання наступних солей E1 та E2 з таблиці E було описано у прикладі 1 і прикладі 2 відповідно. Інші солі можуть бути отримані за процедурами, аналогічними описаним у наведеному нижче прикладі 12: Приклад 12 Цей приклад ілюструє отримання гідрохлориду 2-хлор-N-(2-{1-[4-(5-хлор-піримідин-2-іл)бензил]-піперидин-4-іл}-4-трифторметилфеніл)-ізонікотинаміду (сполука Е3 з таблиці Е): 25 UA 103540 C2 H Cl + N N F3C N N H Cl Cl O N 5 Розчин 2-хлор-N-(2-{1-[4-(5-хлор-піримідин-2-іл)-бензил]-піперидин-4-іл}-4трифторметилфеніл)-ізонікотинаміду (1 г, приклад 1) у дихлорметані (50 мл) обробляли газом соляної кислоти протягом 2 хвилин. Тверду речовину білого кольору, що утворилася, промивали діетиловим ефіром і висушували під високим вакуумом для отримання вказаної у заголовку сполуки (1 г) у вигляді порошку білого кольору. M.p. 282-283 °C. Таблиця E Сполуки формули (Ie) HX 2 R N 3 R N 4 R (Ie) N NH 8 R 5 R № сполуки E1 E2 E3 E4 E5 E6 E7 1 R 2-хлор-пірид4-ил2-хлор-пірид4-ил2-хлор-пірид4-ил2-хлор-пірид4-ил2-хлор-пірид4-ил2-хлор-пірид4-ил2-хлор-пірид4-ил O R 2 1 R R 3 R 4 R 5 R 8 HX M.p. H -CF3 H H Cl CH3CO2H 222-223 °C H -CF3 H H F CH3CO2H 154 °C H -CF3 H H Cl HCl 282-283 °C H CF3 H H Cl 225 °C H CF3 H H Cl H CF3 H H Cl H CF3 H H Cl 2-гідроксібензойна кислота 2,3,4,5-тетрагідроксі-6оксогексанова кислота 2-хлор-бензойна кислота Фосфорна кислота 3-гідроксі-пропан1-сульфонова кислота Етансульфонова кислота Толуол-4сульфонова кислота E8 2-хлор-пірид4-ил H CF3 H H Cl E9 2-хлор-пірид4-ил H CF3 H H Cl E10 2-хлор-пірид4-ил H CF3 H H Cl Отримання наступних солей було описано у прикладі 5 і прикладі 6 відповідно: 26 165 °C 166 °C 125 °C 183 °C 260 °C 242 °C UA 103540 C2 Таблиця F Сполуки формули (If) HX N 3 R N N 4 R N NH (If) 8 R 5 R № сполуки F1 F2 1 R 2-хлор-пірид-4ил2-хлор-пірид-4ил 1 R O 4 R -CF3 H H -CF3 H H R 3 R 5 R 8 HX M.p. Cl CH3CO2H 254-255 °C F CH3CO2H 143 °C Препарат 1 4-(5-хлор-піримідин-2-іл)-бензальдегід H O N N 5 10 15 Cl Дихлор-біс(трифенілфосфін) паладію (3,5 г) додавали до перемішуваного розчину 4формілбензолборонової кислоти (32,5 г), 2,5-дихлор-піримідину (30 г) у толуолі (1000 мл) й етанолі (100 мл) в атмосфері аргону. Розчин очищали за допомогою аргону, та додавали водний розчин карбонату натрію (2N) (200 мл). Реакційну суміш перемішували за температури 60 °C протягом 90 хвилин, охолоджували до кімнатної температури, розводили етилацетатом і послідовно промивали насиченим водним розчином бікарбонату натрію, водою та розсолом. Об'єднані органічні екстракти обробляли активованим вугіллям, висушували над сульфатом натрію, фільтрували через Hyflo® та випарювали під вакуумом. Залишок розтирали з діетиловим ефіром (100 мл), тверду речовину відділяли шляхом фільтрації та висушували під високим вакуумом для отримання 4-(5-хлор-піримідин-2-іл)-бензальдегіду у вигляді твердої речовини білого кольору. M.p. 186 °C. 1H ЯМР (400 МГц, DMSO) 8,10 (d, 2H), 8,55 (d, 2H), 9,1 (s, 2H). Препарат 2 4-(5-фтор-піримідин-2-іл)-бензальдегід H O N N 20 25 F Вказану в заголовку сполуку отримували за процедурою, аналогічною описаній для препарату 1, починаючи з 2-хлор-5-фтор-піримідину для отримання 4-(5-хлор-піримідин-2-іл) + бензальдегіду у вигляді твердої речовини білого кольору. MS (ES+) 203 (MH ); 1H ЯМР (400 МГц, CDCl3) 8,0 (d, 2H), 8,6 (d, 2H), 28,75 (s, 2H). Біологічні приклади Цей приклад ілюструє пестицидні/інсектицидні властивості сполук формули (I). Проводилися наступні дослідження: Spodoptera littoralis (єгипетська бавовняна совка): 27 UA 103540 C2 5 10 15 20 25 30 35 40 45 50 Листки бавовни поміщали на агар в 24-лунковий титраційний мікропланшет і обприскували досліджуваними розчинами при нормі внесення 200 ppm. Після висушування листки заражали 5 личинками першого личинкового віку (L1). Через 3 дні після обробки (DAT) взірці перевіряли на смертність, харчову поведінку та регулювання росту. Ефективність представлених нижче сполук у боротьбі зі Spodoptera littoralis склала не менш 80 %: A1, A2, A3, A4, A5, A6, A7, A8, A9, A10, A11, A12, A13, A14, A15, A16, A17, A18, A19, A20, A21, A22, A23, A24, A25, A26, A27, A28, A29, A30, A31, A32, A33, A34, A35, A36, A37, A38, A39, A40, A41, A42, A43, A44, A45, A46, A47, A48, A49, A50, A51, A52, A53, A54, A55, A56, A57, A58, A59, A60, B1, B2, B3, B4, B5, B6, B7, B8, B9, B10, B11, B12, B13, B14, B15, B16, B17, B18, B19, B20, B21, B22, B23, B24, B25, B26, C1, C2, C3, C4, C5, C6, C7, C8, C9, C10, C11, C12, C13, C14, C15, C16, C17, D1, D2, D3, D4, D5, E1, E2, E4, E5, E6, E7, E8, E9, E10, F1, F2. Heliothis virescens (тютюнова совка): Яйця (віком 0-24 години) поміщали у 24-лунковий титраційний мікропланшет на штучне поживне середовище і обробляли досліджуваними розчинами при нормі внесення 200 ppm (концентрація в лунці 18 ppm) шляхом відмірювання піпеткою. По закінченні інкубаційного періоду у 4 дні взірці перевіряли на смертність яєць, смертність личинок і регуляцію росту. Ефективність представлених нижче сполук у боротьбі зі Heliothis virescens склала не менш 80 %: A1, A2, A3, A4, A5, A6, A7, A8, A9, A10, A11, A12, A13, A14, A15, A16, A17, A18, A19, A20, A21, A22, A23, A24, A25, A26, A27, A28, A29, A30, A31, A32, A33, A34, A35, A36, A37, A38, A39, A40, A41, A42, A43, A44, A45, A46, A47, A48, A49, A50, A51, A52, A53, A54, A55, A56, A57, A58, A59, A60, B1, B2, B3, B4, B5, B6, B7, B8, B9, B10, B11, B12, B13, B14, B15, B16, B17, B18, B19, B20, B21, B22, B23, B24, B25, B26, C1, C2, C3, C4, C5, C6, C7, C8, C9, C10, C11, C12, C13, C14, C15, C16, C17, D1, D2, D3, D4, D5, E1, E2, E4, E5, E6, E7, E8, E9, E10, F1, F2. Plutella xylostella (капустяна серпокрила міль): 24-лунковий титраційний мікропланшет (MTP) зі штучним поживним середовищем обробляли досліджуваними розчинами при нормі внесення 200 ppm (концентрація у лунці 18 ppm) шляхом відмірювання піпеткою. Після висушування MTP заражали личинками другого личинкового віку (L2) (7-12 личинок на лунку). По закінченні інкубаційного періоду у 6 днів взірці перевіряли на смертність личинок і регуляцію росту. Ефективність представлених нижче сполук у боротьбі зі Plutella xylostella склала не менш 80 %: A1, A2, A3, A4, A5, A6, A7, A8, A9, A10, A11, A12, A13, A14, A15, A16, A17, A18, A19, A20, A21, A22, A23, A25, A26, A27, A28, A29, A30, A31, A32, A33, A34, A35, A36, A37, A38, A39, A40, A41, A42, A43, A44, A45, A46, A47, A48, A49, A50, A51, A52, A53, A54, A55, A56, A57, A58, A59, A60, B1, B2, B3, B4, B5, B6, B7, B8, B9, B10, B11, B12, B13, B14, B15, B16, B17, B18, B19, B20, B21, B22, B23, B24, B25, B26, C1, C2, C3, C4, C5, C6, C7, C8, C9, C10, C11, C12, C13, C14, C15, C16, C17, D1, D2, D3, D4, D5, E1, E2, E4, E5, E6, E7, E8, E9, E10, F1, F2. Diabrotica balteata (кукурудзяна коренева гусениця): 24-лунковий титраційний мікропланшет (MTP) зі штучним поживним середовищем обробляли досліджуваними розчинами при нормі внесення 200 ppm (концентрація у лунці 18 ppm) шляхом відмірювання піпеткою. Після висушування MTP заражали личинками другого личинкового віку (L2) (6-10 личинок на лунку). По закінченні інкубаційного періоду у 5 днів взірці перевіряли на смертність личинок і регуляцію росту. Ефективність представлених нижче сполук у боротьбі з Diabrotica balteata склала не менш 80 %: A1, A2, A3, A4, A5, A6, A7, A8, A9, A10, A11, A12, A13, A14, A15, A16, A17, A18, A19, A20, A21, A22, A23, A24, A25, A27, A28, A30, A32, A33, A34, A35, A37, A38, A39, A40, A41, A42, A43, A44, A45, A46, A47, A48, A49, A52, A53, A54, A55, A56, A57, A58, A59, A60, B1, B2, B3, B4, B5, B6, B7, B8, B9, B10, B11, B12, B13, B14, B15, B16, B17, B18, B19, B20, B21, B22, B23, B24, B25, B26, C1, C2, C3, C4, C5, C6, C7, C8, C9, C10, C11, C12, C17, D1, D2, D3, D4, D5, E1, E2, E4, E5, E6, E7, E8, E9, E10, F1, F2. 28
ДивитисяДодаткова інформація
Назва патенту англійськоюInsecticidal compounds
Автори англійськоюCassayre, Jerome Yves, Pitterna, Thomas, Corsi, Camilla, Maienfisch, Peter
Автори російськоюКассеир Жером Ив, Питтерна Томас, Корси Камилла, Майенфиш Петер
МПК / Мітки
МПК: C07D 401/14, A01N 43/54, A01P 7/04
Мітки: сполуки, інсектицидні
Код посилання
<a href="https://ua.patents.su/31-103540-insekticidni-spoluki.html" target="_blank" rel="follow" title="База патентів України">Інсектицидні сполуки</a>
Попередній патент: Інсектицидні сполуки
Наступний патент: Прихована кулеметна установка
Випадковий патент: Пристрій для вимірювання ступеня електризації вибухових речовин