Заміщені тетраліни та індани
Номер патенту: 80297
Опубліковано: 10.09.2007
Автори: Меттьюз Джей М., Лі Джанг, Демарест Кейт Т., Чен Сяолі, Рибчинскі Філіп
Формула / Реферат
1. Сполука формули І
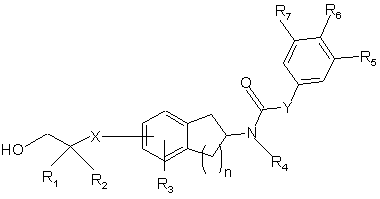
Формула І
чи її фармацевтично прийнятна сіль, С1-5-складний ефір чи С1-5-амід, у якій кожний з R1 та R2 незалежно означає Н, С1-6-алкіл, (CH2)mNRaRb, (CH2)mOR8, (CH2)mNH(CO)R8 чи (CH2)mCO2R8, де кожний з Ra, Rb та R8 незалежно означає Н чи С1-5-алкіл, або R1 та R2 разом з атомом карбону, до якого вони приєднані, утворюють С3-7-циклоалкіл,
m має значення від 1 до 6,
n дорівнює 1 чи 2,
X означає О чи S, де X знаходиться в положенні 5 чи 6, якщо n дорівнює 1, і де
X знаходиться у положенні 6 чи 7, якщо n дорівнює 2,
R3 означає Н, феніл, С1-3-алкоксигрупу, С1-3-алкілтіогрупу, галоїд, ціаногрупу, С1-6-алкіл, нітрогрупу, NR9R10, NHCOR10, CONHR10 та COOR10, і R3 знаходиться в орто- чи мета-положенні стосовно X,
R4 означає Н чи -(С1-5-алкілен)-R15, де R15 означає Н, С1-7-алкіл, [ді-(С1-2-алкіл)аміно]-(С1-6-алкілен), (С1-3-алкоксіацил)-(С1-6-алкілен), С1-6-алкоксигрупу, С3-7-алкеніл чи С3-8-алкініл, де R4 має не більше ніж 9 атомів карбону, причому R4 може також означати -(С1-5-алкілен)R15, де R15 означає С3-8-циклоалкіл, феніл, феніл-О-, феніл-S- чи 5-6-членний одновалентний гетероциклічний радикал з 1-2 гетероатомами, вибраними з N, О та S,
Y означає NH, NH-CH2 та О,
кожний з R5 та R7 незалежно вибирають з Н, С1-6-алкілу, галоїду, ціаногрупи, нітрогрупи, COR11, COOR11, С1-4-алкоксигрупи, С1-4-алкілтіогрупи, гідроксильної групи, фенілу, NR11R12 та 5-6-членного одновалентного гетероциклічного
радикала з 1-2 гетероатомами, вибраними з N, О та S,
R6 вибирають з С1-6-алкілу, галоїду, ціаногрупи, нітрогрупи, COR13, COOR13, С1-4-алкоксигрупи, С1-4-алкілтіогрупи, гідроксильної групи, фенілу, NR13R14 та 5-6-членного одновалентного гетероциклічного радикала з 1-2 гетероатомами, вибраними з N, О та S, крім того, R5 та R6 або R6 та R7 можуть утворювати разом двовалентний фрагмент, насичений чи ненасичений, вибраний з -(СН2)3-, -(СН2)4- та (CH1-2)pN(CH1-2)q,
р дорівнює 0-2 і q дорівнює 1-3, причому сума (р + q) складає щонайменше 2, кожний з R9 та R10 незалежно означає С1-6-алкіл, кожний з R11, R12, R13 та R14 незалежно означає Н чи С1-6-алкіл, причому кожний із зазначених вище гідрокарбільних та гетерокарбільних фрагментів може бути заміщений 1-3 замісниками, незалежно вибраними з F, Сl, Вr, І, аміногрупи, метилу, етилу, гідроксильної групи, нітрогрупи, ціаногрупи та метоксигрупи.
2. Сполука за п. 1, у якій один з R1 та R2 означає метил чи етил.
3. Сполука за п. 2, у якій кожний з R1 та R2 означає метил.
4. Сполука за п. 1, де R1 та R2 разом означають циклобутил чи циклопентил.
5. Сполука за п. 1, у якій R3 означає Н.
6. Сполука за п. 1, у якій R3 означає С1-3-алкоксигрупу, С1-3-алкілтіогрупу, галоїд, ціаногрупу, С1-6-алкіл, нітрогрупу, NR9R10, NHCOR10, CONHR10 чи COOR10.
7. Сполука за п. 1, у якій R4 означає Н чи С2-7-алкіл.
8. Сполука за п. 7, у якій R4 означає Н чи С2-5-алкіл.
9. Сполука за п. 8, у якій R4 означає етил.
10. Сполука за п. 8, у якій R4 означає Н.
11. Сполука за п. 1, у якій n дорівнює 1.
12. Сполука за п. 1, у якій n дорівнює 2.
13. Сполука за п. 1, у якій Y означає NH-СН2.
14. Сполука за п. 1, у якій Y означає NH.
15. Сполука за п. 1, у якій X означає S.
16. Сполука за п. 1, у якій X означає О.
17. Сполука за п. 1, у якій щонайменше один з R5 та R7 означає Н.
18. Сполука за п. 17, у якій R6 означає С1-4-алкіл, галоїдметоксигрупу, галоїдметилтіогрупу чи ді-(С1-3-алкіл)аміногрупу.
19. Сполука за п. 18, у якій R6 означає трифлюорметоксигрупу, дифлюорметоксигрупу, трифлюорметил, трифлюорметилтіогрупу, т-бутил, ізопропіл чи диметиламіногрупу.
20. Сполука за п. 3, у якій R3 означає Н, R4 означає С2-7-алкіл і Y означає NH.
21. Сполука за п. 20, у якій X означає S.
22. Сполука за п. 20, у якій n дорівнює 1.
23. Сполука за п. 20, у якій n дорівнює 2.
24. Сполука за п. 20, у якій R4 означає С2-5-алкіл.
25. Сполука за п. 24, у якій R4 означає етил.
26. Сполука за п. 20, у якій R6 означає трифлюорметоксигрупу, дифлюорметоксигрупу, трифлюорметил, трифлюорметилтіогрупу, т-бутил, ізопропіл чи диметиламіногрупу.
27. Сполука за п. 1, у якій кожний з R1 та R2 незалежно означає Н, С1-6-алкіл, (CH2)mNRaRb чи (CH2)mOR8, де кожний з Ra, Rb та R8 незалежно означає Н чи С1-6-алкіл,
m має значення від 1 до 6,
n дорівнює 1 чи 2,
X означає О чи S, причому X знаходиться в положенні 5 чи 6, якщо n дорівнює 1, і X знаходиться в положенні 6 чи 7, якщо n дорівнює 2,
R3 означає Н, феніл, С1-3-алкоксигрупу, С1-3-алкілтіогрупу, галоїд, С1-6-алкіл чи NR9R10, і R3 знаходиться в орто- чи мета-положенні стосовно X,
R4 означає Н чи -(С1-5-алкілен)R15, де R15 означає Н, С1-7-алкіл, [ді-(С1-2-алкіл)аміно]-(С1-6-алкілен), (С1-3-алкоксіацил)-(С1-6-алкілен), С1-6-алкоксигрупу чи С3-7-алкеніл, причому R4 містить не більше ніж 9 атомів карбону,
R4 може також означати -(С1-5-алкілен)-R15, де R15 означає С3-6-циклоалкіл, феніл, феніл-О-, феніл-S- чи 5-6-членний одновалентний гетероциклічний радикал з 1-2 гетероатомами, вибраними з N, О та S,
Y означає NH чи NHCH2,
кожний з R5 та R7 незалежно вибирають з Н, С1-5-алкілу, галоїду, COR11, COOR11, С1-4-алкоксигрупи, С1-4-алкілтіогрупи, гідроксильної групи та NR11R12,
R6 вибирають з С1-6-алкілу, галоїду, COR13, COOR13, С1-4-алкоксигрупи, С1-4-алкілтіогрупи, фенілу, NR13R14 та 5-6-членного одновалентного гетероциклічного радикала з 1-2 гетероатомами, вибраними з N, О та S, кожний з R9 та R10 незалежно означає С1-5-алкіл, кожний з R11, R12, R13 та R14 незалежно означає Н чи С1-5-алкіл, причому кожний із зазначених вище гідрокарбільних та гетерокарбільних фрагментів може бути заміщений 1-3 замісниками, незалежно вибраними з F, Сl, аміногрупи, метилу, етилу, гідроксильної групи та метоксигрупи.
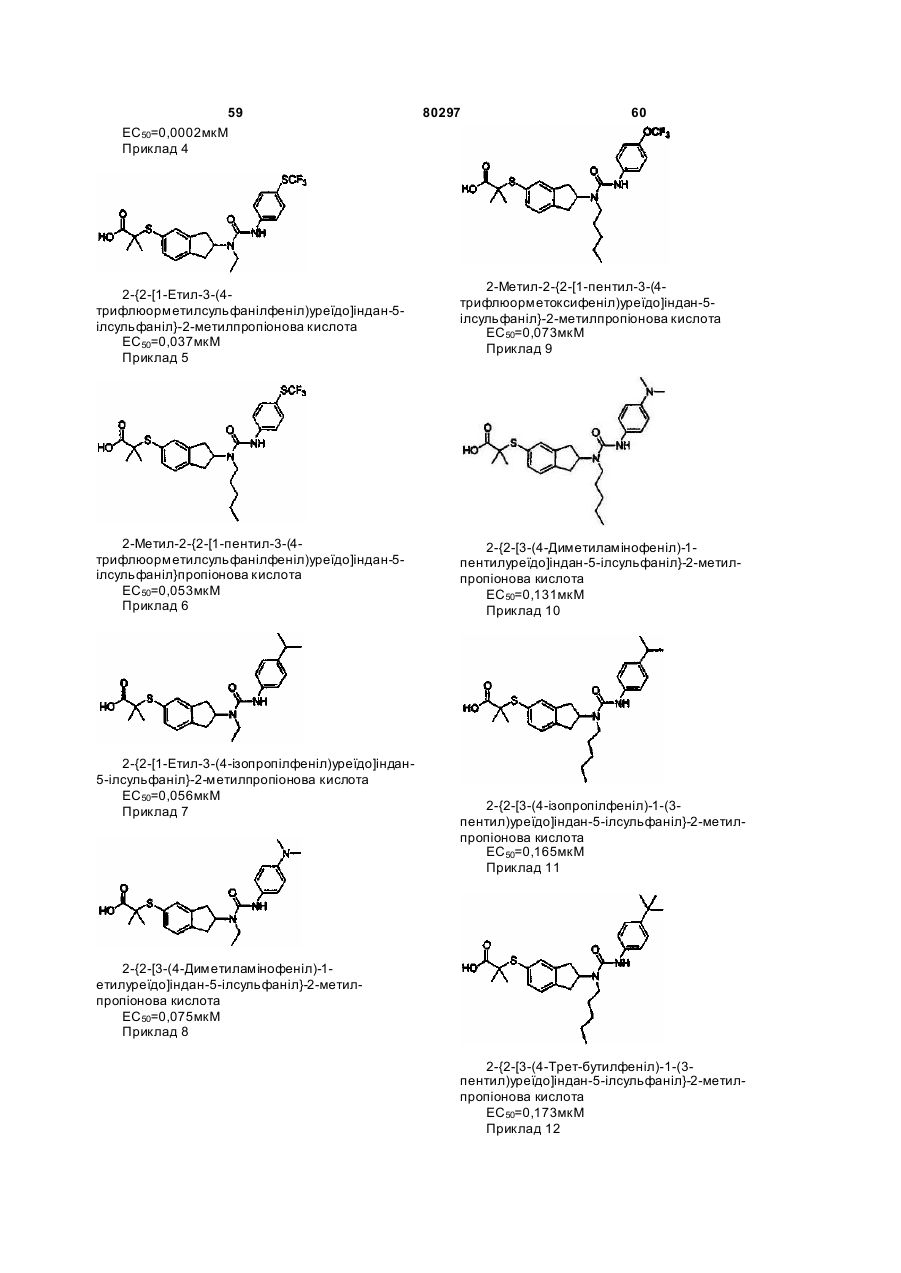
28. Сполука за п. 1, вибрана з:
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти,
2-{2-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-{2-[1-етил-3-(4-трифлюорметилсульфанілфеніл)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-метил-2-{2-[1-пентил-3-(4-трифлюорметилсульфанілфеніл)уреїдо]індан-5-ілсульфаніл}пропіонової кислоти,
2-{2-[1-етил-3-(4-ізопропілфеніл)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-метил-2-{2-[1-пентил-3-(4-трифлюорметоксифеніл)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-{2-[3-(4-диметиламінофеніл)-1-етилуреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-метил-2-{2-[1-(3-метилбутил)-3-(4-трифлюорметоксифеніл)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-{2-[3-(4-ізопропілфеніл)-1-(3-метилбутил)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-метил-2-{2-[1-пент-4-еніл-3-(4-трифлюорметоксифеніл)уреїдо]індан-5-ілсульфаніл}пропіонової кислоти,
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-метокси-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти,
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-флюор-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти,
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-хлор-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти,
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-бром-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти,
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-метил-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти та
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-трифлюорметокси-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти.
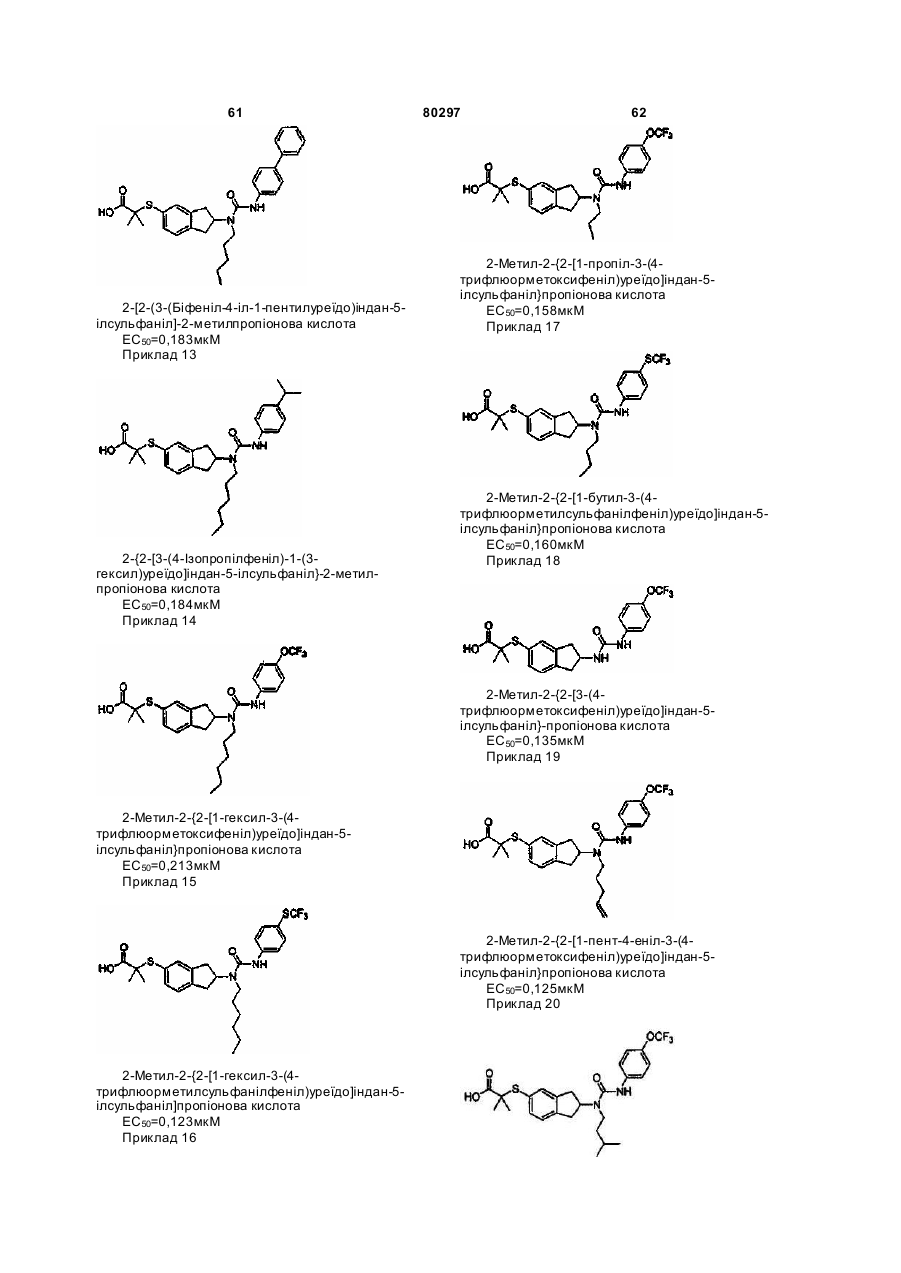
29. Сполука за п. 1, вибрана з:
2-метил-2-{2-[1-гексил-3-(4-трифлюорметилсульфанілфеніл)уреїдо]індан-5-ілсульфаніл}пропіонової кислоти,
2-{2-[3-(4-диметиламінофеніл)-1-пентилуреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-метил-2-{2-[3-(4-трифлюорметоксифеніл)уреїдо]індан-5-ілсульфаніл}-пропіонової кислоти,
2-метил-2-{2-[1-пропіл-3-(4-трифлюорметоксифеніл)уреїдо]індан-5-ілсульфаніл}пропіонової кислоти,
2-метил-2-{2-[1-бутил-3-(4-трифлюорметилсульфанілфеніл)уреїдо]індан-5-ілсульфаніл}пропіонової кислоти,
2-{2-[3-(4-ізопропілфеніл)-1-(3-пентил)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-{2-[3-(4-трет-бутилфеніл)-1-(3-пентил)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-[2-(3-(біфеніл-4-іл-1-пентилуреїдо)індан-5-ілсульфаніл]-2-метилпропіонової кислоти,
2-{2-[3-(4-ізопропілфеніл)-1-(3-гексил)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-метил-2-{2-[1-бутил-3-(4-трифлюорметоксифеніл)уреїдо]індан-5-ілсульфаніл}пропіонової кислоти,
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-метокси-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти,
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-флюор-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти,
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-хлор-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти,
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-бром-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти,
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-метил-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти та
2-метил-2-{2-[1-гексил-3-(4-трифлюорметоксифеніл)уреїдо]індан-5-ілсульфаніл}пропіонової кислоти.
30. Сполука за п. 1, вибрана з:
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти,
2-{6-[3-(4-трифлюорметоксифеніл)уреїдо]-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти,
2-{2-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-флюор-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти,
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-метил-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти,
2-{2-[1-етил-3-(4-трифлюорметилсульфанілфеніл)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти та
2-метил-2-{2-[1-пропіл-3-(4-трифлюорметоксифеніл)уреїдо]індан-5-ілсульфаніл}пропіонової кислоти.
31. Сполука за п. 1, вибрана з:
2-{2-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-{2-[1-етил-3-(4-трифлюорметилсульфанілфеніл)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонової кислоти,
2-метил-2-{2-[1-пропіл-3-(4-трифлюорметоксифеніл)уреїдо]індан-5-ілсульфаніл}пропіонової кислоти та
2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3-флюор-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонової кислоти.
32. Фармацевтична композиція, яка містить як активний інгредієнт сполуку за п. 1, 20, 27, 28, 30 чи 31.
33. Спосіб лікування чи інгібування розвитку PPAR-альфа-медійованої хвороби, який включає введення пацієнту, що потребує лікування, фармацевтично ефективної кількості композиції, яка містить сполуку за п. 1, 20, 27, 28 чи 31.
34. Спосіб за п. 33, у якому зазначену PPAR-альфа-медійовану хворобу вибирають з дисліпідемії та серцево-судинних хвороб.
35. Спосіб за п. 34, у якому зазначена хвороба є дисліпідемією.
36. Спосіб за п. 34, у якому зазначену дисліпідемію вибирають з гіперліпідемії фази І, передклінічної гіперліпідемії, гіперліпідемії фази II, гіперхолестеринемії, гіпо-HDL-холестеринемії та гіпертригліцеридемії.
37. Спосіб за п. 34, у якому зазначена серцево-судинна хвороба є атеросклерозом, ішемічною хворобою серця, коронарною хворобою чи гіпертензією.
38. Спосіб за п. 33, 35 чи 36, який додатково включає стадію введення пацієнту спільно ефективної кількості агента зниження рівня ліпідів.
39. Спосіб за п. 33, 35, 36 чи 38, який додатково включає стадію введення пацієнту спільно ефективної кількості агента зниження кров'яного тиску.
Текст
1. Сполука формули І C2 2 (19) 1 3 80297 4 F, Сl, Вr, І, аміногрупи, метилу, е тилу, гідроксилькожн ий з R 5 та R 7 не за лежно ви бир ають з Н , ної гр упи, ні трогр упи, ціаногр упи та метоксигрупи. С 1- 5 -а лкі лу, гало їду, C OR 11 , COOR 11 , С1- 42. Сполука за п. 1, у якій один з R1 та R2 означає алкоксигрупи, С1- 4-алкілтіогр упи, гідроксильної метил чи етил. групи та NR 11R12 , 3. Сполука за п. 2, у якій кожний з R1 та R2 означає R6 вибирають з С1-6-алкілу, гало їду, COR 13, метил. COOR 13, С 1- 4-алкоксигр упи , С1- 4-алкілтіогр упи, 4. С по лук а з а п . 1 , де R 1 та R 2 ра зо м оз на фенілу, NR 13R 14 та 5-6-членного одновалентного ча ють цик ло бути л чи циклопентил. гетероциклічного радикала з 1-2 гетероатомами, 5. Сполука за п. 1, у якій R 3 означає Н. вибраними з N, О та S, кожний з R9 та R10 незалеж6. Сполука за п. 1, у якій R3 означає С1-3но означає С 1- 5 -алкіл, кожний з R11, R12, R13 та R14 алкоксигрупу, С1-3-алкілтіогрупу, галоїд, ціаногрупу, незалежно означає Н чи С 1- 5-алкіл, причому кожний С1-6-алкіл, нітрогрупу, NR9R10, NHCOR10, CONHR10 чи із зазначених вище гідрокарбільних та гетерокарбіCOOR10. льних фра гментів може бути заміщений 1-3 замі7. Сполука за п. 1, у якій R4 означає Н чи С 2-7-алкіл. сниками, незалежно вибраними з F, Сl, аміногру8. Сполука за п. 7, у якій R4 означає Н чи С 2-5-алкіл. пи, метилу, етилу, гідроксильної групи та 9. Сполука за п. 8, у якій R 4 означає етил. метоксигрупи. 10. Сполука за п. 8, у якій R4 означає Н. 28. Сполука за п. 1, вибрана з: 11. Сполука за п. 1, у якій n дорівнює 1. 2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]12. Сполука за п. 1, у якій n дорівнює 2. 5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-213. Сполука за п. 1, у якій Y означає NH-СН2. метилпропіонової кислоти, 14. Сполука за п. 1, у якій Y означає NH. 2-{2-[1-етил-3-(415. Сполука за п. 1, у якій X означає S. трифлюорметоксифеніл)уреїдо]індан-516. Сполука за п. 1, у якій X означає О. ілсульфаніл}-2-метилпропіонової кислоти, 17. Сполука за п. 1, у якій щонайменше один з R 5 та 2-{2-[1-етил-3-(4R7 означає Н. трифлюорметилсульфанілфеніл)уреїдо]індан-518. Сполука за п. 17, у якій R6 означає С 1- 4-алкіл, ілсульфаніл}-2-метилпропіонової кислоти, галоїдметоксигр уп у, галоїдметилтіогрупу чи ді-(С12-метил-2-{2-[1-пентил-3-(4трифлюорметилсульфанілфеніл)уреїдо]індан-53-алкіл)аміногрупу. 19. Сполука за п. 18, у якій R6 означає три флюоілсульфаніл}пропіонової кислоти, рметоксигруп у, ди флюорметоксигрупу, трифлюо2-{2-[1-етил-3-(4-ізопропілфеніл)уреїдо]індан-5рметил, трифлюорметилтіогрупу, т-бутил, ізопропіл ілсульфаніл}-2-метилпропіонової кислоти, чи диметиламіногрупу. 2-метил-2-{2-[1-пентил-3-(420. Сполука за п. 3, у якій R 3 означає Н , R4 трифлюорметоксифеніл)уреїдо]індан-5означа є С 2- 7-а лкіл і Y означає NH. ілсульфаніл}-2-метилпропіонової кислоти, 21. Сполука за п. 20, у якій X означає S. 2-{2-[3-(4-диметиламінофеніл)-1-етилуреїдо]індан22. Сполука за п. 20, у якій n дорівнює 1. 5-ілсульфаніл}-2-метилпропіонової кислоти, 23. Сполука за п. 20, у якій n дорівнює 2. 2-метил-2-{2-[1-(3-метилбутил)-3-(424. Сполука за п. 20, у якій R4 означає С2-5-алкіл. трифлюорметоксифеніл)уреїдо]індан-525. Сполука за п. 24, у якій R4 означає етил. ілсульфаніл}-2-метилпропіонової кислоти, 26. Сполука за п. 20, у якій R6 означає трифлюор2-{2-[3-(4-ізопропілфеніл)-1-(3метоксигрупу, дифлюорметоксигрупу, три флюорметилбутил)уреїдо]індан-5-ілсульфаніл}-2метил, трифлюорметилтіогруп у, т-бутил, ізопропіл метилпропіонової кислоти, чи диметиламіногрупу. 2-метил-2-{2-[1-пент-4-еніл-3-(427. Сполука за п. 1, у якій кожний з R1 та R2 незатрифлюорметоксифеніл)уреїдо]індан-5лежно означає Н, С1-6-алкіл, (CH2)mNRaRb чи ілсульфаніл}пропіонової кислоти, (CH2)mOR8, де кожний з Ra, Rb та R8 незалежно озна2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]чає Н чи С 1-6-алкіл, 3-метокси-5,6,7,8-тетрагідронафталін-2m має значення від 1 до 6, ілсульфаніл}-2-метилпропіонової кислоти, n дорівнює 1 чи 2, 2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3X означає О чи S, причому X знаходи ться в полофлюор-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}женні 5 чи 6, якщо n дорівнює 1, і X знаходиться в 2-метилпропіонової кислоти, положенні 6 чи 7, якщо n дорівнює 2, 2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3R3 означає Н, феніл, С1-3-алкоксигрупу, С1-3хлор-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2алкілтіогрупу, галоїд, С1-6-алкіл чи NR9R10, і R3 знаметилпропіонової кислоти, ходиться в орто- чи мета-положенні стосовно X, 2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3R4 озна чає Н чи -(С1-5-а лкілен )R 15, де R 15 ознабром-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2чає Н , С 1-7 -а лкіл, [ді-(С 1-2 -алкіл)аміно]-(С1-6метилпропіонової кислоти, алкілен), (С1-3-алкоксіацил)-(С1-6-алкілен), С1-62-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3алкоксигрупу чи С3-7-алкеніл, причому R4 містить не метил-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}більше ніж 9 атомів карбону, 2-метилпропіонової кислоти та R4 може також означати -(С1-5-алкілен)-R15 , де 2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3R15 означає С 3-6-циклоалкіл, феніл, феніл-О-, трифлюорметокси-5,6,7,8-тетрагідронафталін-2феніл-S- чи 5-6-членний одновалентний ге тероілсульфаніл}-2-метилпропіонової кислоти. циклічний радикал з 1-2 гетероатомами, вибрани29. Сполука за п. 1, вибрана з: ми з N, О та S, Y означає NH чи NHCH2, 5 80297 6 2-метил-2-{2-[1-гексил-3-(42-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3трифлюорметилсульфанілфеніл)уреїдо]індан-5флюор-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}ілсульфаніл}пропіонової кислоти, 2-метилпропіонової кислоти, 2-{2-[3-(4-диметиламінофеніл)-12-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3пентилуреїдо]індан-5-ілсульфаніл}-2метил-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}метилпропіонової кислоти, 2-метилпропіонової кислоти, 2-метил-2-{2-[3-(42-{2-[1-етил-3-(4трифлюорметоксифеніл)уреїдо]індан-5трифлюорметилсульфанілфеніл)уреїдо]індан-5ілсульфаніл}-пропіонової кислоти, ілсульфаніл}-2-метилпропіонової кислоти та 2-метил-2-{2-[1-пропіл-3-(42-метил-2-{2-[1-пропіл-3-(4трифлюорметоксифеніл)уреїдо]індан-5трифлюорметоксифеніл)уреїдо]індан-5ілсульфаніл}пропіонової кислоти, ілсульфаніл}пропіонової кислоти. 2-метил-2-{2-[1-бутил-3-(431. Сполука за п. 1, вибрана з: трифлюорметилсульфанілфеніл)уреїдо]індан-52-{2-[1-етил-3-(4ілсульфаніл}пропіонової кислоти, трифлюорметоксифеніл)уреїдо]індан-52-{2-[3-(4-ізопропілфеніл)-1-(3ілсульфаніл}-2-метилпропіонової кислоти, пентил)уреїдо]індан-5-ілсульфаніл}-22-{2-[1-етил-3-(4метилпропіонової кислоти, трифлюорметилсульфанілфеніл)уреїдо]індан-52-{2-[3-(4-трет-бутилфеніл)-1-(3ілсульфаніл}-2-метилпропіонової кислоти, пентил)уреїдо]індан-5-ілсульфаніл}-22-метил-2-{2-[1-пропіл-3-(4метилпропіонової кислоти, трифлюорметоксифеніл)уреїдо]індан-52-[2-(3-(біфеніл-4-іл-1-пентилуреїдо)індан-5ілсульфаніл}пропіонової кислоти та ілсульфаніл]-2-метилпропіонової кислоти, 2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-32-{2-[3-(4-ізопропілфеніл)-1-(3-гексил)уреїдо]інданфлюор-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}5-ілсульфаніл}-2-метилпропіонової кислоти, 2-метилпропіонової кислоти. 2-метил-2-{2-[1-бутил-3-(432. Фармацевтична композиція, яка містить як трифлюорметоксифеніл)уреїдо]індан-5активний інгредієн т сполук у за п. 1, 20, 27, 28, 30 ілсульфаніл}пропіонової кислоти, чи 31. 2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]33. Спосіб лік ування чи ін гібування розви тку 3-метокси-5,6,7,8-тетрагідронафталін-2PPAR-аль фа-медійовано ї хвороби, який включає ілсульфаніл}-2-метилпропіонової кислоти, введення пацієнту, що потребує лікування, фар2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3мацевтично е фекти вної кількості композиції, яка флюор-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}містить сполук у за п. 1, 20, 27, 28 чи 31. 2-метилпропіонової кислоти, 34. Спосіб за п. 33, у якому зазначену PPAR2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3альфа-медійовану хворобу вибирають з дисліпіхлор-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2демії та серцево-судинних хвороб. метилпропіонової кислоти, 35. Спосіб за п. 34, у якому зазначена хвороба є 2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3дисліпідемією. бром-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-23 6. Сп осі б за п . 34 , у я ком у заз на чен у ди сліметилпропіонової кислоти, пі демі ю ви бир ають з гіперліпідемії фази І, пере2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]-3дклінічної гіперліпідемії, гіперліпідемії фази II, гіметил-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}перхолестеринемії, гіпо-HDL-холестеринемії та 2-метилпропіонової кислоти та гіпертригліцеридемії. 2-метил-2-{2-[1-гексил-3-(43 7 . С по сіб з а п . 34 , у як ом у за зна чен а се ртрифлюорметоксифеніл)уреїдо]індан-5це во -суди нн а хво ро ба є атеросклерозом, ішеілсульфаніл}пропіонової кислоти. мічною хворобою серця, коронарною хворобою 30. Сполука за п. 1, вибрана з: чи гіпертензією. 2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]38. Спосіб за п. 33, 35 чи 36, який додатково 5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2включа є стадію введення пацієнту спільно ефекметилпропіонової кислоти, тивної кількості агента зниження рівня ліпідів. 2-{6-[3-(4-трифлюорметоксифеніл)уреїдо]-5,6,7,839. С по сі б за п . 33 , 35 , 36 чи 38 , як ий до да ттетрагідронафталін-2-ілсульфаніл}-2ко во включа є ста ді ю введення паці єн ту спільметилпропіонової кислоти, но е фек ти вно ї кількості а ген та зн иження кро2-{2-[1-етил-3-(4в'яно го тиску. трифлюорметоксифеніл)уреїдо]індан-5ілсульфаніл}-2-метилпропіонової кислоти, Ця заявка не є попередньою [патентною заявкою США №60/419935, поданою 21 жовтня 2002р.], та попередньою [патентною заявкою США №60/495270, поданою 15 серпня 2003p., під назвою "Заміщені тетраліни та індани"]. Винахід стосується заміщених тетралінових та інданових похідних, композицій, що їх містять, та способів їхнього використання. Альфа-форма пероксисомального проліфератор-активованого рецептора (PPAR-альфа), що є 7 80297 8 членом сімейства ядерних рецепторів, група лічає С3-5-циклоалкіл, феніл, феніл-О-, феніл-S- чи ганд-активованих транскрипційних факторів, є не5-6-членний одновалентний гетероциклічний раобхідним транскрипційним фактором, який регудикал з 1-2 гетероатомами, вибраними з Ν, Ο та S; лює гени, пов'язані з метаболізмом жирних кислот Υ позначає NH, NH-CH2 чи О; та дією інсуліну. кожний з R5 та R6 незалежно вибирають з Н, Рецептори PPAR-альфа присутні переважно у С1-6-алкілу, галоїду, ціаногрупи, нітрогрупи, COR11, печінці. Гени, регульовані PPAR-альфа, включаCOOR11, С1- 4-алкоксигрупи, С1-4-алкілтіогрупи, гідють ферменти, які беруть участь у бета-окисненні роксильної групи, фенілу, NR11R 12 та 5-6-членного жирних кислот, транспортний протеїн жирних кисодновалентного гетероциклічного радикала з 1-2 лот печінки та апо-А1, що є важливим компоненгетероатомами, вибраними з Ν, Ο та S; том ліпопротеїдів високої густини (HDL). СелектиR6 вибирають з С1-6-алкілу, галоїду, ціаногрувні високоафінні агоністи PPAR-альфа посилюють пи, нітрогрупи, COR13, COOR13 , С1-4-алкоксигрупи, печінкове окиснення жирних кислот, що у свою С1-4-алкілтіогрупи, гідроксильної групи, фенілу, чергу знижує рівні циркулюючих тригліцеридів та NR13R11 та 5-6-членного одновалентного гетероцивільних жирних кислот. Зниження циркулюючих клічного радикала з 1-2 гетероатомами, вибранитригліцеридів може медіювати спостережуване ми з Ν, Ο та S; зниження чи поліпшення інсулінорезистентності у крім того, R5 та R6 або R6 та R7 можуть разом інсулінрезистентних чи діабетичних тварин, які утворювати двовалентний фрагмент, насичений одержували агоністи PPAR-альфа. Курс лікування чи ненасичений, вибраний з -(СН2)3-, -(СН2)4- та такими речовинами у тваринних моделях ожиріння CH1-2)pN(CH1-2)q , асоційований з втратою ваги. Фібрати, які є відоp дорівнює 0-2 і q дорівнює 1-3, де сума (р+q) мими засобами лікування гіперліпідемії, є слабкидорівнює щонайменше 2; ми агоністами PPAR-альфа. кожний з R9 та R10 незалежно позначає С 1-5Приклади відомих агоністів PPAR-альфа, що алкіл; використовуються з різною метою при гіперліпідекожний з R11, R12, R13 та R14 незалежно познамії, діабеті чи атеросклерозі, включають фібрати, чає Η чи С 1-6-алкіл; такі як фенофібрат (Fournier), гемфіброзил (Parkeде кожний із зазначених вище гідрокарбільних Davis/Pfizer, Mylan, Watson), клофібрат (Wyethта гетерокарбільних фрагментів може бути заміAyerst, Novopharm), безафібрат та ципрофібрат і щений 1-3 замісниками, незалежно вибраними з F, уреідофібрати, такі як GW 7647, GW 9578 та GW СІ, Вr, І, аміногрупи, метилу, етилу, гідроксильної 9820 (GlaxoSmithKline). групи, нітрогрупи, ціаногрупи та метоксигрупи. Винахід стосується сполук нижченаведеної Винахід також розкриває композиції, які вклюформули (І): чають одну чи кілька сполук формули (І) та фармацевтичний носій чи ексципієнт. Ці композиції та описані нижче способи можуть додатково включати фармацевтично активні агенти, такі як агенти зниження рівня ліпідів чи агенти зниження кров'яного тиску, або обидва ці види агентів. Інший аспект винаходу включає способи використання розкритих сполук чи композицій у різних способах профілактики, лікування чи інгібування розвитку хвороби, медійованої PPAR-альфа. Приклади PPAR-альфа-медійованих хвороб включаабо її фармацевтично прийнятної солі, С1-5ють дисліпідемію та атеросклероз. Дисліпідемія складного ефіру чи С1- 5-аміду, де кожний з R1 та R2 включає гіпертригліцеридемію, гіперхолестериненезалежно позначає Н, С1-6-алкіл, (CH2)mNRaRb, мію, змішану гіперліпідемію та гіпo-HDL(CH2)mOR8, (CH2)mNH(CO)R8 чи (CH2)mCO2R8, де холестеринемію. Наприклад, дисліпідемія може кожний з Ra, Rb, та R8 незалежно позначає Η чи С 1бути одним чи кількома з таких станів: низькі HDL 6-алкіл, або R 1 та R 2 разом з атомом карбону, до (200мг/дл) якого вони приєднані, утворюють С3-7-циклоалкіл; та високі LDL (>150мг/дл). m має значення від 1 до 6; Додаткові ознаки та переваги винаходу будуть n дорівнює 1 чи 2; зрозумілі з наведених далі детального опису, приX позначає О чи S; причому X знаходиться в кладів та формули винаходу. положенні 5 чи 6, якщо n дорівнює 1; і X знахоА. Терміни диться в положенні 6 чи 7, якщо n дорівнює 2; Зазначені далі терміни визначаються нижче та R3 позначає Н, феніл, С1-3-алкоксигрупу, С 1-3за їхнім застосуванням у даному описі. алкілтіогрупу, галоїд, ціаногрупу, С1-6-алкіл, нітро"Алкіл" включає необов'язково заміщені лінійні груп у, NR 9R10, NHCOR10, CONHR10 та COOR10; і R3 та розгалужені вуглеводні, у яких видалений щознаходиться в орто- чи мета-положенні стосовно найменше один гідроген для утворення радикальX; ної групи. Алкільні групи включають метил, етил, R4 позначає Η чи -(С1-5-алкілен)-R15, де R15 попропіл, ізопропіл, бутил, ізобутил, т-бутил, 1значає Н, С1-7-алкіл, [ді-(С1-2-алкіл)аміно]-(С1-6метилпропіл, пентил, ізопентил, втор-пентил, гекалкілен), (С1-3-алкоксіацил)-(С1-6-алкілен), С1-6сил, гептил, октил і т.д. Алкіл включає циклоалкіл, алкоксигрупу, С3-7-алкеніл чи С 3-8-алкініл, причому такий як циклопропіл, циклобутил, циклопентил, та R4 містить не більш ніж 9 атомів карбону; R4 може циклогексил. також позначати -(С -алкілен)-R , де R позна1-5 15 15 9 80297 10 "Алкеніл" включає необов'язково заміщені ліОдновалентний гетероциклічний радикал танійні та розгалужені вуглеводневі радикали, такі як кож включає сконденсовані, наприклад, біциклічні, названі вище, із щонайменше одним карбонкільця, такі як необов'язково конденсовані з некарбоновим подвійним зв'язком (sp2). Алкеніли обов'язково заміщеним карбоциклічним чи гетеровключають етеніл (або вініл), проп-1-еніл, проп-2циклічним п'яти- чи шестичленним ароматичним еніл (або аліл), ізопропеніл (або 1-метилвініл), буткільцем. Наприклад, "гетероарил" включає необо1-еніл, бут-2-еніл, бутадієніли, пентеніли, гексав'язково заміщене шестичленне гетероароматичне 2,4-дієніл і т.д. Вуглеводневі радикали, що мають кільце, що містить 1, 2 чи 3 атоми нітрогену, конзмішані подвійні зв'язки та потрійні зв'язки, такі як денсоване з необов'язково заміщеним п'яти- чи 2-пентен-4-ініл, вважаються тут такими, що налешестичленним карбоциклічним чи гетероциклічним жать до алкінілів. Алкеніл включає циклоалкеніл. ароматичним кільцем. Зазначене гетероциклічне Цис- та транс- чи (Е)- та (Ζ)-форми входять до п'яти- чи шестичленне ароматичне кільце, сконобсягу винаходу. денсоване із зазначеним п'яти- чи шестичленним "Алкініл" включає необов'язково заміщені ліароматичним кільцем, може містити 1, 2 чи 3 а тонійні та розгалужені вуглеводневі радикали, такі як ми нітрогену, якщо воно є шестичленним кільцем, названі вище, із щонайменше одним карбонабо 1, 2 чи 3 гетероатоми, вибраних з оксигену, карбоновим потрійним зв'язком (sp). Алкініли нітрогену та сульфур у, якщо воно є п'ятичленним включають етиніл, пропініли, бутиніли та пентинікільцем. ли. Вуглеводневі радикали, які мають змішані поПриклади одновалентних гетероциклічних радвійні зв'язки та потрійні зв'язки, такі як 2-пентен-4дикалів включають тіазоліл, фурил, тієніл, піраніл, ініл, вважаються тут такими, що належать до алкіізобензофураніл, піроліл, імідазоліл, піразоліл, нілів. Алкініл не включає циклоалкініл. ізотіазоліл, ізоксазоліл, піридил, піразиніл, піримі"Алкокси" включає необов'язково заміщену лідиніл, піридазиніл, індолізиніл, ізоіндоліл, індоліл, нійну чи розгалужену алкільну груп у з термінальіндазоліл, пуриніл, хіноліл, фуразаніл, піролідиніл, ним оксигеном, який з'єднує алкільну гр упу з решпіролініл, імідазолідиніл, імідазолініл, піразолідитою молекули. Алкоксигрупи включають ніл, піразолініл, піперидил, піперазиніл, індолініл метоксигрупу, етоксигрупу, пропоксигрупу, ізопрота морфолініл. Наприклад, кращі одновалентні поксигрупу, бутоксигруп у, т-бутоксигрупу, пентокгетероциклічні радикали чи гетероциклічні радикасигрупу і т.д. "Аміноалкіл", "тіоалкіл" та "сульфоніли включають морфолініл, піперазиніл, піролідилалкіл" є аналогічними алкоксигрупі, з ніл, піридил, циклогексиліміногрупу, тієніл і, ще термінальним атомом оксигену алкоксигрупи, закраще, піперидил чи морфолініл. міщеним, відповідно, на NH (або NR), S та SО2. Ілюстративними прикладами гетероарилу є тіГетероалкіл включає алкоксигрупу, аміноалкіл, єніл, фураніл, піроліл, імідазоліл, оксазоліл, тіазотіоалкіл і т.д. ліл, бензотієніл, бензофураніл, бензімідазоліл, "Арил" включає феніл, нафтил, бі феніліл, тетбензоксазоліл, бензотіазоліл. рагідронафтил, інденіл і т.д., причому будь-який з "Ацил" стосується карбонільної групи, приєдних може бути необов'язково заміщеним. Арил наної до атома гідрогену (тобто, формільної групи) також включає арилалкільні групи, такі як бензил, або до необов'язково заміщеного алкільного чи фенетил та фенілпропіл. Арил включає кільцеву алкенільного ланцюга, або до одновалентного систему, яка містить необов'язково заміщене 6гетероциклічного радикала. членне карбоциклічне ароматичне кільце, причому "Галоїд" чи "галоген" включає флюор, хлор, зазначена система може бути біциклічною, з місбром та йод, краще, флюор чи хлор, як замісник точком та/або сконденсованою. Система може на алкільній групі, з одним чи кількома галоїдними включати кільця, які є ароматичними, або частково атомами, такі як трифлюорметил, трифлюорметочи повністю насиченими. Приклади кільцевих сисксигрупа, трифлюорметилтіогрупа, дифлюорметотем включають інденіл, пенталеніл, 1-4ксигрупа чи флюорметилтіогрупа. дигідронафтил, інданіл, бензімідазоліл, бензотіо"Алкандіїл" чи "алкілен" позначає необов'язкофеніл, індоліл, бензофураніл, ізохінолініл і т.д. во заміщені бівалентні алканові радикали з ліній"Одновалентний гетероциклічний радикал" ним чи розгалуженим ланцюгом, такі як, напривключає необов'язково заміщені ароматичні та клад, метилен, етилен, пропілен, бутилен, неароматичні кільця, які містять у кільці атоми капентилен чи гексилен. рбону та щонайменше один гетероатом (О, S, N) "Алкендіїл" позначає, аналогічно до вищевкачи фрагмент, що містить гетероатом (SO2, CO, заного, необов'язково заміщені бівалентні алкенові CONH, COO). Якщо не вказано інше, гетероциклірадикали з лінійним чи розгалуженим ланцюгом, чний радикал може мати валентний зв'язок, який такі як, наприклад, пропенілен, бутенілен, пентеніз'єднує його з рештою молекули через атом карлен чи гексенілен. В таких радикалах атом карбобону, так як у 3-фурилі чи 2-імідазолілі, чи через ну, з'єднаний з нітрогеном, краще, не повинен бути гетероатом, так як у N-піперидилі чи 1-піразолілі. ненасиченим. Краще, моноциклічний одновалентний гетероцик"Ароїл" стосується карбонільної групи, приєдлічний радикал має від 5 до 7 кільцевих атомів, наної до необов'язково заміщеної арильної чи геабо 5-6 кільцевих атомів; у кільці може бути від 1 тероарильної групи, де арил та гетероарил відподо 5 гетероатомів чи гетероатомних фрагментів, відають наведеним вище визначенням. Зокрема, краще, від 1 до 3, чи 1-2. Одновалентний гетеробензоїл є феніл карбонілом. циклічний радикал може бути насиченим, ненасиВ тому значенні, що використовується тут, два ченим, ароматичним (наприклад, гетероарил), радикали, разом з атомом (атомами) до якого вони неароматичним чи сконденсованим. приєднані, можуть утворювати необов'язково за 11 80297 12 міщене 4-7-, 5-7- чи 5-6-членне карбоциклічне чи полегшення симптомів стану чи розладу, що лікугетероциклічне кільце, яке може бути насиченим, ється. ненасиченим чи ароматичним. Зазначені кільця Зробимо три загальні зауваження щодо різних можуть відповідати визначенням, наведеним вище радикалів в цьому описі та формулі винаходу. Пеу розділі Суть винаходу. Конкретні приклади таких рше зауваження стосується валентності. Як для кілець наведені у наступному розділі. усі х вуглеводневих радикалів, будь то насичені, "Фармацевтично прийнятні солі, складні ефіри ненасичені чи ароматичні, циклічні чи ні, лінійні чи та аміди" включають карбоксилатні солі, солі прирозгалужені, а також, аналогічно, усіх гетероциклієднання амінокислот, складні ефіри та аміди, які чних радикалів, кожний радикал включає заміщені забезпечують прийнятне співвідношення корадикали цього типу та моновалентні, бівалентні ристь/ризик, є фармакологічно ефективними та та багатовалентні радикали, як вказано у контексті придатними для введення в контакт з тканинами формули винаходу. Контекст вказує на те, що запацієнтів без неналежної токсичності, подразнення місник є алкіленом чи вуглеводневим радикалом з чи алергічної реакції. Ці солі, складні ефіри та амівидаленими щонайменше двома атомами гідрогеди можуть бути, наприклад, солямі, складними ну (бівалентний) чи більшою кількістю атомів гідефірами та амідами, які містять С1-8-алкільний, С3рогену (багатовалентний). Прикладом бівалентного радикала, що з'єднує дві частини молекули, є Υ 8-циклоалкільний, арильний, С 2-10-гетероарильний чи С2-10-неароматичний гетероциклічний радикал. у формулі (І), який приєднує феніл, заміщений R5, Солі, вільні кислоти та складні ефіри є кращими, R6, та R7 , до решти молекули. ніж аміди, утворені термінальною карбоксилатною По-друге, радикали чи структурні фрагменти в групою/гр упою карбонової кислоти у лівій частині тому значенні, що використовується тут, розуміформули (І). Приклади солей включають гідроються як такі, що включають заміщені радикали чи бромід, гідрохлорид, сульфат, бісульфат, нітрат, структурні фрагменти. Гідрокарбіли включають ацетат, оксалат, валерат, олеат, пальмітат, стеамоновалентні радикали, що містять карбон та гідрат, лаурат, борат, бензоат, лактат, фосфат, тозироген, такі як алкіл, алкеніл, алкініл, циклоалкіл та лат, цитрат, малеат, фумарат, сукцинат, тартрат, циклоалкеніл (будь то ароматичні чи ненасичені), нафтилат, мезилат, глюкогептонат, лактобіонат та а також відповідні двовалентні (або багатовалентлаурилсульфонат. Вони можуть включати катіони ні) радикали, такі як алкілен, алкенілен, фенілен і лужних та лужноземельних металів, таких як нат.д. Гетерокарбіли включають моновалентні та трій, калій, кальцій та магній, а також нетоксичні двовалентні (або багатовалентні) радикали, які амонієві, четвертинні амонієві та амінні катіони, містять карбон, необов'язково, гідроген, та щотакі як тетраметиламоній, метиламін, триметиланайменше один гетероатом. Приклади моноваленмін та етиламін. [Див., наприклад, S.M. Berge, et тних ге терокарбілів включають ацил, ацилоксигруal., "Pharmaceutical Salts," J. Pharm. Sci., 1977, пу, алкоксіацил, одновалентний гетероциклічний 66:1-19], яку включено сюди за посиланням. Прирадикал, гетероарил, ароїл, бензоїл, діалкіламіноклади фармацевтично прийнятних амідів за винагруп у, гідроксіалкіл і т.д. При використанні "алкілу" ходом включають похідні аміаку, первинних С1-6як прикладу, "алкіл" слід розуміти як такий, що алкіламінів та вторинних ді-(С1-5-алкіл)амінів. Втовключає заміщений алкіл, який має одне чи кілька ринні аміни включають 5- чи 6-членні гетероциклізаміщень, наприклад, від 1 до 5, від 1 до 3, чи від 2 чні чи гетероароматичні кільцеві фрагменти, які до 4 замісників. Замісники можуть бути однаковимістять щонайменше один атом нітрогену та, неми (дві гідроксильні групи, диметил), подібними обов'язково, 1-2 додаткові гетероатоми. Кращі (хлорфлюор), чи різними (хлорбензил- чи аміноаміди є похідними аміаку, первинних С1-3метилзаміщені). Приклади заміщеного алкілу алкіламінів та ді-(С1-2-алкіл)амінів. Приклади фарвключають галоїдалкіл (такий як флюорметил, мацевтично прийнятних складних ефірів за винахлорметил, дифлюорметил, перхлорметил, 2ходом включають складні ефіри, які містять С1-7брометил, трифлюорметил та 3-йодциклопентил), алкільні, С5-7-циклоалкільні, фенільні та феніл-(С1гідроксіалкіл (такий як гідрокси метил, гідроксіетил, 2-гідроксипропіл, аміноалкіл (такий як амінометил, 6)-алкільні радикали. Кращі складні ефіри включають метилові та етилові складні ефіри. 2-аміноетил, 3-амінопропіл та 2-амінопропіл), ніт"Пацієнт" чи "суб'єкт" включає ссавців, таких як роалкіл, алкілалкіл і т.д. Ді-(С1-6-алкіл)аміногрупа люді та тварини (собаки, кішки, коні, пацюки, кролі, включає незалежно вибрані алкільні групи, з утвомиші, не-людиноподібні примати), які потребують ренням, наприклад, метилпропіламіногрупи та спостереження, проведення експерименту, лікуізопропілметиламіногрупи, а крім того, діалкіламівання чи профілактики у зв'язку з відповідною хвоногрупи, що мають дві однакові алкільні групи, такі робою чи станом. Краще, пацієнт чи суб'єкт є люяк диметиламіногрупа чи діетиламіногрупа. диною. По-третє, передбачаються лише стабільні "Композиція" включає продукт, який містить сполуки. Наприклад, у випадку присутності визначені інгредієнти у визначеній кількості, а таNR11R12-гр упи, де R може позначати алкенільну кож будь-який продукт, утворений комбінаціями груп у, подвійний зв'язок віддалений від нітрогену визначених інгредієнтів у визначеній кількості. щонайменше на один атом карбону для уникнення "Терапевтично ефективна кількість" чи "ефекутворення енаміну. Аналогічно, якщо -(CH2)p-Nтивна кількість" позначає таку кількість активної (CH2)q - може бути ненасиченим, відповідний атом сполуки чи фармацевтичного агента, що викликає (атоми) гідрогену може бути включений чи опущебіологічну чи медичну відповідь у тканинній систений, як, наприклад, у -(CH2)-N=(CH)-(CH 2)- чи мі, тварині чи людині, бажану для дослідника, ве(CH2)-NH-(CH)=(CH)-. теринара, лікаря чи іншого клініциста, яка включає Сполуки за винаходом далі описані у наступ 13 80297 14 ному розділі. В. Сполуки Даний винахід розкриває композиції, що містять, та способи використання, сполук формули (І), які описані вище у розділі Суть винаходу. Приклади включають такі сполуки, у яких: (а) один з R 1 та R2 позначає метил чи етил; (b) у яких кожний з Етиловий складний ефір 3-(1-карбокси-1R1 та R2 позначає метил; (с) R1 та R2 разом познаметилетилсульфаніл)-7-[1-етил-3-(4чають циклобутил чи циклопентил; (d) R3 позначає трифлюорметоксифеніл)уреїдо]-5,6,7,8Η; (e) R4 позначає Η чи С2-7-алкіл; (e) R4 позначає тетрагідронафталін-2-карбонової кислоти, Η чи С2-5-алкіл; (f) R4 позначає етил; (g) R4 позначає Η; (h) n дорівнює 1; (і) n дорівнює 2; j) Υ позначає NHCH2; (k) Υ позначає ΝΗ; (І) Χ позначає S; (m) X позначає Ο; (n) щонайменше один з R5 та R7 позначає Η; (о) R6 позначає С1-4-алкіл, галоїдметоксигрупу чи галоїдтіометоксигрупу; (р) R6 позначає т-бутил, ізопропіл, трифлюорметил, трифлюорметоксигрупу, трифлюортіометоксигрупу, ди флюор2-{6-[етил-(4метоксигрупу чи диметиламіногрупу; (q) R3 познатрифлюорметоксифеноксикарбоніл)аміно]-3чає Η, R4 позначає С2-7-алкіл, і Υ позначає NH; (r) флюор-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}R4 позначає С2-5-алкіл; (s) R6 позначає циклопропі2-метилπропіонова кислота, лметил, ізопропіл, ізобутил, метилетиламіногрупу 2-{6-[1-етил-3-(4чи діетиламіногрупу; (t) (S)-енантіомер у положенні трифлюорметоксифеніл)уреїдо]-3-метокси-5,6,7,8С-2 індану чи тетраліну; (u) (R)-енантіомер у полотетрагідро-нафталін-2-ілсульфаніл}-2женні С-2 індану чи тетраліну; (ν) у яких R15 познаметилпропіонова кислота, чає С1-7-алкіл, [ді-(С1-2-алкіл)аміно]-(С1-6-алкілен), 2-{6-[1-етил-3-(4(С1-3-алкоксіацил)-(С1-6-алкілен), С1-5-алкоксигрупу, трифлюорметоксифеніл)уреїдо]-3-хлор-5,6,7,8С3-7-алкеніл чи С 3-8-алкініл; (w) R6 позначає трифтетрагідро-нафталін-2-ілсульфаніл}-2люорметилтіогрупу чи трифлюорметоксигрупу; чи метилпропіонова кислота, (х) комбінації наведених вище ознак. 2-{6-[1-етил-3-(4Додатково до кращих сполук належать: трифлюорметоксифеніл)уреїдо]-3-бром-5,6,7,8тетрагідро-нафталін-2-ілсульфаніл}-2метилпропіонова кислота, 2-{6-[1-етил-3-(4трифлюорметоксифеніл)уреїдо]-3-метил-5,6,7,8тетрагідро-нафталін-2-ілсульфаніл}-2метилпропіонова кислота, 2-{6-[1-етил-3-(4трифлюорметоксифеніл)уреїдо]-32-{6-[1-етил-3-(4трифлюорметокси-5,6,7,8-тетрагідронафталін-2трифлюорметоксифеніл)уреїдо]-1,4-дифлюорілсульфаніл}-2-метилпропіонова кислота, 5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-22-{6-[1-етил-3-(4-гідроксифеніл)уреїдо]-5,6,7,8метилпропіонова кислота, тетрагідронафталін-2-ілсульфаніл}-2метилпропіонова кислота, 2-{6-[4-амінофеніл)-1-етилуреїдо]-5,6,7,8тетрагідронафталін-2-ілсульфаніл}-2метилпропіонова кислота. Найкращі сполуки вибирають з: 2-{6-[1-етил-3-(42-{4-хлор-6-[1-етил-3-(4трифлюорметоксифеніл)уреїдо]-5,6,7,8трифлюорметоксифеніл)уреїдо]-1-флюор-5,6,7,8тетрагідронафталін-2-ілсульфаніл}-2тетрагідронафталін-2-ілсульфаніл}-2метилпропіонової кислоти; метилпропіонова кислота, 2-{6-[3-(4-трифлюорметоксифеніл)уреїдо]5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2метилпропіонової кислоти; 2-{2-[1-етил-3-(4трифлюорметоксифеніл)уреїдо]індан-5ілсульфаніл}-2-метил-пропіонової кислоти; 2-{2-[1-етил-3-(4трифлюорметилсульфанілфеніл)уреїдо]індан-52-{3-етил-6-[1-етил-3-(4ілсульфаніл}-2-метилпропіонової кислоти; трифлюорметоксифеніл)уреїдо]-5,6,7,82-{6-[1-етил-3-(4тетрагідронафталін-2-ілсульфаніл}-2трифлюорметоксифеніл)уреїдо]-3-флюор-5,6,7,8метилпропіонова кислота, тетрагідро-нафталін-2-ілсульфаніл}-2метилпропіонової кислоти; і 2-метил-2-{2-[1-пропіл-3-(4 15 80297 16 трифлюорметоксифеніл)уреїдо]індан-5Карбамати ілсульфаніл}пропіонової кислоти. Приклади метил- та етилкарбаматів включаСпоріднені сполуки ють метил- та етил-, 9-флуоренілметил-, та 4Винахід пропонує розкриті сполуки та близько метоксифенацилкарбмати. споріднені, фармацевтично прийнятні форми розЗаміщений етил критих сполук, такі як їхні солі, складні ефіри, аміПриклади заміщених етилкарбаматів включади, кислоти, гідрати чи сольватовані форми; масють 2,2,2-трихлоретил, 2-фенілетил, т-бутил, вініл, ковані чи захищені форми; та рацемічні суміші, або аліл, 1-ізопропілаліл, бензил, п-метоксибензил, пенантіомерно чи оптично чисті форми. Споріднені нітробензил, п-бромбензил, п-хлорбензил, 2,4сполуки включають також сполуки за винаходом, дихлорбензил та дифенілметил. які були модифіковані для того, щоб уможливити Фотолітичне розщеплення їхнє де тектування, наприклад, ізотопно мічені за Приклади груп, придатних для фотолітичного допомогою 18F для використання як зонда у позитрозщеплення, включають м-нітрофеніл, 3,5ронній емісійній томографії (PET) чи однофотонній диметоксибензил, о-нітробензил, 3,4-диметокси-6емісійній комп'ютерній томографії (SPECT). нітробензил та феніл(о-нітрофеніл)метил. Винахід також включає розкриті сполуки, які Аміди мають одну чи кілька функціональних гр уп (наприПриклади амідів включають N-форміл, Nклад, гідроксильну, аміногрупу чи карбоксильну), ацетил, N-трихлорацетил, N-трифлюорацетил, Nмаскованих захисною групою. [Див., наприклад, фенілацетил, N-3-фенілпропіоніл, N-піколіноїл, NGreene and Wuts, Protective Groups in Organic 3-піридилкарбоксамід, N-бензоїл, N-пSynthesis. 3rd ed., (1999) John Wiley & Sons, NY]. фенілбензоїл та фталоїл. Деякі з цих маскованих чи захищених сполук є Захист для карбонільної групи фармацевтично прийнятними; інші є корисними як Циклічні ацеталі та кеталі проміжні сполуки. Синтезовані проміжні сполуки і Приклади циклічних ацеталей та кеталей розкриті тут процеси, та їхні невеликі модифікації, включають 1,3-діоксани та 5-метилен-1,3-діоксан. також входять до обсягу винаходу. Захист для карбоксильної групи Захисні групи гідроксилу Складні ефіри Захист для гідроксильних груп включає метилЗаміщені метилові складні ефіри ові прості ефіри, заміщені метилові ефіри, заміщеПриклади заміщених метилових складних ефіні етилові ефіри, заміщені бензилові ефіри та сирів включають 9-флуоренілметиловий, метокси лілові прості ефіри. метиловий, метилтіометиловий, метоксіетоксимеЗаміщені метилові ефіри тиловий, 2-(триметилсиліл)етоксиметиловий, бенПриклади заміщених простих метилових ефізоксиметиловий, фенациловий, прів включають метоксиметил, метилтіометил, тбромфенациловий, a-метилфенациловий та пбутилтіометил, бензокси метил, пметоксифенациловий. Приклади складних ефірів метоксибензоксиметил, (4-метоксифенокси)метил, також включають лінійні чи розгалужені алкільні т-бутоксиметил. складні ефіри, такі як трет-бутиловий, етиловий, Заміщені етилові ефіри пропіловий, ізопропіловий та бутиловий. Приклади заміщених простих етилових ефірів Заміщені бензилові складні ефіри включають 1-етоксіетил, 1-метил-1-метоксіетил, 1Приклади заміщених бензилових складних метил-1-бензоксіетил, 2,2,2-трихлоретил, т-бутил, ефірів включають трифенілметиловий, дифенілаліл, п-хлорфеніл, п-метоксифеніл та бензил. метиловий, 9-антрилметиловий, 2,4,6Заміщені бензилові ефіри триметилбензиловий, п-бромбензиловий, оПриклади заміщених бензилових ефірів вклюнітробензиловий, п-нітробензиловий, пчають п-метоксибензил, 3,4-диметоксибензил, пметоксибензиловий, 2,6-диметоксибензиловий, галоїдбензил, 2,6-дихлорбензил, п-ціанобензил, ппіпероніловий, 4-піколіловий та п-Р-бензиловий. фенілбензил, дифенілметил. Силілові складні ефіри Складні ефіри Приклади силілових складних ефірів включаКрім простих ефірів, гідроксильна група може ють триметилсиліловий, триетилсиліловий, тбути захищеною складним ефіром. Приклади бутилдиметилсиліловий, ізопропілдиметилсилілоскладних ефірів включають форміат, бензоїлфорвий, фенілдиметилсиліловий та ди-тміат, ацетат, трихлорацетат, три флюорацетат, бутилметилсиліловий. метоксіацетат, феноксіацетат, пС. Способи синтезу хлорфеноксіацетат, бензоат. Винахід пропонує способи одержання розкриСульфонати тих сполук відповідно до традиційних способів Приклади сульфонатів включають сульфат, органічного синтезу, а також способів матричного метансульфонат (мезилат), бензилсульфонат та чи комбінаторного синтезу. Схеми 1-10 описують тозилат. запропоновані шляхи синтезу. Використовуючи ці Захист аміногруп Схеми, наведений нижче опис та приклади, фахіЗахист для аміногруп включає карбамати, амівець в цій області може розробити аналогічні чи ди та спеціальні NH-захисні групи. подібні способи для конкретної сполуки за винахоПриклади карбаматів включають метил- та дом. етил карбамати, заміщені етил карбамати, карбаФахівцю в цій області зрозуміло, що синтез мати, що розщеплюються у присутності допоміжсполук за даним винаходом може бути здійснений них агентів, фотолітично розщеплювані карбамашляхом придбання проміжної сполуки чи захищети, похідні типу сечовини та різні карбамати. них проміжних сполук, описаних у будь-якій з роз 17 80297 18 критих тут схем. Фахівцю в цій області далі зрозутом, таким як бутил нітрит чи ізоамілнітрит у приміло, що в ході будь-якого з процесів одержання сутності каталітичної кількості кислоти, такої як сполук за даним винаходом може бути необхідним хлористоводнева кислота чи бромистоводнева та/або бажаним захистити чутливі чи реакційнозкислота у полярному розчиннику, такому як метадатні групи на будь-якій з молекул. Це може бути нол чи простий ефір, одержують кетооксим 4. Віддосягнуто за допомогою звичайних захисних груп, новлення сполуки 4 може бути здійснене шляхом таких як описані у ["Protective groups in Organic використання придатного відновника (відновників), Synthesis", John Wiley & Sons, 1991]. Ці захисні такого як гідрид літію-алюмінію чи гідроген, та кагрупи можуть бути видалені на зручній стадії з виталізатора, такого як паладій чи платина, у придакористанням відомих фахівцям способів. тному розчиннику, такому як оцтова кислотаПриклади описаних шляхі в синтезу включають сірчана кислота, ТГФ чи метанол, при придатній Приклади синтезу 1-57. Сполуки, аналогічні цільотемпературі. Вибір способу утворення солі може вим сполукам з цих прикладів, можуть бути, і в бути легко визначений фахівцем в цій області. багатьох випадках були одержані аналогічними шляхами. Розкриті сполуки придатні для використання у фундаментальних дослідженнях та як фармацевтичні агенти, як описано у наступному розділі. Загальні рекомендації Кращий синтез сполук формули 14, де X позначає S (і R3 позначає Н) продемонстрований на Схемах 1-5. Використовувані тут абревіатури чи акроніми включають: АсОН (льодяна оцтова кислота); DCC (1,3-дициклогексилкарбодіімід); DCE (1,2дихлоретан); DIC (2диметиламіноізопропілхлориду гідрохлорид); DIEA (діізопропілетиламін); ДМФ (диметилформамід); EDC (1-(3-диметиламінопропіл)-3-етилкарбодіімід); EtOAc (етилацетат); mCPBA (3хлорпероксибензойна кислота); NMI (1метилімідазол); TEA (триетиламін); TFA (трифлюВідповідно до Схеми 3, сполука 2 чи 5 може ороцтова кислота); ТГФ (тетрагідрофуран); TMEDA бути перетворена на сполуку 12. Наприклад, якщо (Ν,Ν,Ν',Ν'-тетраметилетилендіамін). гідрохлорид рацемічного аміну обробляють основою, такою як гідрид натрію чи гідрид літію у полярному апротонному розчиннику, такому як ДМФ чи ТГФ, а потім вводять в реакцію з ангідридом, таким як фталевий ангідрид, при підвищеній температурі, може бути одержаний циклічний імід 6. Розщеплення метиларилових ефірів формули 6 до сполук формули 7 може бути здійснене з викорисВідповідно до Схеми 1, тетраліни можуть бути танням кислоти Льюїса, такої як бромід бору, хлоодержані перетворенням сполуки 1 на сполуку 2. Наприклад, метокси-2-тетралон, такий як 6рид бору, хлорид алюмінію чи триметилсилілйометокси-2-тетралон, може бути оброблений реадид, у неполярних апротонних розчинниках, таких як толуол, дихлорметан чи дихлоретан, при охогентом, таким як ацетат амонію чи аміак або гідролодженні чи без нього. Ацилювання фенолів форксиламін. Відповідний імін може бути відновлений мули 7 до сполуки формули 8 може бути здійснене придатним відновником, таким як боргідрид натрію, ціаноборгідрид натрію чи триацетоксиборгідз використанням тіокарбамоїлхлоридів, таких як рид натрію, і одержаний оксим може бути відновдиметиламінотіокарбамоїлхлорид чи діетилтіокарбамоїлхлорид, та нереакційноздатного третинного лений каталітично з використанням паладію чи аміну, такого як триетиламін, 1,8платини у полярному протонному розчиннику, тадіазабіцикло[5,4,0]ундец-7-ен чи 1,4кому як метанол, етанол чи етилацетат, з одержанням рацемічної сполуки 2. Одержання гідродіазабіцикло[2,2,2.]октан, в апротонному розчинхлоридної солі може бути легко здійснене нику, такому як дихлорметан, ДМФ чи ТГФ, при охолодженні чи без нього. Сполуки формули 8 фа хівцем в цій області. можуть бути піддані термічному перегрупуванню на сполуки формули 9 при температурі в інтервалі від 180°С до 350°С, нерозведеними у вигляді розплаву чи з використанням висококиплячих розчинників, таких як DOWTHERMÒ А (суміш бі фенілу та біфенілового ефіру, що продається, наприклад, фірмою Fluka Chemical Corp., Milwaukee, Wl, USA), Відповідно до Схеми 2, індани можуть бути Ν,Ν-диметиланілін, дифеніловий ефір чи декалін. одержані шляхом перетворення сполуки 3 на споСполуки формули 10 можуть бути одержані зі сполуку 5. Наприклад, коли метоксіінданон, такий як лук формули 9 шля хом обробки придатним нукле5-метоксі-1-інданон, обробляють ацилюючим аген 19 80297 20 офілом, таким як гідразин, динатрійсульфід чи метиламін у придатному полярному розчиннику, Аналогічно, сполуки формули 16 можуть бути такому як етанол чи ТГФ, при підвищеній темпераодержані зі сполуки формули 11 ацилюванням турі. Перетворення сполук формули 10 на сполуки первинного аміну, як зображено на Схемі 5, з одеформули 11 може бути здійснене з використанням ржанням сполук формули 15. Вибір способів знятпридатного реагента, такого як гідроксид калію у тя захисту для одержання сполук формули 16 моспиртовому розчиннику, такому як етанол чи меже бути легко визначений фахівцем в цій області. танол, чи гідрид літію-алюмінію у ТГФ чи ефірі, з наступним алкілуванням за допомогою відповідно заміщеного алкілгалогеніду, такого як трет-бутил2-бромізобутират, етилбромацетат чи етил-2бромбутират, та відновника, такого як боргідрид літію чи боргідрид натрію. Сполуки формули 11 Сполука формули 18 може бути одержана зі можуть бути заміщені з утворенням сполук форсполуки формули 10, як продемонстровано на мули 12 за допомогою карбонової кислоти чи хлоСхемі 6. Наприклад, сполука формули 10 може рангідриду кислоти та придатного відновника, табути оброблена етилформіатом чи форміатом кого як боран-ТГФ чи боран-диметилсульфід, з амонію, нерозведеними чи у присутності придатвикористанням апротонних розчинників, таких як ного розчинника, такого як дихлорметан чи дихлоТГФ, дихлорметан чи гексани. Альтернативно, ретан, з нагріванням чи без нього, з одержанням заміщення може бути здійснене з використанням сполуки формули 17. Сполуки формули 17 можуть альдегіду та відновника, такого як ціаноборгідрид бути перетворені на сполуки формули 18 шляхом натрію чи триацетоксиборгідрид натрію, у придатвикористання придатного реагента, такого як гідних апротонних розчинниках, таких як ТГФ, дихлорид літію-алюмінію у придатному розчиннику, тарметан чи дихлоретан. кому як ТГФ чи ефір, з наступним алкілуванням з використанням відповідно заміщеного алкілгалоїду, такого як трет-бутил-2-бромізобутират, етилбромацетат чи етил-2-бромбутират, та відновника, такого як боргідрид літію чи боргідрид натрію. Відповідно до Схеми 4, сполуки формули 13 можуть бути одержані зі сполук формули 12 шляхом ацилювання вторинного аміну з арилоцтовою кислотою, з використанням тіонілхлориду чи оксалілхлориду, нерозведеними або в толуолі чи дихлорметані, з каталітичною кількістю ДМФ чи без неї. Альтернативно, сполучення можна провести з використанням стандартних умов пептидного синтезу, таких як з використанням EDC, DCC чи DIC у дихлорметані. Якщо Υ = NH чи О, то для одержання сполук формули 13 можуть бути використані арилізоціанат чи арилхлорформіат, відповідно, у неполярному апротонному розчиннику, такому як ТГФ, дихлорметан чи гексани. Вибір способів зняття захисту для одержання сполук формули 14 може бути легко визначений фахівцем в цій області. Кращий синтез сполуки формули 21, у якій X позначає О (і R3 позначає Н), продемонстрований на Схемі 7. Наприклад, якщо ацилюють сполуки формули 2 чи 5 карбоновою кислотою чи хлорангідридом кислоти, як описано вище, то одержують сполуки формули 19. Розщеплення метиларилових ефірів формули 19 до сполуки формули 20 може бути здійснене з використанням кислоти Льюїса, такої як бромід бору, хлорид бору, хлорид алюмінію чи триметилсилілйодид у неполярних апротонних розчинниках, таких як толуол, ди хлорметан чи дихлоретан, при охолодженні чи без нього. Сполуки формули можуть бути перетворені на сполуки формули 21 шляхом обробки придатною основою, такою як карбонат калію, карбонат цезію чи гідроксид калію, та відповідно заміщеним алкіл галоїдом, таким як трет-бутил-2-бромізобутират етилбромацетат чи етил-2-бромбутират, у придатному розчиннику, такому як ДМФ чи метанол. Сполуки формули 24 можуть бути одержані зі сполук формули 22, як продемонстровано на Схе 21 80297 22 мі 8. Наприклад, сполука формули 22 може бути оброблена відповідною основою, такою як бутиллітій чи втор-бутиллітій, у придатному розчиннику, такому як ефір чи ТГФ, з використанням TMEDA і при охолодженні чи без цього, та придатного електрофілу, такого як алкілгалоїди, альдегіди чи дисульфіди, для одержання сполук формули 23. Сполуки формули 23 можуть бути перетворені на сполуки формули 24 у спосіб, аналогічний описаВідповідно до Схеми 10, сполуки формули 22 ному на Схемі 3, для перетворення сполуки 8 на можуть бути легко перетворені на сполуки формусполуку 9. ли 32а, де R5=ОСН3. Наприклад, сполуки формули 22 можуть бути оброблені придатною основою, такою як бутиллітій чи втор-бутиллітій, у придатному розчиннику, такому як ефір чи ТГФ, з використанням TMEDA та охолодження і придатного дисульфіду, такого як диметилдисульфід чи дибензилдисульфід, чи без цього, з утворенням сполук формули 33. Видалення диметиламінотіокарбамату зі сполуки формули 33 здійснюється за допомогою гідроксиду калію чи натрію у придатному розчиннику, такому як вода, метанол чи етанол, з нагріванням чи без, з утворенням сполук формули 34. Сполуки формули 34 можуть бути метиловані для одержання сполук формули 19а за допомогою метилйодиду, диметилсульфату чи діазометану у придатному розчиннику, такому як Альтернативний синтез сполуки формули 32 ДМФ, метанол чи дихлорметан, з використанням представлений на Схемі 9. Наприклад, якщо 4основи, такої як карбонат цезію чи карбонат калію, метилтіофенілоцтову кислоту, що є сполукою фочи без неї. При використані хімії, аналогічної опирмули 26, обробляють оксалілхлоридом чи тіонілсаній на Схемі 9, для перетворення сполук форхлоридом у присутності метанолу, то одержують мули 30 на сполуки формули 32, сполуки формули сполуки формули 27. Обробка сполуки формули 32а можуть бути легко синтезовані зі сполук фор27 кислотою Льюїса, такою як хлорид алюмінію, у мули 19а. хлорованому розчиннику, такому як хлороформ чи дихлоретан, у присутності алкену, такого як етилен, дає тетралони формули 28. З використанням процедури, зображеної на Схемі 1, можуть бути одержані тетраліни формули 29. Сполуки формули 29 можуть бути заміщені для одержання сполук формули 30 з використанням карбонової кислоти за описаних раніше умов проведення реакції сполучення, чи хлорангідриду кислоти з третинним 2-{6-[1-Етил-3-(4аміном, таким як діізопропілетиламін чи триетилатрифлюорметоксифенілуреїдо]-5,6,7,8мін, у придатному розчиннику, такому як дихлортетрагідронафтал-2-ілсульфаніл}-2метан чи дихлоретан. Сполука формули 30 може метилпропіонова кислота. бути перетворена на сполуку формули 31 з викоСполука 1.0 (Приклад 1) ристанням окисника, такого як mСРВА чи перекис A. 6-Ме токси-1,2,3,4-тетрагідронафталін-2водню, у придатному розчиннику, такому як метиіламіну гідрохлорид ленхлорид, з наступною обробкою сполуки форСхема 1. До розчину 6-метокси-2-тетралону мули 30 трифлюороцтовим ангідридом у розчин(10,0г; 56,7ммоль) у МеОН (400мл) додають аценику, такому як хлороформ, чи без нього, з тат амонію (65г; 0,84моль) та реакцію перемішунаступною обробкою третинним аміном, таким як ють протягом 30хв. при кімнатній температурі. До триетиламін чи діізопропілетиламін, у придатному реакції потім додають ціаноборгідрид натрію розчиннику, такому як метанол, з утворенням спо(17,8г; 0,28моль) і реакцію кип'ятять зі зворотним луки формули 31. Альтернативно, видалення захолодильником протягом 1-2год. Реакцію охолохисту тіоефірної групи у сполуках формули 30 моджують, розчинник видаляють при зниженому тисже бути здійснене з використанням основи, такої ку, залишок розводять EtOAc та додають 1Н NaOH як трет-бутилнатрійсульфід, натрій, метилтіол надля гасіння реакції. Водну фазу відокремлюють і трію, у придатному розчиннику, такому як ДМФ, Nорганічну фазу промивають Н 2О, розсолом, осуметил-2-піролідон чи аміак, для одержання сполук шають над Na2SO4, фільтрують та розчинник виформули 31. З використанням хімії, аналогічної до даляють при зниженому тиску, одержуючи сировий описаної на Схемі 3 для перетворення сполуки 10 залишок, який очищають флеш-хроматографією на сполуку 11, сполуки формули 31 можуть бути (SiO2) з елююванням СН 2СІ2/МеОН:NH4OH (10%), легко перетворені на сполуки формули 32. одержуючи 5,0г (50%) 6-метокси-1,2,3,4тетрагідронафталін-2-іламіну у вигляді маслянис 23 80297 24 тої рідини темного кольору. Через розчин названої 5,6,7,8-тетрагідронафталін-2-іловий] складний у заголовку сполуки в ефірі (100мл), охолоджений ефір диметилтіокарбамінової кислоти. до 0°С, барботують НСІ (газ.) до насичення розчиСхема 3. До 2-(6-гідрокси-1,2,3,4ну. С успензію перемішують протягом ще 30хв. при тетрагідронафталін-2-іл)ізоіндол-1,3-діону (25,4г; кімнатній температурі та розчинник випаровують 86,5ммоль), розчиненому у безводному ДМФ при зниженому тиску. Тверду речовину, що зали(200мл), додають 1,4-діазабіцикло[2.2.2]октан шилася, тритур ують з ефіром, фільтрують, проми(48,5г; 4,32моль), а потім диметиламінотіокарбавають ефіром та висушують при зниженому тиску, моїлхлорид (53,4г; 4,32моль) і розчин перемішуодержуючи 4,9г 6-метокси-1,2,3,4ють при кімнатній температурі протягом 4год. Реатетрагідронафталін-2-іламіну гідрохлориду у викцію виливають на воду з льодом (1л) та гляді білої твердої речовини. перемішують протягом 18год. Осад фільтрують, LC/MS (Рідинна хроматографія/маспромивають Н2О та висушують під вакуумом. Сиспектрометрія): C11H15NO: m/z 178 (М+1). рову тверду речовину очищають флешB. 2-(6-Метокси-1,2,3,4-тетрагідронафталін-2хроматографією (SiO2), елююючи градієнтом гекіл)ізоіндол-1,3-діон сани-EtOAc, одержуючи 30г (91%) О-[6-(1,3-діоксоСхема 3. До перемішуваної суспензії 60% NaH 1,3-дигідроізоіндол-2-іл)-5,6,7,8(6г; 0,182ммоль) у ДМФ (400мл) додають 6тетрагідронафталін-2-ілового] складного ефіру метокси-1,2,3,4-тетрагідронафталін-2-іламін (30г; диметилтіокарбамінової кислоти у вигляді білої 0,140моль) порціями при 0°С. Реакційну суміш твердої речовини. 1 нагрівають до кімнатної температури та переміН ЯМР (300МГц, CDCI3): d 7,83-7,86 (м, 2Н), шують протягом ще 1год. Додають фталевий ангі7,70-7,73 (м, 2Н), 7,07-7,10 (д, 1Н), 6,83-6,86 (м, дрид (20,7г; 0,139моль) в 1 порцію при кімнатній 2Н), 4,54-4,65 (м, 1Н), 3,60-3,69 (м, 1Н), 3,46 (с, температурі, після чого реакційну суміш перемі3Н), 3,34 (с, 3Н), 2,88-3,09 (м, 3Н), 2,64-2,78 (м, шують протягом ще 1год., а потім витримують 1Н), 1,97-2,01 (м, 1Н). 18год. при 120°С. Реакції дають охолонути до кімLC/MS: C 21H20N2O3S: m/z 381 (М+1). натної температури, розводять Н2О та екстрагують E. S-[6-(1,3-Діоксо-1,3-дигідроізоіндол-2-іл)кілька разів EtOAc. Об'єднані органічні екстракти 5,6,7,8-тетрагідронаФталін-2-іловий] складний промивають водою, розсолом, осушають над ефір диметилтіокарбамінової кислоти Na2SO4, і розчинник видаляють при зниженому Схема 3. До круглодонної колби на 50мл, обтиску. Сирову тверду речовину тритурують з Меладнаної зворотним холодильником та стрижнем ОН, фільтрують та висушують під вакуумом, одедля перемішування, попередньо нагрітої до 330°С ржуючи 29,1г (67%) 2-(6-метокси-1,2,3,4на піщаній бані, додають О-[6-(1,3-діоксо-1,3тетрагідронафталін-2-іл)ізоіндол-1,3-діону у видигідроізоіндол-2-іл)-5,6,7,8-тетрагідронафталін-2гляді білуватої твердої речовини. іловий] складний ефір диметилтіокарбамінової 1 Н ЯМР (300МГц,CDCI3): d 7,83-7,86 (м, 2Н), кислоти (5,32г; 13,9ммоль) в 1 порцію. Розплав 7,70-7,73 (м, 2Н), 6,96-6,99 (д, 1Н), 6,67-6,72 (м, перемішують протягом 7-8хв. при 330°С, потім 2Н), 4,50-4,59 (м, 1Н), 3,78 (с, 3Н), 3,52-3,61 (м, швидко охолоджують до кімнатної температури 1Н), 2,95-2,98 (м, 2Н), 2,81-2,88 (м, 1Н), 2,65-2,76 потоком N2. Сировий залишок очищають флеш(м, 1Н), 1,97-2,01 (м, 1Н). хроматографією (SiO2), елююючи градієнтом гекLC/MS: C 19H17NO3: m/z 308 (М+1). санів-EtOAc, одержуючи 3,1г (58%) S-[6-(1,3С. 2-(6-Гідрокси-1,2,3,4-тетрагідронафталін-2діоксо-1,3-дигідроізоіндол-2-іл)-5,6,7,8іл)ізоіндол-1,3-діон тетрагідронафталін-2-іловий] складний ефір димеСхема 3. До 2-(6-метокси-1,2,3,4тилтіокарбамінової кислоти у вигляді білої твердої тетрагідронафталін-2-іл)ізоіндол-1,3-діону (29г; речовини. 1 94,3ммоль), розчиненого у безводному СН 2СІ2 Н ЯМР (300МГц, CDCI3): d 7,82-7,86 (м, 2Н), (500мл), охолодженому до -60 °С, додають 1,0М 7,72-7,75 (м, 2Н), 7,23-7,26 (м, 2Н), 7,07-7,10 (д, розчин броміду бору-СН 2СІ2 (471мл) по краплях 1Н), 4,52-4,63 (м, 1Н), 3,61-3,70 (м, 1Н), 2,89-3,09 для підтримання температури реакції в інтервалі (м, 9Н), 2,61-2,75 (м, 1Н), 1,97-2,04 (м, 1Н). від -50 до -60°С. Після закінчення додавання, реаLC/MS: C 21H20N2O3S: m/z 381 (М+1). кційній суміші дають нагрітися до кімнатної темпеF. S-[6-аміно-5,6,7,8-тетрагідронаФталін-2ратури та перемішують протягом ще 4год. Реакцію іловий) складний ефір диметилтіокарбамінової охолоджують до 0°С, гасять насиченим NaHCO3 кислоти (400мл) та перемішують протягом ще 0,5год. при Схема 3. 3-Горлу колбу, обладнану зворотним кімнатній температурі. Осад фільтрують, ретельно холодильником та механічною мішалкою, заванпромивають Н2О, суспендують в ефірі, фільтрують тажують EtOH (115мл) та S-[6-(1,3-діоксо-1,3та висушують під вакуумом, одержуючи 25,4г дигідроізоіндол-2-іл)-5,6,7,8-тетрагідронафталін-2(92%) 2-(6-гідрокси-1,2,3,4-тетрагідронафталін-2іловим] складним ефіром диметилтіокарбамінової іл)ізоіндол-1,3-діону у вигляді білуватої твердої кислоти (8,7г; 23,5ммоль). Додають гідразин речовини. (6,6мл; 2,11моль) однією порцією при кімнатній 1 Н ЯМР (300МГц, ДМСО-d6): d 9,11 (шир.с, 1Н), температурі і реакцію кип'ятять зі зворотним холо7,82-7,89 (м, 4Н), 6,84-6,87 (д, 1Н), 6,52-6,56 (м, дильником при механічному перемішуванні протя2Н), 4,29-4,37 (м, 1Н), 3,45 (шир.с, 1Н), 3,25-3,34 гом 40хв. Реакцію охолоджують до кімнатної тем(м, 1Н), 2,73-2,84 (м, 3Н), 2,37-2,47 (м, 1Н), 1,94ператури і гелеподібну білу тверду речовину 1,98 (м, 1Н). фільтрують та ретельно промивають ефіром. ЕфіLC/MS: C 18H15NO3: m/z 294 (М+1). рні промивні рідини об'єднують, випаровують при D. О-[6-(1,3-Діоксо-1,3-дигідроізоіндол-2-іл)зниженому тиску, і сировий залишок далі тритуру 25 80297 26 ють з ефіром, фільтрують та ефір випаровують метилпропіонової кислоти (1,7г; 4,64ммоль) у ТГФ при зниженому тиску, одержуючи 6,1г (100%) S-[6(42мл) додають по краплях при кімнатній темперааміно-5,6,7,8-тетрагідронафталін-2-ілового) складтурі 1,0М розчин боран-ТГФ (42мл). Реакцію залиного ефіру диметилтіокарбамінової кислоти у вишають при перемішуванні на 18год. при кімнатній гляді жовтої маслянистої рідини. температурі, обережно гасять МеОН і розчинник LC/MS: C 13H18N2OS: m/z251 (M+1). випаровують при зниженому тиску. Залишок масG. Трет-бутиловий складний ефір 2-(6-амінолянистої рідини далі піддають азеотропній перего5,6,7,8-тетрагідронафталін-2-ілсульфаніл)-2нці з МеОН (3´), одержуючи 1,9г (100%) суміші метилпропіонової кислоти трет-бутилового складного ефіру 2-(6-етиламіноСхема 3. До S-[6-аміно-5,6,7,85,6,7,8-тетрагідронафталін-2-ілсульфаніл)-2тетрагідронафталін-2-ілового) складного ефіру метилпропіонової кислоти та її боранового комдиметилтіокарбамінової кислоти (6,1г; 24,4ммоль), плексу у ви гляді маслянистої рідини. розчиненого у МеОН (25мл), додають розчин KОН LC/MS: C 20H31NO2S·BH3 : m/z 308 ((М+ВН3)+1). (4,1г; 73,2ммоль) у МеОН (25мл) при кімнатній J. Трет-бутиловий складний ефір 2-{6-[1-етилтемпературі. Розчин перемішують при кип'ятінні зі 3-(4-трифлюорметоксифеніл)уреїдо]-5,6,7,8зворотним холодильником протягом 5год. та охотетрагідронафталін-2-ілсульфаніл}-2лоджують до кімнатної температури. Додають до метилпропіонової кислоти розчину трет-бутил-2-бромізобутират (16,3г; Схема 4. До суміші трет-бутилового складного 73,2ммоль) та перемішують протягом 16год. при ефіру та боранового комплексу 2-(6-етиламінокімнатній температурі. Додають NaBH4 (9,2г; 5,6,7,8-тетрагідронафталін-2-ілсульфаніл)-22,44моль) і реакцію перемішують протягом ще метилпропіонової кислоти (1,9г; 5,2ммоль), розчи48год. при кімнатній температурі. Реакцію гасять неної у СН2СІ2 (15мл), додають 4за допомогою Н 2О, розчинник випаровують при трифлюорметоксифенілізоціанат (1,6г; 7,8ммоль) і зниженому тиску і сировий залишок розподіляють реакцію перемішують при кімнатній температурі між Н2О та СН2СІ2. Водну фазу екстрагують СН 2СІ2 протягом 18год. Розчинник видаляють при знижеі об'єднані органічні екстракти осушають над ному тиску і сировий залишок очищають флешNa2SO4, фільтрують та випаровують при зниженохроматографією (SiO2), елююючи градієнтом гекму тиску, одержуючи 4,7г (60%) трет-бутилового санів-EtOAc, одержуючи 1,66г (58%) третскладного ефіру 2-(6-аміно-5,6,7,8бутилового складного ефіру 2-{6-[1-етил-3-(4тетрагідронафталін-2-ілсульфаніл)-2трифлюорметоксифеніл)уреїдо]-5,6,7,8метилпропіонової кислоти у вигляді бурої маслятетрагідронафталін-2-ілсульфаніл}-2нистої рідини. метилпропіонової кислоти у вигляді білої піни. LC/MS: C 181H 27NO2S: m/z266 (M+1). LC/MS: C 28H35F3N2 O4S: m/z497 ((M-C 4H8)+1). Η. Трет-бутиловий складний ефір 2-(6Κ. 2-{6-[1-Етил-3-(4ацетиламіно-5,6,7,8-тетрагідронаФталін-2трифлюорметоксифеніл)уреїдо]-5,6,7,8-тетрагідроілсульфаніл)-2-метилпропіонової кислоти нафталін-2-ілсульфаніл}-2-метилпропіонова кисСхема 3. До трет-бутилового складного ефіру лота 2-(6-аміно-5,6,7,8-тетрагідронафталін-2Схема 4. До трет-бутилового складного ефіру ілсульфаніл)-2-метилпропіонової кислоти (4,7г; 2-{6-[1-етил-3-(4-трифлюорметоксифеніл)уреїдо]14,6ммоль), розчиненого у СН 2СІ2 (25мл), додають 5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2DIEA (3,3мл; 18, ммоль) та реакційну суміш охолометилпропіонової кислоти (1,66г; 3,0ммоль), розджують до 0°С. Додають по краплях ацетилхлорид чиненої у СН2СІ2 (15мл), додають TFA (15мл) і (1,25мл; 17,5ммоль) з такою швидкістю, щоб підреакцію перемішують при кімнатній температурі тримувати температуру в інтервалі 0-5°С. Реакції протягом 1,5год. Розчинник видаляють при знижедають нагрітися до кімнатної температури та пеному тиску та залишок очищають флешремішують протягом 16год. Реакцію розводять хроматографією (SiO2), елююючи градієнтом гекСН2СІ2, промивають Н2О, осушають над Na2SO4 та санів-EtOAc, одержуючи 0,643г (43%) 2-{6-[1-етилвипаровують при зниженому тиску. Сирову масля3-(4-трифлюорметоксифеніл)уреїдо]-5,6,7,8нисту рідину очищають флеш-хроматографією тетрагідронафталін-2-ілсульфаніл}-2(SiO2), елююючи градієнтом гексанів-EtOAc, одерметилпропіонової кислоти у вигляді білої твердої жуючи 1,7г (32%) трет-бутилового складного ефіру речовини. 1 2-(6-ацетиламіно-5,6,7,8-тетрагідронафталін-2Н ЯМР (300МГц, CD3OD): d 7,45-7,48 (м, 2Н), ілсульфаніл)-2-метилпропіонової кислоти у вигляді 7,06-7,24 (м, 5Н), 4,44 (м, 1Н), 3,43-3,45 (м, 2Н), жовто-коричневої твердої речовини. 2,96-3,02 (м, 4Н), 2,00-2,05 (м, 2Н), 1,41-1,46 (с, 1 Н ЯМР (300МГц, CDCI3): d 7,23-7,26 (м, 2Н), 6Н), 1,21-1,29 (м, 3Н). 6,99-7,01 (д, 1Н), 5,46-5,48 (м, 1Н), 4,25-4,29 (м, LC/MS: C 24H27F3N2 O4S: m/z 497 (М+1). 1Н), 3,08-3,15 (дд, 1Н), 2,82-2,88 (м, 2Н), 2,58-2,66 (м, 1Н), 2,01-2,04 (м, 1Н), 1,98 (с, 3Н), 1,70-1,82 (м, 1Н), 1,43 (с, 15Н). LC/MS: C 20H29NO3S: m/z 308 (М+1). І. Трет-бутиловий складний ефір 2-(6етиламіно-5.6.7.8-тетрагідронаФталін-2ілсульфаніл)-2-метилпропіонової кислоти Схема 3. До розчину трет-бутилового складного ефіру 2-(6-ацетиламіно-5,6,7,8тетрагідронафталін-2-ілсульфаніл)-22-{2-[1-Етил-3-(4 27 80297 28 трифлюорметоксифеніл)уреїдо]індан-5твердої речовини. Органічну фазу промивають ілсульфаніл}-2-метил-пропіонова кислота. Н2О, випаровують при зниженому тиску і тверду Сполука 2.0 (Приклад 2) речовину тритур ують з МеОН, фільтрують та виА. 5-Ме токсііндан-1,2-діон-2-оксим сушують, одержуючи додатково 19,7 (33%) г 2-(5Схема 2. До розчину 5-метоксііндан-1-ону метоксііндан-2-іл)ізоіндол-1,3-діону у вигляді білої (75,8г; 0,467моль) у МеОН (1,4л) при 45°С додатвердої речовини. 1 ють по краплях бутилнітрит (81мл; 0,693моль) на Н ЯМР (300МГц, CD3OD): d 7,83-7,87 (м, 2Н), протязі 45хв. Потім до гарячого розчину на протязі 7,68-7,74 (м, 2Н), 7,10-7,13 (д, 1Н), 6,73-6,78 (м, 20хв. додають концентровану НСІ (45мл) і реакцію 2Н), 5,08-5,21 (м, 1Н), 3,79 (с, 3Н), 3,48-3,65 (м, залишають при перемішуванні при 45°С ще на 1,52Н), 3,07-3,18 (м, 2Н). 2год. Реакційну суспензію охолоджують, осад фіLC/MS: C 18H15NO3: m/z 294 (М+1). льтрують, промивають кілька разів холодним МеD. 2-(5-Гідроксііндан-2-іл)ізоіндол-1,3-діон ОН та висушують під вакуумом, одержуючи 55,8г Схема 3. До 2-(5-метоксііндан-2-іл)ізоіндол(62%) 5-метоксііндан-1,2-діон-2-оксиму у вигляді 1,3-діону (19,7г; 67ммоль), розчиненого у безводтвердої речовини бежевого кольору. ному СН 2СІ2 (350мл) та охолодженого до -60°С, 1 Н ЯМР (300МГц, CD3OD): d 7,80-7,83 (м, 1Н), додають по краплях 1,0М розчин броміду бору6,95 (шир.с, 2Н), 3,92 (с, 3Н), 3,78 (с, 2Н), 3,47 СН2СІ2 (340мл) з такою швидкістю, щоб підтриму(шир.с, 1Н). вати внутрішню температуру в інтервалі від -50 до LC/MS: C 10H9NO 3: m/z 192 (М+1). -60°С. Реакційній суміші дають нагрітися до кімнаВ. 5-Ме токсііндан-2-іламіну гідрохлорид тної температури та перемішують протягом ще Схема 2. До 5-метоксііндан-1,2-діон-2-оксиму 5год. Реакцію охолоджують до 0°С, гасять насиче(55,7г; 0,291моль), суспендованого у льодяній оцним NaHCO3 (500мл) та перемішують протягом ще товій кислоті (0,99л), додають концентровану 0,5год. при кімнатній температурі. Осад фільтруH2SO4 (67мл), а потім 10% Pd-C (27г) і реакцію ють, промивають Н2О, суспендують в ефірі, фільтперемішують в апараті Парра при тиску Н 2 414кПа рують та висушують під вакуумом, одержуючи (60psi) протягом 18год. Реакцію продувають N2, 14,8г (79%) 2-(5-гідроксііндан-2-іл)ізоіндол-1,3фільтрують крізь шар целіту та промивають АсОН. діону у вигляді твердої речовини бежевого кольоРозчинник видаляють при зниженому тиску до 1/5 ру. 1 об'єму і решту розчинника розводять Н 2О (500мл), Н ЯМР (300МГц, ДМСО-d6): d 9,16 (с, 1Н), охолоджують до 0 °С та нейтралізують до рН 10 за 7,82-7,91 (м, 4Н), 6,98-7,01 (д, 1Н), 6,56-6,62 (м, допомогою 50% водного NaOH. Водну фазу кілька 2Н), 4,91-5,03 (м, 1Н), 3,27-3,43 (м, 3Н), 2,99-3,10 разів ретельно екстрагують СНСІ3 та екстракти (м, 2Н). об'єднують, промивають Н2О, розсолом, осушають LC/MS: C 17H13NO3: m/z 280 (М+1). над Na2SO4, фільтрують та випаровують при зниF. О-[2-(1,3-Діоксо-1,3-дигідроізоіндол-2женому тиску, одержуючи 77,3г (66%) сирової маіл)індан-5-ілового] складного eфipv диметилтіокаслянистої рідини. Маслянисту рідину піддають рбамінової кислоти флеш-хроматографії (SiO2), елююючи 40:2,2:0,2 Схема 3. До 2-(5-гідроксііндан-2-іл)ізоіндолCHCI3:MeOH:NH 4OH, одержуючи 43,8г (37%) мас1,3-діону (31г; 0,11моль), розчиненого у безводнолянистої рідини темного кольору. Маслянисту ріму ДМФ (400мл), додають 1,4-діазабіцикло[2.2.2]дину розчиняють в ефірі (1л), охолоджують до 0°С октан (62г; 0,55моль), а потім диметиламінотіокарі розчин насичують НСІ (газ.). Розчинник видалябамоїлхлорид (68г; 0,55моль) і розчин перемішують при зниженому тиску та тверду речовину триють при кімнатній температурі протягом 16год. турують з ефіром, фільтрують та промивають ефіРеакцію виливають на воду з льодом (1л) і перером, одержуючи 43,8г (30%) 5-метоксііндан-2мішують протягом 18год. Осад фільтрують, проіламіну гідрохлориду у вигляді білої твердої речомивають Н2О та висушують під вакуумом, одервини. жуючи 41,6г (100%) О-[2-(1,3-діоксо-1,31 Н ЯМР (300МГц, CD3OD): d 7,08-7,11 (д, 1Н), дигідроізоіндол-2-іл)індан-5-ілового] складного 6,77 (с, 1Н), 6,69-6,72 (д, 1Н), 3,78-3,85 (м, 1Н), ефіру диметилтіокарбамінової кислоти у вигляді 3,77 (с, 3Н), 3,08-3,19 (м, 2Н), 2,57-2,68 (м, 2Н), твердої речовини бежевого кольору. 1 1,51 (с, 2Н). Н ЯМР (300МГц, CDCI3): d 7,82-7,87 (м, 2Н), LC/MS: C 10H9NO 3: m/z 192 (М+1). 7,69-7,75 (м, 2Н), 7,17-7,24 (д, 1Н), 6,87-6,93 (м, Т.пл.=240-241°С. 2Н), 5,13-5,25 (м, 1Н), 3,53-3,68 (м, 2Н), 3,46 (с, С. 2-(5-Метоксііндан-2-іл)ізоіндол-1,3-діон 3Н), 3,34 (с, 3Н), 3,09-3,23 (м, 2Н). Схема 3. До суспензії 60% NaH (8г; 0,240моль) G. S-[2-(1,3-Діоксо-1,3-дигідроізоіндол-2у ДМФ (250мл), охолодженої до 0°С, додають 5іл)індан-5-іловий] складний ефір диметилтіокарметоксііндан-2-іламіну гідрохлорид (40,0г; 0,2моль) бамінової кислоти і суспензію перемішують протягом 1год. при кімнаСхема 3. До круглодонної колби на 50мл, обтній температурі. Додають фталевий ангідрид (30г; ладнаної зворотним холодильником та стрижнем 0,2моль) однією порцією і суспензію перемішують для перемішування, попередньо нагрітої до 330°С протягом ще 1-1,5год. при кімнатній температурі, а на піщаній бані, додають О-[2-(1,3-діоксо-1,3потім перемішують при 120°С протягом 96год. Редигідроізоіндол-2-іл)індан-5-іловий] складний ефір акцію охолоджують та розводять EtOAc. Органічну диметилтіокарбамінової кислоти (6,30г; фазу промивають Н 2О, утворений осад фільтру18,7ммоль) в 1 порцію. Розплав перемішують проють, промивають EtOAc, МеОН та висушують під тягом 12хв. при 338°С, швидко охолоджують до вакуумом, одержуючи 25,2г (43%) 2-(5кімнатної температури потоком Ν 2 і сировий залиметоксііндан-2-іл)ізоіндол-1,3-діон у вигляді білої шок очищають флеш-хроматографією (SiO2), 29 80297 30 елююючи градієнтом гексани-EtOAc, одержуючи кімнатної температури, перемішують протягом 3,88г (61%) 3-[2-(1,3-діоксо-1,3-дигідроізоіндол-216год., розводять СН 2СІ2, промивають Н2О, осуіл)індан-5-ілового] складного ефіру диметилтіокашають над Na2SO4 та випаровують при зниженому рбамінової кислоти у вигляді білуватої твердої тиску. Сирову маслянисту рідину очищають флешречовини. хроматографією (SiO2), елююючи градієнтом гек1 санів-EtOAc, одержуючи 11,7г (71%) третН ЯМР (300МГц, CDCI3): d 7,81-7,87 (м, 2Н), бутилового складного ефіру 2-(27,69-7,74 (м, 2Н), 7,22-7,36 (м, 3Н), 5,10-5,22 (м, 1Н), 3,59-3,67 (м, 2Н), 3,06-3,23 (м, 9Н). ацетиламіноіндан-5-ілсульфаніл)-2метилпропіонової кислоти у вигляді твердої речоLC/MS: C 20H18N2O3S: m/z367 (M+1). вини бежевого кольору. Н. S-(2-Аміноіндан-5-іловий) складний ефір 1 диметилтіокарбамінової кислоти Н ЯМР (300МГц, CDCI3): d 7,31-7,35 (м, 2Н), Схема 3. 3-Горлу колбу, обладнану зворотним 7,15-7,18 (д, 1Н), 5,73 (м, 1Н), 4,68-4,78 (м, 1Н), холодильником та механічною мішалкою, заван3,25-3,39 (дд, 2Н), 2,74-2,80 (д, 2Н), 1,94 (с, 3Н), тажують EtOH (98мл) та S-[2-(1,3-діоксо-1,31,43 (с, 15Н). дигідроізоіндол-2-іл)індан-5-іловим] складним ефіLC/MS: C 19H27NO3S: m/z 294 (М+1). ром диметилтіокарбамінової кислоти (6,9г; K. Трет-бутиловий складний ефір 2-(220,6ммоль). Додають гідразин (5,8мл; 186ммоль) в етиламіноіндан-5-ілсульФаніл)-2-метилпропіонової 1 порцію при кімнатній температурі та реакцію накислоти грівають до кипіння зі зворотним холодильником Схема 3. До розчину трет-бутилового складнопри механічному перемішуванні протягом 30хв. го ефіру 2-(2-ацетиламіноіндан-5-ілсульфаніл)-2Реакцію охолоджують до кімнатної температури і метилпропіонової кислоти (11,7г; 33,5ммоль) у гелеподібну білу тверду речовину фільтрують та ТГФ (280мл) додають по краплях при кімнатній промивають кілька разів ефіром. Ефірні промивні температурі 1,0М розчин боран-ТГФ (226мл). Реарідини об'єднують, випаровують при зниженому кцію залишають при перемішуванні на 5год. при тиску і сировий залишок далі тритурують з ефіром, кімнатній температурі, охолоджують до 0°С, гасять фільтрують та е фір випаровують при зниженому МеОН (100мл) та випаровують при зниженому тиску, одержуючи 4,6г (95%) 8-(2-аміноіндан-5тиску. Залишкову маслянисту рідину далі піддають ілового) складного ефіру диметилтіокарбамінової азеотропній перегонці з МеОН (3´), одержуючи 11г кислоти у вигляді бурої маслянистої рідини. (100%) суміші трет-бутилового складного ефіру 21 Н ЯМР (300МГц, CDCI3): d 7,15-7,33 (м, 3Н), (2-етиламіноіндан-5-ілсульфаніл)-23,80-3,88 (м, 1Н), 3,05-3,22 (м, 8Н), 2,64-2,72 (м, метилпропіонової кислоти та її боранового ком1Н), 2,17 (шир.с, 2Н). плексу у ви гляді маслянистої рідини. LC/MS: C 12H16N2OS: m/z 237 (M+1). LC/MS: C 19H29NO2S·BH3 : m/z 336 ((М+ВН3)+1). І. Трет-бутиловий складний ефір 2-(2L. Трет-бутиловий складний ефір 2-{2-[1-етиламіноіндан-5-ілсульфаніл)-2-метилпропіонової 3-(4-трифлюорметоксифеніл)уреїдо]індан-5кислоти ілсульфаніл)-2-метилпропіонової кислоти Схема 3. До S-(2-аміноіндан-5-ілового) складСхема 4. До суміші трет-бутилового складного ного ефіру диметилтіокарбамінової кислоти (4,9г; ефіру та боранового комплексу 2-(220,9ммоль), розчиненого у МеОН (60мл), додають етиламіноіндан-5-ілсульфаніл)-2-метилпропіонової розчин KОН (11,8г; 0,210моль) у МеОН (110мл) кислоти (11,0г; 33ммоль), розчиненої у СН2СІ2 при кімнатній температурі. Розчин перемішують (100мл), додають 4при кипінні зі зворотним холодильником протягом трифлюорметоксифенілізоціанат (10,2г; 5год. та о холоджують до кімнатної температури. 50,2ммоль) і реакцію залишають при перемішуДодають до розчину трет-бутил-2-бромізобутират ванні при кімнатній температурі на 18год. Розчин(7,0г; 31,3ммоль) та перемішують протягом 18год. ник видаляють при зниженому тиску і сировий запри кімнатній температурі. Розчинник випаровують лишок очищають флеш-хроматографією (SiO2), при зниженому тиску і сировий залишок розподіелююючи градієнтом гексанів-EtOAc, одержуючи ляють між Н2О та EtOAc. Водну фазу екстрагують 11,2г (62%) трет-бутилового складного ефіру 2-{2EtOAc і об'єднані органічні екстракти промивають [1-етил-3-(4-трифл юорметоксифеніл)уреїдо]інданН2О, розсолом, осушають над Na2SO4, фільтр ують 5-ілсульфаніл}-2-метилпропіонової кислоти у вита випаровують при зниженому тиску, одержуючи гляді білої піни. 1 4,9г (76%) трет-бутилового складного ефіру 2-(2Н ЯМР (300МГц, CDCI3): d 7,30-7,36 (м, 4Н), аміноіндан-5-ілсульфаніл)-2-метилпропіонової 7,10-7,19 (м, 3Н), 6,31 (с, 1Н), 4,97-5,08 (м, 1Н), кислоти у вигляді бурої маслянистої рідини. 3,22-3,39 (м, 4Н), 3,01-3,09 (дд, 2Н), 1,42-1,44 (м, LC/MS: C 17H25NO2S: m/z 308 (M+1). 15Н), 1,23-1,28 (т, 3Н). J. Трет-бутиловий складний ефір 2-(2LC/MS: C 27H33F3N2 O4S: m/z 483 ((М-С4Н8)+1). ацетиламіноіндан-5-ілсульФаніл)-2Μ. 2-{2-[1-Етил-3-(4метилпропіонової кислоти трифлюорметоксиФеніл)уреїдо]індан-5Схема 3. До трет-бутилового складного ефіру ілсульфаніл}-2-метилпропіонова кислота 2-(2-аміноіндан-5-ілсульфаніл)-2-метилпропіонової Схема 4. До трет-бутилового складного ефіру кислоти (14,6г; 47,4ммоль), розчиненої у СН 2СІ2 2-{2-[1-етил-3-(4(100мл), додають TEA (8,6мл; 61,7ммоль) та реактрифлюорметоксифеніл)уреїдо]індан-5ційну суміш охолоджують до 0°С. Додають по краілсульфаніл}-2-метилпропіонової кислоти (4,8г; плях ацетилхлорид (4,1мл; 57,6ммоль) з такою 8,91ммоль), розчиненого у СН 2СІ2 (15мл), додають швидкістю, щоб підтримувати температуру в інTFA (15мл) і реакцію перемішують при кімнатній тервалі 0-5°С. Реакцію залишають нагрітися до температурі протягом 2год. Розчинник видаляють 31 80297 32 при зниженому тиску та залишок очищають флешхроматографією (SiO2), елююючи градієнтом гексанів-EtOAc, одержуючи 3,13г (73%) 2-{2-[1-етил-3(4-трифлюорметоксифеніл)уреїдо]індан-5ілсульфаніл}-2-метил-пропіонової кислоти у вигляді білої твердої речовини. 1 Н ЯМР (300МГц, CDCI3): d 7,29-7,35 (м, 4Н), 7,15-7,17 (д, 1Н), 7,08-7,11 (д, 2Н), 6,45 (с, 1Н), 4,94-5,04 (м, 1Н), 3,18-3,36 (м, 4Н), 2,98-3,07 (м, 2Н), 1,48 (с, 6Н), 1,19-1,28 (т, 3Н). LC/MS: C 23H25F3N2 O4S: m/z483 (M+1). Сполуку 2.3 (0,22г; 32% для 2 стадій; біла твеТ.пл.=73-77°С. рда речовина) одержують згідно зі шляхом 2 та Наступні 14 сполук були одержані згідно зі синтезом Сполуки 2.2, використовуючи замість Схемами 3 та 4 та стадіями J, K, L та Μ Шляху 2, з ацетилхлориду валерилхлорид. 1 використанням відповідних реагентів замість укаН ЯМР (CD3OD): d 0,844-0,890 (т, 3Н), 1,20заних та регулюванням реакційних умов: 1,31 (м, 4Н), 1,39 (с, 6Н), 1,45-1,58 (м, 2Н), 3,07(S)-2-{2-[1-Етил-3-(43,22 (м, 6Н), 4,89-4,99 (м, 1Н), 7,15-7,18 (м, 1Н), трифлюорметоксифеніл)уреїдо]індан-57,33-7,35 (м, 2Н), 7,33-7,35 (м, 1Н), 7,40 (с, 1Н), ілсульфаніл}-2-метилпропіонова кислота 7,50-7,57 (м, 4Н). Сполука 2.1 (Приклад 3) LC/MS: C 26H31F3N2 O3S 2: m/z541 (M+1). 2-{2-[1-Етил-3-(4-ізопропілфеніл)уреїдо]індан5-ілсульфаніл}-2-метил-пропіонова кислота Сполука 2.4 (Приклад 6) Проміжну сполуку L (11г) шляху 2 розділяють методом хіральної хроматографії (колонка Chiralpak AD; ізократичний градієнт гексан/метанол/етанол: 92/4/4), одержуючи (S)-ізомер проміжної сполуки L (4,8г). Використовуючи Стадію Μ шляху 2, одержують сполуку 2.1 (3,1г). LC/MS: C 23H25F3N2 O4S: m/z483 (M+1). 2-{2-[1-Етил-3-(4трифлюорметилсульфанілфеніл)уреїдо]індан-5ілсульфаніл}-2-метилпропіонова кислота. Сполука 2.2 (Приклад 4) Сполуку 2.2 (0,33г; 57% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2, використовуючи замість 4трифлюорметоксифенілізоціанату 4трифлюортіометоксіізоціанат. 1 Н ЯМР (CD3OD): d 1,16-1,20 (т, 3Н), 1,38 (с, 6Н), 3,09-3,23 (м, 4Н), 3,37-3,44 (кв, 2Н), 4,95-5,06 (м, 1Н), 7,14-7,17 (м, 1Н), 7,32-7,35 (м, 1Н), 7,40 (с, 1Н), 7,55 (с, 4Н). LC/MS: C 23H25F3N2 O3S 2: m/z499 (M+1). 2-Метил-2-{2-[1-пентил-3-(4трифлюорметилсульфанілфеніл)уреїдо]-індан-5ілсульфаніл}пропіонова кислота Сполука 2.3 (Приклад 5) Сполуку 2.4 (0,18г; 34% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2, використовуючи замість 4трифлюорметоксифенілізоціанату 4ізопропілфенілізоціанат. 1 Н ЯМР (CD3OD): d 1,16-1,23 (м, 9Н), 1,38 (с, 6Н), 2,82-2,87 (м, 1Н), 3,10-3,21 (м, 4Н), 3,37-3,39 (м, 2Н), 4,99-5,04 (м, 1Н), 7,14-7,17 (м, 3Н), 7,237,26 (м, 2Н), 7,32-7,50 (м, 2Н), 7,40 (с, 1Н). LC/MS: C 25H32N2O3S: m/z441 (M+1). 2-{2-[3-(4-Диметиламінофеніл)-1етилуреїдо]індан-5-ілсульфаніл}-2метилпропіонова кислота Сполука 2.5 (Приклад 7) Сполуку 2.5 (0,34г; 66% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2, використовуючи замість 4трифлюорметоксифенілізоціанату 4диметиламінофенілізоціанат. 1 Н ЯМР (CD3OD): d 1,15-1,20 (т, 3Н), 1,42 (с, 6Н), 2,88 (с, 1Н), 3,05-3,69 (м, 4Н), 3,31-3,69 (м, 2Н), 4,94-5,06 (м, 1Н), 6,78-6,81 (м, 2Н), 7,16-7,21 (м, 3Н), 7,29-7,41 (м, 2Н). LC/MS: C 24H31N3O3S: m/z442 (M+1). 2-Метил-2-{2-[1-пентил-3-(4 33 трифлюорметоксифеніл)уреїдо]індан-5ілсульфаніл}-2-метилпропіонова кислота Сполука 2.6 (Приклад 8) 80297 34 тилхлориду валерилхлорид. LC/MS: C 28H38N2O3S: m/z 483 (М+1). 2-{2-[3-(4-Трет-бутилфеніл)-1-(3пентил)уреїдо]індан-5-ілсульфаніл}-2метилпропіонова кислота Сполука 2.9 (Приклад 11) Сполуку 2.6 (0,29г; 77% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2, використовуючи замість ацетилхлориду валерилхлорид. 1 Н ЯМР (CD3OD): d 0,847-0,893 (т, 3Н), 1,201,29 (м, 4Н), 1,39 (с, 6Н), 1,58-1,60 (м, 2Н), 3,043,29 (м, 6Н), 4,89-4,99 (м, 1Н), 7,14-7,17 (м, 3Н), 7,32-7,34 (м, 1Н), 7,40-7,45 (м, 3Н). LC/MS: C 26H31F3N2 O4S: m/z 525 (М+1). 2-{2-[3-(4-Диметиламінофеніл)-1пентилуреїдо]індан-5-ілсульфаніл}-2метилпропіонова кислота Сполука 2.7 (Приклад 9) Сполуку 2.7 (0,25г; 36% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.5, використовуючи замість ацетилхлориду валерилхлорид. 1 Н ЯМР (CD3OD): d 0,869-0,915 (т, 3Н), 1,171,31 (м, 4Н), 1,44 (с, 6Н), 1,57-1,65 (м, 2Н), 2,91 (с, 6Н), 3,12-3,29 (м, 6Н), 4,94-5,02 (м, 1Н), 6,80-6,83 (д, 2Н), 7,17-7,23 (м, 3Н), 7,32-7,38 (м, 2Н). LC/MS: C 27H37N3O3S: m/z 484 (М+1). 2-{2-[3-(4-Ізопропілфеніл)-1-(3пентил)уреїдо]індан-5-ілсульфаніл}-2метилпропіонова кислота Сполука 2.8 (Приклад 10) Сполуку 2.8 (5мг; 14% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.4, використовуючи замість аце Сполуку 2.9 (4мг; 9% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.3, використовуючи замість 4трифлюортіофенілізоціанату 4-третбутилфенілізоціанат. LC/MS: C 29H40N2O3S: m/z497 (M+1). 2-[2-(3-(Біфеніл-4-іл-1-пентилуреїдо)індан-5ілсульфаніл]-2-метилпропіонова кислота Сполука 2.10 (Приклад 12) Сполуку 2.10 (3мг; 7% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.3, використовуючи замість 4трифлюортіофенілізоціанату4-біфенілілізоціанат. LC/MS: C 31H36N2O3S: m/z517 (M+1). 2-{2-[3-(4-Ізопропілфеніл)-1-(3гексил)уреїдо]індан-5-ілсульфаніл}-2метилпропіонова кислота Сполука 2.11 (Приклад 13) Сполуку 2.11 (13мг; 44% для 2 стадій; масляниста рідина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.4, використовуючи замість валерилхлориду капроїлхлорид. LC/MS: C 29H40N2O3S: m/z497 (M+1). 35 2-Метил-2-{2-[1-гексил-3-(4трифлюорметоксифеніл)уреїдо]індан-5ілсульфаніл}пропіонова кислота Сполука 2.12 (Приклад 14) 80297 Сполуку 2.12 (18мг; 54% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2, використовуючи замість валерилхлориду капроїлхлорид. LC/MS: C 27H33F3N2 O4S: m/z 539 (М+1). 2-Метил-2-{2-[1-гексил-3-(4трифлюорметилсульфанілфеніл)уреїдо]-індан-5ілсульфаніл}пропіонова кислота Сполука 2.13 (Приклад 15) 36 Сполуку 2.15 (11мг; 32% для 2 стадій; масляниста рідина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.2, використовуючи замість ацетилхлориду бутирилхлорид. LC/MS: C 25H29F3N2 O3S 2: m/z 527 (М+1). 2-Метил-2-{2-[3-(4трифлюорметоксифеніл)уреїдо]індан-5ілсульфаніл}-пропіонова кислота Сполука 2.16 (Приклад 18) Сполуку 2.16 (11мг; 49% для 2 стадій; масляниста рідина) одержують згідно зі шляхом 2 ацилюванням 4-трифлюорметоксифенілізоціанатом. LC/MS: C 21H21F3N2 O4S: m/z 455 (М+1). Шлях 3 2-Метил-2-{2-[1-пент-4-еніл-3-(4трифлюорметоксифеніл)уреїдо]індан-5ілсульфаніл}пропіонова кислота Сполука 3.0 (Приклад 19) Сполуку 2.13 (14мг; 36% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.2, використовуючи замість валерилхлориду капроїлхлорид. LC/MS: C 27H33F3N2 O3S 2: m/z 555 (М+1). 2-Метил-2-{2-[1-пропіл-3-(4трифлюорметоксифеніл)уреїдо]індан-5ілсульфаніл}пропіонова кислота Сполука 2.14 (Приклад 16) Сполуку 2.14 (1,2мг; 3% для 2 стадій; масляниста рідина) одержують згідно зі шляхом 2, використовуючи замість ацетилхлориду пропіонілхлорид. LC/MS: C 24H27F3N2 O4S: m/z 497 (М+1). 2-Метил-2-{2-[1-бутил-3-(4трифлюорметилсульфанілфеніл)уреїдо]індан-5ілсульфаніл}пропіонова кислота Сполука 2.15 (Приклад 17) До трет-бутилового складного ефіру (2-(2аміноіндан-5-ілсульфаніл)-2-метилпропіонової кислоти 0,220г; 0,72ммоль), розчиненого у DCE (4мл), додають пент-4-еналь (0,060мг; 0,72ммоль), а потім триацетоксиборгідрид натрію (0,21г; 1,0ммоль) і реакційну суміш перемішують протягом 18год. при кімнатній температурі. Реакційну суміш розводять СН 2СІ2, промивають Н 2О, розсолом, осушають над Na2SO4, фільтрують та розчинник випаровують при зниженому тиску, одержуючи трет-бутиловий складний ефір 2-метил-2(2-пент-4-еніламіноіндан-5ілсульфаніл)пропіонової кислоти у вигляді сирової маслянистої рідини. Сполуку 3.0 (0,149мг; 40% для 3 стадій; біла тверда речовина) одержують згідно зі шляхом 2 і стадіями L та Μ шляхом ацилювання 4трифлюорметоксифенілізоціанатом. LC/MS: C 26H29F3N2 O4S: m/z 522 (М+1). Наступні 2 сполуки були одержані згідно зі 37 80297 38 Схемами 3 та 4, Шляхом 3, Стадіями L та Μ Шляху 2, при належному заміщенні реагентів та регулюСполуку 1.1 (41мг; 68% для 2 стадій; біла твеванні реакційних умов: рда речовина) одержують згідно зі шляхом 1, ви2-Метил-2-{2-[1-(3-метилбутил)-3-(4користовуючи замість ацетилхлориду бутирилхлотрифлюорметоксифеніл)уреїдо]-індан-5рид. ілсульфаніл}-2-метилпропіонова кислота LC/MS: C 26H31F3N2 O4S: m/z 525 (М+1). Сполука 3.1 (Приклад 20) 2-{6-[1-Бутил-3-(4трифлюорметилсульфанілфеніл)уреїдо]-5,6,7,8тетрагідронафталін-2-ілсульфаніл}-2метилпропіонова кислота Сполука 1.2 (Приклад 23) Сполуку 3.1 (13мг; 29% для 3 стадій; біла тверда речовина) одержують згідно зі шляхом 3, використовуючи замість пент-4-еналю ізобутиральдегід та ацилювання 4трифлюорметоксифенілізоціанатом. LC/MS: C 26H31F3N2 O4S: m/z 525 (М+1). 2-{2-[3-(4-Ізопропілфеніл)-1-(3метилбутил)уреїдо]індан-5-ілсульфаніл}-2метилпропіонова кислота Сполука 3.2 (Приклад 21) Сполуку 3.2 (11мг; 27% для 3 стадій; біла тверда речовина) одержують згідно зі шляхом 3 та синтезом сполуки 3.1, використовуючи замість 4трифлюорметоксифенілізоціанату4ізопропілфенілізоціанат. 1 Н ЯМР (CD3OD): d 0,877-0,895 (дд, 6Н), 1,191,22 (дд, 6Н), 1,42-1,53 (м, 9Н), 2,80-2,89 (м, 1Н), 2,99-3,08 (м, 2Н), 3,17-3,48 (м, 4Н), 4,98-5,03 (м, 1Н), 6,26 (с, 1Н), 7,10-7,22 (м, 5Н), 7,32-7,35 (м, 2Н). LC/MS: C 28H38N2O3S: m/z 483 (M+1). Наступні 3 сполуки були одержані згідно зі Схемами 1 та 3 і Стадіями J та K Шляху 1, при належному заміщенні реагентів та регулюванні реакційних умов: 2-{6-[1-Бутил-3-(4трифлюорметоксифеніл)уреїдо]-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонова кислота Сполука 1.1 (Приклад 22) Сполуку 1.2 (23мг; 34% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 1 та синтезом Сполуки 1.1, використовуючи бутирилхлорид замість ацетилхлориду і 4трифлюортіофенілізоціанат замість 4трифлюорметоксифенілізоціанату. LC/MS: C 26H31F3N2 O3S 2: m/z541 (M+1). 2-{6-[1-Гексил-3-(4трифлюорметоксифеніл)уреїдо]-5,6,7,8-тетрагідронафталін-2-ілсульфаніл}-2-метилпропіонова кислота Сполука 1.3 (Приклад 24) Сполуку 1.3 (36мг; 57% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 1, використовуючи замість ацетилхлориду капроїлхлорид. LC/MS: C 28H35F3N2 O4S: m/z 553 (М+1). Наступні 2 сполуки були одержані згідно зі Схемами 3 та 4 і Стадіями L та Μ шляху 2, при належному заміщенні реагентів та регулюванні реакційних умов: 2-{2-[3-(3-Бром-4-трифлюорметоксифеніл)-1етилуреїдо]індан-5-ілсульфаніл}-2метилпропіонова кислота Сполука 2.17 (Приклад 25) Сполуку 2.17 (0,018г; 19% для 3 стадій; біла тверда речовина) одержують згідно зі шляхом 2, використовуючи замість 4 39 80297 40 трифлюорметоксифенілізоціанату 3-бром-4В. Трет-бутиловий складний ефір 2-метил-2трифлюорметоксифенілізоціанат. До 3-бром-4(2-метиламіноіндан-5-ілсульфаніл)пропіонової трифлюорметоксіаніліну (0,214г; 0,836ммоль) у кислоти ТГФ (1мл) додають ди-трет-бутилдикарбонат Схема 6. До S-(2-форміламіноіндан-5-ілового) (0,255г; 1,17ммоль), а потім 4складного ефіру диметилтіокарбамінової кислоти диметиламінопіридин (0,102г; 0,835ммоль). Після (0,772г; 2,9ммоль) у ТГФ (9мл) під N2 додають припинення виділення бульбашок газу (30хв.) до1,0М розчин гідриду літію-алюмінію (9мл) при 0°С. дають розчин трет-бутилового складного ефіру 2Реакцію нагрівають до кімнатної температури, а (2-етиламіноіндан-5-ілсульфаніл)-2потім перемішують при кип'ятінні зі зворотним хометилпропіонової кислоти (0,058г; 0,167ммоль) у лодильником протягом 24год. Реакцію охолоджуТГФ (1мл) і реакційну суміш перемішують протягом ють до 0°С, гасять Н 2О і розчинник видаляють при 18год. при кімнатній температурі. Використовуючи зниженому тиску. Залишок розчиняють у МеОН Стадії K та L шляху 2, одержують названу у заго(4мл), до якого додають Cs 2CO3 (0,304г; ловку сполуку. 0,93ммоль), трет-бутил-2-бромізобутират LC/MS: C 23H24BrF3N2 O4S: m/z 563 (М+1). (0,311мл; 1,39ммоль) та NaBH4 (2,0г; 52,8ммоль). 2-{2-[1-Етил-3-(3Реакційну суміш перемішують протягом 18год., трифлюорметоксифеніл)уреїдо]індан-5розчинник видаляють при зниженому тиску і залиілсульфаніл}-2-метилпропіонова кислота шок розподіляють між EtOAc та Н2 О. Шари роздіСполука 2.18 (Приклад 26) ляють, водну фазу екстрагують EtOAc, органічні екстракти об'єднують, промивають розсолом, осушають над Na2SO4, фільтр ують та випаровують при зниженому тиску. Сировий залишок очищають флеш-хроматографією (SiO2), елююючи градієнтом СН2СІ2-МеОН, одержуючи 0,186г (20%) третбутилового складного ефіру 2-метил-2-(2метиламіноіндан-5-ілсульфаніл)пропіонової кислоти у вигляді маслянистої рідини. Сполуку 2.18 (13мг; 12% для 3 стадій; біла LC/MS: C 18H27NO2S: m/z 321 (М+1). тверда речовина) одержують згідно з Прикладом Сполуку 2.19 (44мг; 65% для 2 стадій; біла 2.0, використовуючи замість 4тверда речовина) одержують згідно зі шляхом 2 і трифлюорметоксифенілізоціанату 3Стадіями L та М, використовуючи замість 4трифлюорметоксифенілізоціанат. До розчину картрифлюорметоксифенілізоціанату 4бонілдіімідазолу (0,454г; 2,8ммоль) у ТГФ (2мл), диметиламінофенілізоціанат. нагрітому до 50°С, додають по краплях 3LC/MS: C 23H29N3O3S: m/z 428 (М+1). трифлюорметоксіанілін (0,522г; 2,94ммоль). Через 2-{2-[1-(3-Циклопентилпропіл)-3-(415хв. реакцію охолоджують та додають до розчину трифлюорметоксифеніл)уреїдо]індан-5трет-бутилового складного ефіру 2-(2ілсульфаніл}-2-метилпропіонова кислота етиламіноіндан-5-ілсульфаніл)-2-метилпропіонової Сполука 2.20 (Приклад 28) кислоти (0,077г; 0,22ммоль) у ТГФ (1мл). LC/MS: C 23H25F3N2 O4S: m/z 483 (М+1). 2-{2-[3-(4-Диметиламінофеніл)-1метилуреїдо]індан-5-ілсульфаніл}-2метилпропіонова кислота. Сполука 2.19 (Приклад 27) А. 3-(2-Форміламіноіндан-5-іловий) складний ефір диметилтіо-карбамінової кислоти Схема 6. До S-[2-аміноіндан-5-ілового) складного ефіру диметилтіокарбамінової кислоти (2,0г; 8,46ммоль) у СНСІ3 (10мл) додають етилформіат (50мл) і реакцію нагрівають при 55°С протягом 24год. Реакцію охолоджують, розчинник видаляють при зниженому тиску і сирову маслянисту рідину очищають фле ш-хроматографією (SiO2), елююючи градієнтом етилацетату-метанолу, одержуючи 0,77г (35%) S-(2-форміламіноіндан-5ілового) складного ефіру диметилтіокарбамінової кислоти у вигляді білої твердої речовини. LC/MS: C 13H16N2O2 : m/z 264 (М+1). Сполуку 2.20 (39мг; 49% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2, використовуючи замість ацетилхлориду 3циклопентилпропіонілхлорид. LC/MS: C 29H35F3N2 O4S: m/z 565 (М+1). 2-[2-(3-Індан-5-іл-1-пентилуреїдо)індан-5ілсульфаніл}-2-метил-пропіонова кислота Сполука 2.21 (Приклад 29) 41 80297 Сполуку 2.21 (9,3мг; 24% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.3, використовуючи валерилхлорид замість ацетилхлориду і інданілізоціанат замість 4-трифлюорметоксифенілізоціанату. LC/MS: C 28H36N2O3S: m/z 481 (М+1). 2-Метил-2-{2-[3-(4-метил-3-нітрофеніл)-1пентилуреїдо]індан-5-ілсульфаніл}пропіонова кислота Сполука 2.22 (Приклад 30) Сполуку 2.22 (5,0мг; 12% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.3, використовуючи замість 4трифлюорметоксифенілізоціанату 4-метил-3нітрофенілізоціанат. LC/MS: C 26H33N3O5S: m/z 500 (М+1). 2-Метил-2-{2-[1-нафталін-1-ілметил-3-(4трифлюорметоксифеніл)уреїдо]-індан-5ілсульфаніл}пропіонова кислота Сполука 3.4 (Приклад31) Сполуку 3.4 (2,9мг; 4% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 3, використовуючи замість пент-4-еналю 1-нафтальдегід. LC/MS: C 32H29F3N2 O4S: m/z 595 (М+1). 2-{2-[3-(4-Метоксифеніл)-1-пропілуреїдо]індан5-ілсульфаніл}-2-метил-пропіонова кислота Сполука 2.23 (Приклад 32) 42 Сполуку 2.23 (21мг; 64% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.14, використовуючи замість 4трифлюорметоксифенілізоціанату 4метоксифенілізоціанат. LC/MS: C 24H27F3N2 O4S: m/z 443 (М+1). 2-{2-[3-(3,5-Диметилфеніл)-1пропілуреідо]індан-5-ілсульфаніл}-2-метилпропіонова кислота Сполука 2.24 (Приклад 33) Сполуку 2.24 (19мг; 57% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.14, використовуючи замість 4трифлюорметоксифенілізоціанату 3,5диметилфенілізоціанат. LC/MS: C 25H32N2O3S: m/z441 (M+1). 2-{2-[1-(2-Метоксіетил)-3-(4трифлюорметилсульфанілфеніл)уреїдо]-індан-5ілсульфаніл}-2-метилпропіонова кислота Сполука 2.25 (Приклад 34) Сполуку 2.25 (7,0мг; 16% для 2 стадій; масляниста рідина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.2, використовуючи замість ацетилхлориду метоксіацетилхлорид. LC/MS: C 24H27F3N2 O4S 2: m/z 529 (М+1). 2-Метил-2-{2-[1-пропіл-3-(4трифлюорметилфеніл)уреїдо]індан-5ілсульфаніл}пропіонова кислота Сполука 2.26 (Приклад 35) 43 80297 44 Сполуку 2.26 (20мг; 56% для 2 стадій; біла синтезом Сполуки 2.4, використовуючи замість тверда речовина) одержують згідно зі шляхом 2 та ацетилхлориду метиловий складний ефір 5синтезом Сполуки 2.14, використовуючи замість 4хлоркарбонілпентанової кислоти. трифлюорметоксифенілізоціанату 4LC/MS: C 30H40N2O5S: m/z541 (M+1). трифлюорметилфенілізоціанат. 2-Метил-2-[2-(3-нафталін-2-іл-1LC/MS: C 24H27F3N2 O3S 2: m/z 481 (М+1). пентилуреїдо)індан-5-ілсульфаніл]-пропіонова 2-Метил-2-{2-[1-(4,4,4-трифлюорбутил)-3-(4кислота трифлюорметоксифеніл)-уреїдо]індан-5Сполука 2.30 (Приклад 39) ілсульфаніл}пропіонова кислота Сполука 2.27 (Приклад 36) Сполуку 2.27 (10мг; 26% для 2 стадій; масляниста рідина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.0, використовуючи замість ацетилхлориду три флюорметилбутирилхлорид. LC/MS: C 25H26F6N2 O4S: m/z 564 (М+1). 2-{2-[1-(3-Циклопентилпропіл)-3фенілуреїдо]індан-5-ілсульфаніл}-2метилпропіонова кислота Сполука 2.28 (Приклад 37) Сполуку 2.28 (38мг; 56% для 2 стадій; масляниста рідина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.0, використовуючи циклопентилпропіонілхлорид замість ацетилхлориду та фенілізоціанат замість 4трифлюорметоксифенілізоціанату. LC/MS: C 28H36N2O3S: m/z 481 (М+1). Метиловий складний ефір 6-[1-[5-(1-карбокси1-метилетилсульфаніл)-індан-2-іл]-3-(4ізопропілфеніл)уреїдо]гексанової кислоти Сполука 2.29 (Приклад38) Сполуку 2.29 (12мг; 38% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та Сполуку 2.30 (15мг; 39% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.3, використовуючи замість 4трифлюортіометоксифенілізоціанату 2нафтилізоціанат. LC/MS: C 29H34N2O3S: m/z491 (M+1). 2-{2-[1-Циклогексилметил-3-(4трифлюорметоксифеніл)уреїдо]індан-5ілсульфаніл]-2-метилпропіонова кислота Сполука 2.31 (Приклад 40) Сполуку 2.31 (15мг; 25% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.0, використовуючи замість ацетилхлориду циклогексилацетилхлорид. LC/MS: C 28H33F3N2 O4S: m/z551 (M+1). 2-{2-[1-Ізобутил-3-(4трифлюорметоксифеніл)уреїдо]індан-5ілсульфаніл}-2-метилпропіонова кислота Сполука 3.5 (Приклад 41) Сполуку 3.5 (10мг; 12% для 2 стадій; масляниста рідина) одержують згідно зі шляхом 3 та синтезом Сполуки 3.0, використовуючи замість пент5-еналю 2-метилпропіоновий альдегід. LC/MS: C 25H29F3N2 O4S: m/z511 (M+1). 2-{2-[3-(3,4-Дихлорфеніл)-1гептилуреїдо]індан-5-ілсульфаніл}-2-метилпропіонова кислота 45 Сполука 2.32 (Приклад 42) 80297 Сполуку 2.32 (6,7мг; 12% для 2 стадій; масляниста рідина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.0, використовуючи гептаноїлхлорид замість ацетилхлориду і 3,4дихлорфенілізоціанат замість 4трифлюорметоксифенілізоціанату. LC/MS: C 27H34CI2N2O 3S: m/z 538 (М+1). 2-{2-[1-(2-Диметиламіноетил)-3-(4трифлюорметилсульфанілфеніл)-уреїдо]індан-5ілсульфаніл}-2-метилпропіонова кислота Сполука 2.33 (Приклад 43) Сполуку 2.33 (1,9мг; 4% для 2 стадій; масляниста рідина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.2, використовуючи диметиламіноацетилхлорид замість ацетилхлориду і 4трифлюорметилтіофенілізоціанат замість 4трифлюорметоксифенілізоціанату. LC/MS: C 25H30F3N3 O3S 2: m/z 542 (М+1). 2-{2-[3-(3-Хлорфеніл)-1-гептилуреїдо]індан-5ілсульфаніл}-2-метил-пропіонова кислота Сполука 2.34 (Приклад 44) Сполуку 2.34 (7,4мг; 14% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.32, використовуючи 3хлорфенілізоціанат замість 4трифлюорметоксифенілізоціанату. LC/MS: C 27H35CIN2O3S: m/z 542 (М+1). 1-{2-[1-Гептил-3-(4трифлюорметоксифеніл)уреїдо]індан-5ілсульфаніл}-циклобутанкарбонова кислота 46 Сполука 2.35 (Приклад45) Сполуку 2.35 (1,0мг; 1,3% для 2 стадій; біла тверда речовина) одержують згідно зі шляхом 2 та синтезом Сполуки 2.32, використовуючи замість трет-бутил-2-бромізобутирату етил-1бромциклобутанкарбоксилат. LC/MS: C 29H35F3N2 O4S: m/z 565 (М+1). 2-Метил-2-{7-[1-пропіл-3-(4трифлюорметоксифеніл)уреїдо}-5,6,7,8тетрагідронафталін-2-ілсульфаніл}пропіонова кислота Сполука 1.4 (Приклад 46) Сполуку 1.4 (53мг; 25% для 2 стадій; масляниста рідина) одержують згідно зі шляхом 1 та синтезом Сполуки 1.0, використовуючи замість ацетилхлориду пропіонілхлорид. LC/MS: C 25H29F3N2 O4S: m/z511 (M+1). Наступні дві сполуки можуть бути одержані згідно зі Схемами 10 та 4, Стадіями І, J та K шляху 1, при належному заміщенні реагентів та регулюванні реакційних умов: 2-{6-[1-Етил-3-(4трифлюорметоксифеніл)уреїдо]-3-метокси-5,6,7,8тетрагідронафталін-2-ілсульфаніл}-2метилпропіонова кислота Сполука 1.5 (Приклад 47) Сполука 1.5 (9,8мг; масляниста рідина) може бути одержана згідно зі шляхом 1, стадіями І, J та K, і Схемами 4 та 10. 1 Н ЯМР (300МГц, CD3OD): d 7,45-7,48 (д, 2Н), 7,15-7,18 (м, 3Н), 6,71 (с, 1Н), 4,43-4,79 (м, 1Н), 3,75 (с, 3Н), 3,43-3,45 (м, 2Н), 2,88-3,08 (м, 4Н), 1,99-2,03 (м, 2Н), 1,38 (с, 6Н), 1,25-1,52 (т, 3Н). LC/MS: C 25H29F3N2 O5S: m/z 527 (М+1). Шлях 4 47 80297 48 2-метилпропіонової кислоти у ви гляді маслянистої рідини. 1 Н ЯМР (300МГц, CDCI3): d 6,89-6,92 (д, 1Н), 6,58-6,65 (м, 2Н), 5,85-5,88 (м, 1Н), 4,24-4,30 (м, 1Н), 2,99-3,06 (дд, 1Н), 2,76-2,86 (м, 2Н), 2,51-2,59 (дц, 1Н), 2,04 (с, 2Н), 1,98-2,02 (м, 1Н), 1,74-1,79 2-{6-[1-Етил-3-(4(м, 1Н), 1,54 (с, 6Н), 1,46 (с, 9Н). трифлюорметоксифеніл)уреїдо]-5,6,7,8-тетрагідроLC/MS: C 20H29NO4: m/z 292 (М+1). нафталін-2-ілокси}-2-метилпропіонова кислота Наступні сполуки були одержані згідно зі СхеСполука 4.0 (Приклад 48) мами 3 та 4 і Стадіями І, J та K шляху 1, при налеA. N-(6-Ме токси-1,2.3.4-тетрагідронафталін-2жному заміщенні реагентів та регулюванні реакіл)ацетамід ційних умов: Схема 7. До перемішуваної суспензії 6Сполуку 4.0 (0,0168г; 23% для 2 стадій; масметокси-1,2,3,4-тетрагідронафталін-2-іламіну ляниста рідина) одержують згідно зі шляхом 1 та (2,54г; 14,3ммоль) у СН 2СІ2 (20мл) додають DIEA синтезом Сполуки 1.0. (3,4мл) і реакційну суміш охолоджують до 0°С. LC/MS: C 24H27F3N2 O5 : m/z 481 (М+1). Додають по краплях ацетилхлорид (1,22мл; 2-{6-[3-(4-Трет-бутилфеніл)-1-етилуреїдо]-317,1ммоль) при 0°С і реакції дають нагрітися до метокси-5,6,7,8-тетрагідро-нафталін-2кімнатної температури та перемішують протягом ілсульфаніл}-2-метилпропіонова кислота 18год. Реакційну суміш розводять СН 2СІ2, промиСполука 1.6 (Приклад 49) вають Н2О, осушають над Na2SO4, фільтрують та розчинник видаляють при зниженому тиску, одержуючи сирову тверду речовину. Очистка флешхроматографією (SiO2) з елююванням гексанамиEtOAc дає 1,57г (50%) N-(6-метокси-1,2,3,4тетрагідронафталін-2-іл)ацетамід у вигляді білої твердої речовини. LC/MS: C 13H17NO2: m/z220 (M+1). Сполука 1.6 (10мг; масляниста рідина) може B. N-(6-Гідрокси-1.2.3.4-тетрагідронафталін-2бути одержана, використовуючи замість 4іл)ацетамід трифлюорметоксифенілізоціанату 4-третСхема 7. До суспензії N-(6-метокси-1,2,3,4бутилфенілізоціанат, згідно зі Шляхом 1, стадії І, J тетрагідронафталін-2-іл)ацетаміду (1,57г; та K, і С хемами 4 та 10. 7,2ммоль) у СН 2СІ2 (70мл), охолодженої до -60°С, LC/MS: C 28H38N2O4S: m/z 499 (М+1). додають по краплях розчин броміду бору-СН 2СІ2 2-{6-[1-Етил-3-(4(36мл) таким чином, щоб підтримувати температутрифлюорметоксифеніл)уреїдо]-3-флюор-5,6,7,8ру реакції в інтервалі від -50 до -60°С. Желеподібтетра-гідронафталін-2-ілсульфаніл}-2ній суспензії дають нагрітися до кімнатної темпеметилпропіонова кислота ратури та перемішують протягом 30хв. Реакцію Сполука 1.7 (Приклад 50) охолоджують до 0°С, гасять насич.NaНСО3 та перемішують протягом 30хв. при кімнатній температурі. Суміш екстрагують СН 2СІ2 (2´), екстракти об'єднують, осушають над Na2SO4, фільтрують та випаровують при зниженому тиску, одержуючи сирову тверду речовину, яку очищають флешхроматографією (SiO2), елююючи градієнтом СН2СІ2-МеОН, одержуючи 1,13г (76%) N-(6Сполука 1.7 (16мг; 30% після 2 стадій; біла гідрокси-1,2,3,4-тетрагідронафталін-2-іл)ацетаміду тверда речовина) може бути одержана згідно зі у вигляді твердої речовини бежевого кольору. шляхом 1, стадії І, J та K, і Схемами 4 та 10. 1 LC/MS: C 12H15NO2: m/z 206 (M+1). Н ЯМР (300МГц, CDCI3): d 7,46-7,51 (м, 2Н), C. Трет-бутиловий складний ефір 2-(67,25-7,28 (д, 1Н), 7,17-7,20 (д, 2Н), 6,92-6,95 (д, ацетиламіно-5,6,7,8-тетрагідро-нафталін-2-ілокси)1Н), 4,43 (м, 1Н), 3,42-3,49 (м, 2Н), 2,90-3,11 (м, 2-метилпропіонової кислоти 4Н), 2,02-2,07 (м, 2Н), 1,45 (с, 6Н), 1,25-1,31 (т, 3Н). Схема 7. До суспензії N-(6-гідрокси-1,2,3,4LC/MS: C 25H29F3N2 O5S: m/z 515 (М+1). тетрагідронафталін-2-іл)ацетаміду (0,439г; 2-{6-[1-Етил-3-(42,1ммоль) у ДМФ (6мл) додають Cs 2CO3 (1,7г; трифлюорметоксифеніл)уреїдо]-3-хлор-5,6,7,85,2ммоль) та трет-бутил-2-бромізобутират (2,1мл; тетра-гідронафталін-2-ілсульфаніл}-29,4ммоль) і реакційну суміш перемішують при метилпропіонова кислота 100°С протягом 18год. Реакцію охолоджують до Сполука 1.8 (Приклад 51) кімнатної температури, розводять EtOAc, промивають Н2О, розсолом, осушають над Na2SO4, фільтрують та розчинник видаляють при зниженому тиску, одержуючи сирову маслянисту рідину, яку очищають флеш-хроматографією (SiO2), елююючи градієнтом гексани-EtOAc, одержуючи 0,51г (69%) трет-бутилового складного ефіру 2-(6ацетиламіно-5,6,7,8-тетрагідронафталін-2-ілокси)Сполука 1.8 (15мг; 22% після 2 стадій; біла 49 80297 50 тверда речовина) може бути одержана згідно зі метилпропіонова кислота шляхом 1, стадії І, J та K, і Схемами 4 та 10. Сполука 1.12 (Приклад 55) LC/MS: C 25H29F3N2 O5S: m/z 532 (М+1). 2-{6-[1-Етил-3-(4трифлюорметоксифеніл)уреїдо]-3-бром-5,6,7,8тетра-гідронафталін-2-ілсульфаніл}-2метилпропіонова кислота Сполука 1.9 (Приклад 52) Сполука 1.9 (55мг; 43% для 2 стадій; біла тверда речовина) може бути одержана згідно зі шляхом 1, стадії І, J та K, і Схемами 4 та 10. 1 Н ЯМР (300МГц, CDCI3): d 7,45-7,48 (м, 3Н), 7,36 (с, 1Н), 7,15-7,18 (д, 2Н), 4,41-4,79 (м, 1Н), 3,40-3,47 (м, 2Н), 2,90-3,07 (м, 4Н), 2,01-2,03 (м, 2Н), 1,45 (с, 6Н), 1,24-1,29 (т, 3Н). LC/MS: C 25H29F3N2 O5S: m/z 576 (М+1). 2-{6-[1-Етил-3-(4трифлюорметоксифеніл)уреїдо]-3-метил-5,6,7,8тетра-гідронафталін-2-ілсульфаніл}-2метилпропіонова кислота Сполука 1.10 (Приклад 53) Сполука 1.10 (73мг; 26% для 2 стадій; біла тверда речовина) може бути одержана згідно зі шляхом 1, стадії І, J та K, і Схемами 4 та 10. 1 Н ЯМР (300МГц, CDCI3): d 7,45-7,48 (м, 2Н), 7,22 (с, 1Н), 7,15-7,18 (д, 2Н), 7,02 (с, 1Н), 4(41-4,79 (м, 1Н), 3,40-3,47 (м, 2Н), 2,85-3,03 (м, 4Н), 2,39 (с, 3Н), 2,01-2,03 (м, 2Н), 1,41 (с, 6Н), 1,24-1,29 (т, 3Н). LC/MS: C 25H29F3N2 O5S: m/z 511 (М+1). 2-{6-[1-Етил-3-(4трифлюорметоксифеніл)уреїдо]-3трифлюорметокси-5,6,7,8-тетрагідронафталін-2ілсульфаніл}-2-метилпропіонова кислота Сполука 1.11 (Приклад 54) Сполука 1.11 (118мг; 58% для 2 стадій; біла тверда речовина) може бути одержана згідно зі шляхом 1, стадії І, J та K, і Схемами 4 та 10. 1 Н ЯМР (300МГц, CDCI3): d 7,45-7,48 (д, 2Н), 7,37 (с, 1Н), 7,12-7,18 (м, 3Н), 4,44 (м, 1Н), 3,433,48 (м, 2Н), 2,97-3,21 (м, 4Н), 2,03-2,05 (м, 2Н), 1,42 (с, 6Н), 1,25-1,30 (т, 3Н). LC/MS: C 25H29F3N2 O5S: m/z 580 (М+1). 2-{6-[1-Етил-3-(4трифлюорметоксифеніл)уреїдо]-3-феніл-5,6,7,8тетра-гідронафталін-2-ілсульфаніл}-2 Сполука 1.12 (118мг; 58% для 2 стадій; біла тверда речовина) може бути одержана згідно зі шляхом 1, стадії І, J та K, і Схемами 4 та 10. 1 Н ЯМР (300МГц, CDCI3): d 7,45-7,48 (д, 2Н), 7,29-7,38 (м, 6Н), 7,15-7,18 (д, 2Н), 7,10 (с, 1Н), 4,46 (м, 1Н), 3,44-3,49 (м, 2Н), 2,98-3,06 (м, 4Н), 2,04-2,06 (м, 2Н), 1,26-1,30 (т, 3Н), 1,14 (с,6Н). LC/MS: C 25H29F3N2 O5S: m/z 573 (М+1). 2-{6-[1-Етил-3-(4-гідроксифеніл)уреїдо]-5,6,7,8тетрагідронафталін-2-ілсульфаніл}-2метилпропіонова кислота (Приклад 56) 2-{6-[4-Амінофеніл)-1-етилуреїдо]-5,6,7,8тетрагідронафталін-2-ілсульфаніл}-2метилпропіонова кислота (Приклад 57) Шлях 5 Трет-бутиловий складний ефір 2-[3-хлор-6(етил-п-толілоксикарбоніл-аміно)-5,6,7,8тетрагідронафталін-2-ілсульфаніл]-2метилпропіонової кислоти. Сполука 5.0 (Приклад 58) До суміші трет-бутилового складного ефіру та боранового комплексу 2-(3-хлор-6-етиламіно5,6,7,8-тетрагідронафталін-2-ілсульфаніл)-2метил-пропіонової кислоти (80мг; 201мкмоль), розчиненої у СН 2СІ2 (2мл), додають при 0°С птолілхлорформіат (35мкл; 241мкмоль). Реакцію повільно нагрівають до кімнатної температури та залишають при перемішуванні при кімнатній температурі на 6 днів. Розчинник видаляють при зниженому тиску і сировий залишок очищають флешхроматографією (SiO2), елююючи градієнтом гексанів-EtOAc, одержуючи 30мг (29%) третбутилового складного ефіру 2-[3-хлор-6-(етил-птолілоксикарбоніламіно)-5,6,7,8тетрагідронафталін-2-ілсульфаніл]-2метилпропіонової кислоти у вигляді прозорої мас 51 80297 52 лянистої рідини. трифлюорметоксифенілового складного ефіру 11 хлоретилового складного ефіру вугільної кислоти у Н ЯМР (300МГц, CDCI3): d 6,67-7,29 (м, 6Н), 4,28 (м, 1Н), 3,40 (м, 2Н), 2,87-2,97 (м, 4Н), 2,33 (с, вигляді безбарвної маслянистої рідини. 1 3Н), 1,89-2,06 (м, 2Н), 1,39-1,46 (м, 15Н), 1,21-1,31 Н ЯМР (400МГц, CDCI3): d 7,26 (м, 4Н), 6,49 (м, 3Н). (кв, 1Н), 1,91 (д, 3Н). Сполуку 5.0 (23мг; 59%) одержують згідно зі B. 4-Трифлюорметоксифеніловий складний стадією Μ шля ху 2. ефір етил-(6-метокси-1,2,3,4-тетрагідронафталін1 2-іл)карбамінової кислоти Н ЯМР (300МГц, CD3OD): d 6,96-7,34 (м, 6Н), Схема 1. До суміші 6-метокси-2-тетралону 4,27 (м, 1Н), 3,49 (м, 2Н), 2,91-3,14 (м, 4Н), 2,32 (с, (950мг; 5,39ммоль), 2М етиламіну у ТГФ (5,4мл; 3Н), 2,10 (м, 2Н), 1,45 (м, 6Н), 1,28 (м, 3Н). 10,78ммоль) та оцтової кислоти (648мг; LC/MS: C 24H28CINO4S: m/z 462 (M+1). 10,78ммоль) у СН 2СІ2 (5мл) додають триацетокси2-{3-Хлор-6-[(4боргідрид натрію (2,29г; 10,78ммоль). Реакційну хлорфеноксикарбоніл)етиламіно]-5,6,7,8суміш перемішують при кімнатній температурі протетрагідро-нафталін-2-ілсульфаніл}-2тягом 3год., потім додають 1Н розчин NaOH та метилпропіонова кислота екстрагують ефіром (3 рази). Об'єднані органічні Сполука 5.1 (Приклад 59) екстракти осушають над Na2SO4 та розчинник видаляють при зниженому тиску, одержуючи світложовту маслянисту рідину. Цю маслянисту рідину додають до розчину 4трифлюорметоксифенілового складного ефіру 1хлоретилового складного ефіру вугільної кислоти (1,23г; 4,31ммоль) у толуолі (8мл), і реакційну суСполуку 5.1 (34мг; 35% для 2 стадій; біла твеміш перемішують протягом 1год. при кімнатній рда речовина) одержують згідно зі шляхом 5, витемпературі, а потім 1год. при 90°С. Реакції дають користовуючи 4-хлорфенілхлорформіат замість похолонути до кімнатної температури, розводять толілхлорформіату, та стадією Μ шля ху 2. Et2O та промивають 1Н водн. НСІ та насиченим 1 NаНСО3. Органічний екстракт осушають над Н ЯМР (300МГц, CD3OD): d 7,11-7,39 (м, 6Н), Na2SO4 та розчинник видаляють при зниженому 4,30 (м, 1Н), 3,47 (м, 2Н), 2,91-3,15 (м, 4Н), 2,06 (м, тиску. Флеш-хроматографія залишку градієнтом 2Н), 1,45 (м, 6Н), 1,28 (м, 3Н). гексану-СН 2СІ2 дає 1,05г (48%) 4LC/MS: C 23H25CI2NO4S: m/z482 (M+1). 2-{6-[Етил-(4трифлюорметоксифенілового складного ефіру етил-(6-метокси-1,2,3,4-тетрагідронафталін-2трифлюорметоксифеноксикарбоніл)аміно]-5,6,7,8іл)карбамінової кислоти у вигляді білої твердої тетрагідронафталін-2-ілсульфаніл}-2речовини. метилпропіонова кислота 1 Сполука 5.2 (Приклад 60) Н ЯМР (400МГц, CDCI3): d 7,10-7,30 (м, 4Н), 6,99 (д, 1Н), 6,71 (д, 1Н), 6,64 (с, 1Н), 4,33 (м, 1Н), 3,77 (с, 3Н), 3,41 (м, 2Н), 2,93 (м, 4Н), 2,04 (м, 2Н), 1,31 (м, 3Н). LC/MS: C 21H23F3NO 4: m/z410 (M+1). С. 4-Трифлюорметоксифеніловий складний ефір етил-(6-гідрокси-1,2,3.4-тетрагідронафталін2-іл)карбамінової кислоти Сполука 5.2 може бути одержана згідно зі Схема 1. Розчин 4шляхом 5, використовуючи 4трифлюорметоксифенілового складного ефіру трифлюорметоксифеніловий складний ефір 1етил-(6-метокси-1,2,3,4-тетрагідронафталін-2хлоретилового складного ефіру вугільної кислоти іл)карбамінової кислоти (898,6мг; 2,19ммоль) у замість п-толілхлорформіату, та стадією Μ шлябезводному СН2СІ2 (8мл) охолоджують до -78°С та ху 2. додають повільно 1,0М розчин броміду боруАльтернативно, сполука 5.2 може бути одерСН2СІ2 (6,57мл, 6,57ммоль). Після закінчення дожана з використанням таких процедур: давання, реакційній суміші дають нагрітися до кімA. 4-Трифлюорметоксифеніловий складний натної температури, гасять МеОН (10мл) та переефір 1-хлоретилового складного ефіру вугільної мішують протягом ще 2год. Розчинники кислоти випаровують та залишок очищають флешСхема 1. Розчин 1-хлоретилхлорформіату хроматографією з гексаном-EtOAc (2,5:1), одер(1,03г; 7,20ммоль) у СН 2СІ2 (10мл) охолоджують жуючи 649,4мг (75%) 4до 0°С, додають трифлюорметоксифенол (1,09г; трифлюорметоксифенілового складного ефіру 6,0ммоль) та триетиламін і одержаний розчин наетил-(6-гідрокси-1,2,3,4-тетрагідронафталін-2грівають до кімнатної температури. Після перемііл)карбамінової кислоти у вигляді білої твердої шування протягом 3год. реакцію гасять насиченим речовини. 1 NaHCO3 та екстрагують EtOAc (3 рази). Об'єднані Н ЯМР (300МГц, CDCI3): d 7,05-7,30 (м, 4Н), органічні екстракти промивають водою, розсолом, 6,90 (м, 1Н), 7,41-7,60 (м, 2Н), 5,05 (с, 1Н), 4,30 (м, осушають над Na2SO4 і розчинник видаляють при 1Н), 3,41 (м, 2Н), 2,90 (м, 4Н), 1,99 (м, 2Н), 1,31 (м, зниженому тиску. Сировий залишок очищають 3Н). флеш-хроматографією, елююючи гексаном-EtOAc LC/MS: C 20H21F3NO 4: m/z 396 (M+1). (10:1), одержуючи 1,54г (90%) 4D. 4-Трифлюорметоксифеніловий складний 53 80297 54 ефір етил-(6-триізопропіл-силанілсульфанілтетрагідронафталін-2-ілсульфаніл)-21,2.3.4-тетрагідронаФталін-2-іл)карбамінової кисметилпропіонова кислота лоти Схема 1. Розчин трет-бутилового складного Схема 1. Розчин 4ефіру 2-{6-[етил-(4трифлюорметоксифенілового складного ефіру трифлюорметоксифеноксикарбоніл)аміно]-5,6,7,8етил-(6-гідрокси-1,2,3,4-тетрагідронафталін-2тетрагідронафталін-2-ілсульфаніл}-2іл)карбамінової кислоти (245,1мг; 0,62ммоль) у метилпропіонової кислоти (120,8мг; 0,22ммоль) у безводному СН 2СІ2 (3мл) та ТГФ (3мл) охолоджуСН2СІ2 (4мл) охолоджують до -78°С та додають ють до -30°С, додають послідовно триетиламін повільно трифлюороцтову кислоту (4мл). Реакцій(216мкл, 1,55ммоль) та трифлюорметансульфононій суміші дають нагрітися до кімнатної темперавий ангідрид (125мкл, 0,74ммоль). Одержану сутури та перемішують протягом 1,5год. Розчинники міш перемішують при кімнатній температурі протяпотім випаровують та залишок очищають флешгом 2год., потім гасять водою та екстрагують Et2O хроматографією з СН 2СІ2-МеОН (94:6), одержуючи (3 рази). Об'єднані органічні екстракти промивають 2-{6-[етил-(4водою, розсолом, осушають над Na2SO4 та розтрифлюорметоксифеноксикарбоніл)аміно]-5,6,7,8чинник видаляють при зниженому тиску. Флештетрагідронафталін-2-іл-сульфаніл}-2хроматографія залишку з гексаном-EtOAc (5:1) дає метилпропіонову кислоту у вигляді білої твердої 301,6мг (92%) трифлату. Цей трифлат (279,8мг; речовини. 1 0,53ммоль) та тетракіс(трифенілфосфін)паладій Н ЯМР (400МГц, CDCI3): d 6,96-7,28 (м, 7Н), (61,2мг; 0,053ммоль) додають до толуольного роз4,30 (м, 1Н), 3,39 (м, 2Н), 2,85-3,10 (м, 4Н), 2,06 (м, чину, утвореного з триізопропілсилантіолу 2Н), 1,49 (с, 6Н), 1,28 (м, 3Н). (126мкл, 0,58ммоль) та NaH (13,9мг; 0,58ммоль) LC/MS: C 24H27F3NO 5S: m/z 498 (М+1). при кімнатній температурі. Одержану суміш двічі D. Композиції та введення вакуум ують та кип'ятять зі зворотним холодильниСполуки за даним винаходом можуть бути ком протягом 4год. і концентрують при зниженому включені до складу різних фармацевтичних форм, тиску. Флеш-хроматографія залишку з гексаномпризначених для введення. Для приготування таEtOAc (10:1) дає 261,8мг (87%) 4ких фармацевтичних композицій ефективну кільтрифлюорметоксифенілового складного ефіру кість певної сполуки, у формі солі приєднання осетил-(6-триізопропілсиланілсульфаніл-1,2,3,4нови чи кислоти, як активний інгредієнт, ретельно тетрагідро-нафталін-2-іл)карбамінової кислоти у змішують з фармацевтично прийнятним носієм. вигляді світлої маслянистої рідини. Носій може набувати різноманітних форм у 1 Н ЯМР (300МГц, CDCI3): d 6,82-7,29 (м, 7Н), залежності від форми препарату, бажаної для 4,32 (м, 1Н), 3,40 (м, 2Н), 2,81-3,05 (м, 4Н), 2,05 (м, введення. Такі фармацевтичний композиції, кра2Н), 1,12-1,34 (м, 6Н), 1,03-1,10 (м, 18Н). ще, є разовими дозованими формами, придатниLC/MS: C 29H41F3NO 3SSi: m/z 568 (М+1). ми, краще, для перорального введення чи паренE. Трет-бутиловий складний ефір 2-(6-Гетилтеральної ін'єкції. Наприклад, при виготовленні (4-трифлюорметоксифеноксикарбоніл)аміно]композицій у вигляді дозованих форм для перора5,6,7,8-тетрагідронафталін-2-ілсульфаніл)-2льного введення, може бути застосоване будь-яке метил-пропіонової кислоти придатне фармацевтичне середовище. Такі сереСхема 1. Розчин 4довища включають воду, гліколі, масла, спирти і трифлюорметоксифенілового складного ефіру т.п. у випадку рідких препаратів для перорального етил-(6-триізопропілсиланілсульфаніл-1,2,3,4введення, таких як суспензії, сиропи, еліксири та тетрагідронафталін-2-іл)карбамінової кислоти розчини; або тверді носії, такі як крохмалі, цукри, (260,0мг; 0,46ммоль) та трет-бутил-2каолін, змащувальні речовини, зв'язуючі, розпушубромізобутирату (130мкл, 0,69ммоль) у безводновальні агенти і т.п., у випадку порошків, пілюль, му ТГФ (2мл) охолоджують до 0°С, додають 1,0М капсул та таблеток. Через зручність введення, розчин TBAF (690мкл, 0,69ммоль), а потім реакцію таблетки та капсули є найкращими дозованими нагрівають до кімнатної температури, перемішуформами для перорального введення, у яких звиють протягом 1год. та розводять водою, екстрагучайно використовують тверді фармацевтичні носії. ють Et2O (3 рази). Об'єднані органічні екстракти Для парентеральних композицій носій буде звиосушають над Na2SO4 та розчинник видаляють чайно включати стерильну воду, принаймні, здебіпри зниженому тиску. Сировий залишок очищають льшого, хоч можуть бути включені інші інгредієнти, флеш-хроматографією, елююючи гексаном-EtOAc наприклад, для поліпшення розчинності. Можуть (7:1), одержуючи 229,2мг (90%) трет-бутилового бути одержані, наприклад, розчини для ін'єкцій, у складного ефіру 2-{6-[етил-(4яких носій включає сольовий розчин, розчин глютрифлюорметоксифеноксикарбоніл)аміно]-5,6,7,8кози чи суміш сольового та глюкозного розчинів. тетрагідронафталін-2-ілсульфаніл}-2Також можуть бути виготовлені суспензії для ін'єкметилпропіонової кислоти у вигляді світлої масляцій, у яких можуть бути використані придатні рідкі нистої рідини. носії, суспендувальні агенти і т.п. В композиціях, 1 придатних для підшкірного введення, носій необоН ЯМР (300МГц, CDCI3): d 6,95-7,28 (м, 7Н), в'язково включає агент посилення проникнення 4,34 (м, 1Н), 3,41 (м, 2Н), 2,96 (м, 2Н), 2,91 (м, 2Н), та/або придатний змочувальний агент, необов'яз3,41 (м, 2Н), 2,06 (м, 2Н), 1,44 (с, 6Н), 1,42 (с, 9Н), ково, разом з придатними домішками будь-якого 1,28 (м, 3Н). характеру у невеликій кількості, що не мають знаLC/MS: C 28H34F3NO 5SNa: m/z 576 (M+Na). чного шкідливого впливу на шкіру. Такі домішки F. 2-(6-[Етил-(4можуть сприяти введенню до шкіри та/або можуть трифлюорметоксифеноксикарбоніл)аміно1-5.6.7.8 55 80297 56 бути корисними для виготовлення бажаної компомає хіральний центр в положенні С-2. Для цієї зиції. Ці композиції можуть бути введені різними сполуки, (S)-ізомер є більш активним, ніж (R)шляхами, наприклад, у вигляді трансдермального ізомер. пластиря, засобу для місцевого введення чи рідкої Фахівці в області лікування розладів чи станів, мазі. Солі приєднання кислот сполуки формули І, медійованих PPAR-альфа, можуть легко визначизавдяки їхній підвищеній розчинності у воді порівти ефективну добову кількість з наведених тут няно з відповідною основною формою, є більш кращих результатів випробувань та іншої інфорпридатними для виготовлення водних композицій. мації. Загалом, передбачається, що терапевтично Особливо зручно виготовляти вищезгадані ефективна доза буде складати від 0,001мг/кг до фармацевтичні композиції у вигляді дозованих 5мг/кг ваги тіла, краще, від 0,01мг/кг до 0,5мг/кг лікарських форм через зручність їхнього введення ваги тіла. Може виявитися зручним введення тета рівномірність доз. Дозовані лікарські форми в рапевтично ефективної дози у вигляді двох, трьох, тому значенні, що використовується в опису, сточотирьох чи більше субдоз з відповідними інтерсуються фізично окремих одиниць, придатних для валами часу протягом доби. Зазначені субдози застосування як разові дози, кожна з яких містить можуть бути приготовлені як разові дозовані лікарпопередньо визначену кількість активногоінгредіські форми, наприклад, такі, що містять від 0,05мг єнта, розраховану на продукування бажаного тедо 250мг чи 750мг, зокрема, від 0,5 до 50мг, активрапевтичного ефекту, у поєднанні з потрібним фаного інгредієнта на разову дозовану форму. Прирмацевтичним носієм. Прикладами таких разових клади включають дозовані форми, що містять 2мг, дозованих форм є таблетки (включаючи таблетки 4мг, 7мг, 10мг, 15мг, 25мг та 35мг. Сполуки за виз надрізом чи таблетки з покриттям), капсули, пінаходом можуть також бути виготовлені у вигляді люлі, пакетики з порошками, облатки, розчини чи композицій з уповільненим вивільненням чи комсуспензії для ін'єкцій, пакетики, що містять 5 чи позицій для підшкірного введення чи трансдерма15мл суспензії препарату для перорального ввельних пластирів. Розкрита сполука може також дення і т.п., та їхні кратні частки. бути введена до композиції спрею чи іншої компоФармацевтично прийнятні солі приєднання кизиції для локального введення чи введення шляслот включають терапевтично активні нетоксичні хом інгаляції. форми солей приєднання кислоти, які можуть Точні дози та частота введення залежать від утворювати розкриті сполуки. Вони можуть бути конкретної сполуки формули (І), що використовузручно одержані шляхом обробки основної форми ється, конкретного стану, що лікується, тяжкості відповідною кислотою. Придатні кислоти включастану, що лікується, віку, ваги та загального фізичють, наприклад, неорганічні кислоти, такі як галоїного стану конкретного пацієнта, а також інших дводневі кислоти, наприклад, хлористоводневу чи ліків, які може приймати пацієнт, як добре відомо бромистоводневу кислоту; сірчану; азотну; фосфа хівцям в цій області. Крім того, очевидно, що форну і т.п. кислоти; чи органічні кислоти, такі як, зазначена ефективна добова кількість може бути наприклад, оцтова, пропіонова, гліколева, молочзменшена чи збільшена у залежності від реакції на, піровиноградна, щавлева, малонова, бурштипацієнта, що лікується, та/або у залежності від нова, малеїнова, фумарова, яблучна, винна, лиоцінки лікаря, який призначив сполуки за даним монна, метансульфонова, етансульфонова, винаходом. Зазначені тут інтервали величин ефебензолсульфонова, п-толуолсульфонова, циклактивних добових доз є, таким чином, лише орієнмова, саліцилова, п-аміносаліцилова, памоєва і товними. т.п. кислоти. Термін сіль приєднання кислоти таНаступний розділ включає детальну інформакож включає сольвати, які є здатними утворювати цію, що стосується використання розкритих сполук розкриті сполуки, а також їхні солі. Такими сольвата композицій. тими є, наприклад, гідрати, алкоголяти і т.п. НаЕ. Використання впаки, сольова форма може бути перетворена Сполуки за даним винаходом є фармацевтичшляхом обробки лугами на форму вільної основи. но активними, наприклад, як агоністи PPARСтереоізомерні форми охоплюють всі можливі альфа. Згідно з одним аспектом винаходу, сполуки ізомерні форми, які можуть мати сполуки формули є, краще, селективними агоністами PPAR-альфа, (І). Якщо не вказується чи зазначається інше, хіміякі мають показник активності (наприклад, відночна назва сполуки позначає суміш всіх можливих шення активності щодо PPAR-альфа до активності стереохімічно ізомерних форм, причому зазначена щодо PPAR-гамма) 10 чи більше, краще, 15, 25, суміші містить всі діастереомери та енантіомери 30, 50 чи 100 або більше. базової молекулярної структури. Конкретніше, Агоністи PPAR-альфа є корисними для лікустереогенні центри можуть мати (R)- чи (S)вання, профілактики чи інгібування розвитку одноконфіурацію; замісники на бівалентних циклічних го чи кількох з таких станів чи хвороб: фаза І гінасичених радикалах можуть мати цис- чи трансперліпідемії, передклінічна гіперліпідемія, фаза II конфіурацію. Винахід охоплює стереохімічно ізогіперліпідемії, гіпертензія, ІХС (ішемічна хвороба мерні форми, включаючи діастереоізомери, а тасерця), коронарна хвороба та гіпертригліцеридекож їхні суміші з будь-яким співвідношенням розмія. Кращі сполуки за винаходом є корисними для критих сполук. Розкриті сполуки можуть також зниження рівнів у сироватці ліпопротеїдів нізької існувати в таутомерних формах. Такі форми, хоч густини (LDL), ліпопротеїдів проміжної густини не вказані явно у ви щенаведеному описі та у на(IDL) та/або LDL малої густини та інши х а терогенведених нижче формулах, мають вважатися такиних молекул чи молекул, які спричинюють атероми, що входять до обсягу даного винаходу. Наприсклеротичні ускладнення, тим самим зменшуючи клад, у Сполуці 2.1 чи Прикладі 3, інданове кільце серцево-судинні ускладнення. Кращі сполуки є 57 80297 58 також корисними для підвищення рівнів у сироватAtromid, Lopid та Тrісоr. ці ліпопротеїдів високої густини (HDL), для зниПриклади агентів для зниження кров'яного тиження рівнів у сироватці тригліцеридів, LDL та/або ску включають антигіпертензивні агенти, такі як вільних жирних кислот. Бажано також знижувати інгібітори ангіотензин-конвертуючого фермента FPG/HbA1c. (АСЕ) (Accupril, Altace, Captopril, Lotensin, Mavik, Комбінована терапія Monopril, Prinivil, Univasc, Vasotec та Zestril), адреСполуки за даним винаходом можуть бути виноблокатори (такі як Cardura, Dibenziline, Hylorel, користані у комбінації з іншими фармацевтично Hytrin, Minipress та Minizide), альфа/бетаактивними агентами. Такі агенти включають агенти адреноблокатори (такі як Coreg, Normodyne та зниження рівня ліпідів та агенти зниження кров'яTrandate), блокатори кальцієвих каналів (такі як ного тиску. Adalat, Calan, Cardene, Cardizem, Covera-HS, Фахівцям в цій області відомі способи визнаDilacor, DynaCirc, Isoptin, Nimotop, Norvace, Plendil, чення ефективних доз для терапевтичного та Procardia, Procardia XL, Sula, Tiazac, Vascor та профілактичного застосування розкритих фармаVerelan), діуретики, антагоністи рецепторів ангіоцевтичних композицій чи розкритих комбінацій тензину II (такі як Atacand, Avapro, Cozaar та ліків, незалежно від того, входять вони до складу Diovan), бета-адреноблокатори (такі як Betapace, однієї композиції чи ні. Для терапевтичного застоBlocadren, Brevibloc, Cartrol, Inderal, Kerlone, сування, термін "спільна ефективна кількість" в Lavatol, Lopressor, Sectral, Tenormin, Toprol-XL та тому значенні, що використовується тут, означає Zebeta), вазодилататори (такі як Deponit, Dilatrate, таку кількість кожної активної сполуки чи фармаSR, Imdur, Ismo, Isordil, Isordil Titradose, Monoket, цевтичного агента, окремо чи в комбінації, що виNitro-Bid, Nitro-Dur, Nitrolingual Spray, Nitrostat та кликає біологічну чи медичну відповідь у тканинній Sorbitrate) та їхні комбінації (такі як Lexxel, Lotrel, системі, тварини чи людини, якої домагається доTarka, Teczem, Lotensin HCT, Prinzide, Uniretic, слідник, ветеринар, лікар чи інший клініцист, яка Vaseretic, Zestoretic). включає полегшення симптомів хвороби чи розлаF. Приклади ду, що лікується. Для профілактичного застосуНаступні хімічні та біологічні приклади мають вання (тобто, інгібування початку чи розвитку розілюструвати винахід, не обмежуючи його. ладу), термін "спільна ефективна кількість" Приклад 1 стосується такої кількості кожної активної сполуки чи фармацевтичного агента, окремо чи у комбінації, яка лікує чи інгібує у суб'єкта початок чи розвиток розладу, як цього домагається дослідник, ветеринар, лікар чи інший клініцист. Таким чином, даний винахід пропонує комбінації двох чи більше лікарських засобів, у яких, наприклад, (а) кожний лікарський засіб вводять у незалежно терапевтич2-{6-[1-Етил-3-(4но чи профілактично ефективній кількості; (b) щотрифлюорметоксифеніл)уреїдо]-5,6,7,8найменше один лікарський засіб у комбінації ввотетрагідронафталін-2-ілсульфаніл}-2дять у кількості, що є субтерапевтичною чи метилпропіонова кислота субпрофілактичною при його окремому введенні, ЕС50=0,023мкМ але є терапевтичною чи профілактичною при ввеПриклад 2 денні у комбінації з другим чи додатковими лікарськими засобами за винаходом; чи (с) обидва лікарські засоби (чи більшу їхню кількість) вводять у кількості, що є субтерапевтичною чи субпрофілактичною при окремому введенні, але є терапевтичною чи профілактичною при введенні разом. Як агоністи PPAR-альфа, сполуки за винаходом можуть бути більш активними та ефективними щодо зниження тригліцеридів, ніж відомі фібрати. 2-{2-[1-Етил-3-(4Сполуки за даним винаходом можуть також поситрифлюорметоксифеніл)уреїдо]індан-5лювати метаболізм жирів та/або ліпідів, забезпеілсульфаніл}-2-метил-пропіонова кислота чуючи спосіб втрати ваги, втрати кількості жиру, ЕС50=0,027мкМ зниження індексу маси тіла, зниження ліпідів (такоПриклад 3 го як зниження тригліцеридів) або лікування ожиріння чи стану надлишкової ваги. Приклади агентів для зниження ліпідів включають засоби посилення екскреції на основі жовчної кислоти, похідні фібринової кислоти, нікотинову кислоту та інгібітори HMGCoA-редуктази. Конкретні приклади включають статини, такі як LIPITORÔ , ZOCORÔ , PRAVACHOLÔ , LESCOLÔ і MEVACORÔ , пітавастатин (нісвастатин) (Nissan, Kowa Kogyo, Sankyo, (S)-2-{2-[1-Етил-3-(4Novartis) та їхні форми з уповільненим вивільнентрифлюорметоксифеніл)уреїдо]індан-5ням, такі як ADX-159 (ловастатин з уповільненим ілсульфаніл}-2-метилпропіонова кислота вивільненям), а також Colestid, Locholest, Questran, 59 ЕС50=0,0002мкМ Приклад 4 2-{2-[1-Етил-3-(4трифлюорметилсульфанілфеніл)уреїдо]індан-5ілсульфаніл}-2-метилпропіонова кислота ЕС50=0,037мкМ Приклад 5 2-Метил-2-{2-[1-пентил-3-(4трифлюорметилсульфанілфеніл)уреїдо]індан-5ілсульфаніл}пропіонова кислота ЕС50=0,053мкМ Приклад 6 2-{2-[1-Етил-3-(4-ізопропілфеніл)уреїдо]індан5-ілсульфаніл}-2-метилпропіонова кислота ЕС50=0,056мкМ Приклад 7 80297 60 2-Метил-2-{2-[1-пентил-3-(4трифлюорметоксифеніл)уреїдо]індан-5ілсульфаніл}-2-метилпропіонова кислота ЕС50=0,073мкМ Приклад 9 2-{2-[3-(4-Диметиламінофеніл)-1пентилуреїдо]індан-5-ілсульфаніл}-2-метилпропіонова кислота ЕС50=0,131мкМ Приклад 10 2-{2-[3-(4-ізопропілфеніл)-1-(3пентил)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонова кислота ЕС50=0,165мкМ Приклад 11 2-{2-[3-(4-Диметиламінофеніл)-1етилуреїдо]індан-5-ілсульфаніл}-2-метилпропіонова кислота ЕС50=0,075мкМ Приклад 8 2-{2-[3-(4-Трет-бутилфеніл)-1-(3пентил)уреїдо]індан-5-ілсульфаніл}-2-метилпропіонова кислота ЕС50=0,173мкМ Приклад 12
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted tetralins and indanes
Автори англійськоюChen Xiaoli, Matthews Jay M., Matthews, Jay, M., Demarest Keith T., Rybczynski Philip, Lee Jung
Назва патенту російськоюЗамещенные тетралины и инданы
Автори російськоюЧен Сяоли, Меттьюз Джей М., Демарест Кейт T., Рибчински Филип, Ли Джанг
МПК / Мітки
МПК: A61P 3/06, C07C 275/28, C07C 275/34, C07C 323/52, A61P 9/10, C07C 323/44, A61P 9/12
Мітки: тетраліни, заміщені, індани
Код посилання
<a href="https://ua.patents.su/36-80297-zamishheni-tetralini-ta-indani.html" target="_blank" rel="follow" title="База патентів України">Заміщені тетраліни та індани</a>
Попередній патент: Імідазолопіридини та їх застосування у терапії
Наступний патент: Похідні 1н-1,2,4-триазол-3-карбоксаміду як ліганди рецепторів канабіноїдів-св1
Випадковий патент: Вітровий двигун