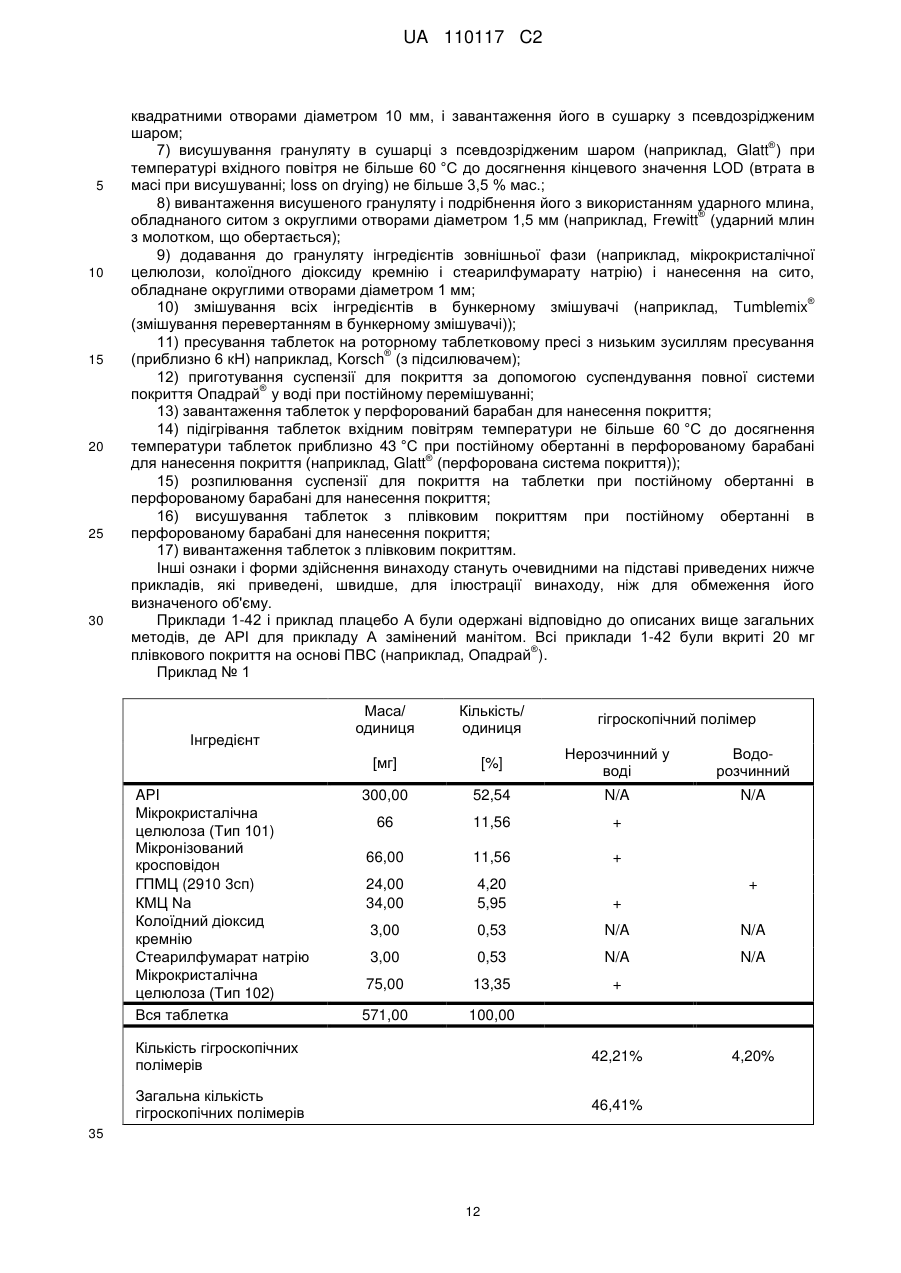
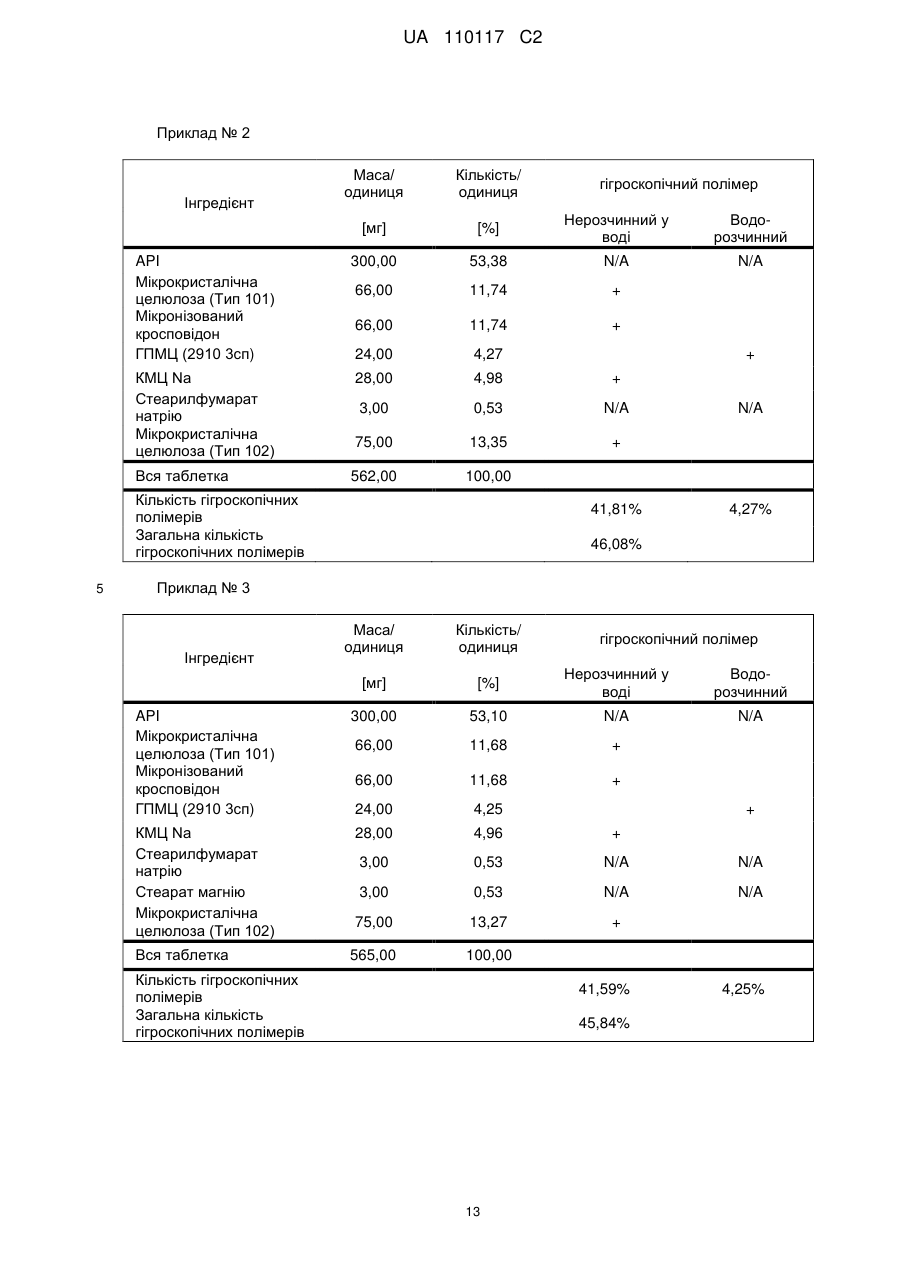
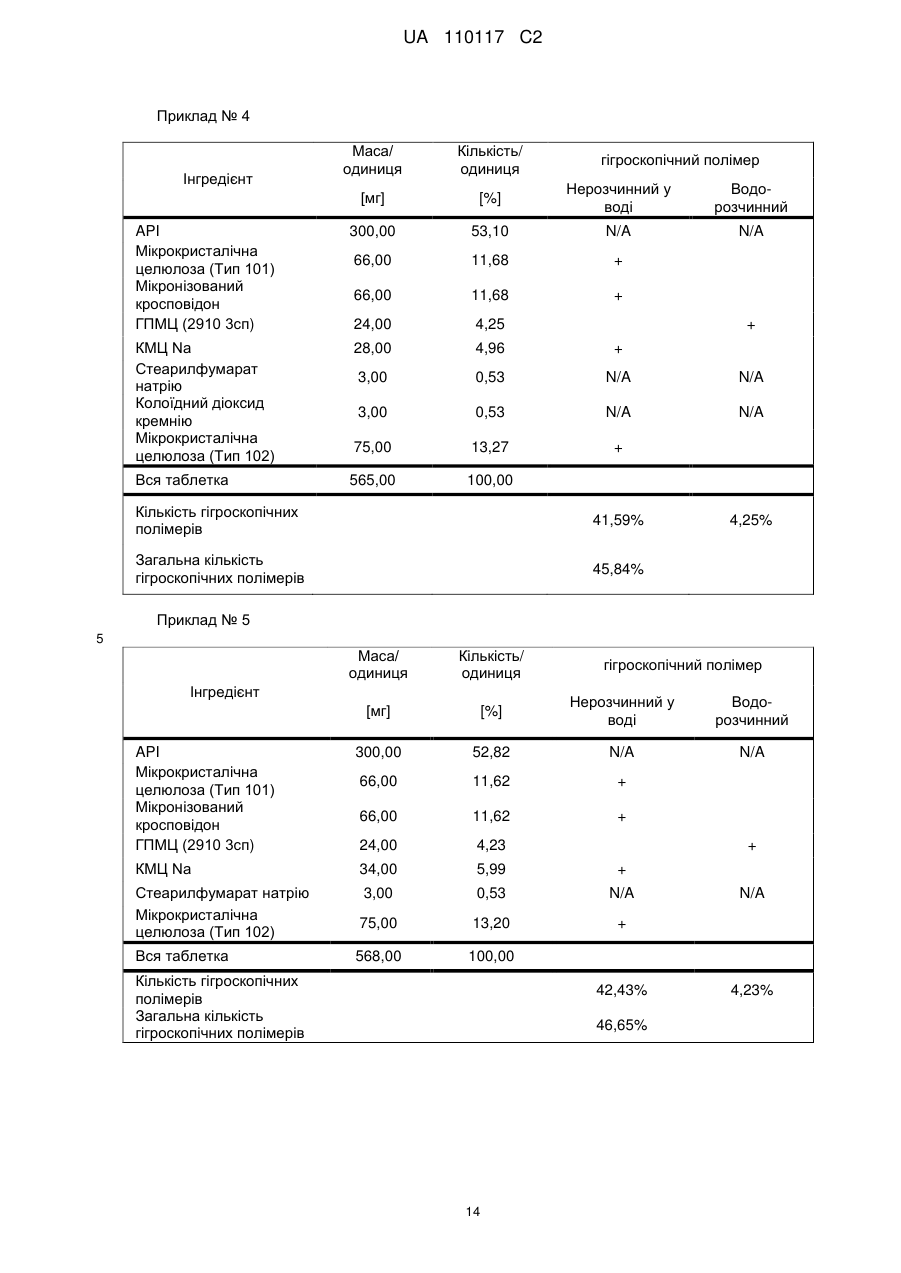
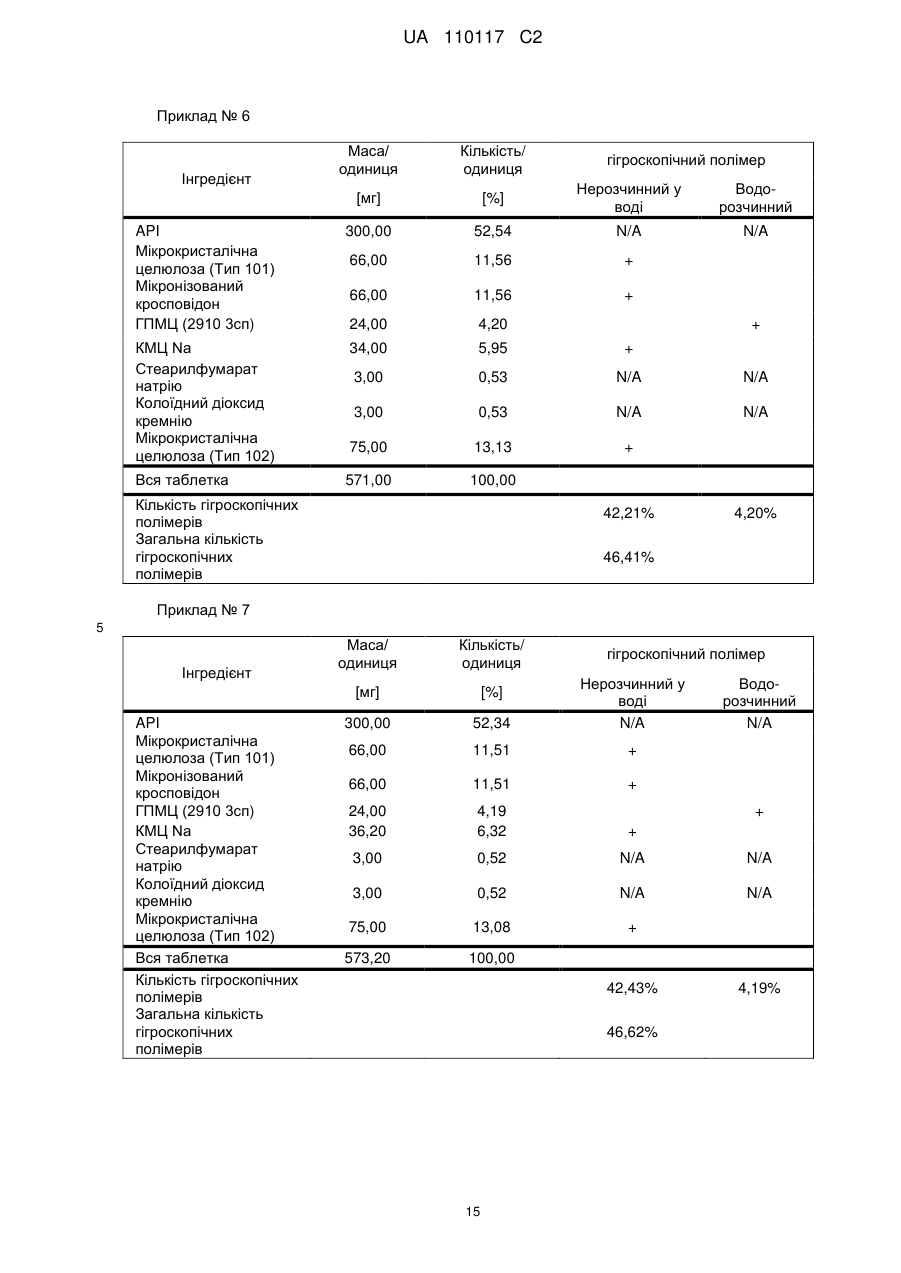
Композиція, що містить s-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоат і кроскармелозу натрію
Номер патенту: 110117
Опубліковано: 25.11.2015
Автори: Мейер Бернар, Крабіхлєр Міхаела, Вінценбург Карстен
Формула / Реферат
1. Композиція, що містить:
a) від 48 % до 55 % мас. S-[2-([[1-(2-eтилбутил)-циклогексил]-кapбoніл]aмiнo)феніл]2-
метилпропантіоату;
b) від 24 % до 26 % мас. мікрокристалічної целюлози;
c) від 11 % до 12 % мас. мікронізованого кросповідону;
d) від 4 % до 5 % мас. гідроксипропілметилцелюлози;
e) від 4 % до 6 % мас. кроскармелози натрію,
яка має форму таблетки.
2. Композиція за п.1, що містить:
a) від 48 % до 55 % мас. S-[2-([[1-(2-eтилбутил)-циклогексил]-кapбoніл]aмiнo)феніл]2-
метилпропантіоату;
b) від 24 % до 26 % мас. мікрокристалічної целюлози;
c) від 11 % до 12 % мас. мікронізованого кросповідону;
d) від 4 % до 5 % мас. гідроксипропілметилцелюлози;
e) від 4 % до 6 % мас. кроскармелози натрію,
f) від 0 до 1 % мас. стеарату магнію;
g) від 0 до 1 % мас. колоїдного діоксиду кремнію;
h) від 0 до 1% мас. стеарилфумарату натрію.
3. Композиція за будь-яким з пп. 1-2, де S-[2-([[1-(2-eтилбутил)-циклогексил]-кapбoніл]aмiнo)феніл]2-метилпропантіоат має кристалічну форму.
Текст
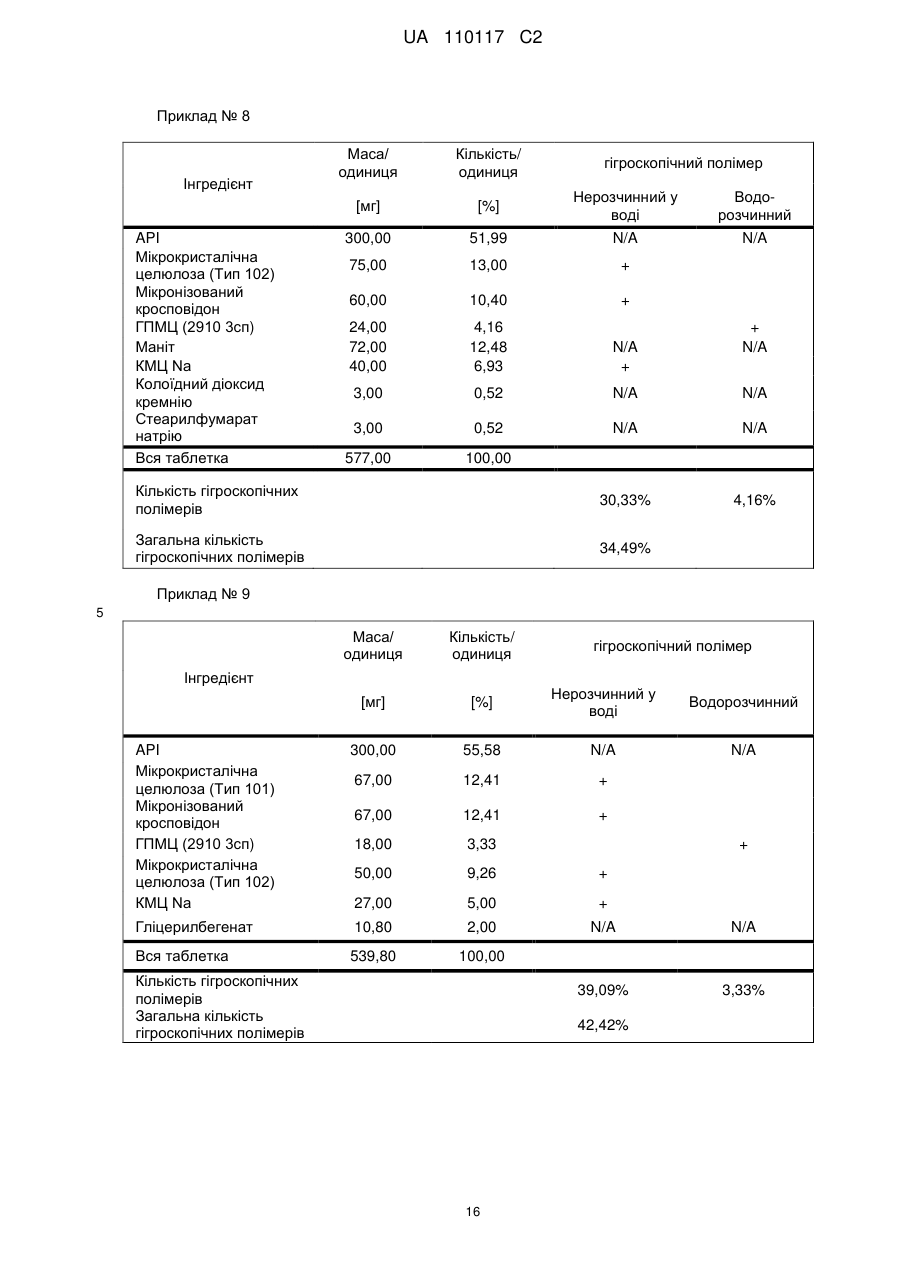
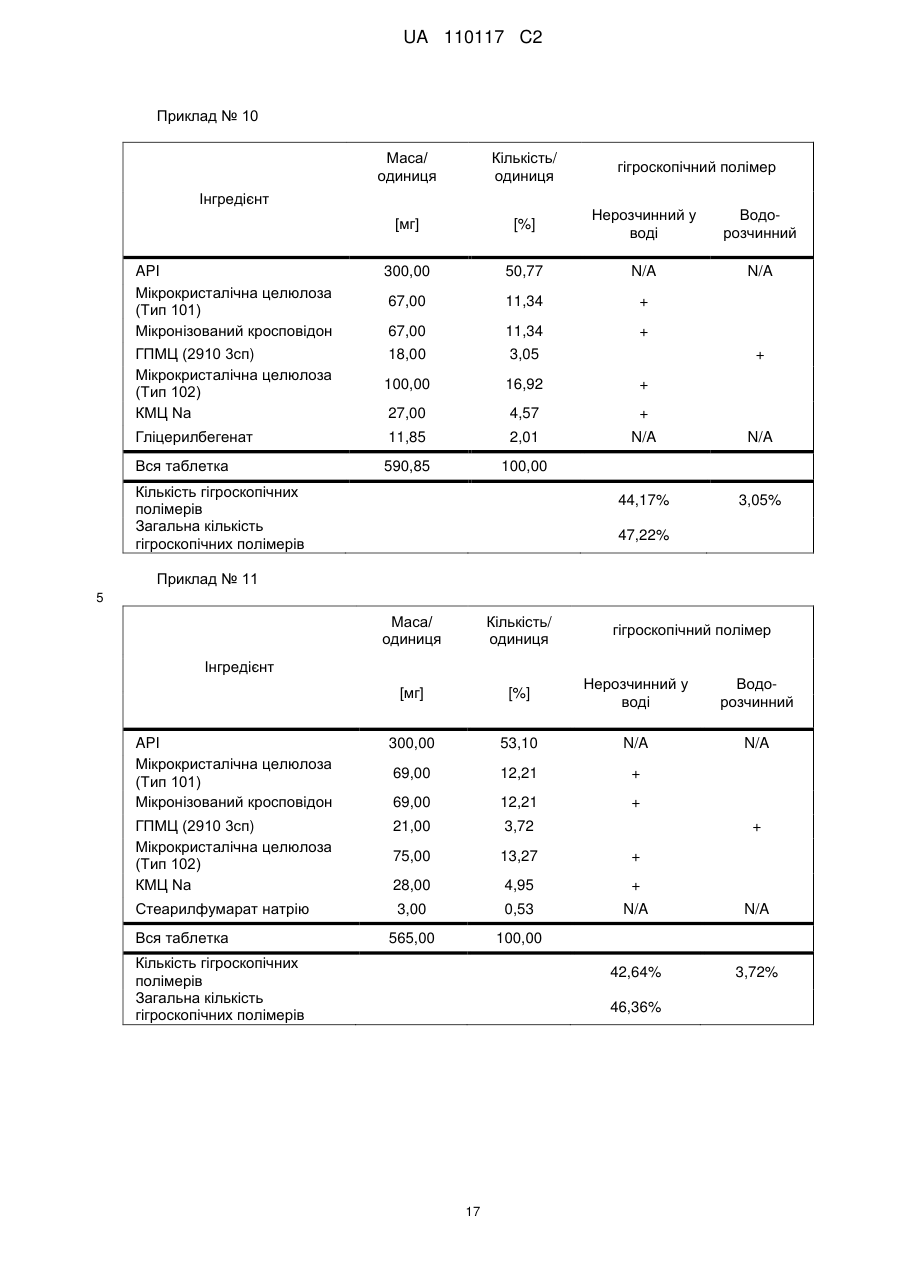
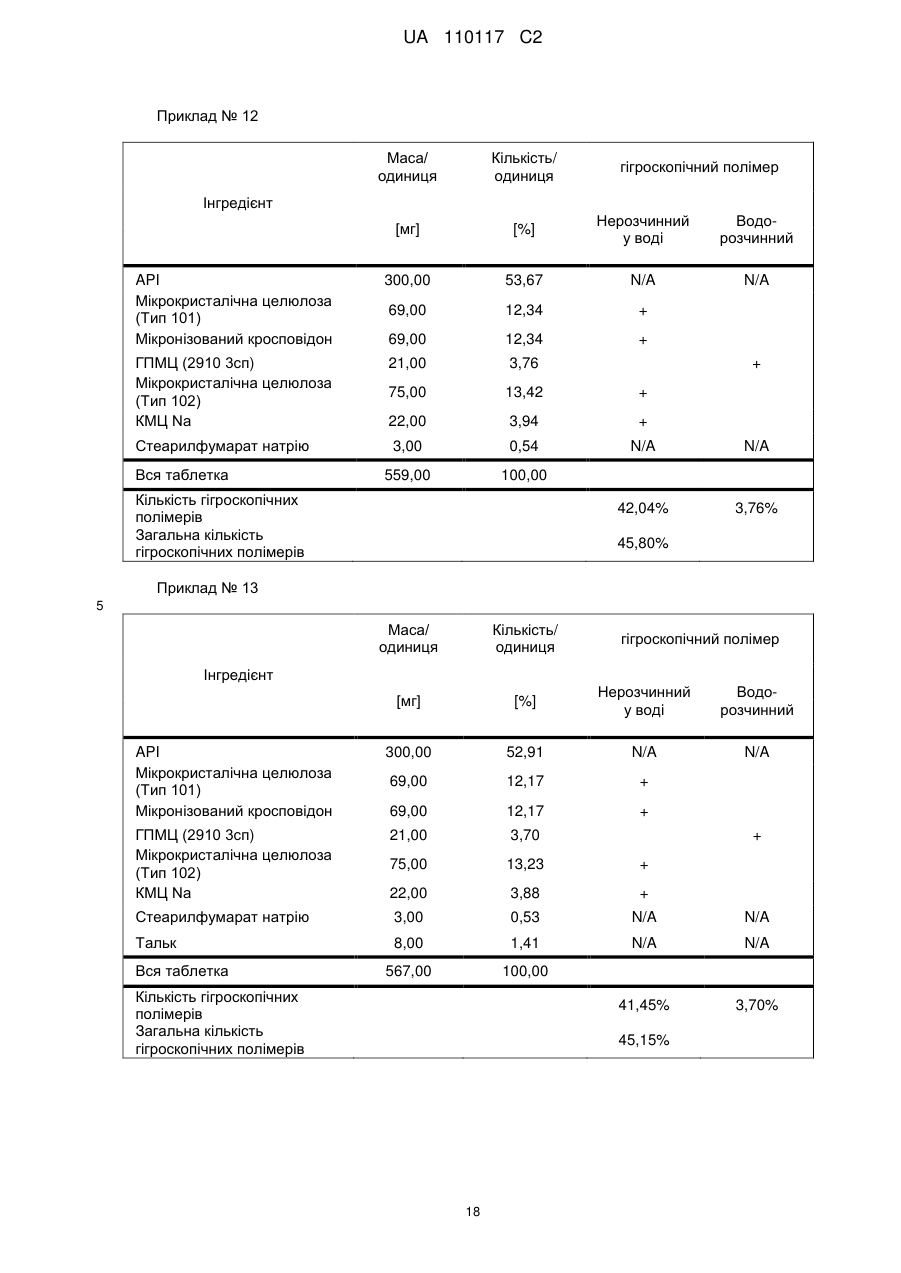
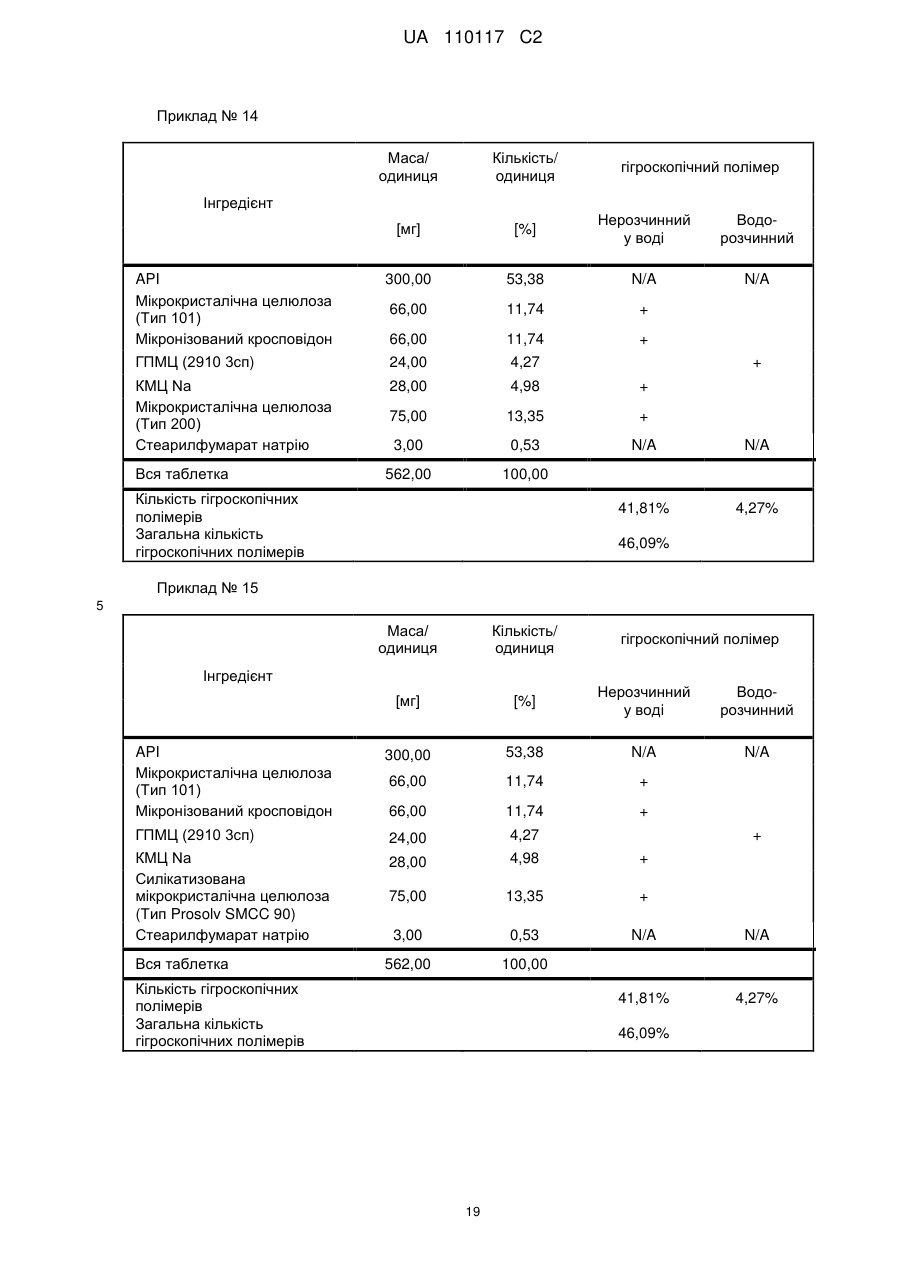
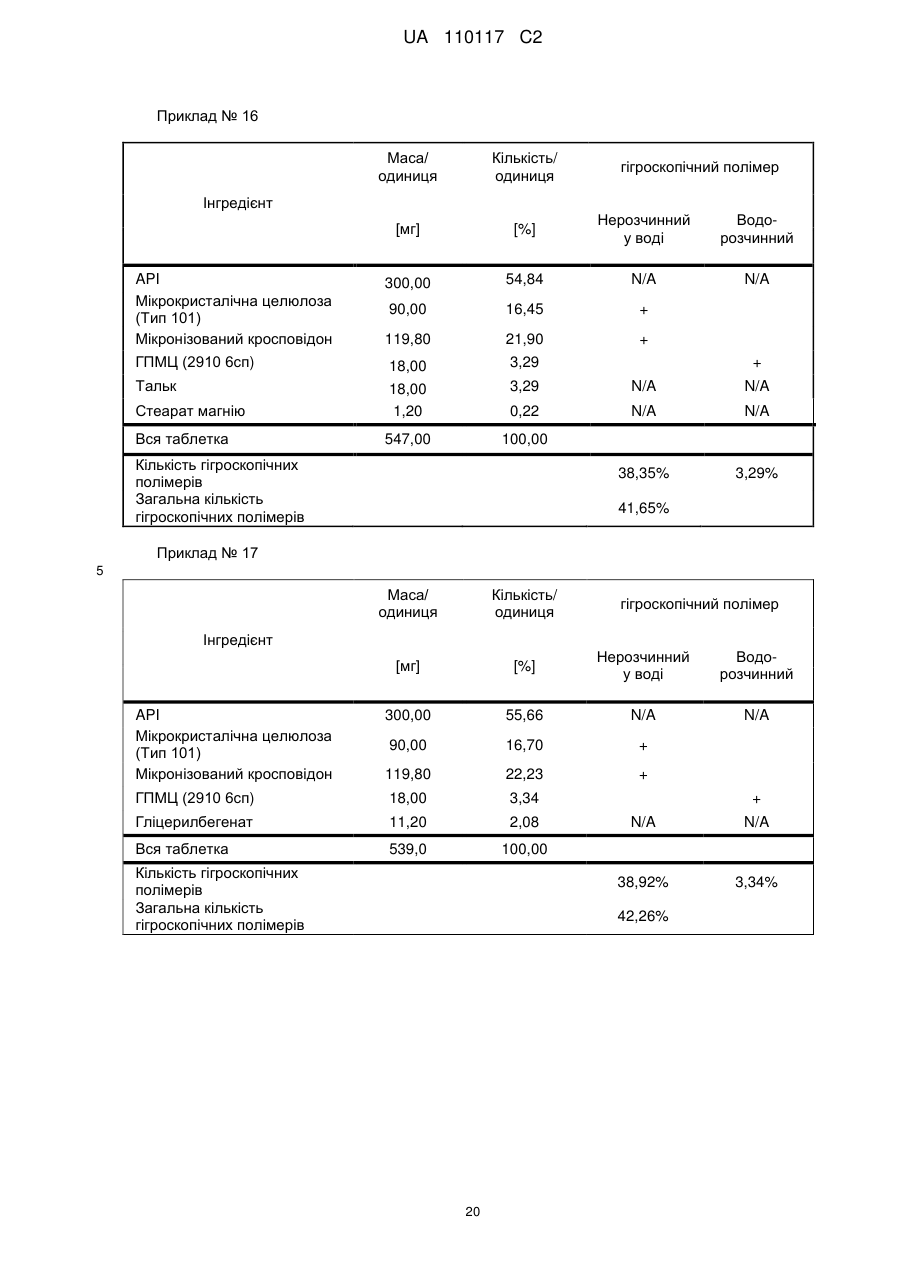
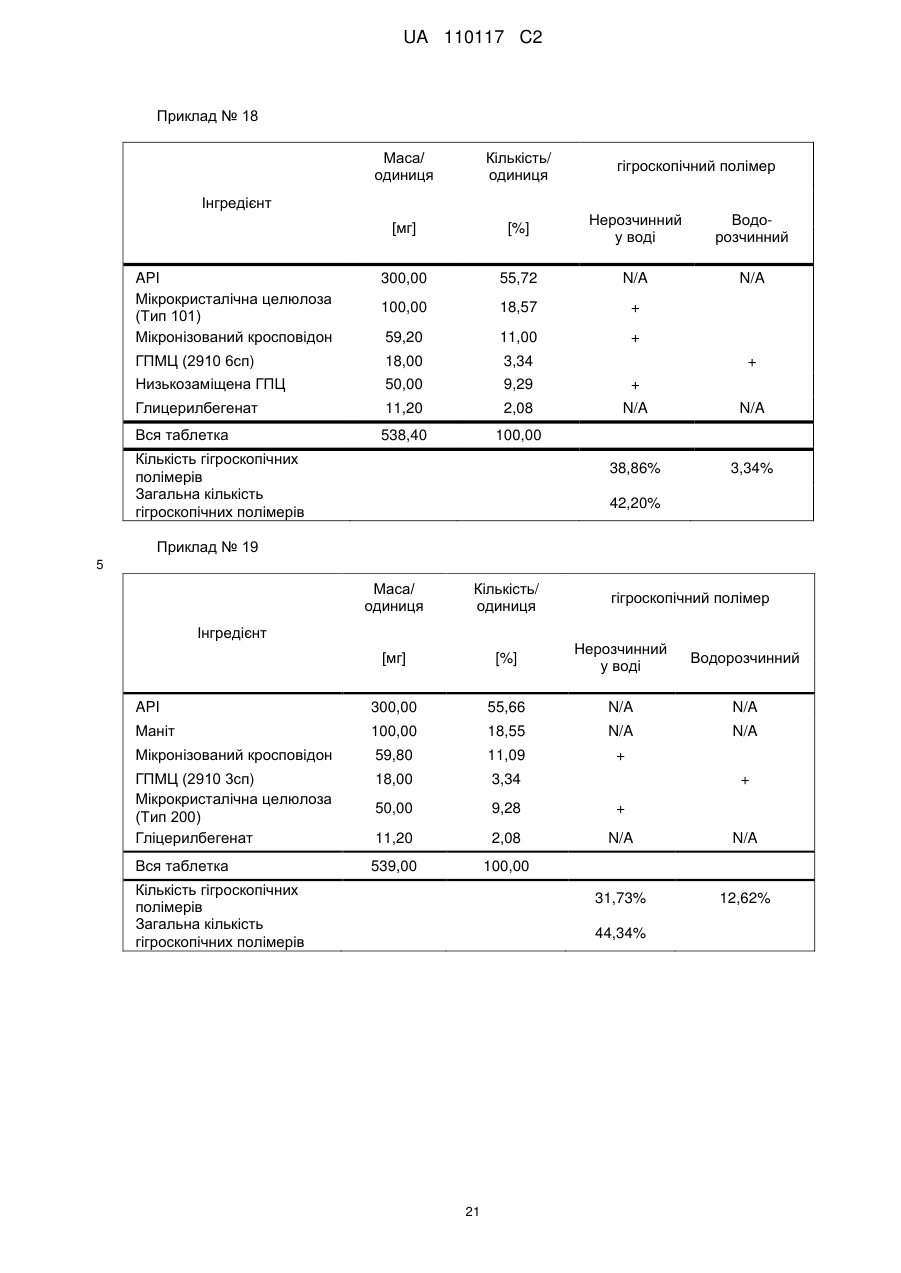
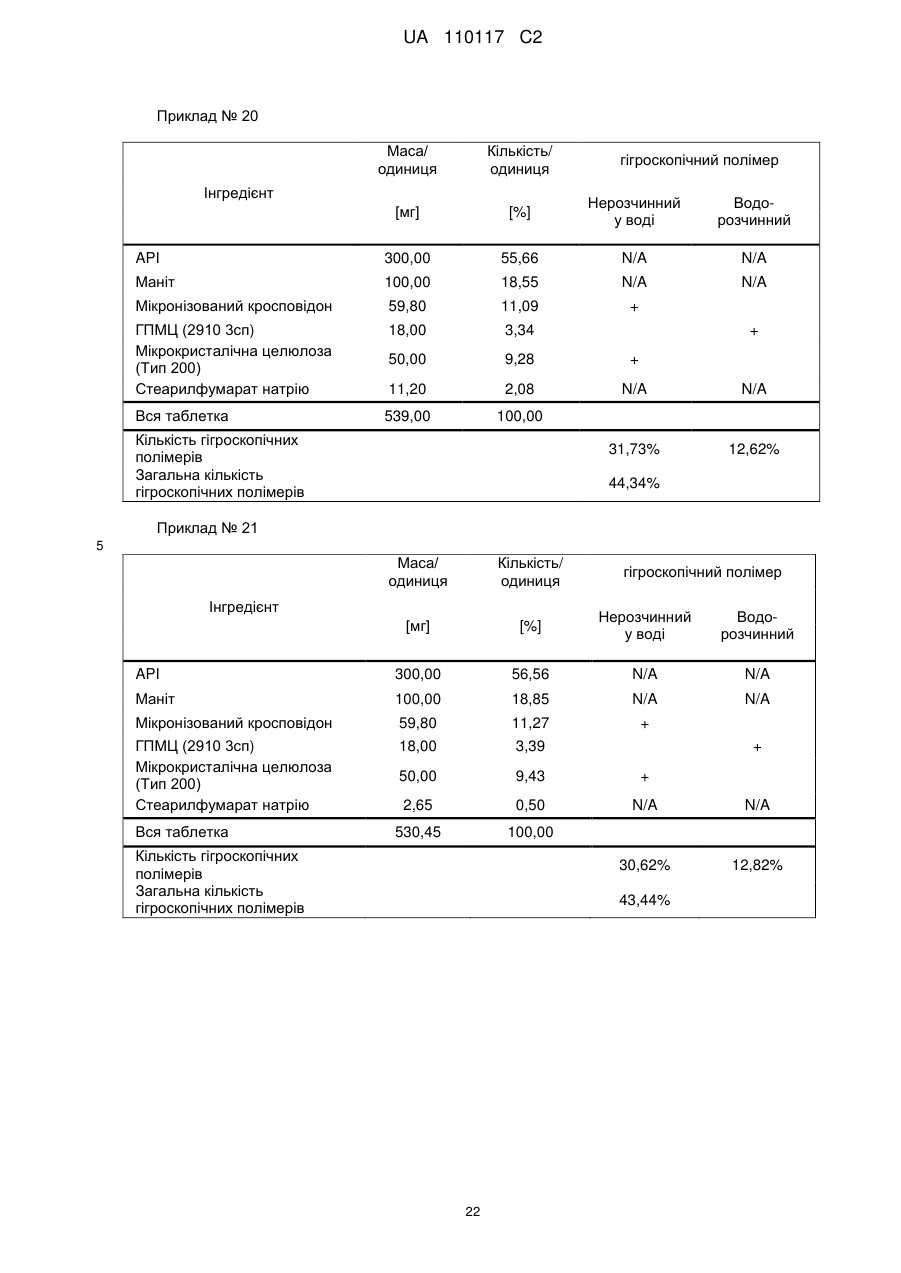
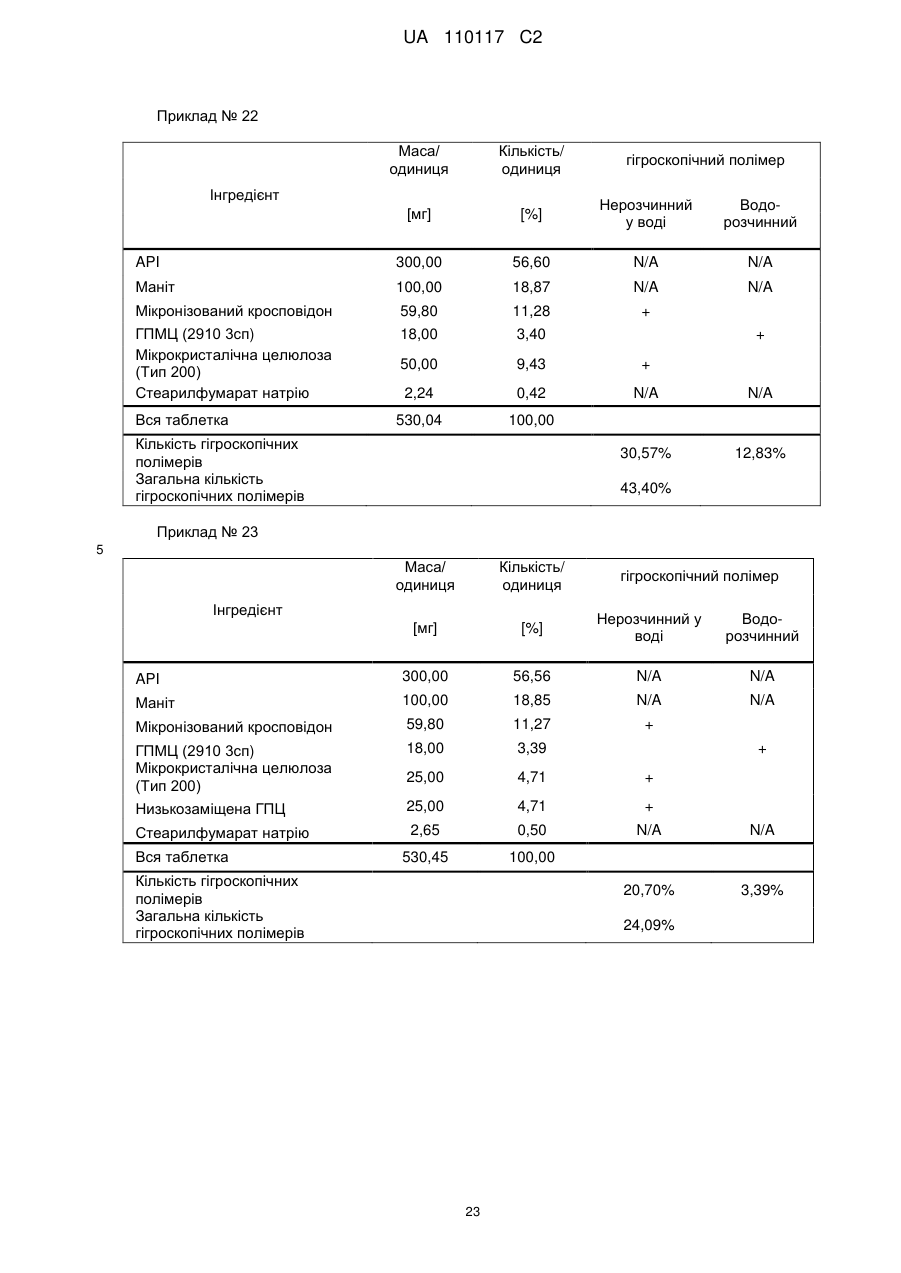
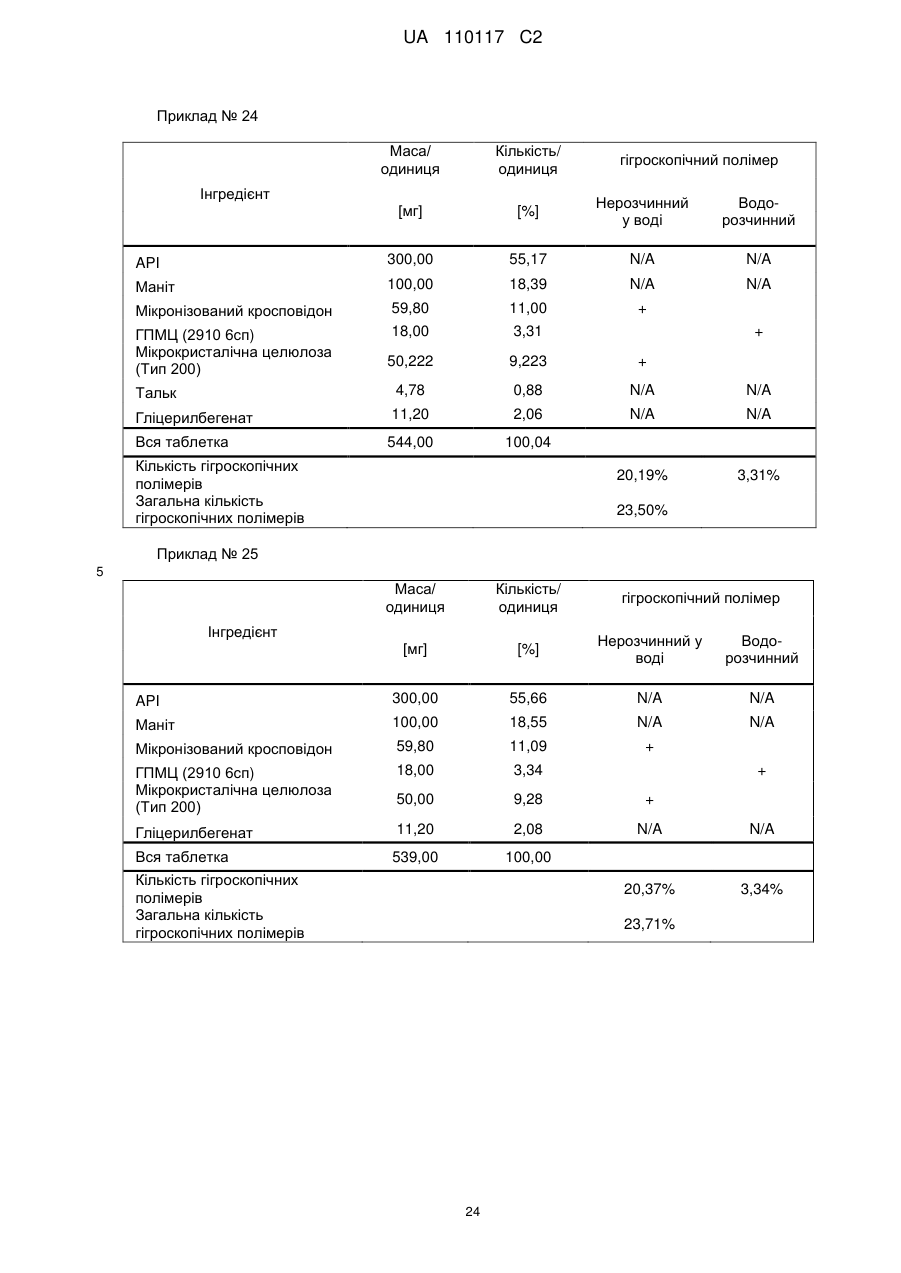
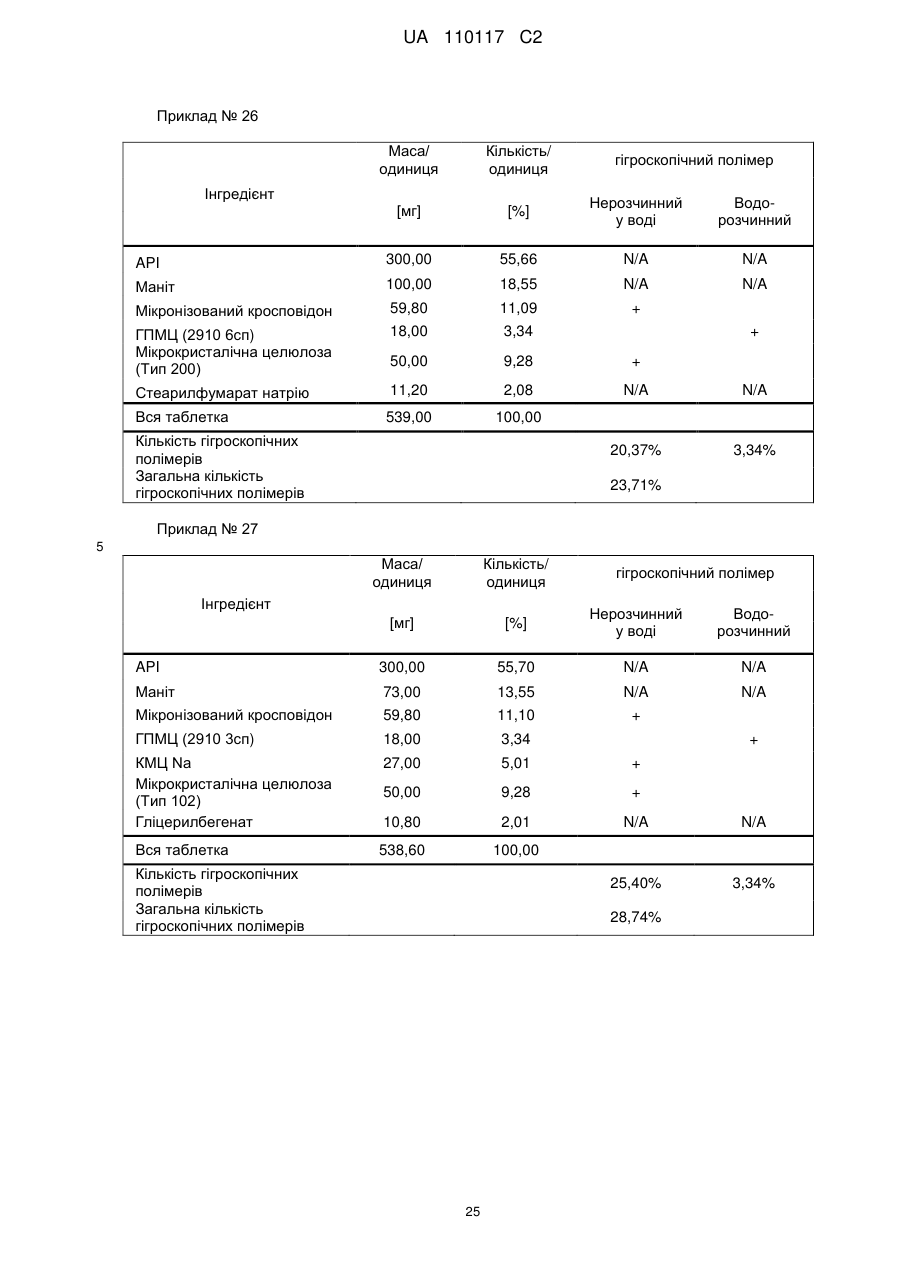
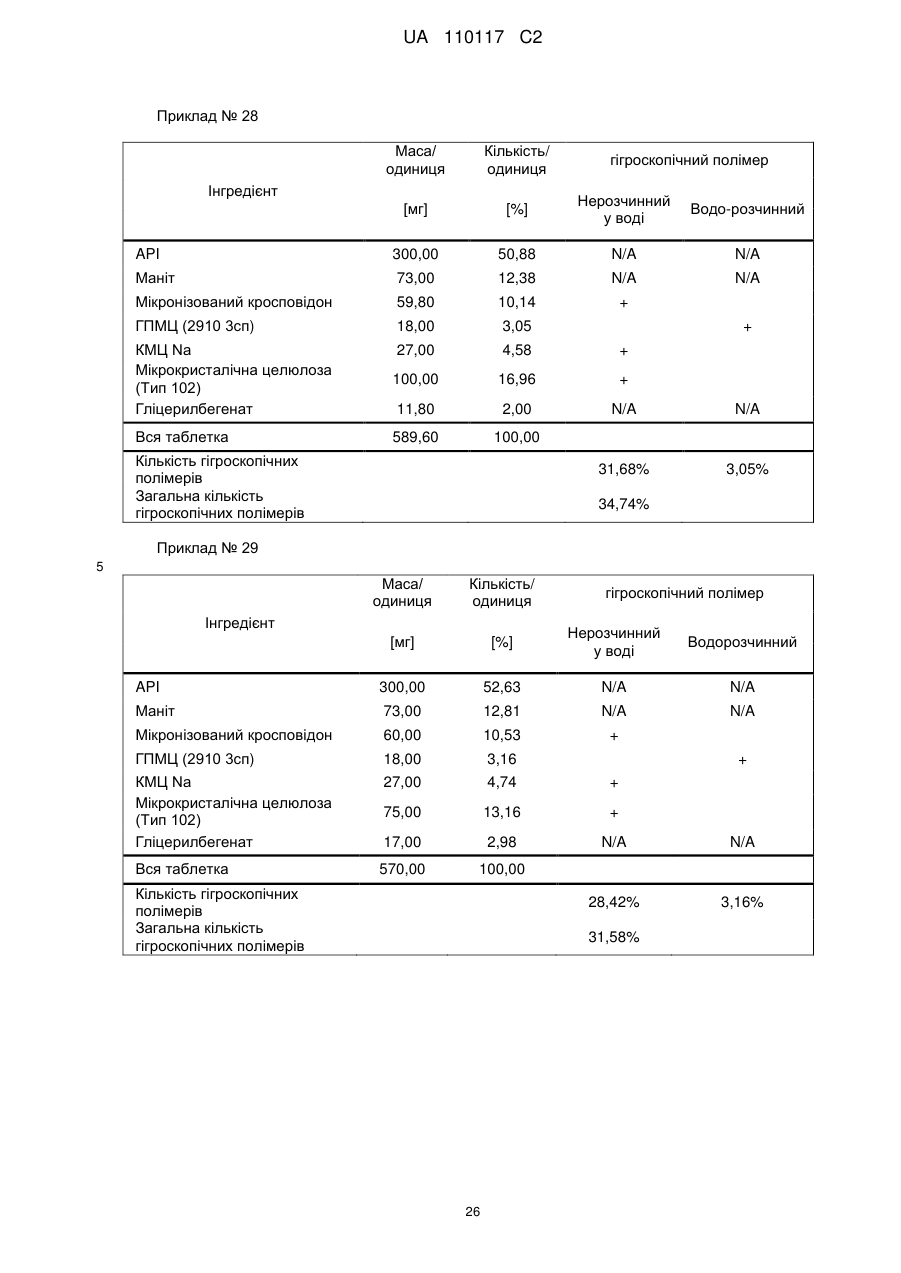
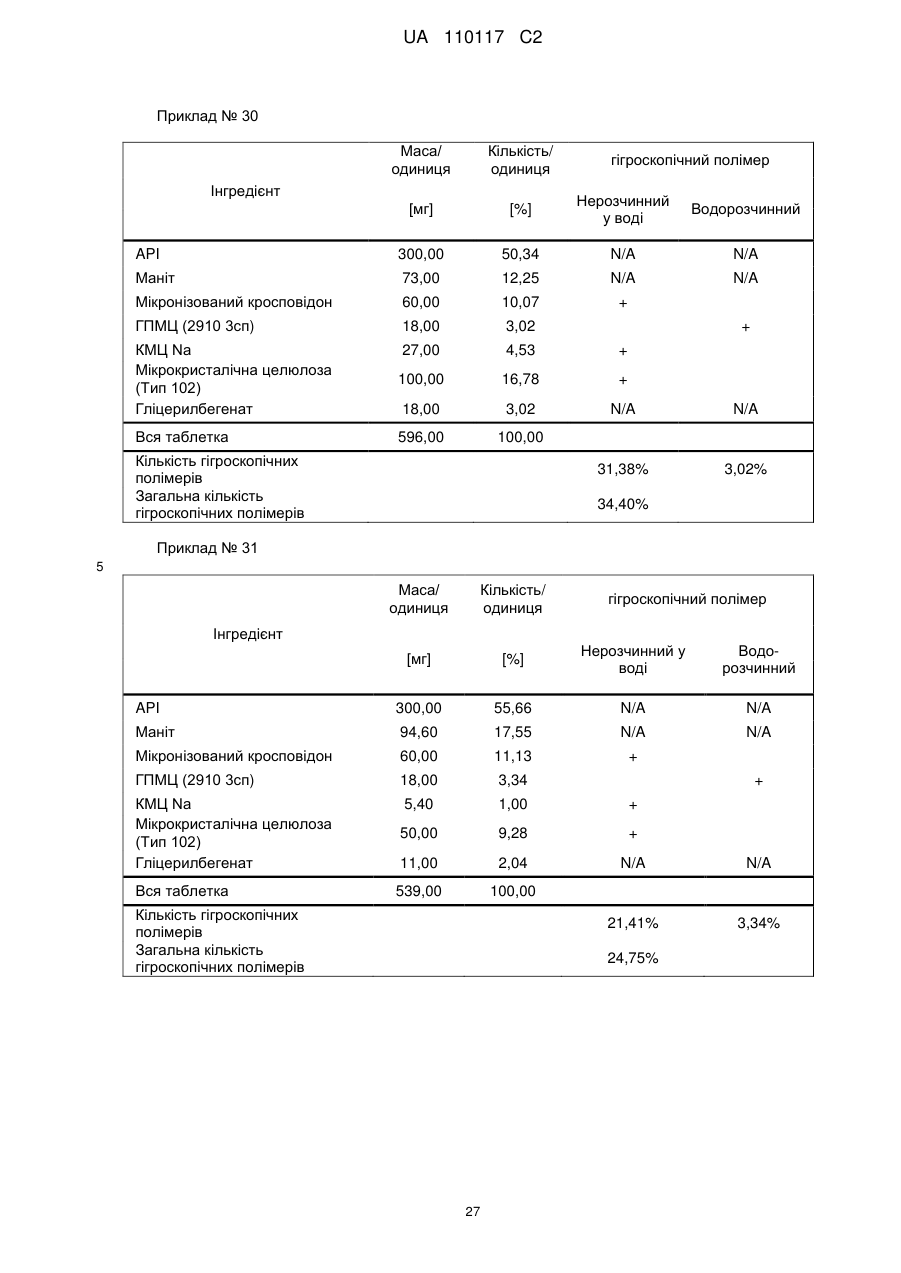
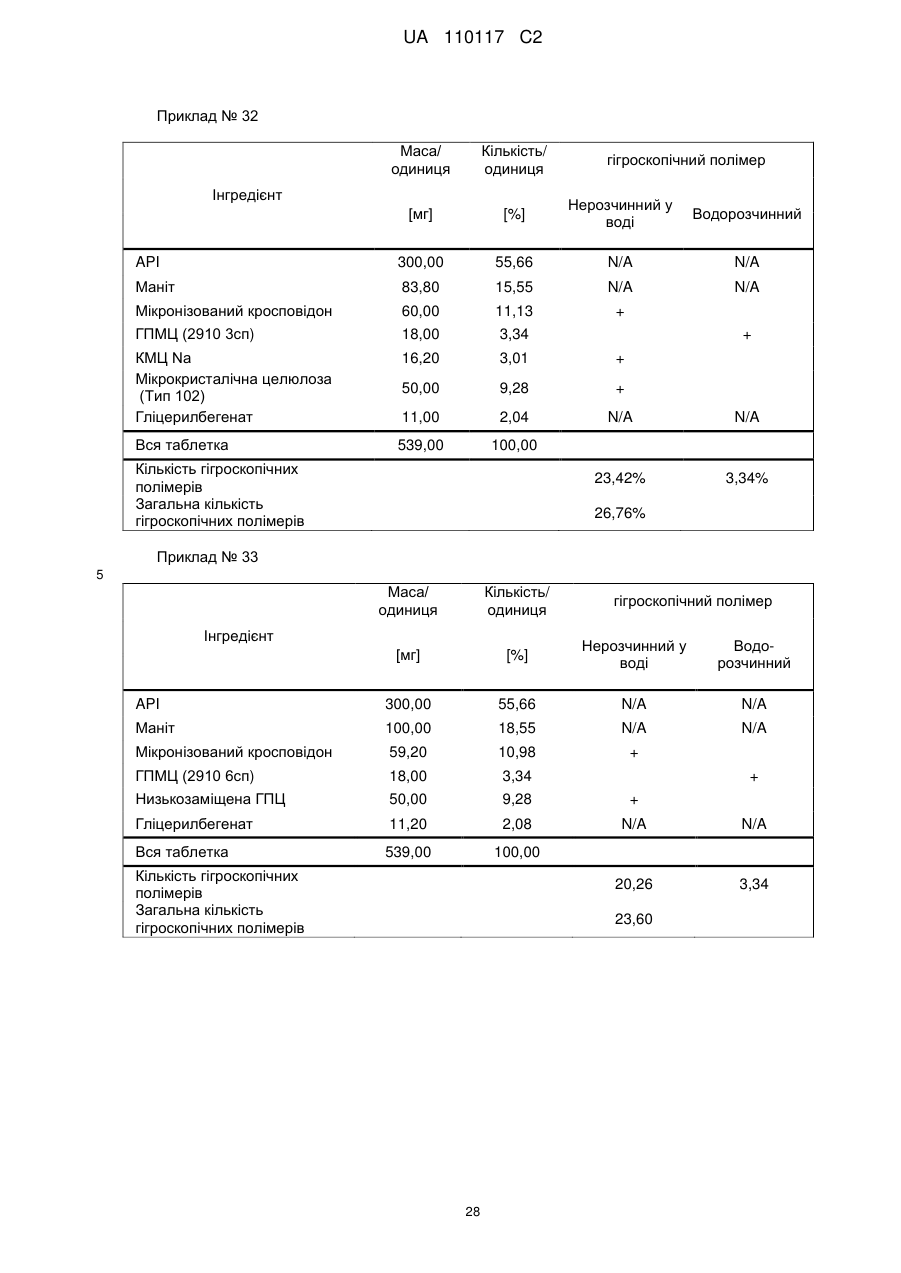
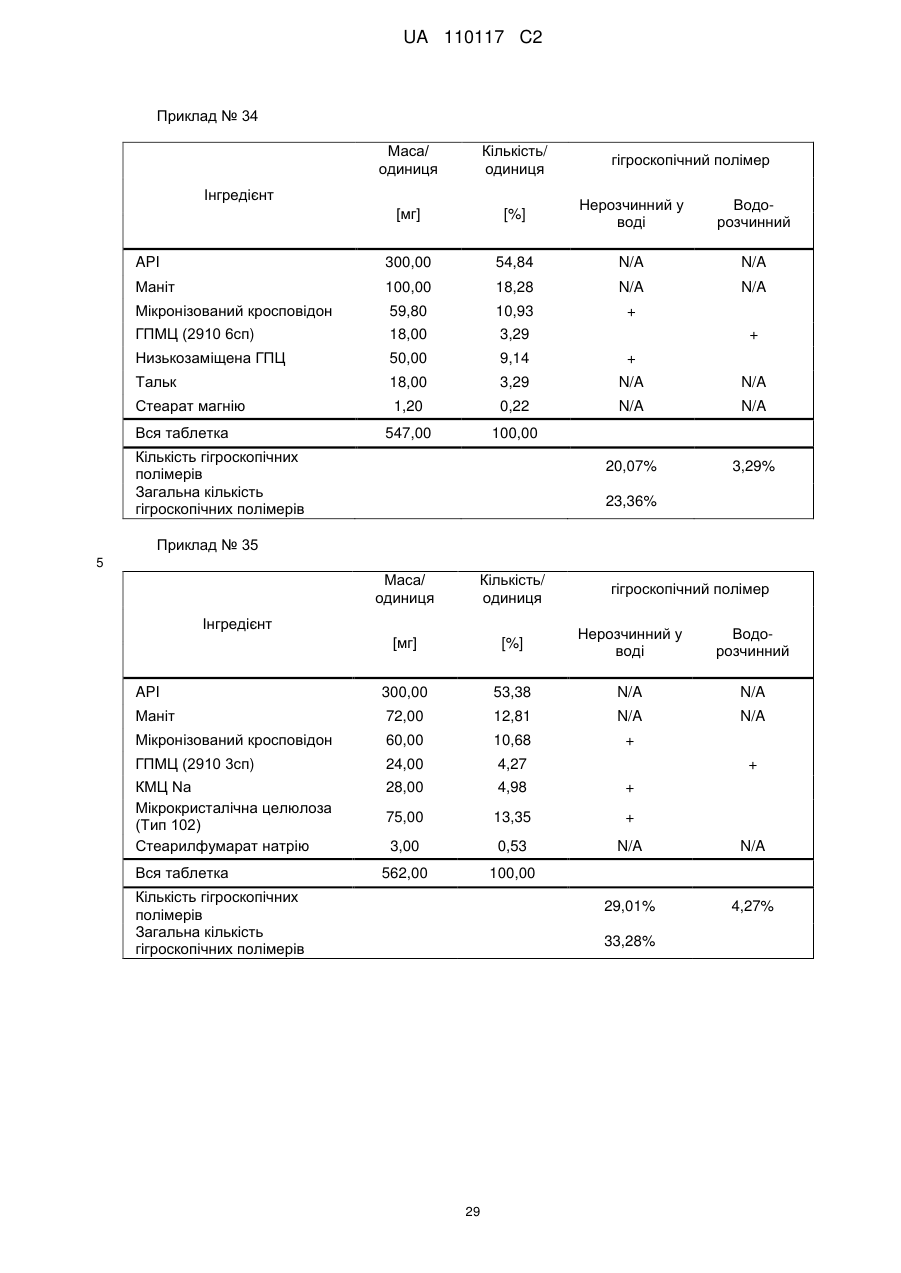
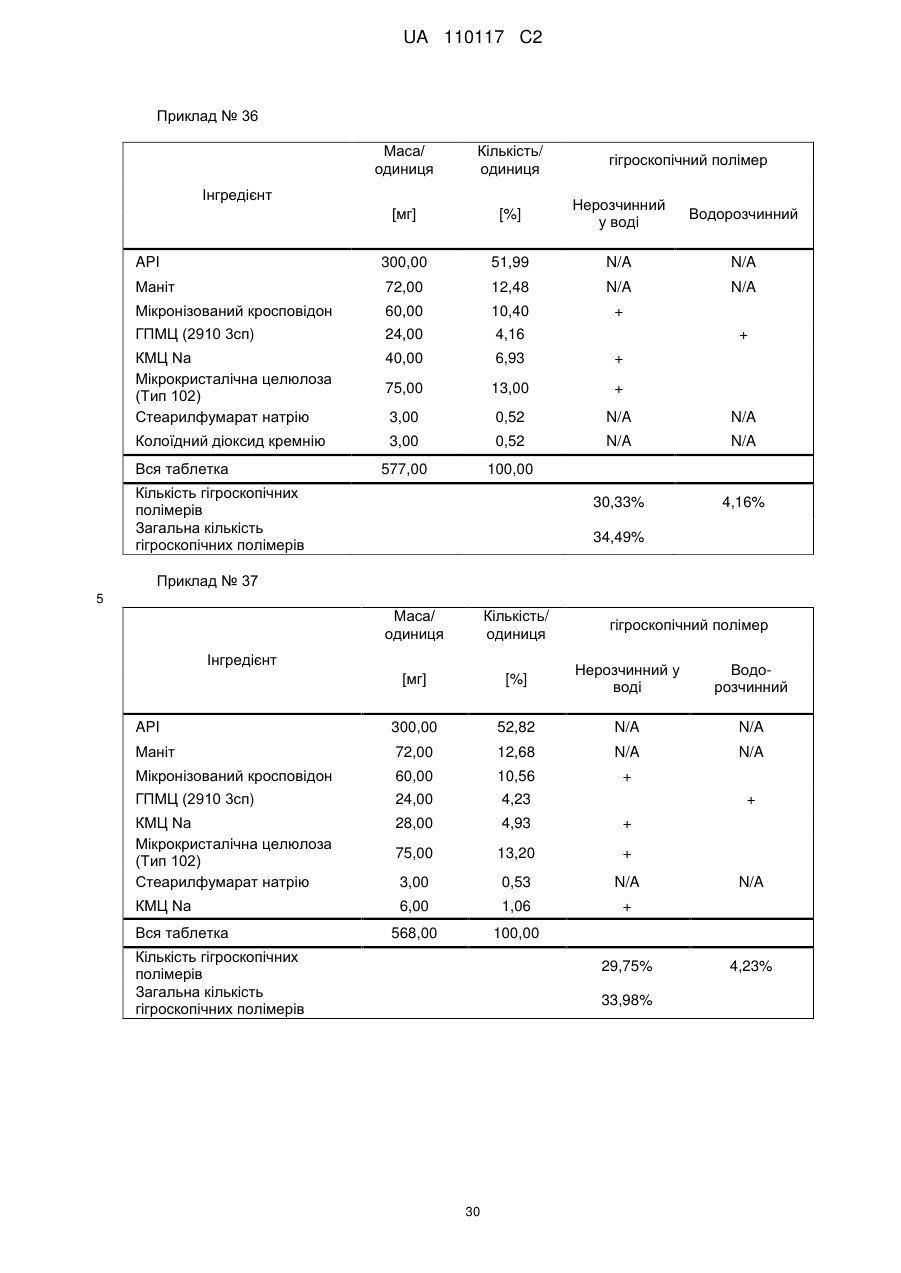
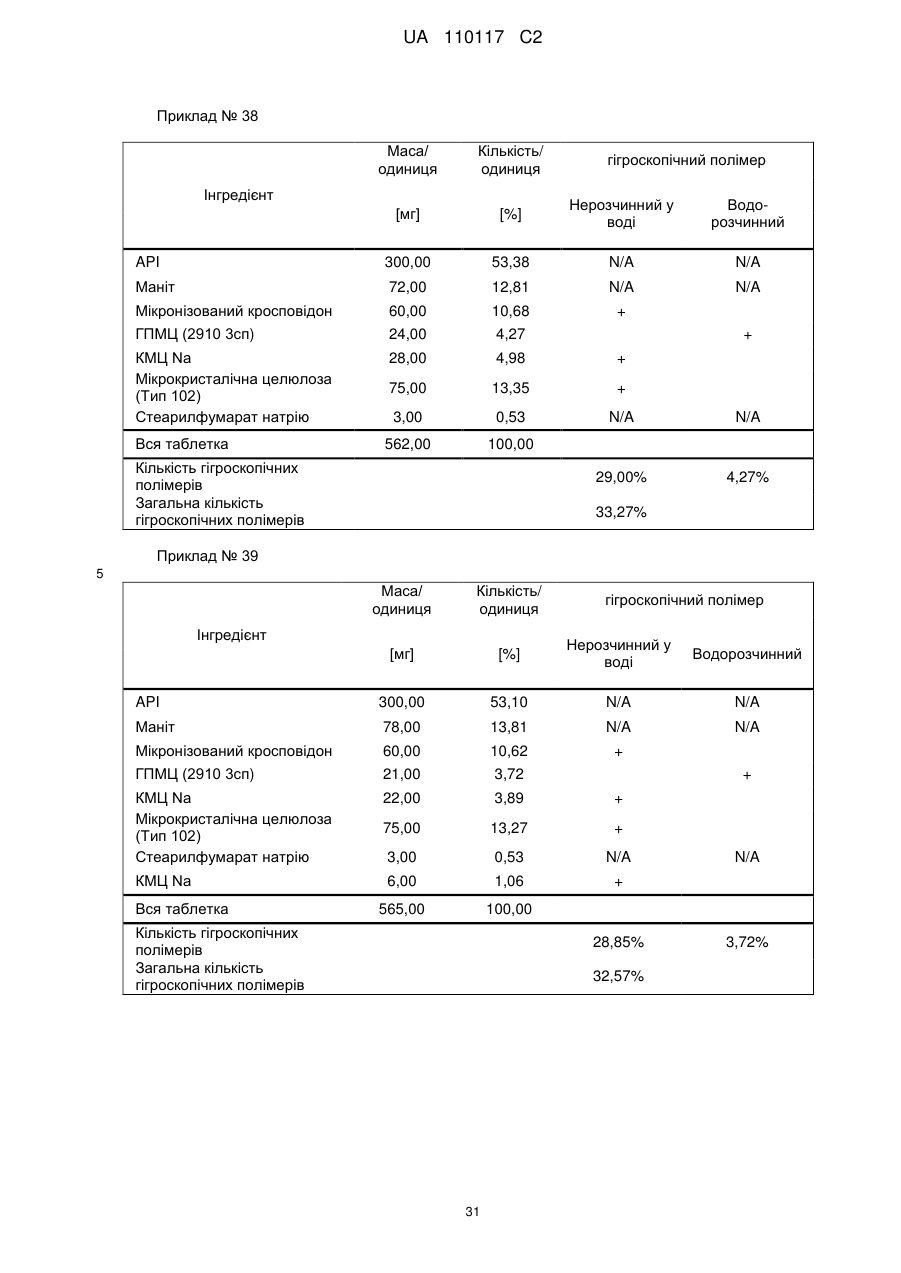
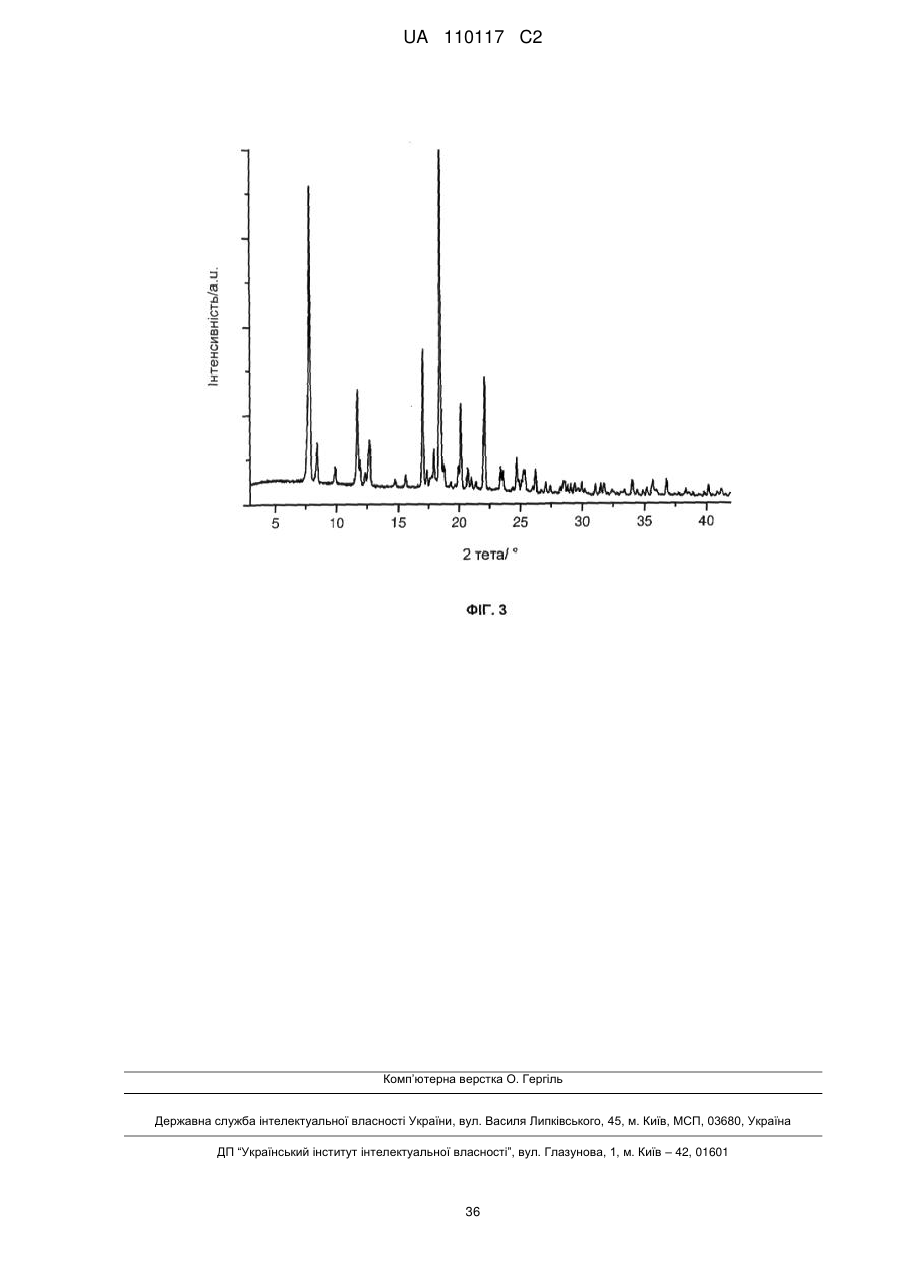
Реферат: Винахід стосується композиції, що містить: a) від 48 % до 55 % мас. S-[2-([[1-(2-eтилбутил)циклогексил]-кapбoніл]aмiнo)феніл]2-метилпропантіоату; b) від 24 % до 26 % мас. мікрокристалічної целюлози; c) від 11 % до 12 % мас. мікронізованого кросповідону; d) від 4 % до 5 % мас. гідроксипропілметилцелюлози; e) від 4 % до 6 % мас. кроскармелози натрію, яка має форму таблетки. UA 110117 C2 (12) UA 110117 C2 UA 110117 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід належить до препарату на основі гігроскопічної матриці, до способу його одержання і до його застосування при лікуванні захворювань. У зв'язку з тим, що активні фармацевтичні інгредієнти, які включають складноефірну, амідну або тіоефірну функціональну групу, часто чутливі до вологи і часто проявляють хімічну несумісність з широким спектром загальноприйнятно вживаних фармацевтичних наповнювачів, звичайні підходи до приготування препаратів, такі як системи доставки лікарського засобу на основі ліпідів, не можуть бути розглянуті. Включення лікарської речовини в гігроскопічну полімерну матрицю може бути небезпечне, як у зв'язку з хімічною, так і у зв'язку з фізичною стабільністю. Поглинання вологи наповнювачами в твердих лікарських формах може призвести до значних проблем, пов'язаних із стабільністю, якщо активний фармацевтичний інгредієнт, що міститься у них, нестабільний у воді у зв'язку з наявністю функціональної групи, чутливої до гідролізу. Хоча теоретично гігроскопічні полімери здатні до зв'язування вологи в препараті, захищаючи, таким чином, активний фармацевтичний інгредієнт від гідролізу, для досягнення цього захисту потрібна достатньо велика кількість полімеру, що зазвичай призводить до закупорювання або розтріскування таблеткового препарату швидкого вивільнення. Тому зазвичай необхідно запобігати поглинанню вологи в процесі зберігання, як відповідного препарату, так і первинної упаковки. При одержанні композиції згідно з даним винаходом спостерігається несподівано краща текучість, ніж при одержанні попередніх композицій, що включають гідрофобну, нестійку до води сполуку, що має воскову консистенцію. Наприклад, композиція згідно з даним винаходом не виявляє надмірного лійкоподібного потоку. У першому аспекті даного винаходу запропонована фармацевтична композиція, що включає гідрофобну, нестійку до води сполуку, що має воскову консистенцію, і суперрозпушувач. У другому аспекті даного винаходу запропонована фармацевтична композиція, що включає гідрофобну, нестійку до води сполуку, що має воскову консистенцію, суперрозпушувач і щонайменше два розріджувача, що мають насипну щільність до ущільнення нижче 800 г/л. У винаході також запропонований спосіб лікування або попередження серцево-судинного розладу у ссавця за допомогою введення ссавцеві, що потребує такого лікування, терапевтично ефективної кількості фармацевтичної композиції, розробленої винаходом. У винаході також запропонований препарат для лікування або попередження серцевосудинного розладу. Композиція згідно з даним винаходом для застосування при лікуванні або попередженні серцево-судинного розладу, також складає частину винаходу. Препарат на основі гігроскопічної матриці корисний для хімічної стабілізації гідрофобної і чутливої до гідролізу сполуки, що має воскову консистенцію, наприклад, інгібітора транспортного білка холестеринових ефірів (CETP, cholesteryl ester transfer protein inhibitor), а також для стабілізації фізичних властивостей таблетки, що містить цей препарат. Короткий опис графічних матеріалів: Фіг. 1 є тривимірною реконструкцією всіх рентгенівських зрізів таблетки, одержаної згідно з прикладом 1. Фіг. 2 є тривимірною реконструкцією всіх рентгенівських зрізів таблетки, яка відповідає плацебо прикладу A. На фіг. 3 проілюстрована порошкова рентгенівська дифрактограма S-[2-([[1-(2-етилбутил)циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоату кристалічної форми, також відомої як форма A. Якщо не вказане інше, наступні терміни, використовувані в описі і у формулі винаходу, мають приведені нижче значення: Термін “насипна щільність до ущільнення” належить до вимірювання щільності сипкої, неущільненої речовини, де об'єм речовини включає повітря, захоплене між частинками. Насипну щільність до ущільнення вимірюють у градуйованому циліндрі відповідно до Європейської фармакопеї. Термін “розріджувач” належить до наповнювача, що доповнює розмір таблетки або капсули, робить її практичною для одержання і зручною для застосування споживачем. Відповідні розріджувачі включають, наприклад, фармацевтично прийнятні об'ємоутворюючі агенти, такі як ® мікрокристалічна целюлоза (наприклад, Avicel ), мікронізований кросповідон, целюлозний порошок, лактоза, висушена розпилюванням, безводна лактоза, моногідрат лактози, двоосновний фосфат кальцію, цукри, цукрові спирти, кукурудзяний крохмаль, крохмаль, прежелатинізований крохмаль, колоїдний діоксид кремнію, полісахариди і їх суміші. Термін “гідрофобний” означає нерозчинний у воді, такий, що насилу поглинає вологу або схильний до шкідливого впливу води, або несумісний з водою, або такий, що має низьку спорідненість з нею. Іншими словами, гідрофобний лікарський засіб або сполука не повинні 1 UA 110117 C2 5 10 15 20 25 30 35 40 45 50 55 спонтанно диспергуватися у воді. Конкретно термін “гідрофобний” означає, що logP складає більше 3. logP вимірюють або, за відсутності експериментальних даних, обчислюють як clogP згідно з моделлю, розробленою Морігучі (S. Moriguchi, S. Hirono, I. Nakagome, H. Hirano (1994). "Comparison of reliability of logP values for drugs calculated by several methods" Chem Pharm Bull 1994, 42: 976-978). Термін “гігроскопічний полімерний наповнювач (наповнювачі)” означає полімерний наповнювач (наповнювачі), який поглинає вологу, наприклад, за допомогою абсорбції або адсорбції, навіть при такій низькій відносній вологості, як 50 %, при кімнатній температурі (наприклад, приблизно 25 °C). Поглинання вологи вимірюють, наприклад, за допомогою динамічної сорбції пари при кімнатній температурі. Як приклад, гігроскопічність можна виміряти способом, описаним у 6-му виданні Європейської фармакопеї (2008), розділ 5.11. Методом динамічної сорбції пари вимірюють змінення маси, вироблюване в результаті змінення концентрації пари, що оточує препарат. Відповідними “гігроскопічними полімерними наповнювачами” є гідроксипропілметилцелюлоза, гідроксипропілцелюлоза, низькозаміщена гідроксипропілцелюлоза, гідроксиетилметилцелюлоза, карбоксиполіметилен, метилцелюлоза, етилцелюлоза, гідроксиетилцелюлоза, ацетат целюлози, полівінілпіролідон, зшитий полівінілпіролідон, мікронізований зшитий полівінілпіролідон, натрієва сіль карбоксиметилцелюлози, кальцієва сіль карбоксиметилцелюлози, зшита карбоксиметилцелюлоза, мікрокристалічна целюлоза, силікатизована мікрокристалічна целюлоза, целюлозний порошок, карбоксиметилкрохмаль, крохмаль, прежелатинізований крохмаль або їх суміш. Зокрема, “гігроскопічні полімерні наповнювачі” належать до гідроксипропілметилцелюлози, натрієвої солі карбоксиметилцелюлози, мікрокристалічної целюлози і мікронізованого зшитого полівінілпіролідону. Приклади “нерозчинних у воді гігроскопічних полімерів” при кімнатній температурі (наприклад, приблизно 25 °C) включають низькозаміщену гідроксипропілцелюлозу, карбоксиполіметилен, етилцелюлозу, ацетат целюлози, зшитий полівінілпіролідон, мікронізований зшитий полівінілпіролідон, кальцієву сіль карбоксиметилцелюлози, мікрокристалічну целюлозу, силікатизовану мікрокристалічну целюлозу, целюлозний порошок і крохмаль. Термін “суперрозпушувач” належить до розпушувачів, які дуже швидко розширюються при контакті з водою. Загалом, суперрозпушувачами є розпушувачі, які можна застосовувати в частковій кількості у порівнянні з кількістю звичайних розпушувачів, щоб одержати такий самий ефект. Приклади суперрозпушувачів включають натрієву сіль зшитої карбоксиметилцелюлози (також відому як кроскармелоза натрію), натрієву сіль гліколяту крохмалю і зшитий полівінілпіролідон (також відомий як кросповідон). Кроскармелоза натрію є у продажу від FMC ® ® Corp. під торговою назвою Ac-Di-Sol і від Avebe Corp. під торговою назвою Primellose . Натрієва сіль гліколяту крохмалю є у продажу від Penwest Pharmaceuticals Co. під торговою ® ® назвою Explotab і від Avebe Corp. під торговою назвою Primojel . Кросповідон є у продажу від ® BASF Corp. під торговою назвою Kollidon CL і від International Specialty Chemicals Corp. під ® торговою назвою Polyplasdone . Кроскармелоза також є у продажу від Mingtai Chemical Co. Ltd ® під торговою назвою DISOLCEL і від J. Rettenmaier & Söhne GmbH + Co (JRS) під торговою ® назвою Vivasol . Найбільш переважними суперрозпушувачами є кроскармелоза натрію і кросповідон. Термін “нестійкий до води” означає наявність чутливої до гідролізу функціональної групи, такої як складний ефір, амід або тіоефір. Термін “воскова консистенція” означає температуру склопереходу (Tg) нижчу за 25 °C. Термін “галогено” означає хлоро, бромо, йодо або фторо. “Арил” означає одновалентне моноциклічне або біциклічне ароматичне вуглеводневе угруповання. Конкретніше термін “арил” включає, але не обмежений ними, феніл, 1-нафтил, 2нафтил і тому подібне, кожний з яких може бути заміщеним або незаміщеним. “(C2-C6)алкеніл” належить до прямого або розгалуженого ланцюга з атомів вуглецю в кількості від 2 до 6, зокрема, з атомів вуглецю в кількості від 2 до 4, що містить щонайменше один подвійний зв'язок. Приклади алкенілу включають етеніл, пропеніл, проп-2-еніл, ізопропеніл, н-бутеніл, ізобутеніл і трет-бутеніл. “(C1-C8)алкіл” належить до розгалуженого або прямоланцюжкового вуглеводневого ланцюга з атомів вуглецю в кількості від одного до восьми, такого як метил, етил, н-пропіл, ізопропіл, нбутил, ізобутил, втор-бутил, трет-бутил, пентил, гексил і гептил. Переважним є (C1-C6) алкіл. “Галогено-(C1-C8) алкіл” належить до алкілу, як визначено вище, заміщеного одним або більше атомами галогену, переважно атомами галогену в кількості від одного до трьох. Кращим галогено-(C1-C8)алкілом є хлор- і фтор-( C1-C8) алкіл. 2 UA 110117 C2 bc 5 10 15 bd bd bc “Аралкіл” належить до угруповання, що має формулу -R -R , де R є арилом, і R є (C1C6)алкіленом, як визначено в даному описі. ab ab “(C1-C6)алкокси” означає угруповання, що має формулу -OR , де R є (C1-C6)алкільним угрупованням, як визначено в даному описі. Приклади алкоксигруп включають, але не обмежені ними, метокси, етокси, ізопропокси і тому подібне. “(C3-C8)циклоалкіл” належить до одного насиченого карбоциклічного кільця, такого як циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил і циклооктил. “C3-C8циклоалкілC1-C8алкіл” належить до алкілу, як визначено вище, заміщеного одним (C3C8) циклоалкілом, як визначено вище. ag ag, ag “Ацил” означає групу, що має формулу -C(O)-R , -C(O)-OR , -C(O)-OC(O)R або -C(O)ag ah ag NR R , де R є атомом водню, (C1-C6)алкілом, галогено(C1-C6) алкілом або аміно, як ah визначено в даному описі, і R є атомом водню або (C1-C6) алкілом, як визначено в даному описі. Якщо не вказане інше, весь відсотковий вміст визначений у відсотках за масою від загальної маси композиції. У конкретній формі здійснення гідрофобною, нестійкою до води сполукою, що має воскову консистенцію, є інгібітор CETP у формі тіоефірного похідного, такий як розкрито в EP 1020439 A1. Конкретні тіоефірні сполуки включають, наприклад, сполуки, що мають формулу I Y R NH 1 S X 2 Z 4 X X 3 X 20 25 30 (I) де R є C1-C8алкілом, C2-C6алкенілом, галогеноC1-C8алкілом, C3-C8циклоалкілом, C3C8циклоалкілC1-C8алкілом, арилом, аралкілом або 5- або 6-членною гетероциклічною групою, що має від 1 до 3 атомів азоту, кисню або сірки, 1 2 3 4 X , X , X и X незалежно є атомом водню, атомом галогену, C1-C8алкілом, галогеноC1C8алкілом, C1-C6алкокси, ціано, нітро, ацилом або арилом, Y є -CO- або -SO2; і Z є атомом водню, C1-C8алкілом, C3-C8циклоалкілом або C3-C8циклоалкілC1-C8алкілом. У кращій формі здійснення даного винаходу інгібітором CETP у формі тіоефірного похідного є S-(2-{[1-(2-етилбутил)-циклогексанкарбоніл]-аміно}-феніл)ефір тіоізомасляної кислоти, також відомий як S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоат, далцетрапіб або сполука, що має формулу I’ O NH S O 35 40 45 (I’) Показано, що S-[2-([[1-(2-етилбутил)циклогексил]карбоніл]аміно)феніл]2-метилпропантіоат є інгібітором активності CETP у людей (de Grooth et al., Circulation, 105, 2159-2165 (2002)) і кроликів (Shinkai et al., J. Med. Chem., 43, 3566-3572 (2000); Kobayashi et al., Atherosclerosis, 162, 131-135 (2002); і Okamoto et al., Nature, 406 (13), 203-207 (2000)). Показано, що S-[2-([[1-(2-етилбутил)циклогексил]карбоніл]аміно)феніл]2-метилпропантіоат підвищує рівень холестерину ЛПВЩ (ліпопротеїнів високої щільності) в плазмі у людей (de Grooth et al., див. вище) і у кроликів (Shinkai et al., див. вище; Kobayashi et al., див. вище; Okamoto et al., див. вище). Крім того, показано, що S-[2-([[1-(2етилбутил)циклогексил]карбоніл]аміно)феніл]2-метилпропантіоат знижує рівень холестерину ЛПНЩ (ліпопротеїнів низької щільності) в плазмі у людей (de Grooth et al., див. вище) і кроликів (Okamoto et al., див. вище). Додатково S-[2-([[1-(2етилбутил)циклогексил]карбоніл]аміно)феніл]2-метилпропантіоат інгібує прогресування атеросклерозу у кроликів (Okamoto et al., див. вище). S-[2-([[1-(2етилбутил)циклогексил]карбоніл]аміно)феніл]2-метилпропантіоат, а також способи одержання і 3 UA 110117 C2 5 10 15 20 25 30 35 40 45 50 55 60 застосування цієї сполуки, описані в патенті EP № EP1020439, Shinkai et al., J. Med. Chem. 43:3566-3572 (2000) або WO 2007/051714, WO 2008/074677 або WO2011/000793. У кращій формі здійснення інгібітор CETP у формі тіоефірного похідного (наприклад, сполука, що має формулу I або I’), є твердою речовиною в кристалічній або аморфній формі, краще в кристалічній формі. У конкретній формі здійснення S-[2-([[1-(2етилбутил)циклогексил]карбоніл]аміно)феніл]2-метилпропантіоат знаходиться в кристалічній формі A. Форма A характеризується порошковою рентгенівською дифрактограмою (ПРД), що має піки приблизно при 7,9°, 8,5°, 11,7°, 12,7°, 17,1°, 18,0°, 18,5°, 20,2°, 22,1°, 24,7° ± 0,2°, зокрема, піками ПРД, спостережуваними при куті дифракції2 тета 7,9°, 11,7°, 17,1°, 18,5° (±0,2°). Фармацевтичну композицію можна застосовувати для лікування або попередження серцевосудинного розладу, що включає, але не обмежений ними, атеросклероз, периферичне судинне захворювання, дисліпідемію (наприклад, гіперліпідемію), гіпербеталіпопротеїнемію, гіпоальфаліпопротеїнемію, гіперхолестеринемію, гіпертригліцеридемію, сімейну гіперхолестеринемію, стенокардію, ішемію, серцеву ішемію, удар, інфаркт міокарду, реперфузійне пошкодження, ангіопластичний рестеноз, гіпертензію, серцево-судинне захворювання, коронарну хворобу серця, захворювання коронарних артерій, гіперліпопротеїнемію, судинні ускладнення діабету, ожиріння або ендотоксемії у ссавця, зокрема, у людини (тобто чоловіка або жінки). Відповідно, у винаході запропонований спосіб лікування або профілактики серцевосудинного розладу у ссавця, що включає введення ссавцеві (краще ссавцеві, що потребує цього) терапевтично ефективної кількості фармацевтичної композиції. Ссавець краще є людиною (тобто чоловіком або жінкою). Людина може належати до будь-якої раси (наприклад, до європеоїдної раси або монголоїдної раси). Краще серцево-судинний розлад вибраний з групи, що складається з атеросклерозу, периферичного судинного захворювання, дисліпідемії, гіпербеталіпопротеїнемії, гіпоальфаліпопротеїнемії, гіперхолестеринемії, гіпертригліцеридемії, сімейної гіперхолестеринемії, стенокардії, ішемії, серцевої ішемії, удару, інфаркту міокарду, реперфузійного пошкодження, ангіопластичного рестенозу, гіпертензії і судинних ускладнень діабету, ожиріння або ендотоксемії у ссавця. Ще краще серцево-судинний розлад вибраний з групи, що складається з серцево-судинного захворювання, коронарної хвороби серця, захворювання коронарних артерій, гіпоальфаліпопротеїнемії, гіпербеталіпопротеїнемії, гіперхолестеринемії, гіперліпідемії, атеросклерозу, гіпертензії, гіпертригліцеридемії, гіперліпопротеїнемії, периферичного судинного захворювання, стенокардії, ішемії та інфаркту міокарду. У певних формах здійснення даного винаходу фармацевтична композиція містить: від 10 % до 69 % мас., краще від 40 % до 60 % мас., ще краще від 48 % до 55 % мас. гідрофобної, нестійкої до води сполуки, що має воскову консистенцію. У певних формах здійснення даного винаходу фармацевтична композиція містить: від 1 % до 10 % мас., краще від 5 % до 10 % мас., ще краще від 4 % до 8 % мас. суперрозпушувача. У певних формах здійснення даного винаходу фармацевтична композиція містить від 30 % до 70 % мас., краще від 30 % до 60 % мас., ще краще від 40 % до 50 % мас. щонайменше двох розріджувачів, що мають насипну щільність до ущільнення нижче 800 г/л. У конкретній формі здійснення в даному винаході запропонована фармацевтична композиція, що містить: - від 10 % до 69 % мас., краще від 40 % до 60 % мас., ще краще від 48 % до 55 % мас. гідрофобної, нестійкої до води сполуки, що має воскову консистенцію; - від 1 % до 10 % мас., краще від 5 % до 10 % мас., ще краще від 4 % до 8 % мас. суперрозпушувача і - від 30 % до 70 % мас., краще від 30 % до 60 % мас., ще краще від 40 % до 50 % мас. щонайменше двох розріджувачів, що мають насипну щільність до ущільнення нижче 800 г/л. У певних формах здійснення даного винаходу, як визначено в даному описі, суперрозпушувачем є гігроскопічний полімерний наповнювач. Зокрема, гігроскопічний полімерний наповнювач як суперрозпушувач є кроскармелозою натрію. У конкретній формі здійснення в даному винаході запропонована композиція, що містить: a) S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоат і b) кроскармелозу натрію. У певних формах здійснення даного винаходу, як визначено в даному описі, композиція додатково містить щонайменше один додатковий гігроскопічний полімерний наповнювач. У певних формах здійснення даного винаходу, як визначено в даному описі, композиція додатково містить щонайменше два гігроскопічних полімерних наповнювача. 4 UA 110117 C2 5 10 15 20 25 30 35 40 45 50 55 60 У певних формах здійснення даного винаходу, як визначено в даному описі, композиція додатково містить щонайменше три гігроскопічних полімерних наповнювача, два з яких є розріджувачами, що мають насипну щільність до ущільнення нижче 800 г/л. У певних формах здійснення даного винаходу, як визначено в даному описі, композиція містить від 10 % до 69 % мас. S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2метилпропантіоату. У певних формах здійснення даного винаходу фармацевтична композиція містить: від 10 % до 69 % мас., краще від 40 % до 60 % мас., ще краще від 48 % до 55 % мас. S-[2-([[1-(2етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоату. У певних формах здійснення даного винаходу, як визначено в даному описі, композиція містить від 1 % до 10 % мас., краще від 5 % до 10 % мас., ще краще від 5 % до 8 % мас. кроскармелози натрію. Конкретніше в певній формі здійснення композиція містить від 5 % до 7 % мас. кроскармелози натрію. У певних формах здійснення даного винаходу, як визначено в даному описі, композиція містить щонайменше 30 % мас. гігроскопічних полімерних наповнювачів, зокрема, від 44 % до 50 % мас., конкретніше від 46 % до 48 % мас., де гігроскопічні полімерні наповнювачі є гідроксипропілметилцелюлозою, кроскармелозою натрію, мікрокристалічною целюлозою і мікронізованим зшитим полівінілпіролідоном. У певних формах здійснення даного винаходу, як визначено в даному описі, композиція містить щонайменше 30 % мас., краще від 34 % до 44 % мас., ще краще від 40 % до 44 % мас. гігроскопічних полімерних наповнювачів. У певних формах здійснення даного винаходу, як визначено в даному описі, композиція містить щонайменше 30 % мас., краще від 34 % до 44 % мас., ще краще від 40 % до 44 % мас. додаткових гігроскопічних полімерних наповнювачів. У конкретній формі здійснення в даному винаході запропонована композиція, що містить: - від 10 % до 69 % мас., краще від 40 % до 60 % мас., ще краще від 48 % до 55 % мас. S-[2([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоату; - від 1 % до 10 % мас., краще від 5 % до 10 % мас., ще краще від 4 % до 8 % мас. кроскармелози натрію і - від 30 % до 90 % мас., краще від 34 % до 44 % мас., ще краще від 40 % до 44 % мас. гігроскопічних полімерних наповнювачів; де гігроскопічні полімерні наповнювачі вибрані з гідроксипропілметилцелюлози, мікрокристалічної целюлози і мікронізованого зшитого полівінілпіролідону. У певних формах здійснення даного винаходу, як визначено в даному описі, композиція містить: a) від 48 % до 55 % мас. S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2метилпропантіоату; b) від 4 % до 8 % мас. кроскармелози натрію; c) від 32 % до 41 % мас. нерозчинного у воді гігроскопічного полімеру; і d) від 4 % до 5 % мас. водорозчинного гігроскопічного полімеру. У певних формах здійснення даного винаходу, як визначено в даному описі, гігроскопічні полімерні наповнювачі вибрані з гідроксипропілметилцелюлози, гідроксипропілцелюлози, низькозаміщеної гідроксипропілцелюлози, гідроксиетилметилцелюлози, карбоксиполіметилену, метилцелюлози, етилцелюлози, гідроксиетилцелюлози, ацетату целюлози, полівінілпіролідону, зшитого полівінілпіролідону, мікронізованого зшитого полівінілпіролідону, кальцієвої солі карбоксиметилцелюлози, зшитої карбоксиметилцелюлози, мікрокристалічної целюлози, силікатизованої мікрокристалічної целюлози, целюлозного порошку, карбоксиметилкрохмалю, крохмалю і прежелатинізованого крохмалю. У певних формах здійснення даного винаходу, як визначено в даному описі, гігроскопічні полімерні наповнювачі є гідроксипропілметилцелюлозою, мікрокристалічною целюлозою і мікронізованим зшитим полівінілпіролідоном. У іншій формі здійснення у винаході запропонований спосіб одержання композиції, що включає наступні стадії: a) змішування і гранулювання S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2метилпропантіоату, кросповідону, мікрокристалічної целюлози, кроскармелози натрію і гідроксипропілметилцелюлози; b) розпилювання на грануляти, одержані на стадії а), ГПМЦ в кількості аж до 0,5 % мас. у воді або в суміші, що містить 10 %-30 % мас. етанолу/70 %-90 % мас. води; і c) змішування мікрокристалічної целюлози, колоїдного діоксиду кремнію і стеарилфумарату натрію з сухими гранулятами, одержаними згідно стадії с). 5 UA 110117 C2 5 10 15 20 25 30 35 40 45 50 55 У певних формах здійснення даного винаходу, як визначено в даному описі, два розріджувача є гігроскопічними полімерними наповнювачами. Зокрема, гігроскопічні полімерні наповнювачі як розріджувачі є етилцелюлозою, мікронізованим зшитим полівінілпіролідоном, мікрокристалічною целюлозою, силікатизованою мікрокристалічною целюлозою, целюлозним порошком, крохмалем, прежелатинізованим крохмалем. У певних формах здійснення даного винаходу, як визначено в даному описі, присутні щонайменше два гігроскопічних полімерних наповнювача. У певних формах здійснення даного винаходу, як визначено в даному описі, суперрозпушувач і щонайменше один з розріджувачів або щонайменше два розріджувача є гігроскопічними полімерними наповнювачами. Краще щонайменше суперрозпушувач і один з розріджувачів є гігроскопічними полімерними наповнювачами. У певних формах здійснення даного винаходу, як визначено в даному описі, суперрозпушувач і два розріджувача є гігроскопічними полімерними наповнювачами. У певних формах здійснення даного винаходу, як визначено в даному описі, міститься щонайменше 30 % мас., краще від 44 % до 50 % мас. гігроскопічних полімерних наповнювачів. У певних формах здійснення даного винаходу суперрозпушувач є кроскармелозою натрію. Зокрема, даний винахід включає аж до 6 % мас. кроскармелози натрію. У винаході запропонована фізично стабільна фармацевтична композиція, що містить щонайменше один гідрофобний і нестійкий до води інгібітор транспортного білка холестеринового ефіру (CETP) або його комбінацію, поміщену в таблетку з хімічно захисної гігроскопічної полімерної матриці, що складається щонайменше з одного гігроскопічного полімеру, наприклад, гідроксипропілметилцелюлози (ГПМЦ), гідроксипропілцелюлози (ГПЦ), низькозаміщеної гідроксипропілцелюлози (Н-ГПЦ), гідроксиетилметилцелюлози (ГЕМЦ), карбоксиполіметилену (карбомеру), метилцелюлози (МЦ), етилцелюлози (ЕЦ), гідроксиетилцелюлози (ГЕЦ), ацетату целюлози, полівінілпіролідону (ПВП), зшитого полівінілпіролідону (кросповідону), мікронізованого зшитого полівінілпіролідону (мікронізованого кросповідону), натрієвої солі карбоксиметилцелюлози (кроскармелози натрію, КМЦ Na), кальцієвої солі карбоксиметилцелюлози (кроскармелози кальцію, КМЦ Ca), зшитої карбоксиметилцелюлози (зшитої КМЦ), мікрокристалічної целюлози (МКЦ), силікатизованої мікрокристалічної целюлози (силікатизованої МКЦ), целюлозного порошку, карбоксиметилкрохмалю (натрієвої солі гліколяту крохмалю), крохмалю (кукурудзяного крохмалю, картопляного крохмалю, рисового крохмалю, пшеничного крохмалю, тапіокового крохмалю), прежелатинізованого крохмалю або їх комбінації в кількості, що краще становить 40 % мас. або більше на одиницю. У винаході запропонована фізично стабільна фармацевтична композиція, що містить щонайменше S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоат або його комбінацію, поміщену в таблетку з хімічно захисної гігроскопічної полімерної матриці, що складається щонайменше з одного гігроскопічного полімеру, наприклад, гідроксипропілметилцелюлози (ГПМЦ), гідроксипропілцелюлози (ГПЦ), низькозаміщеної гідроксипропілцелюлози (Н-ГПЦ), гідроксиетилметилцелюлози (ГЕМЦ), карбоксиполіметилену (карбомеру), метилцелюлози (МЦ), етилцелюлози (ЕЦ), гідроксиетилцелюлози (ГЕЦ), ацетату целюлози, полівінілпіролідону (ПВП), зшитого полівінілпіролідону (кросповідону), мікронізованого зшитого полівінілпіролідону (мікронізованого кросповідону), натрієвої солі карбоксиметилцелюлози (кроскармелози натрію, КМЦ Na), кальцієвої солі карбоксиметилцелюлози (кроскармелози кальцію, КМЦ Ca), зшитої карбоксиметилцелюлози (зшитої КМЦ), мікрокристалічної целюлози (МКЦ), силікатизованої мікрокристалічної целюлози (силікатизованої МКЦ), целюлозного порошку, карбоксиметилкрохмалю (натрієвої солі гліколяту крохмалю), крохмалю (кукурудзяного крохмалю, картопляного крохмалю, рисового крохмалю, пшеничного крохмалю, тапіокового крохмалю), прежелатинізованого крохмалю або їх комбінації в кількості, що краще становить 40 % мас. або більше на одиницю. Зокрема, в даному винаході запропонована фізично стабільна фармацевтична композиція, що містить щонайменше один гідрофобний і нестійкий до води інгібітор транспортного білка холестеринового ефіру (CETP), поміщений в таблетку з хімічно захисної гігроскопічної полімерної матриці, що складається з гідроксипропілметилцелюлози, натрієвої солі карбоксиметилцелюлози, мікрокристалічної целюлози і мікронізованого зшитого полівінілпіролідону. Зокрема, в даному винаході запропонована фізично стабільна фармацевтична композиція, що містить щонайменше S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2метилпропантіоат, поміщений в таблетку з хімічно захисної гігроскопічної полімерної матриці, 6 UA 110117 C2 5 10 15 що складається з гідроксипропілметилцелюлози, натрієвої солі карбоксиметилцелюлози, мікрокристалічної целюлози і мікронізованого зшитого полівінілпіролідону. У винаході запропонована фізично стабільна фармацевтична композиція, що містить щонайменше S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоат, поміщений в таблетку з хімічно захисної гігроскопічної полімерної матриці, що складається з гідроксипропілметилцелюлози, натрієвої солі карбоксиметилцелюлози, мікрокристалічної целюлози і мікронізованого зшитого полівінілпіролідону в кількості, що краще становить 40 % мас. або більше на одиницю. Зазвичай приведення чутливого до вологи активного фармацевтичного інгредієнта у контакт з великою кількістю гігроскопічних полімерів, таких як ГПМЦ, ГПЦ, ПВП, кросповідон, КМЦ, зшита КМЦ і МЦ, вважають небезпечним для фізичної стабільності. Несподівано було виявлено, що у випадку гідрофобного, чутливого до гідролізу інгібітора CETP можна спостерігати протилежний ефект. Стабілізація обох речовин, активного інгредієнта і таблетки швидкого вивільнення, можлива за допомогою поміщення активного інгредієнта в гігроскопічну полімерну матрицю, що складається з наступних речовин: Інгредієнт Інгібітор CETP у формі тіоэфіру Нерозчинний у воді гігроскопічний полімер Водорозчинний гігроскопічний полімер Інші наповнювачі 20 25 30 35 40 45 50 55 Відносна кількість серцевини таблетки [%] > 50% > 40% > 4% < 6% Крім того, було несподівано виявлено, що збільшення кількості гігроскопічних полімерів у порівнянні з її звичайним діапазоном від 10-20 % мас. до більше ніж 30 % мас. у присутності гідрофобної сполуки не приводить до закупорювання або розтріскування препарату у вигляді таблетки швидкого вивільнення, як можна було б чекати. Таким чином, гідрофобна сполука запобігає утворенню тріщин таблетки швидкого вивільнення, якщо більше ніж 30 % мас. таблетки складається з гігроскопічних полімерних наповнювачів. У іншій формі здійснення в даному винаході запропонована композиція, що містить: a) від 48 % до 55 % мас. інгібітора CETP у формі тіоефірного похідного; і b) щонайменше 30 %, краще від 44 % до 50 % мас. гігроскопічних полімерних наповнювачів від маси композиції. У іншій формі здійснення в даному винаході запропонована композиція, що містить: a) від 48 % до 55 % мас. інгібітора CETP у формі тіоефірного похідного; b) від 40 % до 45 % мас. нерозчинного у воді гігроскопічного полімеру; c) від 4 % до 5 % мас. водорозчинного гігроскопічного полімеру. У певних формах здійснення даного винаходу щонайменше два розріджувача, що мають насипну щільність до ущільнення нижче 800 г/л, є мікрокристалічною целюлозою і манітом. У певних формах здійснення даного винаходу, щонайменше два розріджувача, що мають насипну щільність до ущільнення нижче 800 г/л, є мікрокристалічною целюлозою і мікронізованим кросповідоном. У певних формах здійснення даного винаходу масове відношення мікрокристалічної целюлози і маніту складає приблизно від 9:1 до 1:1. У певних формах здійснення даного винаходу масове відношення мікрокристалічної целюлози і мікронізованого кросповідону складає приблизно від 5:1 до 5:3. У іншій формі здійснення в даному винаході запропонована композиція, що містить: - від 48 % до 55 % мас. інгібітора CETP у формі тіоефірного похідного; і -щонайменше 30 % мас., краще від 44 % до 50 % мас. гідроксипропілметилцелюлози, кроскармелози натрію, мікрокристалічної целюлози і мікронізованого зшитого полівінілпіролідону. У іншій формі здійснення в даному винаході запропонована композиція, що містить: a) від 48 % до 55 % мас. інгібітора CETP у формі тіоефірного похідного; b) від 4 % до 8 % мас. кроскармелози натрію; і c) від 35 % до 44 % мас. гідроксипропілметилцелюлози, мікрокристалічної целюлози і мікронізованого кросповідону. У іншій формі здійснення в даному винаході запропонована композиція, що містить: a) від 48 % до 55 % мас. інгібітора CETP у формі тіоефірного похідного; b) менше 12 % мас. мікронізованого кросповідону; і c) від 35 % до 44 % мас. гідроксипропілметилцелюлози, мікрокристалічної целюлози і кроскармелози натрію. 7 UA 110117 C2 5 10 15 20 25 30 35 40 45 50 55 У іншій формі здійснення в даному винаході запропонована композиція, що містить: a) інгібітор CETP у формі тіоефірного похідного, конкретніше S-[2-([[1-(2-етилбутил)циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоат; b) кроскармелозу натрію. У іншій формі здійснення в даному винаході запропонована композиція, що містить: a) інгібітор CETP у формі тіоефірного похідного, конкретніше S-[2-([[1-(2-етилбутил)циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоат; b) мікрокристалічну целюлозу; c) мікронізований кросповідон; d) гідроксипропілметилцелюлозу; і e) кроскармелозу натрію. У іншій формі здійснення в даному винаході запропонована композиція, що містить: a) інгібітор CETP у формі тіоефірного похідного, конкретніше S-[2-([[1-(2-етилбутил)циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоат; b) маніт; c) мікронізований кросповідон; d) гідроксипропілметилцелюлозу; e) кроскармелозу натрію. У іншій формі здійснення в даному винаході запропонована композиція, що містить: a) інгібітор CETP у формі тіоефірного похідного, конкретніше S-[2-([[1-(2-етилбутил)циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоат; b) маніт; c) мікронізований кросповідон; d) гідроксипропілметилцелюлозу; e) кроскармелозу натрію; f) мікрокристалічну целюлозу. У іншій формі здійснення в даному винаході запропонована композиція, що містить: a) від 48 % до 55 % мас. інгібітора CETP у формі тіоефірного похідного, конкретніше S-[2([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-етилпропантіоату; b) від 24 % до 26 % мас. мікрокристалічної целюлози; c) від 11 % до 12 % мас. мікронізованого кросповідону; d) від 4 % до 5 % мас. гідроксипропілметилцелюлози; e) від 4 % до 6 % мас. кроскармелози натрію. У іншій формі здійснення в даному винаході запропонована композиція, що містить: a) від 48 % до 55 % мас. інгібітора CETP у формі тіоефірного похідного, конкретніше S-[2([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]-2-етилпропантіоату; b) від 24 % до 26 % мас. мікрокристалічної целюлози; c) від 11 % до 12 % мас. мікронізованого кросповідону; d) від 4 % до 5 % мас. гідроксипропілметилцелюлози; e) від 4 % до 6 % мас. кроскармелози натрію; f) від 0 до 1 % мас. стеарату магнію; g) від 0 до 1 % мас. колоїдного діоксиду кремнію; h) від 0 до 1 % мас. стеарилфумарату натрію. У іншій формі здійснення в даному винаході запропонована композиція, що містить: a) від 48 % до 55 % мас. інгібітора CETP у формі тіоефірного похідного, конкретніше S-[2([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоату; b) від 10 % до 14 % мас. маніту; c) від 8 % до 12 % мас. мікронізованого кросповідону; d) від 2 % до 6 % мас. гідроксипропілметилцелюлози; e) від 5 % до 9 % мас. кроскармелози натрію. У іншій формі здійснення в даному винаході запропонована композиція, що містить: a) від 48 % до 55 % мас. інгібітора CETP у формі тіоефірного похідного, конкретніше S-[2([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоату; b) від 10 % до 14 % мас. маніту; c) від 8 % до 12 % мас. мікронізованого кросповідону; d) від 2 % до 6 % мас. гідроксипропілметилцелюлози; e) від 5 % до 9 % мас. кроскармелози натрію; f) від 11 % до 15 % мас. мікрокристалічної целюлози. У певних формах здійснення даного винаходу композиція є фармацевтичною композицією. 8 UA 110117 C2 5 10 15 20 25 30 35 40 45 50 55 60 Фармацевтична композиція може мати, наприклад, форму пілюлі, капсули або таблетки, де кожна форма містить зумовлену кількість інгібітора CETP у формі тіоефіру, і, зокрема, містить покриття для полегшення прийому всередину, а також у формі порошку або гранул. Зокрема, фармацевтична композиція має форму таблетки, що містить інгібітор CETP у формі тіоефірного похідного і компоненти таблетки, застосовувані і описані в даному винаході. Для перорального введення тонкоподрібнені порошки або гранули можуть містити розріджувачі, диспергатори та/або поверхнево-активні агенти і можуть знаходитися, наприклад, у капсулах або саше в сухому стані, або в таблетках, де можна включати зв'язуючі або змащувальні речовини. У фармацевтичній композиції можуть також бути такі інгредієнти, як підсолоджувачі, коригенти, консерванти, суспендуючі агенти, загусники та/або емульгатори. У конкретній формі здійснення композиція, описана в даному винаході, вкрита плівковим покриттям на основі полівінілового спирту (покриттям на основі ПВС), зокрема, покриттям на основі 20 мг або менше ПВС, конкретніше покриттям на основі 15 мг ПВС. У певних формах здійснення даного винаходу композиція містить від 100 мг до 600 мг S-[2([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоату. Зокрема, композиція містить від 150 мг до 450 мг S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2метилпропантіоату. Конкретніше композиція містить від 250 мг до 350мг S-[2-([[1-(2-етилбутил)циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоату. Найконкретніше композиція містить від 250 мг до 350 мг S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2метилпропантіоату. У іншій формі здійснення даного винаходу композиція для застосування для дитячого віку містить від 25 мг до 300 мг S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2метилпропантіоату. Зокрема, композиція для застосування для дитячого віку містить від 75 мг до 150 мг S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоату. Інгібітор CETP можна вводити ссавцеві в будь-якому відповідному дозуванні (наприклад, для досягнення терапевтично ефективної кількості). Наприклад, відповідна доза терапевтично ефективної кількості сполуки I для введення пацієнтові складатиме приблизно від 100 мг до приблизно 1800 мг на добу. Бажана доза краще складає приблизно від 300 мг до приблизно 900 мг на добу. Краща доза складає приблизно 600 мг на добу. У іншій формі здійснення у винаході запропонований набір, що включає фармацевтичну композицію, що містить терапевтично ефективну кількість інгібітора CETP у формі тіоефірного похідного і щонайменше 30 % мас. гігроскопічних полімерних наповнювачів від маси композиції, вказівки із застосування препарату, також відомі як “листок-вкладиш”, блістерну упаковку або пляшку (з ПЕВЩ (поліетилену високої щільності) або скла) і контейнер. Вказівки із застосування препарату краще включають рекомендації для пацієнта по введенню інгібітора CETP у формі тіоефірного похідного (наприклад, сполуки, що має формулу (I’)) при їді, зокрема, для поліпшення біодоступності інгібітора CETP у формі тіоефірного похідного. У іншій формі здійснення у винаході запропонований набір, що включає композицію, як описано в даному винаході, вказівки із застосування препарату, також відомі як “листоквкладиш”, блістерну упаковку або пляшку (з ПЕВЩ (поліетилену високої щільності) або скла) і контейнер. Вказівки із застосування препарату краще включають рекомендації для пацієнта по введенню інгібітора CETP у формі тіоефірного похідного (наприклад, сполуки, що має формулу (I’)) при їді, зокрема, для поліпшення біодоступності інгібітора CETP у формі тіоефірного похідного. У іншій формі здійснення у винаході запропонований набір, що включає композицію, що містить терапевтично ефективну кількість S-[2-([[1-(2-етилбутил)-циклогексил]карбоніл]аміно)феніл]2-метилпропантіоату і щонайменше 30 % мас. гігроскопічних полімерних наповнювачів від маси композиції, вказівки із застосування препарату, блістерну упаковку або пляшку і контейнер. У конкретній формі здійснення у винаході запропонований набір, як описано в даному винаході, де вказівки із застосування препарату включають рекомендації для пацієнта по введенню S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоату при їді. У іншій формі здійснення у винаході запропонована таблетка, що включає композицію, як описано в даному винаході. У іншій формі здійснення у винаході запропонована композиція, як описано в даному винаході, для одержання лікарського засобу для лікування або попередження серцевосудинного розладу, зокрема, де S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2метилпропантіоат вводять у добовій дозі від 100 мг до 1800 мг, зокрема, від 300 мг до 900 мг, конкретніше 600 мг, краще де S-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2метилпропантіоат вводять при їді. 9 UA 110117 C2 5 10 15 20 25 30 35 40 45 50 55 60 У іншій формі здійснення в даному винаході запропонований спосіб одержання композиції, як описано в даному винаході, що включає наступні стадії: a) змішування і гранулювання нестійкої до води сполуки, що має воскову консистенцію, мікронізованого кросповідону, мікрокристалічної целюлози, кроскармелози натрію і необов'язково гідроксипропілметилцелюлози; b) розпилювання на грануляти, одержані згідно стадії а), 0,5 % мас. гідроксипропілметилцелюлози у воді або в суміші 10 %-30 % мас. етанолу/70 %-90 % мас. води, краще в суміші 20 % мас. етанолу/80 % мас. води; c) висушування гранулятів; і d) змішування мікрокристалічної целюлози, колоїдного діоксиду кремнію і стеарилфумарату натрію з сухими гранулятами, одержаними згідно стадії с). У іншій формі здійснення в даному винаході запропонований спосіб одержання композиції, як описано в даному винаході, що включає наступні стадії: a) змішування і гранулювання нестійкої до води сполуки, що має воскову консистенцію, мікронізованого кросповідону, маніту, кроскармелози натрію і гідроксипропілметилцелюлози; b) розпилювання на грануляти, одержані згідно стадії а), 0,5 % мас. гідроксипропілметилцелюлози у воді або в суміші 10 %-30 % мас. етанолу/70 %-90 % мас. води, краще в суміші 20 % мас. етанолу/80 % мас. води; c) висушування гранулятів; і d) змішування мікрокристалічної целюлози, колоїдного діоксиду кремнію і стеарилфумарату натрію з сухими гранулятами, одержаними згідно стадії с). У іншій формі здійснення в даному винаході запропонований спосіб одержання композиції, як описано в даному винаході, що включає наступні стадії: a) змішування і гранулювання нестійкої до води сполуки, що має воскову консистенцію, мікронізованого кросповідону, мікрокристалічної целюлози і кроскармелози натрію; b) розпилювання на грануляти, одержані згідно стадії а), 0,5 % мас. гідроксипропілметилцелюлози в суміші 10 %-30 % мас. етанолу/70 %-90 % мас. води, краще в суміші 20 % мас. етанолу/80 % мас. води; c) висушування гранулятів; і d) змішування мікрокристалічної целюлози, колоїдного діоксиду кремнію і стеарилфумарату натрію з сухими гранулятами, одержаними згідно стадії с). У іншій формі здійснення в даному винаході запропонований спосіб одержання композиції, як описано в даному винаході, що включає наступні стадії: a) змішування і гранулювання нестійкої до води сполуки, що має воскову консистенцію, мікронізованого кросповідону, мікрокристалічної целюлози, кроскармелози натрію і гідроксипропілметилцелюлози; b) розпилювання на грануляти, одержані згідно стадії а), грануляційної рідини, що складається з суміші 10 %-30 % мас. етанолу/70 %-90 % мас. води, конкретніше з суміші 20 % мас. етанолу/80 % мас. води; c) висушування гранулятів; d) змішування мікрокристалічної целюлози, колоїдного діоксиду кремнію і стеарилфумарату натрію з сухими гранулятами, одержаними згідно стадії с); e) пресування таблеток; f) підігрівання таблеток вхідним повітрям температури не більше 60 °C до досягнення температури таблеток приблизно 43 °C; ® g) розпилювання на таблетки суспензії для покриття Опадрай ; і h) висушування таблеток, вкритих плівкою, при постійному обертанні у перфорованому барабані для нанесення покриття. Спосіб одержання У даному описі АРІ належить до активної речовини, що є гідрофобною, нестійкою до води сполукою, що має воскову консистенцію, зокрема, до інгібітора CETP у формі тіоефірного похідного, конкретніше до інгібітора CETP у формі тіоефірного похідного, що має формулу (I) або (I’). У прикладах 1-45 АРІ належить до S-(2-{[1-(2-етилбутил)-циклогексанкарбоніл]-аміно}феніл)ефіру тіоізомасляної кислоти, що має формулу (I’), у кристалічній формі. Композиція за даним винаходом може бути одержана будь-яким відомим способом, результатом якого є підтримування АРІ по суті у кристалічній формі (кількість гідрофобного АРІ в аморфній формі не перевищує 10 % мас.). Крім того, композиція за даним винаходом може бути одержана будь-яким відомим способом, результатом якого є підтримування АРІ по суті у кристалічній формі (кількість гідрофобної, нестійкої до води сполуки, що має воскову консистенцію, по суті в аморфній формі не перевищує 10 % мас.). 10 UA 110117 C2 5 10 15 20 25 30 35 40 45 50 55 Спосіб одержання фармацевтичної композиції згідно з даним винаходом може включати наступні стадії: 1) розчинення гідроксипропілметилцелюлози (0,5 % мас. від загальної кількості гідроксипропілметилцелюлози) у суміші 20 % мас. етанолу і 80 % мас. води при постійному перемішуванні; 2) завантаження гідрофобної, нестійкої до води сполуки, що має воскову консистенцію, мікронізованого кросповідону, мікрокристалічної целюлози, кроскармелози натрію і решти частини гідроксипропілметилцелюлози у гранулятор (мішалку з великими зсувними зусиллями, ® наприклад, Diosna ), що є вертикальним гранулятором з лопатевою мішалкою з нижнім приводом; 3) змішування інгредієнтів сухого грануляту з використанням лопатевої мішалки і подрібнювача; 4) зволоження грануляту шляхом розпилювання грануляційної рідини при постійному перемішуванні з використанням лопатевої мішалки і подрібнювача; 5) замішування зволоженого грануляту з використанням лопатевої мішалки і подрібнювача; 6) вивантаження вологого грануляту, просіювання його через конусний млин [наприклад, ® Frewitt (млин, що просіює, з лопатевою мішалкою, що обертається)], обладнаний ситом з квадратними отворами діаметром 10 мм, і завантаження його у сушарку з псевдозрідженим шаром; ® 7) висушування грануляту в сушарці з псевдозрідженим шаром (наприклад, Glatt ) при температурі вхідного повітря не більше 60 °C до досягнення кінцевого значення LOD (втрата в масі при висушуванні; loss on drying) не більше 3,5 % мас.; 8) вивантаження висушеного грануляту і подрібнення його з використанням ударного млина, ® обладнаного ситом з округлими отворами діаметром 1,5 мм (наприклад, Frewitt (ударний млин з молотком, що обертається); 9) додавання до грануляту інгредієнтів зовнішньої фази (наприклад, мікрокристалічної целюлози, колоїдного діоксиду кремнію і стеарилфумарату натрію) і нанесення на сито, обладнане округлими отворами діаметром 1 мм; ® 10) змішування всіх інгредієнтів у бункерному змішувачі (наприклад, Tumblemix (змішування перевертанням в бункерному змішувачі)); 11) пресування таблеток на роторному таблетковому пресі з низьким зусиллям пресування ® (приблизно 6 кН) наприклад, Korsch (з підсилювачем); 12) приготування суспензії для покриття за допомогою суспендування повної системи ® покриття Опадрай у воді при постійному перемішуванні; 13) завантаження таблеток у перфорований барабан для нанесення покриття; 14) підігрівання таблеток вхідним повітрям температури не більше 60 °C до досягнення температури таблеток приблизно 43 °C при постійному обертанні у перфорованому барабані ® для нанесення покриття (наприклад, Glatt (перфорована система покриття)); 15) розпилювання суспензії для покриття на таблетки при постійному обертанні у перфорованому барабані для нанесення покриття; 16) висушування таблеток з плівковим покриттям при постійному обертанні у перфорованому барабані для нанесення покриття; 17) вивантаження таблеток з плівковим покриттям. Альтернативно, як приклад для композиції з гідроксипропілметилцелюлозою 6 сП, спосіб одержання фармацевтичної композиції згідно з даним винаходом може включати наступні стадії: 1) розчинення всієї гідроксипропілметилцелюлози в суміші 20 % мас. етанолу і 80 % мас. води при постійному перемішуванні; 2) завантаження гідрофобної, нестійкої до води сполуки, що має воскову консистенцію, мікронізованого кросповідону, мікрокристалічної целюлози і кроскармелози натрію в гранулятор ® (мішалку з великими зсувними зусиллями, наприклад, Diosna ), що є вертикальним гранулятором з лопатевою мішалкою з нижнім приводом; 3) змішування інгредієнтів сухого грануляту з використанням лопатевої мішалки і подрібнювача; 4) зволоження грануляту за допомогою розпилювання грануляційної рідини при постійному перемішуванні з використанням лопатевої мішалки і подрібнювача; 5) замішування зволоженого грануляту з використанням лопатевої мішалки і подрібнювача; 6) вивантаження вологого грануляту, просіювання його через конусний млин [наприклад, ® Frewitt (млин, що просіює, з лопатевою мішалкою, що обертається)], обладнаний ситом з 11 UA 110117 C2 5 10 15 20 25 30 квадратними отворами діаметром 10 мм, і завантаження його в сушарку з псевдозрідженим шаром; ® 7) висушування грануляту в сушарці з псевдозрідженим шаром (наприклад, Glatt ) при температурі вхідного повітря не більше 60 °C до досягнення кінцевого значення LOD (втрата в масі при висушуванні; loss on drying) не більше 3,5 % мас.; 8) вивантаження висушеного грануляту і подрібнення його з використанням ударного млина, ® обладнаного ситом з округлими отворами діаметром 1,5 мм (наприклад, Frewitt (ударний млин з молотком, що обертається); 9) додавання до грануляту інгредієнтів зовнішньої фази (наприклад, мікрокристалічної целюлози, колоїдного діоксиду кремнію і стеарилфумарату натрію) і нанесення на сито, обладнане округлими отворами діаметром 1 мм; ® 10) змішування всіх інгредієнтів в бункерному змішувачі (наприклад, Tumblemix (змішування перевертанням в бункерному змішувачі)); 11) пресування таблеток на роторному таблетковому пресі з низьким зусиллям пресування ® (приблизно 6 кН) наприклад, Korsch (з підсилювачем); 12) приготування суспензії для покриття за допомогою суспендування повної системи ® покриття Опадрай у воді при постійному перемішуванні; 13) завантаження таблеток у перфорований барабан для нанесення покриття; 14) підігрівання таблеток вхідним повітрям температури не більше 60 °C до досягнення температури таблеток приблизно 43 °C при постійному обертанні в перфорованому барабані ® для нанесення покриття (наприклад, Glatt (перфорована система покриття)); 15) розпилювання суспензії для покриття на таблетки при постійному обертанні в перфорованому барабані для нанесення покриття; 16) висушування таблеток з плівковим покриттям при постійному обертанні в перфорованому барабані для нанесення покриття; 17) вивантаження таблеток з плівковим покриттям. Інші ознаки і форми здійснення винаходу стануть очевидними на підставі приведених нижче прикладів, які приведені, швидше, для ілюстрації винаходу, ніж для обмеження його визначеного об'єму. Приклади 1-42 і приклад плацебо A були одержані відповідно до описаних вище загальних методів, де АРІ для прикладу A замінений манітом. Всі приклади 1-42 були вкриті 20 мг ® плівкового покриття на основі ПВС (наприклад, Опадрай ). Приклад № 1 API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон ГПМЦ (2910 3сп) КМЦ Na Колоїдний діоксид кремнію Стеарилфумарат натрію Мікрокристалічна целюлоза (Тип 102) Вся таблетка Кількість/ одиниця [мг] Інгредієнт Маса/ одиниця [%] Нерозчинний у воді Водорозчинний 300,00 52,54 N/A N/A 66 11,56 + 66,00 11,56 + 24,00 34,00 4,20 5,95 + 3,00 0,53 N/A N/A 3,00 0,53 N/A N/A 75,00 13,35 + 571,00 100,00 гігроскопічний полімер + Кількість гігроскопічних полімерів 42,21% Загальна кількість гігроскопічних полімерів 46,41% 35 12 4,20% UA 110117 C2 Приклад № 2 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон ГПМЦ (2910 3сп) 300,00 53,38 N/A N/A 66,00 11,74 + 66,00 11,74 + 24,00 4,27 КМЦ Na Стеарилфумарат натрію Мікрокристалічна целюлоза (Тип 102) 28,00 4,98 + 3,00 0,53 N/A 75,00 13,35 + Вся таблетка 562,00 100,00 Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів 5 гігроскопічний полімер + 41,81% N/A 4,27% 46,08% Приклад № 3 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон ГПМЦ (2910 3сп) 300,00 53,10 N/A N/A 66,00 11,68 + 66,00 11,68 + 24,00 4,25 КМЦ Na Стеарилфумарат натрію Стеарат магнію Мікрокристалічна целюлоза (Тип 102) 28,00 4,96 + 3,00 0,53 N/A N/A 3,00 0,53 N/A N/A 75,00 13,27 + 565,00 100,00 Інгредієнт Вся таблетка Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 41,59% 45,84% 13 4,25% UA 110117 C2 Приклад № 4 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон ГПМЦ (2910 3сп) 300,00 53,10 N/A N/A 66,00 11,68 + 66,00 11,68 + 24,00 4,25 КМЦ Na Стеарилфумарат натрію Колоїдний діоксид кремнію Мікрокристалічна целюлоза (Тип 102) 28,00 4,96 + 3,00 0,53 N/A N/A 3,00 0,53 N/A N/A 75,00 13,27 + Вся таблетка 565,00 100,00 Інгредієнт гігроскопічний полімер + Кількість гігроскопічних полімерів 41,59% Загальна кількість гігроскопічних полімерів 45,84% 4,25% Приклад № 5 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон ГПМЦ (2910 3сп) 300,00 52,82 N/A N/A 66,00 11,62 + 66,00 11,62 + 24,00 4,23 КМЦ Na 34,00 5,99 + Стеарилфумарат натрію Мікрокристалічна целюлоза (Тип 102) 3,00 0,53 N/A 75,00 13,20 + 568,00 100,00 Інгредієнт Вся таблетка Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 42,43% 46,65% 14 N/A 4,23% UA 110117 C2 Приклад № 6 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон ГПМЦ (2910 3сп) 300,00 52,54 N/A N/A 66,00 11,56 + 66,00 11,56 + 24,00 4,20 КМЦ Na Стеарилфумарат натрію Колоїдний діоксид кремнію Мікрокристалічна целюлоза (Тип 102) 34,00 5,95 + 3,00 0,53 N/A N/A 3,00 0,53 N/A N/A 75,00 13,13 + Вся таблетка 571,00 100,00 Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 42,21% 4,20% 46,41% Приклад № 7 5 API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон ГПМЦ (2910 3сп) КМЦ Na Стеарилфумарат натрію Колоїдний діоксид кремнію Мікрокристалічна целюлоза (Тип 102) Вся таблетка Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів Кількість/ одиниця [мг] Інгредієнт Маса/ одиниця [%] 300,00 52,34 Нерозчинний у воді N/A 66,00 11,51 + 66,00 11,51 + 24,00 36,20 4,19 6,32 + 3,00 0,52 N/A N/A 3,00 0,52 N/A N/A 75,00 13,08 + 573,20 100,00 гігроскопічний полімер + 42,43% 46,62% 15 Водорозчинний N/A 4,19% UA 110117 C2 Приклад № 8 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний 300,00 51,99 N/A N/A 75,00 13,00 + 60,00 10,40 + 24,00 72,00 40,00 4,16 12,48 6,93 N/A + 3,00 0,52 N/A N/A 3,00 0,52 N/A N/A 577,00 100,00 Кількість гігроскопічних полімерів 30,33% 4,16% Загальна кількість гігроскопічних полімерів 34,49% Інгредієнт API Мікрокристалічна целюлоза (Тип 102) Мікронізований кросповідон ГПМЦ (2910 3сп) Маніт КМЦ Na Колоїдний діоксид кремнію Стеарилфумарат натрію Вся таблетка гігроскопічний полімер + N/A Приклад № 9 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон ГПМЦ (2910 3сп) Мікрокристалічна целюлоза (Тип 102) КМЦ Na 300,00 55,58 N/A N/A 67,00 12,41 + 67,00 12,41 + 18,00 3,33 50,00 9,26 + 27,00 5,00 + Гліцерилбегенат 10,80 2,00 N/A N/A Вся таблетка 539,80 100,00 39,09% 3,33% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 42,42% 16 UA 110117 C2 Приклад № 10 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон 300,00 50,77 N/A N/A 67,00 11,34 + 67,00 11,34 + ГПМЦ (2910 3сп) Мікрокристалічна целюлоза (Тип 102) КМЦ Na 18,00 3,05 100,00 16,92 + 27,00 4,57 + Гліцерилбегенат 11,85 2,01 N/A N/A Вся таблетка 590,85 100,00 44,17% 3,05% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 47,22% Приклад № 11 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон 300,00 53,10 N/A N/A 69,00 12,21 + 69,00 12,21 + ГПМЦ (2910 3сп) Мікрокристалічна целюлоза (Тип 102) КМЦ Na 21,00 3,72 75,00 13,27 + 28,00 4,95 + Стеарилфумарат натрію 3,00 0,53 N/A N/A 565,00 100,00 42,64% 3,72% гігроскопічний полімер Інгредієнт Вся таблетка Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів + 46,36% 17 UA 110117 C2 Приклад № 12 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон 300,00 53,67 N/A N/A 69,00 12,34 + 69,00 12,34 + ГПМЦ (2910 3сп) Мікрокристалічна целюлоза (Тип 102) КМЦ Na 21,00 3,76 75,00 13,42 + 22,00 3,94 + Стеарилфумарат натрію 3,00 0,54 N/A N/A 559,00 100,00 42,04% 3,76% гігроскопічний полімер Інгредієнт Вся таблетка Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів + 45,80% Приклад № 13 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон 300,00 52,91 N/A N/A 69,00 12,17 + 69,00 12,17 + ГПМЦ (2910 3сп) Мікрокристалічна целюлоза (Тип 102) КМЦ Na 21,00 3,70 75,00 13,23 + 22,00 3,88 + Стеарилфумарат натрію 3,00 0,53 N/A N/A Тальк 8,00 1,41 N/A N/A 567,00 100,00 41,45% 3,70% гігроскопічний полімер Інгредієнт Вся таблетка Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів + 45,15% 18 UA 110117 C2 Приклад № 14 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон 300,00 53,38 N/A N/A 66,00 11,74 + 66,00 11,74 + ГПМЦ (2910 3сп) 24,00 4,27 КМЦ Na Мікрокристалічна целюлоза (Тип 200) Стеарилфумарат натрію 28,00 4,98 + 75,00 13,35 + 3,00 0,53 N/A N/A Вся таблетка 562,00 100,00 41,81% 4,27% гігроскопічний полімер Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів + 46,09% Приклад № 15 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон 300,00 53,38 N/A N/A 66,00 11,74 + 66,00 11,74 + ГПМЦ (2910 3сп) 24,00 4,27 КМЦ Na Силікатизована мікрокристалічна целюлоза (Тип Prosolv SMCC 90) Стеарилфумарат натрію 28,00 4,98 + 75,00 13,35 + 3,00 0,53 N/A N/A Вся таблетка 562,00 100,00 41,81% 4,27% гігроскопічний полімер Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів + 46,09% 19 UA 110117 C2 Приклад № 16 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон 300,00 54,84 N/A N/A 90,00 16,45 + 119,80 21,90 + ГПМЦ (2910 6сп) 18,00 3,29 Тальк 3,29 N/A N/A Стеарат магнію 18,00 1,20 0,22 N/A N/A Вся таблетка 547,00 100,00 38,35% 3,29% гігроскопічний полімер Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів + 41,65% Приклад № 17 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон 300,00 55,66 N/A N/A 90,00 16,70 + 119,80 22,23 + ГПМЦ (2910 6сп) 18,00 3,34 Гліцерилбегенат 11,20 2,08 Вся таблетка 539,0 100,00 гігроскопічний полімер Інгредієнт + N/A 38,92% Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів N/A 3,34% 42,26% 20 UA 110117 C2 Приклад № 18 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API Мікрокристалічна целюлоза (Тип 101) Мікронізований кросповідон 300,00 55,72 N/A N/A 100,00 18,57 + 59,20 11,00 + ГПМЦ (2910 6сп) 18,00 3,34 Низькозаміщена ГПЦ 50,00 9,29 + Глицерилбегенат 11,20 2,08 N/A N/A Вся таблетка 538,40 100,00 38,86% 3,34% гігроскопічний полімер Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів + 42,20% Приклад № 19 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 55,66 N/A N/A Маніт 100,00 18,55 N/A N/A Мікронізований кросповідон 59,80 11,09 + ГПМЦ (2910 3сп) Мікрокристалічна целюлоза (Тип 200) Гліцерилбегенат 18,00 3,34 50,00 9,28 + 11,20 2,08 N/A N/A Вся таблетка 539,00 100,00 31,73% 12,62% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 44,34% 21 UA 110117 C2 Приклад № 20 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 55,66 N/A N/A Маніт 100,00 18,55 N/A N/A Мікронізований кросповідон 59,80 11,09 + ГПМЦ (2910 3сп) Мікрокристалічна целюлоза (Тип 200) Стеарилфумарат натрію 18,00 3,34 50,00 9,28 + 11,20 2,08 N/A N/A Вся таблетка 539,00 100,00 31,73% 12,62% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 44,34% Приклад № 21 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 56,56 N/A N/A Маніт 100,00 18,85 N/A N/A Мікронізований кросповідон 59,80 11,27 + ГПМЦ (2910 3сп) Мікрокристалічна целюлоза (Тип 200) Стеарилфумарат натрію 18,00 3,39 50,00 9,43 + 2,65 0,50 N/A N/A Вся таблетка 530,45 100,00 30,62% 12,82% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 43,44% 22 UA 110117 C2 Приклад № 22 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 56,60 N/A N/A Маніт 100,00 18,87 N/A N/A Мікронізований кросповідон 59,80 11,28 + ГПМЦ (2910 3сп) Мікрокристалічна целюлоза (Тип 200) Стеарилфумарат натрію 18,00 3,40 50,00 9,43 + 2,24 0,42 N/A N/A Вся таблетка 530,04 100,00 30,57% 12,83% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 43,40% Приклад № 23 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 56,56 N/A N/A Маніт 100,00 18,85 N/A N/A Мікронізований кросповідон 59,80 11,27 + ГПМЦ (2910 3сп) Мікрокристалічна целюлоза (Тип 200) 18,00 3,39 25,00 4,71 + Низькозаміщена ГПЦ 25,00 4,71 + Стеарилфумарат натрію 2,65 0,50 N/A N/A 530,45 100,00 20,70% 3,39% Інгредієнт Вся таблетка Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 24,09% 23 UA 110117 C2 Приклад № 24 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 55,17 N/A N/A Маніт 100,00 18,39 N/A N/A Мікронізований кросповідон 59,80 11,00 + ГПМЦ (2910 6сп) Мікрокристалічна целюлоза (Тип 200) 18,00 3,31 50,222 9,223 + Тальк 4,78 0,88 N/A N/A Гліцерилбегенат 11,20 2,06 N/A N/A Вся таблетка 544,00 100,04 20,19% 3,31% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 23,50% Приклад № 25 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 55,66 N/A N/A Маніт 100,00 18,55 N/A N/A Мікронізований кросповідон 59,80 11,09 + ГПМЦ (2910 6сп) Мікрокристалічна целюлоза (Тип 200) 18,00 3,34 50,00 9,28 + Гліцерилбегенат 11,20 2,08 N/A N/A Вся таблетка 539,00 100,00 20,37% 3,34% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 23,71% 24 UA 110117 C2 Приклад № 26 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 55,66 N/A N/A Маніт 100,00 18,55 N/A N/A Мікронізований кросповідон 59,80 11,09 + ГПМЦ (2910 6сп) Мікрокристалічна целюлоза (Тип 200) 18,00 3,34 50,00 9,28 + Стеарилфумарат натрію 11,20 2,08 N/A N/A Вся таблетка 539,00 100,00 20,37% 3,34% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 23,71% Приклад № 27 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 55,70 N/A N/A Маніт 73,00 13,55 N/A N/A Мікронізований кросповідон 59,80 11,10 + ГПМЦ (2910 3сп) 18,00 3,34 КМЦ Na Мікрокристалічна целюлоза (Тип 102) Гліцерилбегенат 27,00 5,01 + 50,00 9,28 + 10,80 2,01 N/A N/A Вся таблетка 538,60 100,00 25,40% 3,34% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 28,74% 25 UA 110117 C2 Приклад № 28 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водо-розчинний API 300,00 50,88 N/A N/A Маніт 73,00 12,38 N/A N/A Мікронізований кросповідон 59,80 10,14 + ГПМЦ (2910 3сп) 18,00 3,05 КМЦ Na Мікрокристалічна целюлоза (Тип 102) Гліцерилбегенат 27,00 4,58 + 100,00 16,96 + 11,80 2,00 N/A N/A Вся таблетка 589,60 100,00 31,68% 3,05% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 34,74% Приклад № 29 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 52,63 N/A N/A Маніт 73,00 12,81 N/A N/A Мікронізований кросповідон 60,00 10,53 + ГПМЦ (2910 3сп) 18,00 3,16 КМЦ Na Мікрокристалічна целюлоза (Тип 102) Гліцерилбегенат 27,00 4,74 + 75,00 13,16 + 17,00 2,98 N/A N/A Вся таблетка 570,00 100,00 28,42% 3,16% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 31,58% 26 UA 110117 C2 Приклад № 30 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 50,34 N/A N/A Маніт 73,00 12,25 N/A N/A Мікронізований кросповідон 60,00 10,07 + ГПМЦ (2910 3сп) 18,00 3,02 КМЦ Na Мікрокристалічна целюлоза (Тип 102) Гліцерилбегенат 27,00 4,53 + 100,00 16,78 + 18,00 3,02 N/A N/A Вся таблетка 596,00 100,00 31,38% 3,02% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 34,40% Приклад № 31 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 55,66 N/A N/A Маніт 94,60 17,55 N/A N/A Мікронізований кросповідон 60,00 11,13 + ГПМЦ (2910 3сп) 18,00 3,34 КМЦ Na Мікрокристалічна целюлоза (Тип 102) Гліцерилбегенат 5,40 1,00 + 50,00 9,28 + 11,00 2,04 N/A N/A Вся таблетка 539,00 100,00 21,41% 3,34% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 24,75% 27 UA 110117 C2 Приклад № 32 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 55,66 N/A N/A Маніт 83,80 15,55 N/A N/A Мікронізований кросповідон 60,00 11,13 + ГПМЦ (2910 3сп) 18,00 3,34 КМЦ Na Мікрокристалічна целюлоза (Тип 102) Гліцерилбегенат 16,20 3,01 + 50,00 9,28 + 11,00 2,04 N/A N/A Вся таблетка 539,00 100,00 23,42% 3,34% Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 26,76% Приклад № 33 5 Маса/ одиниця Кількість/ одиниця [мг] [%] Нерозчинний у воді Водорозчинний API 300,00 55,66 N/A N/A Маніт 100,00 18,55 N/A N/A Мікронізований кросповідон 59,20 10,98 + ГПМЦ (2910 6сп) 18,00 3,34 Низькозаміщена ГПЦ 50,00 9,28 + Гліцерилбегенат 11,20 2,08 N/A N/A Вся таблетка 539,00 100,00 20,26 3,34 Інгредієнт Кількість гігроскопічних полімерів Загальна кількість гігроскопічних полімерів гігроскопічний полімер + 23,60 28
ДивитисяДодаткова інформація
Назва патенту англійськоюComposition comprising s-[2-([[1-(2-ethylbutyl)-cyclohexyl]-carbonyl]amino)phenyl]2-methylpropanethioate and croscarmellose sodium
Автори англійськоюKrabichler, Michaela, Meyer, Bernard, Winzenburg, Carsten
Назва патенту російськоюКомпозиция, содержащая s-[2-([[1-(2-этилбутил)-циклогексил]-карбонил]амино)фенил]2-метилпропантиоат и кроскармелозу натрия
Автори російськоюКрабихлер Михаела, Мейер Бернар, Винценбург Карстен
МПК / Мітки
МПК: A61K 9/20, A61P 9/00, A61K 31/265
Мітки: кроскармелозу, натрію, s-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоат, композиція, містить
Код посилання
<a href="https://ua.patents.su/38-110117-kompoziciya-shho-mistit-s-2-1-2-etilbutil-ciklogeksil-karbonilaminofenil2-metilpropantioat-i-kroskarmelozu-natriyu.html" target="_blank" rel="follow" title="База патентів України">Композиція, що містить s-[2-([[1-(2-етилбутил)-циклогексил]-карбоніл]аміно)феніл]2-метилпропантіоат і кроскармелозу натрію</a>
Попередній патент: Спосіб дифузійного борохромування сталевих виробів
Наступний патент: Мікобактеріальна антигенна композиція
Випадковий патент: Спосіб визначення ступеня максимального радіонуклідного забруднення іхтіофауни прісноводних водойм