Спосіб контролю азотвмісних шкідливих домішок
Номер патенту: 18718
Опубліковано: 25.12.1997
Автори: Тєрєщєнко Маргаріта Івановна, Савушкін Ігорь Алєксандровіч, Жігунова Ларіса Ніколаєвна, Хоровєц Грігорій Анатольєвіч, Сорокін Владімір Ніколаєвіч
Формула / Реферат
Способ контроля азотсодержащих вредных примесей, заключающийся в том, что готовят пробу, пропускают ее через мембрану, определяют часть азотсодержащих соединений, проводят математическую обработку результатов для расчета всех остальных азотсодержащих соединений, отличающийся тем, что предварительно измеряют дозу облучения, полученную пробой, затем пробу пропускают через гидрофильную целлофановую мембрану до полного отделения анализируемых веществ, определяют концентрацию нитрит- и нитрат-ионов, а по содержанию нитрит-ионов и полученной дозе определяют концентрацию диметилнитрозоамина по формуле
где k - концентрация нитрит-ионов в моль/л;
χ - доза облучения, р;
у - концентрация диметилнитрозоамина в моль/л.
Текст
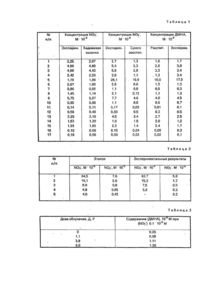
Изобретение относится к аналитической химии и может быть использовано для раздельного непрерывного контроля азотсодержащих вредных примесей - нитрит-нитрат-ионов, нитрозосоединений в биомассе в режиме автоматического определения. Известно, что к одним из основных, постоянно увеличивающихся примесей в окружающей среде относятся нитраты, нитриты, нитрозосоединения, определяемые методами: гравиметрическим, ионообменным, отгонки в виде аммония, микродиффузии, экстракции с помощью тетрафениларсенийхлорида, газометрическим, спектроскопическим, электрохимическим, хроматографическим [1]. Однако, существующие методы анализа азотсодержащих вредных примесей длительны, трудоемки, плохо воспроизводимы и имеют низкую достоверность результатов. Известен способ автоматического спек-трофотометрического обнаружения нитратов в микрограммовых количествах [2]. Способ основан на восстановлении нитрата до аммиака с помощью сплава Деварда в щелочной среде, который подают в адсорбирующий аппарат из стекла для отделения аммиака, в форме которого спектрофотометрически в автоматическом режиме определяется нитрат. Недостатком способа является то, что на практике трудно учесть мешающее влияние ионов NH4+ и NO2- и других азотсодержащих органических вредных примесей; влияющих на результаты анализа, а также плохая воспроизводимость результатов, которые в значительной мере зависят от того, насколько выдерживаются условия реакции, т.е. температура, время восстановления, рН. Кроме того, при анализе биомассы метод является прерывным, так как подготовка каждой пробы производится отдельно. Наиболее близким по технической сущности является способ непрерывного одновременного контроля аммиака и нитрата в воде [3]. Способ включает операции: подготовка пробы, отделение азотсодержащих веществ пропусканием через мембрану, идентификацию азотсодержащих веществ с математической обработкой. Подготовка пробы заключается в восстановлении нитрата до аммиака титаном (III). Аммиак отделяют с помощью микропористой .трубча той мембраны из политетрафторэтилена, после чего идентифицирует аммиак и нитрат в воде флуорометрически с математической обработкой. Недостатком способа является плохая воспроизводимость, а значит, и достоверность анализа, зависящие от условий реакции восстановления и мешающего влияния азотсодержащих органических примесей. Цель изобретения - повышение точности и экспрессности определения нитрат-нитрит-ионов и диметилнитрозоамина (ДМНА) в биомассе за счет удаления мешающих примесей. Поставленная цель достигается тем, что предварительно проводят дозиметрию пробы, затем пробу пропускают через гидрофильную целлофановую мембрану до полного отделения анализируемых веществ. Далее осуществляют раздельную идентификацию нитрат-нитрит-ионов, а по содержанию нитрит-ионов и полученной дозе определяют ДМН А по формуле у = к · f(x), где k - концентрация нитрит-ионов в моль/л; x - доза облучения, Р: у - концентрация диметилнитрозоамина в моль/л. Примеры выполнения способа. Образцы биомассы (морковь, сок, кровь, тушка), а также эталонные образцы (стандарт), содержащие нитрит-ионы (NO2-), нитрат-ионы (NO3-) и диметилнитрозоамин (ДМНА) в количестве от 0,02 до 4 кг, после подготовки пробы, включающей дозиметрию для всех образцов, а также для твердых образцов - резку, гомогенизацию и кислотную экстракцию в 0,1 Η ΗСІ, для жидких - центрифугирование - пропускали через гидрофильную целлофановую мембрану. Целлофановую мембрану предварительно термообрабатывали при 60°С в реакторе, содержащем низкомолекулярные пептиды в течение 1,5 часа. При этом мембрана приобретает гидрофильные свойства, позволяющие не пропускать мешающие примеси для определения азотсодержащих ве ществ, оставаясь "открытой" для анализируемых ионов. Полноту определения контролировали до отрицательной реакции на NО2-. После мембраны раствор анализировался на спектрофотометре СФ-18 на качественное и количественное содержание NО2- и NО2--ионов по методике (Методические рекомендации по определению нитратов и нитритов, утвержденной МЗ БССР "Организации и методика санитарного контроля за содержанием нитратов в пищевых продуктах в условия х БССР. Минск, 1986). Причем, осуществлялась раздельная идентификация по каждому иону, и по кривым - содержание ДМН А в зависимости от N02-noHa рассчитывалось количество ДМН А, поскольку многочисленные экспериментальные зависимости (ДМНА) от (NO2) показывают корреляцию независимо от характера биомассы. Полученные результаты приведены в табл.1-3. В табл.1 в графе № 1 представлены пробы биомассы: 1-5 - морковь, 6-9 - кровь, 10-17 - тушка. В графе 2 приведены концентрации N03 -иона, полученные способом согласно изобретению: в графе 3 концентрации NО2-. полученные независимым методом с помощью кадмиевой колонки (Всесоюзный симпозиум - канцерогенные нитрозосоединения и их предшественники". Таллин, 1984). В графе 4 приведены концентрации NО2-, полученные способом по изобретению; в графе 5 концентрации NО2-, полученные по методике (Методические рекомендации по определению нитратов и нитритов, утвержденной МЗ БССР "Организация и методика санитарного контроля за содержанием нитратов в пищевых продуктах в условиях БССР (рекомендации). Минск, 19.86). В графе 6 приведены концентрации ДМНА, рассчитанные способом согласно изобретению; в графе 7 данные по ДМНА, подтвержденные независимым методом с термоэнергетическим анализатором в качестве детектора (Содержание канцерогенных нитрозоаминов в пищевых продуктах Молдавской ССР. - Гигиена и санитария, 4, 1988), которые согласуются с получениями по формуле. В табл.2 приведены данные, полученные предложенным способом. В табл.3 приведена зависимость концентраций ДМНА в крови от полученной дозы при концентрации NО20,1*10-6м. Такие же зависимости существуют и для други х биообразцов (тушка, морковь, сок). Многочисленные опыты показывают, что в биомассе имеется корреляция между количественным содержанием NО3- , NО2--ионами и ДМНА. Подобная корреляция, естественно, количественно другая, между количественным содержанием этих ионов и ДМНА существует и после получения биомассы. Каждой дозе облучения соответствуе т свой коэффициент. Обработка экспериментальных данных позволила получить аналитическую зависимость корреляционных коэффициентов между NО3-, NО 2--ионами и ДМНА в диапазоне доз облучения от 0 до 53,2 рентген при содержании NО2--ионами 0,1*10-6м. Математическая обработка результатов состоит в усреднении количественного содержания NО2--иона, нахождении корреляционного коэффициента, соответствующего данным дозе облучения и значению усредненного количественного содержания NО2-·-иона и определении (расчете) содержания ДМНА по этим величинам. Алгоритмы построения интерполяционной кривой. Для получения математической зависимости концентрации ДМНА от дозы облучения и концентрации иона NО2- использовался следующий алгоритм:интерполировалась зависимость концентрации ДМНА от дозы облучения при фиксированной концентрации иона NО2- из середины рабочего диапазона. Интерполяция производилась формулами нормального (Гауссова) статистического распределения методом вычитания с последующим сведением остатка к линейной зависимости. С помощью построенной таким образом функции находилась линейная зависимость концентрации ДМНА от концентрации NО2 где у - концентрация ДМНА, моль/л; К - концентрация NО2-, моль/л; X - доза облучения, Р. Таким образом, данный способ повышает качество контроля NО2-, NО3--ионов, канцерогенного ДМНА за счет следующего: - повышения воспроизводимости и достоверности анализа; - селективности раздельного измерения по каждому из азотсодержащих соединений: нитридов, нитратов, ДМН А. Способ дает возможность автоматизировать процесс контроля нитрит-, нитрат-ионов и ДМНА в биомассе (растворы, кровь, растения, ткани животных и т.д.). Способ позволяет, не проводя чрезвычайно трудоемкую работу по выделению канцерогенного ДМНА, рассчитать его количество, исходя из данных по содержанию нитрита, что сокращает время контроля за канцерогенами на сутки.
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for control of nitrogen-containing harmful admixtures
Назва патенту російськоюСпособ контроля азотосодержащих вредных примесей
МПК / Мітки
МПК: G01N 33/48, G01N 33/02, G01N 21/79
Мітки: спосіб, контролю, азотвмісних, шкідливих, домішок
Код посилання
<a href="https://ua.patents.su/4-18718-sposib-kontrolyu-azotvmisnikh-shkidlivikh-domishok.html" target="_blank" rel="follow" title="База патентів України">Спосіб контролю азотвмісних шкідливих домішок</a>
Попередній патент: Контейнер для запліднення яйцеклітин
Наступний патент: Спосіб очищення виробів
Випадковий патент: Спосіб лікування залізодефіцитної анемії вагітних