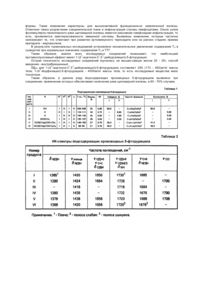
Йодвмісні похідні 5-фторурацилу, що проявляють протипухлинну дію
Номер патенту: 21615
Опубліковано: 06.01.1998
Автори: Комарова Ірина Володимирівна, Натаров Валерій Володимирович, Скачек Ірина Борисівна, Сомова Олена Віталіівна, Кустова Світлана Петрівна, Божко Тетяна Степанівна, Яременко Федір Георгійович, Петрук Василь Іванович, Ром-Бугославська Олена Семенівна
Формула / Реферат
Йодсодержащие производные 5-фторурацила, проявляющие противоопухолевое действие общей формулы
СО – (
ОR
R
где R - Н, ОН, ОСОСН3, ОСО(СН2)2СООСН2, ОСО(СН2)2СООС2Н5,
R1, R2, R3 - водород или йод, п – 0 или 1.
Текст
Изобретение относится к новому классу биологически активных веществ, а именно, к йодсодержащим производным 5-фторурацила, проявляющим противоопухолевое действие при неоперабельных формах рака щитовидной железы. В литературе описаны комплексы переходных металлов с салициловой кислотой, их сольваты, смеси, применение которых приводит к снижению скорости роста опухоли, увеличению выживаемости, снижению метастазирования опухоли [1]. Однако в литературе нет данных о том, что такого рода соединения использовались в терапии рака щитовидной железы. Известен препарат дийодбензотеф (N-2,5-дийодбензоил-NI,NI,NII,NII-диэтилентриамид фосфорной кислоты), применяемый при раке щитовидной железы [2]. При этом отмечается сильное токсическое действие данного препарата на структурный состав крови. Базовым объектом и прототипом заявляемым соединениям является препарат 5-фторурацил, нашедший применение при лечении опухолей щитовидной железы, формулы: Однако 5-фторурацил вызывает лишь незначительное угнетение роста опухолевых процессов в щитовидной железе [3]. Задачей изобретения является поиск новых соединений, обладающих противоопухолевым действием при неоперабельных формах рака щитовидной железы, мало токсичных и более эффективных по сравнению с имеющимися в арсенале. Для решения указанной задачи предлагается новый ряд химических соединений - йодсодержащие производные 5-фторурацила общей формулы: где R = H, OH, OCOCH3, OCO(CH2)2COOCH3, OCO(CH2)2COOC2H5; R1 и R2 и R3 = H или 1; n = 0 или 1, проявляющие противоопухолевое действие. В ряду исследуемых соединений отмечают излечение рака щитовидной железы в 60 - 70% случаев по сравнению с 30% случаев при лечении 5-фторурацилом. Наиболее высокую противоопухолевую активность при лечении рака щитовидной железы отмечают у 1-(21-ацетокси-31,51-дийодсалицил)-5фторурацила, на втором месте - 1-(21-карбэтоксипропионил-31,51-дийодсалицил)-5-фторурацил, на третьем - 1-(41-йодфенацил)-5-фторурацил. Предлагаемые соединения мало токсичные и относятся к IV классу безопасности, по сравнению с 5фторурацилом, ЛД50 которого составляет 52,1мг/кг массы тела мышей при внутрибрюшинном введении. Указанные соединения получают при взаимодействии мононатриевой соли 5-фторурацила или 2,4бис(триметилсилил)-5-фторурацила с хлорангидридами производных йодбензойных кислот или с 4-йод-21бромацетофеноном в среде ацетонитрила. Состав и структура синтезированных соединений подтверждены данными элементного анализа, ИК, ПМР и масс-спектроскопией, а индивидуальность - методом ТСХ в системе чистого хлороформа (см. табл.1, 2). Пример1. Мононатриевая соль 5-фторурацила. К горячему раствору 9г едкого натра (0,4 моля) в 200мл воды прибавляют 30г (0,2 моля) 5фторурацила. Реакционную массу оставляют при комнатной температуре в течение суток, затем растворитель упаривают до 1/10 объема, при охлаждении выпадает белый кристаллический осадок. Получено 22г (60% теор.) мононатриевой соли 5-фторуратцила (п/к из 2-пропанола). Найдено, %: F - 13,1. C4H2O2N2FNa. Вычислено, %: F - 12,5. Пример 2. 2,4-Бис(триметилсилил)-5-фторурацил. Нагревают 9г 5-фторурацила (0,07 моля) в смеси 20мл гексаметилдисилазана и 2мл триметилхлорсилана при температуре 140 - 160°C на протяжении 6 часов. Затем избыток силильных агентов упаривают, остаток смешивают с 60мл сухого ацетонитрила. Раствор ацетонитрила содержит 66 молей 2,4-бис(триметилсилил)-5-фторурацила. Пример 3. 3,5-Дийодсалициловая кислота. К суспензии 23г салициловой кислоты (0,16 молей) в 0,8л дистиллированной воды при перемешивании прибавляют 290г (1,8 молей) водного раствора йодхлорида, после чего перемешивание продолжают в течение 15 минут и оставляют массу стоять при комнатной температуре в течение суток. К реакционной массе прибавляют раствор 60г (0,6 молей) натрия гипосульфита в 100мл воды (проба на присутствие свободного йода) до получения массы прозрачного цвета. Затем прибавляют 25% раствор аммиачной воды до pH 5, смесь охлаждают, образовавшийся осадок фильтруют, промывают водой, сушат, получают 37г 3,5-дийодсалициловой кислоты с т.пл. 228 - 230°C. Найдено, %: I - 61,9. C7H4I 2O3. Вычислено, %: I - 64,8. Rf ~ 0,65. Пример 4. 2-Карбметоксипропионил-3,5-дийодсалициловая кислота. К суспензии 8г (0,02 моля) 3,5-дийодсалициловой кислоты в 50мл пиридина при охлаждении массы до температуры (-10 ± 2)°C и при перемешивании порциями прибавляют 5г (0,03 моля) хлорангидрида монометилового эфира янтарной кислоты. Реакционную смесь перемешивают в течение двух часов. Затем массу вливают в раствор серной кислоты (35мл концентрированной серной кислоты и 500мл воды). Выпавшее масло отделяют экстракцией хлороформом. Хлороформные экстракты промывают водой до pH ~ 7, сушат над безводным натрия сульфатом, фильтруют, растворитель полностью упаривают. Остаток кристаллизуют из гексана, получают 9,5г продукта с т.пл. 52 - 54°C. Найдено, %: I - 46,5. C12H10I 2O6. Вычислено, %: I - 50,4, Rf ~ 0,62. Пример 5. 2-Карбэтоксипропионил-3,5-дийодсалициловая кислота. Аналогично синтезу 2-карбметоксипропионил-3,5-дийодсалициловой кислоты, из 6г (0,02 молей) 3,5дийодсалициловой кислоты в 50мл пиридина и 3,5г (0,02 молей) хлорангидрида моноэтилового эфира янтарной кислоты получено 7,5г продукта с т.пл. 50 - 52°C. Найдено, %: I - 42,0. C13H12I 2O6. Вычислено, %: I - 50,4. Rf ~ 0,66. Пример 6. 2-Ацетокси-3,5-дийодсалициловая кислота. Смесь 15г (0,04 моля) 3,5-дийодсалициловой кислоты, 25мл уксусного ангидрида (0,3 моля) и 1 - 2 капли серной кислоты кипятят в течение 30 минут. Горячую массу фильтруют от механических примесей, фильтрат оставляют при комнатной температуре в течение 12 часов. Выпавший осадок отфильтровывают, промывают спиртом, фильтрат вливают в ледяную воду, выпавший при этом осадок фильтруют, промывают спиртом, сушат. Получают 12,5г продукта с т.пл. 158 - 160°C. Найдено, %: I - 58,8; C8H6I 2O4. Вычислено, %: I - 60,4. Rf ~ 0,46. Пример 7. 4-Йод-21-бромацетофенон. 24,2г (0,07 моля) 21-ацетофенона растворяют в 60мл уксусной кислоты при температуре 60°C, далее порциями прибавляют 15,7г (5,04мл) (0,2 моля) брома. После прибавления 3/4 количества брома образуется осадок, массу перемешивают и оставляют в течение 0,5 часа. После охлаждения реакционной массы осадок фильтруют, промывают спиртом, сушат. Получено 26,4г продукта с т.пл. 114 - 115°C. C8H6IOBr. Rf ~ 0,85. Пример 8. Хлорангидриды йодбензойных кислот. Смесь 0,1 моля производного йодбензойной кислоты и 0,12 моля тионилхлорида в 0,5 молях абсолютного хлороформа оставляют при комнатной температуре в течение суток. Затем на водяной бане упаривают растворитель и избыток тионилхлорида. Маслянистую массу кристаллизуют из гексана, получают кристаллический продукт. Т.пл. для хлорангидридов йодбензойных кислот в °C составляют: 3,5-дийодсалициловой кислоты - 67 86; м-йодбензойной - 92 - 93; 2-ацетокси-3,5-дийодсалициловой кислоты - 101 - 102; 2карбметоксипропионил-3,5-дийодсалициловой кислоты - 64 - 65; 2-карбэтоксипропионил-3,5дийодсалициловой кислоты - 66 - 67. Пример 9. 1-(31, 51-дийодсалицил)-5-фторурацил. Смесь 2г (0,01 моля) мононатриевой соли 5-фторурацила, 6г (0,01 моля) хлорангидрида 3,5дийодсалициловой кислоты в 80мл абсолютного диметилформамида кипятят на масляной бане при температуре 130°C в течение 5 часов. Горячую массу фильтруют от механических примесей. После охлаждения реакционную смесь вливают в раствор соленой воды, образуется осадок, который отфильтровывают, промывают водой, сушат. Получают 2,6г продукта 1 (R - OH, R1 = R3-I, R2 - H, n = 0). Аналогичным способом были получены 1-(21-карбметоксипропионил-31,51-дийодсалицил)-5фторурацил (продукт V, где R - OCO(CH2)2COOCH3, R1 = R3-I, R2 - H, n = 0) и 1-(21-карбэтоксипропионил31,51-дийодсалицил)-5-фторурацил (продукт VI, где R - OCO(CH2)2COOC2H5, R1 = R3-I, R2 = H, n = 0). Пример 10. 1-(31-йодбензоил)-5-фторурацил. К раствору 4г (0,015 молей) хлорангидрида 3-йодбензойной кислоты в 20мл абсолютного ацетонитрила прибавляют 13мл (0,022 молей) раствора 2,4-бис(триметилсилил)-5-фторурацила в ацетонитриле. Реакционную смесь оставляют при комнатной температуре в течение суток, затем массу вливают в 100мл воды, образующуюся маслянистую массу кристаллизуют из абсолютного ацетонитрила, получают 3г продукта III, где R = R2 = R3 - H, R1 - I, n = 0. Аналогичным способом были получены 1-(41-йодфенацил)5-фторурацил (продукт II, где R = R1 = R3 = H, R2 = I, n = 1) и 1-(21-ацетокси-31,51-дийодсалицил)-5-фторурацил (продукт IV, где R = OCOCH3, R1 = R3-I, R2 - H, n = 0). Изучение биологической активности некоторых представителей класса йодсодержащих производных 5-фторурацила, а именно, 1-(21-ацетокси-31,51-дийодсалицил)-5-фторурацил, 1-(21-карбэтоксипропионил31,51-дийодсалицил)-5-фторурацил и 1-(41-йодфенацил)5-фторурацила, проводили на экспериментальной модели опухоли, щитовидной железы у крыс. Данную модель вызывали путем смазывания одной доли щитовидной железы крыс 5% раствором 20метилхолантрена. Образование опухоли устанавливали с помощью гистологического исследования щитовидной железы. Крысам после введения канцерогена через три месяца, семикратно, один раз в три дня порциями внутрибрюшинно вводили одно из исследуемых средств. 1-(21-Ацетокси-31,51-дийодсалицил)- и 1-(41-йодфенацил)-5-фторурацилы применяли в дозе 10мг/кг массы тела, а 1-(21-карбэтоксипропионилт-31,51-дийодсалицил)-5-фторурацил - 6мг/кг массы тела в течение месяца. В качестве растворителя был использован 2% раствор крахмала, а для 1-(41-йодфенацил)-5фторурацила - водный раствор димексида (1 : 7). Специфический противоопухолевый эффект изучаемых соединений оценивали по данным гистологии ткани щитовидной железы, взятой после забоя экспериментальных животных. Железу фиксировали в среде Карнуа, после чего срезы ткани окрашивали гематоксилин-эозином по Майеру. Морфологический анализ проводили согласно требованиям, предъявляемым к морфофункциональным исследованиям. Состояние гипофизарно-тиреоидной системы оценивали по показателям содержания Т 3, Т4 и ТТГ в сыворотке крови, уровень гормонов определяли радиоиммунологическим или иммуноферментным способом. Цифровые данные были обработаны статистически с помощью критерия Стьюдента. По данным гистологической картины модель опухоли щитовидной железы, которая вызвана введением 20-метилхолантрена, характеризуется следующими проявлениями. Наблюдаются очаги фолликулярно-папиллярного рака щитовидной железы с преобладанием средних и мелких фолликулов, заполненных достаточно густым коллоидом с большим количеством пристеночных резорбционных вакуолей. Опухолевые клетки кубической или призматической формы, крупнее, чем обычные фолликулярные клетки, с нежной, светлой, зернистой цитоплазмой, которая иногда вакуолизована, с большими гипохромными, иногда вытянутыми или овальными ядрами с хорошо очерченной оболочкой и мелкими рассеянными вкраплениями хроматина. В центрах размножения ядра тироцитов круглые, гиперхромные, часто в состоянии, митоза. Встречаются группы фолликулов неправильной формы, которые образуют кисты. Отмечается умеренное разрастание фиброзной ткани с развитием ее преимущественно по периферии железы. Приблизительно у 10% животных найдены клетки типа фибробластов, которые могут указывать на развитие фибросаркомы. Крупные с одним, двумя или гиперхромными ядрами клетки опухоли образуют беспорядочно расположенные коллагеновые пучки. Мышечная капсула такой железы утолщена, умеренно инфильтрована лимфоцитами. В строме железы отмечают жировые участки. У превалирующего количества животных при моделировании опухоли щитовидной железы выявлены признаки папиллярно-фолликулярного рака, а в от дельных случаях - саркомы. Курсовое введение 5-фторурацила крысам, которые были предварительно обработаны 20метилхолантреном, приводило к резкому уменьшению объема щитовидной железы ввиду разрушения фолликулов, отмечалась десквамация эпителиальных клеток, их разрушение, пикноз ядер, утолщение капсулы и промежуточных перегородок. По периферии железы проявлялось мощное развитие межфолликулярной соединительной ткани, на этом фоне можно увидеть группы дистрофично измененных фолликулярных клеток. У 4 крыс из 6 наблюдались небольшие островки метаплазии в виде накопления округлых клеток. Функциональная активность железы была резко снижена, при этом уменьшение секреторной активности щитовидной железы не компенсировалось ускорением периферического дейодирования Т 4, одновременно значительно (на 50%) увеличилось содержание ТТГ в сыворотке крови. После курсового введения 1-(21-ацетокси-31,51-дийодсалицил)-5-фторурацила крысам с экспериментальной опухолью признаки новообразований в щитовидной железе были выявлены только у 25% животных, однако отмечалось незначительное угнетение функциональной активности железы: фолликулярные клетки плоские, за полненные коллоидом, местами проявляется десквамация эпителия. Высокоактивных фолликулов в паренхиме не отмечалось. Междольные перегородки умеренно утолщены, по периферии железы проявляются островки склеротичности фолликулов, их эпителий плоский или деструкторизованный. Капсула железы с умеренным фиброзом. Относительная масса железы достоверно ниже, чем у крыс в контроле и у животных с экспериментальной опухолью, которые не подвергались лечению. Содержание Т 3 в сыворотке крови крыс в 2 раза ниже, чем в контроле, при незначительном уменьшении содержания Т 4, что указывает на падение секреторной активности щитовидной железы и одновременное освобождение периферического дейодирования Т4. Результаты наблюдений свидетельствуют о выраженном противоопухолевом действии 1-(21-ацетокси1 1 3 ,5 -дийодсалицил)-5-фторурацила. При проверке противоопухолевой активности 1-(21-карбэтоксипропионил-31,51-дийодсалицил)-5фторурацила выявлены признаки резкого угнетения функциональной активности железы: паренхима железы представлена крупными и средними фолликулами, которые заполнены большим количеством коллоида с редкими пристеночными резорбционными вакуолями. Тиреоидный эпителий резко уплощен, отмечается пикноз ядер. У значительного количества крыс отмечается компенсаторная гиперплазия тиреоидного эпителия в фолликулах, в центре которых проявляется шар базальных клеток с округлым гиперхромным ядром. Последние интенсивно делятся, образуя многошаровой эпителий с веретеновидными ядрами. После заполнения фолликула коллоидом клетки базального шара не обнаруживались, все клетки тиреоидного эпителия стали однотипными с круглым ядром. Островки новообразований в щитовидной железе проявились в 40% случаев в форме фолликулярно-папиллярного рака. Клетки, характерные для саркомы щитовидной железы, не обнаруживались. Значительно увеличилась масса щитовидной железы, а масса тела уменьшилась в связи с проявлением общей интоксикации, благодаря чему коэффициент отношения массы железы к массе тела в среднем увеличился с 8,4 до 12,0. Резко уменьшился уровень сывороточных Т 3 и Т4 первый с содержанием в сыворотке ТТГ, возможно благодаря механизму обратной связи увеличился на 42%. Таким образом, исследуемое вещество проявило умеренный противоопухолевый эффект. Было проверено противоопухолевое действие 1-(4-йодфенацил)-5-фторурацила. Из шести крыс, которые получали это вещество, у четырех животных при гистологическом изучении выявлены признаки рака щитовидной железы, но его общее влияние на железу отличалось от действия предыдущих производных 5-фторурацила. Почти вся паренхима представлена крупными фолликулярными клетками, их цитоплазма была светлой, слегка вакуолизованной. Ядро большое, четко очерчено, гипохромное, часто неправильной формы. Такие изменения характерны для высокоактивной функционально напряженной железы. Отмечено также розрастание соединительной ткани и инфильтрация стромы лимфоцитами. Около узлов фолликулярно-папиллярного рака щитовидной железы имеется массивная лимфоидная инфильтрация, то есть, проявляется заинтересованность иммунной системы. Выявлены изменения, которые частично напоминают те, что отмечают при развитии аутоиммунного тиреоидита или на ранних стадиях приема препарата - мерказолила. В результате гормональных исследований установлено незначительное увеличение содержания Т 4 в сыворотке при нормальных значениях содержания Т 3 и ТТГ. Таким образом, анализ всех исследуемых соединений показывает, что наибольший противоопухолевый эффект имеет 1-(21-ацетокси-31,51-дийодсалицил)-5-фторурацил. Острая токсичность исследуемых соединений изучалась на мышах-самцах весом 20 - 25г, способ введения - внутрибрюшинный. ЛД50 для 1-(21-ацетокси-31,51-дийодсалицил)-5-фторурацила составляет 295 (173 - 462)мг/кг массы тела; 1-(41-йодфенацил)-5-фторурацила - 4000мг/кг массы тела, то есть исследуемые вещества мало токсичные. Таким образом, в данном ряду йодсодержащих производных 5-фторурацила выявлено три соединения, применение которых обеспечивает излечение рака щитовидной железы, в 60 - 70% случаев.
ДивитисяДодаткова інформація
Автори англійськоюNatarov Valerii Volodymyrovych, Kustova Svitlana Petrivna, Skachek Iryna Borysivna, Yaremenko Fedir Heorhiiovych, Komarova Iryna Volodymyrivna, Petruk Vasyl Ivanovych, Bozhko Tetiana Stepanivna
Автори російськоюНатаров Валерий Владимирович, Кустова Светлана Петровна, Скачек Ирина Борисовна, Яременко Федор Георгиевич, Комарова Ирина Владимировна, Петрук Василий Иванович, Божко Татьяна Степановна
МПК / Мітки
МПК: A61K 31/625, A61P 35/00, C07D 239/553
Мітки: йодвмісні, протипухлинну, 5-фторурацилу, проявляють, дію, похідні
Код посилання
<a href="https://ua.patents.su/4-21615-jjodvmisni-pokhidni-5-ftoruracilu-shho-proyavlyayut-protipukhlinnu-diyu.html" target="_blank" rel="follow" title="База патентів України">Йодвмісні похідні 5-фторурацилу, що проявляють протипухлинну дію</a>
Попередній патент: Аварійна автоматика
Наступний патент: Спосіб лікування переломів нижньої щелепи і пристрій для його здійснення
Випадковий патент: Гербіцидна композиція для захисту посівів зернових колосових від злакових та дводольних бур'янів