Фармацевтично стійкий препарат оксалату платини для парентерального застосування
Формула / Реферат
1. Фармацевтически устойчивый препарат оксалата платины для парентерального применения, отличающийся тем, что включает раствор оксалата платины в воде при концентрации от 1 до 5 мг/мл и рН от 4,5 до 6,0, в котором после хранения в течение фармацевтического допустимого срока содержание оксалата платины равно по крайней мере 95 % от начального содержания и раствор сохраняется чистым, бесцветным и свободным от осадка.
2. Препарат по п.1, отличающийся тем, что концентрация оксалата платины равна около 2 мг/мл воды и рН раствора имеет среднее значение около 5,3.
3. Препарат по п. 1 или по п. 2, отличающийся тем, что раствор оксалата платины имеет удельное вращение в диапазоне от + 74,5° до + 78,0°.
4. Препарат по одному из пп. 1-3, отличающийся тем, что является водным раствором оксалата платины, готовым для использования и содержащемся в герметично закрытом контейнере.
5. Препарат по п. 4, отличающийся тем, что упомянутый контейнер содержит единицу активной дозы от 50 до 100 мг оксалата платины, которая может быть использована путем вливания.
6. Препарат по п. 4 или п. 5, отличающийся тем, что упомянутым контейнером является стеклянный пузырек для фармацевтического применения, закрытый пробкой, по крайней мере часть поверхности которого, распространяющаяся внутрь пузырька, является инертной относительно упомянутого раствора.
7. Препарат по п. 6, отличающийся тем, что пространство между упомянутым раствором и упомянутой пробкой заполнено инертным газом.
8. Препарат по п. 4 или по п. 5, отличающийся тем, что упомянутым контейнером является эластичный мешочек для вливания или ампула.
9. Препарат по п. 4 или п. 5, отличающийся тем, что упомянутый контейнер является составным элементом устройства для вливания, имеющего инъекционный микронасос.
Текст
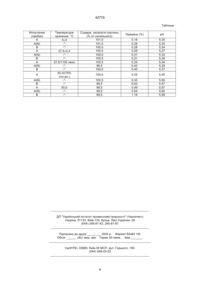
1. Фармацевтически устойчивый препарат оксалата платины для парентерального применения, отличающийся тем, что включает раствор оксалата платины в воде при концентрации от 1 до 5 мг/мл и рН от 4,5 до 6,0, в котором после хранения в течение фармацевтического допустимого срока содержание оксалата платины равно по крайней мере 95% от начального содержания и раствор сохраняется чистым, бесцветным и свободным от осадка. 2. Препарат по п. 1, отличающийся тем, что концентрация оксалата платины равна около 2 мг/мл воды и рН раствора имеет среднее значение около 5,3. C2 (54) ФАРМАЦЕВТИЧНО СТІЙКИЙ ПРЕПАРАТ ОКСАЛАТУ ПЛАТИНИ ДЛЯ ПАРЕНТЕРАЛЬНОГО ЗАСТОСУВАННЯ 42779 злокачественная гепатома, рак уротелии, рак простаты, и т.д., и более широко, другие типы твердых опухолей. В настоящее время для доклинических и клинических испытаний оксалат платины доступен в пузырьках в виде лиофилизата, который реструктурируют непосредственно перед введением водой для инъекций или изотоническим 5% раствором глюкозы, и разбавляют 5% раствором глюкозы; введение производится посредством вливания, внутривенно. Однако, такая форма дозировки требует использования производственного процесса (лиофилизации), который является относительно сложным и дорогостоящим, также как этап реструктурирования при применении, требующий навыка и осторожности. Кроме того, на практике доказано, что такой способ несет риск совершить ошибку при реструктурировании раствора; действительно, для реструктурирования фармацевтических препаратов для инъекций из лиофилизата или для разбавления жидких препаратов общепринято использовать 0,9% раствор NaCI; ошибочное использование такого раствора в случае оксалата платины в лиофилизированном виде было бы весьма вредно для активного копмонента, т.к. приводит к образованию осадка (производная дихлоро-даш-платины) с NaCI и вызывает быстый распад указанного препарата. Таким образом, во избежание риска неправильного применения препарата и для обеспечения доступности для практикующего врача или медицинской сестре препарата оксалата платины, который может быть использован без выполнения вышеупомянутых действий, были проведены исследования с целью получения раствора оксалата платины для инъекций, который был бы готов для использования и, кроме того, оставался бы фармацевтически устойчивым при хранении в течение допустимой продолжительности времени согласно признанным стандартам, был более простым и менее дорогим в производстве, чем лиофилизат, и в то же время обладал химической чистотой (отсутствием изомеризации) и терапевтической активностью, эквивалентной активности реструктурированного лиофилизата. Это и является задачей настоящего изобретения. Изобретатели показали, что эта цель может быть достигнута удивительным и неожиданным способом при использовании для введения парентеральным способом в качестве лекарственной формы водного раствора оксалата платины, в котором концентрация активного компонента и рН находятся в пределах определенных соответствующих диапазонов и в котором активный компонент свободен от какого-либо кислотного или щелочного агента, буфера или других добавок. Было обнаружено, в частности, что водные растворы оксалата платины недостаточно устойчивы, если они имеют концентрацию, меньшую чем около 1 мг/мл. Соответственно, предметом настоящего изобретения является фармацевтически устойчивый препарат оксалата платины для парентерального применения, в котором оксалат платины растворен в воде при концентрации в диапазоне от 1 до 5 мг/мл и рН в диапазоне от 4,5 до 6,0, при этом содержание оксалата платины в препарате остается равным по крайней мере 95% от начального содержания и раствор остается прозрачным, бесцветным и свободным от какого-либо осадка при хранении в течение фармацевтически допустимого времени. Этот препарат свободен от любых других компонентов и, в принципе, не должен содержать больше, чем около 2% примесей. Предпочтительно, чтобы концентрация оксалата платины в воде была равна около 2 мг/мл, а кислотность (рН) раствора имела среднее значение около 5,3. Устойчивость водного раствора оксалата платины также была подтверждена путем измерения удельного вращения, который лежит в диапазоне от +74,5° до +78,0°. Таким образом, термин "фармацевтически устойчивый" необходимо также понимать как стабильность удельного вращения оксалата платины, а именно оптической чистоты раствора (нет изомеризации). Далее, "фармацевтически допустимая продолжительность", в течение которой препарат согласно изобретению должен остаться устойчивым, необходимо здесь понимать как соответствующую продолжительностям, требуемым обычно в этой области, т.е. например, в течение 3-5 лет при комнатной температуре или при охлаждении. Получение препарата согласно изобретению может быть осуществлено предпочтительно путем растворения оксалата платины в пригодной для инъекций воде при контролируемом перемешивании, если требуется, и при предварительном нагревании приблизительно до 40°С, последующей фильтрации для получения прозрачного раствора и одной или несколькими фильтрациями для получения стерильного раствора. После заполнения и закрытия первичных сосудов препарат может быть затем стерилизован посредством нагревания в автоклаве. Предпочтительно, препарат согласно изобретению имеет вид водного раствора оксалата платины, который готов к использованию и помещен в герметически закрытый сосуд. В частном варианте изобретения, препарат согласно изобретению расфасован как единица активной дозы, предназначенной для введения посредством вливания и содержащей 50 или 100 мл оксалата платины в подобранном для желательной концентрации количестве воды для инъекций. Эту дозу целесообразно поместить в пузырек, изготовленный из нейтрального стекла для фармацевтического применения, закрытом пробкой, поверхность которой, по крайней мере простирающаяся внутрь пузырька, нейтральна относительно водного раствора оксалата платины, а пространство между указанным раствором и указанной пробкой, если желательно, заполнено инертным газом. Герметически закрытый пузырек может также быть, например, эластичным мешочком для вливания, ампулой или быть, кроме того, составным элементом устройства для вливания, имеющего инъекционный микронасос. Водный раствор оксалата платины можно вводить внутривенно обычным путем, а если тре 2 42779 буется - одновременно с другими веществами, терапевтически активными или неактивными, при их физико-химической совместимостью с платиновой производной и в соответствии с практикой, принятой в лечении рака. Оксалат платины может быть предписан в дозах в пределах от 50 до 200 мг/м2 поверхности тела, предпочтительно от 100 до 130 мг/м2 на каждое назначение, продолжительность применения в пределах приблизительно от 2 до 5 часов, обычно курс применения назначают с промежутком от 3 до 5 недель и полное лечение включает в себя от 6 до 10 курсов. Изобретение описано ниже более подробно со ссылками на следующие примеры относительно препаратов для инъекций по изобретению, их изготовления и стабильности во времени. Пример 1. Получение водного раствора оксалата платины Термостатируемый контейнер, изготовленный из стекла или устойчивой к коррозии стали, заполнили приблизительно на 80% необходимым количеством воды для инъекций и эту воду нагрели до 40±5°С при перемешивании (800-1200 оборотов/минуту). Количество оксалата платины, необходимого для получения концентрации, например, 2 мг/мл, отдельно взвесили и добавили к нагретой воде. Емкость для взвешивания трижды ополоснули водой для инъекций, которую также добавили к основной смеси. Последнюю затем размешивали при указанной температуре в течение 30±5 минут или более, если необходимо, до полного растворения оксалата платины. По одному из вариантов для уменьшения содержания кислорода в воде через нее пробулькивали азот. Раствор затем довели до желаемого объема или веса путем добавления воды для инекций и затем гомогенизировали в течение следующих 10±2 минут (800-1200 оборотов/минуту) и, наконец, охладили приблизительно до 30°С при перемешивании. В этой стадии образцы растворов взяли для проведения обычных испытаний и проверок, и раствор подвергли стерильной фильтрации известным способом, в результате которой получили прозрачный фильтрат, и до разливки раствор хранили при 15-30°С. Предпочтительно, в качестве исходного оксалата платины использовали апирогенный продукт фармацевтического качества и оптически чистый (>99,9%), например, типа полученного по способу, запатентованному Танака КК (Tanaka КК). Пример 2. Упаковка Водный раствор оксалата платины, например в концентрации 2 мг/мл, затем залили в асептических условиях, предпочтительно в инертной атмосфере, например азота, в стерилизованные апирогенные стеклянные пузырьки, емкостью 50 мл. Для получения лучшей стабильности водного раствора оксалата платины предпочтительно использовать нейтральное стекло типа I. Что касается пробки, то можно использовать, например, пробки, изготовленные из тефлона или эластомера на основе галогенированного бутила, возможно с соответствующим покрытием, в частности из фторированного полимера (например типа "Оmniflех", который выпускается Helvoet Pharma), так, чтобы по крайней мере поверхность, простирающаяся внутрь пузырька, была инертной относительно водного раствора оксалата платины. Пространство между пробкой и водным раствором может быть заполнено, если желательно, инертным газом, например азотом. Пример 3. Испытания стабильности Испытания стабильности во времени проводились на водных растворах оксалата платины, полученных как описано выше и хранившихся в различных контейнерах с использованием двух различных пробок, а именно: Пробка А: "Оmnіflех" Пробка A(N): "Omninex", с заполнением свободного объема N2 Пробка В: "Grey Butyl", то же Испытания проводились через 13 недель при нескольких различных температурах, а именно 5+3°С (температура холодильника), 27,5+2,5°С (температура окружающей среды), 40°С (при относительной влажности 75%) и 50°С для создания искусственного ускорения явления деградации со временем; кроме того, испытание при 27,5°С было повторено в присутствии сильного источника света (1100 люкс). Использовался применяемый в практике метод анализа, а именно высокоразрешающая жидкостная храмотография (High Performance Liquid Chromagraphy - HPLC), описанная, например, в Journal of Parenteral Drag Assoc., c. 108-109, 1979. Анализ пиков храмотограмм делает возможным определить содержание и процент примесей, главной из которых была щавелевая кислота. Кроме того, при каждом испытании измерялись рН, цвет и опалесценция раствора обычными методами, описанными в фармокопее. Полученные результаты, которые сведены в таблице, показывают, что при всех экспериментальных условиях стабильность водного раствора оксалата платины по изобретению может рассматриваться как фармацевтически допустимой, если рассматривать процентное содержание сохранившегося оксалата платины и содержание примесей, которое оказалось более низким, чем допускается даже после более чем 3-х месячного хранения при 50°С. Кислотность (рН) также оставалась стабильной. Кроме того, все растворы оставались чистыми, бесцветными и свободными от осадка, видимого невооруженным глазом. Наконец, было также показано, что растворы остались оптически чистыми (никакой изомеризации), измеренное удельное вращение находилось в диапазоне от около +75,7° до около +76,2°, т.е. надежно в допустимых пределах (от +74,5° до +78,0°). Другая серия измерений для температуры окружающей среды и для температуры 40°С также подтвердила стабильность водного раствора оксалата платины в течение более 10 месяцев. 3 42779 Таблица Испытание (пробка) А A(N) В А A(N) В А A(N) В А A(N) В А A(N) В Температура хранения, °С 5±3 -''-''27,5±2,5 -''-''27,5/1100 люкс -''-''40,0/(75% отн.вл.) -''-''50,0 -''-'' Содерж. оксалата платины (% от начального) 101,0 101,0 100,0 100,0 100,0 100,5 100,5 99,5 100,0 Примеси (%) pH 0,18 0,28 0,28 0,29 0,31 0,31 0,34 0,42 0,40 5,35 5,35 5,34 5,37 5,33 5,36 5,34 5,29 5,37 100,0 0,35 5,45 100,5 99,5 99,5 99,0 99,5 0,35 0,63 0,49 0,54 1,16 5,50 5,47 5,57 5,65 5,59 __________________________________________________________ ДП "Український інститут промислової власності" (Укрпатент) Україна, 01133, Київ-133, бульв. Лесі Українки, 26 (044) 295-81-42, 295-61-97 __________________________________________________________ Підписано до друку ________ 2002 р. Формат 60х84 1/8. Обсяг ______ обл.-вид. арк. Тираж 50 прим. Зам._______ ____________________________________________________________ УкрІНТЕІ, 03680, Київ-39 МСП, вул. Горького, 180. (044) 268-25-22 ___________________________________________________________ 4
ДивитисяДодаткова інформація
Назва патенту англійськоюPharmaceutical resistant preparation of platinum oxalate for the parenteral application
Автори англійськоюIBRAHIM HOUSSAM, MAUVERNAY ROLLAND-YVES
Назва патенту російськоюФармацевтически устойчивый препарат оксалата платины для парэнтерального применения
Автори російськоюИбрагим Хуссам, Мовернай Ролланд-Ивс
МПК / Мітки
МПК: A61K 31/282
Мітки: парентерального, фармацевтично, застосування, оксалату, препарат, стійкий, платини
Код посилання
<a href="https://ua.patents.su/4-42779-farmacevtichno-stijjkijj-preparat-oksalatu-platini-dlya-parenteralnogo-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Фармацевтично стійкий препарат оксалату платини для парентерального застосування</a>
Попередній патент: Розширювач, що здатний чинити відтягувальну дію на тканини зовнішньої стінки частини анатомічного утворення людини
Наступний патент: Робочий механізм багатополюсного автоматичного вимикача низької напруги
Випадковий патент: Картоновий піддон