Спосіб одержання сорбенту для вилучення перехідних металів з розчинів
Номер патенту: 51520
Опубліковано: 26.07.2010
Автори: Трохимчук Анатолій Костянтинович, Ульберг Зоя Рудольфівна, Андріанова Олена Борисівна, Лещенко Віталій Миколайович
Формула / Реферат
1. Спосіб одержання сорбенту для вилучення іонів перехідних металів з розчинів взаємодією силікагелю і зшивального агента з наступною обробкою отриманого модифікованого силікагелю комплексоутворюючим агентом, який відрізняється тим, що як зшивальний агент використовують полігексаметиленгуанідин (ПГМГ) загальної формули:
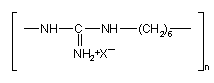 ,
,
де Х - аніон неорганічної кислоти, n = 30-90,
а як комплексоутворюючий агент застосовують динатрієву сіль етилендіамінтетраоцтової кислоти (ЕДТА).
2. Спосіб за п. 1, який відрізняється тим, що застосовують ПГМГ у формі гідрохлориду.
3. Спосіб за п. 1 або 2, який відрізняється тим, що взаємодію силікагелю з ПГМГ проводять у водному середовищі при рН = 2,0-9,0.
4. Спосіб за пп. 1 або 2, або 3, який відрізняється тим, що ПГМГ вводять у кількості 6-12 % мас.
5. Спосіб за будь-яким з пп. 1-4, який відрізняється тим, що обробку модифікованого силікагелю ЕДТА проводять у водному середовищі при рН = 2,5-7,0.
6. Спосіб за будь-яким з пп. 1-5, який відрізняється тим, що обробку модифікованого силікагелю ЕДТА проводять при масовому співвідношенні компонентів 40-80:1 відповідно.
Текст
1. Спосіб одержання сорбенту для вилучення іонів перехідних металів з розчинів взаємодією силікагелю і зшивального агента з наступною обробкою отриманого модифікованого силікагелю комплексоутворюючим агентом, який відрізняється тим, що як зшивальний агент використовують полігексаметиленгуанідин (ПГМГ) загальної формули: , Корисна модель відноситься до способів одержання сорбентів для вилучення та концентрування іонів металів, зокрема іонів перехідних металів, з розчинів і може бути застосована для вилучення (у тому числі групового) цих металів у процесах хімічного аналізу. Сорбційні методи концентрування й розділення неорганічних іонів займають одне із провідних місць у неорганічному аналізі. Вилучення іонів металів з розчинів комплексоутворюючими сорбентами на основі кремнезему - один із перспективних методів концентрування мікроелементів. Використання в якості функціональних груп різних комплексоутворюючих специфічних або групових реагентів дозволяє створювати сорбенти з заданими сорбційними характеристиками. Відомим є сорбент для вилучення Іонів перехідних металів з розчинів на основі кремнезему з функціональними комплексоутворюючими іміноді ацетатними групами, який одержують взаємодією кремнезему і зшивального агенту з наступною обробкою отриманого продукту комплексоутворюючим реагентом. При цьому як зшивальний агент використовують -хлорпропілтрихлорсилан або амінопропілтриетоксісилан (АПТМС) у кількості 8,5-17,0% мас., а як комплексоутворюючий агент імінодіоцтову кислоту у кількості 1,5-3,0% мас., проводячи обробку отриманого на перші стадії продукту імінодіоцтовою або монохлороцтовою кислотою при 20-годинному кип'ятінні зі зворотним холодильником та періодичному додаванні K2СО3 до рН=6,0-8,0. Після промивання водою та розчином сірчаної кислоти одержують сорбент, ємність якого щодо іонів міді складає 0,1-0,2мг екв/г. При застосуванні відомого сорбенту для вилучення перехідних металів час встановлення хімічної рівноваги складає 2-10хв. у широкому інтервалі концентрацій іонів (5-0,5мг/мл), а коефіцієнт роз 51520 n (13) U (CH2)6 (11) NH _ NH2+X UA С (19) NH де Х - аніон неорганічної кислоти, n=30-90, а як комплексоутворюючий агент застосовують динатрієву сіль етилендіамінтетраоцтової кислоти (ЕДТА). 2. Спосіб за п.1, який відрізняється тим, що застосовують ПГМГ у формі гідрохлориду. 3. Спосіб за п.1 або 2, який відрізняється тим, що взаємодію силікагелю з ПГМГ проводять у водному середовищі при рН=2,0-9,0. 4. Спосіб за пп.1 або 2, або 3, який відрізняється тим, що ПГМГ вводять у кількості 6-12% мас. 5. Спосіб за будь-яким з пп.1-4, який відрізняється тим, що обробку модифікованого силікагелю ЕДТА проводять у водному середовищі при рН=2,5-7,0. 6. Спосіб за будь-яким з пп.1-5, який відрізняється тим, що обробку модифікованого силікагелю ЕДТА проводять при масовому співвідношенні компонентів 40-80:1 відповідно. 3 51520 поділу між водним розчином І сорбентом, який визначали для іонів цинку (вихідна концентрація 10-2-10-5г/л), знаходиться у межах 0,551,84 105мл/г. Хоча відомий сорбент має задовільну ємність та забезпечує ефективне вилучення іонів перехідних металів з малоконцентрованих водних розчинів, синтез його є досить складним (тривалість, необхідність постійного контролю рН), потребує використання органічних розчинників (толуол), небезпечних (монохлороцтова кислота) та дорогих (АПТМС) вихідних компонентів. Завданням корисної моделі є створення нового способу одержання сорбенту для вилучення та концентрування іонів перехідних металів з розчинів, який дозволяє спростити синтез сорбенту без погіршення його якісних характеристик та підвищити екологічну безпечність процесу. Поставлене завдання виконано новим способом одержання сорбенту для вилучення перехідних металів з розчинів взаємодією силікагелю і зшивального агенту з наступною обробкою отриманого модифікованого силікагелю комплексоутворюючим агентом, в якому, згідно з корисною моделлю, як зшивальний агент використовують полігексаметиленгуанідин (ПГМГ) загальної формули: NH С NH2 NH _ (CH2)6 +X n де Х - аніон неорганічної кислоти, n = 30 90, а як комплексоутворюючий агент застосовують динатрієву сіль етилендіамінтетраоцтової кислоти (ЕДТА). У пропонованому способі можуть бути використані полігексаметиленгуанІдини, в яких аніоном є – РО43-, NO3-, Сl- та інші, однак рекомендується застосовувати полігексаметиленгуанідин у формі гідрохлориду як найбільш доступний реагент, що випускається промисловістю. Взаємодію силікагелю з ПГМГ проводять у водному середовищі при рН=2,0-9,0. ПГМГ вводять у кількості 6-12%. Обробку модифікованого силікагелю ЕДТА проводять також у водному середовищі в діапазоні рН від 2,5 до 7,0 і масове співвідношення компонентів витримують рівним 40-80:1, відповідно. Як силікагелеву основу для одержання сорбенту можна використовувати силікагелі мезопористої або широкопористої структури. Спосіб, що заявляється, забезпечує одержання нового сорбенту, який містить на поверхні силікагелю активні групи етилендіамінтетраацетату, що утворюють комплекси с іонами перехідних металів, завдяки чому досягається ефективне вилучення цих іонів з водних розчинів. При цьому як процес модифікування силікагелю полігексаметиленгуанідином, так і наступна обробка комплексоутворюючем відбуваються у водному середовищі в широкому інтервалі рН, без застосування екологічно небезпечних та дорогих реагентів, тим самим досягається значне спрощення синтезу сорбенту, здешевлення процесу та поліпшення його екології. 4 Таким чином, завдання корисної моделі виконано з досягненням необхідного технічного результату. Нижче наведені приклади здійснення способу, що заявляється, які підтверджують ефективність нового сорбенту в оптимальних умовах проведення процесу сорбції. Приклад 1. У круглодонну колбу об'ємом 1дм3 вносять 5г полігексаметиленгуанідину у формі гідрохлориду (товарний продукт "полісепт", Мм 10000), далі ПГМГх. Додають 75см3 дистильованої води і перемішують при кімнатній температурі протягом 30 хвилин до повного розчинення ПГМГх. Після цього до отриманого розчину додають 50г (10% мас) силікагелю (силікагель Silica Gel 60 фірми "Merck" фракція 0,06-0,16мм, середній діаметр пір 12нм, питома поверхня 260м2/г) і перемішують протягом 1 години. Отриманий продукт відмивають від надлишку ПГМГх дистильованою водою в апараті Сокслета протягом 24 годин і сушать під вакуумом при нагріванні до 80°С на водяній бані. 40г отриманого модифікованого силікагелю переносять у колбу об'ємом 1 дм3, додають 200см3 0,01М водного розчину ЕДТА (масове співвідношення модифікований силікагель:ЕДТА складає 60:1), додають НС1 до рН=3 і перемішують протягом 30-40 хвилин. Утворений продукт переносять на фільтр та промивають великою кількістю дистильованої води (1-2дм3) під тиском, а потім отриманий зразок сорбенту (зразок 1) висушують при температурі 80°С. Приклад 2. У круглодонну колбу об'ємом 0,5дм3 вносять 2г ПГМГх. Додають 50см3 дистильованої води і перемішують при кімнатній температурі протягом 30 хвилин до повного розчинення ПГМГх. Після цього процес взаємодії ПГМГх і 25г (8% мас) силікагелю ведуть як описано в прикладі 1. Отриманий модифікований силікагель масою 3 25 г переносять в колбу об'ємом 0,5дм , додають 3 100см 0,01М розчину ЕДТА (масове співвідношення модифікований силікагель:ЕДТА складає 75:1), додають НСІ до рН=5 і перемішують протягом 30-40 хвилин. Утворений продукт переносять на фільтр та промивають великою кількістю дистильованої води (1-2дм3) під тиском, а потім отриманий зразок сорбенту (зразок 2) висушують при температурі 80°С. Оцінку сорбційних властивостей отриманих зразків нового сорбенту проводили, визначаючи його ємність та коефіцієнт розподілу при вилученні іонів металів: міді(ІІ), нікелю(ІІ), цинку(ІІ), свинцю(ІІ) і кобальту(ІІ) з водних розчинів в широкому інтервалі концентрацій (10-2-10-5М) в оптимальних умовах процесу сорбції. Для цього попередньо вивчали кінетику процесу сорбції іонів кожного з металів і визначали час встановлення хімічної рівноваги ( р) (приклад 3), а також проводили дослідження впливу рН розчину на ефективність сорбції для визначення рН максимальної сорбції іонів кожного з металів (приклад 4). 5 51520 Приклад 3. Для визначення часу встановлення хімічної рівноваги процесу сорбції проводять дослідження кінетики сорбції вказаних металів. В 10 конічних 3 3 колб об'ємом 50см вносять по 25см розчинів Іо-4 3 нів міді(сCu(II)=0,4 10 ммоль/см ), нікелю(cNi(II)=0,2 10-4ммоль/см3), цинку(cZn(II)=0,2 104 ммоль/см3), свинцю(cPb(II)=0,1 10-4ммоль/см3) та кобальту(cCo(II)=0,2 10-4ммоль/см3) і додають по 0,5г зразка 1 або зразка 2 отриманого сорбенту. Суміш струшують протягом різних періодів часу і аналізують вміст іонів в кожному розчині спектрофотометричне за інтенсивністю забарвлення комплексів міді, кобальту, цинку та свинцю з 4-(2пірідилазо)резорцином [2], а нікелю - з диметилгліоксимом [3] та визначають час встановлення хімічної рівноваги ( р). Для усіх вищезазначених іонів при застосуванні обох зразків сорбенту час встановлення рівноваги р=1-2 хвилини. Приклад 4. Для вивчення залежності ефективності сорбції від рН реакційного середовища та визначення оптимального значення рН, необхідного для оцінки в подальшому ємності нового сорбенту, для кож 6 ного з досліджуваних іонів металів проводять серію аналогічних досліджень: до 8 контактних колб об'ємом 50см3 вносять по 0,5г зразка 1 або зразка 2 досліджуваного сорбенту, додають по 25 см3 розчинів, що вказані у прикладі 3, при різних значеннях рН: від 1 до 8 (відповідне рН забезпечують додаванням розчинів хлористоводневої кислоти або гідроксиду натрію) та інтенсивно перемішують протягом 2 хвилин. Потім проводять декантацію кожного розчину і визначають в ньому рівноважну концентрацію відповідного іону (як описано в прикладі 3) та розраховують ступінь його сорбції. Будують графік в координатах ступінь сорбції(R)/одиниці рН і з нього визначають ділянку значень рН, на який досягається максимальна ступінь сорбції (рНmax), а також значення рН 50%ної сорбції (рН1/2) для іонів кожного з досліджуваних металів. Отримані та наведені нижче у табл. 1 дані свідчать про те, що максимальна ступінь сорбції для всіх металів досягається на ділянці значень рН від 3 до 7. Таблиця 1 рН1/2 рНmах мідь(ІІ) 2,0 3,2-7,0 нікель(ІІ) 1,8 3,4-7,0 Приклад 5. Визначення ємності та коефіцієнту розподілу нового сорбенту щодо іонів досліджуваних металів виконують, проводячи сорбцію іонів кожного з металів з розчинів, що мають різну концентрацію, в оптимальних умовах: р 2 хв., рН=5. В 10 контактних колб кожної серії дослідів об'ємом 50см3 вносять по 0,5г зразка 1 або 2 досліджуваного сорбенту, додають по 25см3 розчину іонів металів з різною їх концентрацією (в ммолях на 1см3). При цьому в першій серії дослідів додають 10 розчинів іонів міді, концентрації яких змінюється в межах 0,2 10-4-0,16 10-3, в другій серії дослідів додають розчини іонів нікелю, концентрація яких змінюється від 0,1 10-4 до 0,17 10-3, у третій серії - розчини іонів цинку, концентрація яких змінюється від 0,1 10-4 до 0,15 10-3, у четвертій серіїрозчини іонів свинцю, що мають концентрацію в межах 0,1 10-4-0,4 10-3, та в п'ятій - розчини іонів кобальту з концентрацією від 0,1 10-4 до 0,2 104 ммоль/см3. Процес сорбції ведуть, перемішуючи суміш не менше ніж 2 хвилини. Потім проводять декантацію розчинів, вимірюють в кожному з них рівноважну концентрацію іонів відповідного металу та розраховують ступінь сорбції (R) за формулою: Co Cрівн R 100 % Co цинк(ІІ) 2,2 3,8-7,0 свинець(ІІ) 1,9 3,5-6,0 кобальт(П) 2,5 3,9-7,0 де C o і Cрівн - початкова і рівноважна концентрація іонів у розчині, ммоль/см. Серед отриманих значень R визначають максимальне значення (Rmax), та в умовах досліду досягнення максимальної сорбції визначають ємність відповідного зразка сорбенту (а) за формулою: V (Co Cрівн ) m V- об'єм досліджуваного розчину, см3; m - маса сорбенту, г. Використовуючи отримані дані про значення ступеня сорбції (R) , у кожному досліді розраховують значення коефіцієнту розподілу (K d ) іонів кожного з металів між розчином та сорбентом за формулою: R V Kd 100 R m У табл. 2 наведені дані про ємність та максимальні значення коефіцієнту розподілу для обох зразків сорбенту, одержаного способом, що заявляється. Дані таблиці 2 свідчать про те, що пропонованим способом одержують ефективний сорбент для вилучення іонів перехідних металів з розчинів, причому значне спрощення процесу синтезу сорбенту не призводить до погіршення його якісних характеристик. 7 51520 8 Таблиця 2 Показник Ємність сорбенту а, ммоль/г Максимальний коефіцієнту розподілу Кd, см3/г Зразок 1 Зразок 2 Зразок 1 Зразок 2 Джерела інформації: 1. Кудрявцев Г.В., Лисичкин Г.В., Сапожников Ю.А., Кузнецов Р.А. Авт. свид. СССР, №850204 Бюл. изобр., 1981, №28. Комп’ютерна верстка Н. Лиcенко Іони металу мідь(ІІ) нікель(ІІ) цинк(ІІ) свинець(ІІ) кобальт(ІІ) 0,041 0,042 0,039 0,041 0,037 0,025 0,027 0,023 0,026 0,021 0,24 105 0,24 105 0,21 105 0,16 105 0,12 104 0,19 105 0,18 105 0,18 105 0,14 105 0,10 104 2. А.В.Иванов, В.Н.Фигуровская, В.М.Иванов // Вестн. Моск. Ун-та. Сер. 2. Химия. -1992. -33, №6.с.570-574; 3. Органические реактивы для определения неорганических ионов, Ni. -М.: НИИТЭХИМ, 1970. 68с. Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for producing sorbent for removal of transition metal ions from solutions
Автори англійськоюTrokhymchuk Anatolii Kostiantynovych, Leschenko Vitalii Mykolaiovych, Andrianova Olena Borysivna, Ulberh Zoia Rudolfivna
Назва патенту російськоюСпособ получения сорбента для удаления ионов переходных металлов из растворов
Автори російськоюТрохимчук Анатолий Константинович, Лещенко Виталий Николаевич, Андрианова Елена Борисовна, Ульберг Зоя Рудольфовна
МПК / Мітки
МПК: B01J 20/10, B01J 45/00
Мітки: вилучення, перехідних, одержання, сорбенту, спосіб, розчинів, металів
Код посилання
<a href="https://ua.patents.su/4-51520-sposib-oderzhannya-sorbentu-dlya-viluchennya-perekhidnikh-metaliv-z-rozchiniv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання сорбенту для вилучення перехідних металів з розчинів</a>
Попередній патент: Спосіб профілактики та лікування ендотеліальної дисфункції при операціях на органах черевної порожнини
Наступний патент: Пристрій затискний комбінований
Випадковий патент: Бурове долото








