Спосіб реалізації фармакологічної інформації
Номер патенту: 70468
Опубліковано: 15.10.2004
Автори: Дем'яненко Василь Васильович, Саушев Антон Сергійович, Бігуняк Володимир Васильович, Бігуняк Наталя Володимирівна
Формула / Реферат
Спосіб реалізації фармакологічної інформації, який включає етап передачі фармакологічних властивостей від медикаментозного засобу на відповідний біодетектор організму за допомогою носія електромагнітної природи, який відрізняється тим, що носієм фармакологічної інформації використовують матеріал з високими діелектричними і хвилепровідними властивостями у вигляді смужки синтетичної полімерної тканини на основі поліуретанових і поліамідних волокон, причому частину тканинного матеріалу попередньо просочують водним розчином медикаментозного засобу, витримують упродовж 20-40 хвилин і висушують при 15-22°С, після чого від висушеної просоченої частини відокремлюють непросочений клаптик, який досліджують на наявність фармакологічної інформації і використовують за призначенням.
Текст
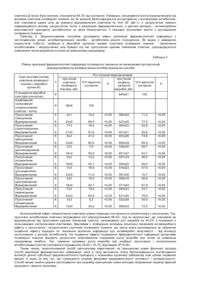
Винахід належить до біології, медицини, біофізики і радіофізики, зокрема до сфери біоінформаційних технологій, і може бути використаний при розробці принципово нових способів неінвазивного лікування на основі застосування принципів генерації, трансформації і ретрансляції біологічної інформації. Відомий спосіб реалізації фармакологічної інформації, який включає етап передачі фармакологічних властивостей медикаментозного засобу біодетектору відповідних тканин організму [1]. За відомим способом, реалізацію фармакологічної інформації, а саме на етапі передачі її відповідному біодетектору в організмі, здійснюють шляхом забезпечення умов безпосереднього контактування молекул (атомів, іонів) введеного в організм медикаментозного засобу з відповідними структурно-функціональними утвореннями організму. Традиційно це здійснюють або прийманням медикаментозного засобу всередину - ентерально, наприклад, ковтанням, або в клізмах чи свічках - ректально, а також парентерально, наприклад, введенням за допомогою шприца з порожнистою голкою медикаментів у рідкому стані у тканини, середовища і порожнини організму, наприклад, підшкірно, внутрішньом'язово, внутрішньовенно, внутрішньоплеврально, внутрішньоочеревинно, паранефрально, люмбально. Існують інші, аналогічні, шляхи реалізації фармакологічної інформації шляхом введення ліків в організм, наприклад, за допомогою закрапування в ніс, очі, аплікацій медикаментозних засобів, у тому числі втирання мазей, тощо. До аналогічних шляхів забезпечення реалізації фармакологічної інформації слід віднести також методики електрофорезу і фонофорезу. Недоліком відомого способу є недостатня технологічність, що випливає з того, що виконання умов реалізації фармакологічної інформації пов'язано з попереднім забезпеченням безпосереднього контактування молекул або атомів медикаментозного засобу з певними структурами організму. В багатьох випадках це пов'язано з мобілізацією в організмі механізмів біохімічної асиміляції і деградації незасвоєних медикаментозних засобів та продуктів їх метаболізму, що досить часто супроводжується негативними наслідками: від інтоксикації при передозуванні, до алергії - в результаті спотворення функції імунокомпетентної системи, нерідко - за рахунок несприятливого впливу на неї медикаментозних засобів. Ще одним несприятливим результатом дії на організм певних медикаментозних засобів (це, в першу чергу, стосується гормональних засобів) є формування так званого синдрому відміни, який виникає внаслідок гальмування синтезу власних регуляторних сполук при поступленні їх ззовні: за умов припинення подальшого надходження гормонів в організм власний ендокринний орган залишається неспроможним забезпечити адекватний фізіологічним потребам синтез власного продукту (гормону) з усіма несприятливими, нерідко фатальними для організму наслідками. Відомий спосіб реалізації фармакологічної інформації, який включає етап передачі фармакологічних властивостей від медикаментозного засобу на відповідний біодетектор організму за посередництвом носія електромагнітної природи [2]. За відомим способом фармакологічну інформацію вводять в організм на основі використання електричного струму, елементами замкненого електричного кола якого виступає сам організм і водний розчин медикаментозного засобу. Саме з електричними параметрами водного розчину медикаментозної речовини, об'єднаними поняттям так званого патерну у відомому способі пов'язують сутність фармакологічного інформаційного процесу. Недоліком відомого способу є недостатній рівень технологічності, що випливає з високої ймовірності деформації молекулярного каркасу медикаментозного засобу внаслідок електролітичної дисоціації при застосуванні електричного струму як головного носія інформації гіпотетичного патерна. Крім того, інформаційні процеси на рівні тканин, за сучасними науковими уявленнями, лежать в межах вкрай високочастотних хвильових процесів [3]. З зазначених позицій медичні технології з формуванням інформаційних процесів на основі застосування електричного струму є недостатньо коректними з методологічної точки зору, оскільки в енергетичному плані носій інформації, а саме електричний струм, і власне об'єкт інформаційного впливу молекула медикаментозного засобу є категоріями неспівставними. На цьому тлі фактично неконтрольований рівень відтворюваності ефектів інформаційного впливу, за відомим способом, стримує реальне впровадження його в практику як дійового способу медикаментозної корекції функцій організму на основі реалізації фармакологічної інформації. В основу винаходу поставлено завдання вдосконалити відомий спосіб, в якому шляхом застосування як носія фармакологічної інформації полімерного матеріалу з високими хвилепровідними властивостями в ділянці спектру електромагнітного випромінювання, що співпадає з спектром інформаційних хвильових процесів у живому організмі, досягають створення умов для неінвазивної ретрансляції молекулярної фармакологічної інформації від модифікованого молекулою медикаменту носія до тканинного біодетектора організму, а отже - підвищення технологічності способу. При вирішенні поставленого завдання були взяті до уваги сучасні уявлення про інформаційні процеси в живому, за якими нейро-гормональний і гуморальний механізми не є єдино можливими в процесах формування, трансформації і передачі біологічної інформації. Значна роль у біоінформаційних процесах належить електромагнітним випромінювальним процесам, причому частина біоінформаційних впливів проходить у межах керованих високочастотних хвильових процесів: від світлооптичних інформаційних каналів, що реалізуються на рівні феномену надслабкого світіння [3] - до біорезонансних явищ у мікрохвильовому спектральному діапазоні [46]. Останні пов'язують з фундаментальними властивостями біомолекул та клітини як структурно-функціональної субодиниці організованої біосистеми, а також біологічних тканин випромінювати і резонансно сприймати електромагнітні коливання у мікрохвильовому (міліметровому) спектральному діапазоні. Через надзвичайно низький (нетепловий) рівень енергетики вказаного випромінювання і одночасно достатньо виразні, а головне відтворювані, біологічні ефекти названий феномен пов'язують з біоінформаційними процесами. Було взято до уваги й те, що такий важливий елемент генератора для здійснення направленого інформаційного випромінювального впливу у надвисокочастотному (НВЧ) діапазоні - хвилепровід, згідно вимог законів фізики надвисокочастотного радіозв'язку, має бути виконаним із полімерного матеріалу з високими діелектричними та хвилепровідними властивостями. Такими є матеріали з фторопласту, поліефірних, поліамідних і поліуретанових смол, волокон та ін. Нарешті, з позицій сучасних уявлень про природу і властивості реліктового випромінювання [7, 8], останнє може бути розглянуте як природний генератор коливальних процесів на рівні молекулярних і субклітинних структур у цьому ж таки НВЧ діапазоні, що може виконувати роль своєрідної електромагнітної, набираючи значення активного фактора в процесах реалізації біологічної інформації як такої. Виходячи з наведеного, поставлене завдання вирішують тим, що у відомому способі реалізації фармакологічної інформації, який включає етап передачі фармакологічних властивостей від медикаментозного засобу на відповідний біодетектор організму за посередництвом носія електромагнітної природи, відповідно до винаходу носієм фармакологічної інформації використовують матеріал з високими діелектричними і хвилепровідними властивостями у вигляді смужки синтетичної полімерної тканини на основі поліуретанових і поліамідних волокон, причому частину тканинного матеріалу попередньо просочують водним розчином медикаментозного засобу, витримують упродовж 20-40 хвилин і висушують при 15-22°С, після чого від висушеної просоченої частини відокремлюють непросочений клаптик, який досліджують на наявність фармакологічної інформації і використовують за призначенням. Перелік фігур: Фіг.1 Схема постановки досліду К - контрольний клаптик полімерної тканини Д - дослідний клаптик полімерної тканини КА - контрольний клаптик полімерної тканини, просочений фармакологічним агентом Фіг.2 Ріст колоній мікроорганізмів (золотистий стафілокок) при посіві клаптиків полімерної тканини і інкубату: а) контрольний посів (клаптик К) б) дослід (клаптик Д) в) просочений антибіотиком клаптик КА Спосіб здійснюють таким чином. На клаптик матеріалу з високими діелектричними і хвилепровідними властивостями, викроєний у вигляді смужки тканини на полімерній основі, наприклад, з поліамідних і поліуретанових волокон, розпластаної на стерильному предметному склі (фіг.1), з одного кінця наносять водний розчин медикаментозного засобу, наприклад, антибіотика, в об'ємі 50-100мкл у стандартній концентрації, забезпечуючи просочення ним тканинної смужки (клаптик КА), слідкуючи при цьому, щоб розчин незаходив за умовну межу по лінії 00'. Через 20-40 хвилин від тканинної смужки відрізають дослідний клаптик Д по вказаній на фіг.1 лінії 00'. За контроль беруть аналогічний клаптик К з попередньо ізольованої полімерної тканини. Отримані у такий спосіб три клаптики тканини, а саме КА, Д і К, вміщують у три стерильні пробірки, і до кожної з них вносять рівний об'єм стандартизованої суспензії тестової мікробної культури, наприклад, 5-6мл, інкубують впродовж 20-40хв і висушують при 15-22°С. Після інкубації на відповідно промаркіровані чашки Петрі з живильним середовищем висівають окремо інкубовані тканинні клаптики і інкубат - суспензію тестової культури мікроорганізмів. Ріст колоній здійснюють при 37°С впродовж 48год., після чого проводять мікробіологічний аналіз, порівнюючи кількість колоній мікроорганізмів у відповідних пробах, роблячи висновок про результати дослідження. Приклад 1. З синтетичної тканини на полімерній основі з поліамідних і поліуретанових волокон вирізали прямокутну смужку, як наведено на фіг.1. З одного кінця тканинної смужки (наприклад, справа) нанесли водний розчин антибіотика тетрациклінового ряду в об'ємі 0,10мл у розведенні 1:1000, просочивши ним всю товщу тканини на площі 300-400мм 2. Через 30 хвилин і висушування нанесеної плями з іншого - непросоченого краю прямокутної смужки відрізали рівний за площею клаптик тканини. Отримані два клаптики, а також контрольний, який попередньо був відрізаний від ізольованої інтактної тканини, окремо помістили в стерильні промарковані пробірки. В кожну з них внесли по 4мл змиву стандартизованої суспензії культури золотистого стафілококу і інкубували при кімнатних умовах впродовж 30хв. Після цього з пробірок обережно виймали клаптики тканини і вміщували їх на живильне середовище у відповідно промаркірованих чашках Петрі. Окремо з кожної пробірки після видалення тканинних клаптиків висівали на середовище суспензію мікробів. Посіви в чашках Петрі вирощували при 37°С впродовж 48год. Результати заносили в робочу таблицю (табл.1) і аналізували. З наведених у таблиці даних видно, що просочення полімерної тканини антибіотиком, на відміну від контролю, супроводжується суттєвим зниженням росту тестової культури мікроорганізму довколо просоченого клаптика. Таблиця 1 Характер росту колоній мікроорганізмів на живильному середовищі у чашках Петрі відповідно до умов експерименту (n=10; Х±m) Клаптик полімерної тканини а) просочений антибіотиком (КА) б) відрізаний від просоченої смужки тканинної смужки(Д) в) інтактний клаптик - контроль (К) При посіві клаптика полімерної тканини, абс. Ріст колоній мікроорганізмів %% відносно При посіві інкубатуконтролю суспензії мікроорганізмі в, абс. %% відносно контролю 0 0 364+31 58,2 9±3 26,8 527±33 84,3 71±7 100,0 625±39 100,0 Відповідно і ріст колоній посіяного інкубату менш інтенсивний, ніж у контролі. Так, посів просоченого антибіотиком клаптика (КА) не виявив росту колоній, а в інкубаті після виймання цього клаптика - 364±31, що становило 58,2% від контрольного рівня. Ці результати (фіг.2) характеризують, власне, вихідний рівень антимікробної активності антибіотика, що був застосований для просочення тканинного клаптика, що й забезпечило зниження росту колоній в інкубаті на 41,8%. Про наявність ефекту реалізації фармакологічної інформації свідчать результати мікробіологічного посіву з непросоченого антибіотиком клаптику Д (фіг.3). З наведених у табл.1 даних видно, що ріст мікроорганізмів довкола клаптика Д становив в середньому 9±3 колоній, тобто 26,8% від контрольного рівня. Інтенсивність росту мікроорганізмів при посіві інкубату після виймання клаптика Д також була нижчою, становлячи 84,3% від контролю. Очевидно, гальмування росту мікроорганізмів під впливом клаптиків полімерної тканини, які не зазнали безпосереднього контактування з молекулами антибіотика, але становили єдине ціле до моменту відокремлення клаптиків по лінії 00' (фіг.1), є результатом певного інформаційного впливу, результатом якого є реалізація фармакологічних, у даному випадку - антимікробних властивостей препарату (антибіотика) за умов безконтактної її передачі волокнами взятої у дослідження полімерної тканини. Приклад 2. Запропонованим способом досліджено ефект реалізації фармакологічної інформації з застосуванням різних антибактеріальних засобів - антибіотиків різного походження. Як видно з наведених результатів (табл.2), інкубація в мікробній суспензії окремо клаптиків полімерної тканини - просочених антибіотиками і непросочених, але бувши х під час просочення єдиним тканинним клаптем, супроводжується зниженням числа мікробних колоній на живильному середовищі. Таблиця 2 Рівень реалізації фармакологічної інформації полімерною тканиною за показниками ростуколоній мікроорганізмів під впливом різних антибактеріальних засобів Серії дослідів (посіви клаптиків полімерної тканини і мікробної суспензії) Стандартна мікробна культура (контроль) Інкубований ізольований (непросочений) клаптик - контр. Просочений пеніциліном Відокремлений Просочений стрептоміцином Відокремлений Просочений ампіциліном Відокремлений Просочений диклоксациліном Відокремлений Просочений оксациліном Відокремлений Просочений доксицикліном Відокремлений Просочений еритроміцином Відокремлений Просочений левоміцином Відокремлений Просочений лінкоміцином Відокремлений n при посіві клаптика полімерної тканини, абс. Ріст колоній мікроорганізмів при посіві %% відносно %% відносно інкубатуР контролю суспензії контролю мікробів, абс. 9 546±51 Р 100 9 38±6 100 6 4±1 10,5
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod of pharmacological intervention
Автори англійськоюBihuniak Volodymyr Vasyliovych, Demianenko Vasyl Vasyliovych
Назва патенту російськоюСпособ фармакологического воздействия
Автори російськоюБигуняк Владимир Васильевич, Демьяненко Василий Васильевич
МПК / Мітки
МПК: C08G 69/00, A61K 31/74, C08G 71/00, C12Q 1/06, C12R 1/01, C12Q 1/04
Мітки: реалізації, інформації, фармакологічно, спосіб
Код посилання
<a href="https://ua.patents.su/4-70468-sposib-realizaci-farmakologichno-informaci.html" target="_blank" rel="follow" title="База патентів України">Спосіб реалізації фармакологічної інформації</a>
Попередній патент: Спосіб спільного використання ресурсу цифрової системи
Наступний патент: Лікарський засіб для профілактики та лікування системного остеопорозу в постменопаузальному періоді
Випадковий патент: Спосіб перемішування сталі в ковші