Спосіб оцінки абсолютної доступності лікарських засобів до тканин організму
Номер патенту: 29084
Опубліковано: 10.01.2008
Автори: Зіньковський Володимир Григорович, Годован Владлена Володимирівна, Жук Ольга Вікторівна, Кресюн Валентин Йосипович
Формула / Реферат
Спосіб оцінки абсолютної доступності лікарських засобів (ЛЗ) до тканин організму, який відрізняється тим, що спочатку обчислюють площі під концентраційними кривими ЛЗ у крові (![]() ) і в органах (
) і в органах (![]() ) для різних інтервалів часу після введення речовини (t) за формулою "методу трапецій", ділять їх на відповідні величини концентрацій в тканинах (Сi,t) і обчислені інтеграли концентрацій ЛЗ у крові при нескінченній експозиції (
) для різних інтервалів часу після введення речовини (t) за формулою "методу трапецій", ділять їх на відповідні величини концентрацій в тканинах (Сi,t) і обчислені інтеграли концентрацій ЛЗ у крові при нескінченній експозиції (![]() ), після чого визначають величини, обернені рівноважній константі розподілу (1/Крі), і кількості ЛЗ, що надходить з крові в одиницю об’єму досліджуваного органа (1/qi), шляхом регресійного аналізу одержаних даних у відповідності з рівнянням (1):
), після чого визначають величини, обернені рівноважній константі розподілу (1/Крі), і кількості ЛЗ, що надходить з крові в одиницю об’єму досліджуваного органа (1/qi), шляхом регресійного аналізу одержаних даних у відповідності з рівнянням (1):
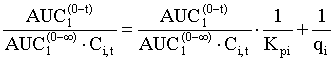 , (1)
, (1)
де: ![]() - площа під концентраційною кривою ЛЗ у крові від 0 до t;
- площа під концентраційною кривою ЛЗ у крові від 0 до t;
![]() - площа під концентраційною кривою ЛЗ у крові в інтервалі від 0 до
- площа під концентраційною кривою ЛЗ у крові в інтервалі від 0 до ![]() ;
;
![]() - рівноважна константа розподілу ЛЗ між кров’ю і органами;
- рівноважна константа розподілу ЛЗ між кров’ю і органами;
![]() - кількість ЛЗ, що надходить з крові в одиницю об’єму досліджуваного органа, при цьому визначувані параметри фармакокінетики (
- кількість ЛЗ, що надходить з крові в одиницю об’єму досліджуваного органа, при цьому визначувані параметри фармакокінетики (![]() ,
,![]() ,
,![]() ,
,![]() ) також обчислюють відповідно рівнянням (2), (4) і (5), що є варіантами рівняння (1):
) також обчислюють відповідно рівнянням (2), (4) і (5), що є варіантами рівняння (1):
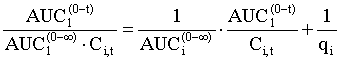 , (2)
, (2)
величину ![]() визначають як:
визначають як:
![]() , (3)
, (3)
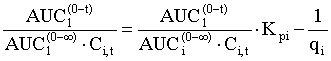 , (4)
, (4)
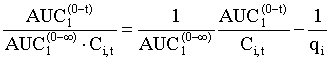 , (5)
, (5)
де позначення аналогічні рівнянню (1), а, визначивши з даних рівнянь величину qt, обчислюють величину абсолютної біодоступності ліків до тканини Wai за рівнянням (6):
, (6)
де: ![]() - концентрація ЛЗ в тканині (і-тому компартменті) у момент часу t;
- концентрація ЛЗ в тканині (і-тому компартменті) у момент часу t;
![]() - об’єм компартмента (і);
- об’єм компартмента (і);
![]() - кількість ЛЗ, яка надійшла та елімінувала з тканини в інтервалі часу від t=0 до t=
- кількість ЛЗ, яка надійшла та елімінувала з тканини в інтервалі часу від t=0 до t=![]() після введення досліджуваної речовини у масі Д;
після введення досліджуваної речовини у масі Д;
![]() - маса тварини;
- маса тварини;
d - доза введеного в організм ЛЗ (розмірність "маса ліків/маса тварини");
![]() - величина константи швидкості зворотного масопереміщення ЛЗ з тканини (відсік і) у кров (відсік 1), а також визначають величину константи швидкості зворотного масопереміщення ЛЗ з тканини (відсік і) у кров (відсік 1) за рівнянням (7):
- величина константи швидкості зворотного масопереміщення ЛЗ з тканини (відсік і) у кров (відсік 1), а також визначають величину константи швидкості зворотного масопереміщення ЛЗ з тканини (відсік і) у кров (відсік 1) за рівнянням (7):
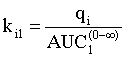 , (7)
, (7)
і по значенню частки від ділення кількості ЛЗ, що надійшла з крові в одиницю об’єму досліджуваного органа, на величину дози введеного ЛЗ в організм судять про абсолютну доступність ліків до тканин (органів) організму.
Текст
Спосіб оцінки абсолютної доступності лікарських засобів (ЛЗ) до тканин організму, який відрізняється тим, що спочатку обчислюють площі під концентраційними кривими ЛЗ у крові 3 29084 судять про абсолютну доступність ліків до тканин Корисна модель відноситься до області медицини, а саме фармакології, і може бути використаний для визначення параметрів фармакокінетики лікарських засобів (ЛЗ) в організмі. Біологічну доступність ліків визначають як частину дози, яка досягає системного кровотоку (центральної камери кінетичної схеми розподілу) після їх введення [1]. Біофармацевтичне визначення доступності ліків до внутрішнього середовища організму ґрунтується на зіставленні результатів дослідження кінетики їх вмісту у крові після внутрішньо- і позасудинного введення [1, 2]. Оскільки «біофазою дії» більшості ЛЗ є ті чи інші тканини або морфофункціональні структури, в яких звичайно здійснюють кількісне їх визначення у фармакокінетичних експериментах, то актуальним є обґрунтовування чітких критеріїв оцінки доступності ЛЗ до досліджуваних тестоб’єктів і розробка методів їх обчислення. У фармакокінетичних дослідженнях використується тільки метод визначення абсолютної біодоступності ЛЗ у крові [1, 2]. У сучасній фармакокінетиці відсутні критерії оцінки доступності ЛЗ або біологічно активних речовин (БАР) до органів і тканин, а також методи їх обчислення. У основу корисної моделі поставлена задача розробки способу оцінки «абсолютної доступності» ЛЗ до тканин організму (W ai) шляхом аналізу даних їх фармакокінетики, що дозволить підвищити точність і надійність методів фармакологічного прогнозування дії ліків на організм. Поставлена задача вирішується тим, що, згідно корисної моделі, спочатку обчислюють площі під концентраційними кривими ЛЗ у крові (AUC1(0-t)) і в органах (AUCi(0-t)) для різних інтервалів часу після введення речовини (t) за формулою «методу трапецій», ділять їх на відповідні величини концентрацій в тканинах (Ci,t) і обчисленні інтеграли концентрацій ЛЗ у крові при ( 0 - ¥) нескінченній експозиції (AUC1 ), після чого визначають величини, зворотні рівноважній константі розподілу (1/Кpі), і кількості ЛЗ, що поступає з крові в одиницю об’єму досліджуваного органу (1/qi), шляхом регресійного аналізу одержаних даних у відповідності з рівнянням (1): AUC( 0 -t ) 1 ( AUC10 -¥ ) × Ci, t = ( AUC10 -t ) AUC(0 1 - ¥) 1 1 × + × Ci,t Kpi qi , де: AUCi - площа під концентраційною кривою ЛЗ у крові від 0 до t; (0-t) ( 0 - ¥) AUC1 - площа під концентраційною кривою ЛЗ у крові в інтервалі від 0 до ¥ ; Крі - рівноважна константа розподілу ЛЗ між кров’ю і органами; qi - кількість ЛЗ, що поступає з крові в одиницю об’єму досліджуваного органу, 4 (органів) організму. при цьому, визначувані параметри ( 0 - ¥) ( 0 - ¥) фармакокінетики (AUC1 , AUCi , Kpi, qi) також обчислюють відповідно рівнянням (2), (4) і (5), що є варіантами рівняння (1): ( AUC10 - t ) ( AUC10 - ¥ ) = × Ci, t 1 AUC( 0 - ¥) i величину AUCi AUC(0 - ¥) i ( AUC10 - t ) AUC( 0 1 -¥ ) × Ci, t = = ( AUC10 - ¥ ) AUC( 0 -t ) 1 - ¥) AUC( 0 i ( AUC10 - t ) ( AUC10 - ¥) ( 0 - ¥) × Ci,t = × Ci, t AUC( 0 - t ) 1 Ci, t + 1 qi , визначають як: × Kpi × K pi × 1 qi , , 1 ( AUC10 - ¥) AUC( 0 - t ) 1 Ci, t 1 qi , де позначення аналогічні рівнянню (1), а, визначивши з даних рівнянь величину qi, обчислюють величину абсолютної біодоступністі ліків до тканини W ai за рівнянням (6): ¥ q Q M k Wai = i = i × = i1 Ci,t × dt d Vi Д d ò 0 , де: Сіt - концентрація ЛЗ в тканині («і-тому» компартменті) у момент часу t; Vi - об’єм компартмента (i); Qi - кількість ЛЗ, яка поступила та елімінувала з тканини в інтервалі часу від t=0 до t= ¥ після введення досліджуваної речовини у масі Д; М - маса тварини; d - доза введеного в організм ЛЗ (розмірність «маса ліків/маса тварини»); кi1 - величина константи швидкості зворотного масопереміщення ЛЗ з тканини (відсік i) у кров (відсік 1), а також визначають величину константи швидкості зворотного масопереміщення ЛЗ з тканини (відсік i) у кров (відсік 1) за рівнянням (7): qi ki1 = AUC( 0 - ¥) 1 , і по значенню частки від ділення кількості ЛЗ, що поступила з крові в одиницю об’єму досліджуваного органу на величину дози введеного ЛЗ в організм судять про абсолютну доступність ліків до тканин (органів) організму. Вище викладене підтверджує наявність причинно-наслідкових зв’язків між сукупністю заявлених ознак і досягнутими результатами. Спосіб здійснюється наступним чином. По-перше, запропоновано обґрунтовування критерію біодоступності ліків до тканини (W ai). Основною фармакокінетичною характеристикою тканини, яка представлена у кінетичній схемі розподілу ЛЗ в організмі деяким («і-тим») ком (1) 5 29084 партментом (об’ємом Vi), є його кількість (Qi), яка поступила та елімінувала з тканини в інтервалі часу від t=0 до t= ¥ після введення досліджуваної речовини в дозі Д. Швидкість надходження досліджуваного ЛЗ у n момент часу (t) із крові в тест-об’єкт ( (1i) t ) є рівною добутку його кількості (А1t) на константу швидкості процесу його масопереміщення (k1i) з крові (компартмент (1) об’ємом (V1)) в (i): ì ïn(1i)t = k 1i × V1 × C1t , í ïC1t = A1t / V1, î де: С1t - концентрація ЛЗ у крові у момент часу t. Швидкість елімінації БАР у момент часу (t) з n компартмента (i) ( (1i) t ) дорівнює добутку його вмісту (Ait) на константу зворотного масопереміщення (ki1) з (i) в (1): ìn(1i )t = k i1 × Vi × Cit , ï í ïCit = A it / Vi , î де Сi,t – концентрація ЛЗ в тканині («і-тому» компартменті) у момент часу t. Швидкість зміни вмісту речовини у досліджуваному компартменті у момент (і) складає: dCit n(1i )t - n(i1)t= Vi dt , Інтегруючи за часом (від 0 до ¥ ) перші рівняння систем рівнянь (8) і (9) і рівняння (10), визначають, чому рівні кількість речовини, яка поступила в компартмент (Q1i) і яка елімінувала з нього (‘Qi1): ¥ ¥ ì ïQ = n (1i)t × dt = k1i × V 1 × C1t × dt, ï 1i 0 0 ï ï ¥ ¥ ï í' Qi1 = n (i1)t × dt = k i1 × Vi × Cit × dt, ï 0 0 ï Q1i =' Qi1. ï ï ï î ò ò ò ò ¥ ò C dt it 0 ¥ òC 1t dt 0 Величини i , розраховані на підставі аналізу даних концентрацій БАР у крові (C1t) і тканині (Cit), у фармакокінетиці позначають ( ( AUC10 -¥ ) AUC(0 -¥ ) AUC10 -¥ ) i як: і . Величину використовують при визначенні біодоступності ліків [1, 2]. Безпосереднє визначення величини Q1i (розмірність: «маса») у більшості випадків є складним: 1) у експерименті звичайно визначають концентрації ліків (Cit) у зразках (пробах) досліджуваного тест-об’єкту, а не його кількості в компартментах; 2) величина (Vi) є умовною і часто фізичному визначенню не підлягає; 6 3) у експерименті звичайно вводять дослідним тваринам однакові (фіксовані) «питомі» дози (d) (розмірність «маса ліків/маса тварини»): d=Д/M, де М - маса тварини; Д - доза (маса) ЛЗ, яка вводиться. Зручнішою є оперування величиною «питомої кількості» ЛЗ, яка поступає в одиницю об’єму (або маси) тканини: qi=Qi/Vi= AUC(0-)¥ .ki1, i З урахуванням рівнянь (11-13) «біодоступність ліків до тканини» («і-того» компартменту кінетичної схеми його розподілу в біосистемі) (W ai) може бути представлена наступним виразом: (8) ¥ Wai = qi Qi M k i1 = × = Ci,t × dt d Vi Д d ò 0 , Як видно з рівняння (14), для обчислення величини (W ai) необхідно попередньо розрахувати площу під фармакокінетичною кривою ЛЗ в ¥ æ ö ç ÷ AUCi( 0 - ¥ ) » Ci,t × dt ÷ ç ç ÷ 0 ø і константу (або тканини è суму констант) його елімінації з тест-об’єкту (в даному прикладі - це ki1). Значення d (мг/кг) задається умовами експерименту. Таким чином, після обгрунтовання критерію біодоступністі ліків до тканини спосіб обчислювання здійснюється наступним чином: у рівняння (10) підставляємо значення V(1i) t і V(i1)t з перших рівнянь систем рівнянь (8) і (9). Одержане фундаментальне рівняння матеріального балансу розподілу речовини між кров’ю (відсік (1)) і тканинами (відсік (i)), інтегруємо за часом (від 0 до t); замість інтегралів концентрації підставляємо (9) ò ( AUC10 - t ) AUC(0 - t ) i відповідні величини і . Паралельно інтегруємо це ж рівняння за часом від ¥, 0 до замість множника (k1iVі)/(ki1Vі) підставляємо величину рівноважної константи розподілу (Крі) речовини між кров’ю (відсік 1) і тканиною (відсік i), ділимо одержане рівняння матеріального балансу ЛЗ і представляємо результати у вигляді чотирьох лінійних анаморфоз, які є результуючими рівняннями чотирьох варіантів методу регресійного аналізу дослідних даних (рівняння (1), (2), (4) і (5)). Приведені віще рівняння дозволяють виконати лінійний регресійний аналіз даних методом найменших квадратів відповідно до рівняння: yx=a+xyb, де ух і xу - одержані в досліді величини, а а і b шукані параметри процесу. У табл. 1 представлені величини, які використовуються для виконанні регресійного аналізу і які визначаються на підставі даного аналізу Номер рівняння yх (10) (11) xy 7 29084 ( 0- t ) AUC( 0 - t ) 1 (1) AUC( 0 - ¥ ) 1 AUC i ( AUC10-¥ ) × Ci,t AUC (0 - t ) 1 (2) (5) C i,t AUC( 0 - t) i AUC ( 0- ¥ ) × Ci,t i AUC( 0 - t) i AUC ( 0- ¥ ) × Ci,t i AUC ( AUC10 -t ) Ci,t Розроблені варіанти регресійного аналізу не являються рівнозначними і при аналізі результатів дослідження може бути віддана перевага одному з них, виходячи з наступного. Якщо величина ( 0-¥ ) AUCi не може бути визначена методом трапецій, то вона, як і інші параметри, може бути обчислена з рівняння (2), з наступним залученням AUC(0 - ¥) 1 рівняння (3), аналогічно - величина - з рівнянь (3) і (5). Визначивши з даних рівнянь величину qt, обчислюють величину W ai за рівнянням (6). Приклад використання пропонованих варіантів регресійного методу аналізу даних 14 фармакокінетики С-феназепама (7-бром-5ортохлорфеніл)-1,2-дигідро-2Н-1,4-бенздіазепін-2она-2-14С (І)) в організмі мишей лінії BALB/c. Зміна вмісту вихідної сполуки (І) у плазмі крові і головному мозку мишей при внутрішньоочеревинному введенні їм 14С-І (питома активність 2 Cu/mol) у дозі 14мг/кг представлено на Фіг.1 (результати виконаного авторами раніше дослідження [4]). За допомогою запропонованих методів регресійного аналізу можливе визначення ( 0-¥ ) ( AUC10 - ¥) AUCi параметрів ( запропонованих , , qi, Kpi) кожним із варіантів, які вимагають попереднього визначення величин ( 0-¥ ) AUCi Параме три (0 - t ) 1 (0-¥ ) × C i, t i AUC ( AUC10 - ¥) або (і) . На Фіг.2 наведена, як приклад, графічна інтерпретація процесів розподілу сполуки І між кров’ю (1) і головним мозком (і) мишей у відповідності з рівнянням (1). На Фіг.3 наведена, як приклад, графічна інтерпретація процесів розподілу сполуки І між кров’ю (1) і головним мозком (і) мишей у відповідності з рівнянням (2). На Фіг.4 наочно наведена графічна інтерпретація процесів розподілу сполуки І між кров’ю (1) і головним мозком (і) мишей у відповідності з рівнянням (4). На Фіг.5 наочно наведена, як приклад, графічна інтерпретація процесів розподілу сполуки І між кров’ю (1) і головним мозком (і) мишей у відповідності з рівнянням (5). Результати регресійного аналізу процесів розподілу 14С-І між плазмою крові і головним мозком мишей, трансформовані у величини, відповідні ух і ху, які обчислені методом найменших квадратів та у відповідності з рівняннями (1), (2), (4), (5), наведені у табл. 2. Таблиця 1 K pi 1 qi × Ci,t ( AUC 10 - t ) ( AUC 10 -¥ ) × C i,t (4) 8 Крі qі wai Ki1 ( AUC10 - ¥) ( 0-¥ ) AUCi 1 варіант,1 q заснова i ний на 1 рівнянні qi (1) 1,68 - 1 q 714,3 i 4,25 1,79 ... 2 варіант, заснова ний на рівнянні (2) 1,68 714,3 4,25 1,79 ... 399,8 400,0 2 3 4 1 варіант, ( 0-¥ ) варіант, AUC заснова i заснова ний на K ний на рівнянні pi рівнянні (4) (5) 1,68 10-¥ )1,70 AUC( 666,7 1 666,7 3,97 3,97 1,77 1,77 224,6 222,2 ... ... Запропоноване технічне рішення вперше дозволяє одночасно комплексно оцінити основні параметри фармакокінетики ліків, які характеризують масопереміщення цих речовин між центральним кінетичним відсіком їх розподілу (1) (кров’ю, плазмою крові) і периферичними компартментами (досліджуваними органами і тканинами), що не було можливим у сучасній фармакокінетиці. Література: 1. Boroujerdi М. Bioavalability and Bioequivalence evaluation/ In.: Pharmacokinetics Principles an applications. - McGraw-Hill Companies, 2002. - P.315-331. 2. Проблемы фармакокинетики: Итоги науки и техники/ Серия Фармакология. Химиотерапевтические средства. - Москва, 1984. Т.14. - 227с. 3. Соловьев В.Н., Фирсов А.А., Филов В.А. Фармакокинетика. -М.: Медицина, 1980. - 421с. 4. Экспериментальное изучение генетических различий в метаболизме распределения 14Сфеназепама/ С.Б. Серединин, В.Г. Зиньковский, Н.Я. Головенко, И.В. Рыбина// Химикофармацевтический журнал. - 1981. - №9. - С.23-26. 9 29084 10
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for assessment of absolute drug penetrability into organism tissues
Автори англійськоюHodovan Vladlena Volodymyrivna, Zinkovskyi Volodymyr Hryhorovych, Zhuk Olha Viktorivna, Kresiun Valentyn Yosypovych
Назва патенту російськоюСпособ оценки абсолютной проникаемости лекарственных средств (лс) в ткани организма
Автори російськоюГодован Владлена Владимировна, Зиньковский Владимир Григорьевич, Жук Ольга Викторовна, Кресюн Валентин Иосифович
МПК / Мітки
МПК: A61B 10/02
Мітки: засобів, тканин, доступності, лікарських, оцінки, абсолютної, організму, спосіб
Код посилання
<a href="https://ua.patents.su/5-29084-sposib-ocinki-absolyutno-dostupnosti-likarskikh-zasobiv-do-tkanin-organizmu.html" target="_blank" rel="follow" title="База патентів України">Спосіб оцінки абсолютної доступності лікарських засобів до тканин організму</a>
Попередній патент: Спосіб визначення опору сталей корозійно-механічному руйнуванню
Наступний патент: Диспергатор
Випадковий патент: Спосіб одержання порошкоподібних композицій для безалкогольних напоїв









