Спосіб визначення параметрів розподілу лікарських засобів у крові, органах і тканинах організму
Номер патенту: 19966
Опубліковано: 15.01.2007
Автори: Зіньковський Володимир Георгійович, Щукін Сергій Ігоревич, Годован Владлена Володимирівна, Кресюн Валентин Йосипович, Жук Ольга Вікторівна
Формула / Реферат
Спосіб визначення параметрів розподілу лікарських засобів у крові, органах і тканинах організму, що включає знаходження величин площ під концентраційними фармакокінетичними кривими в крові та органах (тканинах) і їх відношень, який відрізняється тим, що визначають інтеграл концентрації (площа під концентраційною кривою) в інтервалі від 0 до ![]() величини концентрації лікарського засобу в крові та органах (тканинах) організму за формулою визначення та знаходять частку від ділення площі під концентраційною кривою лікарського засобу в крові на його концентрацію в досліджуваному органі (тканині), потім аналогічно обчислюють співвідношення площі під концентраційною кривою лікарського засобу в органі (тканині) до його концентрації в органі, після чого визначають рівноважні константи розподілу і константи швидкостей масоперенесення речовини шляхом пропонованих трьох варіантів методу регресивного аналізу за рівняннями:
величини концентрації лікарського засобу в крові та органах (тканинах) організму за формулою визначення та знаходять частку від ділення площі під концентраційною кривою лікарського засобу в крові на його концентрацію в досліджуваному органі (тканині), потім аналогічно обчислюють співвідношення площі під концентраційною кривою лікарського засобу в органі (тканині) до його концентрації в органі, після чого визначають рівноважні константи розподілу і константи швидкостей масоперенесення речовини шляхом пропонованих трьох варіантів методу регресивного аналізу за рівняннями:
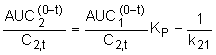 ,
,
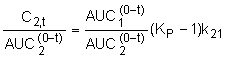 ,
,
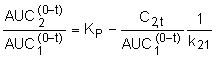 ,
,
де: ![]() і
і ![]() - площі під концентраційними кривими від 0 до
- площі під концентраційними кривими від 0 до ![]() в органі (тканині) і крові відповідно,
в органі (тканині) і крові відповідно, ![]() - концентрація лікарського засобу в органі (тканині),
- концентрація лікарського засобу в органі (тканині), ![]() - рівноважна константа розподілу лікарського засобу і крові, органах і тканинах,
- рівноважна константа розподілу лікарського засобу і крові, органах і тканинах, ![]() - константа швидкості масоперенесення лікарського засобу з органу у кров.
- константа швидкості масоперенесення лікарського засобу з органу у кров.
Текст
Спосіб визначення параметрів розподілу лікарських засобів у крові, органах і тканинах організму, що включає знаходження величин площ під концентраційними фармакокінетичними кривими в крові та органах (тканинах) і їх відношень, який відрізняє ться тим, що визначають інтеграл концентрації (площа під концентраційною кривою) в інтервалі від 0 до t величини концентрації лікарського засобу в крові та органах (тканинах) організму за формулою визначення та знаходять частку від ділення площі під концентраційною кривою лікарського засобу в крові на його концентрацію в досліджуваному органі (тканині), потім аналогічно обчислюють співвідношення площі під концентраційною кривою лікарського засобу в органі (ткани ні) до його концентрації в органі, після чого визначають рівноважні константи розподілу і константи швидкостей масоперенесення речовини шляхом пропонованих трьох варіантів методу регресивного аналізу за рівняннями: Корисна модель відноситься до області медицини, а саме фармакології, і може бути використана для визначення параметрів фармакокінетики лікарських засобів (ЛЗ) в організмі. Дослідження механізмів і визначення кількісних показників процесів розподілу ЛЗ в організмі, зокрема оборотного масопереносу речовин між кров'ю і різними тканинами, є однією з основних задач сучасної експериментальної фармакокінетики. Актуальність досліджень в цьому напрямку визначається тим, що, по-перше, "біофази дії ЛЗ" (відсіки кінетичних схем їх розподілу, що містять рецепторно-ефекторні супрамолекулярні комплекси), також як і осередки патологічних процесів, є тими або іншими тканинами (органами, морфофізіологічними структурами) і зворотно обміню ються з кров'ю (звичайно дифузійно) ксенобіотиками (зокрема, ЛЗ), які поступають у вн утрішнє середовище організму ззовні; по-друге, ті або інші тканини є місцями розвитку небажаних ефектів, викликаних дією ЛЗ на організм. У зв'язку з цим, терапевтичні і токсичні (максимально допустимі) концентрації ЛЗ в крові повинні визначатися з урахуванням "відносної тропності" цих речовин до досліджуваних біосубстратів. Згаданий показник відповідає константі рівноваги (КР) процесів розподілу досліджуваної речовини між кров'ю і досліджуваною тканиною і є однією з фундаментальних (термодинамічних) характеристик системи "ліки - організм". Відомий метод визначення рівноважної константи розподілу (КР) введеної в організм ЛЗ між AUC( 0- t ) AUC( 0- t ) 1 2 1 = KP , C2,t C2, t k 21 C2,t AUC(0 - t ) 2 AUC( 0- t ) 2 = AUC( 0- t ) 1 AUC( 0- t ) 2 =K P AUC( 0- t ) 1 де: AUC(0 - t ) і 2 (K P - 1)k 21 , C2, t 1 , ( AUC10 -t ) k 21 ( AUC10 - t ) - площі під концентрацій (13) (19) UA (11) 19966 в органі (тканині), KP - рівноважна константа розподілу лікарського засобу і крові, органах і тканинах, k 21 - константа швидкості масоперенесення лікарського засобу з органу у кров. U ними кривими від 0 до t в органі (тканині) і крові відповідно, C 2,t - концентрація лікарського засобу 3 19966 4 кров'ю, органом (тканиною) шляхом аналізу безпо( 0- t m ) (0 -¥ ) AUCi » AUCi + AUC( t m -¥ ) i (4) середньо вимірюваних у фармакокінетичному екснеобхідно показати, що зміна у часі показника перименті величин - відношення концентрації ксенобіотику в тканині, визначеного у момент AUC(0 - t ) , наближається (при t®¥) до AUC(0 -¥ ) . i i досягнення максимальної концентрації (С2,t) до 2. Неможливість визначення величини його концентрації в крові (С1,t) [1]. AUC(0 -¥ ) в ти х випадках, коли фармакокінетичні Недоліком вказаного методу є те, що визнаi чення КР є точковим (однократним), а величина результати описують тільки «висхідну гілку» фарСmах не завжди може бути визначений точно, тамакокінетичної кривої (тобто: tm≤Tmax) вмісту ліків в кож як і Тmах. крові або тканині. Відомий також метод визначення констант В основу корисної моделі поставлено задачу розподілу ксенобіотика в організмі, заснований на удосконалення способів визначення параметрів регресійному аналізі лінійної залежності між велирозподілу біологічно активних речовин та лікарсьчинами площ під фармакокінетичними кривими ких засобів між кров'ю, органами і тканинами оргаконцентрацій ЛЗ в крові і тканині [2, 3]. нізму шляхом визначення параметрів їх фармакоПроте вказаний метод є наближеним, оскільки кінетики, що дозволить підвищити точність і не дозволяє точно визначити КР через відхилення вірогідність способу. від лінійності процесу в початкові інтервали часу. Поставлена задача вирішується тим, що, згідНайбільш близьким до технічного рішення, що но корисної моделі, визначають інтеграл величини заявляється, є метод, який широко використовуконцентрації ЛЗ в крові та органах (тканинах) орється у фізіологічному (перфузійному) моделюганізму (площ під концентраційною кривою) в інванні фармакокінетики [4]. У даному методі паратервалі від 0 до t величини концентрації ЛЗ у крові метри кінетичної схеми розподілу ксенобіотику в та органах (тканинах) організму за формулою виорганізмі оцінюють, використовуючи величину значення та знаходять частку від ділення площі ( під концентраційною кривою ЛЗ (ККЛЗ) у крові на AUC10 - ¥) площі під фармакокінетичною кривою його концентрацію в досліджуваному органі (ткадосліджуваної речовини в крові (1): нині), потім аналогічно обчислюють співвідношен¥ Q 1 ня площі під ККЛЗ в органі (тканині) до його конце(0 - ¥ ) » ò C1dt » AUC1 нтрації в органі, після чого визначають рівноважні V1 k el. (1) 0 константи розподілу і константи швидкостей масоде: Q - кількість речовини, що поступила в орпереносу ЛЗ шляхом регресійного аналізу одерганізм, kel - константа її елімінації з організму. жаних даних по рівнянню (5): При умові t®¥ константа рівноваги дорівнює: AUC( 0- t ) AUC( 0- t ) 1 2 1 AUC( 0- ¥) k12 V1 = KP 2 » » KP C2,t C2, t k 21 (5) AUC( 0- ¥) k 21V2 (2) 1 (0 - t ) (0 - t ) де AUC2 і AUC1 площі під концентраде: AUC1(0-¥) і АUС2(0-¥) - площі під фармакокінетичними кривими концентрацій ЛЗ в крові ційними кривими від 0 до t в органі (тканині) і крові(камера 1) і органі (камера 2); k12 і k21 - константи відповідно, С2,t - концентрація ЛЗ в органі (тканині), швидкостей процесів надходження з крові в тканиКP - рівноважна константа розподілу ЛЗ між кров'ю ну і зворотного процесу, V1 і V2 - об'єми розподілу та органом (тканиною), k21 - константа швидкості в крові і тканині. масопереносу ЛЗ з органу у кров; Недоліками цього методу є: або відповідно рівнянь (6) чи (7): 1. Можливість виникнення грубих помилок, поC2,t AUC( 0- t ) 1 в'язаних з необхідністю екстраполяційної оцінки = (K P - 1)k 21 термінальної частини площі під фармакокінетичAUC(0 - t ) AUC( 0- t ) (6) 2 2 ною кривою в інтервалі часу досліду (tm®¥) (де tm ( 0- t ) AUC2 C2, t 1 термінальний (найбільший у виконаній дослідній = KP ( 0- t ) (0 -t ) k серії) час визначення ЛЗ у досліджуваних біосубсAUC1 AUC1 21 (7) тратах). В класичних фармакокінетичних досліде позначення аналогічні рівнянню (5). дженнях визначення термінальної частини площі Вище викладене підтверджує наявність припід фармакокінетичною кривою концентрації ЛЗ в чинно-наслідкових зв'язків між сукупністю заявледосліджуваному об'єкті ґрунтується на постулатах: них ознак і досягнутими результатами. а) "фармакокінетична крива" є сумою експонент; б) Спосіб здійснюється наступним чином. у термінальній частині вона представлена найпоФундаментальне рівняння (2) інтегруємо за вільнішою з них; в) експоненційний множник найчасом (від 0 до t), замість інтегралів концентрацій повільнішої (термінальної) експоненти (kel) визна( підставляємо відповідні величини ( AUC10 - t ) і чає кінетику процесу елімінації ЛЗ з біосубстрату в інтервалі часу (tm-¥). Якщо перераховані пропозиAUC(0 - t ) ) і представляємо результати у вигляді 2 ції реалізуються в досліді, то: трьох лінійних анаморфоз, що є результуючими Ci, t m рівняннями трьох варіантів методу регресійного AUC( t m -¥ ) = i km аналізу дослідних даних (див. рівняння (5)-(7)). (3) Наведені вище рівняння дозволяють виконати де: Ci,tm - концентрація ЛЗ при t=tm. лінійний регресійний аналіз даних методом найПриведені припущення вірні, але в практиці не менших квадратів відповідно до рівняння: завжди здійснювані. Тому, визначаючи величину: ( ) 5 19966 6 yх=а+xуb (8) У табл. 1 представлені величини, що викорисде ух і xу - одержані в досліді величини, а а і b товуються при виконанні регресійного аналізу і шукані параметри процесу. визначаються. Таблиця 1 Номер рівняння ух хy a b 5 AUC(20 -t ) AUC( 0 -t ) 1 C2, t C2, t 1 k 21 KР C2, t AUC( 0 -t ) 1 k21 KP·k21 KP 1 k 21 6 AUC(20 -t ) AUC(20 -t ) AUC(20 -t ) 7 C2, t AUC( 0 -t ) 1 AUC( 0 -t ) 1 Розроблені варіанти регресійного аналізу не є рівнозначними і в дослідженні може бути віддано перевагу одному з них, виходячи із наступних міркувань. Значення AUC( 0 -t ) 1 і, відповідно, зворотні AUC(20 -t ) їм величини значно змінюються в початковому періоді розподілу ЛЗ в організмі, коли в досліді реєструють «висхідні гілки» фармакокінетичних кривих. В таких досліджуваних серіях оптимальним є використання рівняння (6). Рівняння (5) оптимальне для дослідження при аналізі «низхідних гілок» фармакокінетичних кривих. Приклад використання пропонованих варіантів регресійного методу для аналізу параметрів фармакокінетики 7-бром-5-феніл-1,2-дигідро-3-окси2Н-1,4-бенздіазепін-2-ону - метаболіту, який утворюється в організмі після введення досліджуваним тваринам 7-бром-5-феніл-1,2-дигідро-2Н-1,4бенздіазепін-2-ону (I). Зміна вмісту 3-оксипохідного І в головному мозку і плазмі крові мишей в інтервалі 0,5-6год після внутрішньоочеревинного введення їм 2-14С-І (0,214 Сі/mol) в дозі 1,4мг/кг представлено на Фіг.1 (результати виконаного авторами раніше дослідження [5]). Параметри процесів розподілу, які представлені у Фіг.1, не можуть бути обчислені на підстави способу, обраного як прототип, оскільки в тимчасовому інтервалі досліду немає можливості визначити константи швидкості процесів елімінації сполук з біосубстратів (в інтервалі від t®¥), що вивчаються. За допомогою запропонованих варіантів регресійного аналізу дана задача була успішно вирішена. У Фіг.2 наглядно наведена як приклад графічна інтерпретація розподілу між кров'ю (1) і головним мозком (2) мишей 3-оксипохідного І у відповідності з рівнянням (5). У Фіг.3 наведена графічна інтерпретація розподілу між кров'ю (1) і головним мозком (2) мишей 3-оксипохідного І у відповідності з рівнянням (6). У Фіг.4 наведена графічна інтерпретація розподілу між кров'ю (1) і головним мозком (2) мишей 3-оксипохідного І у відповідності рівняння (7). Результати регресійного аналізу процесів розподілу 3-оксипохідного І між кров'ю і головним мозком мишей, трансформованих у величини, відповідні ух і ху рівнянь (5)-(7) (див. табл. 1), виконаного методом найменших квадратів, приведені у табл. 2. Таблиця 2 Параметри КР k21 k12 1 варіант, заснований на рівнянні (5) 5,13 3,08 15,79 2 варіант, заснований на рівнянні (6) 5,73 6,46 37,19 У порівнянні з прототипом заявлене технічне рішення дозволяє підвищити точність визначення параметрів рівноважної константи розподілу і констант швидкості масопереносу ЛЗ між кров'ю і органом (тканиною), а також одночасно визначати як величину КР, так і значення константи швидкості процесу зворотного масопереносу ЛЗ з досліджуваної тканини (наприклад, «біофази їх дії») у кров (k21). Визначення цієї величини дозволяє оцінити середній час перебування (mean residence time MRT2) ліків в «біофазі його дії» методом позамодельним і незалежним від властивостей і кількості периферичних відсіків (органів і тканин), зворотно 3 варіант, заснований на рівнянні (7) 5,16 2,91 15,00 взаємозв'язаних з кров'ю, що неможливо при застосуванні існуючих методів. Література: 1. Сумрий С.К., Жук О.В., Карпинчик В.А. Фармакокинетика тилорона в организме мышей при его внутривенном и пероральном способе введения // Ліки України. - 2003. - №6. - С. 27-29. 2. Жук О.В., Зіньковський В.Т., Сумрій С.К. Визначення процесів необоротного зв'язування 3Наміксину в органах і тканинах мишей // Досягнення біології та медицини. - 2004. - №1(3). - С. 80-84. 3. Зіньковський В.Г., Щукін C.I. Розробка методів позамодельного аналізу процесів розподілу 7 19966 8 ксенобіотиків між кров'ю, органами й тканинами partition ratios. Gueorguieva I., Nestorov I. A., et al. // при їхньому однократному введенні в організм // Pharmacokinet. Pharmacodyn. - 2004. - V. 31(3). - P. Досягнення біології та медицини. - 2005. - № 2 (6). 185-213. - С. 27-33. 5. Зиньковский В.Г. Биокинетика и структура 4. Development of a whole body physiologically новых психотропных препаратов, их предшестbased model to characterise the pharmacokinetics of венников и метаболитов: дисс... докт. биол. наук. benzodiazepines. 1: estimation of rat tissue-plasma Одесса, 1994. - 528 с. Комп’ютерна в ерстка А. Крижанівський Підписне Тираж 26 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for assessing parameters of drug distribution in blood, organs, and tissues of body
Автори англійськоюHodovan Vladlena Volodymyrivna, Zinkovskyi Volodymyr Heorhiovych, Zhuk Olha Viktorivna, Kresiun Valentyn Yosypovych
Назва патенту російськоюСпособ определения параметров распределения лекарственных средств в крови, органах и тканях организма
Автори російськоюГодован Владлена Владимировна, Зиньковский Владимир Георгиевич, Жук Ольга Викторовна, Кресюн Валентин Иосифович
МПК / Мітки
МПК: A61B 10/00
Мітки: засобів, параметрів, органах, тканинах, розподілу, крові, спосіб, лікарських, визначення, організму
Код посилання
<a href="https://ua.patents.su/4-19966-sposib-viznachennya-parametriv-rozpodilu-likarskikh-zasobiv-u-krovi-organakh-i-tkaninakh-organizmu.html" target="_blank" rel="follow" title="База патентів України">Спосіб визначення параметрів розподілу лікарських засобів у крові, органах і тканинах організму</a>
Попередній патент: Магнійоксіетилідендифосфонатогерманат, який характеризується вазодилататорною дією
Наступний патент: Спосіб одержання композиційних електродугових покриттів
Випадковий патент: Пристрій для різання листового металу








