Спосіб отримання чистих ізомерних 5- та 7-метил-8-нітрохінолінів
Номер патенту: 84756
Опубліковано: 25.10.2013
Автори: Водзінський Сергій Валентинович, Галкин Борис Миколайович, Кириченко Ганна Михайлівна, Ішков Юрій Васильович
Формула / Реферат
Спосіб отримання чистих ізомерних 5- та 7-метил-8-нітрохінолінів, що полягає у розділенні суміші ізомерних 5- та 7-метил-8-нітрохінолінів, що отримані нітруванням відповідних 5- та 7-метил-хінолінів, який відрізняється тим, що розділення ізомерів відбувається за допомогою дробової кристалізації після реакції нітрування.
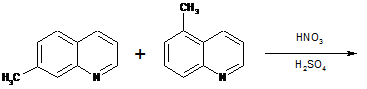

Текст
Реферат: UA 84756 U UA 84756 U 5 10 15 20 25 30 35 40 45 Корисна модель належить до органічної хімії та може бути використана для отримання ізомерних 5-метил-8-нітрохіноліну та 7-метил-8-нітрохіноліну, які є цінними вихідними сполуками для отримання речовин з високою фунгіцидною активністю та цінними електролюмінесцентними властивостями, які можуть знайти застосування в агрохімічній та електронній галузях промисловості. Зазвичай ці сполуки легко синтезуються нітруванням індивідуальних ізомерно чистих 5метилхіноліну та 7-метилхіноліну [Claret P.Α., Osborne A.G. Synthesis and nitration of 7 alkylquinolines // Tetrahedron.-1977. - Vol. 33, № 14. - P. 1465-1467.], але проблема полягає саме в отриманні останніх у чистому вигляді. Справа у тому, що обидві сполуки одночасно утворюються у співвідношенні, як правило, 1:4 при взаємодії 3-амінотолуену з гліцерином в умовах реакції Скраупа, але їх розділення є дуже важкою задачею. Через те, що ізомерні метилхіноліни мають дуже близькі температури кипіння, їх неможливо розділити дистиляцією. Досягнутий рівень розвитку в даній галузі характеризується наступними прикладами. Відомий спосіб отримання 5-метил-8-нітрохіноліну та 7-метил-8-нітрохіноліну, який полягає у введенні у реакцію Скраупа з гліцерином, відповідно, 5-метил-2-нітрофеніламіну та 3-метил-2нітрофеніламіну [Capps J.D. Some derivatives of 7-Methylquinoline // J. Amer.Chem. Soc., 1947. Vol. 69, № 1. - P. 179-181.]. Недоліками цього способу окрім невисоких виходів є необхідність використання як окислювача дуже отруйного оксиду арсену (V) та складність синтезу вихідних ізомерних 5-та 3-метилфеніламінів, що значно збільшує собівартість цільових продуктів. Відомий спосіб, вибраний як найближчий аналог, який полягає спочатку в розділенні дробовою кристалізацією суміші сульфатів 5-метил- та 7-метилхінолінів, їх пікратів або хлорплатинатів, причому виділити з суміші мінорний 5-метилхінолін значно важче, ніж його ізомер-7-метилхінолін, якого у суміші приблизно 80 % [Родионов В.Μ., Беркенгейм М.А. Синтез Βz-хинолинальдегидов // Журн. общей химии.-1944. - Т. 14, № 4-5. - С. 330-336, Palmer M.H. 710. The Scraup reaction. Formation of 5-and 7-substituted quinolines // J. Chem. Soc.-1962. - P. 3645-3652.]. Це знаходить певне відображення у цінах цих ізомерів: вартість 5-метилхіноліну (CAS 7761-55-44) та 7-метилхіноліну (CAS 612-60-2) сягає відповідно 250 та 80 доларів США за 1 г сполуки з чистотою 95 % [Ark Pharm. Ink (Chicago, USA), Bepharm (Shanghai, China)]. На другій стадії процесу ізомерно чисті 5-метилхіноліну та 7-метилхіноліну легко нітруються з одержанням цільових 5-метил-8-нітрохіноліну та 7-метил-8-нітрохіноліну. Отже недоліком методу прямого нітрування ізомерно чистих 5-метилхіноліну та 7-метилхіноліну є дуже висока вартість вихідних сполук. В основу корисної моделі поставлена задача розробки нового способу одержання 5-метил8-нітрохіноліну та 7-метил-8-нітрохіноліну без необхідності використання ізомерно чистих вихідних сполук - 5-метилхіноліну та 7-метилхіноліну, що значно здешевлює цільові продукти. Поставлена задача вирішується за рахунок способу отримання чистих ізомерних 5-та 7метил-8-нітрохінолінів, який полягає у розділенні суміші ізомерних 5- та 7-метил-8нітрохінолінів, що отримані нітруванням відповідних 5- та 7-метил-хінолінів, згідно з корисною моделлю, розділення ізомерів відбувається за допомогою дробової кристалізації після реакції нітрування. Пропонований спосіб здійснюється наступним чином. До суміші 5-метилхіноліну та 7-метилхіноліну (~1:1), що отримана після реакції Скраупа між 3-амінотолуеном та гліцерином, після виділення з неї більшої частини чистого 7-метилхіноліну, додають "нітруючу суміш" (HNO3+H2SO4), внаслідок чого утворюється суміш 5-метил-8нітрохіноліну та 7-метил-8-ні-трохіноліну (~1:1) з незначною домішкою 5-метил-6-нітрохіноліну. CH3 HNO3 + H3C H2SO4 N N CH3 + H3C N N O N O O N O 1 UA 84756 U 5 10 15 20 25 30 35 40 45 50 55 Після проведення декількох послідовних кристалізацій з оцтової кислоти та етилового спирту ця суміш досить легко розділяється на індивідуальні ізомери, на відміну від вихідних ізомерних 5- та 7-метилхіноліпів. Причинно-наслідковий зв'язок між сукупністю ознак, що заявляються, та технічним результатом полягає у наступному - запропонований спосіб здійснення реакції нітрування суміші 5-та 7-метилхінолінів, збагаченої 5-ізомером, дозволяє отримувати суміш 5-метил-8нітрохіноліну та 7-метил-8-нітрохіноліну, яка досить легко розділяється на індивідуальні ізомери шляхом послідовних кристалізацій з оцтової кислоти та етилового спирту. Отримання ізомерних 5-метил-8-нітрохіноліну та 7-метил-8-нітрохіноліну запропонованим способом ілюструється наступним прикладом. Структура отриманих сполук підтверджується дослідженнями отриманих зразків різними фізико-хімічними методами проведеними у Одеському національному університеті імені І.І. Мечникова. Приклад 1. а) Нітрування суміші 5- та 7-метилхінолінів. Суміш 82 г (0,57 моль) 5- та 7метилхінолінів (~50:50 %) (отриману по реакції Скраупа між 3-амінотолуеном та гліцерином [Bradford L., Elliot T.J., Rowe F.M. The Skraup reaction with m-substituted anilines // J. Chem. Soc.1947. - P. 437-445.] після виділення з неї більшої частини 7-метилхіноліну) при інтенсивному перемішуванні та охолодженні крижаною водою обережно додавали до 225 мл концентрованої сірчаної кислоти (d=1,84) з такою швидкістю, щоб температура не перевищувала 40 °C, потім охолоджували до 20 °C та трьома порціями додавали суміш 42 мл (0,68 моль) 72 % азотної кислоти та 65 мл концентрованої сірчаної кислоти, підтримуючи температуру не вище 35 °C. Перемішування продовжували ще 3 години, потім нагрівали на киплячій водяній бані 1 годину та охолоджували до кімнатної температури. Реакційну суміш виливали на 1 кг колотого льоду, розбавляли крижаною водою до об'єму 5 л та нейтралізували 10 % розчином NaOH до рН 4. Осад, який випадав, через 1 год. відфільтровували, промивали водою та сушили на повітрі. Вихід 81-83 г (~76 %) суміші 5-метил- та 7-метил-8-нітрохінолінів. В маточному розчині залишалася невелика кількість 5-метил-8-нітрохіноліну та основна маса 5-метил-6нітрохіноліну, тому не потрібно нейтралізувати реакційну суміш до рН вище, ніж 4. б) Розділення суміші 5- та 7-метил-8-нітрохінолінів. Отриману суміш 5- та 7-метилхінолінів (82 г) розчиняли у 200 мл гарячої оцтової кислоти (крижаної), фільтрували та залишали на ніч. Осад, який випадав, знову розчиняли в 60 мл оцтової кислоті, залишали на піч, фільтрували та промивали 20 мл крижаної оцтової кислоти і потім 100 мл гарячої води (70 °C). Отримували 7метил-8-нітрохінолін забруднений невеликою кількістю червоного барвника. Цю речовину розчиняли у 15 л 20 % оцтової кислоти, додавали 40 г активованого вугілля, кип'ятили І год., фільтрували, охолоджували до 5 °C, осад, який випадав, відфільтровували та отримували 33-37 і- 7-метил-8-нітрохіноліну з Τ пл. 186-188 °C. Літ. Τ пл. 188 °C [Claret Ρ.Α., Osborne A.G. Synthesis and nitration of 7 alkylquinolines // Tetrahedron.-1977. - Vol. 33, № 14. - P. 1465-1467.]. Аналіз вмісту азоту, вуглецю та водню проводили з використанням елементного CHNаналізатору. Знайдено, %: С 64,12; Н 4,53; N 14,58. C10H8N2O2 Розраховано, %: С 63,82; Η 4,28; + Ν 14,89. Мас-спектр, m/z (відн. інт.) 188.0583 (100, Μ ), 171(46), 158(24), 143(20), 142(52), 141(37), 130(29), 129(15), 116(25), 115(29), 77(14), 63(13). Спектр ПМР, δ, м. д.: 8,95 д (1 Η, J23 3,2 Гц, H-2хінолін), 8,50 д (1Η, J34 8,4 Гц, Н-4хінолін), 8,12 д (1Η, J56 8,4 Гц, Н-5хінолін), 7.66 м (2Н, Н3,6хінолін), 2,48 с (3H, СН3). Оцтові маточники після виділення 7-метил-8-нітрохіноліну об'єднували, упарювали до об'єму 60 мл та кристалізували з 10 л 10 % оцтової кислоти з додаванням 40 г активованого вугілля. Вихід 35-38 г 5-метил-8-нітрохіноліну з домішкою 7-метил-8-нітрохіноліну. Цю речовину кристалізували з етанолу (~100 мл). Осад, який був чистим 5-метил-8-нітрохіноліном промивали етанолом, водою та сушили на повітрі. Вихід 32-33 г, Τ пл. 136 °C. Літ. Τ пл. 138 °C [Manske R.H.F., Marion L., Leger F. The synthesis and the characterization of the monomethyl-and dimethylquinolines // Can. J. Res.-1942. - Vol. 20B, № 1. - P. 133-152.]. Знайдено, %: С 63,61; Η 4,43; Ν 14,71. C10H8N2O2 Розраховано, %: С 63,82; Η 4,28; Ν 14,89. Мас-спектр, m/z (відн. інт.) 188.0589 + (54, Μ ), 158(35), 142(23), 141(14), 140(20), 130(100), 116(20), 115(46), 103(15), 89(16), 77(19), 63(20). Спектр ПМР, δ, м. д.: 9,01 д (1Н, J23 0,2 Гц, Н-2хінолін), 8,57 д (1Η, J34, 8,8 Гц, H-4хінолін), 8,06 д (1Η, J67 7,2 Гц, Н-7хінолін), 7,70 дд (1Η, J23 4,0 Гц, J34, 7,2 Гц Н-3хінолін), 7,55 д (1Η, J76 7,8 Гц, Н6хінолін), 2,75 с (3H, СН3). Спиртовий маточник упарювали та використовували для виділення 7-метил-8-нітрохіноліну методом, описаним вище. Таким чином, наведений приклад свідчить про те, що спосіб, що заявляється, забезпечує просте отримання і розділення ізомерних 5-метил-8-нітрохіноліну та 7-метил-8-нітрохіноліну з досить високими виходами та чистотою. 60 2 UA 84756 U ФОРМУЛА КОРИСНОЇ МОДЕЛІ 5 Спосіб отримання чистих ізомерних 5- та 7-метил-8-нітрохінолінів, що полягає у розділенні суміші ізомерних 5- та 7-метил-8-нітрохінолінів, що отримані нітруванням відповідних 5- та 7метилхінолінів, який відрізняється тим, що розділення ізомерів відбувається за допомогою дробової кристалізації після реакції нітрування CH3 HNO3 + H3C H2SO4 N N CH3 + H3C N N O N O O N O . 10 Комп’ютерна верстка І. Скворцова Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 3
ДивитисяДодаткова інформація
Автори англійськоюIshkov Yurii Vasyliovych, Halkin Borys Mykolaiovych, Kyrychenko Hanna Mykhailivna, Vodzinskii Serhii Valentynovych
Автори російськоюИшков Юрий Васильевич, Галкин Борис Николаевич, Кириченко Анна Михайловна, Водзинский Сергей Валентинович
МПК / Мітки
МПК: C07D 215/18
Мітки: чистих, 7-метил-8-нітрохінолінів, спосіб, отримання, ізомерних
Код посилання
<a href="https://ua.patents.su/5-84756-sposib-otrimannya-chistikh-izomernikh-5-ta-7-metil-8-nitrokhinoliniv.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання чистих ізомерних 5- та 7-метил-8-нітрохінолінів</a>
Попередній патент: Спосіб прогнозування летального випадку у новонароджених з синдромом системної запальної відповіді, які перенесли тяжку асфіксію при народженні
Наступний патент: Голка в’язальної машини
Випадковий патент: Ортопедичний корсет









