Застосування декаметоксину як фармацевтично активної речовини для лікування шлунково-кишкового тракту та кишкових інфекцій перорально
Формула / Реферат
1. Застосування декаметоскину як фармацевтично активної речовини для лікування шлунково-кишкового тракту (ШКТ) та кишкових інфекцій перорально.
2. Застосування декаметоксину як фармацевтично активної речовини за п. 1 для лікування ШКТ та кишкових інфекцій мікробної і вірусної етіології перорально.
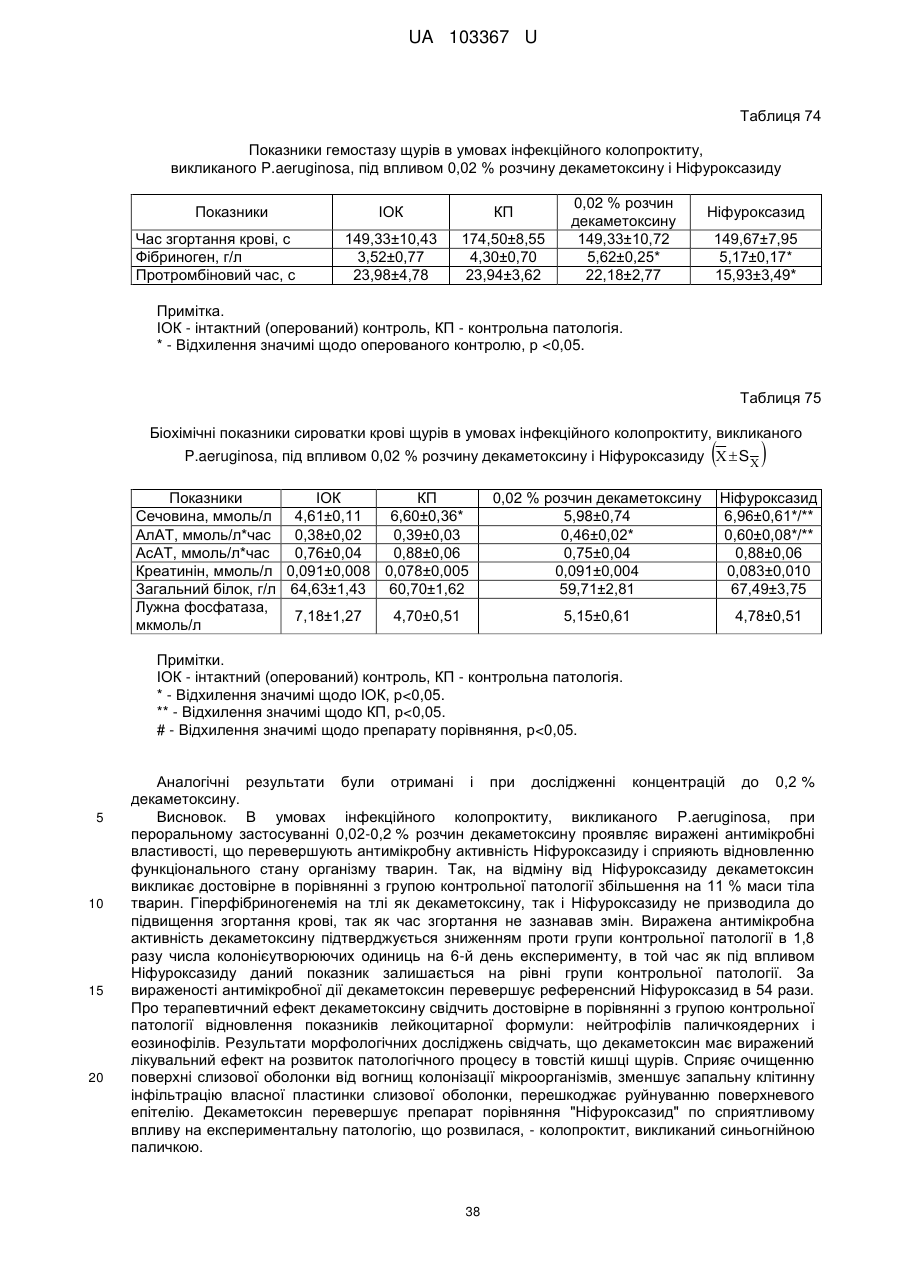
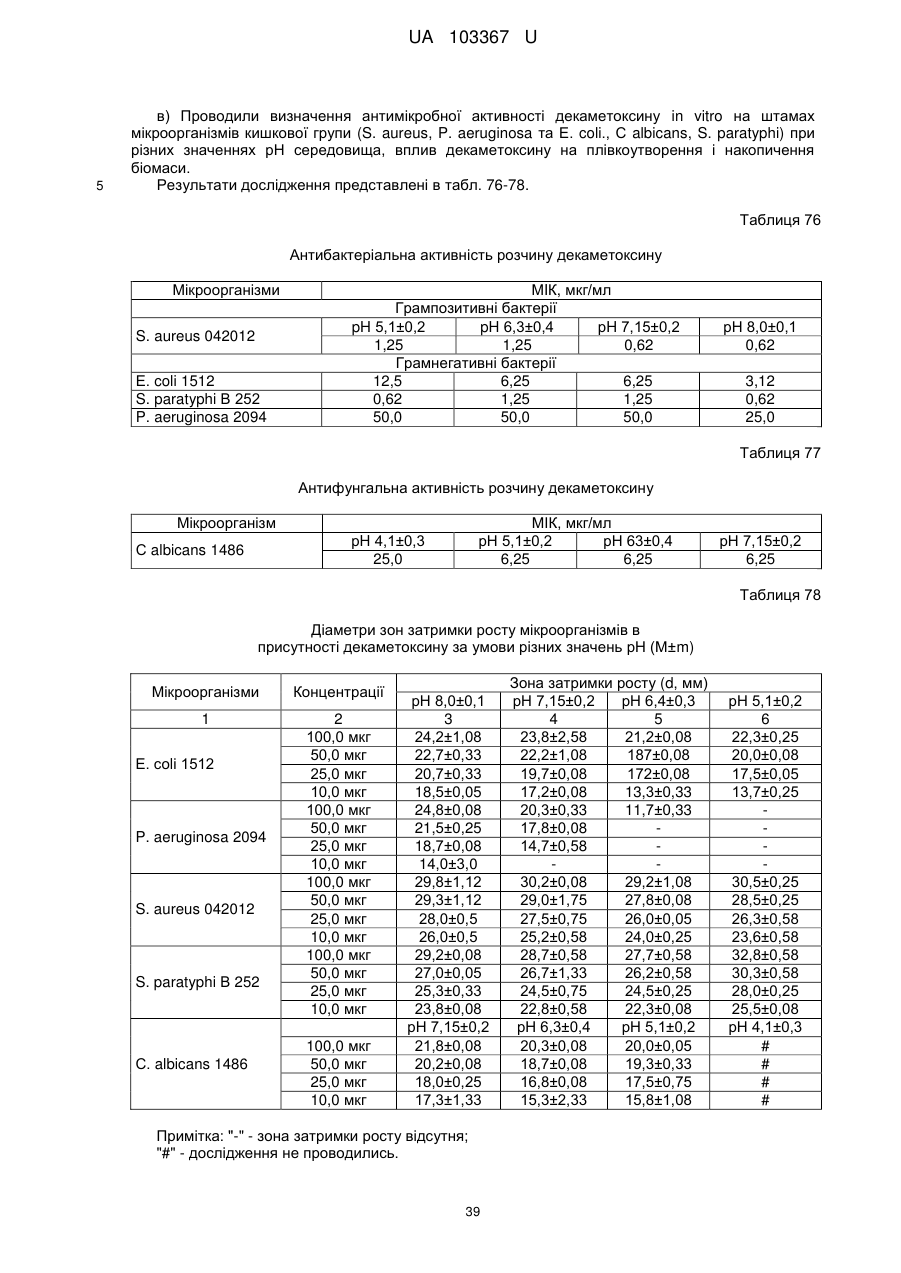
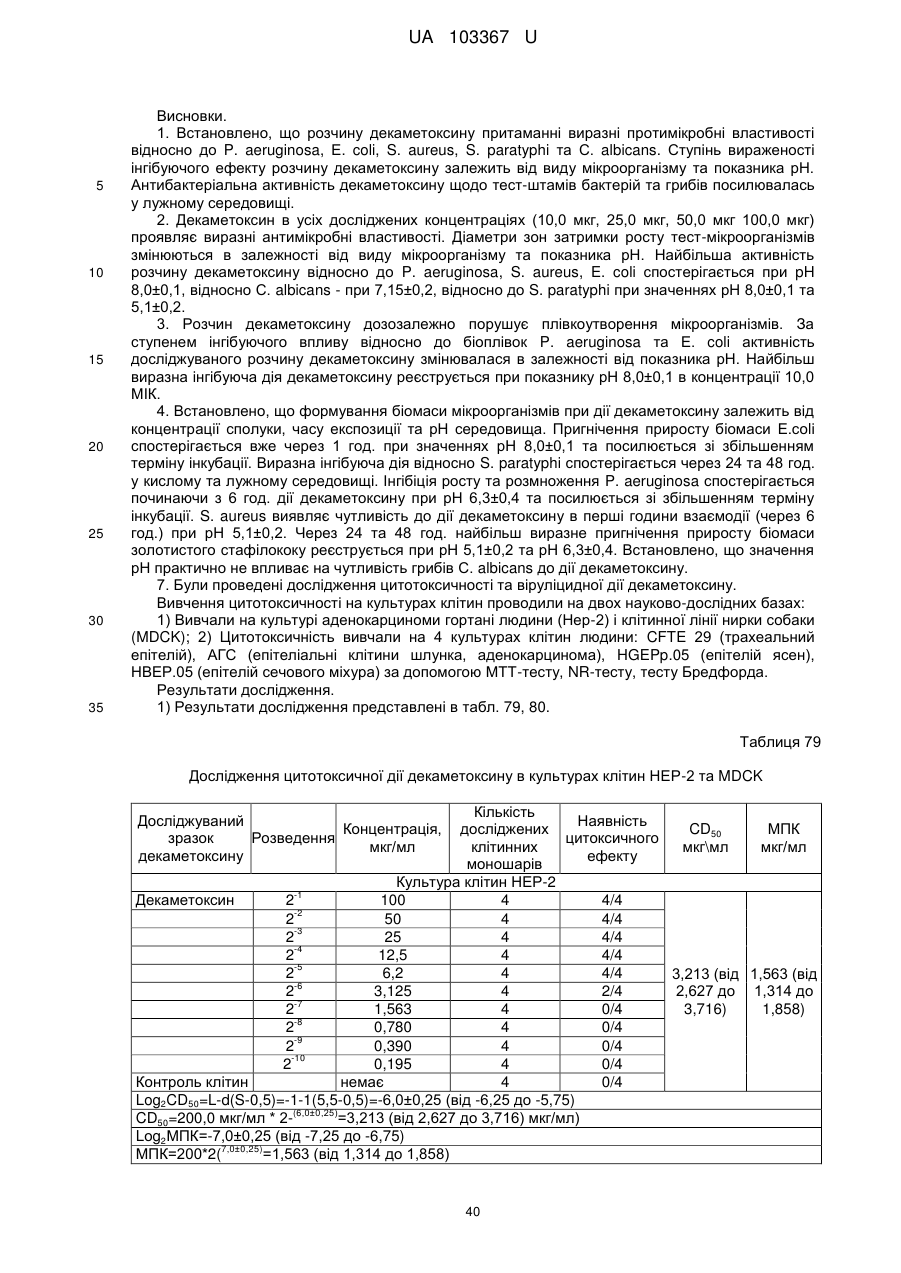
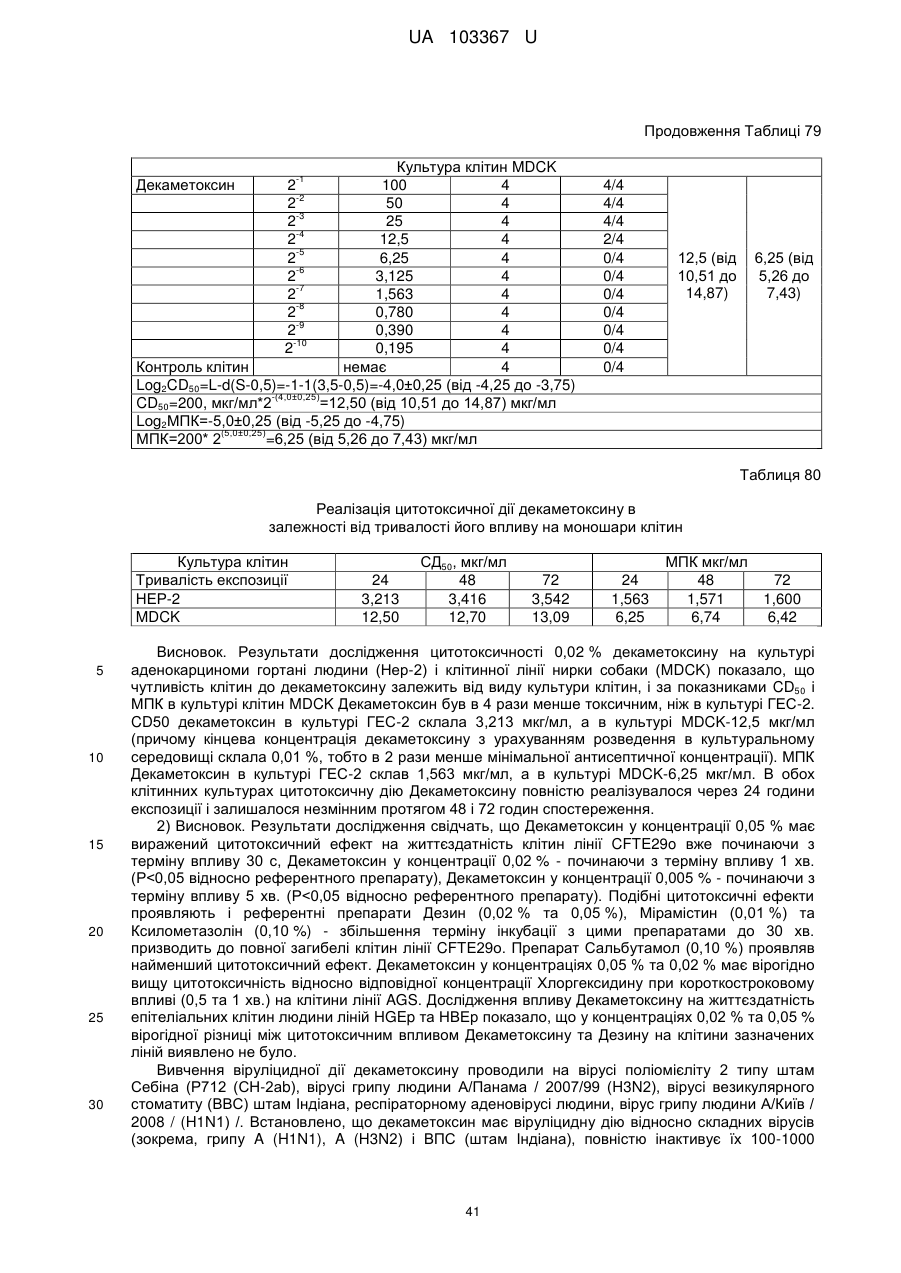
3. Застосування декаметоксину як фармацевтично активної речовини за п. 1 для лікування ШКТ та кишкових інфекцій перорально, зокрема інфекційного колопроктиту.
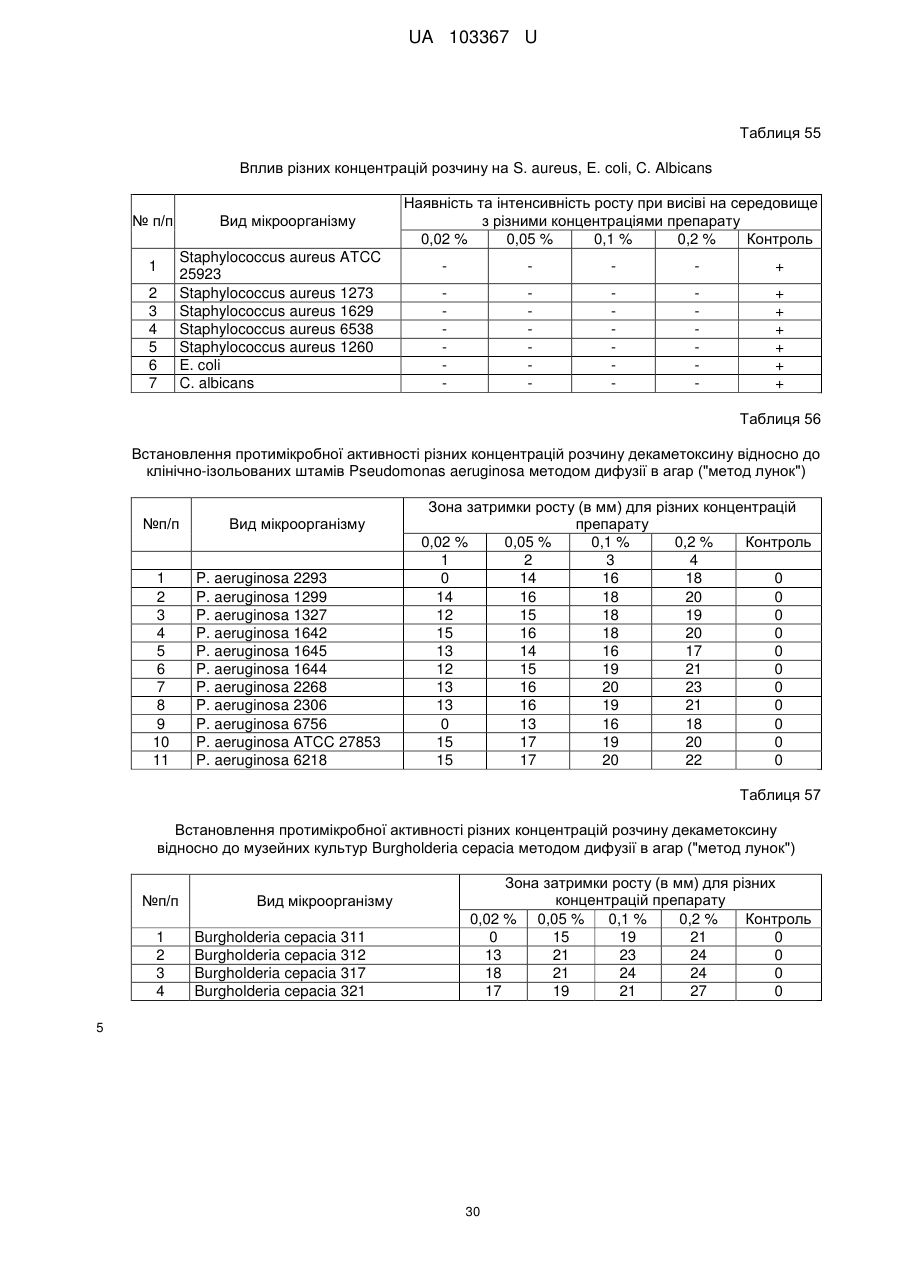
4. Застосування декаметоксину як фармацевтично активної речовини за п. 1 для лікування ШКТ та кишкових інфекцій у вигляді водного розчину з концентрацією 0,02-0,2 %.
5. Застосування декаметоксину як фармацевтично активної речовини за п. 1 для лікування ШКТ та кишкових інфекцій перорально, в складі фармацевтичних композицій.
6. Застосування декаметоксину як фармацевтично активної речовини за п. 1 для лікування ШКТ та кишкових інфекцій перорально, в складі фармацевтичних композицій рідкого типу.
Текст
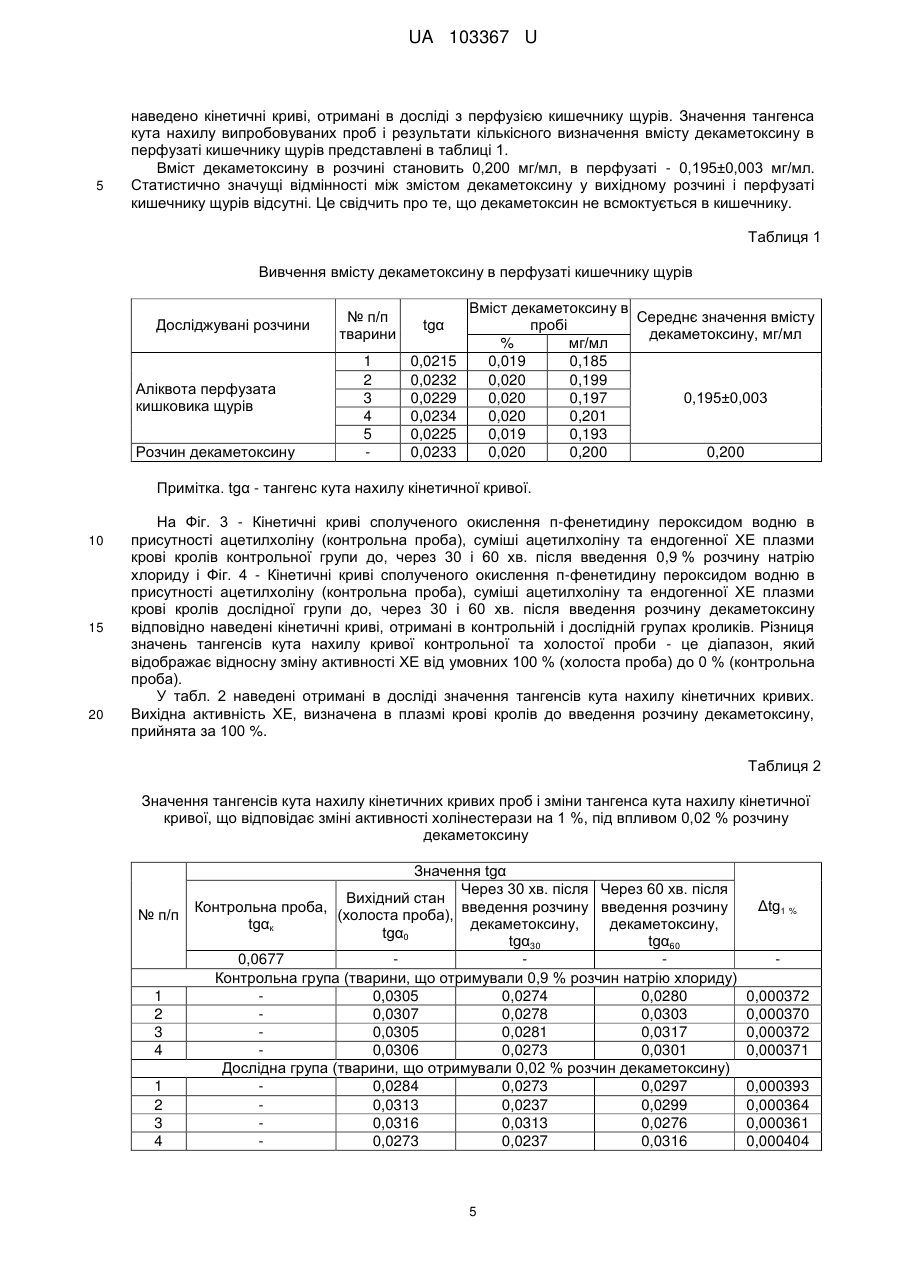
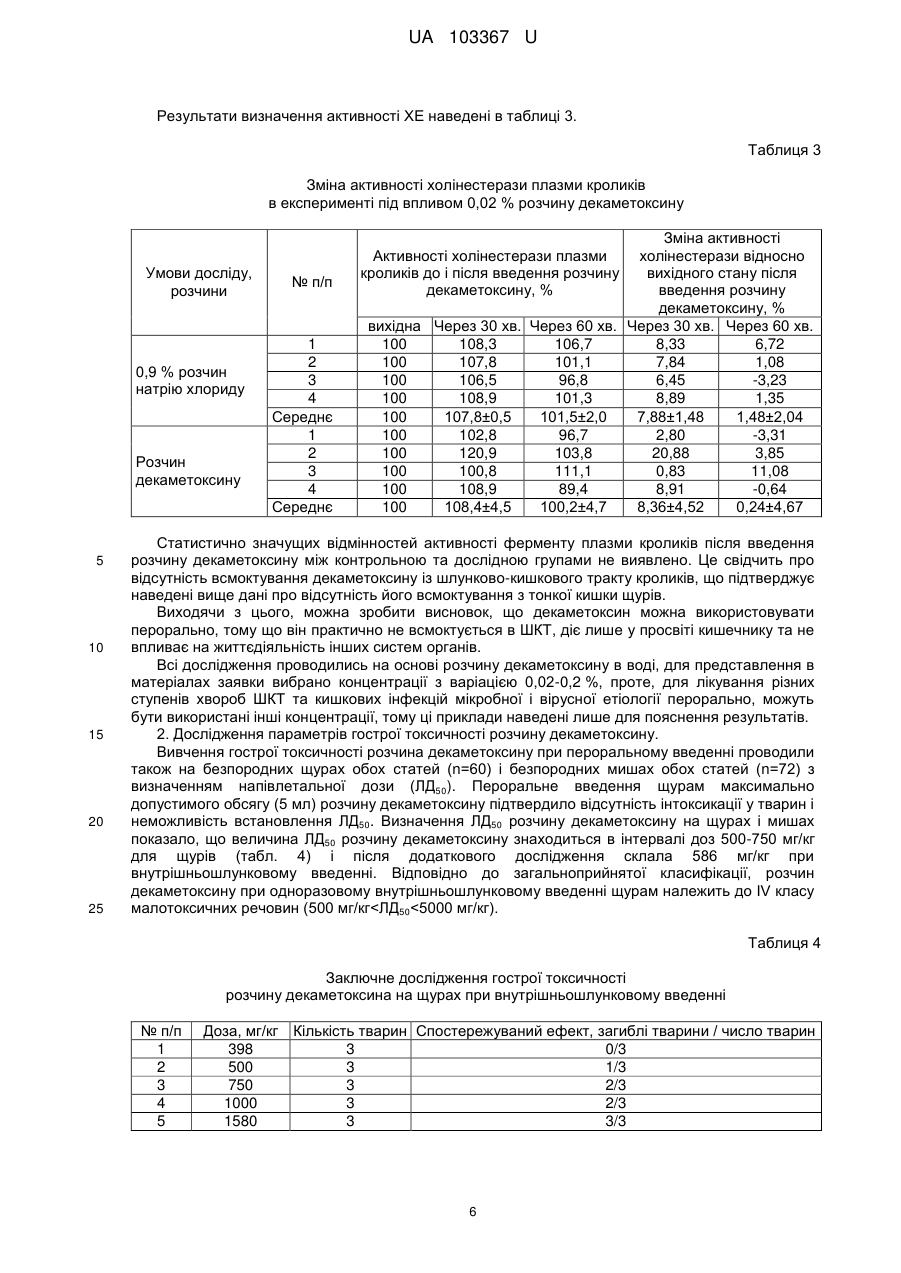
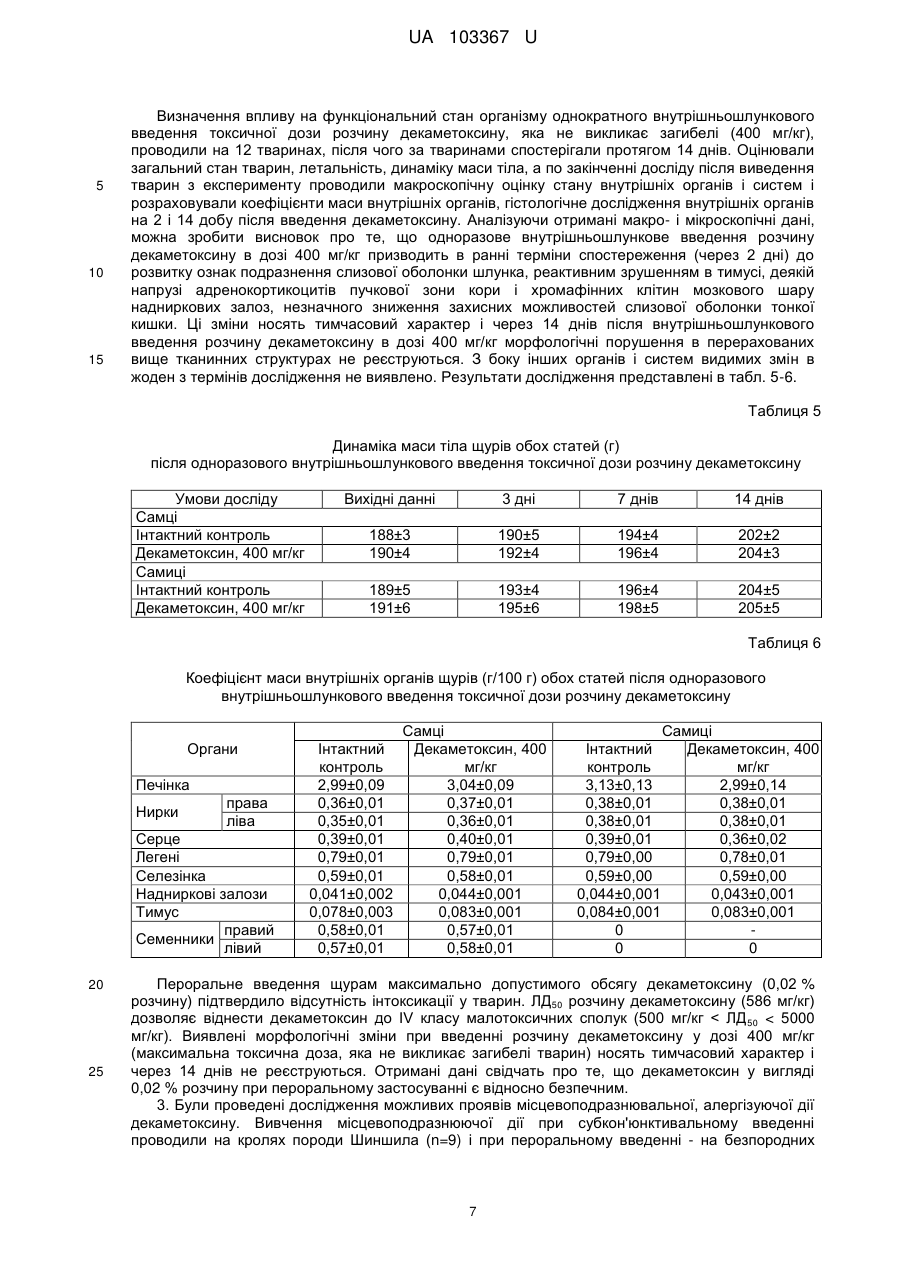
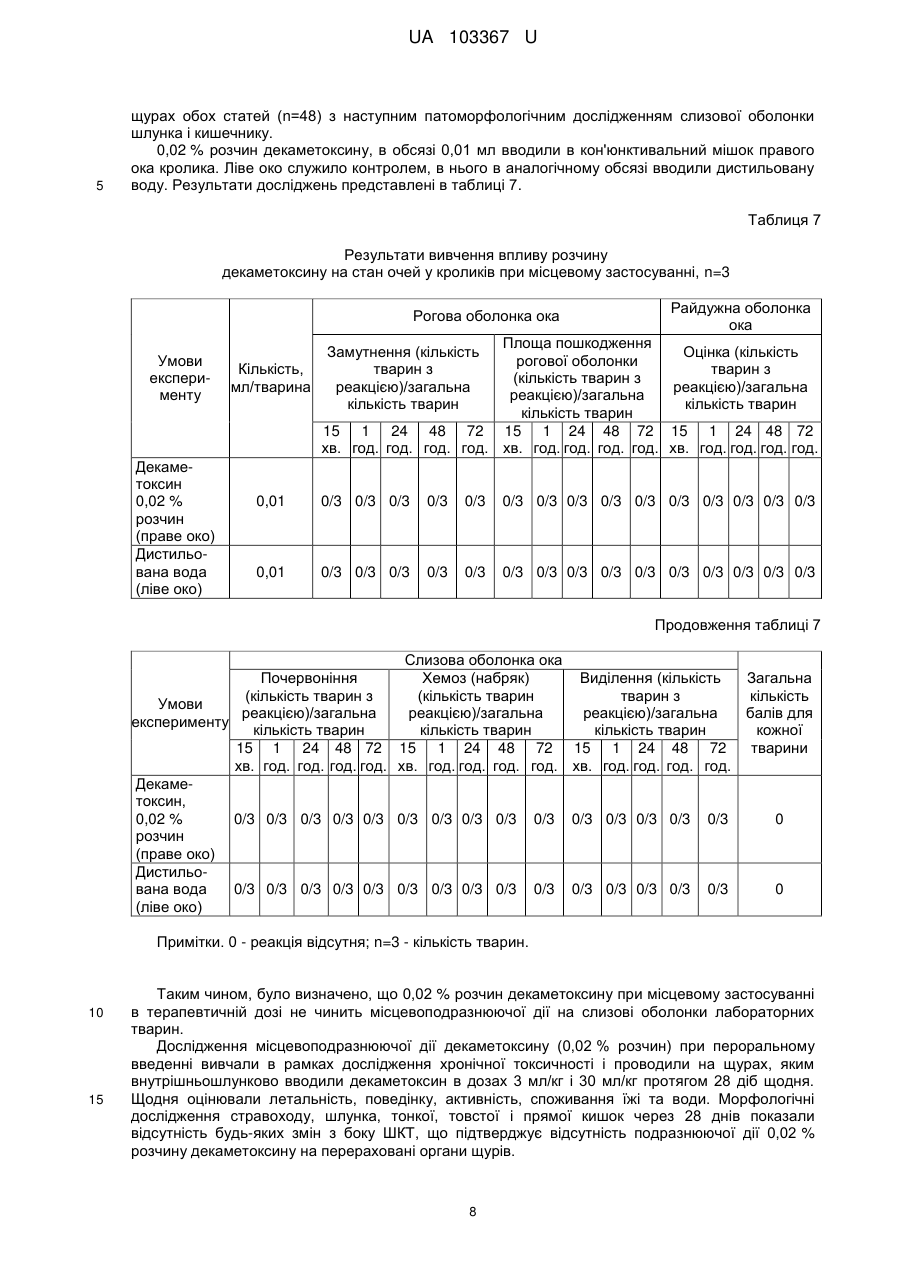
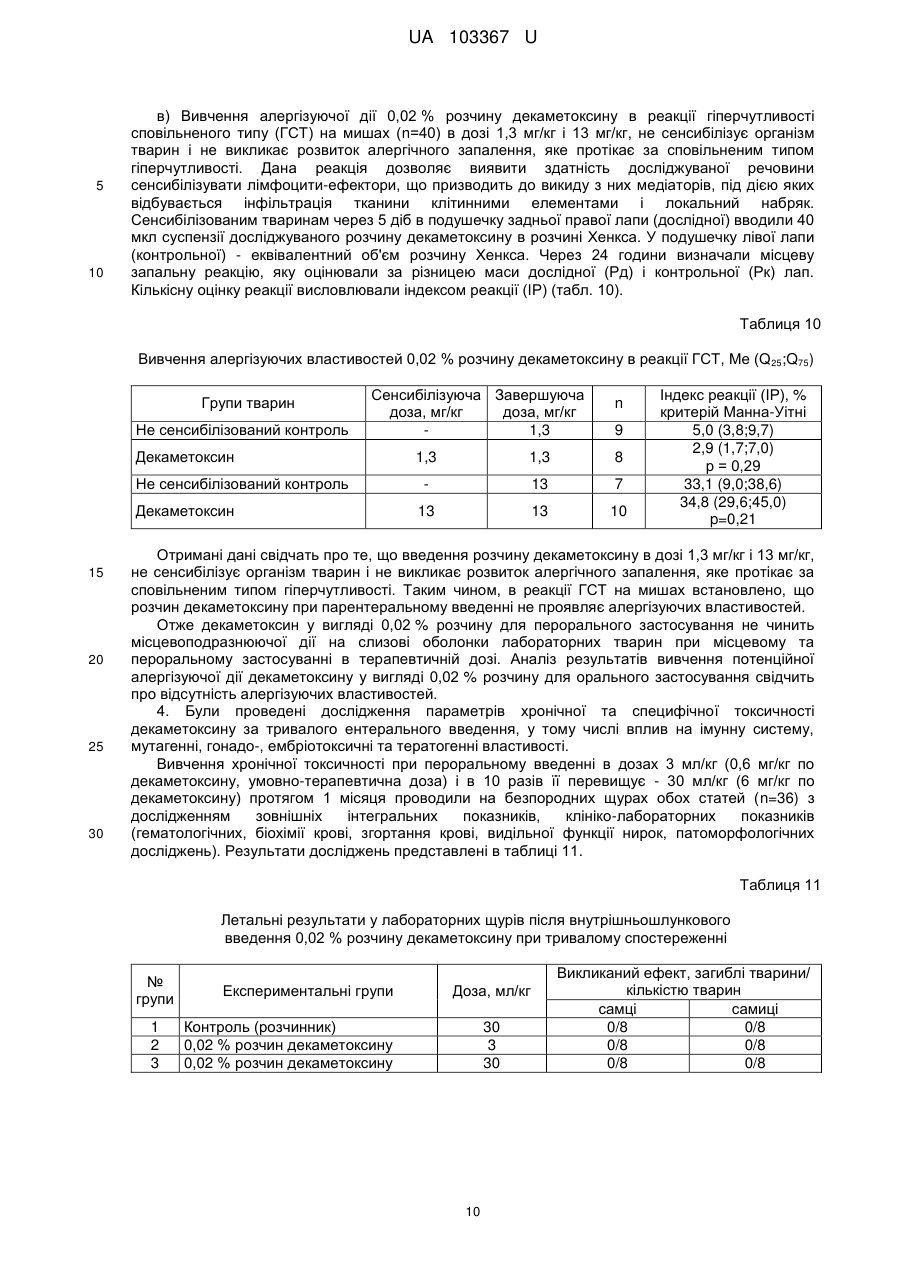
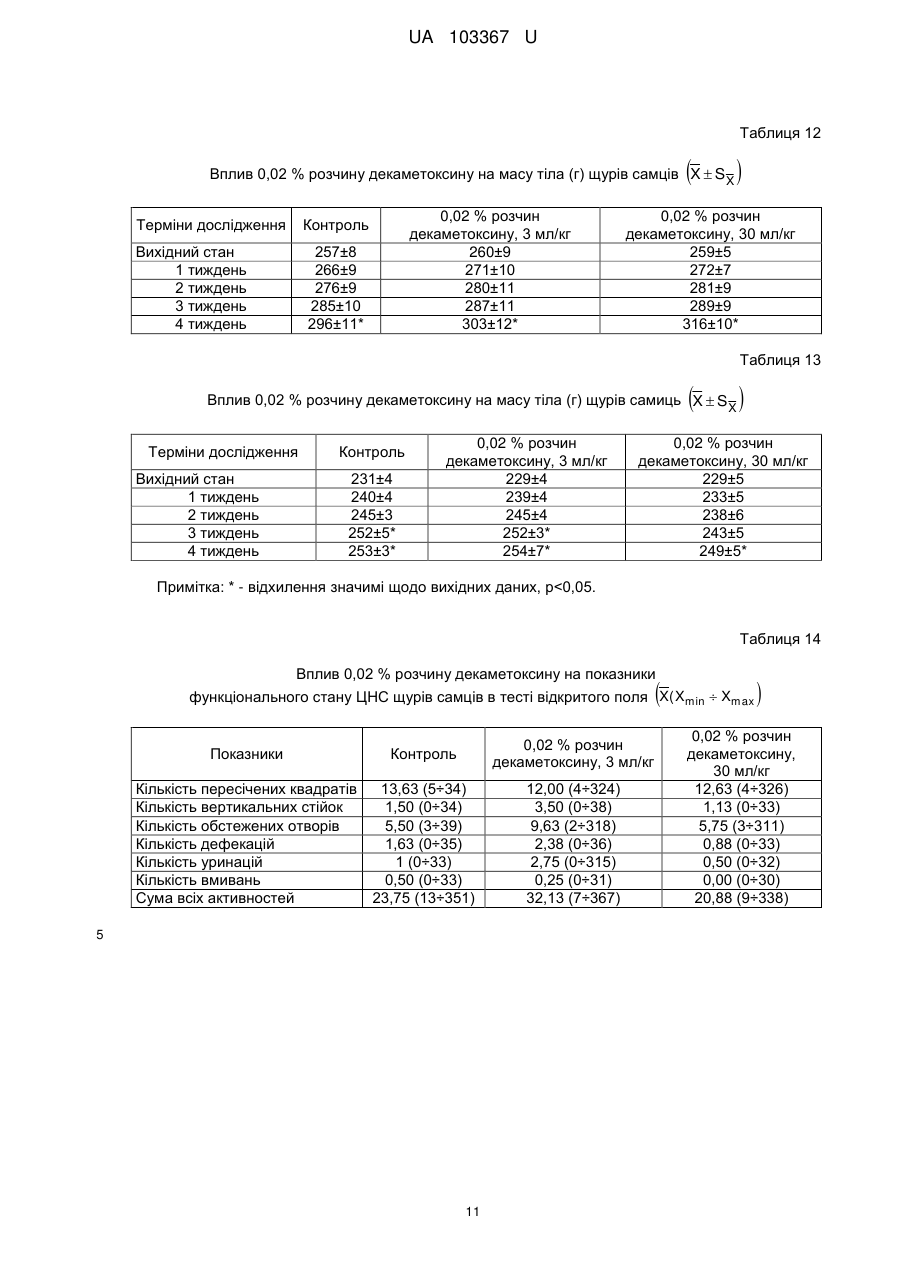
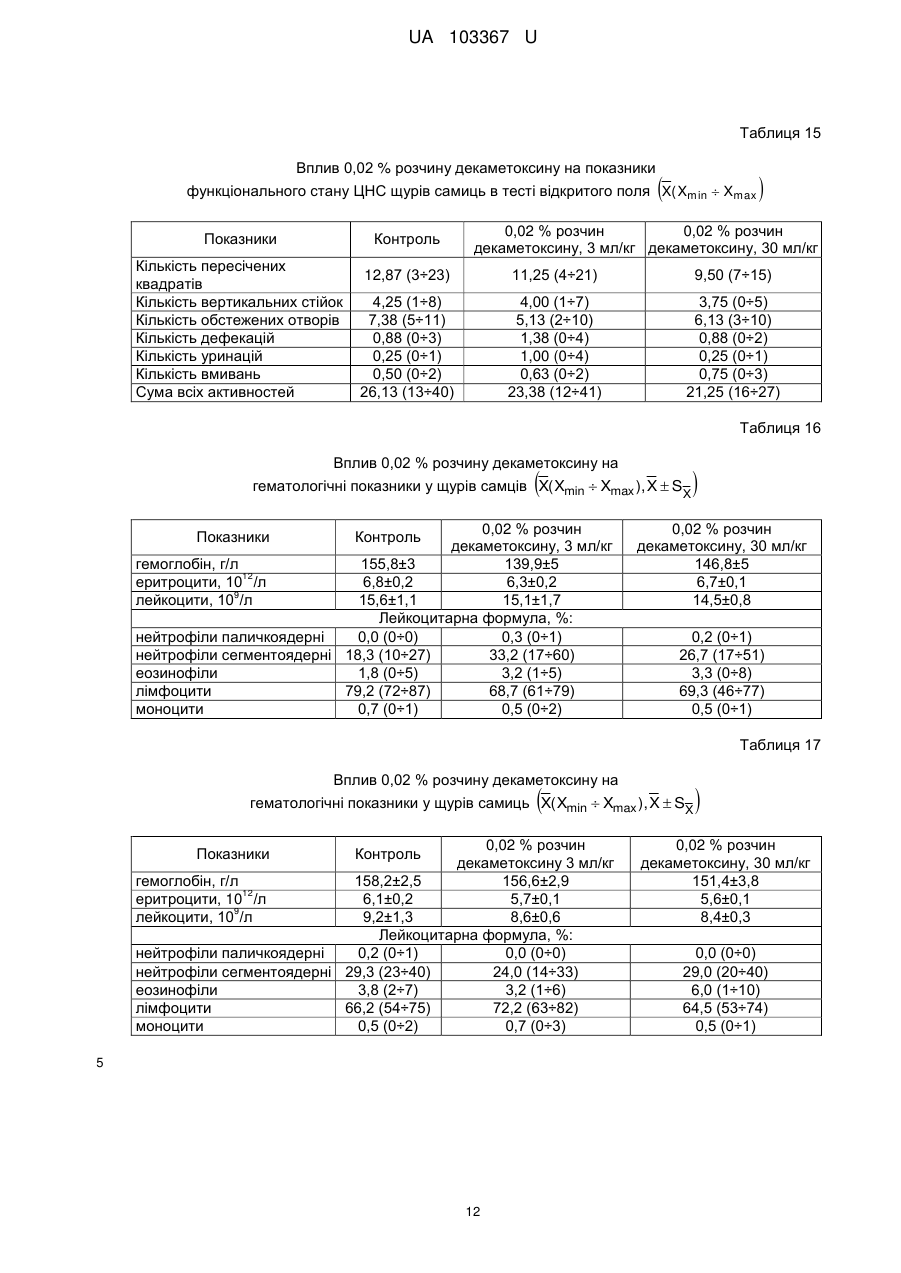
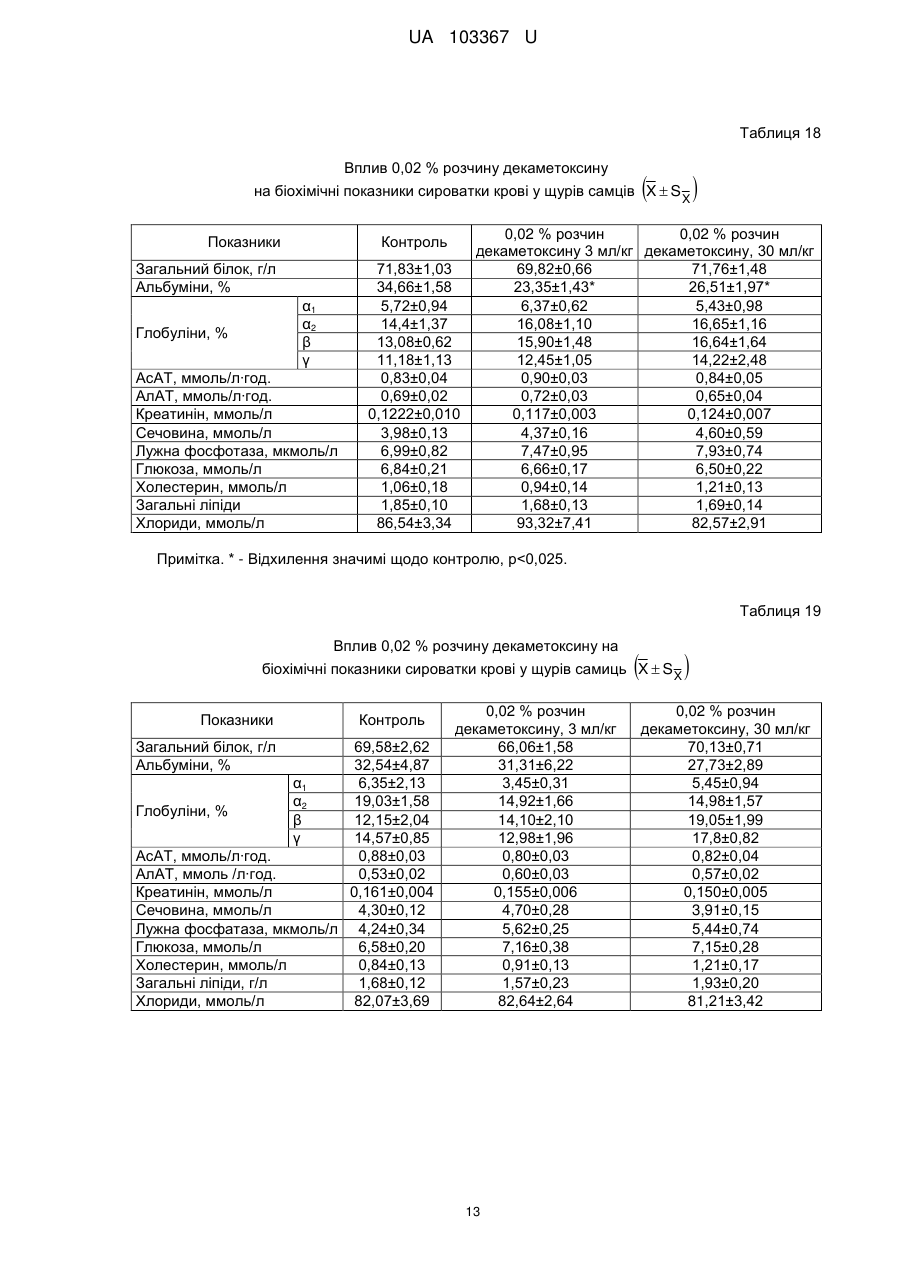
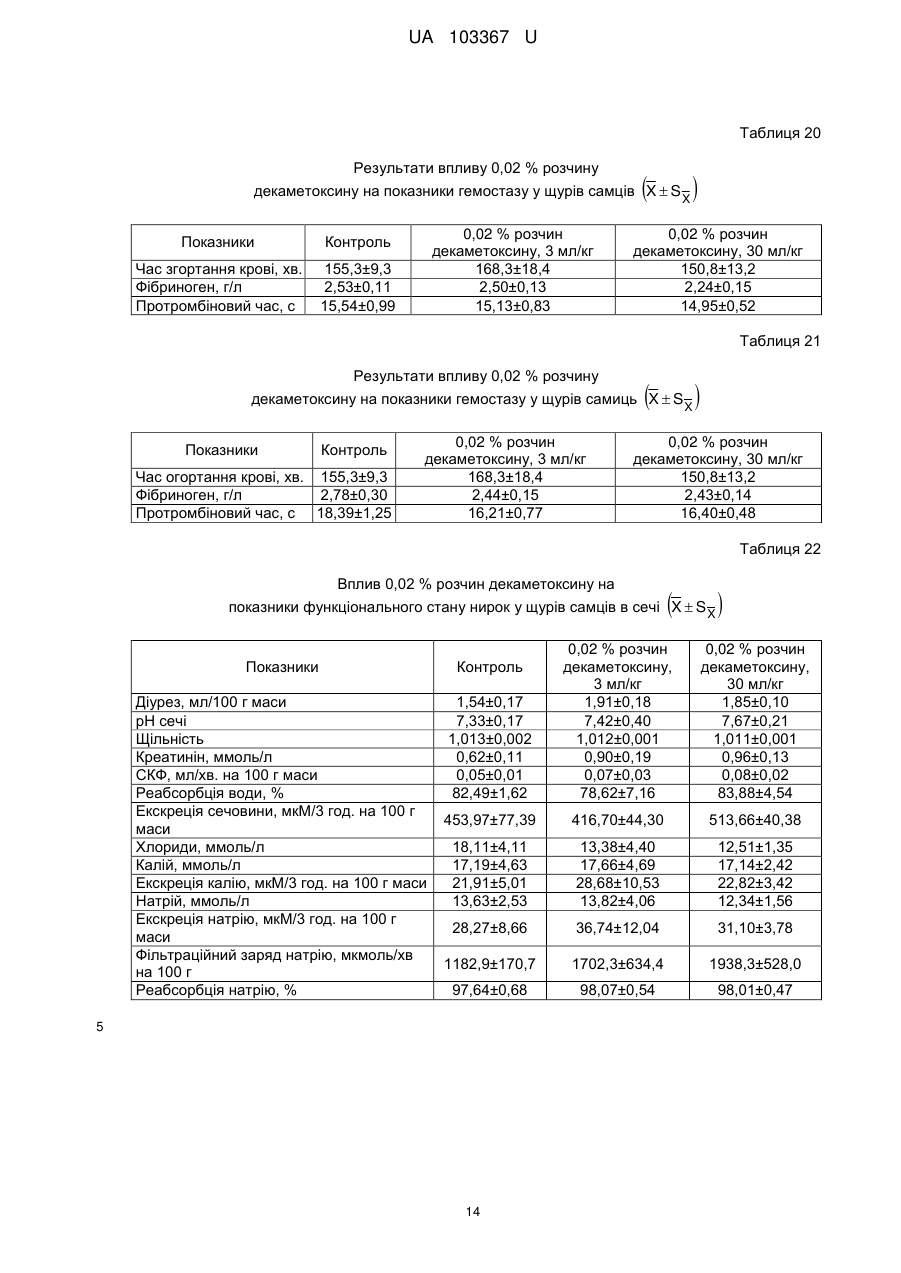
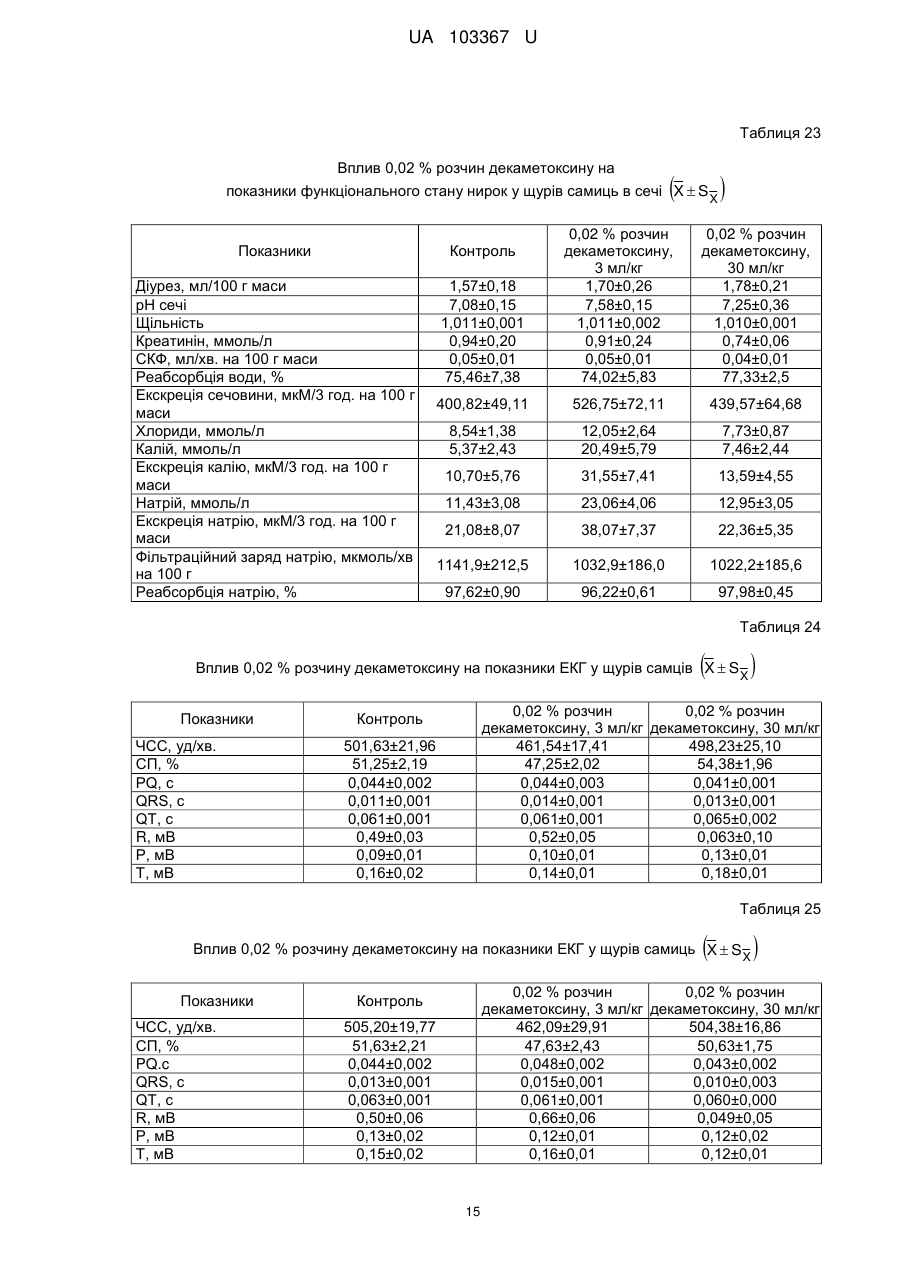
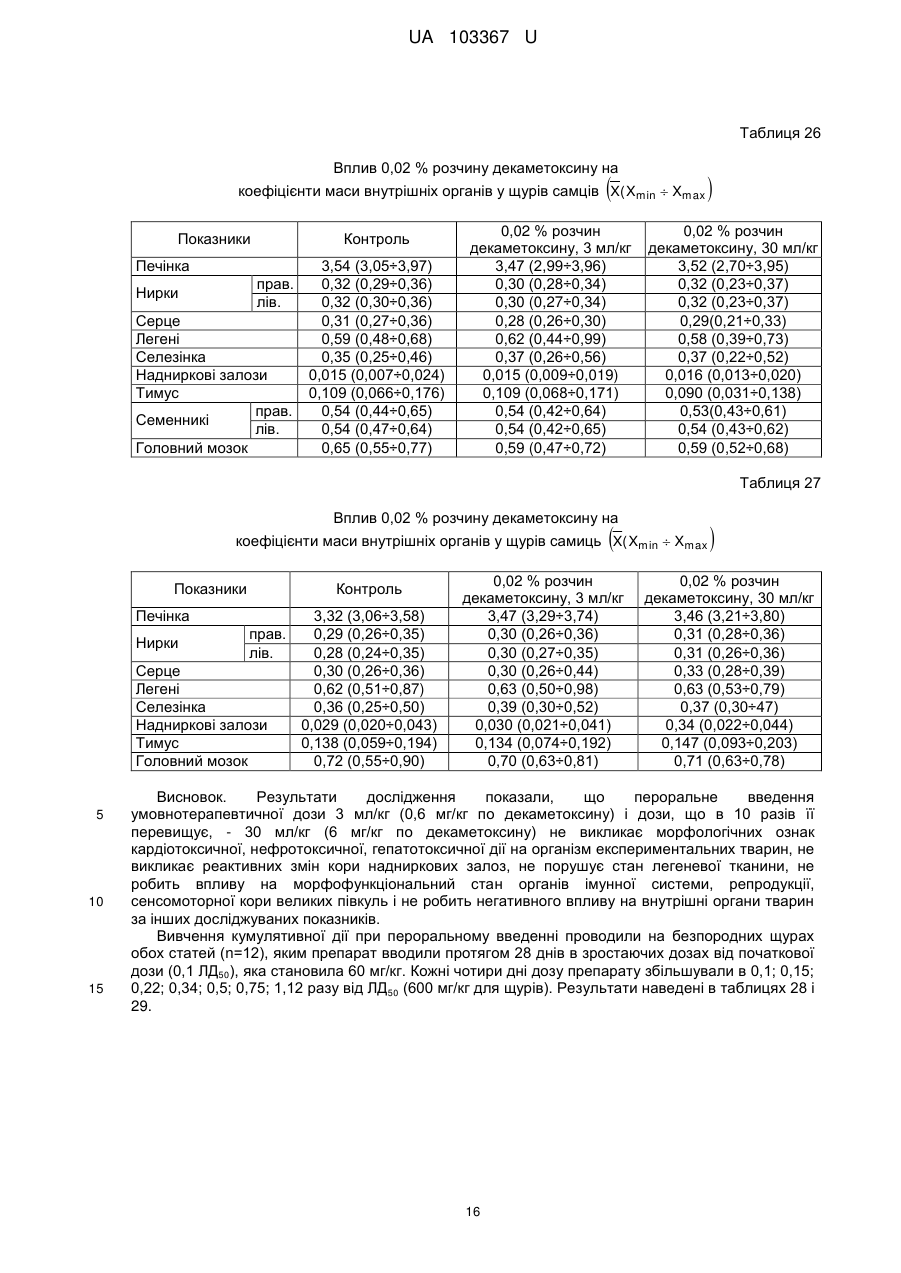
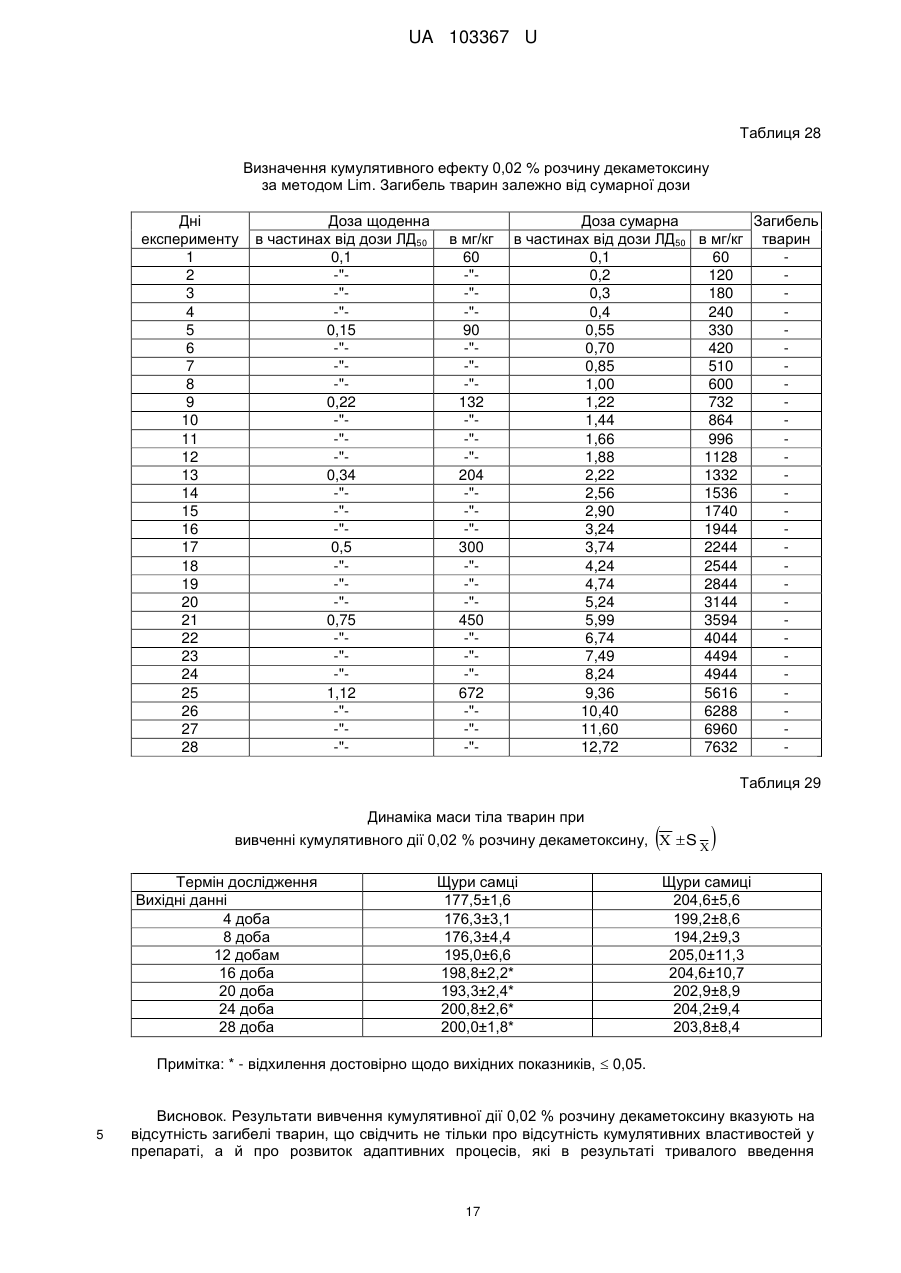
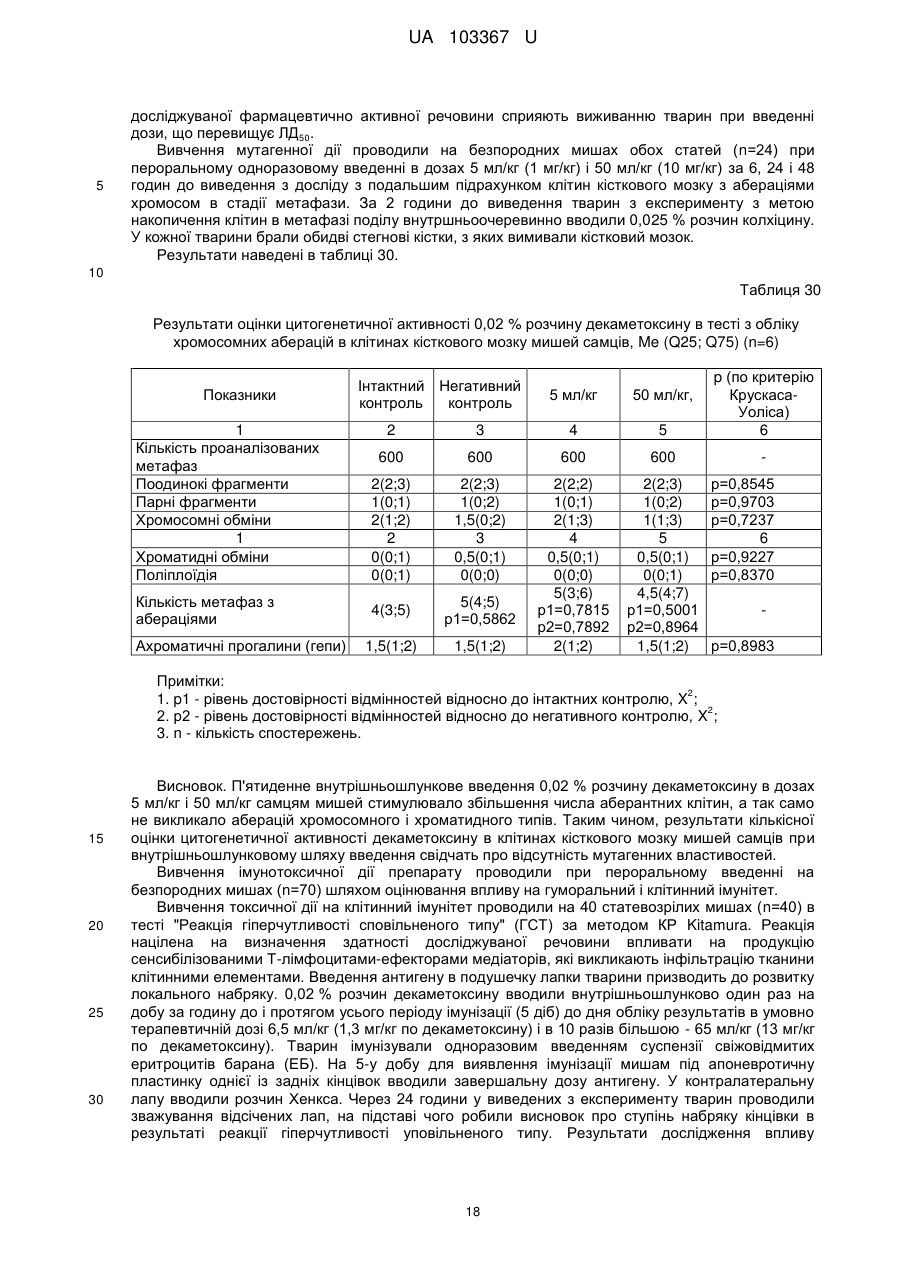
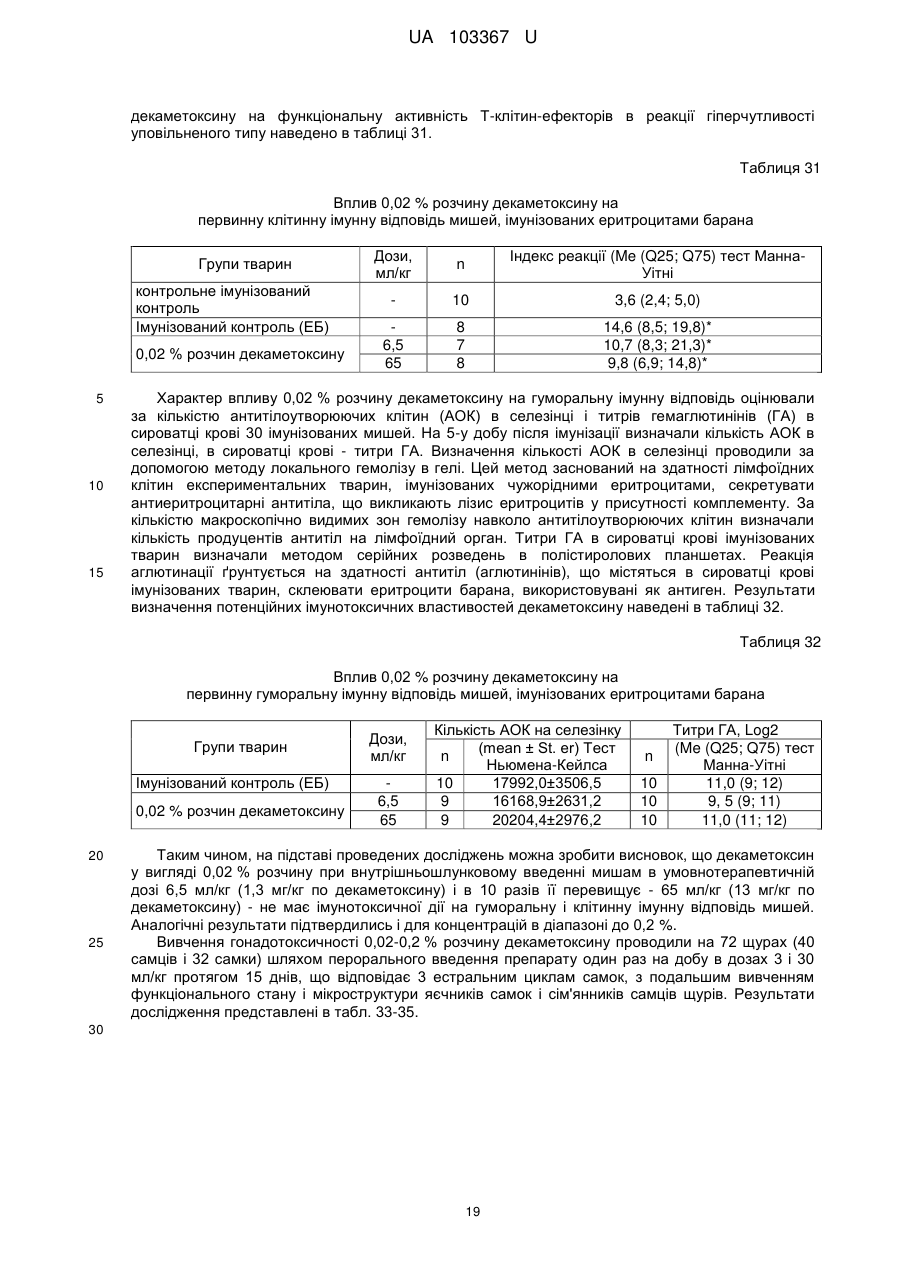
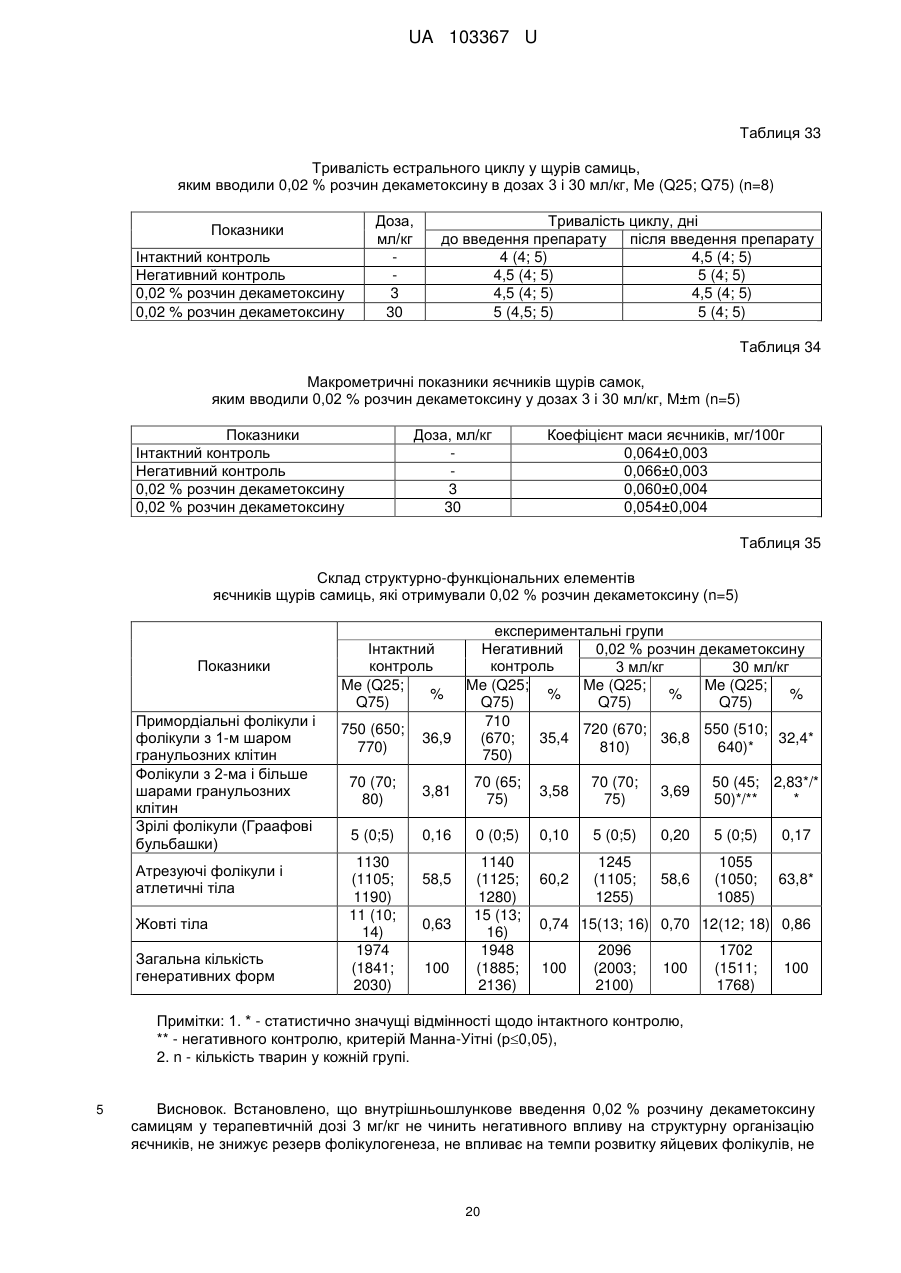
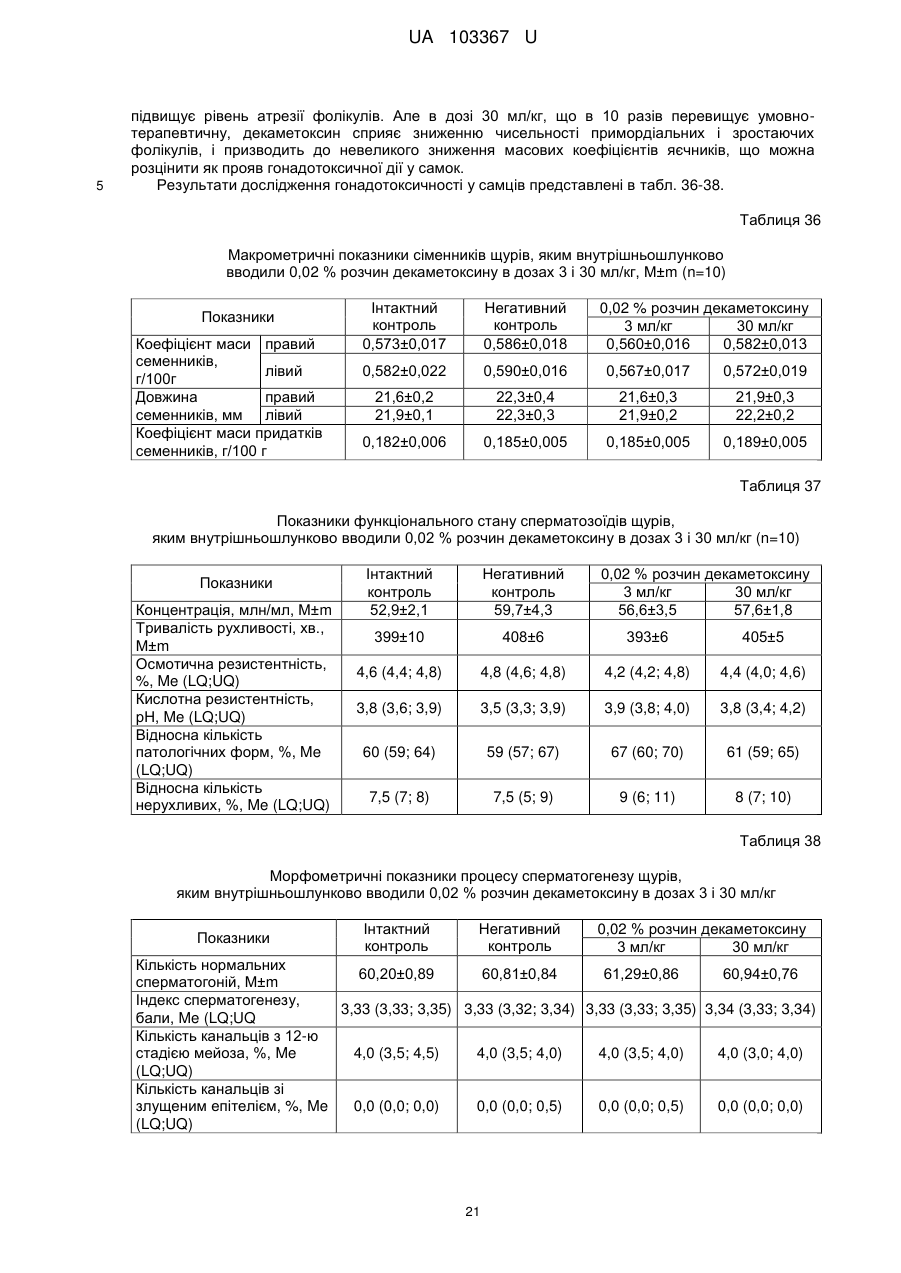
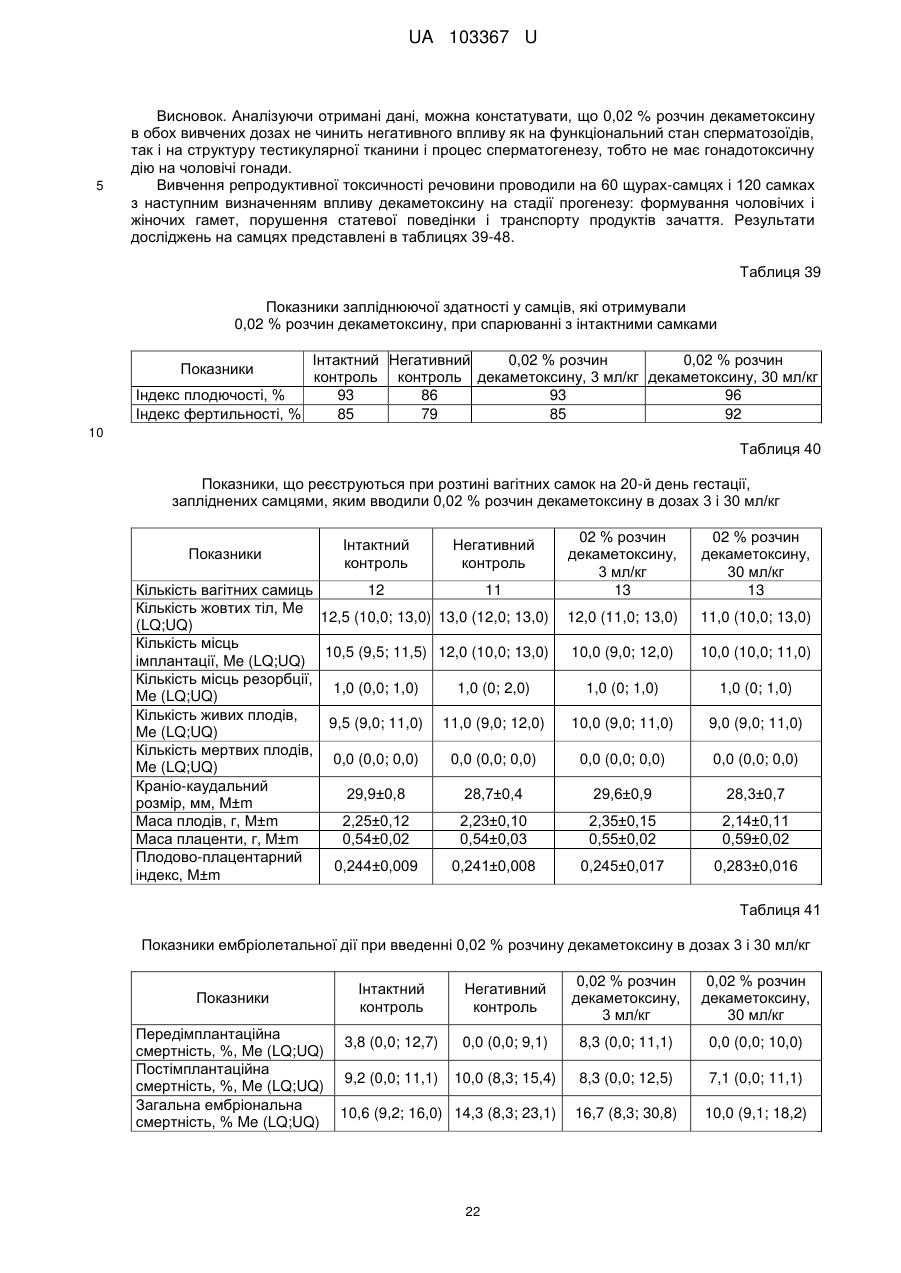
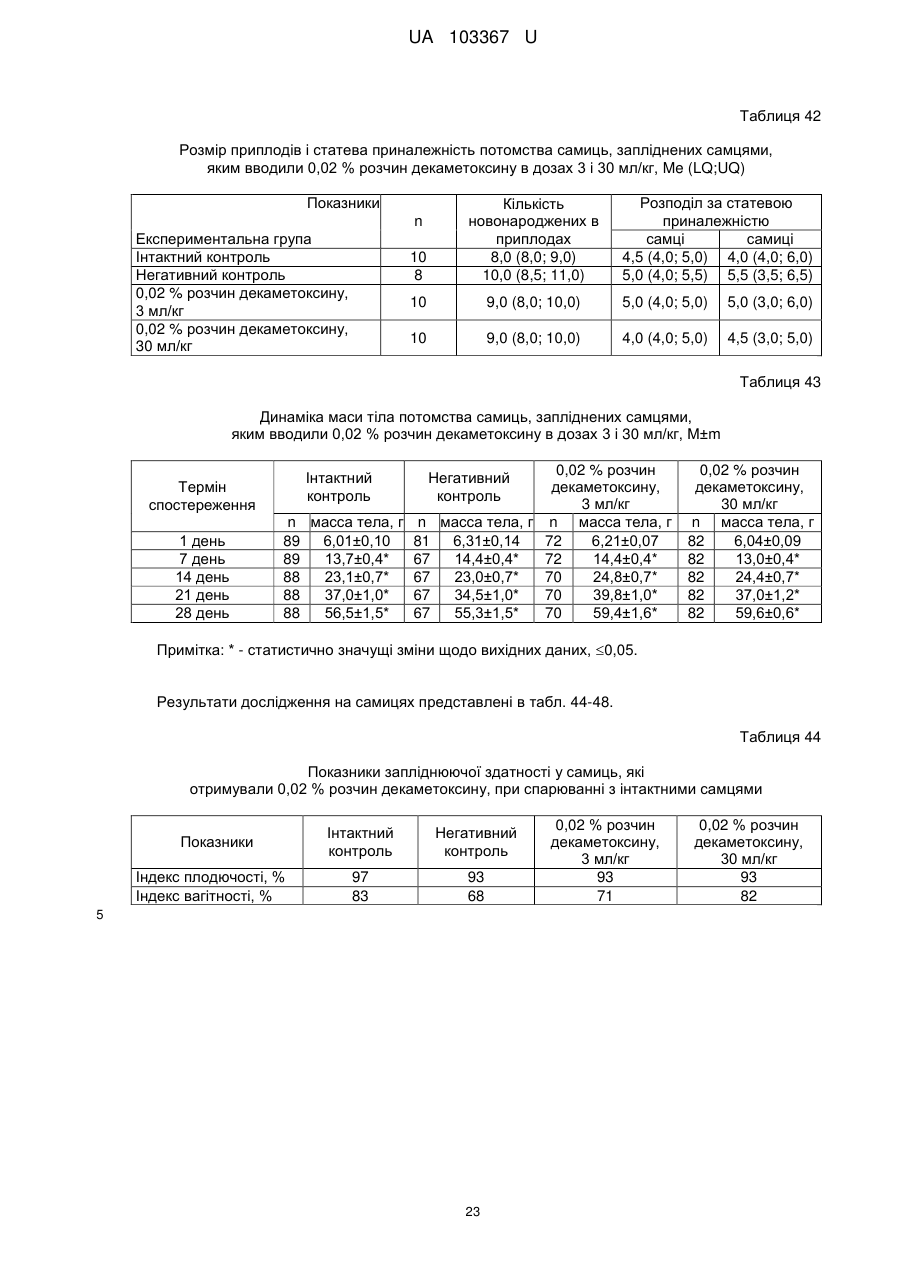
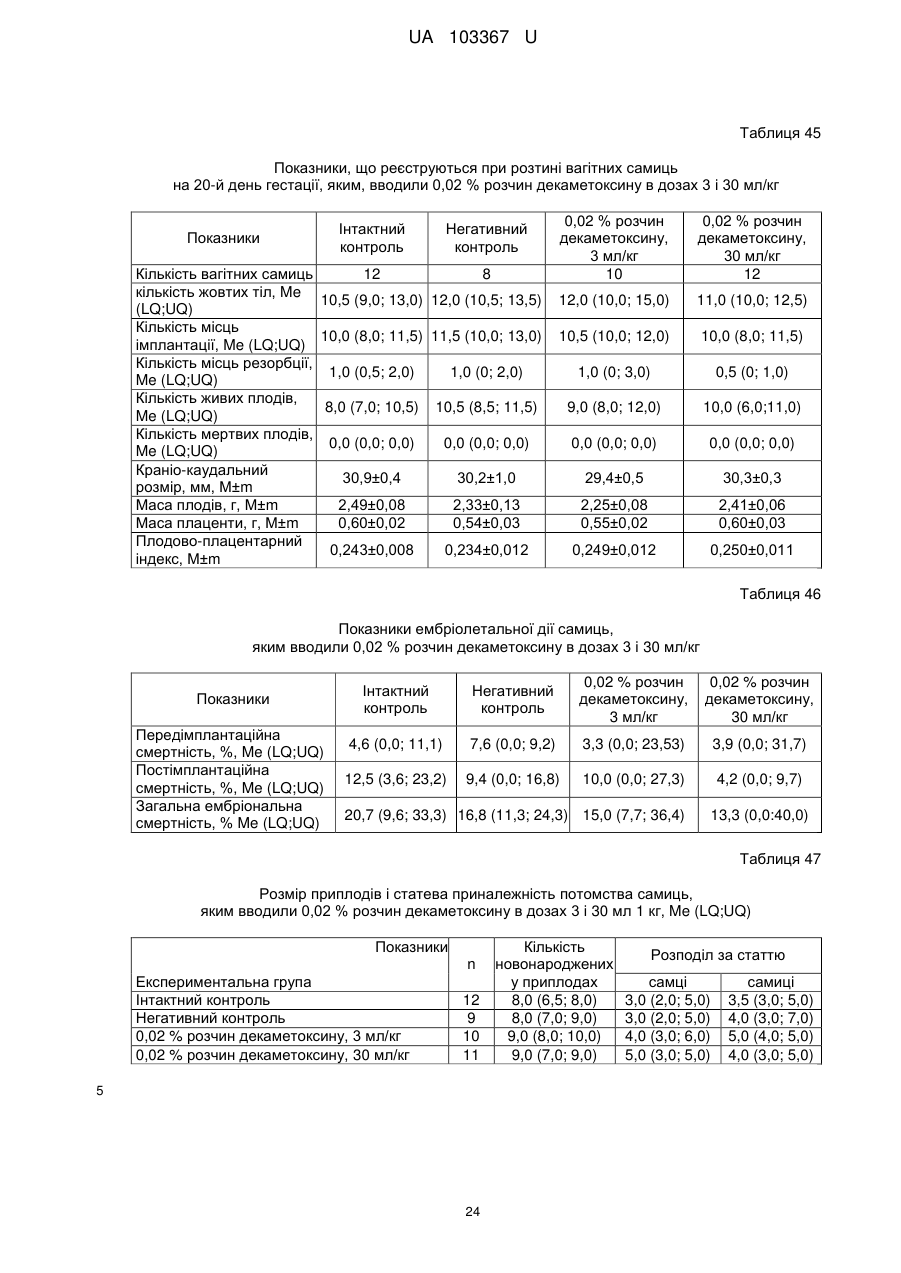
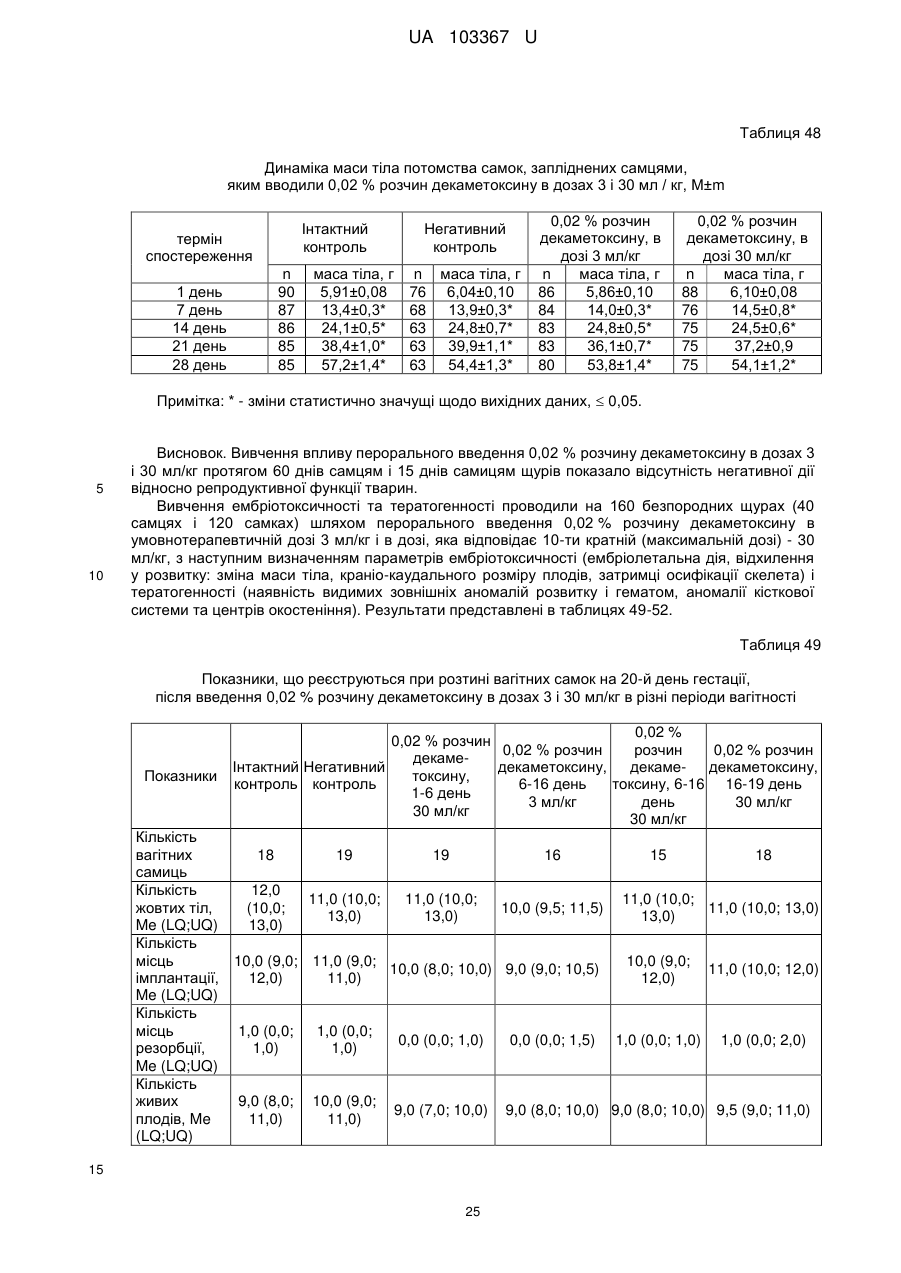
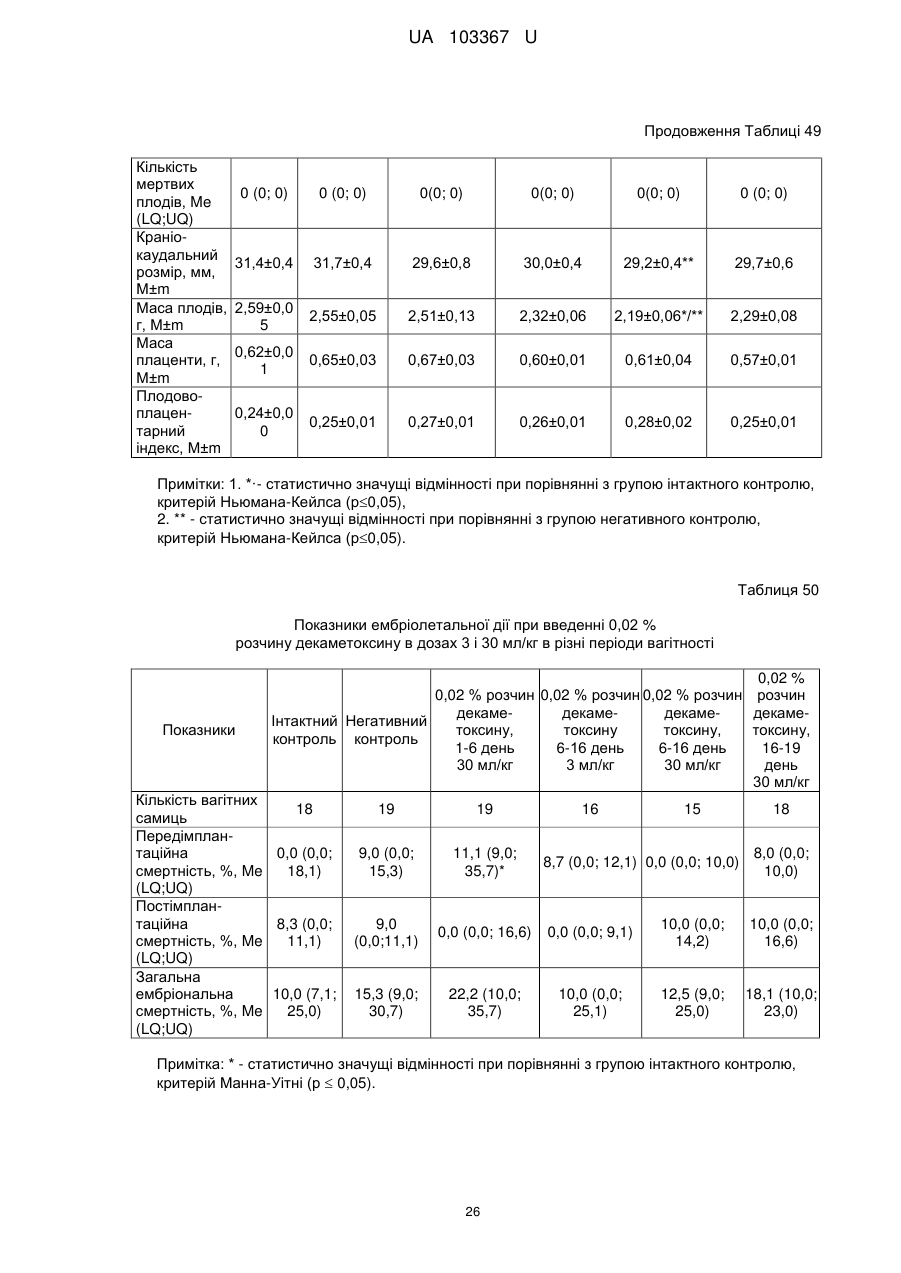
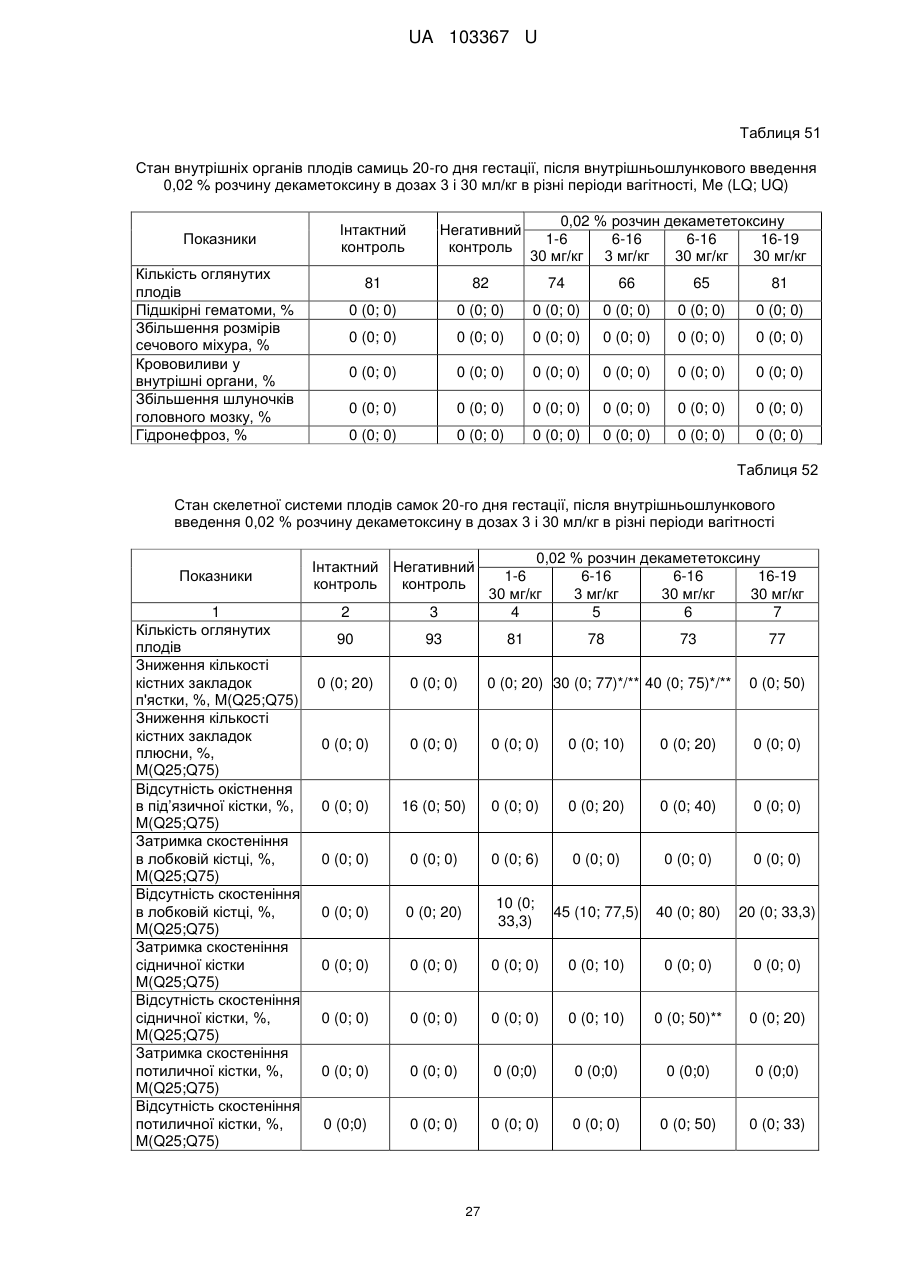
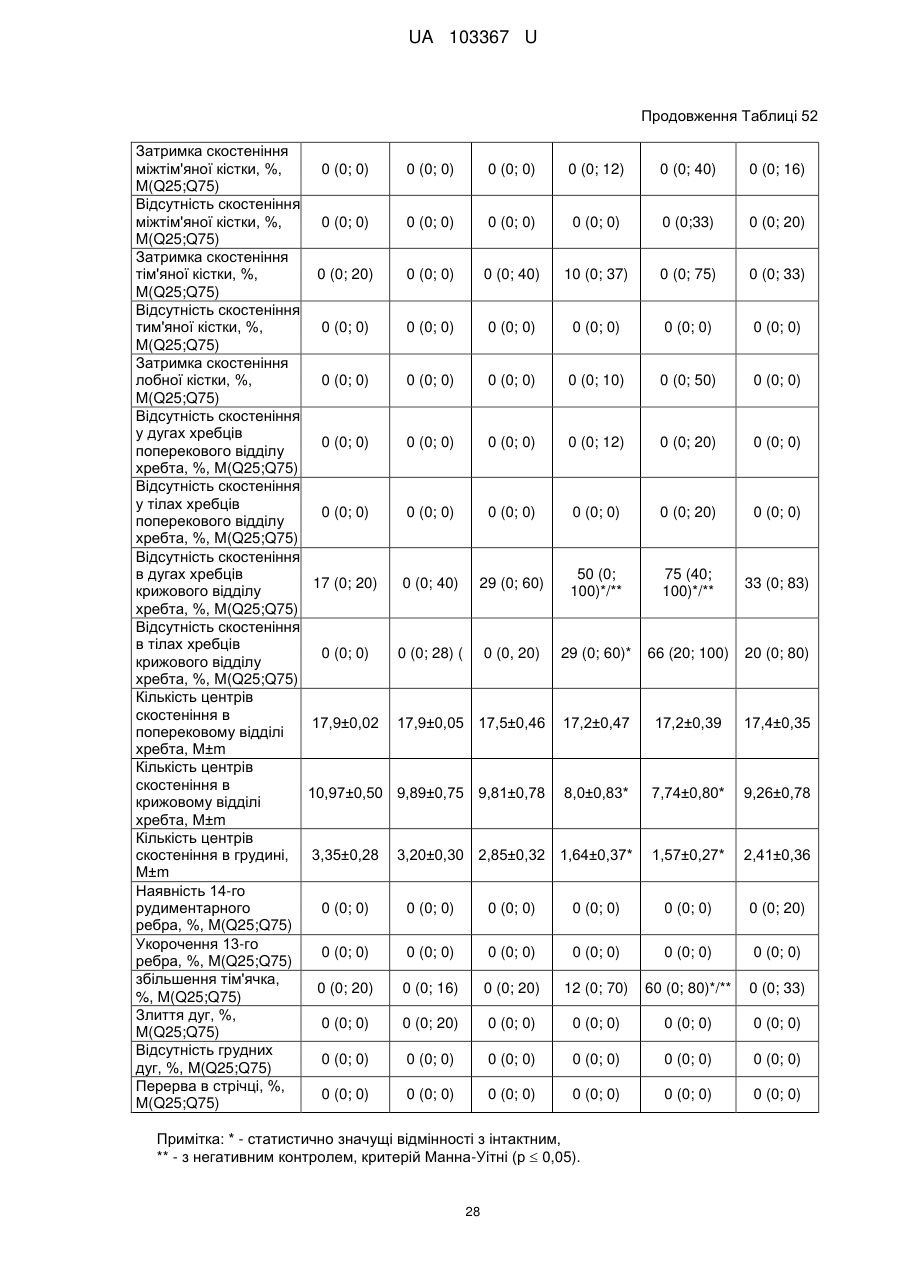
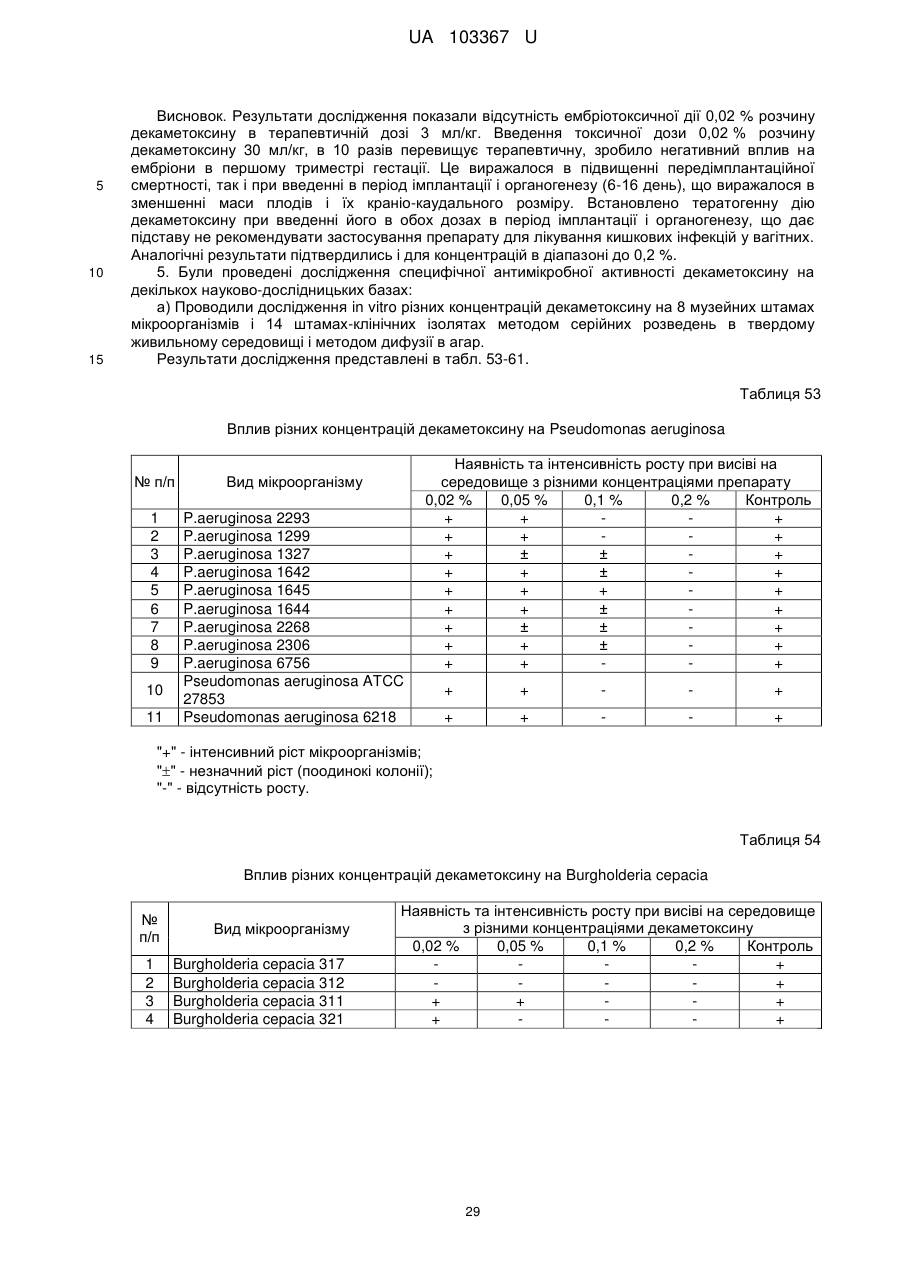
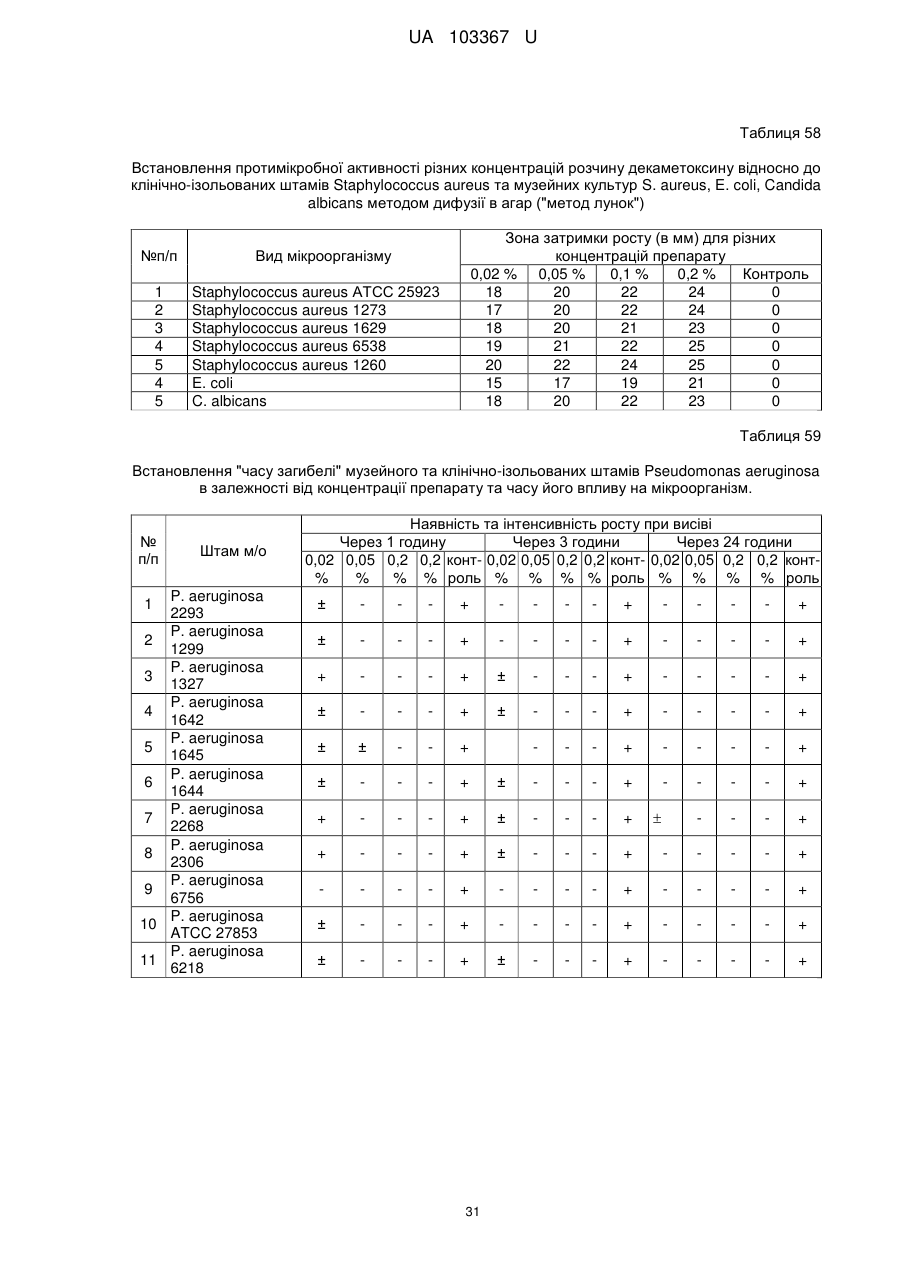
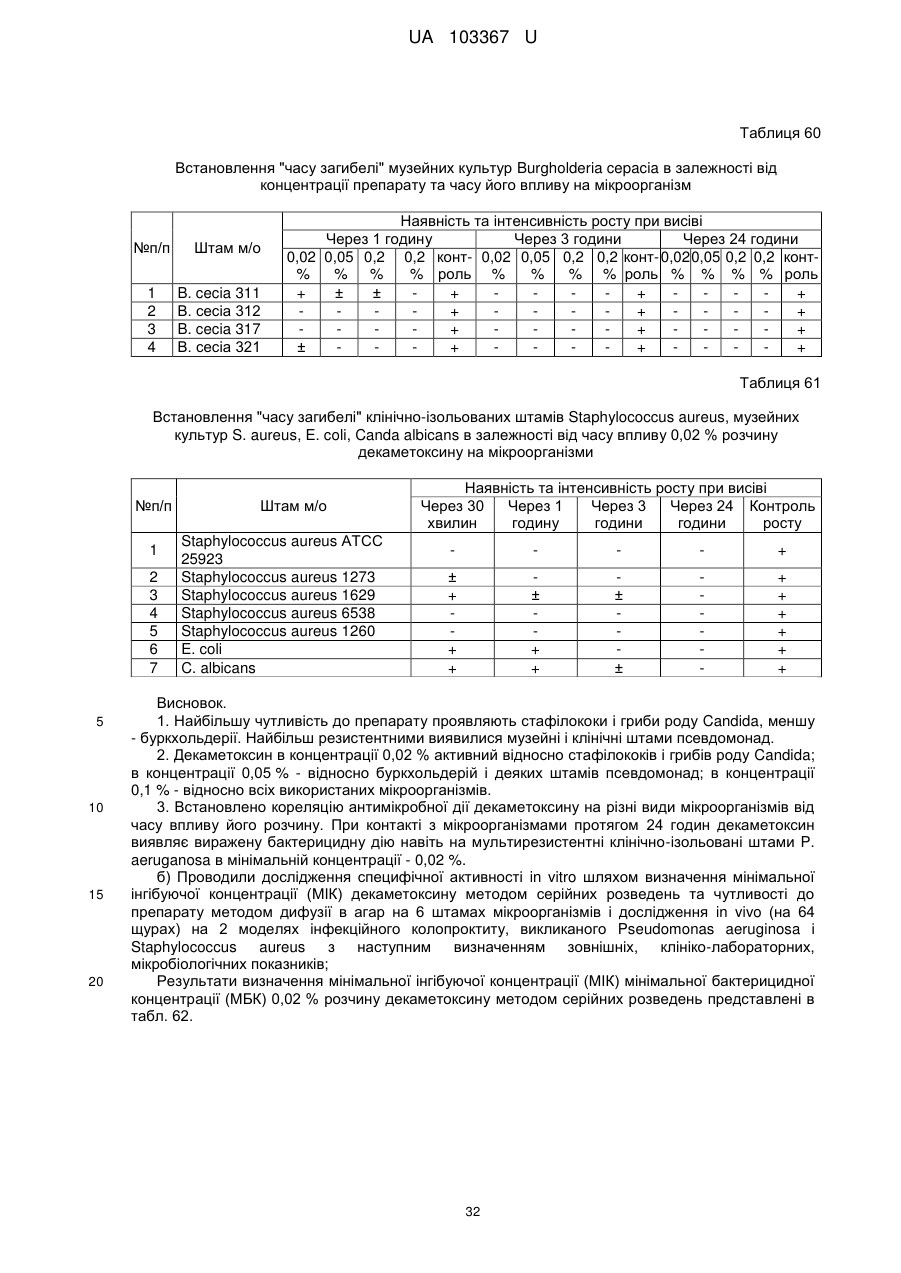
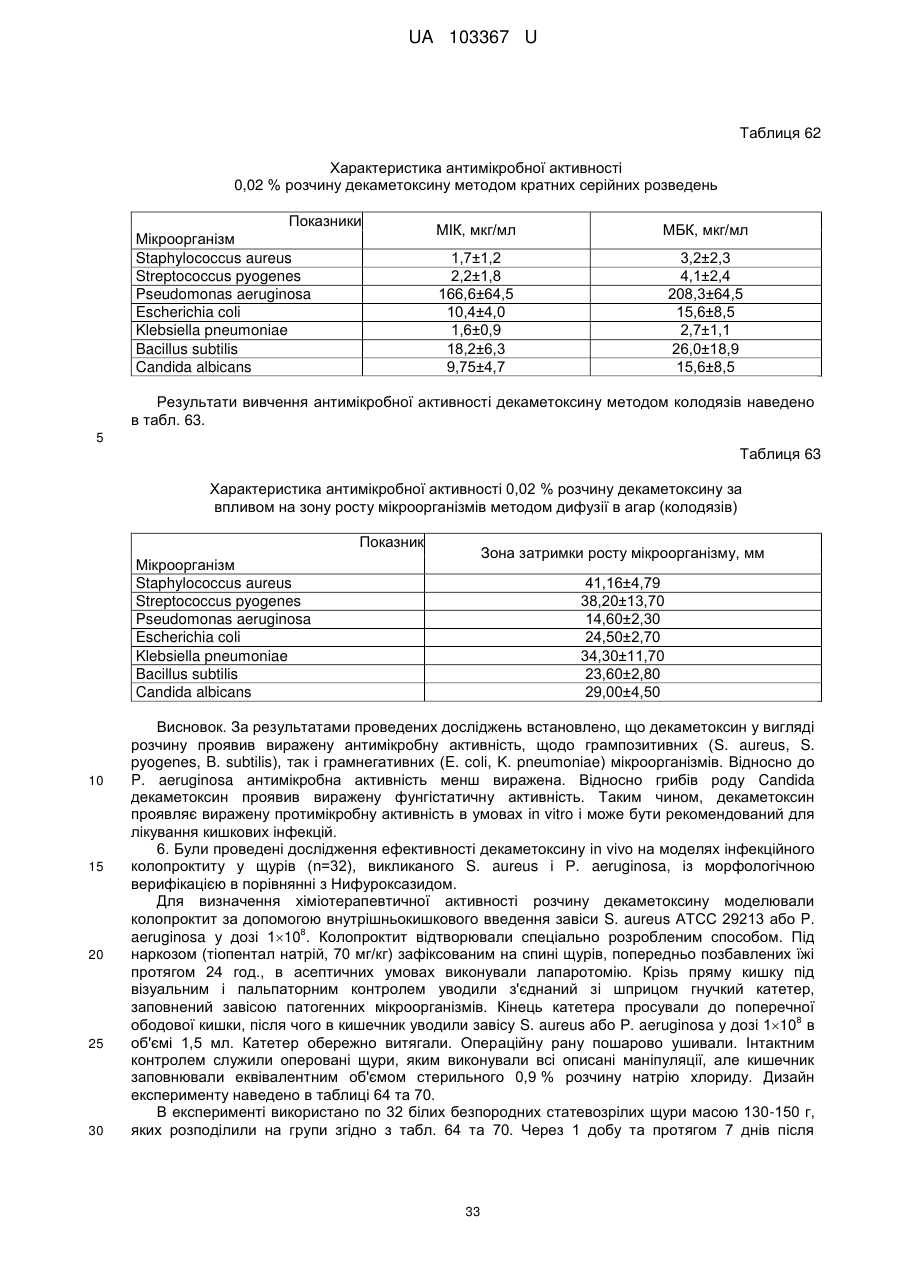
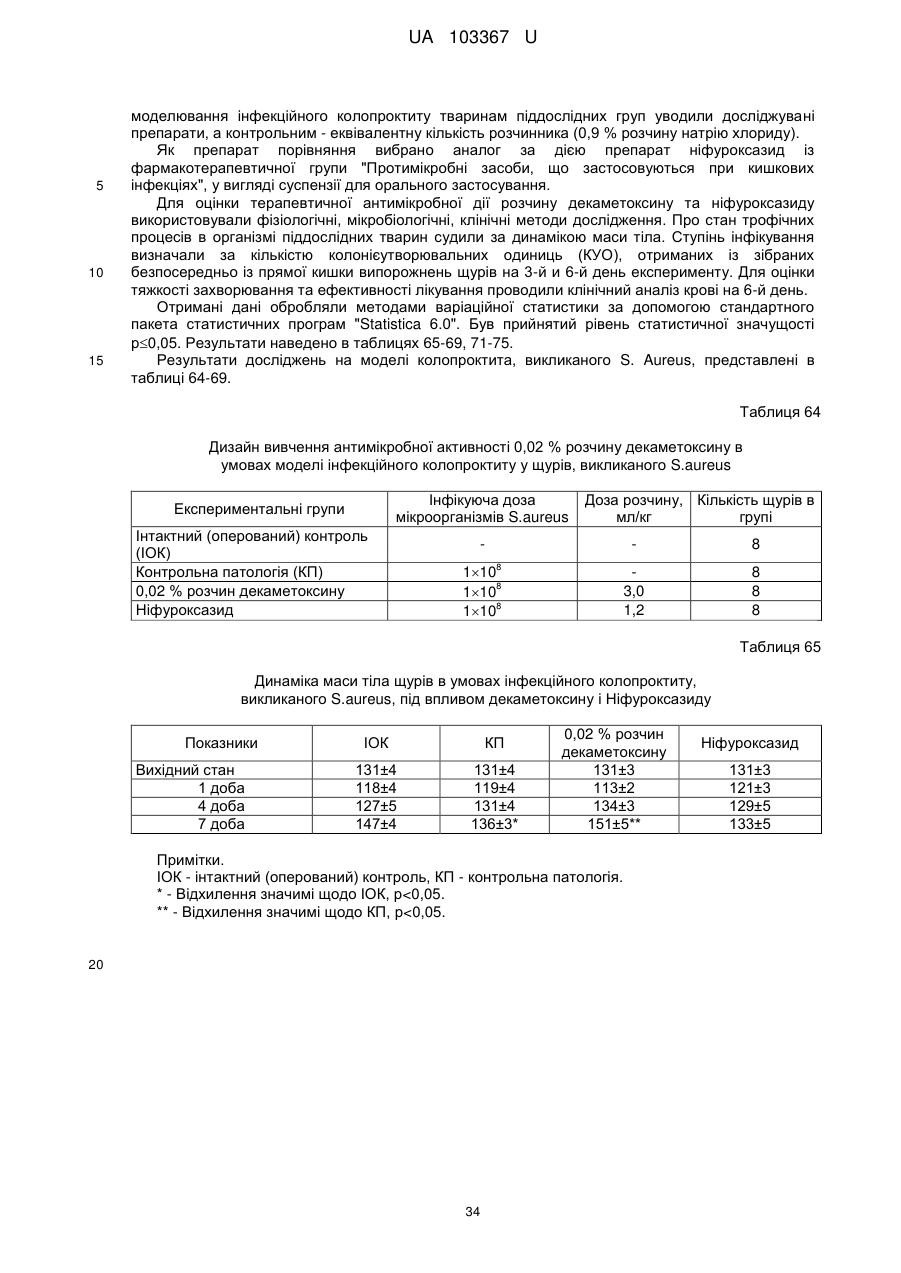
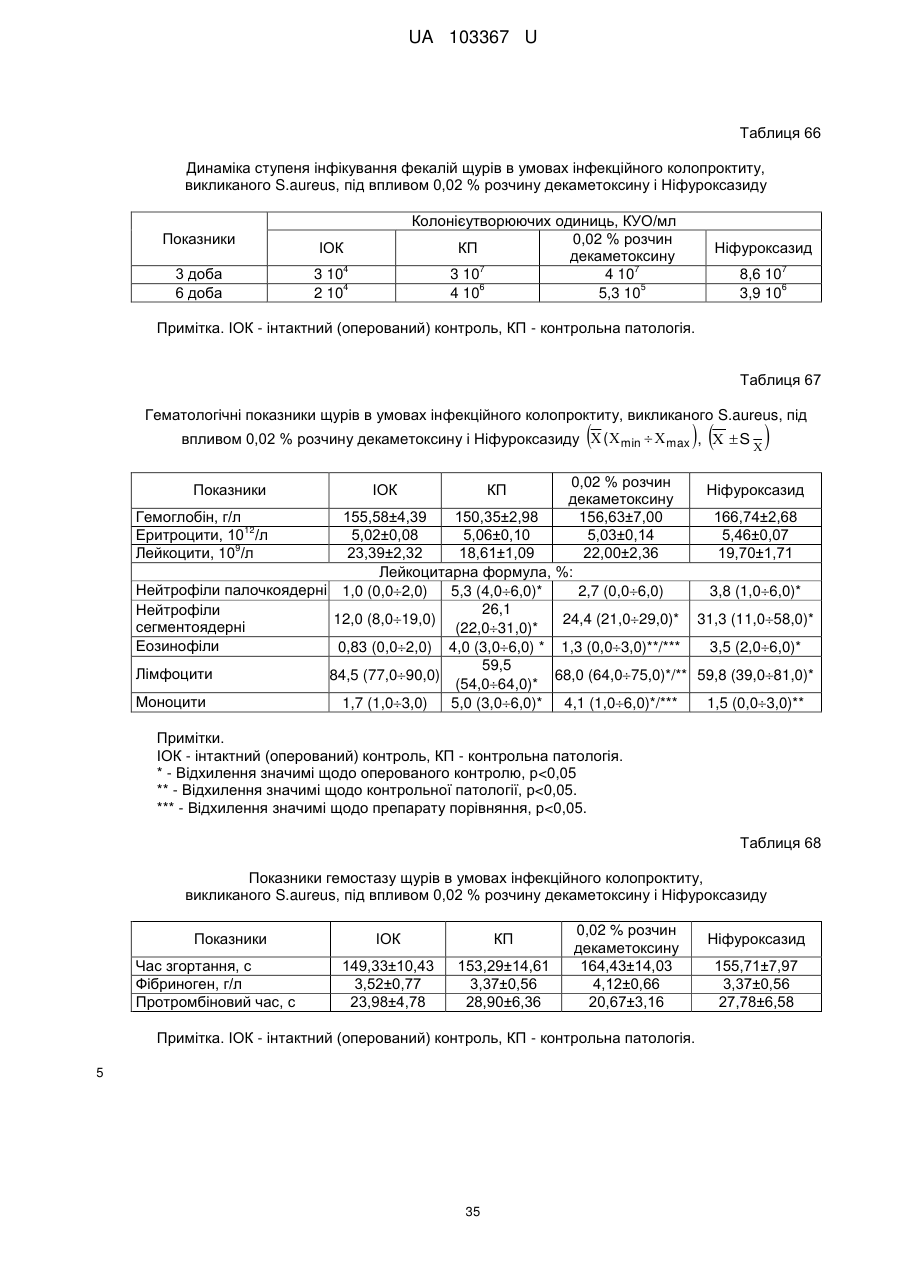
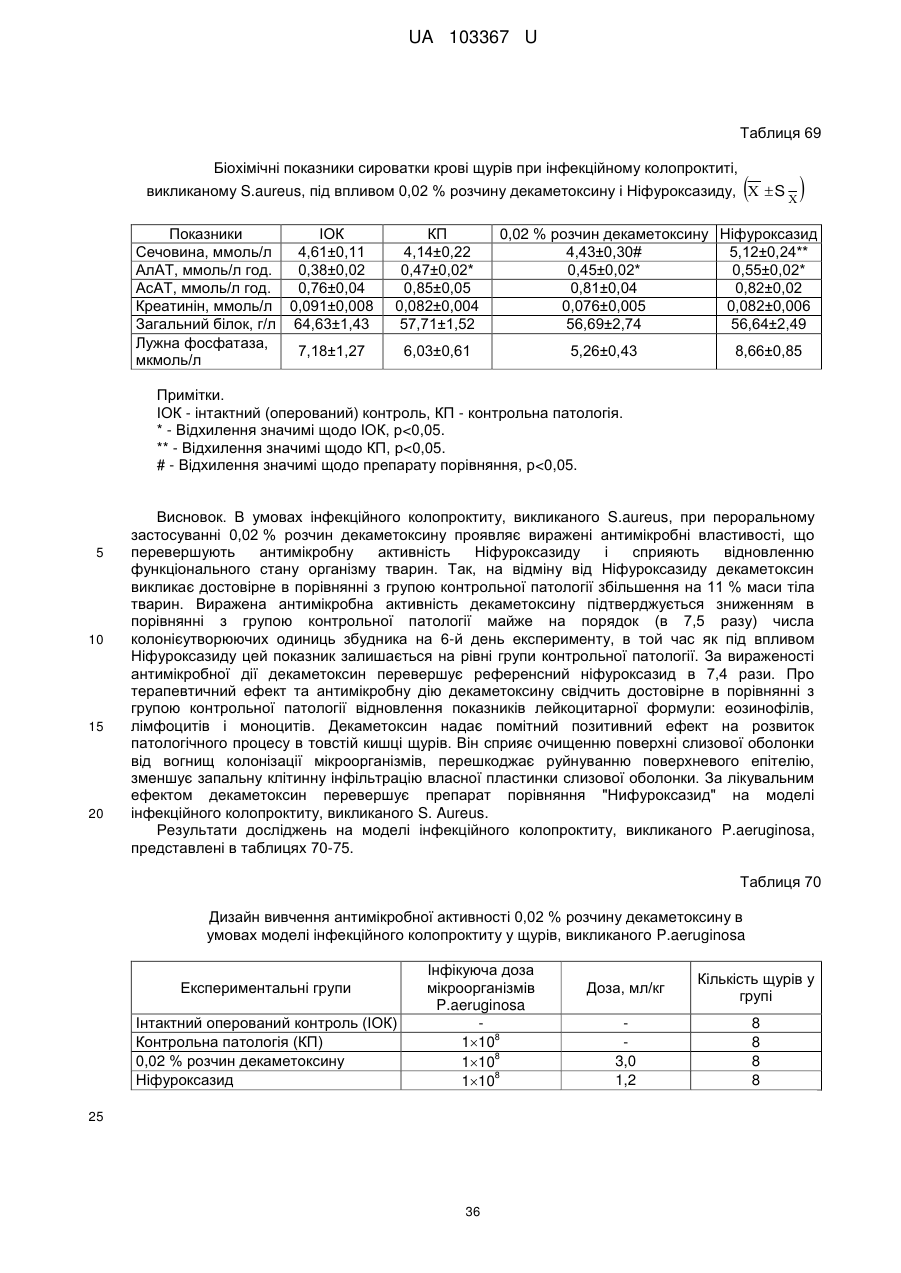
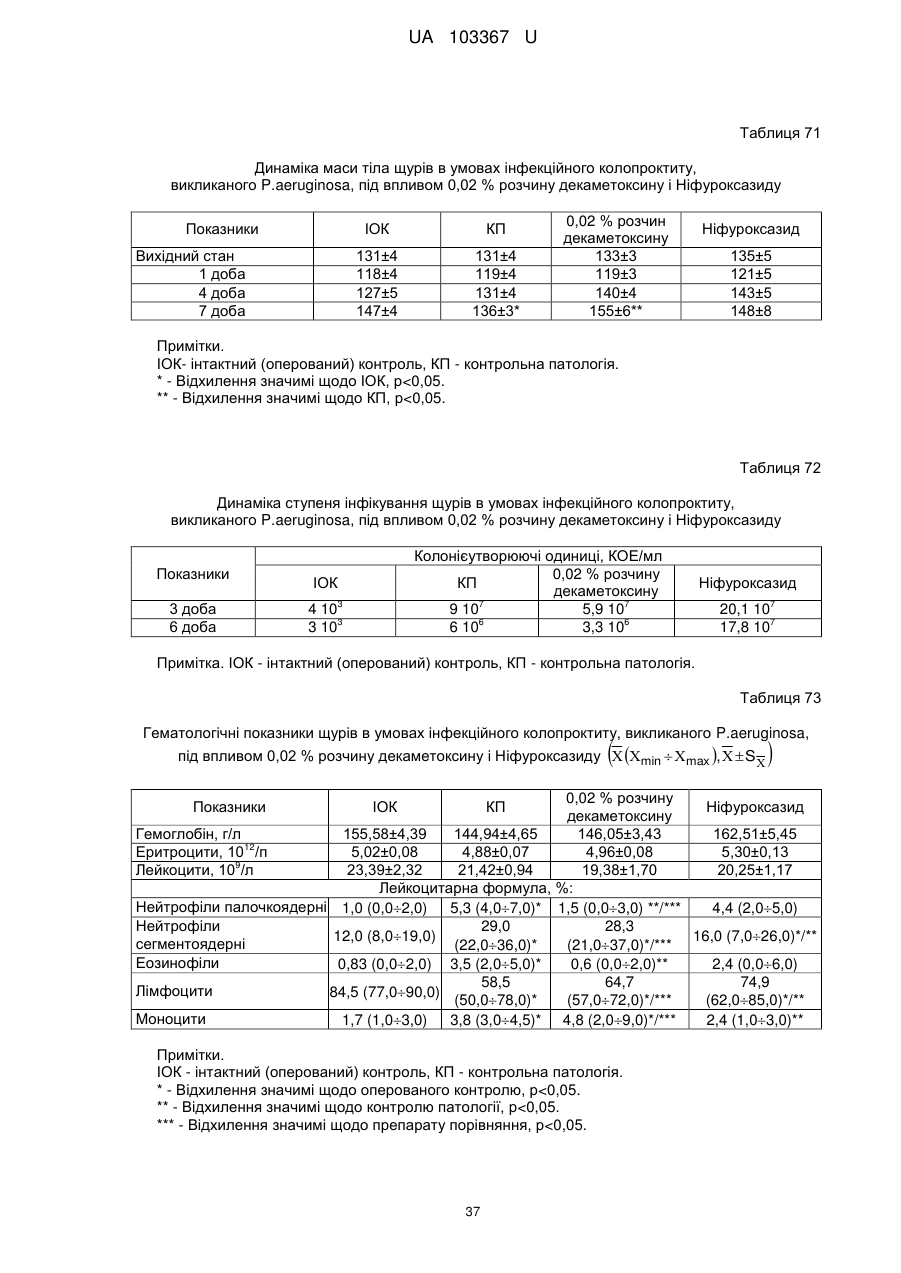
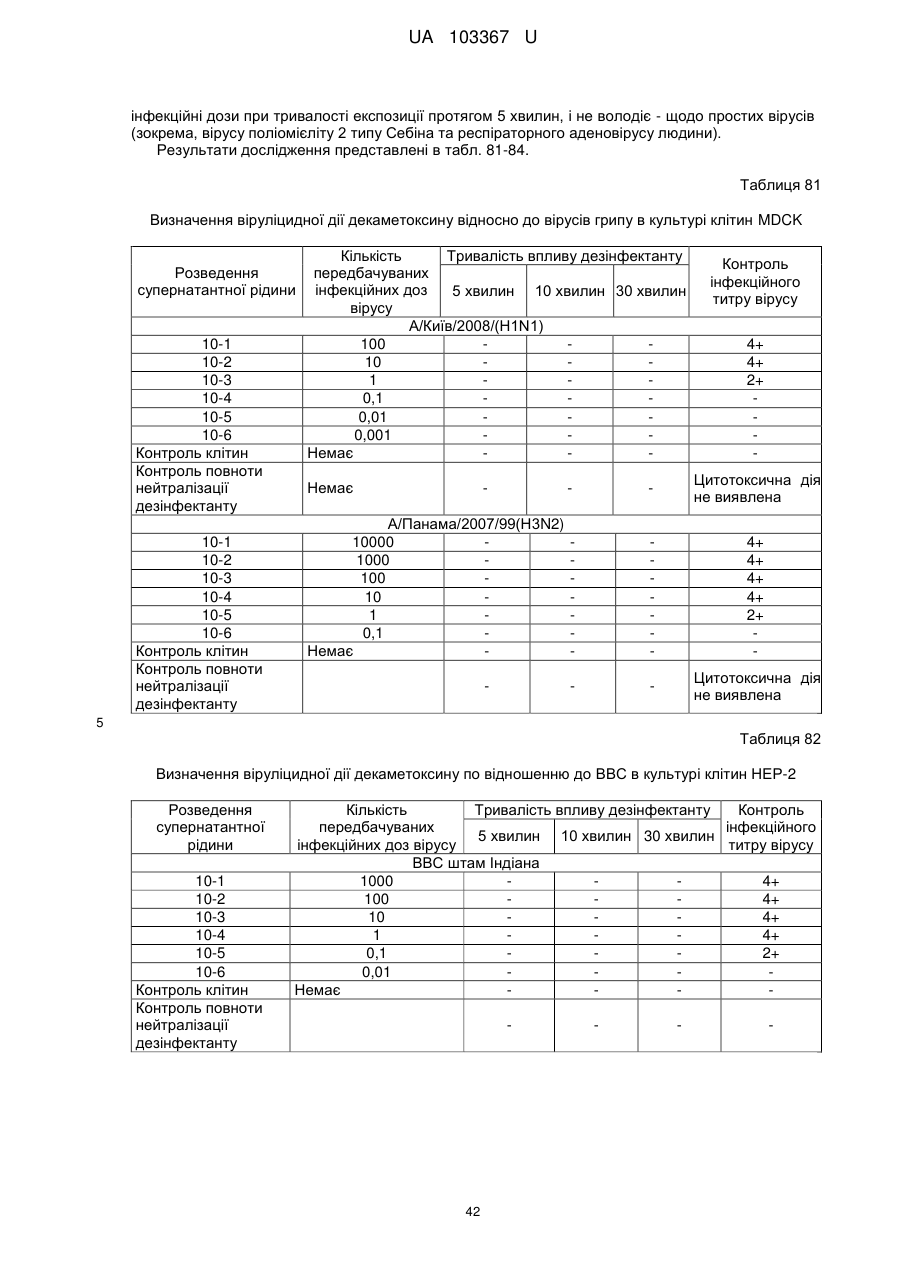
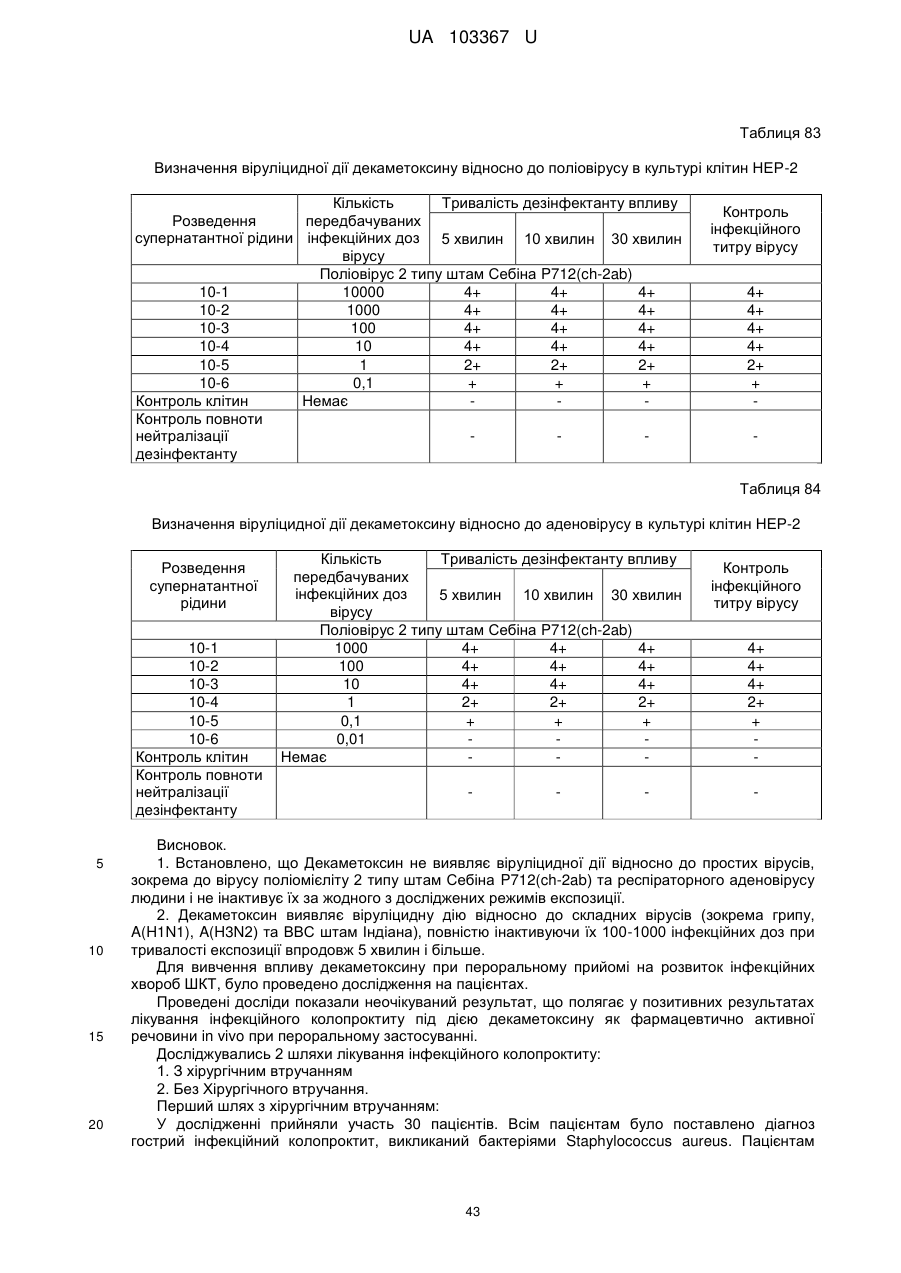
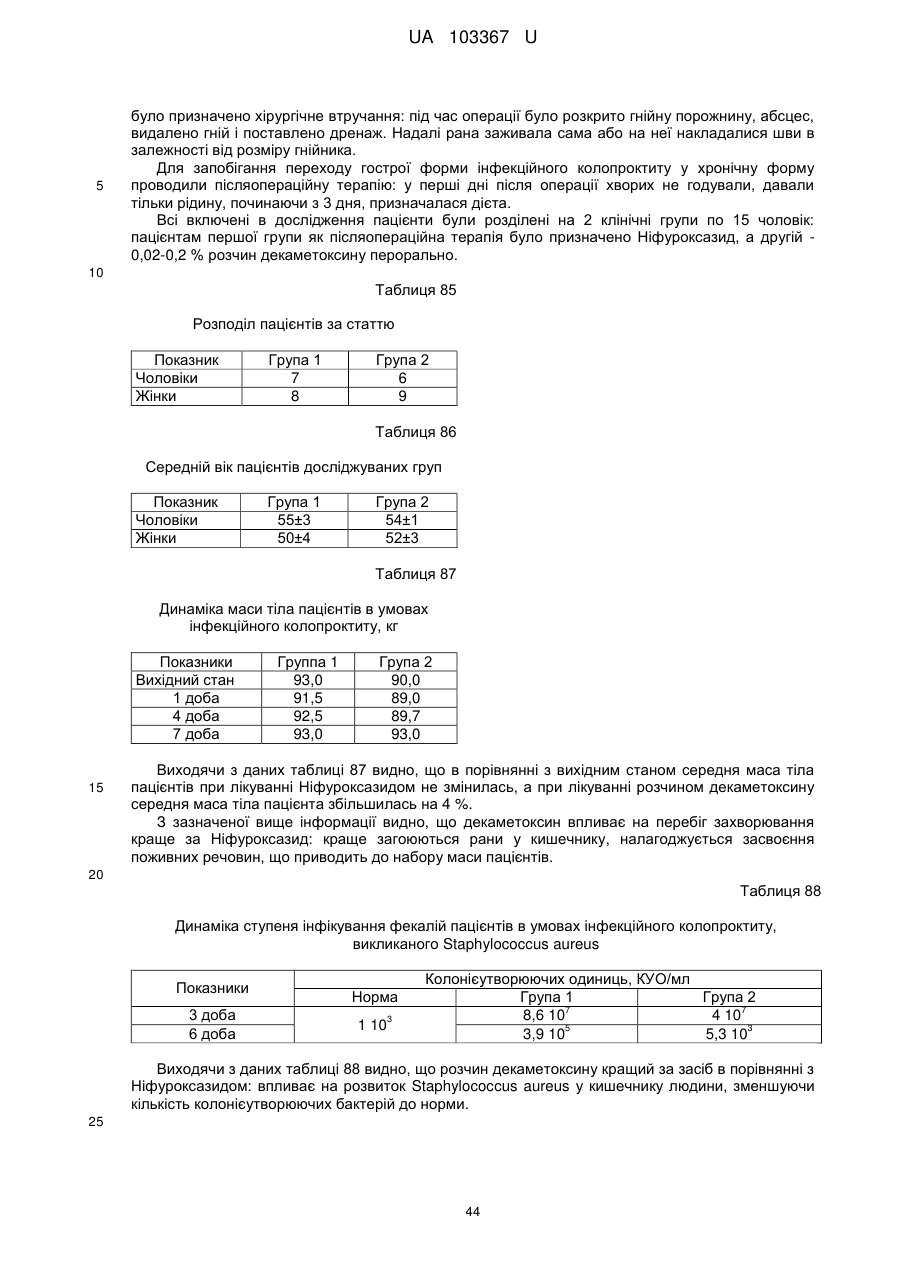
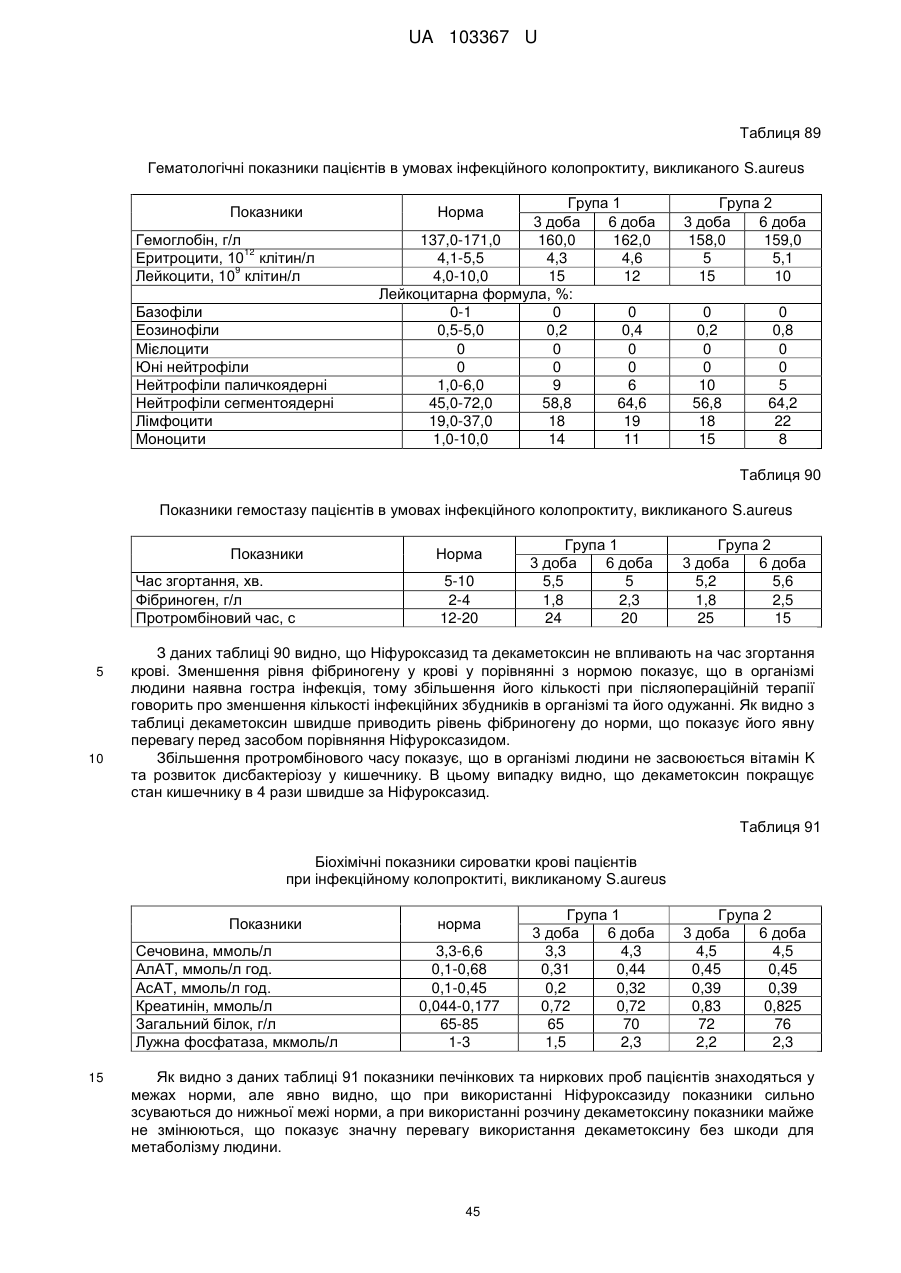
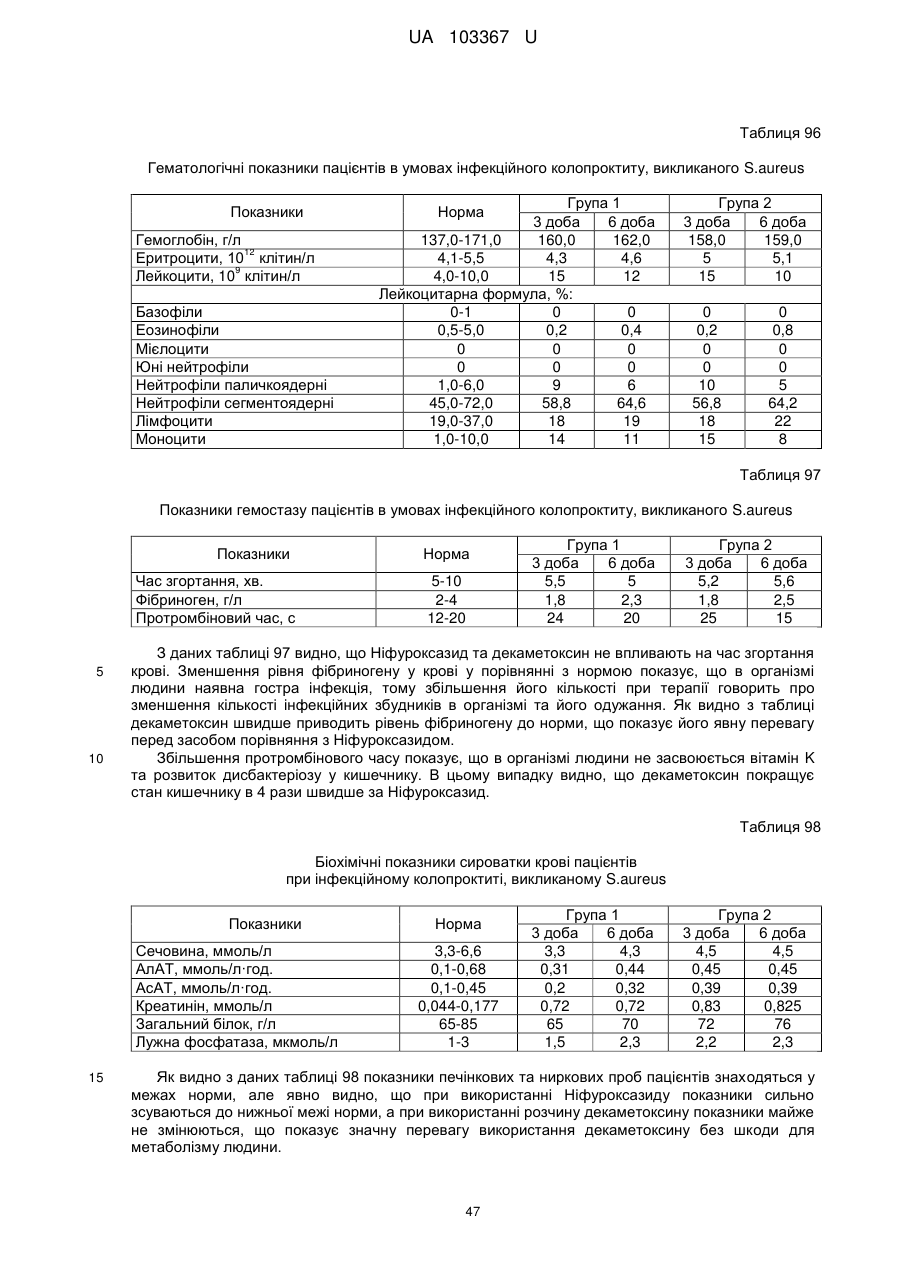
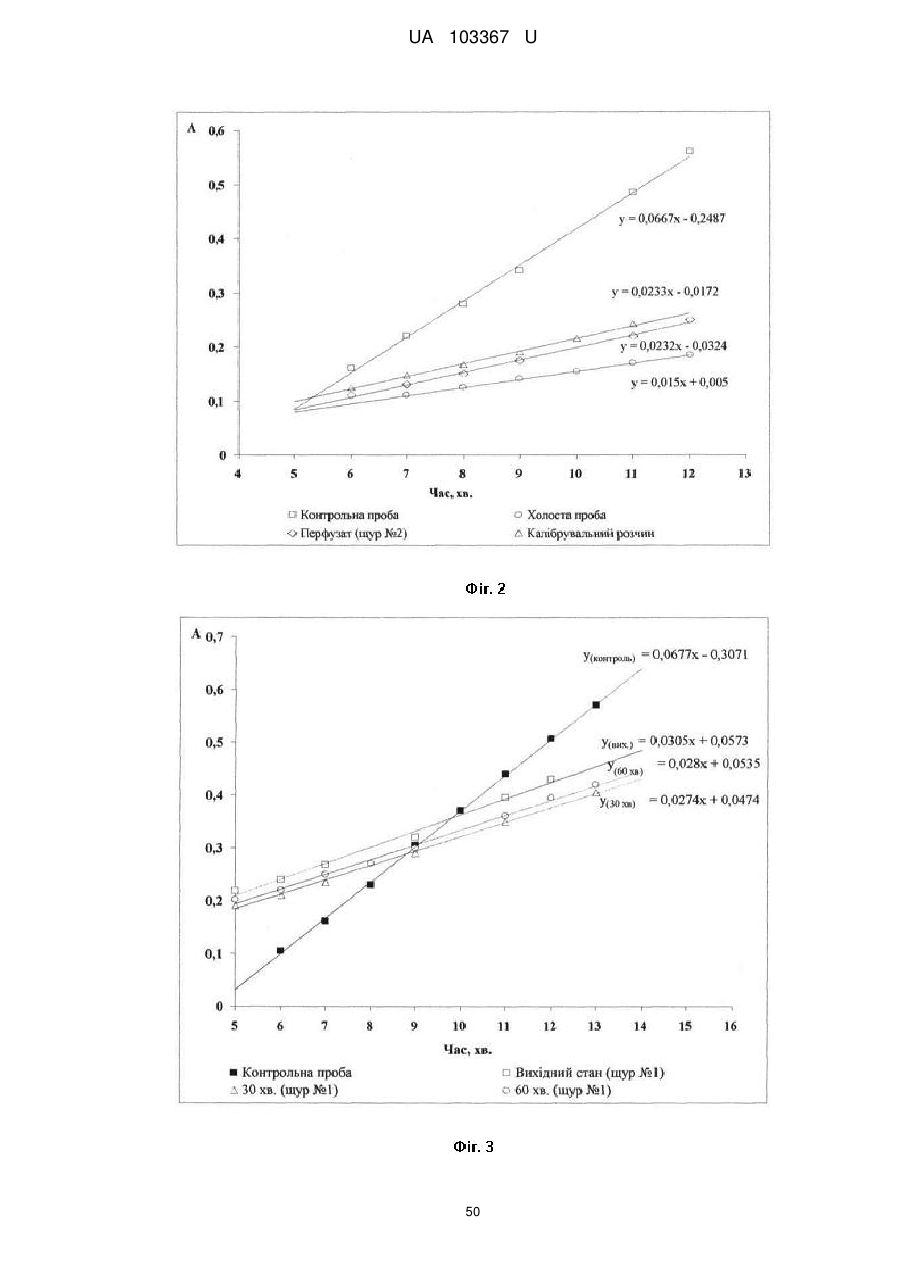
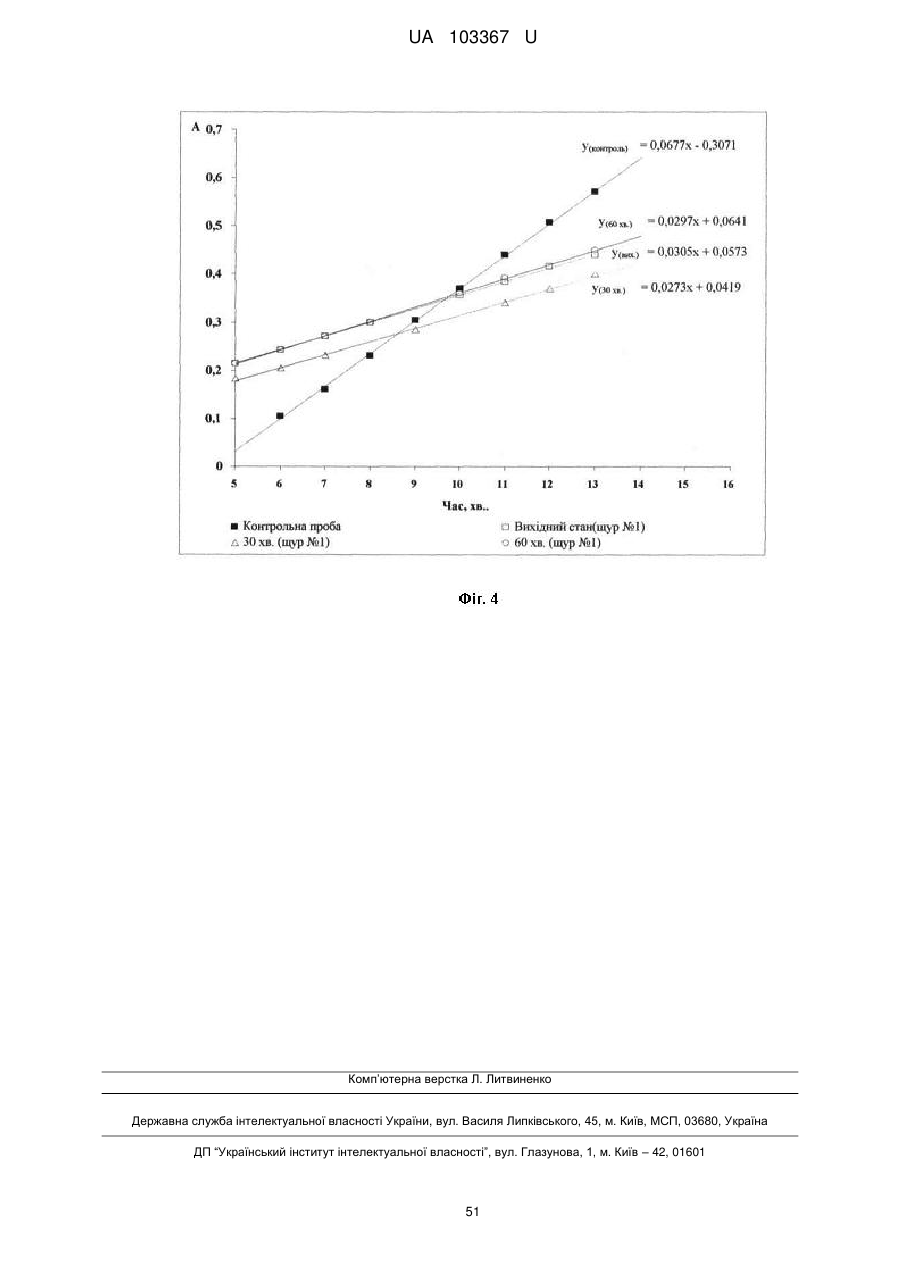
Реферат: Застосування декаметоскину як фармацевтично активної речовини для лікування шлунковокишкового тракту та кишкових інфекцій перорально. UA 103367 U (12) UA 103367 U UA 103367 U 5 10 15 20 25 30 35 40 45 50 55 60 Корисна модель належить до нового застосування декаметоксину як фармацевтично активної речовини для лікування кишкових інфекцій мікробної та вірусної етіології перорально. Декаметоксин - хімічна сполука [1,10-декаметилен-біс(N,N-диметилментоксикарбонілметил) амонію дихлорид], білий кристалічний порошок зі слабким запахом, легкорозчинний у воді, по хімічній структурі й антимікробній дії близкий до етонію. Має широкий спектр антимікробної дії на грампозитивні (стафілокок, стрептокок, пневмокок), грамнегативні (гонокок, менінгокок) коки, коринебактерії дифтерії, ентеробактерії, псевдомонади, найпростіші, дерматофіти, дріжджоподібні гриби роду Candida, хламідії та віруси. В процесі застосування дуже повільно утворюються резистентні до декаметоксину варіанти мікроорганізмів, (http://compendium.com.ua/akt/68/610/decametoxinum). У зв'язку з тим, що декаметоксин є поверхнево-активною речовиною, він змінює проникність мембрани мікробної клітини, приводячи до деструкції та загибелі мікроорганізмів, що обумовлює його бактерицидну дію [Pashynskaya V.A., 2002; Shchetina V.N., 1990]. Антисептична дія препарату ґрунтується не лише на бактерицидній, а й на бактеріостатичній активності. Бактеріостатична дія обумовлена наступними механізмами: а) інактивація екзотоксинів мікроорганізмів, що було продемонстровано на збудниках дифтерії, і що дозволило в 1994 році рекомендувати декаметоксин для боротьби з епідемією дифтерії [Ковальчук В.П., 2002]; б) зниження адгезії патогенних мікроорганізмів [Жорняк О.І., Стукан O.K., Сухляк В.В., 2010; Жорняк О.І., Стукан O.К., 2010]. Так, наприклад, декаметоксин в концентрації 10 мкг/мл різко знижує адгезію коринебактерій, сальмонел, стафілококів та ешерихій. Зниження адгезії може досягатися або конкурентним зв'язуванням з бактеріальними адгезинами, або з поверхневими рецепторами клітин хазяїна; в) руйнування білків фімбрій, джгутиків, розташованих на поверхні мембран (як відомо, головна функція фімбрій - забезпечення адгезії грамнегативних бактерій до клітин господаря, а джгутиків - пересування мікроорганізмів). г) блокування функції клітинної стінки (трансмембранний транспорт метаболітів, харчування, дихання), пригнічення клітинного дихання, синтез білка і поділу клітини. Так, було показано, що декаметоксин блокує дихальний ланцюг синьогнійної палички [Bievskiǐ AN, 1994]; що в присутності декаметоксину значно знижується активність дегідрогеназ у кишковій паличці, синьогнійній паличці, Micrococcus lysodeikticus [Shchetina VN, 1990], дегідрогеназ стафілокока і Candida albicans [Мороз В.М., 2002], що свідчить про пригнічення аеробного окислення глюкози, сукцината і пірувата, в той час як активність аспартата і аланінамінотрансферази, навпаки, зростає [Shchetina VN, 1990]; формує комплекси з бактеріальною ДНК [Sorokin VA, 1990; Kukhar 'V.P., 1989]. Порушення клітинного метаболізму і ділення забезпечує значний лікувальний ефект без лізису мікробної клітини [Пасічників С.П.; Фещенко Ю.І., 2002]. Декаметоксин застосовується для місцевого лікування захворювань порожнини рота (стоматити, виразково-некротичний гінгівіт, дистрофічно-запальна форма пародонтозу I-ІІ ступеня у стадії загострення), глотки, гортані (при ґінґівіті, кандидозі слизової оболонки порожнини рота, фарингіті, ларингіті, тонзилітах); для санації порожнини рота, глотки, носоглотки у носіїв патогенного стафілококу, дифтерійної палички, кандиди; профілактика вторинної інфекції після хірургічних втручань у порожнині рота, зіві, гортані; місцево також для лікування гнійничкових бактеріальних та грибкових захворювань шкіри, мікробної екземи, гнійнозапальних уражень м'яких тканин (абсцеси, карбункули, флегмони, фурункули, гнійні рани, панариції). Також застосовується ендобронхіально при абсцесі легенів, бронхоектатичній хворобі, кістозній гіпоплазії легенів, ускладненій нагноюванням, хронічному бронхіті у фазі загострення. Місцево застосовується при проктиті та виразковому коліті. В офтальмології у вигляді очних крапель застосовується при кон'юнктивіті та блефарокон'юнктивіті та для обробки контактних лінз. Декаметоксин застосовується також для стерилізації медичних інструментів, приладів, шовного матеріалу, гумових рукавичок та для хімічної стерилізації та консервації кістково-сухожильних трансплантатів [http://uk.wikipedia.org/]. В сучасній медицині для лікування кишкових інфекцій мікробної та вірусної етіології використовуються такі препарати, як: Ніфуроксазид, Фталазол, Фуразолідон, Інтестопан. Але ці засоби мають свої недоліки. Ніфуроксазид - кишковий антисептик, похідне 5-нітрофурану; активний відносно більшості збудників кишкових інфекцій (у тому числі штамів-мутантів, стійких до інших протимікробних засобів). Проявляє локальну антибактеріальну дію в просвіті кишки відносно деяких видів грампозитивних бактерій з сімейства Staphylococcus і деяких видів грамнегативних бактерій з сімейства Enterobacteriaceae: видів Yersinia spp., Escherichia spp., Citrobacter spp., Enterobacter spp., Klebsiella spp., Salmonella spp. Недоліком засобу є те, що на відміну від декаметоксину він 1 UA 103367 U 5 10 15 20 25 30 35 40 45 50 55 60 не проявляє антибактеріальної дії на бактерії видів Proteus vulgaris, Proteus mirabilis i Pseudomonas aeruginosa [http://cornpendium.com.ua/info/172054/gedeon-richter/nifuroksazidrikhter]. Фталазол, як і інші сульфаніламідні препарати, перешкоджає включенню параамінбензойної кислоти (ПАБК) в синтез фолієвої кислоти мікробної клітини. Це призводить до порушення утворення фолієвої кислоти, що бере участь у синтезі пуринових і піримідинових основ, від яких залежить ріст і розвиток мікроорганізмів. Цей ефект розвивається поступово, тому в мікробній клітині є деякі запаси ПАБК. Тому фталазол потрібно вводити в досить високих дозах. В іншому випадку можуть утворюватися стійкі штами збудників, що не піддаються надалі дії сульфаніламідних препаратів. Має протипоказання: підвищена індивідуальна чутливість до препаратів сульфаніламідного ряду; хвороби системи крові; дифузний токсичний зоб; хронічна ниркова недостатність; гломерулонефрит; гострий гепатит; кишкова непрохідність. І також має ряд побічних дій з боку: нервової системи, серцево-судинної системи, системи крові, органів шлунково-кишкового тракту (ШКТ), дихальної системи, сечовидільної системи, алергічні та токсико-алергічні реакції [http://www.rlsnet.ru/tn_index_id_5378.htm]. Фуразолідон - антибактеріальний лікарський засіб групи нітрофуранів, синтетичне похідне 5нітрофурфуролу, що має виражену протимікробну активність відносно грамнегативних аеробних мікроорганізмів, меншою мірою чутливі до дії препарату грампозитивні аеробні мікроорганізми, деякі найпростіші і гриби (зокрема гриби роду Candida). Фармакологічна дія препарату безпосередньо залежить від дози, при застосуванні невисоких доз фуразолідон надає бактеріостатичний ефект, при збільшенні дози відзначається виражена бактерицидна активність. Недоліками цього засобу є те, що його не можна приймати довгостроково, тому що при тривалому застосуванні препарату можливий розвиток гемолітичної анемії і метгемоглобінемії (переважно у новонароджених і грудних дітей), а також задишки, кашлю, гіпертермії і нейротоксичних реакцій. При застосуванні підвищених доз препарату у пацієнтів можливий розвиток токсичних уражень печінки, у тому числі гострого токсичного гепатиту. Крім того, можливий розвиток поліневриту (нейротоксична дія) і гематотоксичної дії фуразолідону [http://www.piluli.kharkov.ua/drugs/drug/furazolidonum/]. Інтестопан - препарат має антибактеріальну та антипротозойну (пригнічує життєдіяльність найпростіших організмів) активністю і близький за механізмом дії до хлорхінальдолу. Недоліком цього засобу є наявність брому в молекулі діючої речовини, що може призвести до небезпечних побічних дій на організм [http://www.piluli.kharkov.ua/drugs/drug/2211/]. Незважаючи на доволі широкий спектр дії вказаних у рівні техніки засобів для лікування кишкових інфекцій мікробної та вірусної етіології, а саме: сальмонельоз, дизентерія, дифтерія, ентерит, гастрит, гастроентерит, ентероколіт, гастроентероколіт, бруцельоз, проктит, сигмоїдит, коліт та інш., існують деякі захворювання, що лікуються лише хірургічним шляхом, наприклад інфекційний колопроктит. Інфекційний колопроктит - це запалення тканин, що оточують пряму кишку. З різних причин, а іноді і без наявної причини, в анальному каналі утворюється мікроотвір, через який інфекція з просвіту прямої кишки проникає в біляпрямокишкову клітковину. Розвивається запалення, формується гнійник, який мимоволі розкривається назовні або в просвіт прямої кишки. Після звичайного розтину гнійника при гострому інфекційному колопроктиті, без ліквідації його внутрішнього отвору, у 80-98 % хворих в подальшому формуються свищі прямої кишки (хронічний інфекційний колопроктит). Гострий інфекційний колопроктит зазвичай починається гостро, клінічна картина досить яскрава: з'являється погіршення загального стану, слабкість, нездужання, підвищення температури тіла, озноб, болі в області заднього проходу і промежини. У зоні заднього проходу утворюється невелика хвороблива припухлість, з якої пізніше розвивається гнійник, який може перебувати як безпосередньо під шкірою промежини, так і глибоко між м'язами промежини і сідниць. Якщо своєчасно не проводять адекватне лікування, запалення поширюється на суміжні клітинні простори, відбувається прорив гнійника в пряму кишку або назовні через шкіру промежини. Болі стихають, знижується температура тіла, поліпшується загальний стан хворого Але прорив гнійника не призводить до повного одужання, хвороба продовжує прогресувати з формуванням нових свищів прямої кишки (хронічний інфекційний колопроктит). Лікування гострого інфекційного колопроктиту - тільки хірургічне. Усі без винятку пацієнти потребують екстреної хірургічної допомоги. Основні принципи операції: 1) розтин і дренування гнійника; 2 UA 103367 U 5 10 15 20 25 30 35 40 45 50 55 2) ліквідація його внутрішнього отвору, через яке порожнина гнійника зв’язується з прямою кишкою. Операція проводиться під наркозом. Після операції проводять перев'язки, призначають антибіотики, вітаміни, засоби, що підвищують імунітет. Розтин гнійника не є радикальною операцією: після неї, як правило, виникають повторні нагноєння (формується хронічний інфекційний колопроктит). Причина такого явища в збереженні запального каналу (свища) між прямою кишкою і навколишніми тканинами. При цьому відбувається повторне зараження кишковою флорою через внутрішній отвір свища, що постійно підтримує запальний процес. Для повного лікування необхідна повторна операція - радикальна, тому приводить до повного виліковування. В результаті такої операції зв'язок між порожниною кишки і гнійника ліквідується. Тривале існування запального вогнища в промежині веде до появи дратівливості, безсоння, головного болю, знижується працездатність, можливий розвиток неврастенії, імпотенції. Зволікання погіршує не тільки загальний стан хворого, але й прогноз, оскільки підвищується ймовірність поширення гнійного процесу по клітинних просторах таза, руйнування м'язових структур сфінктера, тазового дна і стінки прямої кишки. На сьогоднішній день єдиний метод лікування хворих зі свищами прямої кишки - радикальна операція, коли крім розтину гнійника ліквідовується внутрішній отвір, який став власне джерелом цього захворювання [http://www.doctor-maximov.ru/paraproktit/]. Як зазначено вище, лікування гострого інфекційного колопроктиту можливе тільки хірургічним шляхом, під час операції здійснюється лише механічне усування гнійника та джерела запалення, виконується дренування гною антисептичними засобами. Але це призводить лише до часткового одужання пацієнта, бо мікроби, що знаходяться в просвіті відділів ШКТ, можуть легко потрапити до вже пошкодженої ділянки, яка лише починає загоюватись, і це може призвести до відновлення запального процесу і переходу гострої форми захворювання до хронічної. Саме для того, щоб уникнути потрапляння бактерій з інших відділів ШКТ є доцільним використання засобів, що мають антимікробні властивості не тільки як місцевого засобу, але й як перорального засобу, що буде знищувати патогенну мікрофлору в просвіті всіх відділів ШКТ, яка може спровокувати поновлення захворювання. Перевагою перорального застосування фармацевтично активної речовини є те, що її дія поширюється на всі ділянки ШКТ, бо огортає всі слизові оболонки при проходженні речовини від ротової порожнини до прямої кишки, а не якусь конкретну ділянку, як при використанні місцево діючих засобів. Слід зазначити також те, що при використанні засобів місцевої дії людина потребує допомоги спеціаліста чи спеціальних засобів для проведення маніпуляції, що, безумовно, ускладнює лікування захворювання. В цьому випадку пероральне застосування має дуже суттєву перевагу, бо не потребує сторонньої допомоги і може здійснюватися хворим самостійно і навіть у домашніх умовах. Аналіз публікацій на тему застосування декаметоксину показав, що він ніколи не використовувався як засіб для перорального введення. Відомі методи використання даного антисептика обмежувались лише на недовгостроковій дії декаметоксину на поверхні шкіри або слизових оболонок. Ці методи включають: інгаляції, полоскання, санацію, дренаж розчинами декаметоксину, примочки, нанесення мазей, гелів, паст, що включають декаметоксин як один з компонентів. Причиною того, що декаметоксин не використовувався як пероральний лікарський засіб може бути відсутність інформації про гостру токсичність декаметоксину, хронічну та специфічну токсичність за тривалого ентерального введення декаметоксину, можливу місцевоподразнювальну та алергізуючу дію, його всмоктуваність та вплив на активність холінестерази крові, також є невизначеною ефективність декаметоксину як антимікробного засобу in vivo, також основною причиною невикористання декаметоксину - це належність його до ПАВ. Таким чином є стійке переконання щодо використання декаметоксину виключно, як ПАВ, тобто для обробки поверхонь, не для внутрішнього застосування. Ще одною причиною невикористання декаметоксину як внутрішнього засобу є його дуже гіркий і неприємний смак. Задачею технічного рішення є вдосконалення лікування кишкових інфекцій мікробної та вірусної етіології. Також задачею цього технічного рішення - є винайдення нової фармацевтично активної речовини для лікування кишкових інфекцій мікробної та вірусної етіології. Ще однією задачею представленого технічного рішення є винайдення нової фармацевтично активної речовини для лікування інфекційного колопроктиту без хірургічного втручання. 3 UA 103367 U 5 10 15 20 25 30 35 40 45 50 55 60 Задача вирішується застосуванням декаметоксину перорально, як принципово нової фармацевтично активної речовини для лікування кишкових інфекцій мікробної та вірусної етіології на прикладі інфекційного колопроктиту. Задача вирішується також застосуванням декаметоксину, як фармацевтично активної речовини для лікування ШКТ та кишкових інфекцій мікробної і вірусної етіології перорально, може бути у вигляді водного розчину з концентраціями в діапазоні 0,02-0,2 % або у вигляді інших фармацевтичних композицій, зокрема рідкого типу. Авторами корисної моделі було запропоновано використання декаметоксину для лікування інфекційних хвороб ШКТ, виходячи з прояву ним широкого спектра антимікробної дії, для цього були проведені дослідження щодо його токсичності при пероральному застосуванні, та щодо визначення його дії на ряд хвороб ШКТ. В результаті були винайдені нові властивості декаметоксину та його вплив на хвороби, які раніше не підлягали медикаментозному лікуванню та доведена можливість його використання перорально завдяки відсутності токсичної дії його на організм. Суть технічного рішення пояснюється кресленнями, де на Фіг. 1 - схема визначення антихолінестеразної активності. Фіг. 2 - кінетичні криві окиснення п-фенетидину (холоста проба). Фіг. 3 - кінетичні криві окиснення п-фенетидину (контрольна група). Фіг. 4 - кінетичні криві окиснення п-фенетидину (дослідна група). Для визначення можливості використання декаметоксину перорально авторами були проведені наступні дослідження: 1. Дослідження здатності декаметоксину до всмоктування із шлунково-кишкового тракту (резорбтивна дія) шляхом визначення його концентрації в перфузаті кишечнику in situ та впливу на активність холінестерази (ХЕ) крові за орального введення; Досліди виконували на 5 білих рандомбредних щурах-самцях і на 8 кроликах породи Шиншила. Ізольовану ділянку кишки перфузували розчином декаметоксину концентрацією 0,02-0,2 %, протягом 30 хв. У перфузаті визначали вміст декаметоксину по реакції інгібування екзогенної ХЕ. Порівнювали ступінь інгібування реакції в присутності перфузату і розчину декаметоксину (0,02 %), що дозволило визначити вміст останнього в перфузаті. Зниження концентрації декаметоксину в перфузаті в порівнянні з таким у вихідному розчині вказує на всмоктування цієї сполуки в кишечнику щурів. В експериментальній групі кролів здатність розчину декаметоксину всмоктуватися в кров визначали за впливом на активність ХЕ через 30 і 60 хв. після одноразового перорального введення в дозі 6 мл/кг, що відповідає 1,2 мг/кг декаметоксину. Проби крові брали до, через 30 і 60 хв. після введення розчину декаметоксину. Тваринам контрольної групи замість розчину декаметоксину вводили 0,9 % розчин натрію хлориду. Як індикаторну реакцію на ацетилхолін використовували реакцію окислення п-фенетидину пероцтовою кислотою (СН3СО3Н), утвореної in situ в допоміжній реакції пергідролізу (з надлишком пероксиду водню) ацетилхоліну - субстрату ферментативної реакції. Схема методу представлена на Фіг. 1. Використано розчин ХЕ 200 АО/мл (ацилгідролаза сироватки крові коня К.Ф.3.1.1.8 НВО "Біомед", Росія VI кл, флакон по 80 мг з активністю 25 АО/мг) і розчин субстрату - ацетилхолін. Визначення проводили спектрофотометрично при 358 нм в кюветі з товщиною шару 10 мм. Швидкість даної реакції характеризує тангенс кута нахилу прямолінійної початкової ділянки кінетичної кривої після індукційного періоду в координатах "оптична щільність продукту окислення п-фенетидину - год.". Активність ХЕ в крові кроликів визначали описаним вище ензимо-кінетичним методом (Фіг. 1 - Схема визначення антихолінестеразної активності інгібіторів за невитраченим ацетилхоліном із використанням індикаторної реакцій сполученого окиснення п-фенетидину (хромоген) пероксидом водню), заснованим на використанні як індикаторної реакції на ацетилхолін окислення п-фенетидину (Хромоген) пероцтовою кислотою, утвореною в початковій реакції пергідролізу (з надлишком пероксиду водню), що дозволяє контролювати активність ферменту ХЕ в присутності екзогенного інгібітора - декаметоксину (Інгібітор). Зниження активності ХЕ через 30 і 60 хв після введення тваринам розчину декаметоксину у порівнянні з вихідною і такою у тварин контрольної групи слугувало маркером всмоктування декаметоксину в шлунковокишковому тракті. Результати дослідження представлені на Фіг. 2-4 та таблицях 1-3. На Фіг. 2 - Кінетичні криві сполученого окислення п-фенетидину пероксидом водню в присутності АХ (контрольна проба), АХ+ХЕ (холоста проба), суміші (ХЕ+декаметоксин)+АХ (калібрувальна проба), суміші (ХЕ+перфузат)+АХ (випробовувана проба) (Примітка: АХ - ацетилхолін, ХЕ - холіноестераза) 4 UA 103367 U 5 наведено кінетичні криві, отримані в досліді з перфузією кишечнику щурів. Значення тангенса кута нахилу випробовуваних проб і результати кількісного визначення вмісту декаметоксину в перфузаті кишечнику щурів представлені в таблиці 1. Вміст декаметоксину в розчині становить 0,200 мг/мл, в перфузаті - 0,195±0,003 мг/мл. Статистично значущі відмінності між змістом декаметоксину у вихідному розчині і перфузаті кишечнику щурів відсутні. Це свідчить про те, що декаметоксин не всмоктується в кишечнику. Таблиця 1 Вивчення вмісту декаметоксину в перфузаті кишечнику щурів Досліджувані розчини Аліквота перфузата кишковика щурів Розчин декаметоксину № п/п тварини tgα 1 2 3 4 5 0,0215 0,0232 0,0229 0,0234 0,0225 0,0233 Вміст декаметоксину в Середнє значення вмісту пробі декаметоксину, мг/мл % мг/мл 0,019 0,185 0,020 0,199 0,020 0,197 0,195±0,003 0,020 0,201 0,019 0,193 0,020 0,200 0,200 Примітка. tgα - тангенс кута нахилу кінетичної кривої. 10 15 20 На Фіг. 3 - Кінетичні криві сполученого окислення п-фенетидину пероксидом водню в присутності ацетилхоліну (контрольна проба), суміші ацетилхоліну та ендогенної ХЕ плазми крові кролів контрольної групи до, через 30 і 60 хв. після введення 0,9 % розчину натрію хлориду і Фіг. 4 - Кінетичні криві сполученого окислення п-фенетидину пероксидом водню в присутності ацетилхоліну (контрольна проба), суміші ацетилхоліну та ендогенної ХЕ плазми крові кролів дослідної групи до, через 30 і 60 хв. після введення розчину декаметоксину відповідно наведені кінетичні криві, отримані в контрольній і дослідній групах кроликів. Різниця значень тангенсів кута нахилу кривої контрольної та холостої проби - це діапазон, який відображає відносну зміну активності ХЕ від умовних 100 % (холоста проба) до 0 % (контрольна проба). У табл. 2 наведені отримані в досліді значення тангенсів кута нахилу кінетичних кривих. Вихідна активність ХЕ, визначена в плазмі крові кролів до введення розчину декаметоксину, прийнята за 100 %. Таблиця 2 Значення тангенсів кута нахилу кінетичних кривих проб і зміни тангенса кута нахилу кінетичної кривої, що відповідає зміні активності холінестерази на 1 %, під впливом 0,02 % розчину декаметоксину № п/п 1 2 3 4 1 2 3 4 Значення tgα Через 30 хв. після Через 60 хв. після Вихідний стан Контрольна проба, введення розчину введення розчину (холоста проба), tgαк декаметоксину, декаметоксину, tgα0 tgα30 tgα60 0,0677 Контрольна група (тварини, що отримували 0,9 % розчин натрію хлориду) 0,0305 0,0274 0,0280 0,0307 0,0278 0,0303 0,0305 0,0281 0,0317 0,0306 0,0273 0,0301 Дослідна група (тварини, що отримували 0,02 % розчин декаметоксину) 0,0284 0,0273 0,0297 0,0313 0,0237 0,0299 0,0316 0,0313 0,0276 0,0273 0,0237 0,0316 5 Δtg1 % 0,000372 0,000370 0,000372 0,000371 0,000393 0,000364 0,000361 0,000404 UA 103367 U Результати визначення активності ХЕ наведені в таблиці 3. Таблиця 3 Зміна активності холінестерази плазми кроликів в експерименті під впливом 0,02 % розчину декаметоксину Умови досліду, розчини 0,9 % розчин натрію хлориду Розчин декаметоксину 5 10 15 20 25 № п/п 1 2 3 4 Середнє 1 2 3 4 Середнє Зміна активності холінестерази відносно вихідного стану після введення розчину декаметоксину, % вихідна Через 30 хв. Через 60 хв. Через 30 хв. Через 60 хв. 100 108,3 106,7 8,33 6,72 100 107,8 101,1 7,84 1,08 100 106,5 96,8 6,45 -3,23 100 108,9 101,3 8,89 1,35 100 107,8±0,5 101,5±2,0 7,88±1,48 1,48±2,04 100 102,8 96,7 2,80 -3,31 100 120,9 103,8 20,88 3,85 100 100,8 111,1 0,83 11,08 100 108,9 89,4 8,91 -0,64 100 108,4±4,5 100,2±4,7 8,36±4,52 0,24±4,67 Активності холінестерази плазми кроликів до і після введення розчину декаметоксину, % Статистично значущих відмінностей активності ферменту плазми кроликів після введення розчину декаметоксину між контрольною та дослідною групами не виявлено. Це свідчить про відсутність всмоктування декаметоксину із шлунково-кишкового тракту кроликів, що підтверджує наведені вище дані про відсутність його всмоктування з тонкої кишки щурів. Виходячи з цього, можна зробити висновок, що декаметоксин можна використовувати перорально, тому що він практично не всмоктується в ШКТ, діє лише у просвіті кишечнику та не впливає на життєдіяльність інших систем органів. Всі дослідження проводились на основі розчину декаметоксину в воді, для представлення в матеріалах заявки вибрано концентрації з варіацією 0,02-0,2 %, проте, для лікування різних ступенів хвороб ШКТ та кишкових інфекцій мікробної і вірусної етіології перорально, можуть бути використані інші концентрації, тому ці приклади наведені лише для пояснення результатів. 2. Дослідження параметрів гострої токсичності розчину декаметоксину. Вивчення гострої токсичності розчина декаметоксину при пероральному введенні проводили також на безпородних щурах обох статей (n=60) і безпородних мишах обох статей (n=72) з визначенням напівлетальної дози (ЛД50). Пероральне введення щурам максимально допустимого обсягу (5 мл) розчину декаметоксину підтвердило відсутність інтоксикації у тварин і неможливість встановлення ЛД50. Визначення ЛД50 розчину декаметоксину на щурах і мишах показало, що величина ЛД50 розчину декаметоксину знаходиться в інтервалі доз 500-750 мг/кг для щурів (табл. 4) і після додаткового дослідження склала 586 мг/кг при внутрішньошлунковому введенні. Відповідно до загальноприйнятої класифікації, розчин декаметоксину при одноразовому внутрішньошлунковому введенні щурам належить до IV класу малотоксичних речовин (500 мг/кг
ДивитисяДодаткова інформація
Назва патенту англійськоюApplication of decamethoxinum as pharmaceutically active substances for the treatment of gastro-intestinal tract and intestinal infections orally.
Автори англійськоюDerkach Nataliia Mykolaivna
Назва патенту російськоюПрименение декамэтоксина как фармацевтически активного вещества для лечения желудочно-кишечного тракта и кишечных инфекций перорально.
Автори російськоюДеркач Наталья Николаевна
МПК / Мітки
МПК: A61P 1/00, A61K 31/00
Мітки: речовини, фармацевтично, лікування, перорально, тракту, активної, інфекцій, застосування, кишкових, декаметоксину, шлунково-кишкового
Код посилання
<a href="https://ua.patents.su/53-103367-zastosuvannya-dekametoksinu-yak-farmacevtichno-aktivno-rechovini-dlya-likuvannya-shlunkovo-kishkovogo-traktu-ta-kishkovikh-infekcijj-peroralno.html" target="_blank" rel="follow" title="База патентів України">Застосування декаметоксину як фармацевтично активної речовини для лікування шлунково-кишкового тракту та кишкових інфекцій перорально</a>
Попередній патент: Застосування декаметоксину як фармацевтично активної речовини для лікування інфекційних захворювань шлунково-кишкового тракту та шлункових інфекцій перорально
Наступний патент: Спосіб реабілітації пацієнтів з контрактурою суглобів після поранення, травми та оперативного втручання
Випадковий патент: Каталізатор одержання вуглеводнів із синтез-газу