Спосіб прогнозування клінічного перебігу гострого деструктивного панкреатиту
Номер патенту: 106268
Опубліковано: 25.04.2016
Автори: Андрющенко Дмитро Вікторович, Когут Любомир Миколайович, Андрющенко Віктор Петрович, Андрушевська Ольга Юліанівна
Формула / Реферат
Спосіб прогнозування клінічного перебігу гострого деструктивного панкреатиту, що включає цитологічне дослідження панкреатогенних патологічних рідин, отриманих за допомогою мініінвазивних інтервенційно-сонографічних чи відеолапароскопічних способів, який відрізняється тим, що оцінюють результати цитологічного дослідження та при наявності в мазках нейтрофільних гранулоцитів з ознаками виражених дегенеративних змін ядра (каріопікнозу, каріорексису, каріолізису) і цитоплазми (токсогенної зернистості, вакуолізації) роблять висновок про прогностично несприятливий перебіг захворювання.
Текст
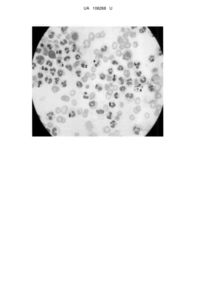
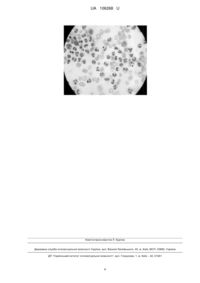
Реферат: Спосіб прогнозування клінічного перебігу гострого деструктивного панкреатиту включає цитологічне дослідження панкреатогенних патологічних рідин, отриманих за допомогою мініінвазивних інтервенційно-сонографічних чи відеолапароскопічних способів. Оцінюють результати цитологічного дослідження та при наявності в мазках нейтрофільних гранулоцитів з ознаками виражених дегенеративних змін ядра (каріопікнозу, каріорексису, каріолізису) і цитоплазми (токсогенної зернистості, вакуолізації) роблять висновок про прогностично несприятливий перебіг захворювання. UA 106268 U (12) UA 106268 U UA 106268 U 5 10 15 20 25 30 35 40 45 50 55 60 Корисна модель стосується медицини, зокрема хірургії, і може бути використана для прогнозування клінічного перебігу гострого деструктивного панкреатиту. Проблема прогнозування перебігу та вибору тактики лікування гострого деструктивного панкреатиту залишається одним з невирішених та актуальних питань сучасної абдомінальної хірургії. Вибрана тактика лікування має бути багатовекторною, патогенетично обґрунтованою, комплексною, включаючи різні компоненти консервативного (інфузійна, дезінтоксикаційна, аналгетична, протизапальна терапія, антибіотикопрофілактика та антибіотикотерапія, корекція моторно-евакуаторних розладів шлунково-кишкового тракту, екстракорпоральна детоксикація, ентеральне і парентеральне харчування тощо) та хірургічного лікування (сучасні мініінвазивні втручання - інтервенційно-сонографічні пункції та дренування обмежених рідинних панкреатогенних скупчень черевної порожнини І заочеревинного простору за допомогою спеціальних дво- чи триступеневих систем типу "pig tail" чи "straight", відеолапароскопія з евакуацією токсичного ексудату із вільної черевної порожнини при розвитку ферментативного перитоніту, та традиційні хірургічні втручання - лапаротомія, оментобурсостомія, ретроперитонеостомія, некрсеквестректомія з формуванням систем відкритого, напіввідкритого та закритого способу дренування гнійних вогнищ). Від правильного вибору того чи іншого способу лікування на певному етапі розвитку захворювання у конкретного пацієнта залежить успіх лікування в цілому. Не дивлячись на весь арсенал доступних на сьогоднішній день засобів, вибір правильної лікувальної тактики є досить складним завданням, тому пошук нових достовірних критеріїв прогнозування перебігу деструктивного панкреатиту є актуальним та вкрай необхідним. Відомий спосіб оцінки тяжкості гострого деструктивного панкреатиту, взятий за прототип, який полягає у цитологічному дослідженні панкреатогенних патологічних рідин, отриманих за допомогою мініінвазивних способів пункції та дренування. При виявленні в мазках атипових клітин епітеліального ряду, а саме мезотеліоцитів з анізоцитозом, анізонуклеозом, ядрами, що відтиснуті до периферії (у вигляді паличок, пісочного годинника), серпоподібних та пікнотичних клітин, роблять висновок про тяжкий, прогностично несприятливий перебіг захворювання [Андрющенко Д.В. Малоинвазивные интервенционные технологи в оценке тяжести клинического течения острого некротического панкреатита / Д.В. Андрющенко, Л.Н. Когут, В.П. Андрющенко // Український журнал хірургії. - 2013. - № 3 (22). - С. 140-144.]. Проте існуючий спосіб визначення ознак тяжкого, прогностично несприятливого перебігу захворювання має дещо обмежене значення, оскільки перераховані цитологічні зміни можуть виявлятись не у всіх випадках тяжкого перебігу гострого деструктивного панкреатиту, тому що мезотеліоцити є вистилкою серозних оболонок (сальникова сумка, вільна черевна порожнина) та не виявляються у пунктатах рідинних скупчень, що локалізуються у позаочеревинному просторі. В основу корисної моделі поставлено задачу пошуку нових, більш універсальних цитологічних критеріїв тяжкості клінічного перебігу гострого деструктивного панкреатиту, які б виявлялись у пунктатах патологічних панкреатогенних рідин різних топографо-анатомічних локалізацій. Поставлена задача вирішується тим, що у способі прогнозування клінічного перебігу гострого деструктивного панкреатиту, що включає цитологічне дослідження панкреатогенних патологічних рідин, отриманих за допомогою мініінвазивних інтервенційно-сонографічних чи відеолапароскопічних способів, згідно з корисною моделлю, оцінюють результати цитологічного дослідження та при наявності в мазках нейтрофільних гранулоцитів з ознаками виражених дегенеративних змін ядра (каріопікнозу, каріорексису, каріолізису) і цитоплазми (токсогенної зернистості, вакуолізації) роблять висновок про прогностично несприятливий перебіг захворювання. У пропонованому способі акцентують увагу на клітинах гранулоцитарного ряду, а саме нейтрофілах, і при виявленні в них ознак виражених дегенеративних змін - каріопікнозу, каріорексису, каріолізису (етапи некробіозу) поряд з іншими ознаками: токсогенної зернистості, вакуолізації цитоплазми - роблять висновок про прогностично несприятливий перебіг захворювання та неефективність обраного методу лікування, що потребує зміни лікувальної тактики з переходом на більш радикальні способи санації гнійно-некротичних вогнищ. Виявлені морфологічні зміни з боку нейтрофільних гранулоцитів є більш універсальними, оскільки останні відносяться до клітин мікрофагів, що відіграють ключову роль в типових процесах запалення, незалежно від його локалізації та мікрооточення. Вони одними з перших клітин імунної системи активно виходять в тканини та шляхом хемотаксису рухаються до вогнища запалення, приймаючи активну участь в боротьбі з мікробними агентами та викликаючи ушкодження уражених тканин. Процеси, які відбуваються на мікрорівні у вогнищі 1 UA 106268 U 5 10 15 20 25 30 35 40 45 50 55 60 запалення, що проявляються в морфологічних змінах нейтрофілів, свідчать про функціональний стан імунної системи пацієнта в цілому та про адекватність запальної відповіді організму інтенсивності ушкоджуючого агента. Оскільки нейтрофільні гранулоцити є авангардом лейкоцитів, то і дегенеративно-дистрофічні зміни, при неповному фагоцитозі чи надто агресивному та вірулентному збуднику, будуть виявлятись у них найшвидше. Дегенеративні зміни лейкоцитів характеризуються відкладанням в клітинах різноманітних ендо- і екзогенних речовин, внаслідок чого вони втрачають здатність до нормального функціонування та поділу, тобто є морфологічною ознакою їх функціональної недостатності. Патологічні речовини, що депонуються в клітині та викликають дегенеративні зміни лейкоцитів, можуть бути різноманітними за своєю природою: ліпіди (жирова дегенерація), пігменти (пігментна дегенерація) та інші. До дегенеративних змін відносяться: токсогенна зернистість нейтрофільних гранулоцитів, вакуолізація ядра та цитоплазми. Утворення токсогенної зернистості відбувається всередині клітин внаслідок фізико-хімічних змін білкової структури цитоплазми під впливом продуктів екзогенної чи ендогенної Інтоксикації. Вакуолізація цитоплазми, що виявляється рідше, ніж токсогенна зернистість нейтрофільних гранулоцитів, та в більш заавансованих випадках розвитку захворювання, може бути проявом триваючої тяжкої інтоксикації, однак має не менш важливе діагностичне та прогностичне значення. Дегенеративно-дистрофічні зміни ядра виявляються пізніше та свідчать про більш тяжкий перебіг захворювання. До пізніх ознак дегенерації, що виявляється в особливо тяжких та прогностично несприятливих випадках перебігу захворювання при персистуючому джерелі ендогенної інтоксикації, відносяться: гіперсегментація ядер, фрагментоз, каріопікноз, каріорексис, хроматиноліз, каріолізис. Крайнім ступенем вираженості дегенеративних змін є цитоліз, тобто повний розпад клітини. Пропонований спосіб ілюструється мікрофотографією, де відображена цитограма пунктату із правого ретроколярного простору з ознаками тяжкого несприятливого перебігу панкреатиту, де 1 - нейтрофіли незмінені, 2 - нейтрофіли в стані каріорексису із збереженою специфічною зернистістю, 3 - нейтрофіли в стані каріорексису (виражена атрофія), 4 - нейтрофіли в стані каріорексису із вираженими ознаками розпаду ядра. Спосіб здійснюють таким чином. З клітинного осаду отриманої за допомогою мшіінвазійних способів панкреатогенної рідини готують мазки за відомою методикою для дослідження серозних рідин та вмісту кістозних утворів [Руководство по клинической лабораторной диагностике: учебное пособие, ч. 1-2, 2-е изд. перераб. и дополн. / М.А. Базарнова, А.И. Воробьев, З.С. Баркаган [и др.] - К.: Выща школа, 1991. - 615 с.]. Для дослідження береться весь отриманий об'єм рідини, до якого додають стабілізатор - 5 % розчин цитрату натрію з розрахунку 20 мл на 100 мл рідини. Клітинний осад отримують шляхом відстоювання або центрифугування зі швидкістю 1,5 тис. об/хв. протягом 510 хв. У випадку великого об'єму рідини (1,5-2 л) перед центрифугуванням застосовують проміжний етап концентрування рідини шляхом відстоювання та зливання надосадової фракції. З осаду готують 4-6 мазків, які висушують на повітрі при кімнатній температурі протягом 1 год. та фарбують за методом Папенгейма. Мікроскопію проводять як нативного, так і пофарбованого препарату при малому та при великому збільшенні оптичного мікроскопа (імерсійна система). При виявленні в мазках нейтрофільних гранулоцитів з ознаками дистрофічних змін цитоплазми (вакуолізація, токсогенна зернистість), а особливо ядра (каріопікноз, каріорексис, каріолізис), роблять висновок про несприятливий перебіг захворювання, неефективність проведеного комплексу лікувальних заходів та про необхідність зміни лікувальної тактики у бік використання більш агресивних хірургічних втручань. Клінічний приклад. Хвора М., 62 p., була прийнята ургентно, через 8 год. від початку захворювання із скаргами на інтенсивні постійні болі в ділянці епігастрію з іррадіацією в обидві поперекові ділянки, нудоту, кількаразову блювоту, що не приносила полегшення, виражену загальну слабкість. Захворювання пов'язує з вживанням алкоголю та гострої їжі напередодні. В анамнезі: Виразкова хвороба шлунка, ІХС, Стабільна стенокардія ФК II А, Постінфарктний та кардіосклеротичний кардіосклероз, Гіпертонічна хвороба II ст. Пневмосклероз. Емфізема легень. Хронічний обструктивний бронхіт в ст. ремісії. Загальний стан на момент госпіталізації оцінено як середньо тяжкий, AT 140/95 мм рт. ст., Ps 80 /хв., живіт симетричний, піддутий, при пальпації болючий у верхньому поверсі, без перитонеальних явищ. Лабораторно при госпіталізації: Нb 140 г/л, L 9,8 Г/л, діастаза сечі 1024 ОД, заг. білок 60,7 г/л, білірубін 21,0 мкмоль/л, сечовина 11,4 ммоль/л, цукор крові 10,0 ммоль/л. На УЗД при поступленні: печінка зерниста, дифузно ущільнена, внутрішньопечінкові протоки та холедох не поширені. Жовчний міхур не блокований, стінка 2 мм, у просвіті міхура множинні 2 UA 106268 U 5 10 15 20 25 30 35 конкременти діаметром 15-20 мм. Підшлункова залоза: 43*29 × 30 мм, дифузно неоднорідна, контур горбистий, не чіткий. Набряк заочеревинного простору, смужка рідини у сальниковій сумці та у вільній черевній порожнині між петлями кишок. На основі клінічної картини, лабораторних та променевих методів обстеження встановлено попередній діагноз: Гострий панкреатит, тяжкий перебіг. Не дивлячись на призначену Інтенсивну консервативну терапію, стан хворої погіршувався, наростала інтенсивність больового синдрому, негативна динаміка лабораторних показників, у зв'язку з чим хвора переведена для подальшого лікування у реанімаційно-анестезіологічне відділення (РАВ). На третій день перебування в РАВ у ділянці епігастрія почав визначатись запальний інфільтрат, негативна динаміка на УЗД органів черевної порожнини у вигляді появи гіпоехогенних інфільтратів в обох ретроколярних та паранефральних просторах з ділянками розрідження розміром 3-4 см. На ФГДС виражена екзодефорація антрального відділу шлунка та цибулини дванадцятипалої кишки з парезом її зацибулинних відділів. Під ультрасонографічним наведенням проведено діагностичну пункцію ретроколярного розрідження справа, отримано до 50 мл бурої мутної рідини без запаху з високою амілолітичною активністю (4096 ОД), яку передано на цитологічне дослідження. Як видно з представленої ілюстрації, лейкоцити у великій кількості у всіх полях зору: нейтрофільні гранулоцити незмінені 1 та з ознаками вираженої атрофії і дискаріозу (ядро в стані каріорексису); до 7-10 в окремих полях зору зі збереженою специфічною зернистістю 2 і без неї 3, деякі клітини з ознаками повного розпаду ядра 4. Дані зміни потрактовано як ознаки прогностично несприятливого перебігу гострого деструктивного панкреатиту, що слугувало причиною відмови від продовження застосування мініінвазивних методик та спонукало до відкритого хірургічного лікування за життєвими показниками, не дивлячись на високий ступінь реанімаційно-анестезіологічного ризику у хворої. Після передопераційної підготовки та максимально можливої корекції зрушень основних життєво важливих систем організму, на 6-у добу після госпіталізації хвора прооперована ретроперитонеостомія, некрсеквестроектомія, підвісна єюностомія під ендотрахеальним наркозом. Стан пацієнтки в ранньому післяопераційному періоді критичний, продовжувалась ШВЛ протягом 2-х діб, проте з поступовою позитивною динамікою. Після стабілізації стану, на 10-у добу післяопераційного періоду хвора переведена в хірургічне відділення, на 42-у добу після госпіталізації, в задовільному стані, з зовнішньою панкреатичною норицею в лівій поперековій ділянці із мінімальними виділеннями з неї, виписана на амбулаторне лікування. Запропонований спосіб прогнозування клінічного перебігу гострого деструктивного панкреатиту дає змогу отримати додаткову інформацію про ефективність застосованих консервативних та мінінвазивних методів лікування, а також встановити додаткові покази до зміни лікувальної тактики з метою досягнення кращих результатів лікування. 40 ФОРМУЛА КОРИСНОЇ МОДЕЛІ 45 Спосіб прогнозування клінічного перебігу гострого деструктивного панкреатиту, що включає цитологічне дослідження панкреатогенних патологічних рідин, отриманих за допомогою мініінвазивних інтервенційно-сонографічних чи відеолапароскопічних способів, який відрізняється тим, що оцінюють результати цитологічного дослідження та при наявності в мазках нейтрофільних гранулоцитів з ознаками виражених дегенеративних змін ядра (каріопікнозу, каріорексису, каріолізису) і цитоплазми (токсогенної зернистості, вакуолізації) роблять висновок про прогностично несприятливий перебіг захворювання. 3 UA 106268 U Комп’ютерна верстка Л. Бурлак Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 4
ДивитисяДодаткова інформація
Назва патенту англійськоюA method of predicting clinical course of acute destructive pancreatitis
Автори англійськоюAndriuschenko Dmytro Viktorovych, Kogut Liubomyr Mykolaiovych, Andrushevska Olha Yulianivna, Andriuschenko Viktor Petrovych
Назва патенту російськоюСпособ прогнозирования клинического течения острого деструктивного панкреатита
Автори російськоюАндрющенко Дмитрий Викторович, Когут Любомир Николаевич, Андрушевская Ольга Юлиановна, Андрющенко Виктор Петрович
МПК / Мітки
МПК: G01N 33/48
Мітки: прогнозування, панкреатиту, деструктивного, гострого, спосіб, перебігу, клінічного
Код посилання
<a href="https://ua.patents.su/6-106268-sposib-prognozuvannya-klinichnogo-perebigu-gostrogo-destruktivnogo-pankreatitu.html" target="_blank" rel="follow" title="База патентів України">Спосіб прогнозування клінічного перебігу гострого деструктивного панкреатиту</a>
Попередній патент: Спосіб діагностики фази інфекційно-септичного процесу у хворих на інфекційний ендокардит
Наступний патент: Анкерний вузол шпали залізобетонної для рейкової колії
Випадковий патент: Спосіб прогнозування виникнення епізодів шлуночкової екстрасистолії у хворих на гіпертонічну хворобу іі стадії