Адаптогенний препарат та спосіб його одержання
Номер патенту: 13788
Опубліковано: 30.06.1998
Автори: Тищенко Галина Миколаївна, Тараховський Мирон Лазаревич, Шевцова Ніла Федорівна, Загорій Володимир Антонович, Ципкун Анатолій Григорович, Денисов Микола Дмитрович, Мельничук Дмитро Олексійович, Гулий Максим Федотович, Стогній Ніна Андріївна, Денисова Маргарита Федорівна, Забарський Олег Шулимович
Формула / Реферат
1. Адаптогенный препарат, содержащий гидрокарбонат натрия и сульфаты магния, марганца и цинка, отличающийся тем, что он дополнительно содержит цитрат натрия, поливинилпирролидин, аэросил, стеарат кальция и крахмал при следующем соотношении компонентов, мас.%:
2. Способ получения адаптогенного препарата, включающий измельчение и смешивание сульфатов магния, марганца и цинка с гидрокарбонатом натрия, отличающийся тем, что в смесь измельченных сульфата магния, гидрокарбоната и цитрата натрия вводят при перемешивании последовательно растворы сульфатов марганца и цинка и поливинилпирролидона, гранулируют, сушат при температуре 45-65°С, снова гранулируют, опудривают смесью аэросила, стеарата кальция и крахмала и полученный целевой продукт таблетируют.
Текст
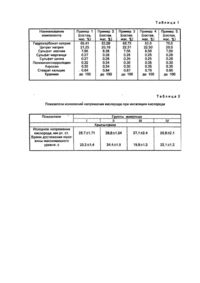
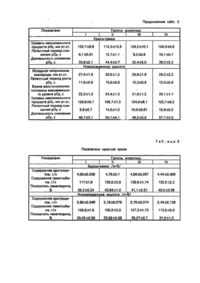
Изобретение относится к медицине, а именно, к лечебным препаратам, используемым для усиления адаптогенных возможностей организма, изобретение также касается способов получения указанных препаратов. При изучении сущности механизмов адаптации организма наблюдаются различные уровни адаптационных реакций: организменный, органный, тканевой, клеточный, субклеточный, молекулярный. Для повышения приспособительных возможностей используют адаптогенные препараты, выбор которых зависит от особенностей патологического состояния. Так, например, при акушерской и экстрагенитальной патологии беременных, сопровождающейся развитием хронической гипоксии плода и новорожденного, в качестве адаптогена применяют метилурацил и пентоксид [1]. Эти препараты способствуют активации биосинтетических процессов клетки, в частности, улучшают показатели красной крови беременных, однако данные препараты не оказывают существенного влияния на состояние плода. В гастроэнтерологической практике для усиления репаративных процессов при различных формах гепатита применяют в качестве средств адаптации эссенциале, карсил, силибор [2], улучшающие в частности, обмен РНК в тканях печени. Однако предупреждение формирования и развития цирротических процессов в печени при использовании данных препаратов не наблюдается. Прототипом предложенного препарата (выбранным по максимальному количеству сходных с изобретением признаков) является солевая смесь, содержащая гидрокарбонат натрия в сочетании с ионами Мо++ Мn++, n++. Эта смесь активизирует реакции карбоксилирования и используется для ускорения регенерации крови при кровопотерях [3]. Однако при хранении обнаружено, что смесь нестабильна, гигроскопична, т.к. при сроке хранения менее 4 месяцев она расслаивается, спрессовывается, нарушается равномерное распределение компонентов. Использование известной смеси как адаптогена неизвестно. Прототипом предложенного способа является способ получения указанной солевой смеси [3], который включает следующие операции: сначала измельчают и смешивают сульфаты магния, марганца и цинка, затем добавляют измельченный гидрокарбонат натрия. Схема получения состава-прототипа несложная, однако, в способе не предусмотрена защита от химического взаимодействия компонентов смеси, равномерное распределение и связывание частиц, не обеспечена минимальная гигроскопичность смеси, что определяет малый срок хранения препарата. Кроме того, использование получаемой смеси затруднено, т.к. в способе не предусмотрено дозирование получаемого препарата. При разработке нового препарата и способе его получения была поставлена задача: создать эффективный адаптогенный препарат, обладающий антигипоксическими, гепатопротекторными свойствами, в отношении беременной, плода и потомства; разработать производственную технологическую схему получения нового стабильного адаптогенного препарата в таблетированной форме со сроком хранения не менее 2 лет, Предложенное изобретение представляет собой комплекс решений: новый состав адаптогенного препарата и способ его получения. Адаптогенный препарат содержит компоненты в следующем соотношении, маc. %: Гидрокарбонат натрия 63,0-70,0 Цитрат натрия 20,0-22,50 Сульфат магния 7,50-8,50 Сульфат марганца 0,25-0,28 Сульфат цинка 0,25-0,28 Поливинилпирролидон 0,30-0,35 Аэросил 0,30-0,35 Стеарат кальция 0,60-0,70 Крахмал Остальное Способ производственного получения адаптогенного препарата включает следующие операции: измельченные сульфат магния и гидрокарбонат и цитрат натрия смешивают, в полученную массу вводят последовательно при перемешивании растворы сульфатов марганца и цинка и поливинилпирролидона, смесь гранулируют, сушат при температуре 45-65°С, снова гранулируют, опудривают смесью аэросила, стеарата кальция и крахмала и таблетируют. Экспериментальные исследования на беременных и потомстве, клинические наблюдения на детях, направленные на изучение действия нового адаптогенного препарата, в сравнении с известными аналогами, показывают принципиальные преимущества нового адаптогена. Так было доказано, что: новый препарат способствует нормализации не только показателей транспорта и капиллярно-тканевой диффузии кислорода, но и улучшению утилизации кислорода в мышечной ткани беременных и новорожденных, что не достигается при использовании метилурацила; новый препарат при введении самкам с моделью хронической гипоксии приводит к улучшению показателей красной крови как у самок-крыс, так и у новорожденных крысят практически до уровня этих показателей у здоровых животных, что не достигается у новорожденных при приеме метилурацила; новый препарат способствует более существенному уменьшению постимплантационной гибели зародышей в сравнении с метилурацилом; новый препарат обладает выраженным гепатопротекторным, а именно, антицирротическим и репаративным эффектом, что принципиально отличает его от других общепринятых препаратов - репарантов печени (карсил, эссенциале, витамины А, Е). Следовательно, благодаря качественному и количественному сочетанию компонентов нового препарата выявляется неожиданный синергический эффект, попытка достижения которого продолжительное время не удавались специалистам, несмотря на существующую общественную потребность. Новый результат заключается в разработке стабильного адаптогенного препарата в дозированной лекарственной форме (таблетки), действующего на органном, тканевом и субклеточном уровне путем проявления антигипоксических и гепатопротекторных свойств у беременных, плодов, новорожденных и детей. В производственой схеме получения препарата исключается химическое взаимодействие компонентов, достигается необходимая гомогенность частиц за счет лучшего их распределения и связывания, существенно снижается гигроскопичность (срок годности препарата - 2 года), разработана таблетированная, строго дозированная форма препарата. Осуществление изобретения подтверждается конкретными примерами состава, способа получения препарата, экспериментальными и клиническими исследованиями специфического действия нового адаптогена в сравнении с известными аналогами. Исследования адаптогенного действия нового препарата путем варьирования соотношения указанных компонентов показывают, что снижение указанных минимальных соотношений компонентов отрицательно влияет на адаптогенную активность препарата, а увеличение максимальных количеств компонентов неоправдено, т.к. адаптогенные свойства препарата практически не улучшаются, а расход компонентов нерентабельно возрастает. Указанный диапазон температур при сушке влажной гранулированной массы объясняется тем, что при уменьшении температуры менее 45° процесс сушки значительно продлевается - более 10 часов, а при росте температуры выше 65°С возможно разложение цитрата натрия. Пример 1. Сначала измельчают гидрокарбонат натрия - 66,41 кг, цитрат натрия 21,25 кг, сульфат магния 7,96 кг на молотковой мельнице, а сульфаты марганца и цинка по 0,27 кг нa шаровой мельнице. В двух стеклянных стаканах (200 мл), снабженных мешалкой и нагревательным устройством помещают отдельно сульфат марганца и сульфат цинка и доливают дистиллированную воду, перемешивают до полного растворения. Приготовляют в нержавстальной емкости (10 л) 0,32% раствор поливинилпирролидона путем растворения в дистиллированной воде при перемешивании. В смеситель (200 л) загружают в указанных количествах взвешенные гидрокарбонат натрия, цитрат натрия, сульфат магния и перемешивают 10 мин. Затем вливают указанные растворы сульфата марганца и сульфата цинка. Перемешивают еще 10 мин, приливают 0,32% раствор поливинилпирролидона, снова перемешивают до получения зернистообразной массы. Влажную массу гранулируют, сушат при температуре 45°С в течение 8 часов в калориферной сушке СШ-14. Высушенную массу снова гранулируют, опудривают в смесителе при перемешивании с 0,32 кг аэросила, 2,56 кг крахмала, 0,64 кг стеарата кальция. А затем таблетируют на таблетпрессе РТМ-41М2В и получают таблетки массой 0,74-0,82 г, состав которой указан в табл.1. Примеры 2-5. Составы 2-5 получают по схеме, описанной в примере 1, но при получении состава 2,4 и 3,5 влажную смесь после гранулирования сушат при 55 и 65°С соответственно. Пример 6. Исследование адаптогенного действия намацита в сравнении с метилурацилом в опытах на модели хронической гипоксии на беременных беспородных белых крысах (25 животных) и новорожденных крысятах от этих крыс (184 животных). Всех животных распределяют на 4 группы: I - интактные беременные самки белых крыс, содержащиеся в условиях вивария и новорожденные крысята от этих самок; II - беременные самки белых крыс, находящиеся на протяжении всей беременности в условиях хронической гипоксии; III - беременные самки белых крыс, находящиеся на протяжении всей беременности в условиях гипоксии, которым ежедневно 1 раз в сутки вводят через зонд новый препарат в дозе 700 мг/кг (составы 1-5); IV - беременные самки белых крыс, находящиеся на протяжении всей беременности в условиях гипоксии, которым ежедневно 1 раз в сутки вводят через зонд метилурацил в дозе 15 мг/кг [4]. Аналогично сформированы группы II—IV новорожденных крысят. Хроническую гипоксическую гипоксию вызывают с помощью барокамеры приточно-вытяжного типа, где животные находятся на "высоте" 3000-3200 м круглосуточно с часовым перерывом для питания. 6.1. У самок на 20-21 день беременности и у новорожденных крысят в первые сутки их постнатальной жизни определяют напряжение кислорода (рО2) и его изменение при ингаляции животному кислорода. Результаты представлены в табл.2. Введение самкам, содержащимся в условиях хронической гипоксии, нового препарата сопровождается нормализацией показателей полярограммы, которые не отличаются от таковых у животных I группы (контрольной). Характерно также, что показатели, характеризующие интенсивность утилизации кислорода тканями у этих животных, достоверно лучше, чем у самок, получающих во время всей беременности метилурацил. Аналогичная закономерность выявляется и при анализе полярограмм новорожденных крысят. Так, если введение самкам метилурацила нормализуют только показатели транспорта и капиллярно-тканевой диффузии кислорода, то применение нового препарата способствует также улучшению утилизации кислорода в мышечной ткани. 6.2. На 20-21 день беременности исследуют содержание эритроцитов, гемоглобина, показатель гематокрита в периферической крови самок. Эти же показатели исследуют у новорожденных крысят от этих самок (табл.3). В периферической крови новорожденных крысят от самок, содержащихся на протяжении всей беременности а условиях гипоксии (группа II), уменьшается содержание эритроцитов и гемоглобина, снижается показатель гематокрита. Введение беременным самкам III группы нового препарата приводит к выраженному увеличению содержания эритроцитов и гемоглобина в периферической крови новорожденных крысят, по сравнению с новорожденными крысятами от нелеченых самок. Следует подчеркнуть, что исследуемые показатели у крысят от самок, получавших новый препарат восстанавливаются до величины, наблюдаемых у крысят J контрольной группы, что не достигается у крысят от самок, получавших метилурацил (группа IV). 6.3. Показатели внутриутробной гибели зародышей у самок представлены в табл.4. Введение самкам нового препарата существенно снижает постимплантационную гибель зародышей. Различия считают достоверными при p< 0,05. Пример 7. Клинические исследования нового препарата. В клинике детской гастроэнтерологии Киевского НИИ педиатрии, акушерства и гинекологии под наблюдением находится 27 детей, из них 18 с хроническим гепатитом и 9 с постнекротическим циррозом печени. Сравнительную оценку результатов лечения проводят на двух группах больных. 1-я группа - получавшая стандартный терапевтический комплекс [2] диетотерапия, витамины А, Е, гепатопротекторы: эссенциале, карсил, силибор и преднизолон, и II-я группа - получавшая, кроме стандартного комплекса, новый препарат. Выборочные результаты представлены в историях болезней. Общая характеристика действия нового препарата в сравнении с известным терапевтическим комплексом показывает, что при усовершенствованном способе лечения отмечается торможение процессов образования соединительной ткани, стимуляция репаративных процессов в тканях печени, что наглядно обнаружено при ультразвуковом исследовании. Побочного эффекта и аллергизирующего действия не выявлено. 7.1. Игорь В.. 9 лет (история болезни Ns 687), диагноз: ХАГ с умеренной активностью процесса. При первичном УЗИ обнаружена периваскулярная инфильтрация, диффузное уплотнение паренхимы печени. После месячного приема стандартного терапевтического комплекса [2] биохимические показатели крови значительно улучшились, однако при контрольном УЗИ отмечено появление уплотнения соединительной ткани в области ворот печени и по ходу портальных сосудов, что расценено как циррозогенная направленность процесса в печени. 7.2. Дима О., 4 года (история болезни № 267), диагноз: хронический активный гепатит (ХАГ) с высокой активностью процесса. При первичном обследовании, по данным ультразвукового исследования (УЗИ) отмечается неравномерное диффузное уплотнение паренхимы печени с тенденцией к разрастанию междолевой соединительной ткани. После месячного приема стандартного терапевтического комплекса [2] совместно с новым препаратом соединительная ткань в междолевых зонах печени при контрольном УЗИ не обнаружена. 7.3. Виталий В., 12 лет (история болезни № 688), диагноз: постгепатитный цирроз печени, осложненный портальной гипертен-зией. При первичном УЗИ выявлено наличие мелких и средних очагов уплотнения соединительной ткани в паренхиме печени с диффузным уплотнением междолевой межуточной ткани. При контрольном УЗИ после месячного приема стандартного терапевтического комплекса [2] совместно с новым,препаратом не зафиксировано средних очагов и отмеченного ранее диффузного уплотнения соединительной ткани. Сохраняются лишь мелкие очаги уплотнения. Таким образом, сравнительные клинические исследования иллюстрируют существенные положительные результаты лечения хронического активного гепатита и цирроза печени у детей при дополнительном применении в комплексе со стандартной терапией нового заявляемого препарата. Представленный экспериментальный и клинический материал по доказательству антигипоксического и гепатопротекторного (антицирротического и репаративного, действия препарата в эксперименте и клинике являются достаточными для рекомендаций по применению нового препарата для беременных, плода, новорожденных и потомства в качестве адаптогене метаболического типа действия. Библиографические данные 1. Беленький Е.Е. и др. Влияние метилурацила и элеутерококка на основной обмен спортсменов в условиях среднегорья. - В кн.: Материалы симпозиума "Высокогорье и красная кровь" и конф. "Высокогорье и лекарства". Фрунзе, 1968, с. 88-89. 2. Лукьянова Е.М. и др. Диагностика и лечение заболеваний гепатопилеарной системы у детей. Методические рекомендации. Киев, 1986, с. 23. 3. Михайловская Л.А. и др. Повышение биосинтетических процессов после крово-тотери методом активации реакции карбок-силирования. - В сб. "Гематология и переливание крови". Киев, "Здоров'я", 1974, вып. 9, с. 102-105. 4. Западнюк И.П. и др. Лабораторные животные. Киев, Вища школа, 1974, с. 304.
ДивитисяДодаткова інформація
Назва патенту англійськоюAdaptogenic drug and method for its preparation
Автори англійськоюHulyi Maksym Fedotovych, Melnychuk Dmytro Oleksiiovych, Tyshchenko Halyna Mykolaivna, Zahorii Volodymyr Antonovych, Denysov Mykola Dmytorvych, Zabarskyi Oleh Shulymovych, Tarakhovskyi Myron Lazarevych, Tsypkun Anatolii Hryhorovych, Denysova Marharyta Fedorivna
Назва патенту російськоюАдаптогенный препарат и способ его получения
Автори російськоюГулый Максим Федотович, Мельничук Дмитрий Алексеевич, Тищенко Галина Николаевна, Загорий Владимир Антонович, Денисов Николай Дмитриевич, Забарский Олег Шулимович, Тараховский Мирон Лазаревич, Цыпкун Анатолий Григорьевич, Денисова Маргарита Федоровна
МПК / Мітки
МПК: A61K 33/10, A61K 33/06, A61K 33/32, A61K 33/30
Мітки: спосіб, препарат, одержання, адаптогенний
Код посилання
<a href="https://ua.patents.su/6-13788-adaptogennijj-preparat-ta-sposib-jjogo-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Адаптогенний препарат та спосіб його одержання</a>
Попередній патент: Спосіб обробки сварних металоконструкцій
Наступний патент: Пристрій для віддаляння кісточок із плодів
Випадковий патент: Спосіб лікування хворих на конвекситальну супратенторіальну менінгіому головного мозку