Спосіб екстракційно-фотометричного визначення мікрокількостей ru(ііі) у присутності pd(іі), rh(ііі) та кольорових металів в електроліті рутеніювання
Номер патенту: 16213
Опубліковано: 17.07.2006
Автори: Рибачук Лариса Миколаївна, Орисик Світлана Іванівна, Пехньо Василь Іванович, Волков Сергій Васильович
Формула / Реферат
1. Спосіб екстракційно-фотометричного визначення мікрокількостей Ru(III) у присутності Pd(II), Rh(III) та кольорових металів в електроліті рутеніювання, який включає утворення комплексних сполук цих металів з органічними реагентами, послідовне вилучення екстрагуванням органічним розчинником спочатку сполук паладію та кольорових металів, а потім - сполук рутенію, вимірювання оптичної густини екстрактів, за якими визначають вміст Ru(III), який відрізняється тим, що як органічний реагент на рутеній використовують гідразон саліцилового альдегіду як ліганд, до реакційного середовища додають основний барвник з максимумом поглинання від 540 до 585 нм, визначення рутенію здійснюють у формі іонних асоціатів ![]() при
при ![]() ;
;
де ![]() - бідипротонований саліциліденгідразон алілтіосемікарбазону,
- бідипротонований саліциліденгідразон алілтіосемікарбазону,
АФ+ - основний барвник із довжиною поглинання від 540 до 585 нм.
2. Спосіб за п. 1, який відрізняється тим, що вилучення Pd(II), Со(ІІ) та Fe(II) (![]() моль/л,
моль/л, ![]() моль/л,
моль/л, ![]() моль/л) проводять екстрагуванням протягом 10 хв. при
моль/л) проводять екстрагуванням протягом 10 хв. при ![]() (Pd(II)),
(Pd(II)), ![]() (Со(II)) та
(Со(II)) та ![]() (Fe(II)) розчином дитизону в чотирихлористому вуглеці (50 % надлишок по відношенню до металу) до повного вилучення металів.
(Fe(II)) розчином дитизону в чотирихлористому вуглеці (50 % надлишок по відношенню до металу) до повного вилучення металів.
3. Спосіб за п. 1, який відрізняється тим, що як гідразон саліцилового альдегіду використовують саліциліденгідразон алілтіосемікарбазону, а як основний барвник - ціаніновий барвник астрафлоксин.
4. Спосіб за п. 1, який відрізняється тим, що величину ![]() регулюють ацетатною буферною сумішшю, реакційне середовище нагрівають при 95-100 °С протягом 35 хвилин, основний барвник додають при кімнатній температурі, іонні комплекси екстрагують бутилацетатом протягом 60 с.
регулюють ацетатною буферною сумішшю, реакційне середовище нагрівають при 95-100 °С протягом 35 хвилин, основний барвник додають при кімнатній температурі, іонні комплекси екстрагують бутилацетатом протягом 60 с.
Текст
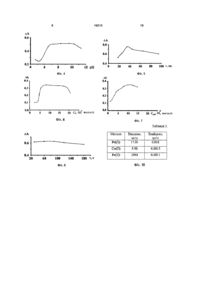
1. Спосіб екстракційно-фотометричного визначення мікрокількостей Ru(III) у присутності Pd(II), Rh(III) та кольорових металів в електроліті рутеніювання, який включає утворення комплексних сполук цих металів з органічними реагентами, послідовне вилучення екстрагуванням органічним розчинником спочатку сполук паладію та кольорових металів, а потім - сполук рутенію, вимірювання оптичної густини екстрактів, за якими визначають вміст Ru(III), який відрізняється тим, що як органічний реагент на рутеній використовують гідразон саліцилового альдегіду як ліганд, до реакційного середовища додають основний барвник з максимумом поглинання від 540 до 585 нм, визначення рутенію здійснюють у формі іонних асоціатів 2 16213 1 3 16213 4 бензилмонооксим, тіосечовина, ацетилацетон та Вилучення Pd(II), Со(ІІ) та Fe(II) (СPd2+=1,69·104 ін [1-9]. моль/л, СCо=1·10-4 моль/л, СFe2+=5,3·10-2 моль/л) Прикладом фотометричного визначення рутепроводять екстрагуванням протягом 10 хв. при нію є методика із використанням ізоамілксантогену рН≈1,3 (Pd(II)), рН≈6,5 (Со(ІІ)) та pH≈8,3 (Fe(II)) (λmах=350 нм, ε=1,18·104) та 6-аміно-5-нітрозо-2,4розчином дитизону в чотирьоххлористому вуглеці 4 піримідиндіолу з піридином (λmах=30 нм, ε =1,2·10 ) (50 % надлишок по відношенню до металу) до по[4, 10]. Чутливішими та контрастнішими є способи вного вилучення металів; визначення рутенію з сульфохлорфенолазородаЯк гідразон саліцилового альдегіду використоніном (λmах=500 нм, ε=1,6·104) та αвують саліциліденгідразон алілтіосемікарбазону, а фурилмонооксимом (λmах=55 нм, ε=1,б·104) [5, 11]. як основний барвник - ціаніновий барвник астрафПрототипом можна вважати спосіб екстракційлоксин; но-фотометричного визначення рутенію з 1-(2Новизна способу екстракційнопіридилазо)-2-фенантролом в метанолі, який пофотометричного визначення рутенію ґрунтується лягає в тому, що рутеній (III) нагрівають з 15на використанні органічного реагенту на цей мекратним надлишком реагенту в ацетатній буфертал, а саме саліциліденгідразону алілтіосемікарній суміші на киплячій водяній бані протягом 50 базону який містить групи (-NH-N=) та (-CS-NHхвилин. Забарвлений комплекс екстрагують хлоN=), проявляє високу комплексоутворюючу здатроформом і вимірюють оптичну густину екстракту. ність з іонами металів, утворюючи інтенсивно заСпіввідношення компонентів в комплексі Ru:L=1:2, барвлені комплексні сполуки з барвником, що дооптимальними є умовами: рН 5,5, λmах=615 нм, зволяє використовувати його в якості реагенту для ε=2,05·104, визначають до 3.03 мкг/мл рутенію (III) розробки екстракційно-фотометричного методу [12]. визначення мікрокількостей рутенію (III) в присутЗавданням корисної моделі є розробка нового, ності паладію (II), родію (III), лужних, лужноземечутливого, вибіркового, експресного екстракційнольних та кольорових металів. фотометричного способу визначення рутенію на Детальніше корисна модель пояснюється та основі утворення ним комплексних сполук з оргапідтверджується графічним матеріалом і конкретнічним лігандом у формі іонних асоціатів з основними прикладами. ним барвником, розширення набору ефективних На фіг.1 представлено структурну формулу реагентів на рутеній на основі полідентатних гідсаліциліденгідразону алілтіосемікарбазону. разонів саліцилового альдегіду (ГСА). На фіг.2 представлено структурну формулу Це завдання можна втілити у способі екстракбарвника - астрафлоксину. ційно-фотометричного визначення рутенію (III) в На фіг.3 в таблиці 1 представлено основні хіприсутності паладію (II), родію (III) та кольорових міко-аналітичні характеристики досліджуваних ІА металів, який включає утворення комплексних Ru(III). сполук рутенію з органічним реагентом, вилучення Кн - константа нестійкості комплексу; екстрагуванням органічним розчинником та виміКн.IА - константа нестійкості іонного асоціату; рювання оптичної густини екстрактів, за якими Обл. лін. Г.Г. - область лінійності градуювальвизначають вміст металу, у якому новим, за цією ного графіку; винаходом, є використання в якості органічного ε - молярний коефіцієнт світлопоглинання; реагенту ГСА, хіміко-аналітичні властивості якого ГВн. - нижня границя виявлення. такі, що при додаванні до нього основного барвниНа фіг.4 представлена залежність різниці знака з максимумом поглинання від 540 до 585 нм, чень оптичної густини ІА Ru(III) від рН реакційного утворюється іонний асоціат, який екстрагується середовища системи Ru-СГАТСК-АФ. органічними розчинниками. На фіг.5 представлено залежність різниці знаСуть корисної моделі полягає в тому, що спочень оптичної густини ІА Ru(III) від тривалості насіб екстракційно-фотометричного визначення мікгрівання системи Ru-СГАТСК-АФ. рокількостей рутенію (III) при сумісній присутності На фіг.6 представлено залежність різниці зназ паладієм (II), родієм (III) та кольоровими метачень оптичної густини ІА Ru(III) від концентрації лами, який включає утворення комплексних сполук ліганду системи Ru-СГАТСК-АФ. цих металів з органічними реагентами, послідовне На фіг.7 представлено залежність різниці знавилучення екстрагуванням органічним розчинничень оптичної густини ІА Ru(III) від концентрації ком спочатку сполук паладію та кольорових метабарвника системи Ru-СГАТСК-АФ. лів, а потім сполук рутенію, вимірювання оптичної На фіг.8 представлено залежність різниці знагустини екстрактів, за якими визначають вміст чень оптичної густини ІА Ru(III) від тривалості ексRu(III). Відрізняється спосіб від прототипу тим, що тракції системи Ru-СГАТСК-АФ. як органічний реагент на рутеній використовують На фіг.9 в таблиці 2 представлено результати гідразон саліцилового альдегіду як ліганд, до реапорівняльної характеристики розробленого та вікційного середовища додають основний барвник з домих методів визначення Ru(III). максимумом поглинання від 540 до 585 нм, вилуε - молярний коефіцієнт світлопоглинання, * чення рутенію здійснюють у формі іонних асоціатів дані відсутні. [Ru(HL)2]-АФ+ при рН=6,5-10,2; На фіг.10 в таблиці 3 представлено результаде (HL)2 - бідипротонований саліциліденгідрати визначення Pd(II) та кольорових металів в елекзон алілтіосемікарбазону, троліті рутеніювання. АФ+ - основний барвник з довжиною поглинанНа фіг.11 в таблиці 4 представлено результаня від 540 до 585 нм; ти визначення Ru(III) в електроліті рутеніювання. 5 16213 6 В якості вихідної солі використовували комерасоціат стійкий на повітрі і не змінює величину ційний трихлорид рутенію із вмістом рутенію 43,73 оптичної густини протягом тривалого часу. Порів%. няльна характеристика чутливості відомих та за0,001 М розчин Ru(III) готували розчиненням пропонованого способу визначення рутенію предточної наважки солі в бідистиляті з додаванням 6 н ставлена в табл. 2 на фіг.9. Запропонований НСl. метод є чутливим та вибірковим. Вихідний гідразон синтезували реакцією конТаким чином, проведені дослідження показаденсації відповідного гідразиду з саліциловим ли, що система Ме:L:АФ може бути використана альдегідом в етанолі [13], структурна формула для розробки екстракційно-фотометричного метоякого показана на фіг.1. ду визначення Ru(III) в промислових об'єктах. 0,01 М розчин гідразону готували розчиненням Водну фазу, що містить Ru(III), Pd(II), Rh(III), точної наважки солі в ДМФА. Со(ІІ) та Fe(II) (СRu3+=1,6·10-4 моль/л, CPd2+=1,69·104 В якості барвника використовували комерціймоль/л, СRh3+=1,6·10-4 моль/л, CCo2+=1,6·10-4 ний препарат основний ціаніновий барвник моль/л, СFe2+=5,3·10-2 моль/л) екстрагують протятетрафторборат-диметиліндо-карбоціаніну (ДІК), гом 10 хв. при pH≈1,3 (Pd(II)), pB≈6,5 (Co(II)) та астрафлоксин (АФ), очищений дворазовою перекpH≈8,3 (Fe(II)) розчином дитизону в чотирьоххлористалізацією з метанолу, структурна формула ристому вуглеці (50 % надлишок по відношенню якого показана на фіг.2. Водно-спиртовий 1·10-3до металу) до повного вилучення металів. Фази 1,6·10-4 М розчин готували розчиненням точної розділяють та аналізують на наявність досліджунаважки солі. ваних елементів атомно-адсорбційним методом. Оптичну густину екстрактів вимірювали на фоРезультати представлені в таблиці 3 на фіг.10. токолориметрі КФК-2-УХЛ 42 (l=0,3). Кислотність До водної фази, що містить Ru(III), Rh(III) середовища контролювали рН-метр(СRu3+=1,6·10-4 моль/л, СRh3+=1,6·10-4 моль/л) долимілівольтметром НІ 8314 з редоксиметричним вають 3,2·10-2 моль/л М розчин саліциліденгідраелектродом НІ 3131 В. зону алілтіосемікарбазону, доводячи ацетатною Для прискорення встановлення рівноваги в буферною сумішшю до рН=8,2 та нагрівають прореакціях комплексоутворення Ru(III) з саліцилідентягом 35 хв. при температурі 95-100°С. Доливають гідразоном алілтіосемікарбазону дослідження пророзчин астрафлоксину (М:АФ=1:1) при кімнатній водили при температурах 95-100°С, екстракцію та температурі для утворення іонного асоціату Ru(III), вимірювання оптичної густини - при кімнатній темякий вилучають бутилацетатом протягом 60 с. пературі. Фази розділяють та аналізують на наявність Нижче наведені приклади та експериментальні Ru(III). дані, які показують суттєвість впливу тривалості Кількість металів знаходили методом добавок. нагрівання та екстракції системи, кислотності сеПравильність методики перевіряли методом ввередовища, концентрації ліганду та барвника на дено - знайдено (табл. 4 на фіг.11) процес комплексоутворення. Отже, аніонний комплекс [Ru(HL)2]- в присутВ градуйовані пробірки з притертими пробками ності основного барвника астрафлоксину в слабвносили 0,05-1,00мл 1·10-3 М розчину рутенію, колужних розчинах існує у формі іонного асоціату 0,05-1,00мл 0,01 М розчину гідразону, створюючи [Ru(HL)2]-АФ+ який характеризується високим знарН середовище від 3 до 12 ацетатною буферною ченням молярного коефіцієнту поглинання, на посумішшю, нагрівали 10-100 хв., при температурі рядок вищим порівняно з літературними даними 95-100°С, доливали 0,05-1,00мл 0,001 М розчину (табл. 2, фіг.9), широким оптимальним інтервалом барвника при кімнатній температурі до об'єму 5мл. значень рН та концентрацій досліджуваних елеЕкстрагували рівним об'ємом екстрагенту протяментів, хорошою вибірковістю. Іонний асоціат стійгом 20-180с. Органічну фазу відділяли, центрифукий на повітрі, не змінює величину оптичної густигували та вимірювали оптичну густину екстрактів в ни протягом тривалого часу. 0,3 см кварцевих кюветах на фотоелектроколориДжерела інформації: метрі. 1. Ayres G., Young F. // Anal. Chem. - 1950. Дані представлені на фіг.4-8 свідчать, що чут22,1277. 1281. ливість визначення рутенію згідно даного способу 2. Rangnekar A., Khopkar S. // Microchim Acta. максимальна при нагріванні системи 35 хв., рН 1968. 272. розчину 6,5-10,2, концентрації гідразону (5,23. Manning D., Menis О. // Anal. Chem. - 1962. 18,0)·10-4 моль/л та барвника (5,0-20,0)·10-5 34, 94. моль/л, часу екстракції 60 с. 4. Малик А.К., Рао Л.Д. СпектрофотометричесВ оптимальних умовах комплексоутворення та кое определение кобальта, никеля, палладия, меекстракції визначено основні хіміко-аналітичні хади, рутения и молибдена после экстракции их изорактеристики досліджуваних ІА Ru(III) (табл. 1 на амилксантогенатов расплавленным нафталином // фіг.3). Журн. аналит. химии. - 2000. - Т. 55, - №8. - С. 830Визначенню Ru(III) не заважають катіони луж833. 2+,1+ 2+ 2+ 3+ 2+ 2+ них елементів, Cu , Ni , Sn , Al , Рb , Ca , 5. Савин С.Б., Гурьева Р.Ф., Трутнева Л.М., Rh3+ та аніони SO42-, СI-, СН3СОО-, Н2РO4-, NO3-, Чалисова Н.Н., Фомина Т.А. и Шубочкин Л.К. РеаСО32-, що вказує на хорошу вибірковість реакції. кции сульфатных, хлоридных и фосфатных комЗаважають визначенню іони Fe2+, Co2+, Pd2+. Обплексных соединений рутения (III) и (IV) с сульфоласть лінійності градуювального графіку характехлорфенолазороданином и их аналитическое ризується достатньо широким інтервалом викоиспользование // Журн. аналит. химии - 1982. - Т. нання закону Бугера-Ламберта-Бера. Іонний 37, - №4. - С. 654-661. 7 16213 8 6. Савостина В.М., Шпигун О.А. и Чебрикова разонами саліцилового альдегіду: Дис. канд. хім. Т.В. Экстракционно-спектрофотометрическое наук: 02.00.01. - К., 2002. - 123 с. определение рутения (III), родия (Ш) и иридия (III) 14. Шленская В.И., Пискунов Е.М., Хвостова по реакции с α-бензилмонооксимом в присутствии В.П. Спектрофотометрическое изучение реакции карбонат-иона // Журн. аналит. химии -1982. - Т. четырехвалентного рутения с родан-ионом и ее 37, - №2. - С. 285-288. аналитическое использование // Вестн. МГУ, сер. 7. Рудницкая О.В., Комозин П.Н., Пичков В.Н., хим. - 1964. - №4. - С. 62-66. Мирошниченко И.В. Исследование взаимодейст15. Majumdar A., Sen Gupta J.Z. // Analyt. Chem вия бромокомплексов рутения (III) с тиомочевиной - 1961. 178, 401. в растворах // Журн. неорг. химии. - 1988. - Т. 33, 16. Езерская Н.А., Солових Т.П. Соединения №1. - С. 140-143. гидроксоэтилендиаминтетраацетата рутения (III) с 8. Бимиш Ф. Аналитическая химия благородкислородом // Журн. аналит. химии. - 1966. - Т. 11, ных металлов. - М.: Мир, 1969. Ч. 2. - 400 с. - №11. - С. 2569-2574. 9. Мазуренко Е.А. Справочник по экстракции. 17. Езерская Н.А., Соловых Т.П. Обратимое К.: Техніка, 1972. - 448 с. взаимодействие этилендиаминтетраацетата руте10. Sindhu R. S., Singh R. P. Spectrophotometric ния с кислородом // Журн. аналит. химии. - 1966. determination of ruthenium (III) using 6-amino-5Т. 11, - №6. - С. 1462-1465. nitroso-2,4-pyrimidinediol and pyridine // J. Indian 18. Hashitani H., Katsuyama К., Motojima К. // Chem. Soc. - 1985. - Vol. 62, №1. - Р. 80-81. Talanta - 1970. 16, 1553. 11. Савостина В.М., Шпигун О.А., Климова 19. Wasey Abdul, Bansal Raj. К., Satake Н.В., Колотыркина И.Я. и Пешкова В.М. СпетроMasatada, Puri Bal. K. Spectrophotometric фотометрическое определение рутения (III) λdetermination of ruthenium (III) and rhodium (III) with фурилмонооксимом // Журн. аналит. химии -1979. 9,10-phenanthrenequinone monoxime after extraction - Т. 34, - №3. - С. 607-609. into molten naphthalene // Bull. Chem. Soc. Jap. 12. Garg B.S., Singh R. P. Solvent extraction & 1983. - Vol. 56, №12. - P. 3603-3607. Spectrophotometric of Ru(III), Rh(III) & Pd(II) using 120. Орысык С.И., Рыбачук Л.Н., Пехньо В.И., (2-pyridylazo)-2-phenanthrol //J. Indian Chem. - 1977. Волков С.В. Синтез, спектроскопия и аналитичес- A15, №4. - Р. 367-369. кое использование координационных соединений 13. Орисик C.I. Синтез, будова, властивості та с салицилиденгидразоном аллилтиосемикарбазовикористання координаційних сполук Rh(III) з гідна // Укр. хим. журнал. - 2005. - Т. 71, - №11-12. - С. 102-108. 9 16213 10 11 Комп’ютерна верстка Г. Паяльніков 16213 Підписне 12 Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for removing ruthenium in the presence of rhodium, palladium, and non-ferrous metals in electrolyte
Автори англійськоюVolkov Serhii Vasyliovych, Orysyk Svitlana Ivanivna, Pekhnio Vasyl Ivanovych
Назва патенту російськоюСпособ экстракционного выделения рутения в присутствии родия, палладия и цветных металлов в электролите
Автори російськоюВолков Сергей Васильевич, Орисик Светлана Ивановна, Пехньо Василий Иванович
МПК / Мітки
МПК: G01N 31/22, C01G 55/00
Мітки: присутності, рутеніювання, екстракційно-фотометричного, ru(ііі, металів, кольорових, визначення, pd(іі, мікрокількостей, спосіб, rh(ііі, електроліти
Код посилання
<a href="https://ua.patents.su/6-16213-sposib-ekstrakcijjno-fotometrichnogo-viznachennya-mikrokilkostejj-ruiii-u-prisutnosti-pdii-rhiii-ta-kolorovikh-metaliv-v-elektroliti-ruteniyuvannya.html" target="_blank" rel="follow" title="База патентів України">Спосіб екстракційно-фотометричного визначення мікрокількостей ru(ііі) у присутності pd(іі), rh(ііі) та кольорових металів в електроліті рутеніювання</a>
Попередній патент: Спосіб прогнозування ризику настання інвалідності після оперативного лікування ускладнених гастродуоденальних виразок
Наступний патент: Спосіб лікування хворих на гіпертонічну хворобу
Випадковий патент: Спосіб отримання органо-мінерального добрива з відходу хімводопідготовки тец і пташиного посліду