Спосіб одержання комплексів включення 7-ізопропоксіізофлавону
Номер патенту: 19813
Опубліковано: 25.12.1997
Автори: Йожеф Сейтлі, Віктор Вайсфайлер, Каталін Калон, Віра Гергелі, Золтан Варгаі, Тамаш Сютш, Агнеш Штадлер
Формула / Реферат
Способ получения комплексов включения 7-изопропоксиизофлавона, имеющего формулу
обладающих способностью всасывания в фармакологически активной концентрации, заключающийся в том, что 7-изопропокси-изофлавон подвергают взаимодействию с альфа, бетта, гамма-циклодекстрином, гептакис-2,6-0-диметил- или 2-гептакис-2,3,6-три-0-метил-бетта-циклодекстрином, или циклодекстриновым полимером с мол.м.4000 в водной или водно-органической среде, при молярном соотношении 7-изопропоксимзофлавона и циклодекстри-нового компонента 1:2 -3,5 с последующим выделением и сушкой целевого продукта.
Текст
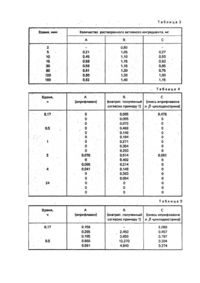
Изобретение относится к клатрату 7-изопропоксиизофлавона (иприфлавона), который может найти применение в медицине для лечения остеопороза и остеомаляции. Известные препараты, содержащие иприфлавон, имеют недостаточную терапевтическую эффективность из-за слабой растворимости и всасываемости. Известен способ получения субстанции иприфлавона. Характеристики соединения следующие: мол.м. 280,3, т.пл.113-118°С, растворимость в воде при 25°С 142 мг/мл. Оно слабо растворимо в ацетоне, но хорошо в хлороформе и диметилформамиде. Известно, что всасываемость и растворимость фармацевтических составов, обладающих слабой растворимостью повышается, если их перемалывают с инертными носителями. Например, перемалывание равных количеств иприфлавона, аэросила (или активированного угля, активированной глины, активированной окиси алюминия) в вибромельнице с использованием стальных шариков позволяет получить составы, растворимость которых выше, чем исходного пирифлавона. Так, продукт с аэросилом имеет растворимость 20,4 мг/мл в 50%-ном водном метаноле через 30 мин при 37°С, в то время как растворимость неизмельченной смеси составляет только 15,0 мг/мл, т.е. растворимость in vitro увеличивается в 1,36 раза. Анализ уровней содержания в крови собак после пeрорального введения показывает, что иприфлавон нельзя обнаружить в крови. Перемалывание с аэросилом увеличивает всасываемость основного метаболита с 0,152 мг · ч/мл до 0,485 мг * ч/мл, что соответствует увеличению в 3,19 раза, Цель изобретения - получение вещества, содержащего 7-изопропоксиизофлавон (иприфлавон) и обладающего способностью всасывания в фармакологически активной концентрации. Указанная цель достигается тем, что согласно способу получения комплексов включения 7изопропоксиизофлавона, имеющего формулу заключающемуся в том, что 7-изопропоксиизофлавон подвергают взаимодействию с a,β,g циклодекетрином, гептакис-2,6,0-ди-метил- или 2-гептакис-2,3,6-три-0-метил- β-циклодекстрином. или циклодекстриновым полимером с мол.м. 4000 в водной или водно-органической среде, при молярном соотношении 7-изопропоксиизофлавона и циклодекстринового компонента 1:2-3,3, с последующим выделением и сушкой целевого продукта. Установлено, что растворимость полученного соединения включения in vitro в 10 раз выше по сравнению с растворимостью иприфлавона введенного perse, а уровень содержания в крови основного метаболита выше в 15-20 раз. Установлена всасываемость пирифлавона в неизменной форме и в фармацевтически эффективной концентрации. Одним из доказательств образования соединения включения является увеличение растворимости иприфлавона в водных растворах. Растворимость иприфлавона в полученных соединениях включения приведена в табл.1. Повышение растворимости наблюдается при использовании всех исследованных циклодекстриновых компонентов. Суммируя результаты представленные в табл.1, можно сказать, что растворимость иприфлавонового клатрата в 4 раза выше относительно активного ингредиента, чем растворимость иприфлавона perse и всасываемость его после пёрорального введения крысам минимум в 10 раз выше по сравнению с уровнем содержания в крови, измеренном после введения свободного активного ингредиента в той же дозе. Неизменный уровень содержания иприфлавона составляет по крайней мере 25% от общего количества материала, который всасывается. При получении предлагаемого соединения включения процесс взаимодействия реагентов осуществляют в водно-органической среде. В качестве органического растворителя можно использовать спирт или кетон. Предпочтительно используют 50%-ный раствор этанола. Выделение целевых продуктов происходит при охлаждении реакционных растворов. Получают кристаллические продукты. Можно осуществлять смешение в водном ацетоне одновременно С выпариванием растворителя, используя димеб или тримеб (диметилциклодекстрин или триметил-циклодекстрин) или растворимый циклодекстриновый полимер, из реакционной смеси можно выделить твердый порошкообразный продукт путем выпаривания, сушки, распыления, сушки при температуре ниже 0°С, или в случае с димебом путем нагревания раствора. Пример 1. Получение иприфлавон-циклодекстринового клатрата, имеющего молярное соотношение 1:2. 11,0 г (39,2 ммоль) иприфлавона и 114,3 г (338,3 ммоль) b-циклодекстрина с содержанием влаги 12,36% растворяют в 2,25 л водного раствора этанола, составляющего 50 об.% при 80°С, интенсивно перемешивая и дают остыть до комнатной температуры. Осажденный кристаллический продукт отфильтровывают и суша т в течение 24 ч при 60°С, что дает 96,4 г продукта в виде рыхлого порошка белого цвета. Размер частиц менее 90/М м. Содержание иприфлавона 10,8 мас.% иприфлавон; b-циклодекстрин 1:2 выход относительно активного ингредиента 94,7% (исходное соотношение иприфлавон: b-циклодекстрин 1:2:3). Для того, чтобы доказать, что указанный продукт действительно является клатратом, проводят различные анализы: термоаналитический анализ, дифракцию рентгеновских лучей и анализ растворимости. Термоаналитическое поведение механической смеси и свободных компонентов является почти одинаковым, но изменения в клатрате, происходящие из-за нагревания можно наблюдать только одновременно с разложением циклодекстрина. При испытании механической смеси дифференциальной сканирующей калориметрией (ДСК) при 115°С устанавливают, что эндотермический пик соответствует точке плавления иприфлавона, но в случае с клатратом пик не наблюдается. Механическая смесь показывает непрерывную потерю массы - в соответствии с уровнем содержания иприфлавона в интервале между 130°С и 250°С. но и в случае с клатратами не наблюдают какой-либо потери в массе или высвобождении органических веществ в том же температурном интервале (анализ термического расширения, АТР). Диаграмма, полученная в результате рентгеноструктурного анализа порошка механической смеси, состоит из добавочных сумм диаграмм порошковых компонентов. Однако диаграмма порошка из клатрата содержит меньше пиков и новые пики (2 q °=6,7; 7,8; 20.9), характеристические для клатрата и отличающиеся от характеристических пиков Д-циклодекстрина (2 q°= 4,5; 10,6; 12,3), а у иприфлавона составляют (2 q°=5,8; 11,5; 17,3; 22,0), указывая на новую кристаллическую структур у и, таким образом, подтверждая косвенно образование клатрата. Для того, чтобы провести испытания, 250 мл дистиллированной воды помещают в колбу емкостью 500 мл и нагревают до 37°С. Затем продукт в количестве, соответствующем 50 мг активного ингредиента, добавляют, затем суспензию, полученную таким образом, перемешивают при 100 об/мин, используя магнитную мешалку. Через определенные интервалы отбирают образцы проб по 2-6 мл и фильтруют на стеклянном фильтре и после разбавления фильтраты исследуют фотометрически в смеси вода:этанол в соотношении 1:1. Полученные результаты приведены в табл.2. Растворение свободного активного ингредиента является относительно медленным, оно достигает величины насыщения иприфлавона (около 1,5 мг/мл) через 40-50 мин, В случае с образцами, содержащими иприфлавон - b-циклодекстриновый клатрат, максимальную концентрацию растворенного иприфлавона получают уже через 1 мин. т.е. активный ингредиент растворяется сразу же - также происходит мгновенное растворение ив начале концентрация активного ингредиента может быть такой же высокой, как и двойной уровень насыщения. Растворение смеси иприфлавона и b-цикло-декстрина является более медленным, концентрация растворенного активного ингредиента достигает величины, определенной тогда, когда растворяют клатрат, только через 30-40 мин, Растворимость активного ингредиента определяют также при различных уровнях содержания pH. Полученные кривые растворимости при pH 1,3 (это соответствует кислотности желудочного сока, HCI) и при pH 7,6 (это соответствует величине pH кишечника, фосфатный буфер) существенно не отличаются от величин растворимости, полученных в дистиллированной воде, соответственно растворимость активного ингредиента не зависит от pH в испытуемом интервале pH. Пример 2. Получение иприфлавона-b-циклодекстринового клатрата, имеющего молярное соотношение 1:2. 0,5 г (1,78 ммоль) иприфлавона растворяют в 50 мл 96%-ного этанола, и раствор, полученный таким образом, добавляют по каплям к раствору из 8,0 г (5,35 ммоль) β-циклодекстрина с содержанием влаги 13,3% в 50 мл дистиллированной воды в течение 2 ч, затем смеси дают остыть до комнатной температуры. После интенсивного перемешивания еще в течение 16 ч полученный продукт отфильтровывают и сушат в течение 24 ч при 60°С, чтобы получить 5,5 г продукта. Содержание иприфлавона: 7,9 мас.%, молярное соотношение иприфлавон: b-цик-лодекстрин = 1:2,29. Выход относительно активного ингредиента 87%. Продукт также содержит свободный циклодекстрин (исходное соотношение иприфлавон: у-циклодекстрин 1:3). Пример 3. Получение иприфлавон-циклодекстринового клатрата, имеющего молярное соотношение 1:2. 0,5. г (1,78 ммоль) иприфлавона растворяют в 10 мл ацетона в роторной ступке и добавляют 4,0 г (3,70 ммоль) а-циклодекст-рина с содержанием влаги 10 мас.% и 2 мл дистиллированной воды. Легкую суспензию, полученную таким образом, гомогенизируют, растирая до те х пор, пока не выпаривается растворитель. После этого продукт, полученный таким образом, сушат в течение 24 ч при 60°С. Он содержит 11,1% активного ингредиента и также свободный a-циклодекстрин. Молярное соотношение иприфлавона κ a-циклодекстрину составляет 1:1.1. Примеры форм выпуска фармацевтических составов, содержащих иприфлавон-циклодекстриновый клатрат в качестве активного ингредиента, и их биологические испытания. Пример 4. Получение комплекса включения иприфлавон-Димеб с молярным соотношением 1:2. 1,2 г (1,03 ммоль) Димеба растворяют в 10 мл дистиллированной воды и добавляют 0,1 г(0,37 ммоль) иприфлавонз. Полученную суспензию взбалтывают 4 дня, затем фильтруют на фильтре G4 и после этого осушают, вымораживают с получением 1,25 г продукта. Он содержит 5,67% активного компонента. Выход по активному компоненту 71% (молярное соотношение иприфлавон: Димеб равно 1:2,8). Пример 5. Получение комплекса включения иприфлавон-Тримеб с молярным соотношением 1:2. 2,03 г (1,73 ммоль) Тримеба растворяют в 250 мл 50%-ного этанола и добавляют 0,14 г (0,5 ммоль) иприфлавона. Полученный раствор перемешивают, затем высушивают разбрызгиванием с получением 1,96 г продукта. Он содержит.6,9% активного компонента. Выход по активному компоненту составляет 96,6% молярное соотношение иприфлавон:тримеб равно (1:3,5). Пример 6. Получение комплекса включения иприфлавон-циклодекстриновый полимер с молярным соотношением 1:2. 2 г (0,2 ммоль) циклодекстринрвого полимера со средней мол.м. 4000 растворяют в 250 мл 50%-ного этанола, затем поступают аналогично примеру 2. Количество полученного продукта составляет 1,85 г, содержание в нем активного компонента 7,2%. Выход по активному компоненту составляет 95,1 %. Пример 7. Сравнивают растворимость известного препарата, содержащего иприфлавон-ямболана в таблетках, содержащих 200 мг иприфлавона (А), таблетки, содержащей 40 мг иприфлавона в форме bциклодекстринового клатрата, полученного согласно примеру 1, и таблетки, содержащей 200 мг иприфлавона и 330 мг b-циклодекстрина при 37°С в 500 мл желудочного сока. Кусочек таблетки помещают в оборудование и определяют количество растворенного материала путем спектрофото-метрии при 247 нм. Составы испытуемых таблеток следующие: таблетка А (известная как таблетка ямболап. К-020484), мг: иприфлавон. 200; амилум максдиc 36; лактоза 60; ПВП 13:эсма спренг 30: тальк 7: стеарат магния 4. Таблетка В. Предлагаемый клатрат, содержащий мг; 40 мг иприфлавона 370; ПВП (поливимил-пирролидон)15. Таблетка С, мг: иприфлавон 200; b-циклодекстрин 330; ПВП 20., Результаты исследований приведены в табл.3. Из результатов видно, что только 0,62 мг иприфлавона растворяются из обычной таблетки, но в случае с таблеткой, содержащей одну пятую активного ингредиента в форме b-циклодекстринового клатрата, по сравнению с количеством активного ингредиента, присутствующего в обычной таблетке, количество растворившегося активного ингредиента удваивается и количество растворенного материала на 30% превышает максимальную величину, полученную при использовании обычных таблеток через 2 мин. В случае с таблеткой, которая содержит иприфлавон и a-циклодекстрин в форме механической смеси, растворение происходит несколько медленнее, но даже в этом случае количество растворенного активного ингредиента выше по сравнению с обычной таблеткой. В испытаниях на всасываемость используют самцов крыс весом 170-200 г. Спустя 16 ч после обездвижения вводят иприфлавон в дозе 25 мг'/кг (группа А), иприфлавон-b-циклодекстриновый клатрат, приготовленный согласно примеру 1 (группа В) и иприфлавон-b-циклодекстриновую смесь (группа С) - оба содержат b-циклодекстрин в экви-молярном соотношении по отношению к активному ингредиенту, после этого животным дают пищу, для крыс воду (по желанию) ab libitum. Материалы для испытания смешивают в течение 5 мин в 2 мл 1 %-ного раствор'а целлюлозы и вводят через желудочную трубк у. Образцы плазмы собирают через 10:30 мин и 1:2 и 4 после лечения, используя кровь, которая вытекает из Vena femoralis после ее перерезывания у животных, которым проводят анестезию эфиром. Образцы крови помещают в пробирки с гепарином, центрифугир уют, подвергают нутч-фильтрованию и хранят глубоко замороженными в ампуле до последующего использования.. Для того, чтобы отобрать образцы мочи после обработки животных помещают в отдельные метаболические емкости, и собирают отдельно мочу и фекалии в течение 24 ч. Образцы мочи хранят до последующего использования, подвергнув глубокому замораживанию. Концентрацию неизменного иприфлавона и его основных метаболитов (7-гидроксиизофлавон) в моче и образцах плазмы определяют с помощью жидкостной хроматографии высокого давления. Для того, чтобы провести жидкостное хроматографирование высокого давления используют жидкостной хроматограф типа RP-18 и в колонке обратного тока Lichrosorb (размер зерна в случае с образцами плазмы 10мм и в случае с образцами мочи 5 mΜ). Скорость потока элюента: 1,5 мл/мин, длина волны УФ-детектора 254 нм, скорость движения бумажной ленты 0,2 см/мин. В случае с образцами плазмы в качестве элюента используют смесь: 0,05 Μ ацетатный буфер (pH 3): ацетонитрил - 60:40, и в случае с образцами мочи смесь ацетатный буфер: ацетонитрил -55:45. Внутренний стандарт - этаноловый раствор 2-метил-7-метокси-4'-нитроизофлавон (100 m г/мл), и для калибрования используют растворы, включающие 100/4 г/мл и 10m г/мл 7-гидро-ксиизофлавона в метаноле. Для того, чтобы подвергнуть анализу образцы плазмы, к 1 мл плазмы добавляют 1 мл ацетатного буфера (pH 5) и фермент глюкуронидазу (арилсульфоназа) (100 FV), разбавив в 10 раз 10 мл дистиллированной воды, и инкубируют при 37°С в течение 24 ч. После инкубирования добавляют 50 мл NaOH, смесь экстрагируют бензолом и центрифугируют. Отделяют органическую фазу, водную фазу подкисляют 400 мл 1Н HCI, и после добавления 50 мл раствора внутреннего этанола, экстрагируют повторно 8 мл бензола. Органическую фазу центрифугируют, выпаривают остаток, растворяют в 100mл элюента, используют для инъекции и измеряют 50 mn этого раствора. Уравнение кривой калибровки: у= 8,2 χ 0,08: коэффициент поправки 0,9999. Для того, чтобы проанализировать образец мочи, к 0,5 мл мочи добавляют 0,5 mл - ацетатного буфера (pH 5) и 10 мл фермента b-глюкуринидазы (арилсульфатаза) (1000 FV) и смесь экстрагируют 8 мл бензола и центрифугир уют. Органическую фазу отделяют, водную фазу подкисляют, добавив 400 мл 1Η HCI, и после добавления 50 мл раствора внутреннего этанола его экстрагируют еще 8 мл бензола. Органическую фазу центрифугир уют, выпаривают и остаток растворяют в 100 mл элюента и инъецируют 10 mл этого раствора в жидкостный хроматограф. Уравнение кривой калибровки: у = 0,911 χ - 0,09: коэффициент поправки 0,9995. В табл. 4 показаны величины концентрации неизменного иприфлавона; в табл. 5 -величины концентрации основного метаболита, определенные в крови животных. Группе А вводят иприфлавон perse, группе В - предлагаемый клатрат и группе С-смесь иприфлавона и bциклодекстрина. На каждом отрезке времени неизменный иприфлавон можно обнаружить только в случае группы В и его количество составляет 50-500 нг/мл, В случае с группой А аналогично группе С неизменный иприфлавон можно обнаружить только через некоторые периоды времени (через 2 и 4 ч). Что касается основного метаболита, то в каждом промежутке времени уровни плазмы в 10-20 раз выше в группе А по сравнению с уровнями групп А и С, которые определены через один и тот же отрезок времени, т.е. величины группы В находятся между 3 и 20 m г/мл, тогда как в случае с группами А и С находятся в интервале от 0,2 до 1,0 m т/мл. Во все х случая х второй пик появляется в кривой плазмы через 2 ч, что может быть результатом интенсивного энтерогепатитного цикла и лучшей всасываемости в малом кишечнике. В табл. 6 показаны результаты жидкостной хроматографии высокого давления образцов мочи. В интервале 0-24 ч в образцах мочи не могут обнаружить неизменный иприфлавон. Однако можно проследить наличие основного метаболита (во всех случаях). Средняя величина содержания 7-гидроксии-зофлавона 9526m г, что соответствует тре хкратному повышению по сравнению с другими группами. Согласно опыту количество основного метаболита составляет 50-55%, от общего количества метаболита, и поэтому общее количество, выделившееся с мочой, в 2 раза выше, чем количество, которое определено de facto. Таким образом, в случае с группой В 40%, в то время как в случае с группами А и Столько 10-14% введенной дозы выделяется с мочой. После введения крысам иприфлавон -b-циклодекстринового клатрата определяют, что можно достичь повышения в 10-15 раз уровня содержания в плазме и в 3 раза повысить количество вещества, выделяющегося с мочой, по сравнению с контрольной группой.
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for preparation of 7-isopropoxyisoflavone inclusion complexes
Автори англійськоюSHTADLER AGNESH, SEJTLI JOZHEF, VAJSFAJLER VIKTOR, VARGAI ZOLTAN, KALON KATALIN, GERGELI VERA, SYUTSH TAMASH
Назва патенту російськоюСпособ получения комплексов включения 7-изопропоксиизофлавона
Автори російськоюАгнеш Штадлер, Йожеф Сейтли, Виктор Вайсфайлер, Золтан Варгаи, Каталин Калон, Вера Гергели, Тамаш Сютш
МПК / Мітки
МПК: A61K 31/724, C08B 37/16, A61P 19/08
Мітки: комплексів, включення, спосіб, одержання, 7-ізопропоксіізофлавону
Код посилання
<a href="https://ua.patents.su/6-19813-sposib-oderzhannya-kompleksiv-vklyuchennya-7-izopropoksiizoflavonu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання комплексів включення 7-ізопропоксіізофлавону</a>
Попередній патент: Вагон-термос для перевезення гарячих зливків
Наступний патент: Пристрій для закріплення рейки на шпалі
Випадковий патент: Спосіб лапароскопічної передньої крурорафії при виконанні антирефлюксних операцій з приводу великих та гігантських параезофагеальних гриж