3(4,5 – дигідротіазол – 2 – іл) амід цис-1,2,2 – триметилциклопентан – 1,3 – дикарбонової кислоти, що стимулює сперматогенез
Номер патенту: 38130
Опубліковано: 15.05.2001
Автори: Яременко Федір Георгійович, Вакула Володимир Миколайович, Свидло Ірина Миколаївна, Сидорова Ірина Василівна, Тарасенко Наталія Євгеніївна, Гладкова Алла Іванівна, Золотухіна Валентина Миколаївна, Васильєва Тетяна Володимирівна, Губаревич Ірина Георгіївна
Текст
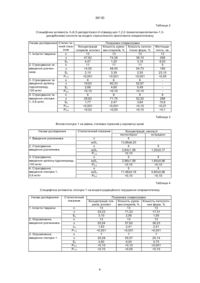
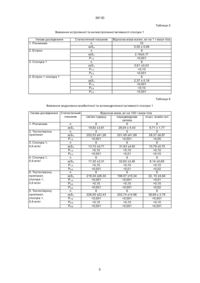
3-(4,5-дигідротіазол-2-іл)амід цис-1,2,2-триметилциклопентан-1,3-дикарбонової кислоти формули: Винахід відноситься до нової біологічно активної сполуки, а саме, - до 3-(4,5-дигідротіазол-2іл)аміду цис-1,2,2-триметилциклопентан-1,3-дикарбонової кислоти, який стимулює сперматогенез. На сьогодні для лікування чоловічої безплідності застосовують гормональні препарати: андрогени (тестостерону пропіонат, тестостерону енантат, омнадрен - для парентерального введення; андріол, метилтестостерон - для перорального вживання) та гонадотропіни. Проте гормонотерапія безпліддя не завжди ефективна і часто супроводжується негативними побічними ускладненнями [1 - 3]. З негормональних засобів корекції сперматогенезу відомі антиестрогени (кломіфен, тамоксифен), які є досить токсичними. Крім того, поряд з антиестрогенною, вони можуть проявляти і естрогенну активність, що при передозуванні пригнічує генеративну функцію сім'яників [1]. Ряд препаратів розроблено на основі амінокислоти аргініну - піроглютамат аргініну (Японія), вігодан (Німеччина). На основі аргініну гідрохлориду виробляють таблетки спермаргін та біоаргінін (Італія), які застосовуються для лікування оліго- та астенозооспермії [4]. Однак ці препарати призначають досить тривалий час (до 3 місяців) у великих дозах (від 500 мг до 4 г на день) [4, 5]. Задача винаходу - пошук нових ефективних малотоксичних сполук, що проявляють сперматомодулюючу дію при відсутності гормональних та антигормональних властивостей. Ця задача вирішується тим, що пропонується сполука 3-(4,5-дигідротіазол-2-іл)амід цис-1,2,2триметилциклопентан-1,3-дикарбонової кислоти формули: N CH3 CH3 S NHCO COOH CH3 що стимулює сперматогенез. 1 NHCO 3 2 CH3 A CH3 (13) CH3 1 COOH , що стимулює сперматогенез. Зазначену сполуку отримують при взаємодії 2амінотіазоліну з ангідридом d,1-камфорної кислоти чи її оптичними антиподами у середовищі органічних розчинників. Приклад. Бензольні розчини 2-амінотіазоліну (10,2 г; 0,1 моль) та камфорного ангідриду (18,2 г; 0,1 моль) змішують і кип'ятять до утворення осаду, який фільтрують, промивають бензолом і висушують. Одержують 23,3 г (82%) 3-(4,5-дигідротіазол2-іл)аміду цис-1,2,2-триметилциклопентан-1,3-дикарбонової кислоти (сполука 1). Сполука 1 являє собою білий або білий з жовтуватим відтінком дрібнокристалічний порошок. Температура плавлення - у межах 167-175°С (з розкладанням). За даними титрування 0,1 М розчином НСlО4 у крижаній оцтовій кислоті, вміст основної речовини становить від 97 до 101%. УФ спектр сполуки 1 у 0,01 М розчині КОН в 38130 1 2 (11) S 5 4 UA 1 5 N (19) 4 38130 метиловому спирті має максимум при довжині хвилі (257 ± 2) нм. Структура сполуки 1 підтверджена даними ІЧ та ЯМР спектроскопії, а індивідуальність - хроматографічними методами. При хроматографуванні в тонкому шарі у системі розчинників хлороформ-етанол-25% аміак (14:7:0,5) на платівках Силуфол U V254 значення Rf сполуки 1 та 2-амінотіазоліну (як можливої домішки) становлять 0,10 та 0,27, відповідно. ІЧ спектр, виміряний у дисках з КВг на приладі Specord M80, має характерні смуги поглинання при 1672 см -1 (СООН), 1704 см -1 (CO-NH) та 1612 см -1 (C=N, гетероцикл). ЯМР спектри вимірювались у розчинах ДМСО-d6 на приладі Bruker AM-300 (300 МГц для 1 Н та 75 МГц для 13С). Дані наведені у таблиці 1. З даних, наведених у таблиці 1, видно, що в ЯМР спектрах фіксуються всі структурні фрагменти сполуки 1, однозначно підтверджуючи цим її хімічну будову. Вивчення специфічної активності сполуки 1 проводили на експериментальних моделях патоспермії різної етіології у щурів популяції Вістар. Модель 1. Порушення сперматогенної функції викликали стресуванням щурів шляхом жорсткої іммобілізації по одній годині протягом семи днів [6]. Сполуку 1 вводили протягом 21 дня після стресування у максимально ефективній дозі (0,6 мг на 1 кг маси тіла) перорально через зонд у вигляді зависі у 1 мл 2% водного розчину крохмалю. Група порівняння отримувала аргініну гідрохлорид, максимально ефективна доза якого дорівнює 100 мг на 1 кг маси тіла [7]. Контрольна група отримувала розчинник за аналогічною схемою. Наступної доби, після припинення експериментальної терапії, щурів забивали, вилучали придаток сім'яника і дозовано (протягом 2 хвилин у 2 мл ізотонічного розчину натрію хлориду) вимивали з нього сперматозоїди. В отриманій таким чином суспензії визначали концентрацію сперміїв, процентний вміст рухливи х та морфологічно аномальних клітин [8]. Методом імуноферментного аналізу визначали рівень статевих гормонів у сироватці крові. Дані, наведені в таблиці 2, свідчать про те, що за умов введення сполуки 1 у стресованих щурів вірогідно зростала концентрація сперміїв, покращувалась рухливість та життєздатність статевих клітин. Позитивний ефект нової субстанції більш виражений, ніж ефект аргініну гідрохлориду в аналогічних умовах. Як видно із таблиці 3, під впливом сполуки 1 у спресованих щурів спостерігалась тенденція до збільшення концентрації тестостерону в периферичній крові порівняно зі стресованими тваринами, яким вводили розчинник. Рівень естрадіолу, навпаки, мав тенденцію до зниження. При застосуванні аргініну гідрохлориду рівень тестостерону лишався таким, як у контролі, а концентрація естрадіолу мала тенденцію до зростання. Отримані дані свідчать, що введення сполуки 1 сприяє абсолютній та відносній андрогенізації організму, що є позитивним для стимуляції сперматогенезу у випадках його порушень, обумовлених дефіцитом тестостерону. Модель 2. Для вивчення специфічної дії спо луки 1 обрали модель радіаційного порушення сперматогенезу [9]. Самці щурів були опромінені на рентгенотерапевтичному апараті РУМ-17 по 0,25 Гр протягом трьох днів. С умарна доза опромінення складала 0,75 Гр. Сполуку 1 у дозі 5,9 мг на 1 кг маси тіла у водному розчині твіну-80 вводили перорально протягом 8 днів, з них останні три дні введення відбувалось на фоні опромінення. Сперматогенну функцію досліджували через 48 днів так само, як описано в моделі 1. Дані, наведені в таблиці 4, свідчать про те, що у тварин, підданих дії радіації на фоні введення сполуки 1, спостерігалась тенденція до збільшення концентрації сперміїв у епідимальній суспензії та вірогідно зменшувалась кількість морфологічно аномальних статевих клітин порівняно з опроміненими тваринами, які отримували розчинник. Вивчення естрогенної та антиестрогенної активності сполуки 1 виконане на інфантильних самках щурів [10]. Як стандарт естрогенної активності використано естрон, олійний розчин якого вводили підшкірно протягом трьох днів по 2 мкг на самку. Сполуку 1 за такою ж схемою вводили перорально в дозі 5,9 мг на 1 кг маси тіла як таку або водночас з естроном. Контрольні самки отримували ін'єкції розчинників. Об'єктом дослідження була матка, яка є естрогензалежним органом, і збільшення її маси свідчить про наявність у досліджуваних сполук естрогенних властивостей. Отримані дані наведені у табл. 5, з якої видно, що після введення естрону відбувалося значне, порівняно з контролем, зростання маси матки. У самок, які отримували сполуку 1, маса матки не відрізнялась від такої у контролі і була значно меншою, ніж після введення естрону. Введення сполуки 1 водночас з естроном не зменшувало естрогенний ефект останнього. Це свідчить, що 3-(4,5-дигідротіазол-2-іл)амід цис1,2,2-триметилциклопентан-1,3 дикарбонової кислоти не має ні естрогенних, ні антиестрогенних властивостей. Андрогенно-анаболічну та антиандрогенну активність вивчали на статевонезрілих самцях щурів, кастрованих за два тижні до початку експерименту. Сполуку 1 вводили перорально в двох дозах - 0,6 та 5,9 мг на 1 кг маси тіла щоденно протягом 7 днів. Андрогенно-анаболічну активність досліджуваної сполуки оцінювали за реакцією андрогензалежних органів - сім'яних пухирців, передміхурової залози та musс. levator ani [11]. При визначенні антиандрогенної активності сполуку 1 вводили водночас з пропіонатом тестостерону (1 мг на 1 кг маси тіла). Зменшення стимулюючої дії останнього на масу андрогензалежних органів кастрованих щурів може свідчити про наявність у сполуки антиандрогенних властивостей [12]. Тварин забивали наступної доби після припинення ін'єкцій. З даних, наведених у таблиці 6, видно, що на відміну від ефекту тестостерону пропіонату, введення якого викликає значне зростання маси андрогензалежних органів, введення сполуки 1 не змінює маси останніх. Це свідчить про відсутність у цієї нової сполуки андрогенно-анаболічних властивостей. Введення сполуки 1 разом з пропіонатом тестостерону не зменшувало андрогенний вплив на 2 38130 акцесорні органи, що свідчить про відсутність у сполуки 1 антиандрогенного ефекту. Гостра токсичність сполуки 1 визначена за методом Літчфільда-Уілкоксона. Встановлено, що ЛД50 при вн утрішньочеревному введенні складає 584 мг на 1 кг маси тіла. При пероральному способі введення ЛД50 визначити не вдалося, бо навіть при введенні 10 г сполуки на 1 кг маси тіла загибель щурів не спостерігалась. Це дозволяє віднести сполуку 1 до класу практично нешкідливих речовин [13]. Таким чином, результати біологічних досліджень свідчать про те, що 3-(4,5-дигідротіазол-2іл)амід цис-1,2,2-триметилциклопентан-1,3-дикарбонової кислоти у малій дозі стимулює сперматогенну функцію, позбавлений гормональних та антигормональних властивостей і відноситься до класу практично нешкідливих речовин. Це дає підстави вважати нову біологічно активну сполуку 3-(4,5-дигідротіазол-2-іл)амід цис1,2,2-триметилциклопентан-1,3-дикарбонової кислоти перспективною для подальшого створення ефективного потенціального засобу для лікування олігозооспермій, обумовлених абсолютною або відносною гіпоандрогенізацією, а також випадків ідіопатичної безплідності у чоловіків. matologenic arrest with arginine // Fertil. Steril. -1976. - V. 27. - р. 282-283. 5. Shill W.P. Recent progress in pharmacological therapy of male subfertility - a review // Andrologia. 1979. - V. 11, № 2. - р. 77-107. 6. Байкова О.В. Цитофизиологические показатели состояния репродуктивных органов крыс-самцов после 7-дневного иммобилизационного стресса и 7-дневной гипокинезии // Космич. биол. и авиакосмич. мед. - 1988. - № 5. - С. 56-59. 7. Гомон О.М. Фармакологічне дослідження солей аргініну як засобу для негормональної корекції сперматогенезу: Автореф.дисс. ... канд. біол. наук. - Одеса, 1997. - 17 с. 8. Саноцкий И.Ф., Фоменко В.Н. Отдаленные последствия влияния химических соединений на организм. - М.: Медицина, 1979. - 232 с. 9. Бриль Э.Е., Дразнин Н.М. Влияние ионизирующего излучения на половые железы // Радиац. эндокринол. - Обнинск, 1971. - С. 123-140. 10. Савченко О.Н. Гормоны яичника и гонадотропные гормоны. - Л.: Медицина, 1967. - 270 с. 11. Кабак Я.М. Практикум по эндокринологии. Основные методы экспериментально-эндокринологических исследований. - М.: Изд-во МГУ, 1968. - 275 с. 12. Резников А.Г., Варга С.В., Демкив Л.П. Экспериментальное изучение антиандрогенной активности 4-нитро-З-трифторметилизобутиранилида (нифтолида) у крыс и морских свинок // Фарм. и токсикол. - 1974. - № 3. - С. 336-341. 13.Сидоров К.К. О классификации токсичности ядов при парентеральных способах введения // Токсикология новых промышленных веществ / Под ред. Летавета А.А., Саноцкого И.В. - М: Медицина, 1973. - Вып. 13. - С. 135. Використана література: 1. Балаболкин М.И., Горохова Т.Ф. Консервативное лечение мужского бесплодия // Сов. медицина. - 1988. - № 5. - С. 36 - 43. 2. Возіанов О.Ф., Горпінченко І.У. Клінічна сексологія і андрологія. - К.: Здоров'я, 1996. - 536 с. 3. Лекарственные препараты. В 3 т. / Под ред. В.Н.Коваленко. - К.: "Мориан Лтд", 1996. 4. Jungling ML., Bunge R.G. The treatment of sper Таблиця 1 ЯМР спектральні параметри 3-(4,5-дигідротіазол-2-іл)аміду цис-1,2,2-триметилциклопентан-1,3-дикарбонової кислоти Атом або група Хімічний зсув ( в м.д.) dС 1-С 2-С 3-СН 4-СНАНв 5-СНСЦД 1-СООН 1-СН3 2-(СН3)2 3-CO-NH 21-С 41-СН2 51-CН2 експ. 55,57 46,01 53,30 22,39 33,17 177,00 20,87 21,57 22,46 175,37 160,93 52,52 31,00 обчисл. 53,4 40,4 51,6 23,3 33,2 180,5 16,4 20,0 22,0 177,8 159,9 57,3 33,1 3 dН, мультиплетність 2,91 т 2,00 м; 1,68 м 2,41 м; 1,37 м в обміні 1,15 с 0,71 с 1,13 с 9,75 с 3,79 м 3,14 т 38130 Таблиця 2 Специфічна активність 3-(4,5-дигідротіазол-2-іл)аміду цис-1,2,2-триметилциклопентан-1,3дикарбонової кислоти на моделі стресогенного пригнічення сперматогенезу Умови дослідження Статис тичний покаКонцентрація зник сперміїв, млн/мл 1. Інтактні тварини n 13 x 47,62 Sx 4,47 2. Стресування та n 11 введення розчинx 14,55 ника Sx 2,10 P1-2
ДивитисяДодаткова інформація
Автори англійськоюYaremenko Fedir Heorhiiovych, Svydlo Iryna Mykolaivna, Vakula Volodymyr Mykolaiovych, Hladkova Alla Ivanivna, Sydorova Iryna Vasylivna, Zolotukhina Valentyna Mykolaivna, Tarasenko Nataliia Yevheniivna, Vasylieva Tetiana Volodymyrivna, Hubarevych Iryna Heorhiivna
Автори російськоюЯременко Федор Георгиевич, Свидло Ирина Николаевна, Вакула Владимир Николаевич, Гладкова Алла Ивановна, Сидорова Ирина Васильевна, Золотухина Валентина Николаевна, Тарасенко Наталия Евгеньевна, Васильева Татьяна Владимировна, Губаревич Ирина Георгиевна
МПК / Мітки
МПК: C07C 61/00, C07D 513/02, A61K 31/166, C07D 277/08, A61P 15/08, A61K 31/167
Мітки: амід, триметилциклопентан, сперматогенез, 3(4,5, стимулює, кислоти, цис-1,2,2, іл, дигідротіазол, дикарбонової
Код посилання
<a href="https://ua.patents.su/6-38130-345-digidrotiazol-2-il-amid-cis-122-trimetilciklopentan-13-dikarbonovo-kisloti-shho-stimulyueh-spermatogenez.html" target="_blank" rel="follow" title="База патентів України">3(4,5 – дигідротіазол – 2 – іл) амід цис-1,2,2 – триметилциклопентан – 1,3 – дикарбонової кислоти, що стимулює сперматогенез</a>
Попередній патент: Спосіб визначення кров’яного тиску
Наступний патент: Бетонополімерний контейнер для зберігання, транспортування та захоронення екологічно шкідливих відходів
Випадковий патент: Пристрій для природної аерації водоймищ