Електроліт для рутеніювання та спосіб його одержання
Номер патенту: 56457
Опубліковано: 15.05.2003
Автори: Машкова Емілія Михайлівна, Лисенко Анатолій Григорович, Бабиченко Владислав Михайлович, Харькова Людмила Борисівна, Іванченко Людмила Миколаївна, Пехньо Василь Іванович, Волков Сергій Васильович
Формула / Реферат
1. Електроліт для рутеніювання, до складу якого входять електроактивний рутенієвий комплекс і сульфамінова кислота, який відрізняється тим, що містить електроактивний рутенієвий комплекс загальної формули:
[Ru2N(H2О)7(ОН)2СІ]Сl2,
а співвідношення рутенію до сульфамінової кислоти складає 1 до 2.
2. Спосіб одержання електроліту для рутеніювання нагріванням трихлориду рутенію з сульфаміновою кислотою, який відрізняється тим, що до розчину трихлориду рутенію в соляній кислоті при рН 1,8 додають сульфамінову кислоту при співвідношенні трихлориду рутенію до сульфамінової кислоти відповідно 1 до 2, після чого суміш нагрівають до встановлення рівноваги.
3. Спосіб за п. 2, який відрізняється тим, що трихлорид рутенію розчиняють у 0,2 н НСІ.
4. Спосіб за п. 2 або 3, який відрізняється тим, що суміш нагрівають при t = 70 - 80°C.
5. Спосіб за пп. 2, 3 або 4, який відрізняється тим, що суміш нагрівають протягом 2 годин.
Текст
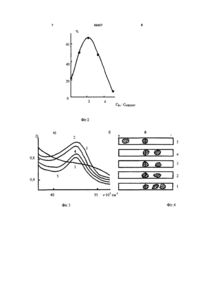
1 Електроліт для рутеніювання, до складу якого входять електроактивний рутенієвий комплекс і сульфамінова кислота, який відрізняється тим, що містить електроактивний рутенієвий комплекс загальної формули [Ru2N(H2O)7(OH)2CI]Cl2 а співвідношення рутенію до сульфамшової кислоти складає 1 до 2 2 Спосіб одержання електроліту для рутеніювання нагріванням трихлориду рутенію з сульфамшовою кислотою, який відрізняється тим, що до розчину трихлориду рутенію в соляній кислоті при рН 1,8 додають сульфамшову кислоту при СПІВІДношенні трихлориду рутенію до сульфамшової кислоти ВІДПОВІДНО 1 до 2, після чого суміш нагрівають до встановлення рівноваги 3 Спосіб за п 2, який відрізняється тим, що трихлорид рутенію розчиняють у 0,2 н НСІ 4 Спосіб за п 2 або 3, який відрізняється тим, що суміш нагрівають при t = 70 - 80°С 5 Спосіб за пп 2, 3 або 4, який відрізняється тим, що суміш нагрівають протягом 2 годин Винахід відноситься до електролітів та способів їх одержування, зокрема до електролітів металів групи платини, а саме рутенію, і може бути використаний в гальваностегії Є відомим, що якість гальванічного покриття і швидкість процесу гальваностегії визначаються складом електроліту, густиною електричного струму, який проходить через поверхню, на якій утворюють покриття, температурою електроліту В теперішній час в країнах ближнього та дальнього зарубіжжя для приготування електроліту рутеніювання використовують |>нггридо-бісакватетрахлорорутенат лужного металу або амонію загальної формули M3[Ru2NCIs (НгО^] (1), який описаний в пат США 4082624, C25D3/50, С01В9/02, 1976 Цей комплекс синтезують шляхом кип'ятіння протягом 2 годин водного розчину трихлориду рутенію RuCb з сульфамшовою кислотою NH2SO3H, причому ці реагенти беруть у співвідношенні солі до кислоти як 2 до 1, після чого відганяють частину води, а комплекс осаджують додаванням розчину КСІ та соляної кислоти Осад відокремлюють фільтруванням після 30-хвилинного перемішування реакційної суміші, після чого його сушать в вакуумі Вихід комплексу (1) складає майже 100% На основі водного розчину комплексу (1) готують електроліт Для підтримування робочого рН 1,3-1,8 в розчин вводять фосфатний буфер КН2РО4 + Н3РО4 (електроліт І) При використанні електроліту І, хоча у цілому утворюються ЯКІСНІ катодні осади, має місце безперервне зменшення виходу металу за струмом, що призводить з часом до погіршення якості катодних осадів через зміну стану ІОНІВ рутенію в електроліті І Задачею винаходу є новий ефективний електроліт для рутеніювання та спосіб його одержання Для вирішення цієї задачі автори пропонують новий електроліт для рутеніювання на основі нового електроактивного рутенієвого комплексу загальної формули [Ru2N (Н2О)7 (ОН)2 СІ] СІ2 (2), а співвідношення рутенію до сульфамшової кислоти складає 1 до 2, а також спосіб його одержання, який полягає в тому, що у відомому способі одержання електроліту для рутеніювання нагріванням трихлориду рутенію з сульфамшовою кислотою, новим є те, що до розчину трихлориду рутенію в соляній кислоті при рН 1,8 додають сульфамшову кислоту при співвідношенні трихлориду рутенію до сульфамшової кислоти ВІДПОВІДНО 1 до 2, після чого суміш нагрівають до встановлення рівноваги, 1 ю (О ю 56457 при цьому трихлорид рутенію розчиняють у 0,2н НСІ, а суміш нагрівають протягом 2 годин при t=70-80°C Новий елеістроліт (II) має вищий вихід рутенію за струмом, ніж такий для відомого (І), що показано на фіг 1, з якої видно, що залежність виходу рутенію за струмом п від температури в електролітах (І) і (II) з підвищенням температури різко зростає, досягаючи максимального значення при t = 70-80°С Причому, в електроліті (II) при t = const вихід рутенію за струмом вищий (фіг 1 крива 1), ніж для електроліту (І) (фіг 1, крива 2) Авторами також встановлено, що оптимальне співвідношення CRU CNH2SO3 - У новому електроліті (II) складає 1 2, що підтверджується даними, показаними на фіг 2-4, на яких відображені ВІДПОВІДНО ВИХІД рутенію за струмом (фіг 2), залежність електронних спектрів поглинання (фіг 3) та електрофореграм (фіг 4) від концентрації сульфаматйонів Залежність п (фіг 2) і D (фіг 3) від Сшгэоз мають екстремальний характер Також видно, що максимальні значення на цих кривих спостерігаються При СПІВВІДНОШеННІ CRU CNH2SO3- = 1 2 Встановлено, що в синтезованому електроліті для рутеніювання утворюється біядерний рутенієвий комплекс (2) при стехіометричному співвідношенні 2моля Ru 1моль NH2SO3H Як показали дослідження, саме цей біядерний комплекс є електроактивним С п і в в і д н о ш е н н я C R U CNH2SO3- = 1 2 є оптимальним для синтезу електроліту для рутеніювання, оскільки такий електроліт працює стабільно і забезпечує найвищий вихід рутенію за струмом На електрофореграмі розчину R11CI3 в 0,2н НСІ спостерігаються 3 види частинок, які з різною швидкістю мігрують в електричному полі нейтральна і дві позитивно заряджені Автори вважають, що це пдроксоаквакомплекси рутенію наступного складу [Ru(H 2 O) 3 OHCl2] 0 , [Ru(H 2 O) 4 OHCI] + , 2+ [Ru(H 2 O) 5 OH] До співвідношення C R U C N H2SO3- = 1 4 в розчині існують 2 види ІОНІВ ОДИН нейтральний і один позитивно заряджений При співвідношенні CRU CNH2SO3- = 1 5 електрофореграма показує утворення в електроліті (II) негативно заряджених комплексів При введенні у електроліт (II) сульфамат-йонів вихід рутенію за струмом спочатку збільшується (фіг 2) Максимальне його значення спостерігається при співвідношенні CRU CNH2so3- =1 2 Подальше збільшення C N H2SO3- ДО с п і в в і д н о ш е н н я CRU CNH2SO3- 1 5 призводить до різкого падіння п, При цьому співвідношенні електрофореграма (фіг 4, ЛІНІЯ 2) показує утворення в електроліті негативно заряджених комплексів В спектрах поглинання цих електролітів (фіг 5) в області 42000-28000см 1 спостерігається одна інтенсивна смуга поглинання, яка в свіжо приготовленому розчині відомого електроліту (І) (фіг 5, крива 2) зсунута в короткохвильову область (35000см 1 ) відносно смуги поглинання розчину (І) (фіг 5, крива 1,34150см 1 ) Після витримування електролітів при t = 70°С протягом 2-х годин максимуми на ЕСП збігаються (фіг 5, криві 1', 2') і різниця спостерігається лише в інтенсивності смуг поглинання, причому в електроліті (І) інтенсивність смуги поглинання при нагріванні зменшується, а в електроліті (її) - зростає Той факт, що після нагрівання протягом 2-х годин смуги поглинання в обох електролітах збігаються, дає можливість допустити ймовірність того, що в електроліті (II) також утворюється біядерний комплекс рутенію, який відрізняється від комплексу рутенію в електроліті (І) меншим вмістом СІюнів Непрямим доказом утворення в електроліті (II) біяденого комплексу Ru є те, що після нагрівання розчину (II) рутеній перестає визначатися в ньому за допомогою тюсечовини - реактиву для фотометричного визначення рутенію, в той час як тюсечовина в розчинах одно ядерного рутенію утворює з ним забарвлені в синій колір комплексні сполуки Утворення азотномостикового біядерного комплексу в електроліті її підтверджують ІЧ - спектри, які знімали як для вихідних кристалічних речовин, так і для розчинів Спектральні характеристики об'єктів дослідження представлені в табличній формі на фіг 6 і у графічному вигляді на фіг 7 ВІДМІННІСТЬ ІЧ-спектрів розчинів 7 і 8 в тому, що відбувся перерозподіл інтенсивності коливань при V 1450, 1378 1300 с м 1 Після нагрівання з'явились коливання при V 885, 650, 325 см 1 (фіг 7, графіки 2 і 3) В розчині 2 (фіг 7, графік 1) також є коливання при 325 см \ що віднесені ВІДПОВІДНО ДО літературних даних до валентних коливань зв'язків Ru-N-Ru (J R Campbell, R J H Clark Rezonance Raman Studies of the Nitndebndged Complex K 3 [Ru2N(H 2 O)2Cl8]JChemSos Dalton, 1981, p 1239-1240) Коливання при 6 5 0 с м 1 віднесені до коливань координованих молекул води, а смуги поглинання при 455, 305 та 285см 1 до валентних коливань (Ru-O) та (Ru-CI) ВІДПОВІДНО Утворення біядерного комплексу (II) із вихідних пдроксохлорокомплексів Ru 3 + при нагріванні можна представити наступним чином Спочатку сульфамат-йон замінює йон хлору у внутрішній сфері рутенієвого комплексу [Ru(H 2 O) 3 OHCl2] 0 + NH2SO3 [Ru(H2O) 3 (OH)CINH2SO 3 ] 0 + СІ [Ru(H 2 O) 4 OHCI] + + NH 2 SO 3 [Ru(H 2 O) 4 (OH)NH 2 SO 3 ] + + СІ Потім утворюється азотно містковий комплекс, в якому атом азоту сульфамат-йону замінює атом хлору в другій молекулі рутенієвого комплексу [Ru(H 2 O) 4 (OH)NH 2 SO 3 ] + + [Ru(H2O) 3 (OH)CINH 2 SO 3 ]° + Н2О [Ru 2 N(H 2 O)7(OH)2CI] + 2 + H 2 SO 3 + СІ Далі суть винаходу показано на графічному матеріалі та конкретних прикладах На фіг 1 показана залежність виходу рутенію за струмом від температури для відомого електроліту (І) і нового електроліту (II) при густиш струму і = 7мА/см 2 На фіг 2 представлений графік залежності виходу рутенію за струмом від співвідношення CRU CNH2SO3" На фіг 3 показана залежність електронних спектрів поглинання в електроліті (II) від концентрації CNH2SO3- CRU = 7,8г/л , розведення 1 25 CNH2so3-, моль/л 1-0, 2-7, 3-15, 4-23, 5-39 На фіг 4 є види електрофореграм електроліту (II) в залежності від к о н ц е н т р а ц і ї CNH2SO3 7,8г/л , розведення 1 25 CNH2SO3- МОЛЬ/Л CRU= 1-0, 2-7, 3-15, 4-23, 5-39 На фіг 5 на кривих 1 і 2 показані ВІДПОВІДНО електронні спектри поглинання в свіжо приготовлених електролітах (І) і (II) при розведенні 1 75 та на ВІДПОВІДНИХ кривих 1' і 2' - після нагрівання протягом 2-х годин при t = 70°С На фіг 6 на кривих 1 і 2 представлені ВІДПОВІДНО електрофореграми свіжо приготовлених електролітів (І) і (II) при розведенні 1 75 та на ВІДПОВІДНИХ кривих 1' і 2' - після нагрівання протягом 2-х годин при t = 70°C На фіг 7 в таблиці представлені ІЧ-спектри досліджуваних розчинів На фіг 8 показані графіки 1, 2 і З ІЧ- спектрів ВІДПОВІДНИХ розчинів № 2, № 7 і № 8, склад яких представлений в таблиці на фіг 7 Стан йонів рутенію в розчинах визначали методами ЕСП-спектроскопм та електрофорезу на папері, кінетика електродних процесів досліджувалася методом вольтамперометрм ІЧ-спектри 56457 знімали на спектрофотометрі SPECORD M80 як для вихідних кристалічних речовин, так і для розчинів (1 краплю його розтирали з КВг) Приклад синтезу сул ьфаматно-хлорид ного електроліту рутеніювання 12,8г хлориду рутенію розтирають в агатовій ступці до утворення однорідного порошку Порошок хлориду рутенію розчиняють в 900мл 0,2н соляної кислоти, нагрітої заздалегідь до 90°С Одержаний розчин переносять до колби на 1л і доводять до мітки гарячою 0,2н НСІ Роблять аналіз приготовленого розчину на вміст рутенію Додають у розчин розраховану КІЛЬКІСТЬ сульфамшовоі кислоти таким чином, щоб співвідношення Ru NH2SO3H=1 2, тобто біля 12г Витримують розчин на водяній бані з зворотнім холодильником при температурі 70°С протягом 2 годин Доводять рН розчину до 1,3-1,5 за допомогою концентрованого розчину гідроксиду амонію 40 20 40 20 Фіг. 60 80 t°C 56457 Фіг, 2 D 0.8 0,4 35 Фіг.З Фіг.4 56457 10 Г 0.8 2' 0.4 2 40 35 V10 3 CM"' Фіг. 6 Фіг. 5 Таблиця 1 2 Склад зіниіВДїОьсад кр. 4 H 2 SO3H+HCl L =0.8M;Ciicf=0,2N UC13 иСіз+НСІСкц-0,04 -aT/n;CHct=0,2N uQa+HCl+NHsSOsH RH- 0,04 г-ат/л; CL= ,08M;CHci=0,2N uCI3+HCH->JH2SO3H Ru-O,3Or-2T/ji; CL= 0,60 ; CHci=0s2 N t=70°C, = 2 час 8 1520 1395 13Q0 1460 1400 1385 1450 1450 3440 3380 1705 1655 1615 1800 1570 1545 1635 1540 1610 1635 3340 1625 1410 1315 1140 1070 3140 2610 2480 1625 1400 1320 1290 1180 1070 CRU- 0,30 г-ат/я; HjSOaH sp. 7 1655 1600 3410 О 3 5 6 V, C ' M 3410 3000 3140 2880 2560 3460 1075 1050 680 1265 1080 1310 1265 1070 1005 800 760 700 700 1310 1280 1070 1015 1005 720 700 550 535 455 410 450 550 375 325 310 330 270 380 550 310 315 1090 ФІг.? 1 745 700 1010 885 855 650 575 455 325 305 285 56457 11 12 1630 1450 1800 1400 725 1000 Підписано до друку 05 06 2003 р 600 Тираж 39 прим ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)236-47-24 200 VCM-l
ДивитисяДодаткова інформація
Назва патенту англійськоюRutheniuming electrolyte and method of its producing
Автори англійськоюVolkov Serhii Vasyliovych, Pekhnio Vasyl Ivanovych, Kharkova Liudmyla Borysivna, Lysenko Anatolii Hryhorovych, Babichenko Vladyslav Mykhailovych
Назва патенту російськоюЭлектролит для рутенирования и способ его получения
Автори російськоюВолков Сергей Васильевич, Пехньо Василий Иванович, Харькова Людмила Борисовна, Лысенко Анатолий Григорьевич, Бабиченко Владислав Михайлович
МПК / Мітки
Мітки: електроліт, рутеніювання, спосіб, одержання
Код посилання
<a href="https://ua.patents.su/6-56457-elektrolit-dlya-ruteniyuvannya-ta-sposib-jjogo-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Електроліт для рутеніювання та спосіб його одержання</a>
Попередній патент: Спосіб лікування папіломатозу слизових оболонок статевих органів у собак
Наступний патент: Спосіб очищення вихлопних газів двигуна внутрішнього згоряння
Випадковий патент: Установка для очищення стічних вод