Спосіб одержання похідних n-(4-індолілпіперідиноалкіл )бензімідазолону або їх солей з кислотами
Формула / Реферат
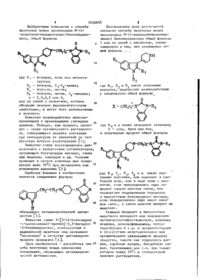
Способ получения производных N-(4-индолилпиперидиноалкил бензимидазолона общей формулы
где R1 - водород, хлор или метоксигруппа;
R2 - водород, C1-С3-алкил;
R3 - водород, метил;
R4 - водород, метил, С3-алкенил,
n = 2, 3, 4, 5 или 6, или их солей с кислотами, отличающийся тем, что соединение общей формулы
где R1, R2 и R3 имеют указанные значения, подвергают взаимодействию с соединением общей формулы
где R4 и n имеют указанные значения;
X - хлор, бром или йод, и полученный продукт общей формулы
где R1, R2, R3, R4 и n имеют указанные значения, или выделяют в свободном виде, или в виде соли с кислотой, если пиперидиновое ядро содержит только простые связи, или подвергают гидрированию водородом в присутствии благородного металла, если пиперидиновое ядро имеет двойную связь, а затем целевой продукт выделяют.
Текст
Способ получения производных Ы-(4-индолилгшперндиноалк.ил б е н з й м и д а з о л о н а общей формулы где R 1 ( R- и R- имеют указанные значения, подвергают взаимодействию с соединением общей формулы где R4 и п имеют указанные значения; X ~ бром или Йод, и получешйдЙ продукт общей формулы 00 где R^ - водород, хлор или метоксигруппа; водоролt алкил водород, метил; водород, метил, Cj-алкеиил, п. = 2,3,4,5 или 6, или их солей с кислоїами о т л и ч а ю щ и й с я тем, что соединение общей формулы R ЇЦ и n имеют указан» ные значения, или выделяют в свобод*-" ^ном виде, или в виде соли с кислотой, если пихтерндинорое ядро содержит только простые связи, или подвергают гидрированию водородом в присутствия благородного металла, если пиперидшювое ядро имеет двойную ' связь, а затем целевой продукт выделяют . где 1 S088665 Изобретение относится к способу Поставленная цель достигается получения 'новых производных К - ( 4 согласно способу получения новых -индолилпиперидинеалкил }бензимидазо-г ГІрОІ-иВОДНЬіХ N " (4-ИгіДОЛшїПНПЄрИДИРЮлока, общей формулы алкил) бензимидазолона общей формулы 1 ипи их солей с кислот ами, з аключающемуся в том, что соединение общей формулы „ . 10 R3 N где Я Э ™ водород, затор или метоксигруппа; 15 R^ - водород, С у С - - а л к н л ; Rj - водород, метил; R4 - водород, метил, С--алкенил; п = 2 , 3 , 4 , 5 или 6, » или пк солей с кислотами, которые 20 обладают ценными фармацевтическими свойствами, и могут быть использованы в медицине. Известно взаимодействие индолилпкперидина с производными галоидных алкилов. Реакция, как правило, проходит ь среде органического растворител я , связывающего кислоту основания при температурах от комнатной до температуры ЮШСШЇЯ растворителя t l j . Известно также восстановление цик- 30 лоалкенов в присутствии катализаторов,, содержащих благородные металлы, такие как платина, палладий и др. Реакцию проводят в мягких условиях при температуре ниже 70°С при нормальном или -3 повышенном давлении [2 J, Наиболее близким к изобретению является соединение формулы где R^, R ? и R имеют указанные значения, подвергают взаимодействию с соединением общей формулы где R, и п имеют указанные значения; X - хлор, бром или код, и полученный продукт общей формулы где R^, К о , К-,» ^ ' / 5 и п имеют ука 4 занные значения, или выделяют в сво . o бодном виде, или в виде соли с кисs обладающее антиаллергической активностью £з ]. Известен также І~£з-(4-бензгидрші-і-пиперазинил)-пропил]-2,3-дигидро- 5 0 -2-бензикндазолон, используемый в медицинской практике под названием "оксатомид" в качестве антиаллергического препарата [ 4 J . Цель изобретения - разработка c n o - s 5 соба попучения новых химических соединений, обладающих антиаллергической активностью. лотой, если пиперидиновое ядро содержит только простые с в я з и , или подвергают гидрированию водородом в присутствии благородного металла, если пиперидиновое ядро имеет двойную связ:>, а затем целевой продукт вы выделяют5. Реакцию проводят в присутствии инертного полярного или неполярного органичєскогосїраетворителя, например этанола, диметилформамида, тетрагидрофурана и т . д . и предпочтительно в присутствии неорганического или органического связывающего кислоту средства, такого как гидроокись натрия, карбонат натрия, бикарбонат катрия, триэтиламин или т . п . при температурах между 20 С и температурой кипения растворителя. 1088665 -3-изопропенил-бенэимидазолона, Последующее гидрирование осущест1,3 г бикарбоната натрия, 30 мл димевляют при температурах около 20°С при тилформамида и 30 мп тетрагидрофуранормальном или повышенном давлении. ня нагревают с обратным холодильниПригодными благородными металлами для ком в течение 16 ч . Затем реакционкатализатора являются палладий или ную смесь вливают в смесь льда и амми' плаїина. ака, экстрагируют этилацетатом и поСоединения общей формулы ( 1 t я в лучаемый раствор промывают водой, ляются основными и за счет этого обсушат и в вакууме упаривают досуха. разуют кислотно-аддитивные соли с Остаток растворяют в простом эфире, неорганическими или органическими прибавляют эфирную соляную кислоту кислотами. Физиологически переносии образующийся осадок 4мльтруют, мые кислотно-аддитивные соли могут сушат и растворяют в 100 мл этанола. быть образованы, например, с галогенПолучаемый раствор охлаждают, при водородистыми кислотами, предпочтитщательном размешивании прибавляют тельно хлористоводородной кислотой 1 16 мл концентрированной серной кислоили бромистоводородной кислотой, ты и оставляют стоять в течение 2 ч азотной , серной, о-фосфорной, винпри 20^С. Затем смесь вливают в смесь ной , лимонной, малеиновой, фумарольда и аммиака, образующийся осадок вой, пропионовой, маслянной, уксусфильтруют и перекристатшизовывают ной, янтарной, метансульфоновой, из этанола,. бензолсульфоновоь, п-толуолсульфоновой кислотами и т . д . Получают 3,2 г (55% от теоретиП р и м е р 1. Гидрохлорид ческого) указанного соединения с N-{3-£ 4~(2-метил-3-индолил)пиперидиточкой плавления І96°С. но]-пропил]бензимидазолона. Аналогично примерам I и 2 получаСмесь, состоящую из 1,06 г 2-меют следующие соединения. тил-3- (1 ,2,5,б-тетра^идропиридил-А- /I . N-[3-|jz+-(-1-метил-3-индолил)-индола, 1,05 г Ы~(3-хлор-пропил)-пиперидино]-пропил ]-бензимидазолон -бенэимидазолона, 0,42 г бикарбоната с точкой плавления 180 С, Выход 62%. натрия, 20 мл диметилформамида и I I . Гидрохлорид N-{3-f4-(3-индо30 20 мл тетрагидрофурана, размешивая» лил) -пиперидино 3-пропил -бензнмиданагревают до 100°С в течение 18 ч, золона с точкой плавления 2А0°С. ВыЗатем реакционную смесь вливают в ход 58%. 0 смесь 200 г льда и 100 мл концентриIII. Гидрохлорид N-J_3- [4-(5-метокрованного аммиака, образующийся осаси-3-индолил)-пиперидїШоЗ-пропил\док фильтруют и перекрисіаллизовы-бензпмидазолона с точкой плавления вают из этанола, . 178"С. Выход 71%. Получают 1,2 г (62% от теоретиАналогично описанному в примере ческого) продукта формулы IV, имею2 из 4-(3-индолил)-пиперидина. 1 щего точку плавления 215 С, у котороIV. N-f3-ГА-(3-ИНДОЛИЛ)-пипериди40 но j-пропклV-N -изопропеиил-бензимидаго R1=H, R 2 ^H, R 3 -CH 3 , n - 3 , R4=H. 1,5 г продукта растворяют в 100 мл золон с точкой плавления 68 С, Вы-*. уксусной кислоты и в течение 24 ч *од 42%. совместно с 0,8 г палладия (5% на V. Гидрохлорид N-{3-£^-(l-H3onpo~ угле) встряхивают при 20°С в водопил-3-индолил)~пиперидино -пропил]родной атмосфере и под давлением -бензимидазолона с точкой плавления 5 ати. Затем катализатор фильтруют 145°С. Выход 66%. и фильтрат вливают в смесь льда и VI. N-f2-С^-(3-индолил)-пиперидиаммиака, причем выделяется свободное ноЗ-этил^-бензимидазолон с точкой основание. Осадок фильтруют, сушат, плавления 116°С. Выход 61Z. І0 растворяют в этаноле и добавлением VII. Гидрохлорид N—f3—£А—(3—ІЇН— эфирной соляной кислоты переводят долил )-пиперидино J-пропил J -N' -метилв гидрохлорид. Получают 1,05 г ( 70% бензимидазолона с точкой плавления от теоретического ) указанного соеди140 6 С Выход 70%. нения с точкой плавления 264-269°С. V I I I . М-{3-[4-(1-пролил-3-индо~ П р и м е р 2. Н-{4-[4-(3-индолил) 55 -пиперидинеJ-бутил ]-бензимидазолон. лил ^-пиперидиноі-пропил ї-бєнзимио Смесь, состоящую из 3 г 4-(3-индадазолон с точкой плавлеїшя 103 С. лил )-пиперидина, 4 г 1-14-хлорбутил )Выход 74%. 1088665 IX. N-[3-[4-(2-метил-5-хлор-3ного антигистаминного действия внутри~индолнл)-пиперидино]-пропил}-бензикожно впрыскивают 3 мкг 0,3 мл гистмидазолон с точкой плавления 124°С. амина а физиологическом растворе Выход 56%. поваренной соли. X. N- [5-[4-(3-индолил)-пипериднПо истечении 30 мин после антино]-пентйл]-бензимидазолон с точкой генного раздражения крыс умерщвляют плавления 137-14О°С, Выход 49%. посредством СО2. Вдоль позвоночного XI. N-[б-[4-(3-индолил)-гшпериди~ столба делают р а з р е з , откидывают кожу HOJ-ГЄКСИЛ j-бензимндазолон с точкой и измеряют диаметр окрашенных в сиплавления 127-130°С. Выход 51%, 10 ний цвет мест (мм). Определяют средФармакологическое исследование нюю площадь каждого пятна (в мм^) новых соединений показало, что дейи по полученным данным рассчитывают ствупт два биологических механизма: среднюю общую площадь для группы обво-первых, соединения стабилизуют работанных крыс. Среднюю площадь тучные клетки и таким образом предот- J5 (в мм ^необработанной контрольной вращают выделение веществ-переносгруппы берут за !00% и определяют чиков, которые имеот место как следдозу исследуемых соединений, вызыствие реакции антигена с антителом вающую 50%-ное снижение окрашенной или с другими стимулирующими вещестплощади необработанной контрольной вами; во-вторых, соединения обладают 20 группы ( З Д ) . • 5й противогистаминными свойствами, т'»е. Результаты опыта приведены в они предотвращают действие гистамина, таблице. главного возбудителя аллергии человека. мг/кг Соединение ; о , Первое свойство обнаружено и с с л е - 25 дованиями по стабилизации тучных 2,5 Пример 1 клеток, второе - исследованиями по антигистаминному действию и оба свой3,8 Пример 2 ства подтверждаются опытом по определению пассивной кожной анафилак4 ,,£ 1 1 30 сии (ЯКА): 2,9 А. Опыт ПКА на крысах. Для дости1П жения воспроизводимых кожных реакций на площади диаметрами 10-15 мм не3,6 IV сенсибилизированным крысам дают р а з бавленную антисыворотку яичного аль- 35 1,6 VI бумина,0,1 мл этой разбавленной акти* сыворотки внутрикожно инъецируют мужIX ским крысам весом 150-160 г по каждой стороне побритой спины, а именно X 4,6 до антигенного раздражения. Исследуе- 40 мые соединения растворяют в воде, смешивают с 0,5 мл раствора 5 мг яичного альбумина и 2%-го Эванс блу и 1 мл/кг этой смеси внутривенно * Известное соединение. 45 инъецируют животным по истечении Новые соединения общей формулы 24 ч после пассивной сенсибилизации. 1 обладают более выраженной антиаллергической активностью. Для исследования оральной активности исследуемые соединения суспенБ . Уменьшение площади с синей дируют в растворе акациевой резины, 50 окраской кожи крыс, вызываемой гисткоторый в количестве 1 мл/кг дают амином. Мужских крыс весом 150-160 г животным при помощи желудочного зонт разделяют на две группы. Крысам обеих да. По истечении 20-30 мин после групп удаляют волосы на спине. Необоральной дачи исследуемых соединений вызывают антигенное раздражеработанной контрольной группе оральние дачей 0,015 мг яичного альбуми55 но дают 10 мл/кг нормального физиолона в 0,5-мл 2%-го раствора Эванс блу. гического раствора поваренной соли По истечении !5 мин после антигеннов 1%-м растворе акациевой резины. го раздражения для возбуждения сильПодвергаемой опыту группе также 8 1088665 7 орально дают 10 мл/кг исследуемого сое динения , суспендированного в I %-м растворе акациевой резины» Кроме того, всем животным внутривенно дают 0,5 мл 2%-го раствора Эванс блу в нормальном физиологическом растворе поваренной соли. По истечении 20 мин после дачи исследуемого соединения или контрольного раствора по 10 обеим сторонам побритой кожи спины крыс внутрикожно инъецируют раствор 3 мкг дифосфата гистамина в нормальном физиологическом растворе поваренной соли. По истечении 15 мин 15 после инъекции гистамина умерщвляют всех крыс при помощи С ; О ротки, вызывающей на 60-80% более вы сокую дегрануляцию по сравнению с нормальной крысиной сывороткой. По истечении 18-24 ч дагот соответствующее исследуемое соединение, а именно при внутривенной даче - немедленно, при внутрибрюшиннон даче - за 5 мин и при оральной даче - за 20 мин до антигенного раздражения, вызываемого 0,5 мг/кг ДВ.ІЖДЬІ кристаллизованного яичного альбумина в 0,005%-ном физиологическом растворе поваренной соли. дуемого соединения (соответственно 5 крыс). Крысам группы 1 внутрибрюшинно дают 3 мл нормальной крысиной сыворотки. Крысам групп IT-V также внутрибрюшинно дают 3 мл антнсыво В описанных опытах и с ел еду FIT активность нового гидроклорида N-{3- [(4-индолил)пилериднно}лропил] бензимидазолона (П ) и указанного и з вестного соединения оксаточид. Результаты опытов сведены в таблице. По истечении 15 мин после вызывания раздражения умерщвляют крыс посредством СО,. В случае, если для чидукцни дегрануляцнн тучных клеток исполь.эовался сополимер N-метилгомоВдоль позвоночного столба делают анизиламина и формальдегида, то групсрез и тщательно отделяют кожу. Кожу пе I внутрибрюшинно дают 3 мл расттыльной стороны откидывают и изме20 вора Ханка со значением рН 7,2-7,4. ряют диаметр окрашенных в синий цвет Положительной контрольной группе пятен. Для каждого синего пятна опи тем группам, которым дали исследуе(мм ределяют площадь (мм (и высчитывают мое соединение, внутрибрюшишю дают среднюю площадь для контрольных 20 мкг/кг указанного соединения в и подопытных групп. Среднюю площадь 25 3 мл раствора Ханка, имеющего значеконтрольной группы берут за 100% ние рН 7,2-7,4. Этих крыс также умерщи путем линейной регрессии опредевляют посредством С > по истечении Г2 ляют дозу исследуемых соединений, 5 мин после внутрибркяаинной инъекции. которая вызывает 50%-ное уменьшение окрашенной площади контрольной групДля определения размера деграну30 пы. ляции тучных кпеток в необработанных В. Ингибнция перитонеальной деи обработанных группах крыс делают грануляции тучных клеток ДТК у крыс, микротомные срезы брыжейки , которые пассивно сенсибилизированных с помоподвергают анализу аналогично методу щью яично-альбуминовой антисыворотки А Фюгнера. Результаты высчитывают в или путем индукции сополимера N-ме35 процентах ингибиции дегрануляции тил-гомоанизиламина и формальдегида. следующим образом.* Мужских крыс весом І 50-160 г подразОпыт-отрицательный Процент деляют на пять групп. Группа I - неИНГИбИ = 100 контроль специфический контроль ДТК (3 крысы), 100 положитель- отрица40 ции Группа "Л - положительный контроль ный конттепьный ДГК (5 крыс). Группы I I I , IV, V роль контроль положительная Д К после дачи исслеТ Исследуемое соединение Оксатомид ДТК антигистаминовое действие 8,3 Отрицат 8,1 I,6 3,0-6,4 8,7 Соединение 9 1088665 Результаты опытов подтверждают двойное преимущество нового соединения перед известным; око обладает значительным стабилизирующим тучные клетки действием наряду с хорошими антнгистамшшыми свойствами и в пять раз активнее известного соединения оксатомида, Редактор С. Патрушева io Соединения общей формули І яли соли с кислотой обладают антиаллергической "эффективностью ч поэтому пригодны для лечения аллергических забо5 леваний, таких как аллергическая .стма, ринит s конъюнктивит, сенная лихорадка, аллергия к пищевым продуктам и другие. СоставиЇель Ж. Сергеева Техред Т .Фанта Корректор А. 'Гнско Заказ 2704/55 Тираж 410 Подписное В И Г Государственного комитета СССР И ИШ по делам изобретений и открытий 113035, Москва, Ж-35, Раушская н а б , , д . 4/5 Филиал П П "Патент", г, Ужгород, ул. Проектная, А П
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for synthesizing derivatives of n-(4-indolylpiperidine alkyl) benzimidazolon or their salts
Назва патенту російськоюСпособ получения производных n-(4-индолилпиперидиноалкил) бензимидазолона или их солей с кислотами
МПК / Мітки
МПК: A61P 9/12, A61K 31/445, A61P 43/00, C07D 401/14, C07B 61/00, A61K 31/4427, A61P 37/08
Мітки: солей, бензимідазолону, спосіб, одержання, кислотами, n-(4-індолілпіперідиноалкіл, похідних
Код посилання
<a href="https://ua.patents.su/6-7228-sposib-oderzhannya-pokhidnikh-n-4-indolilpiperidinoalkil-benzimidazolonu-abo-kh-solejj-z-kislotami.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання похідних n-(4-індолілпіперідиноалкіл )бензімідазолону або їх солей з кислотами</a>
Попередній патент: Контактний плоский дріт
Наступний патент: В’язальна машина
Випадковий патент: Спосіб профілактики післяопераційних ускладнень внаслідок гемороїдектомії