Трансдермальна терапевтична система та спосіб її одержання
Номер патенту: 26560
Опубліковано: 11.10.1999
Автори: ШНАЙДЕР Герхард, Хілле Томас, Хоффманн Ханс-Райнер, Хубер Ханс-Іоахім, КНОХ Аксель, Штаніслаус Фрітц
Формула / Реферат
1. Трансдермальная терапевтическая система для нанесения лекарственного средства на кожу, состоящая из непроницаемого для активного вещества покровного слоя, клейкого резервуарного слоя, контактирующего с ним слоя - депо активного вещества, отличающаяся тем, что резервуарный слой содержит 70 - 90мас.% полимерного материала, выбранного из группы, состоящей из блок-сополимеров на основе стирола и 1,3-диенов, полиизобутилена, полимеров на основе акрилата и/или метакрилата, при этом депо активного вещества непосредственно после изготовления содержит 45 - 60мас.% 25 - 30% - ного раствора физиостигмина.
2. Система по п.1, отличающаяся тем, что она дополнительно содержит отделяемый защитный слой.
3. Система по пп.1 или 2, отличающаяся тем, что резервуарный слой содержит дополнительно до 12мас.% пластификатора на основе сложных эфиров.
4. Система по п.3, отличающаяся тем, что резервуарный слой в качестве пластификатора содержит диоктилциклогексан, ди-н-бутиладипат, триглицериды или изопропилмиристат.
5. Система по любому из пп.1 - 3, отличающаяся тем, что полимерный материал представляет собой полимер на основе акрилата и/или метакрилата и сложных эфиров гидрированной канифоли.
6. Система по п.5, отличающаяся тем, что в качестве эфира гидрированной канифоли полимерный материал содержит ее глицериновый или метиловый эфир.
7. Система по любому из пп.1 - 3, отличающаяся тем, что полимерный материал представляет собой самосшивающийся акрилат - сополимер 2-этил-гексилакриалата, винилацетата, акриловой кислоты и титан-хелат-эфира.
8. Система по любому из пп.1 - 3, отличающаяся тем, что полимерный материал представляет собой несамосшивающийся акрилат - сополимер 2-этил-гексилакрилата, винилацетата и акриловой кислоты.
9. Система по любому из пп.1 - 3, отличающаяся тем, что полимерный материал в качестве полимера на основе метакрилатов содержит сополимер на основе диметиламиноэтилметакрилата и нейтральных эфиров метакриловой кислоты.
10. Система по любому из пп.1 - 3, отличающаяся тем, что в качестве растворителя физостигмина используют масляную, ундециловую, версатиковую кислоты или смесь октадекановых кислот.
11. Способ получения трансдермальной терапевтической системы для нанесения лекарственного средства на кожу путем нанесения его на текстильную основу, которую, в свою очередь, располагают на матрице и снабжают покровным и защитным слоями, отличающийся тем, что предварительно для получения клейкого резервуарного слоя (матрица) смешивают 70 - 90мас.% полимерного материале, выбранного из группы, состоящей из блок-сополимеров на основе стирола и 1,3-диенов, полиизобутилена, полимеров на основе акрилата и/или метакрилата, смесь наносят на антиадгезионную подложку, которую затем удаляют, а на полученной таким образом матрице располагают текстильную основу, на которую наносят 45 - 60мас.% раствора физостигмина с концентрацией 25 - 30мас.% с образованием депо-слоя.
12. Способ по п.11, отличающийся тем, что в качестве полимерного материала используют полимер на основе акрилата и/или метакрилата и сложных эфиров гидрированной канифоли.
13. Способ по п.11, отличающийся тем, что при получении резервуарного слоя добавляют до 12мас.% пластификатора на основе сложных эфиров.
Текст
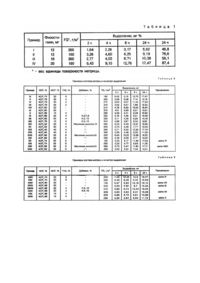
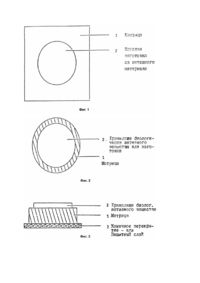
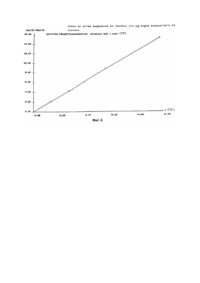
Изобретение касается трансдермальной терапевтической системы, которая содержит физостигмин в качестве активной компоненты, и способа ее получения. Использование физостигмина для лечения болезни Альнхаймера описано в литературе, причем действие вещества оценивается различно разными авторами. Так как этот алкалоид обладает высоким эффектом первого прохождения (first pass effect) - биораспространяемость физостигмина при введении через рот составляет 5%, то отклонения результатов объясняются вариантами применения. В выложенной заявке ФРГ ДЕ-OS №3528979 описан состав, который наряду с физостигмином содержит карбоновую кислоту со средней длиной цепи; этот состав может быть нанесен на бинт, прокладку или компресс, которые закреплены с помощью перевязки. Этот способ применения не представляет собой терапевтическую систему, для которой предусматривается, что бандаж (бинт), компресс или прокладка снабжены резервуарным внутренним слоем, непроницаемой защитной перфорированной пленкой или непроницаемой защитной фольгой, а между резервуаром и кожей наносится не описанная ранее диффузионная управляющая мембрана. Ни диффузионная управляющая мембрана, ни защитные пленки не были описаны раньше. Карбоновые кислоты специально указаны как активное транспортное связующее средство для проникновения лекарства через кожу, так как иначе нельзя было бы обозначить это проникновение через кожный барьер. Это высказывание не является научно обоснованным. В патенте ФРГ ДЕ - PS №3606892 описано ретардационное применение физостигмина и других биологически активных веществ, которое может осуществляться трансдермально (через кожу). Специальная рецептура не раскрыта, а напротив, имеется ссылка на уже описанную рецептуру (патент США US-PS №3921363). Наряду с весьма неопределенными примерами исполнения трансдермальной терапевтической системы ни в одной из обеих вышеупомянутых выложенных заявок не указывается на нестабильность физостигмина, о которой уже было давно известно (bber W., Iharmaz. Ztg. 37, 483/ 1888/; Herrig F., Ma yer H., Mh. Chem. 18, 379 /1897/; Herrig F., Lieb H., Там же, 39, 285 /1918/; Solve y A.A., T. Chem. Soc (London) 101, 978 /1912). Нестабильность вследствие очень быстрого разложения устанавливает узкие границы для использования физостигмина в фармацевтике. Задачей изобретения поэтому является приготовление физостигмина или фармацевтически переносимых солей физостигмина в форме трансдермальной терапевтической системы, которая через 24ч контролируемо отдает физостигмин или его фармацевтически переносимую соль и гарантирует, что физостигмин во время хранения подготовленной трансдермальной терапевтической системы не будет значительно разлагаться. Решение задачи осуществляется благодаря тому, что физостигмин, по крайней мере, 25% - й растворяют в растворителе или смеси растворителей, которые должны быть физиологически переносимыми с тем, чтобы считать, что не только физостигмин, но также и растворитель мигрируют через матрицу. Этот раствор может быть при помощи давления, как например, описано в выложенной заявке ФРГ ДЕ - OS №3629304, нанесен на текстильную заготовку, располагающуюся на матрице, которая предварительно снабжена активным непроницаемым, в случае необходимости, отделяемым защитным слоем. В заключение текстильная заготовка с нанесенным раствором и матрица покрывают предварительно подготовленным, также непроницаемым для активного вещества покровным слоем. С помощью специального штанцевального инструмента, поверхность которого круглая и явно больше, чем поверхность заготовки из нетканого материала, осуществляется вырубка. В заключение делается решетчатая сетка на свободных от активного вещества краях. Этот способ, в принципе, известен и описан в выложенной заявке ФРГ ДЕ -OS №3629304. Однако, в вышеуказанной выложенной заявке в качестве вещества-примера служит никотиновое основание. Так как никотиновое основание при комнатной температуре жидкое, этот способ не может быть адаптирован просто. Напротив, физостигмин должен вводиться высокопроцентным, а именно, 25% - ным в растворе, так как, хотя индивидуальное дозирование порошкообразных компонент распространено в те хнологии твердых лекарственных форм, однако в те хнологии полутвердых лекарственных форм оно абсолютно неизвестно, потому что этот вопрос до сих пор не стоял. Одновременно растворитель должен удовлетворять еще трем важнейшим требованиям: - он не должен разлагать высоко нестабильный физостигмин, - он должен не вызывать никаких сомнений с точки зрения физиологии, - он должен обеспечивать, чтобы физостигмин хорошо растворяющийся во время приготовления системы, во время хранения, однако, растворялся бы крайне незначительно. Карбоновые кислоты, которые содержат более 10 атомов углерода, удовлетворяют названным требованиям. При смешении физостигмина с этими соединениями происходит как повышение растворимости, так и образование солей. Принципиально, однако, что такие заготовки при комнатной температуре являются жидкими. Растворимость биологически активного вещества в матрице понижена (в результате чего будет достигнуто достаточное выделение) благодаря тому, что в матрицу введена высокая доля базисного полимера, например, сополимеризат катионного характера на основе диметиламиноэтилметакрилата и других нейтральных эфиров метакриловой кислоты. В результате этого после нанесения матрицы происходит кислотно-основная реакция между карбоновой кислотой и основным полимером, вследствие чего существенно понижается растворимость активного вещества. На основании данных рецептурных примеров может быть показано, что скорость выделения увеличивается с возрастанием доли основного полимера в матрице. Схематическое построение системы может быть более детально пояснено с помощью прилагаемых схем. Наружный слой 4 может состоять из эластичного или не эластичного материала и иметь один или несколько слоев. Материалы, которые могут быть применены для его изготовления, это полимерные вещества, такие как, например, полиэтилен, полипропилен, полиэтилен-терефталат, полиамид. В качестве других материалов могут также использоваться металлические пленки, такие как алюминиевая фольга, просто фольга или же фольга, покрытая полимерным субстратом (в последнем случае 5). Могут применяться также и текстильные поверхностные образования, если составные части резервуара вследствие и х физических особенностей не могут проходить через текстильный материал. У наиболее предпочтительной формы исполнения покрывной слой 4 состоит из комбинированного материала, который обеспечивает прочность ламината и служит барьером против потерь составных частей ламината. Наряду с этим для этих целей пригодны также пленки, полученные напылением алюминия или комбинированные пленки. К покровному слою 4 примыкает матрица 1. Во время четырнадцатидневного выдерживания (хранения) физостигмин переходит из хранилища биологически активного вещества 2, в матрицу 1 и насыщает ее, таким образом матрица превращается в резервуарный слой. Матрица обладает таким свойством, которое обеспечивает связанность системы. Матрица состоит из основного полимера и, в случае необходимости, обычных добавок. Выбор основного полимера сориентирован на химические и физические свойства физостигмина. В качестве примера могут быть названы следующие полимеры, каучук, каучукоподобные, синтетические гомо-, сополимеры или блок-полимеры, эфир полиакриловой кислоты и его сополимеры. Как правило, речь может идти о всех полимерах, которые могут применяться при изготовлении вязких клеев. Они физиологически но, должны вызывать опасений и не должны разлагать физостигмин. Наиболее предпочтительными являются такие полимеры, которые являются блок-сополимерами на базе стирола и 1,3диена, а также полиизобутилены или полимеры на базе акрилата и/или метакрилата. Из числа блок-сополимеров на базе стирола и 1,3-диена наиболее пригодными являются линейные стирол-изопрен-блок-сополимеры. В качестве полимеров на основе акрилата наиболее предпочтительными будут акрилат-сополимеры 2-этилгексил-акрилата, винилацетата и акриловой кислоты с или без титанхелат-эфира. В качестве метакрилатов предпочтительными являются сополимеры на основе диметил-амино-этил-метакрилата и тейтральных эфиров метакриловой кислоты. В качестве сложного эфира гидрированной канифоли наиболее преимущественное применение находят, в особенности, метиловый - и глицериновый эфиры. Тип возможных добавок зависит от используемого полимера и биологически активного вещества, В соответствии с их функциями эти добавки подразделяются на следующие: пластификаторы, агенты повышения клейкости, стабилизаторы, вещества-носители, добавки, регулирующие диффузионные и пенетрационные процессы, или вещества-наполнители. Рассматриваемые для этих целей, не вызывающие физиологических опасений вещества известны всем специалистам. Резервуарный слой обладает такой способностью к повышению клейкости, которая обеспечивает надежно длительный контакт к коже. Примерами пригодных пластификаторов могут служить диэфиры дикарбоновых кислот, например ди-н-бутиладипат, а также триглицериды, где в первую очередь можно назвать триглицериды со средней длиной цепи каприловой/каприновой кислоты кокосового масла. Между матрицей 1 и покрывным слоем 4 располагается хранилище биологически активного вещества 2. Оно состоит из текстильного образования и раствора физостигмина. Текстильное образование может быть в виде круглой заготовки из нетканого материала (смесь волокон, вискозное волокно) хлопок в соотношении 50 : 50, у которого вес единицы поверхности составляет 40г/м 2 или же 80г/м 2) с диаметром от 20 до 50мм. Возможно также применение и других текстильных материалов и, соответственно, других размеров диаметра. В качестве соединения с, по крайней мере, одной кислой группой предпочтительны высшие жирные кислоты, так как размер возможного кожного раздражения, вызванный мигрированием кислот, зависит от длины цепи кислоты. Примерами пригодных кислот служат масляная кислота, изостеариновя кислота, ундециловая кислота и версатиковая кислота. Отделяемый защитный слой, который находится в соприкосновении с резервуарным слоем, и будет удален перед применением, состоит, например, из тех же самых материалов, которые используются для изготовления покровного слоя 4, при условии, что он должен быть отделяемым, например, посредством силиконовой обработки. Другими отделяемыми защитными слоями могут быть, например, политетрафторэтилен, обработанная бумага, целлофан, поливинилхлорид и другие. Если предлагаемый в соответствии с данным изобретением ламинат перед нанесением защитного слоя будет разделен на применяемые в терапии форматы (кусочки пластыря), то подлежащие нанесению форматы защитного слоя, в этом случае, будут иметь выступающие концы для того, чтобы с их помощью они могли быть легко отделены от пластыря. Ниже более подробно поясняют операции по изготовлению. Прежде всего приготавливается матрица 1, состав которой указывается в отдельных рецептурных примерах. После удаления покрывающей пленки будет сделана круглая заготовка из нетканого материала, поверхность которой должна составлять 13,72см 2. В качестве нетканого материала применяется материал из смеси волокон вискозы/хлопка в соотношении 70 : 30 с весом единицы поверхности 40г на квадратный метр. Затем из матрицы с наложенной на нее заготовкой вырезают прямоугольник площадью 56см 2. Круглая заготовка и матрица изображены на фиг.1 и 2. Теперь с помощью соответствующего приспособления, например, с помощью капельной пипетки физостигмин - 25% - ный в масляной кислоте или 35% - ный в ундециловой кислоте - наносится на нетканый материал. Точные количества устанавливаются в отдельных рецептурах. После нанесения хранилище биологически активного вещества 2 и матрица 2 будут накрыты покровной пленкой 4. Покровной слой это клеевой слой, который состоит из мультиакрил-сополимера, наносимого на полиэфирную пленку толщиной 15мкм. После удаления растворителя вес единицы поверхности составляет 30г/м 2. После покрытия будет высечена круглая поверхность размером 21, 23см 2, так что пропитанная биологически активным веществом заготовка из нетканого материала будет находиться в середине (фиг.3 и 4). В заключение края будут обрешетчены и полученная трансдермальная терапевтическая система выдерживается в течение 14 дней при 40°C. Образование предлагаемой по изобретению системы представлено на фиг.1 - 4. На фиг.1 представлен вид на заготовку из нетканого материала 2, которая накладывается на матрицу 1. После наложения заготовки 2 из нетканого материала на матрицу 1 будет наноситься жидкая композиция биологически активного вещества, благодаря чему будет образовано хранилище биологически активного вещества 2. В заключение с помощью кэширования над матрицей 1 и хранилищем биологически активного вещества 2 наносится покровной слой 4. После чего осуществляется штанцевание. Края будут отделены с помощью решетчатой вырубки. На фиг.2 и 3 показаны схематически вид сверху (фиг.2) и поперечное сечение (фиг.3) изделия, где наглядно видно расположение хранилища биологически активного вещества 2 на матрице 1 и расположение конечного перекрытия 3 после штанцевания. На фиг.4 - система, поперечное сечение. На фиг.1 - 4 приняты следующие обозначения: 1 - матрица; 2 - хранилище биологически активного вещества или же круглая заготовка из нетканого материала; 3 - защитный (конечное перекрытие) слой; 4 - покровной слой; 5 - металлическая пленка (фольга). Пример 1. Изготовление матрицы: 10,91кг 40% - ного раствора самосшивающегося акрилат-сополимера 2этил-гексил-акрилата, винилацетата и акриловой кислоты с титан-хелат-сложным эфиром, смесь растворителей (этилацетат : этанол : гептан : метанол = 64 : 25 : 9 : 2) и 2,4кг 50% - ного раствора катионного сополимеризата на основе диметиламиноэтилметакрилата и нейтрального эфира метакриловой кислоты в этилацетате были смешаны с 360г триглицеридов каприловой/каприновой кислот при комнатной температуре, и при перемешивании. С помощью соответствующего ракеля наносят полученный состав на полиэфирную пленку с напыленным алюминием и накрывают полимерной пленкой (из полиэтилена - низкой плотности) Вес единицы поверхности должен составлять от 260,00 до 275г/м 2. Состав матрицы 1, %: Полиэтиленовая пленка будет удалена и наложен нетканый материал в виде заготовки. На нетканый материал с помощью капельной пипетки будет наноситься смесь 12мг физостигмина и 36мг масляной кислоты. Все последующие примеры и пример 1 приведены в следующи х таблицах, представленных в приложении. Выделение "ин витро" было определено в водяной бане со встряхиванием при 37°C. В качестве акцепторной среды служили 100мл физиологического раствора поваренной соли, который полностью сменялся после 2, 4 и 8ч. Концентрации после 2, 4, 8 и 24ч определялись при помощи УФ-спектроскопии. Приведенные в таблицах значения выделения являются соответствующими суммами измеренных концентраций. Табл.1 показывает образование и "ин витро" выделение в примерах l - lV. В эти х примерах использовалась одна и та же матрица, но количество нанесенного вещества варьировалось; был нанесен физостигмин в виде 25% - ного раствора в масляной кислоте. При этом установили, что с ростом содержания (доли) физостигмина возрастает не только абсолютное, но также и относительное выделение. В примерах lV - XXlll дозировались 20мг физостигмина, растворенные в 60мг масляной кислоты. Варьировались процентный состав матрицы и вес единицы поверхности (FC). Данные матрицы представлены в табл.2. В таблицах использованы следующие сокращения: ACP1 - самосшивающийся акрилат - сополимер 2-этилгексилакрилата, винилацетата и акриловой кислоты с титанхелатэфиром в качестве средства сшивки; ACP2 - несамосшивающийся акрилат - сополимер 2-этилгексилакрилата, винилацетата и акриловой кислоты; NCP - сополимеризат на основе диметиламиноэтилметакрилата и нейтрального сложного эфира метакриловой кислоты; TriG - триглицериды каприловой/каприновой кислот; K.E. - сложный эфир смоляной кислоты канифоли с глицерином. В примерах XXl V - XXXl дозировались 20мг физостигмина, смешанные с 37мг ундециловой кислоты. Варьировались процентный состав матриц и вес поверхности; данные матрицы приведены в табл.3. Фиг.5 и 6 показывают характер "ин витро" - выделения в примере XXX. Так как выделенные количества, представленные в виде зависимости от корня (квадратного) из времени, - как почти во все х примерах - дают прямую, может быть показано, что была разработана система, которая посредством управления матрицей, контролирование "отдает" биологически активное вещество, так что однозначно выполняются требования модели Хигучи. Видно, что выделение молярного отношения карбоновых кислот к базисному полимеру было определено. Можно отметить, что выделение тем выше, чем меньше было введено кислоты и чем больше базисного полимера. Выделение тем выше, чем меньше недиссоциированной кислоты присутствуе т в системе после выдержки; так как в молярных количествах ундециловой кислоты использовалось меньше, чем масляной кислоты, понятно, почему при одной и той же матрице образец с ундециловой кислотой выделяет ("освобождает") физостигмина больше, чем образец с масляной кислотой. Посредством фракционирования пластификатора может быть продемонстрировано, что пластификатор не имеет никакого влияния на процесс "ин витро" - выделения.
ДивитисяДодаткова інформація
Автори англійськоюHille Thomas, Huber Hans-Joachim
Автори російськоюХилле Томас, Хубер Ханс-Иоахим
МПК / Мітки
МПК: A61M 35/00, A61K 31/46
Мітки: система, трансдермальна, терапевтична, спосіб, одержання
Код посилання
<a href="https://ua.patents.su/7-26560-transdermalna-terapevtichna-sistema-ta-sposib-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Трансдермальна терапевтична система та спосіб її одержання</a>
Попередній патент: Спосіб одержання 3-(s)-(-)-(1-карбамоїл-1,1-дифенілметил)-1-[2-(2,3-дигідробензофуран-5-іл)етил]-піролідину або його солі
Наступний патент: Спосіб отримання трансгенної вівці
Випадковий патент: Магніторідинне ущільнення