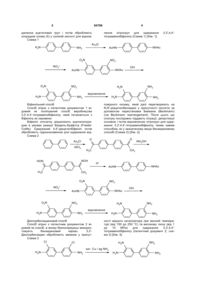
Спосіб одержання 3,3`,4,4` тетраамінобіфенілу
Формула / Реферат
1. Спосіб одержання 3,3',4,4'-тетраамінобіфенілу, при якому здійснюють:
реагування аміногруп сполуки фенілендіаміну, представленої наведеною нижче формулою (1), з неорганічною сполукою сірки,
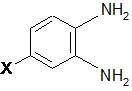 (1)
(1)
(в якій X означає атом хлору, брому або йоду),
з утворенням бензотіадіазольної сполуки, представленої наведеною нижче формулою (2)
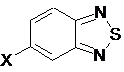 (2)
(2)
(в якій X означає атом хлору, брому або йоду);
сполучення двох молекул сполуки (2) разом з утворенням 5,5'-біс(2,1,3-бензотіадіазолу), представленого наведеною нижче формулою (3)
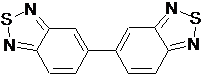 , (3)
, (3)
і депротекцію аміногруп з одержанням 3,3',4,4'-тетраамінобіфенілу, представленого наведеною нижче формулою (4)
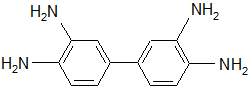 (4).
(4).
2. Спосіб одержання за п. 1, який відрізняється тим, що реакцію сполучення здійснюють у присутності металевої міді.
3. Спосіб одержання за п. 1 або 2, який відрізняється тим, що депротекцію аміногруп здійснюють у відновлювальних умовах.
4. Спосіб одержання за п. 1 або 2, який відрізняється тим, що депротекцію аміногруп здійснюють шляхом відновлення металом.
Текст
1. Спосіб одержання 3,3',4,4'тетраамінобіфенілу, при якому здійснюють: реагування аміногруп сполуки фенілендіаміну, представленої наведеною нижче формулою (1), з неорганічною сполукою сірки, NH2 2 3 94709 далення ацетилових груп і потім обробляють хлоридом олова (II) у соляній кислоті для відновСхема 1 Ac2O H2N NH2 4 лення нітрогруп для одержання тетраамінобіфенілу (Схема 1) [Хім. 1]. NO2+ O2N NO2 NHAc AcHN NO2 H2N NHAc AcHN O2N OH NH2 H2N відновлення NH2 Біфенільний спосіб Спосіб згідно з патентним документом 1 відомий як поліпшений спосіб виробництва 3,3',4,4'-тетраамінобіфенілу, який починається з біфенілу як сировини. Біфеніл спочатку діацилюють ацетилхлоридом в умовах реакції Фрідель-Крафтса (FriedelCrafts). Одержаний 4,4'-діацетилбіфеніл потім обробляють гідроксиламіном для одержання відСхема 2 O Ac2Сl AlCl3 H2N NH2 повідного оксиму, який далі перетворюють на N,N'-діацетилбензидин у присутності кислоти за допомогою перестановки Бекмана (Beckmann) (via Beckmann rearrangement). Після цього цю сполуку послідовно піддають нітрації, депротекції основою і потім відновленню нітрогруп для одержання 3,3',4,4'-тетраамінобіфенілу таким самим способом, як у зазначеному вище бензидиновому способі (Схема 2) [Хім. 2]. O H+ NHAc AcHN H3C CH3 O2N NO2+ O2N H2N NO2 NHAc AcHN NO2 H2N NH2 відновлення Дихлорбензидиновий спосіб Спосіб згідно з патентним документом 2 відомий як спосіб, в якому безпосередньо використовують бензидиновий каркас. 3,3'Дихлорбензидин обробляють аміаком у присутСхема 3 Cl Cl H2N NH2OH CH3 H3C NOH HON 3,3',4,4' NH2 H2N OH NH2 NH2 ності мідного каталізатора при високій температурі (від 150 до 250 °С) та високому тиску (від 1 до 10 МПа) для одержання 3,3',4,4'тетраамінобіфенілу (патентний документ 2, схема 3) [Хім. 3]. кат. Cu / ag NH3 H2N H2N NH2 NH2 5 94709 Спосіб сполучення Спосіб згідно з патентним документом 3 може бути згаданий як спосіб виготовлення 3,3',4,4'тетраамінобіфенілу, в якому не використовують бензидиновий каркас як вихідний матеріал. У цьому способі використовують сполучення Сузукі O2N AcHN (Suzuki) між 4-ацетиламіно-3-нітробромбензолом та 4-ацетиламіно-3-нітрофенілборатом для утворення бензидинового каркаса, з подальшою депротекцією основою та відновленням нітрогруп по черзі для одержання 3,3',4,4'-тетраамінобіфенілу [Хім. 4]. Схема 4 O2N Br + O2N AcHN NHAc H2N H2N Патентний документ 1: Патент США №5,041,666. Патентний документ 2: Патент Японії, викладена публікація №2004-161643. Патентний документ 3: Патентна заявка США №2005/0215823. Непатентний документ 1: Vogel Н., Marvel С.S., J. Polym. Sci., 50, 511 (1961). Heпатентний документ 2: Belenkaya I.A., Shulla T.A., J. Heterocyclic Chem. 11, 1555-1558 (1989). Розкриття винаходу Задачі, на розв'язання яких спрямований винахід. У той же час, згаданий вище бензидиновий спосіб має недолік, який полягає у тому, що він викликає ймовірність погіршення робочих умов і забруднення довкілля, оскільки бензидин, що є вихідним матеріалом, є канцерогеном. Згаданий вище біфенільний спосіб є неефективним, оскільки він потребує багатьох стадій та інтенсивного використання стехіометричної кількості реагентів для одержання 3,3',4,4'тетраамінобіфенілу. Наведений вище дихлорбензидиновий спосіб має недоліки, тому що він потребує особливої уваги до погіршення робочих умов і забруднення довкілля, оскільки використаний дихлорбензидин є мутагеном, і тому, що він вимагає особливого виробничого обладнання, оскільки реакція у присутності аміаку потребує високої температури та високого тиску. Крім того, вищезгаданий спосіб сполучення додатково потребує реакції Грігнарда (Grignard) та подібного для синтезу сполуки борату як вихідного матеріалу для реакції сполучення, а також дорогого каталізатора паладію для реакції зв'язування. Таким чином, існує проблема, яка полягає в тому, кат. PD B(OH)2 O2N NO2 AcHN відновлення 6 OH H2N NO2 NH2 NH2 NH2 що він потребує стадії для відновлення каталізатора, переробки відходів тощо, що ускладнює процес у цілому та збільшує вартість виробництва. Таким чином, об'єктом цього винаходу є забезпечення способу виробництва, здатного ефективно виробляти 3,3',4,4'-тетраамінобіфеніл за допомогою меншої кількості стадій. Вибирають вихідний матеріал, який відрізняється від тих, які використовують у традиційних способах виробництва, для уникнення використання високотоксичних або канцерогенних речовин, таким чином дозволяючи поліпшення робочих умов та забезпечуючи безпеку довкілля. Засоби для розв'язання проблем Автори цього винаходу настійно вивчали способи розв'язання вищезгаданих проблем і знайшли спосіб виробництва 3,3',4,4'тетраамінобіфенілу, що має у своєму складі захист аміногруп 1,2-діаміно-4-галобензолу як вихідного матеріалу, подальшу реакцію сполучення для формування зв'язку вуглець-вуглець і депротекцію аміногруп для одержання 3,3',4,4'тетраамінобіфенілу, у якому полягає цей винахід. Таким чином, цей винахід стосується таких пунктів [1]-[4]. [1] Спосіб виробництва 3,3',4,4'тетраамінобіфенілу, який має у своєму складі: реагування аміногруп сполуки фенілен діаміну, представленої наведеною нижче формулою (1), з неорганічною сполукою сірки [Хім. 5] NH2 (1) X NH2 (в якій X представляє атом хлору, брому або йоду) для утворення сполуки бензотіадіазолу, 7 94709 представленої наведеною нижче формулою (2) [Хім. 6] N S (2) N X (в якій X представляє атом хлору, брому або йоду); сполучення двох молекул сполуки (2) разом для одержання 5,5'-біс(2,1,3-бензотіадіазолу), представленого наведеною нижче формулою (3) [Хім. 7] N N S S N N (3) ; депротекцію аміногруп для одержання 3,3',4,4'тетраамінобіфенілу, представленого наведеною нижче формулою (4) [Хім. 8] NH2 H2N H2N (4). NH2 [2] Спосіб виробництва згідно з наведеним вище пунктом 1, в якому реакцію сполучення проводять у присутності металевої міді. [3] Спосіб виробництва згідно з наведеним вище пунктом 1 або 2, в якому депротекцію аміногруп проводять у відновлювальних умовах. [4] Спосіб виробництва згідно з наведеним вище пунктом 1 або 2, в якому депротекцію аміногруп проводять шляхом відновлення металом. Дія винаходу Спосіб виробництва за цим винаходом забезпечує ефективне виробництво 3,3',4,4'тетраамінобіфенілу із використанням меншої кількості стадій. Відсутність потреби у використанні високотоксичних вихідних матеріалів дозволяє поліпшити робочі умови та забезпечує безпеку довкілля. Кращий варіант здійснення винаходу Цей винахід докладно описаний нижче. Використовують 4-гало-о-фенілендіамін як вихідний матеріал у способі виробництва 3,3',4,4'тетраамінобіфенілу за цим винаходом. Прикладами 4-гало-о-фенілендіаміну є 4-хлор-офенілендіамін та 4-бром-о-фенілендіамін. Захист аміногруп у 4-гало-о-фенілендіаміні У цьому винаході аміногрупи спочатку захищають шляхом реагування 4-гало-офенілендіаміну, представленого наведеною вище формулою (1), з неорганічною сполукою сірки для одержання 5-гало-2,1,3-бензотіадіазолу, представленого наведеною вище формулою (2). У 4-галоо-фенілендіаміні, який використовують у цьому винаході, галоген є хлором, бромом або йодом. У цьому винаході реакцію сполучення 4-галоо-фенілендіаміну використовують для побудови бензидинового каркаса. Коли реакцію сполучення проводять без захисту аміногруп 4-гало-офенілендіаміну, може утворюватись дифеніламін як побічний продукт. Відповідно, ці аміногрупи захищають перед реакцією сполучення функціона 8 льною групою (функціональними групами), яку (які) не видаляють у реакції сполучення. Амідна група, карбамоїльна група, Nсульфонільна група, сульфонамідна група або подібне можуть бути використані тут як така захисна група. Перевагу надають виведенню тіадіазольного кільця з аміногруп для їхнього захисту. Наприклад, спосіб, що ґрунтується на способі згідно з вищезгаданим непатентним документом 2, є кращим для захисту аміногруп. Отже, використовують неорганічну сполуку сірки при перетворенні згаданих вище аміногруп на тіадіазольне кільце. Неорганічні сполуки сірки, які можуть бути застосовані у цьому винаході, включають неорганічні сполуки двовалентної сірки, такі як дихлорид сірки, та неорганічні сполуки чотиривалентної сірки, такі як тіонілхлорид. Серед них перевагу надають тіонілхлориду. Має бути застосований принаймні еквівалентний моль вищезгаданої сполуки, що містить сірку, відносно 1 моль 4гало-о-фенілендіаміну, але краще, коли сполуку, що містить сірку, використовують з надлишком для завершення реакції. У цій реакції може бути використаний розчинник, якщо необхідно. Розчинник може слугувати для розчинення або диспергування 4-гало-офенілендіаміну для ефективного контакту з неорганічною сполукою сірки, для запобігання швидкій та інтенсивній реакції за допомогою ефекту розведення та для адсорбування вивільненого тепла шляхом зрошення (рефлюксу). У цьому винаході можуть бути використані як розчинники вуглеводні, такі як гексан, циклогексан, метилциклогексан, гептан та октан; ароматичні вуглеводні, такі як бензол, толуол, ксилол та етилбензол; та галогеновані розчинники, такі як дихлорметан, хлороформ, дихлоретан, трихлоретан, тетрахлоретан, хлорбензол і дихлорбензол. Серед них у кращому варіанті використовують як розчинники ароматичні вуглеводні. Кількість розчинника, який використовують, у кращому варіанті становить у 2-50 разів більше за вагою, краще від 5 до 30 разів більше за вагою, ніж кількість 4-гало-о-фенілендіаміну. Однак, при використанні тіонілхлориду як неорганічної сполуки сірки, він також може слугувати як розчинник. У цьому разі кількість тіонілхлориду, який використовують, становить у 1,5-10 разів більше за вагою, ніж кількість 4-гало-офенілендіаміну. Для прискорення цієї реакції може бути використана кислота, якщо необхідно. У цьому винаході у кращому варіанті використовують нелеткі протонові кислоти. Серед них особливу перевагу надають сірчаній кислоті. Кількість кислоти, яку використовують, становить у 0,01-1,0 разів більше за вагою, краще від 0,1 до 0,3 разів більше за вагою, ніж кількість 4-гало-о-фенілендіаміну. Цей винахід виконують на повітрі або в інертній атмосфері, такій як азот. Цей винахід звичайно здійснюють шляхом змішування 4-гало-о-фенілендіаміну та неорганічної сполуки сірки з додаванням розчинника та кислоти, якщо необхідно, нагрівання та збовтування. Коли в реакції утворюється газ, такий як хлористий водень, газ, у кращому варіанті, збирають лужною 9 94709 пасткою із зовнішнього боку реакційної посудини. Таку реакцію звичайно здійснюють при температурі від 80 °С до температури зрошення (рефлюксу) реакційного розчину. У цьому винаході реакцію, у кращому варіанті, здійснюють при температурі зрошення (рефлюксу) реакційного розчину. Реакція сполучення Далі, у цій реакції дві молекули 5-гало-2,1,3бензотіадіазолу (2), одержаного у наведеній вищі захисній реакції, з'єднують разом для одержання 5,5'-біс(2,1,3-бензотіадіазолу) (3). 5,5'-Біс(2,1,3бензотіадіазол) (3) є прекурсорною сполукою для 3,3',4,4'-тетраамінобіфенілу. Хоча можуть бути використані різноманітні відомі способи для такої реакції сполучення до досягнення бажаної мети, у цьому винаході реакції Улманна (Ulmann), в якій використовують металеву мідь як агент сполучення, надають перевагу у реакції сполучення з огляду на простоту та економічність реакції. Мідь, яку використовують у цьому винаході, у кращому варіанті знаходиться у формі гранульованої міді, особливо мідної стружки, мідного пилу, мідного порошку та подібного з огляду на ефективність реакції. Мідь має бути використана принаймні в еквімолярній кількості відносно 5-гало-2,1,3бензотіадіазольної сполуки. Однак, у кращому варіанті використовують надлишкову кількість міді відносно кількості 5-гало-2,1,3-бензотіадіазольної сполуки для забезпечення завершення реакції. З іншого боку, враховуючи баланс між стимулюванням реакції сполучення та видаленням міді, що не прореагувала, наприкінці реакції, мідь у кращому варіанті використовують у незначному надлишку відносно 5-гало-2,1,3-бензотіадіазольної сполуки. На підставі цього кількість міді, яку використовують у цій реакції сполучення, становить від 1,01 до 2 моль, краще від 1,1 до 1,6 моль відносно 1 моль 5-гало-2,1,3-бензотіадіазольної сполуки. У реакції сполучення можуть бути використані амідні розчинники, такі як диметилформамід, діетилформамід, диметилацетамід і Nметилпіролідон, та нітробензольні розчинники, такі як нітробензол і нітротолуол, для реакції сполучення у цьому винаході. У цьому винаході у кращому варіанті використовують амідний розчинник, і особливу перевагу надають диметилформаміду. S N N N Кількість розчинника, яку використовують, становить від 2 до 50 разів більше за вагою, краще від 3 до 30 разів більше за вагою, ніж кількість міді, яку використовують. Цю реакцію звичайно здійснюють в інертній атмосфері, такій як азот або аргон. Наведену вище реакцію сполучення звичайно здійснюють шляхом змішування розчинника, такого як диметилформамід, з 5-гало-2,1,3бензотіадіазольною сполукою і міддю та нагрівання суміші. Температура реакції звичайно становить від 100 °С до температури зрошення (рефлюксу) реакційного розчину. Депротекція Здійснюють депротекцію одержаного таким чином 5,5'-біс(2,1,3-бензотіадіазолу) для одержання 3,3',4,4'-тетраамінобіфенілу. Для депротекції аміногруп у бензотіадіазолі можуть бути використані різноманітні способи. Депротекцію у кращому варіанті здійснюють у відновлювальних умовах для того, щоб не пошкодити сформовані аміногрупи. Водневе відновлення металевим каталізатором, відновлення металом і подібним можуть бути використані як спосіб відновлення. Перевагу надають відновленню металом. Прикладами металів є типові метали, такі як натрій, калій, магній, алюміній, і перехідні метали, такі як залізо, цинк та олово. Перевагу надають магнію і цинку. Для цієї реакції потрібне джерело постачання протонів, і для постачання протонів додають розчинник, що містить протони, такий як вода або спирт, або кислота, така як соляна кислота. Для цього потрібні дванадцять електронів для відновлення 5,5'біс(2,1,3-бензотіадіазолу), і електрони, які використовують у цій реакції, постачають з металу (наведена далі формула (А)). Наприклад, коли використовують цинк або магній, що є двовалентними металами, має бути використано принаймні 6 моль такого металу відносно 1 моль 5,5'-біс(2,1,3бензотіадіазолу). Однак, у кращому варіанті використовують надлишкову кількість такого металу відносно теоретичної кількості для забезпечення завершення реакції. Відповідно, у кращому варіанті використовують від 6 до 80 моль такого металу відносно 1 моль 5,5'-біс(2,1,3-бензотіадіазолу) [Хім. 9]. H2N S N 10 + 12e- + 12H+ H2N NH2 NH2 +2H2S (A) Метал, який використовують у цьому винаході, у кращому варіанті є у формі гранул, стружок, пилу, порошку і подібного з огляду на поліпшення ефективності реакції. У депротекції розчинник може бути використаний без обмеження. Серед придатних розчинників є протоновмісні розчинники, такі як вода, спирти та органічні кислоти. Метанол, етанол, пропанол, бутанол і подібне використовують як спирти, в той час як мурашину кислоту, оцтову кислоту, пропіонову кислоту і подібне використовують як органічні кислоти. Кількість розчинника, яку використовують, становить від 2 до 50 разів за вагою більше, краще від 5 до 30 разів за вагою більше, ніж кількість 5,5'біс(2,1,3-бензотіадіазолу). Цей винахід здійснюють на повітрі або в інертній атмосфері, такій як азот або аргон. Реакцію звичайно здійснюють шляхом розчинення 5,5'-біс(2,1,3-бензотіадіазолу) у розчиннику, такому як спирт, з додаванням кислоти, якщо необхідно, та подальшим додаванням і змішуванням металу. Температура реакції звичайно коливаєть 11 ся від 0 °С до температури зрошення реакційної рідини. Приклади Цей винахід конкретно описаний за допомогою ілюстрування наведених далі прикладів, але жодним чином не обмежується цими прикладами. Газову хроматографію (аналітичний інструмент: модель 6890N, виготовлена Agilent Technologies, Ltd., аналітична колонка: колонка DB-1, виготовлена J&W Scientific Inc.), у принципі, використовували для аналізу кожного компонента у прикладах. Високоефективну рідинну хроматографію (аналітичний інструмент: модель LC2010HT, виготовлений SHIMADZU Co., аналітична колонка: колонка RP-18 (ODS), що має кінцеву пробку, виготовлена Kanto Chemical Co. Inc.) використовували для аналізу речовин з низькою леткістю. Приклад 1 Синтез 5-хлор-2,1,3-бензотіадіазолу Готували суміш шляхом змішування 4,0 г (28 ммоль) 4-хлор-о-фенілендіаміну, 14 мл тіонілхлориду та 0,62 мл концентрованої сірчаної кислоти та зрошували впродовж однієї години. Цю суміш охолоджували і потім виливали на лід, і одержаний преципітат фільтрували та збирали. Цей преципітат промивали водою, доки відпрацьована вода не стала нейтральною, і потім ретельно висушували для одержання 4,6 г 5-хлор-2,1,3бензотіадіазолу як неочищеного продукту (точка плавлення від 50 до 54 °С; вихід 96 %). Цей неочищений продукт дистилювали у вакуумі для одержання чистого продукту 5-хлор-2,1,3бензотіадіазолу (точка плавлення 54 °С; вихід 85 %). Синтез 5,5'-біс(2,1,3-бензотіадіазолу) Реакційну суміш 2,2 г (12,9 ммоль) 5-хлор2,1,3-бензотіадіазолу і 1,3 г (20,5 ммоль) мідного порошку нагрівали у 5 мл диметилформаміду при збовтуванні при 150 °С впродовж 20 годин. Цю реакційну суміш охолоджували і потім виливали у воду (40 мл), і одержаний преципітат фільтрували та збирали. Після цього преципітат висушували, екстрагували бензолом (20 мл х 3). Після поєднання цих бензолових екстрактів поєднаний екстракт висушували у вакуумі до повної сухості. Одержаний маслянистий осад розтирали у порошок петролейним ефіром, і видаляли маточний розчин для одержання 1,45 г 5,5'-біс(2,1,3бензотіадіазолу) (точка плавлення від 61 до 62 °С; вихід 83 %). Синтез 3,3',4,4'-тетраамінобіфенілу Розчин метанолу (20 мл), який містить 1,0 г (3,7 ммоль) 5,5'-біс(2,1,3-бензотіадіазолу), нагрівали до 45 °С, до якого додавали 1,6 г (65,8 ммоль) металевого порошку магнію впродовж однієї години при збовтуванні і потім одержану суміш нагрівали при 60 °С впродовж 20 хвилин. Після видалення магнію, що не прореагував, шляхом фільтрації і відгонки метанолу до осаду додавали 94709 12 ізобутилметилефір (10 мл) і розчин насиченого водного нашатирного спирту (20 мл). Одержану суміш збовтували впродовж 10 хвилин. Органічний шар відокремлювали, висушували над безводним сульфатом натрію і потім концентрували до сухості. Цей концентрований осад розчиняли у воді (20 мл), яка містила концентровану соляну (хлористоводневу) кислоту (5 мл). Одержаний розчин охолоджували для осадження кристалів, які збирали фільтрацією і висушували для одержання 1,07 г 3,3',4,4'-тетраамінобіфенілгідрохлориду (вихід 80 %). Приклад 2 Синтез 5-бром-2,1,3-бензотіадіазолу Готували суміш шляхом змішування 4,0 г (21 ммоль) 4-бром-о-фенілендіаміну, 14 мл тіонілхлориду і 0,62 мл концентрованої сірчаної кислоти і зрошували впродовж однієї години. Цю суміш охолоджували і потім виливали на лід, і одержаний преципітат фільтрували та збирали. Цей преципітат промивали водою, доки відпрацьована вода не ставала нейтральною, і потім ретельно висушували для одержання 4,5 г 5-бром-2,1,3бензотіадіазолу як сирого продукту (точка плавлення від 48 до 50 °С; вихід 96,5 %). Цей сирий продукт дистилювали у вакуумі для одержання чистого продукту 5-бром-2,1,3-бензотіадіазолу (точка плавлення 50 °С; вихід 86 %). Синтез 5,5'-біс(2,1,3-бензотіадіазолу) Реакційну суміш, приготовану шляхом додавання 4,6 г (21,4 ммоль) 5-бром-2,1,3бензотіадіазолу і 2 г (31,5 ммоль) мідного порошку до 10 мл диметилформаміду, нагрівали при збовтуванні при 150 °С впродовж 6 годин. Цю реакційну суміш охолоджували і потім виливали у воду (40 мл), і одержаний преципітат фільтрували і збирали. Після висушування цього преципітату його екстрагували бензолом (20 мл х 3). Після поєднання цих бензолових екстрактів поєднаний екстракт висушували у вакуумі до повної сухості. Одержаний маслянистий осад розтирали у порошок петролейним ефіром, і видаляли маточний розчин для одержання 2,1 г 5,5'-біс(2,1,3-бензотіадіазолу) (точка плавлення від 61 до 62 °С; вихід 73 %). Синтез 3,3',4,4'-тетраамінобіфенілу Реакційну суміш, приготовану шляхом додавання 2,5 г (38,2 ммоль) цинку, суспендованого у 6 мл 20 % водного розчину соляної (хлористоводневої) кислоти, до 20 % водного розчину соляної (хлористоводневої) кислоти (6 мл), що містить 1,0 г (3,7 ммоль) 5,5'-біс(2,1,3-бензотіадіазолу), зрошували впродовж 1,5 години при збовтуванні. Реакційну суміш охолоджували і фільтрували. Поки фільтрат концентрували, кристали почали осаджуватись. Цей концентрований розчин охолоджували для збирання кристалів шляхом фільтрації для одержання 1,0 г 3,3',4,4'тетраамінобіфенілгідрохлориду (точка плавлення від 265 до 267 °С; вихід 75 %). 13 Комп’ютерна верстка В. Мацело 94709 Підписне 14 Тираж 24 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for the preparation of 3,3',4,4'-tetraaminobiphenyl
Автори англійськоюYasuda Hiroshi, Domitrovichi Orlov Varely
Назва патенту російськоюСпособ получения 3,3`,4,4` тетрааминобифенила
Автори російськоюЯсуда Хороши, Орлов Валерий Домитровичи
МПК / Мітки
МПК: C07C 209/28, C07C 211/55
Мітки: спосіб, 3,3`,4,4, тетраамінобіфенілу, одержання
Код посилання
<a href="https://ua.patents.su/7-94709-sposib-oderzhannya-3344-tetraaminobifenilu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 3,3`,4,4` тетраамінобіфенілу</a>