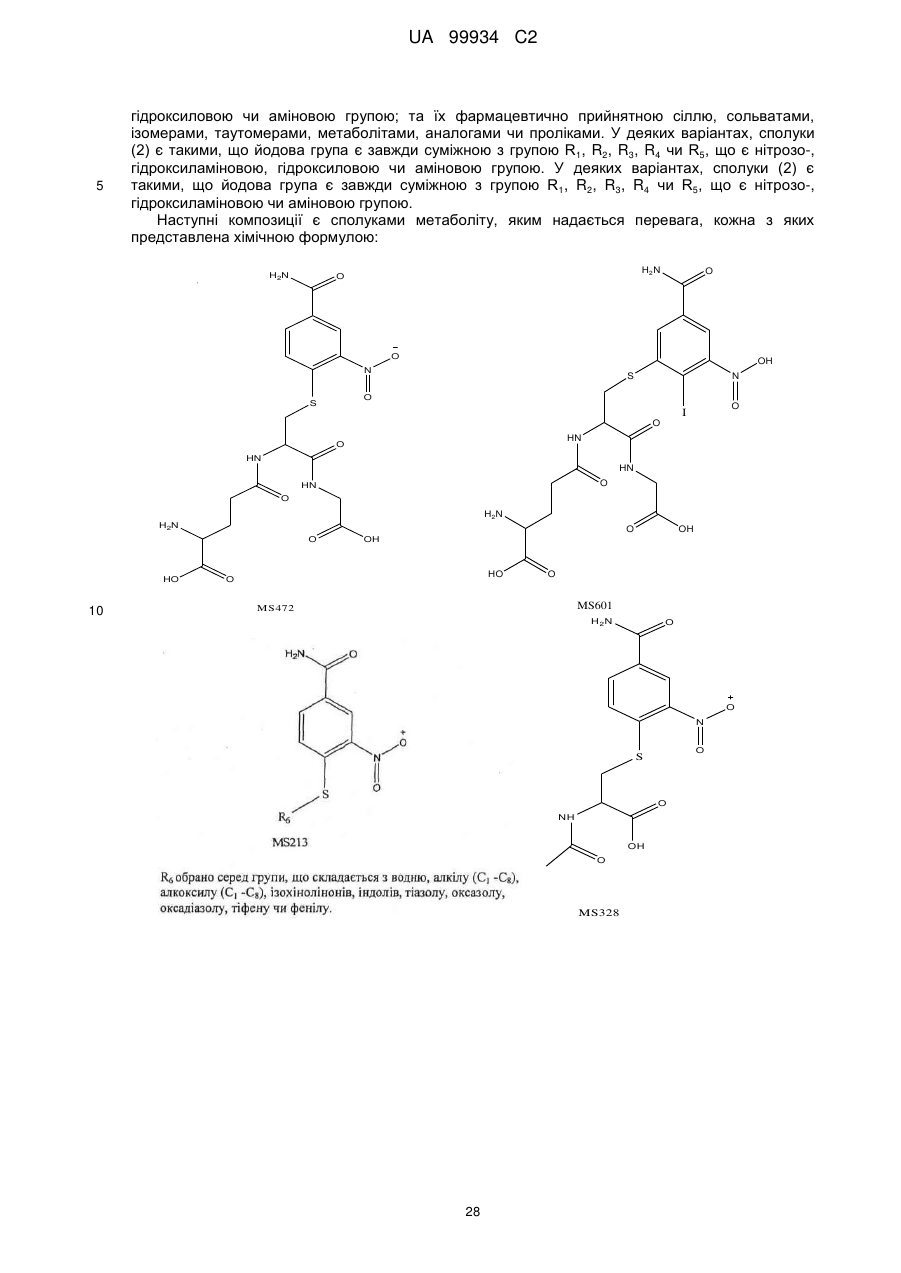
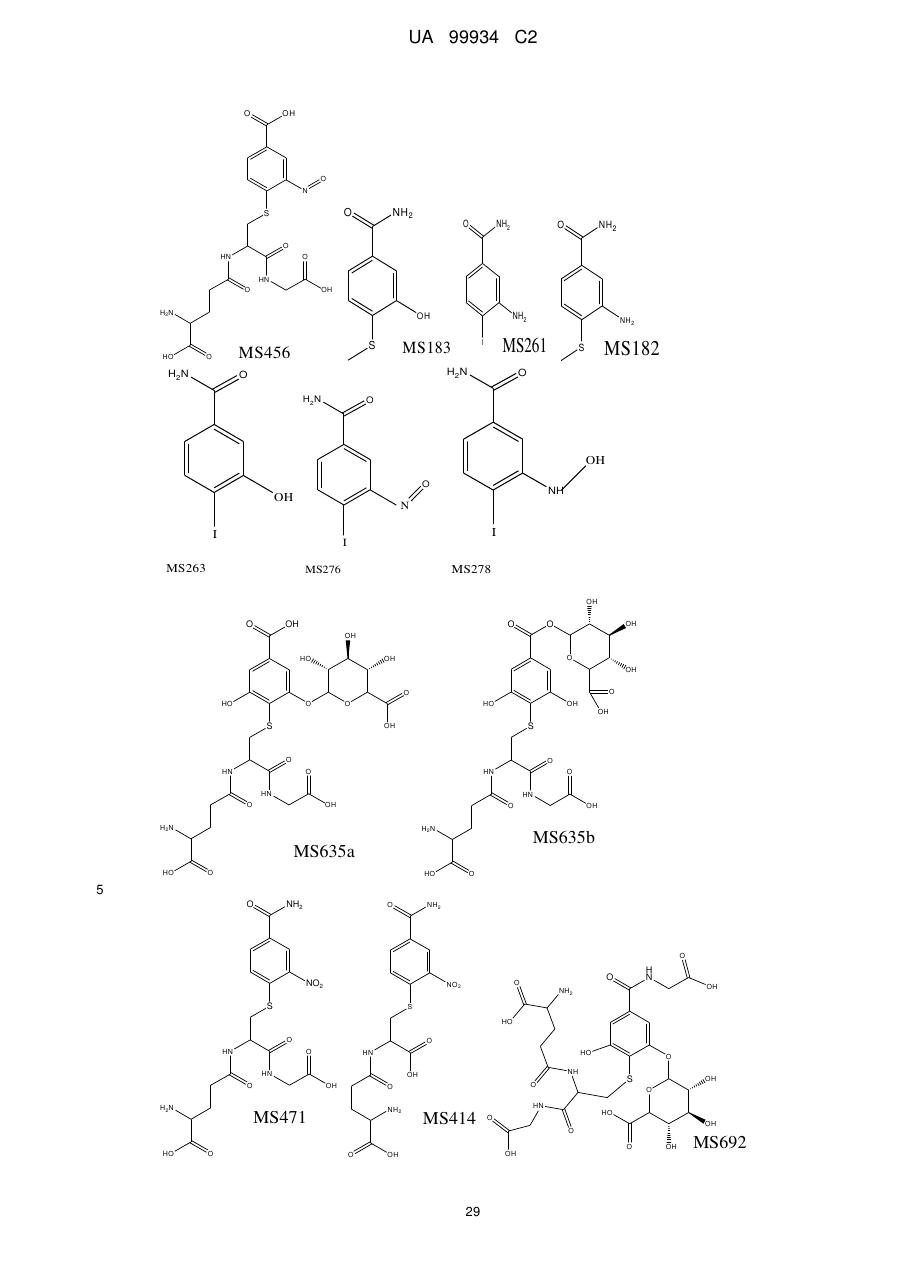
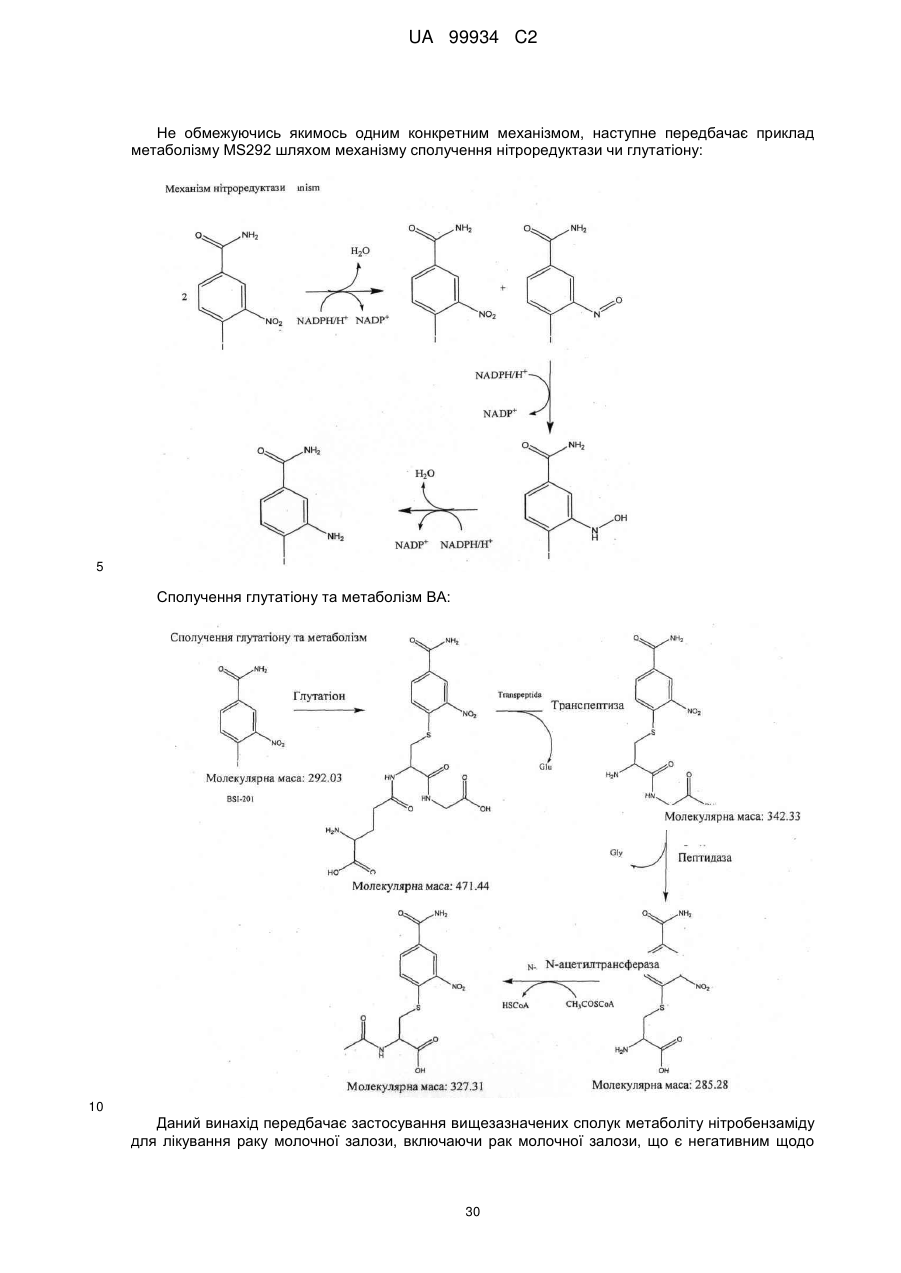
Лікування раку молочної залози за допомогою сполуки 4-йодо-3-нітробензаміду в комбінації з протипухлинними засобами
Номер патенту: 99934
Опубліковано: 25.10.2012
Автори: Оссовская Валерія С., Бредлі Чарльз, Шерман Баррі М.
Формула / Реферат
1. Спосіб лікування раку молочної залози, який є негативний щодо естрогенового рецептора ("ER"), прогестеронового рецептора ("PR") і рецептора людського епідермального фактора росту 2 ("HER2") у пацієнта, що включає призначення пацієнтові, який має рак молочної залози, який є негативним щодо ER, PR і HER2 ефективної кількості 4-йодо-3-нітробензаміду або його метаболіту або фармацевтично прийнятної солі, гемцитабіну і карбоплатину.
2. Спосіб за п. 1, де 4-йодо-3-нітробензамід або його метаболіт, або його фармацевтично прийнятна сіль, гемцитабін і карбоплатин забезпечені в окремих лікарських формах і вводяться послідовно.
3. Спосіб за п. 1, де 4-йодо-3-нітробензамід або його метаболіт, або його фармацевтично прийнятна сіль, гемцитабін і карбоплатин забезпечені в окремих лікарських формах і вводяться одночасно.
4. Спосіб за пп. 1, 2 або 3, де ефективна кількість викликає щонайменше один терапевтичний ефект, вибраний з групи, яка складається із зменшення в розмірі пухлини молочної залози, зменшення метастазування, повної ремісії, часткової ремісії, стабілізації хвороби або повної патологічної регресії.
5. Спосіб за пп. 1, 2 або 3, де досягається рівень клінічної ефективності (CBR = CR (повна ремісія) + PR (часткова ремісія) + SD (стабілізація хвороби) ≥ 6 місяців), у порівнянні з лікуванням вказаним гемцитабіном і вказаним карбоплатином, введеними без 4-йодо-3-нітробензаміду.
6. Спосіб за п. 5, де покращення рівня клінічної ефективності становить приблизно 60 % або вище.
7. Спосіб за пп. 1, 2 або 3, де рак молочної залози знаходиться на стадії І, стадії II або стадії ІІІ.
8. Спосіб за пп. 1, 2 або 3, який додатково включає хірургію, променеву терапію, хіміотерапію, генну терапію, ДНК терапію, вірусну терапію, РНК терапію, ад'ювантну терапію, неоад'ювантну терапію, імунотерапію, нанотерапію або їх поєднання.
9. Спосіб за пп. 1, 2 або 3, який додатково включає призначення пацієнтові гамма-опромінення.
10. Спосіб за пп. 1, 2 або 3, де вказаний рак молочної залози є інвазивною внутрішньопротоковою карциномою.
11. Спосіб за пп. 1, 2 або 3, де вказаний рак молочної залози є метастатичним.
12. Спосіб за пп. 1, 2 або 3, де вводиться ефективна кількість 4-йодо-3-нітробензаміду або його фармацевтично прийнятної солі.
13. Спосіб за п. 12, де пацієнт отримує цикл лікування щонайменше 11 днів, і на 1, 4, 8 і 11 дні циклу пацієнт отримує від приблизно 10 до приблизно 100 мг/кг 4-йодо-3-нітробензаміду або молярно еквівалентну кількість речовини його метаболіту.
14. Застосування 4-йодо-3-нітробензаміду або його метаболіту, або його фармацевтично прийнятної солі, гемцитабіну і карбоплатину для виробництва лікарських препаратів для лікування раку молочної залози, який є негативним щодо естрогенового рецептора ("ER"), прогестеронового рецептора ("PR") і рецептора людського епідермального фактора росту 2 ("HER2").
15. Застосування за п. 14, де 4-йодо-3-нітробензамід або його метаболіт, або його фармацевтично прийнятна сіль, гемцитабін і карбоплатин забезпечені в окремих лікарських формах і вводяться послідовно.
16. Застосування за п. 14, де 4-йодо-3-нітробензамід або його метаболіт, або його фармацевтично прийнятна сіль, гемцитабін і карбоплатин забезпечені в окремих лікарських формах і вводяться одночасно.
17. Застосування за пп. 14, 15 або 16, де ефективна кількість викликає щонайменше один терапевтичний ефект, вибраний з групи, яка складається із зменшення в розмірі пухлини молочної залози, зменшення метастазування, повної ремісії, часткової ремісії, стабілізації хвороби або повної патологічної регресії.
18. Застосування за п. 14, 15 або 16, де рак молочної залози знаходиться на стадії І, стадії II або стадії III.
19. Застосування за п. 14, 15 або 16, де вказаний рак молочної залози є інвазивною внутрішньопротоковою карциномою.
20. Застосування за п. 14, 15 або 16, де вказаний рак молочної залози є метастатичним.
21. Застосування за п. 14, 15 або 16, де вводиться ефективна кількість 4-йодо-3-нітробензаміду або його фармацевтично прийнятної солі.
22. Комбінація 4-йодо-3-нітробензаміду або його фармацевгично прийнятної солі, гемцитабіну і карбоплатину.
23. Комбінація за п. 22, де 4-йодо-3-нітробензамід або його фармацевтично прийнятна сіль, гемцитабін і карбоплатин присутні в одному складі.
24. Комбінація за п. 22, де 4-йодо-3-нітробензамід або його фармацевтично прийнятна сіль, гемцитабін і карбоплатин присутні в різних складах.
25. Композиція, яка включає 4-йодо-3-нітробензамід або його метаболіт, або його фармацевтично прийнятну сіль, гемцитабін і карбоплатин разом з фармацевтично прийнятним носієм.
26. Набір, що включає комбінацію флаконів, де перший флакон включає 4-йодо-3-нітробензамід або його фармацевтично прийнятну сіль, другий флакон включає гемцитабін і карбоплатин, для лікування раку молочної залози, який є негативний щодо естрогенового рецептора ("ER"), прогестеронового рецептора ("PR"), і рецептора людського епідермального фактора росту 2 ("HER2").
27. Набір, що включає комбінацію флаконів, де перший флакон включає 4-йодо-3-нітробензамід або його фармацевтично прийнятну сіль, другий флакон включає гемцитабін і третій флакон включає карбоплатин, для лікування раку молочної залози, який є негативний щодо естрогенового рецептора ("ER"), прогестеронового рецептора ("PR"), і рецептора людського епідермального фактора росту 2 ("HER2").
28. Використання ефективної кількості 4-йодо-3-нітробензаміду або його метаболіту, або фармацевтично прийнятної солі, гемцитабіну і карбонлатину для лікування раку молочної залози, який є негативний щодо естрогенового рецептора ("ER"), прогестеронового рецептора ("PR"), і рецептора людського епідермального фактора росту 2 ("HER2") у пацієнта.
Текст
Реферат: Винахід належить до галузі медицини та стосується лікування раку молочної залози, який є негативним щодо естрогенового рецептора ("ER"), прогестеронового рецептора ("PR") і рецептора людського епідермального фактора росту 2 ("HER2"), із застосуванням ефективної кількості 4-йодо-3-нітробензаміду або його метаболіту, або фармацевтично прийнятної солі, гемцитабіну і карбоплатину. UA 99934 C2 (12) UA 99934 C2 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 Перехресне посилання Ця патентна заявка претендує на пріоритет за попередньою заявкою США з реєстраційним № 60/987,333, що має назву “Лікування потрійного негативного метастатичного раку молочної залози у поєднанні з антиметаболітом, комплексом платини та інгібітором PARP”, зареєстрованої 12 листопада 2007 року (№ у реєстрі патентних повірених 28825-742.101); попередньою заявкою США з реєстраційним № 61/012,364, що має назву “Лікування раку у поєднанні інгібіторами топоізомерази та інгібіторами PARP”, зареєстрованої 7 грудня 2007 року (№ у реєстрі патентних повірених 28825-747.101); та попередньою заявкою США з реєстраційним № 61/058,528, під назвою “Лікування раку молочної залози, яєчника та матки інгібітором PARP”, зареєстрованої 3 червня 2008 року (№ у реєстрі патентних повірених 28825757.101), при цьому кожна з цих заявок включена до даної заявки у повному обсязі шляхом посилання. Передумови Рак належить до групи захворювань, які відзначаються порушенням контролю за ростом клітин. Тільки у Сполучених Штатах щорічна захворюваність на рак оцінюється у понад 1.3 мільйони випадків. Попри застосування хірургії, опромінення, хіміотерапії та гормонів з метою лікування раку, він залишається другою головною причиною смерті у США. Згідно оцінок понад 560.000 американців щороку помирають від раку. Раку клітини одночасно активують декілька метаболічних шляхів, що позитивно та негативно регулюють ріст клітин та некроз клітин. Ця характерна особливість наводить на думку, що модуляція некрозу клітин та ознаки виживання можуть забезпечити нові стратегії підвищення ефективності існуючих видів хіміотерапевтичного лікування. Рак молочної залози зазвичай лікується шляхом поєднання хірургії з метою видалення ракового утворення та ад'ювантної терапії - опромінення, хіміотерапії чи обох цих засобів - з метою впливу на будь-які раку клітини, що могли залишитися після хірургічного втручання. Рак молочної залози може широко класифікуватися за наявністю чи відсутністю рецепторів гормону (HR). Рак з позитивним рецептором гормону (HR+) відзначається експресією одного чи обох жіночих рецепторів гормону - естрогеновий рецептор (ER) чи прогестероновий рецептор (PR). Ад'ювантна терапія для ER+ раку молочної залози часто включає хіміотерапію із селективним модулятором естрогенових рецепторів (SERM), таких як тамоксифен чи ралоксифен. Нажаль, оскільки близько 70 % раку молочної залози є ER-позитивним, решта 30 % раку молочної залози, що є HR-негативним, не піддається лікуванню модуляторами SERM. Відповідно, інші види ад'ювантної хіміотерапії, такі як лікування антрацикліном (окремо чи в поєднанні з таксаном), були випробувані на ER-негативному раку молочної залози. Лікування антрацикліном обмежується максимально допустимою дозою протягом життя, що пов’язана з питаннями кардіотоксичності. Лікування гемцитабіном та карбоплатином є визначеною комбінацією хіміотерапії для пацієнтів, що мають метастатичний рак молочної залози - чи без застосування таксану чи з попереднім застосуванням таксану. Агенти платини продемонстрували багатообіцяючу протипухлинну активність щодо базально-подібного місцево-прогресуючого раку молочної залози. Агенти, що руйнують ДНК, мають багатообіцяючу протипухлинну ефективність проти базально-подібного раку молочної залози, внаслідок дефектів у шляхах репарації ДНК, що є притаманними цьому виду раку молочної залози. Незважаючи на існування антиметаболітів, таких як гемцитабін та агенти комплексу платини, такі як карбоплатин, не існує загальноприйнятого стандарту лікування ER-негативного раку молочної залози. Зокрема, тричі негативний метастатичний рак молочної залози (тобто рак молочної залози, що є ER-негативним, та/чи PR-негативним, та/чи негативним щодо рецептору 2 (HER2) людського епідермального фактору росту) є стійким до стандартного лікування та повністю стійким до хіміотерапії SERM. Таким чином, існує потреба в ефективному лікуванні раку загалом, та зокрема у лікуванні тричі негативного метастатичного раку молочної залози. Попри існування обмеженої кількості варіантів терапевтичного лікування раку, види раку, включаючи тричі негативний рак молочної залози, є особливо складними, оскільки вони можуть бути стійкими до стандартного хіміотерапевтичного чи гормонального лікування. Таким чином, існує потреба в ефективному лікуванні раку загалом, та окремих видів раку. Загальний опис винаходу У деяких варіантах, даний винахід передбачає спосіб лікування раку молочної залози, що є негативним щодо принаймні одного з ER, PR чи HER2 у пацієнта, який передбачає призначення пацієнтові принаймні одного інгібітору PARP. У деяких варіантах, даний винахід передбачає спосіб лікування раку молочної залози, що є негативним щодо принаймні одного з ER, PR чи HER2 у пацієнта, який його потребує, що включає: (a) отримання зразка від пацієнта; (b) дослідження зразка з метою визначення наступного: чи рак є ER-позитивним чи ER-негативним; 1 UA 99934 C2 5 10 15 чи рак є PR-позитивним чи PR-негативним; чи рак є HER2-позитивним чи HER2-негативним; (c) якщо дослідження вказує на те, що рак є негативним щодо принаймні одного з ER, PR чи HER2, лікування пацієнта принаймні одним інгібітором PARP. У деяких варіантах, спосіб також включає лікування пацієнта принаймні одним інгібітором PARP, якщо мають місце дві чи більше наступних умов: (a) рак є ER-негативним, (b) рак є PR-негативним, (c) рак є HER2-негативним. У деяких варіантах, даний винахід передбачає спосіб лікування раку молочної залози, що є негативним щодо принаймні одного з ER, PR чи HER2 у пацієнта, який включає: (a) дослідження зразка від пацієнта на предмет експресії PARP; та (b) якщо експресія PARP перевищує встановлений рівень, призначення пацієнтові принаймні одного інгібітору PARP. Практикуючи будь-який зі способів, що розкриваються у цій заявці, досягається принаймні один терапевтичний ефект, при цьому зазначений принаймні один терапевтичний ефект виражається у зменшенні розміру пухлини молочної залози, скороченню метастазу, повній ремісії, частковій ремісії, стабільності хвороби чи повній патоморфологічній регресії. У деяких варіантах, отримано порівняльний показник клінічної ефективності (CBR = CR + PR + SD ≥ 6 місяців) при лікуванні інгібітором PARP порівняно з лікуванням протипухлинним агентом. У деяких варіантах, покращення показника клінічної ефективності становить принаймні близько 30% порівняно із лікуванням лише самим протипухлинним агентом. У деяких варіантах, інгібітор PARP є інгібітором PARP-1. У деяких варіантах, інгібітор PARP-1 є 4-йодо-3-нітробензамідом чи його метаболітом. У деяких варіантах, інгібітор PARP має Формулу (IIa) чи є її метаболітом: 20 O C R5 NH2 R1 (IIa) R4 R2 R3 25 30 35 40 45 50 , Формула (IIa) де або: (1) принаймні однин із замісників R1, R2, R3, R4 та R5 є завжди замісником, що містить сірку, та решта замісників R1, R2, R3, R4 та R5 незалежно обрані серед групи, що складається з водню, гідроксилу, аміно-, нітро-, йодо-, бромо-, фтор-, хлор-, (C1-C6) алкілу, (C1-C6) алкоксилу, (C3-C7) циклоалкілу та фенілу, де принаймні два з п'яти замісників R 1, R2, R3, R4 та R5 є завжди воднем; чи (2) принаймні один з замісників R1, R2, R3, R4 та R5 не є замісником, що містить сірку та принаймні один з п'яти замісників R1, R2, R3, R4 та R5 є завжди йодо-, та де зазначений йодоє завжди суміжним з групою R1, R2, R3, R4 чи R5, яка є або нітро-, нітрозо, гідроксиламіновою, гідроксиловою чи аміновою групою; та їх фармацевтично прийнятних солей, сольватів, ізомерів, таутомерів, метаболітів, аналогів чи проліків. У деяких варіантах, сполуки (2) є такими, що йодова група є завжди суміжною з групою R1, R2, R3, R4 чи R5, яка є нітрозо-, гідроксиламіновою, гідроксиловою чи аміновою групою. У деяких варіантах, сполуки (2) є такими, що йодова група є завжди суміжною з групою R1, R2, R3, R4 чи R5, яка є нітрозо-, гідроксиламіновою чи аміновою групою. У деяких варіантах, рак молочної залози є метастатичним раком молочної залози. У деяких варіантах, рак молочної залози знаходиться на стадії I, стадії II чи стадії III. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2; та де рак молочної залози є позитивним щодо принаймні одного з ER, PR чи HER2. У деяких варіантах, рак молочної залози має дефіцит на репарацію ДНК шляхом гомологічної рекомбінації. У деяких варіантах, рак молочної залози має порушення функції BRCA1 чи BRCA2. У деяких варіантах, лікування передбачає лікувальний цикл принаймні 11 днів, де на 1, 4, 8 та 11 день циклу, пацієнт отримує від близько 1 до близько 100 мг/кг 4-йодо-3нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, 4-йодо-3нітробензамід приймається перорально, шляхом парентеральної ін'єкції чи вливання (інфузії), чи інгаляції. У деяких варіантах, цикл лікування має тривалість від близько 11 до близько 30 днів. У деяких варіантах, спосіб також включає призначення пацієнтові інгібітору PARP у поєднанні з принаймні одним протипухлинним агентом. Протипухлинний агент є протипухлинним алкілувальним агентом, протипухлинним антиметаболітом, протипухлинними 2 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 антибіотиками, протипухлинним агентом рослинного походження, протипухлинним комплексом платини, протипухлинною похідною камптотецину, протипухлинним інгібітором тирозин кінази, моноклональним антитілом, інтерфероном, модифікатором біологічного відгуку, гормональним протипухлинним агентом, протипухлинним вірусним агентом, інгібітором ангіогенезу, диференціюючим агентом, інгібітором PI3K/mTOR/AKT, інгібітором клітинного циклу, інгібітором апоптозу, інгібітором hsp 90, інгібітором тубуліну, інгібітором репарації ДНК, протиангіогенним агентом, інгібітором тирозин кінази рецептору, інгібітором топоізомерази, таксаном, агентом, націленим на Her-2, антагоністом гормону, агентом, націленим на рецептор фактору росту, чи їх фармацевтично прийнятною сіллю. У деяких варіантах, протипухлинний агент є цитабіном, capeцитабіном, валопіцитабіном чи гемцитабіном. У деяких варіантах, протипухлинний агент обирається серед групи, що складається з Авастину, Сутенту, Нексавару, Рецентину, ABT-869, Акситинібу, Іринотекану, Топотекану, паклітакселу, доцетакселу, лапатинібу, Герцептину, лапатинібу, тамоксифену, інгібітору стероїдної ароматази, інгібітору нестероїдної ароматази, Фулвестранту, інгібітору рецептора епідермального фактору росту (EGFR), Цетуксімабу, Панітумімабу, інгібітору інсуліноподібного рецептору фактору росту 1 (IGF1R), та CP-751871. У деяких варіантах, спосіб також включає призначення пацієнтові інгібітору PARP у поєднанні з більш ніж одним протипухлинним агентом. У деяких варіантах, протипухлинний агент призначається до, як супутній чи після призначення інгібітору PARP. У деяких варіантах, спосіб також включає хірургію, променеву терапію, хіміотерапію, генну терапію, терапію ДНК, вірусну терапію, терапію РНК, терапію ДНК, ад'ювантну терапію , неоад'ювантну терапію, імунотерапію, нанотерапію чи їх поєднання. У деяких варіантах, спосіб також включає призначення пацієнтові інгібітору PARP у поєднанні з гамма опроміненням. У деяких варіантах, зразком є тканина чи зразок рідини організму. У деяких варіантах, зразком є зразок пухлини, зразок крові, зразок плазми крові, зразок рідини черевної порожнини, ексудат чи випіт. У деяких варіантах, спосіб також включає дослідження зразка пацієнта на предмет експресії естрогенового рецептору, прогестеронового рецептору чи рецептору людського епідермального фактору росту 2. У деяких варіантах, даний винахід передбачає спосіб лікування раку молочної залози у пацієнта, що включає призначення пацієнтові принаймні одного інгібітору PARP у поєднанні з принаймні одним протипухлинним агентом. У деяких варіантах, даний винахід передбачає спосіб лікування раку молочної залози у пацієнта, який цього потребує, що включає: (a) отримання зразка від пацієнта; (b) дослідження зразка з метою визначення наступного: чи рак є ER-позитивним чи ER-негативним; чи рак є PR-позитивним чи PR-негативним; чи рак є HER2позитивним чи HER2–негативним; (c) якщо дослідження вказує на те, що рак є негативним щодо принаймні одного з ER, PR чи HER2, лікування пацієнту у поєднанні з терапевтичними агентами, де терапевтичні агенти включають принаймні один інгібітор PARP та принаймні один протипухлинний агент. У деяких варіантах, спосіб також включає лікування пацієнта у поєднанні з терапевтичними агентами, де терапевтичні агенти включають принаймні один інгібітор PARP та принаймні один протипухлинний агент, за наявності двох чи більше наступних умов наступних умов: (a) рак є ER-негативним, (b) рак є PR-негативним, (c) рак є HER2-негативним. У деяких варіантах, даний винахід передбачає спосіб лікування раку молочної залози у пацієнта, що включає: (a) дослідження зразка від пацієнта на предмет експресії PARP; та (b) якщо експресія PARP перевищує визначений рівень, призначення пацієнтові принаймні одного інгібітору PARP та принаймні одного протипухлинного агента. Практикуючи будь-який зі способів, що розкриваються у цій заявці, у деяких варіантах, досягається принаймні один терапевтичний ефект, при цьому зазначений принаймні один терапевтичний ефект проявляється у зменшенні розміру пухлини молочної залози, скороченні метастазу, повній ремісії, частковій ремісії, стабільності хвороби чи повній патоморфологічній регресії. У деяких варіантах, досягнуто покращення показника клінічної ефективності (CBR = CR + PR + SD ≥ 6 місяців) порівняно з лікуванням протипухлинним агентом, але без інгібітору PARP. У деяких варіантах, покращення показника клінічної ефективності становить принаймні близько 60 %. У деяких варіантах, інгібітор PARP є 4-йодо-3-нітробензамідом чи його метаболітом. У деяких варіантах, інгібітор PARP має Формулу (IIa) чи є її метаболітом: 3 UA 99934 C2 O C R5 NH2 R1 (IIa) R4 R2 R3 5 10 15 20 25 30 35 40 45 50 , Формула (IIa) де або: (1) принаймні один з замісників R1, R2, R3, R4 та R5 є завжди замісником, що містить сірку, та решта замісників R1, R2, R3, R4 та R5 незалежно обрані серед групи, що складається з водню, гідроксилу, аміно-, нітро-, йодо-, бромо-, фтор-, хлор-, (C1-C6) алкілу, (C1-C6) алкоксилу, (C3-C7) циклоалкілу та фенілу, де принаймні два з п'яти замісників R 1, R2, R3, R4 та R5 є завжди воднем; чи (2) принаймні один з замісників R1, R2, R3, R4 та R5 не є замісником, що містить сірку та принаймні один з п'яти замісників R1, R2, R3, R4 та R5 є завжди йодо-, та де зазначений йодоє завжди суміжним з групою R1, R2, R3, R4 чи R5, яка є або нітро-, нітрозо-, гідроксиламіновою, гідроксиловою чи аміновою групою; та їх фармацевтично прийнятних солей, сольватів, ізомерів, таутомерів, метаболітів, аналогів чи проліків. У деяких варіантах, сполуки (2) є такими, що йодова група є завжди суміжною з групою R1, R2, R3, R4 чи R5, яка є нітрозо-, гідроксиламіновою, гідроксиловою чи аміновою групою. У деяких варіантах, сполуки (2) є такими, що йодова група є завжди суміжною з групою R1, R2, R3, R4 чи R5, яка є нітрозо-, гідроксиламіновою чи аміновою групою. У деяких варіантах, протипухлинний агент є протипухлинним алкілувальним агентом, протипухлинним антиметаболітом, протипухлинним антибіотиком, протипухлинним агентом рослинного походження, протипухлинним комплексом платини, протипухлинною похідною камптотецину, протипухлинним інгібітором тирозин кінази, моноклональним антитілом, інтерфероном, модифікатором біологічного відгуку, гормональним протипухлинним агентом, протипухлинним вірусним агентом, інгібітором ангіогенезу, диференціюючим агентом, інгібітором PI3K/mTOR/AKT, інгібітор клітинного циклу, інгібітор апоптозу, інгібітором hsp 90, інгібітором тубуліну, інгібітором репарації ДНК, протиангіогенним агентом, інгібітором тирозин кінази рецептору, інгібітором топоізомерази, таксаном, агентом, націленим на Her-2, антагоністом гормону, агентом, націленим на рецептор фактору росту, чи їх фармацевтично прийнятною сіллю. У деяких варіантах, протипухлинний агент є цитабіном, capeцитабіном, валопіцитабіном чи гемцитабіном. У деяких варіантах, протипухлинний агент обирається серед групи, що складається з Авастину, Сутенту, Нексавару, Рецентину, ABT-869, Акситинібу, Іринотекану, Топотекану, паклітакселу, доцетакселу, лапатинібу, Герцептину, лапатинібу, тамоксифену, інгібітору стероїдної ароматази, інгібітору нестероїдної ароматази, Фулвестранту, інгібітору рецептора епідермального фактору росту (EGFR), Цетуксімабу, Панітумімабу, інгібітору інсуліноподібного рецептору фактору росту 1 (IGF1R) та CP-751871. У деяких варіантах, спосіб також включає хірургію, променеву терапію, хіміотерапію, генну терапію, терапію ДНК, вірусну терапію, терапію ДНК, ад'ювантну терапію , неоад'ювантну терапію, терапію РНК, імунотерапію, нанотерапію чи їх поєднання. У деяких варіантах, спосіб також включає призначення пацієнтові інгібітору PARP у поєднанні з гамма опроміненням. У деяких варіантах, рак молочної залози є метастатичним раком молочної залози. У деяких варіантах, рак молочної залози знаходиться на стадії I, стадії II чи стадії III. У деяких варіантах, рак молочної залози є HR-негативним раком молочної залози. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2; та де рак молочної залози є позитивним щодо принаймні одного з ER, PR чи HER2. У деяких варіантах, рак молочної залози має дефіцит на репарацію ДНК шляхом гомологічної рекомбінації. У деяких варіантах, рак молочної залози має порушення функції BRCA1 чи BRCA2. У деяких варіантах, лікування передбачає лікувальний цикл принаймні 11 днів, де: (a) на 1 та 8 дні циклу пацієнт 2 отримує близько 100-5000 мг/м гемцитабіну; (b) на 1 та 8 дні циклу, пацієнт отримує від близько 2 10 до близько 400 мг/м карбоплатину; та (c) на 1, 4, 8 та 11 дні циклу пацієнт отримує від близько 1 до близько 100 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, цикл лікування має тривалість від близько 11 до близько 30 2 днів. У деяких варіантах, на 1 та 8 дні циклу пацієнт отримує близько 100-2500 мг/м 4 UA 99934 C2 2 5 10 15 20 25 30 35 40 45 50 55 60 гемцитабіну та від близько 10 до близько 400 мг/м карбоплатину; та на 1, 4, 8 та 11 дні циклу пацієнт отримує від близько 1 до близько 50 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, на 1 та 8 дні циклу пацієнт отримує близько 2 2 500-2000 мг/м гемцитабіну та від близько 50 до близько 400 мг/м карбоплатину; та на 1, 4, 8 та 11 дні циклу пацієнт отримує від близько 1 до близько 50 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, на 1 та 8 дні циклу пацієнт отримує 2 близько 1000 мг/м гемцитабіну та близько AUC 2 карбоплатину; та на 1, 4, 8 та 11 дні циклу пацієнт отримує близько 1, 2, 3, 4, 6, 8 чи 10, 12, 14, 16, 18 чи 20 мг/кг 4-йодо-3-нітробензаміду. У деяких варіантах, протипухлинний агент вводиться шляхом парентеральної ін'єкції чи вливання. У деяких варіантах, інгібітор PARP є 4-йодо-3-нітробензамідом, який призначається перорально, чи шляхом парентеральної ін'єкції чи вливання, чи інгаляції. У деяких варіантах, спосіб також включає призначення пацієнтові таксану шляхом парентеральної ін'єкції чи вливання. У деяких варіантах, зразком є тканина чи зразок рідини організму. У деяких варіантах, зразком є зразок пухлини, зразок крові, зразок плазми крові, зразок рідини черевної порожнини, ексудат чи випіт. У деяких варіантах, спосіб також включає дослідження зразка пацієнта на предмет експресії естрогенового рецептора, прогестеронового рецептора чи рецептора людського епідермального фактору росту 2. Включення шляхом посилання Усі публікації та патентні заявки, що згадуються у цій специфікації включені до неї шляхом посилання у такому ж об’ємі, як і кожна окрема публікація чи патентна заявка, що була конкретно та окремо зазначена, як така, що є включеною шляхом посилання. Стислий опис фігур Ознаки новизни винаходу визначені докладно у формулі винаходу, що додається. Краще розуміння ознак та переваг даного винаходу буде досягнуто шляхом посилання на наступний детальний опис, який містить ілюстративні варіанти, у яких використовуються принципи винаходу, та його супроводжувальні фігури: ФІГУРА 1 зображує підвищення функціональної активності генної експресії PARP1 у людського первинного раку. Горизонтальна лінія, медіанна експресія PARP1; блочна діаграма, інтерквартильна широта; стовпчики, стандартне відхилення. ФІГУРА 2 зображує ефект 4-йодо-3-нітробензаміду плюс карбоплатин чи гемцитабіну на розвитку іn vitro клітинного циклу TNBC. Життєздатність клітин MDA-MB-463 TNBC визначена кількісно за допомогою аналізу FACS. ФІГУРА 3 зображує пригнічення PARP у периферійних мононуклеарних клітинах крові (PMBCs) пацієнтів, які отримують 4-йодо-3-нітробензамід. ФІГУРА 4 зображує аналіз спектру експресії PARP1, ER, PR та HER2 у зразках людської пухлини молочної залози на прикладі дослідження Стадії 2 метастатичного TNBC (тричі негативного раку молочної залози). Дані нормалізовані відповідно до генної експресії бетаглюкоронідази. Дані представляють аналіз 50 клінічних зразків раку молочної залози та 19 зразків нормальної молочної залози. Вертикальна ліня представляє медіанну генну експресію, а блочна діаграма представляє інтерквартильну широту. ФІГУРА 5 зображує криву Каплана-Мейера PFS (виживання без прогресування захворювання) у пацієнтів з метастатичним TNBC, які отримують 4-йодо-3-нітробензамід плюс гемцитабін/карбоплатин порівняно з самим гемцитабін/карбоплатин. Розподіл PFS за двома напрямками лікування було підсумовано з а допомогою методу Каплана-Мейера. Два напрями порівнюються за допомогою 2-стороннього логарифмічного рангового критерію при 5 % рівні достовірності. G/C, гемцитабін/карбоплатин; G/C+BA, гемцитабін/карбоплатин + 4-йодо-3нітробензамід (BA). ФІГУРА 6 зображує, що 4-йодо-3-нітробензамід (BA) потенціює зупинку клітинного циклу Sта G2/M та посилює протипроліферативний ефект гамма опромінення у людських клітинах MDA-MB-468, уражених тричі негативним раком молочної залози. Детальний опис винаходу У деяких варіантах, даний винахід передбачає спосіб лікування раку молочної залози, що є негативним щодо принаймні одного з ER, PR чи HER2 у пацієнта, який включає призначення пацієнтові принаймні одного інгібітору PARP. У деяких варіантах, досягається принаймні один терапевтичний ефект, при цьому зазначений принаймні один терапевтичний ефект проявляється у зменшенні розміру пухлини молочної залози, скороченні метастазу, повній ремісії, частковій ремісії, повній патоморфологічній регресії чи стабілізації хвороби. У деяких варіантах, отримано порівняльний показник клінічної ефективності (CBR = CR + PR + SD ≥ 6 місяців) шляхом лікування інгібітором PARP порівняно з лікуванням протипухлинним агентом. У деяких варіантах, покращення показника клінічної ефективності становить принаймні близько 30 5 UA 99934 C2 %. У деяких варіантах, інгібітор PARP є інгібітором PARP-1. У деяких варіантах, інгібітор PARP має Формулу (IIa) чи є її метаболітом: O C R5 NH2 R1 (IIa) R4 R2 R3 , Формула (IIa) 5 10 15 20 25 30 35 40 45 50 де або: (1) принаймні один із замісників R1, R2, R3, R4 та R5 є завжди замісником, що містить сірку, та решта замісників R1, R2, R3, R4 та R5 незалежно обрані серед групи, що складається з водню, гідроксилу, аміно-, нітро-, йодо-, бромо-, фтор-, хлор-, (C1-C6) алкілу, (C1-C6) алкоксилу, (C3-C7) циклоалкілу та фенілу, де принаймні два з п'яти замісників R 1, R2, R3, R4 та R5 є завжди воднем; чи (2) принаймні один з замісників R1, R2, R3, R4 та R5 не є замісником, що містить сірку та принаймні один з п'яти замісників R1, R2, R3, R4 та R5 є завжди йодо-, та де зазначений йодоє завжди суміжним з групою R1, R2, R3, R4 чи R5, яка є або нітро-, нітрозо-, гідроксиламіновою, гідроксиловою чи аміновою групою; та їх фармацевтично прийнятних солей, сольватів, ізомерів, таутомерів, метаболітів, аналогів чи проліків. У деяких варіантах, сполуки (2) є такими, що йодова група є завжди суміжною з групою R1, R2, R3, R4 чи R5, яка є нітрозо-, гідроксиламіновою, гідроксиловою чи аміновою групою. У деяких варіантах, інгібітор PARP 1 є 4-йодо-3нітробензамідом чи його метаболітом. У деяких варіантах, рак молочної залози є метастатичним раком молочної залози. У деяких варіантах, рак молочної залози знаходиться на стадії I, II чи стадії III. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2; та рак молочної залози є позитивним щодо принаймні одного з ER, PR чи HER2. У деяких варіантах, рак молочної залози є ER-негативним раком молочної залози. У деяких варіантах, рак молочної залози є ER-негативним та HER2-позитивним. У деяких варіантах, рак молочної залози є ERнегативним та PR-позитивним. У деяких варіантах, рак молочної залози є ER-негативним, а також як HER2-позитивним, так і PR-позитивним. У деяких варіантах, рак молочної залози є PRнегативним раком молочної залози. У деяких варіантах, рак молочної залози є PR-негативним та ER-позитивним. У деяких варіантах, рак молочної залози є PR-негативним та HER2позитивним. У деяких варіантах, рак молочної залози є PR-негативним, а також як ERпозитивним, так і HER2-позитивним. У деяких варіантах, рак молочної залози є HER2негативним раком молочної залози. У деяких варіантах, рак молочної залози є HER2негативним та ER-позитивним. У деяких варіантах, рак молочної залози є HER2-негативним та PR-позитивним. У деяких варіантах, рак молочної залози є HER2-негативним, а також як ERпозитивним, так і PR-позитивним. У деяких варіантах, рак молочної залози є ER-негативним та PR-негативним. У деяких варіантах, рак молочної залози є ER-негативним, PR-негативним та HER-2 позитивним. У деяких варіантах, рак молочної залози є ER-негативним та HER2негативним. У деяких варіантах, рак молочної залози є ER-негативним, HER2-негативним та PR-позитивним. У деяких варіантах, рак молочної залози є PR-негативним та HER2-негативним. У деяких варіантах, рак молочної залози є PR-негативним, HER2-негативним та ER-позитивним. У деяких варіантах, рак молочної залози є ER-негативним, PR-негативним та HER2-негативним. У деяких варіантах, рак молочної залози має дефіцит на репарацію ДНК шляхом гомологічної рекомбінації. У деяких варіантах, лікування передбачає цикл лікування принаймні 11 днів, де на 1, 4, 8 та 11 дні циклу пацієнт отримує від близько 1 до близько 100 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, 4-йодо-3-нітробензамід призначається перорально, та шляхом парентеральної ін'єкції чи вливання, чи інгаляції. У деяких варіантах, цикл лікування триває від близько 11 до близько 30 днів. У деяких варіантах, спосіб також включає призначення пацієнтові інгібітору PARP у поєднанні з принаймні одним протипухлинним агентом. Протипухлинний агент є протипухлинним алкілувальним агентом, протипухлинним антиметаболітом, протипухлинним 6 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 антибіотиком, протипухлинним агентом рослинного походження, протипухлинною органічною сполукою платини, протипухлинною похідною камптотецину, протипухлинним інгібітором тирозин кінази, моноклональним антитілом, інтерфероном, модифікатором біологічного відгуку, гормональним протипухлинним агентом, протипухлинним вірусним агентом, інгібітором ангіогенезу, диференціюючим агентом чи іншим агентом, який відзначається протипухлинною активністю, чи їх фармацевтично прийнятною сіллю. У деяких варіантах, протипухлинний агент є цитабіном, capeцитабіном, валопіцитабіном чи гемцитабіном. У деяких варіантах, протипухлинний агент є комплексом платини. У деяких варіантах, спосіб також включає призначення пацієнтові інгібітору PARP у поєднанні з більш ніж одним протипухлинним агентом. Протипухлинний агент призначається до, як супутній чи після призначення інгібітору PARP. У деяких варіантах, спосіб також включає призначення пацієнтові інгібітору PARP у поєднанні з протиангіогенним агентом, таким як Авастин. У деяких варіантах, спосіб також включає призначення пацієнтові інгібітору PARP у поєднанні з інгібітором топоізомерази, таким як іринотекан чи Топотекан. У деяких варіантах, спосіб також включає призначення пацієнтові інгібітору PARP у поєднанні з таксаном, таким як паклітаксел чи доцетаксел. У деяких варіантах, спосіб також включає призначення пацієнтові інгібітору PARP у поєднанні з агентом, націленим на Her-2, таким як Герцептин. У деяких варіантах, спосіб також включає призначення пацієнтові інгібітору PARP у поєднанні з гормональною терапією, такою як антагоніст гормону тамоксифен. У деяких варіантах, спосіб також включає призначення пацієнтові інгібітору PARP у поєднанні з агентом, націленим на рецептор фактору росту, включаючи інгібітор рецептору епідермального фактору росту (EGFR) та інгібітор інсуліноподібного рецептору (IGF1R) фактору росту 1 (IGF-1). У деяких варіантах, спосіб також включає призначення пацієнтові інгібітору PARP у поєднанні з гамма опроміненням. У деяких варіантах, спосіб також включає хірургію, променеву терапію, хіміотерапію, генну терапію, терапію ДНК, ад'ювантну терапію, неоад'ювантну терапію, терапію РНК, терапію ДНК, вірусну терапію, імунотерапію, нанотерапію чи їх поєднання. Деякі варіанти, описані у цій заявці, передбачають спосіб лікування раку молочної залози у пацієнта, що включає призначення пацієнтові принаймні одного інгібітору PARP та принаймні одного протипухлинного агенту. У деяких варіантах, досягається принаймні один терапевтичний ефект, при цьому зазначений принаймні один терапевтичний ефект проявляється у зменшенні розміру пухлини молочної залози, скороченні метастазу, повній ремісії, частковій ремісії, повній патоморфологічній регресії чи стабілізації хвороби. У деяких варіантах, досягається покращення показника клінічної ефективності (CBR = CR + PR + SD ≥ 6 місяців) порівняно з лікуванням антиметаболітом та комплексом платини, але без інгібітору PARP. У деяких варіантах, покращення показника клінічної ефективності становить принаймні близько 60 %. У деяких варіантах, інгібітор PARP є бензамідом чи його метаболітом. У деяких варіантах, бензамід є 4-йодо-3-нітробензамідом чи його метаболітом. У деяких варіантах, комплекс платини обрано серед групи, що складається з цисплатину, карбоплатину, оксаплатину та оксаліплатину. У деяких варіантах, комплекс платини є карбоплатином. У деяких варіантах, антиметаболіт є цитабіном. У деяких варіантах, антиметаболіт обрано серед групи, що складається з цитабіну, capeцитабіну, гемцитабіну та валопіцитабіну. У деяких варіантах, антиметаболіт є гемцитабіном. У деяких варіантах, спосіб також включає призначення пацієнтові таксану. У деяких варіантах, таксан є паклітакселом чи доцетакселом. У деяких варіантах, рак молочної залози є метастатичним раком молочної залози. У деяких варіантах, рак молочної залози знаходиться на стадії I, II чи III. У деяких варіантах, рак молочної залози є HR-негативним раком молочної залози. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2; та рак молочної залози є позитивним щодо принаймні одного з ER, PR чи HER2. У деяких варіантах, рак молочної залози є HRнегативним раком молочної залози. У деяких варіантах, рак молочної залози є ER-негативним раком молочної залози. У деяких варіантах, рак молочної залози є ER-негативним та HER2позитивним. У деяких варіантах, рак молочної залози є ER-негативним та PR-позитивним. У деяких варіантах, рак молочної залози є ER-негативним, а також як HER2-позитивним, так і PRпозитивним. У деяких варіантах, рак молочної залози є PR-негативним раком молочної залози. У деяких варіантах, рак молочної залози є PR-негативним та ER-позитивним. У деяких варіантах, рак молочної залози є PR-негативним та HER2-позитивним. У деяких варіантах, рак молочної залози є PR-негативним, а також як ER-позитивним, так і HER2-позитивним. У деяких варіантах, рак молочної залози є HER2-негативним раком молочної залози. У деяких варіантах, рак молочної залози є HER2-негативним та ER-позитивним. У деяких варіантах, рак молочної залози є HER2-негативним та PR-позитивним. У деяких варіантах, рак молочної залози є HER2негативним, а також як ER-позитивним, так і PR-позитивним. У деяких варіантах, рак молочної 7 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 залози є ER-негативним та PR-негативним. У деяких варіантах, рак молочної залози є ERнегативним, PR-негативним та HER-2 позитивним. У деяких варіантах, рак молочної залози є ER-негативним та HER2-негативним. У деяких варіантах, рак молочної залози є ER-негативним, HER2-негативним та PR-позитивним. У деяких варіантах, рак молочної залози є PR-негативним та HER2-негативним. У деяких варіантах, рак молочної залози є PR-негативним, HER2негативним та ER-позитивним. У деяких варіантах, рак молочної залози є ER-негативним, PRнегативним та HER2-негативним. У деяких варіантах, рак молочної залози має дефіцит на репарацію ДНК шляхом гомологічної рекомбінації. У деяких варіантах, способи також включають призначення інгібітору PARP у поєднанні з протипухлинним агентом. У деяких варіантах, протипухлинний агент є протипухлинним алкілувальним агентом, протипухлинним антиметаболітом, протипухлинними антибіотиками, протипухлинним агентом рослинного походження, протипухлинним комплексом платини, протипухлинною похідною камптотецину, протипухлинним інгібітор тирозин кінази, моноклональним антитілом, інтерфероном, модифікатором біологічного відгуку, гормональним протипухлинним агентом, інгібітором ангіогенезу, диференціюючим агентом чи іншим агентом, який відзначається протипухлинною активністю, чи їх фармацевтично прийнятною сіллю. У деяких варіантах, комплекс платини є цисплатином, карбоплатином, оксаплатином чи оксаліплатином. У деяких варіантах, антиметаболіт є цитабіном, capeцитабіном, гемцитабіном чи валопіцитабіном. У деяких варіантах, способи також включають призначення пацієнтові інгібітору PARP у поєднанні з більш ніж одним протипухлинним агентом. У деяких варіантах, протипухлинний агент призначається до, як супутній чи після прийому інгібітору PARP. У деяких варіантах, протипухлинний агент є протиангіогенним агентом, таким як Авастин. У деяких варіантах, протипухлинний агент є інгібітором топоізомерази, включаючи, але не обмежуючись, іринотекан, Топотекан, чи камптотецин. У деяких варіантах, протипухлинний агент є таксаном, включаючи, але не обмежуючись, паклітаксел чи доцетаксел. У деяких варіантах, протипухлинний агент є агентом, націленим на Her-2, наприклад, Герцептин. У деяких варіантах, протипухлинний агент є антагоністом гормону, наприклад, тамоксифен. У деяких варіантах, протипухлинний агент є агентом, націленим на рецептор фактору росту. У деяких варіантах, таким агентом є інгібітор рецептору (EGFR) епідермального фактору росту чи інгібітор рецептору (IGF1R) інсуліноподібного фактору росту 1 (IGF-1). У інших варіантах, спосіб також включає хірургію, променеву терапію, хіміотерапію, генну терапію, терапію ДНК, ад'ювантну терапію, неоад'ювантну терапію, вірусну терапію, терапію РНК, імунотерапію, нанотерапію чи їх поєднання. У деяких варіантах, лікування передбачає цикл лікування принаймні 11 днів, де на 1, 4, 8 та 11 дні циклу пацієнт отримує від близько 10 до близько 100 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, лікування передбачає лікувальний цикл принаймні 11 днів, де на 4, 8 та 11 дні циклу пацієнт отримує від близько 1 до близько 50 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, лікування передбачає цикл лікування принаймні 11 днів, де на 1, 4, 8 та 11 дні циклу пацієнт отримує близько 1, 2, 3, 4, 5, 6, 8, чи 10, 12, 14, 16, 18, чи 20 мг/кг 4-йодо-3-нітробензаміду. У деяких варіантах, лікування передбачає цикл лікування принаймні 11 днів, де: (a) на 1 та 8 2 дні циклу пацієнт отримує близько 100-2000 мг/м гемцитабіну; (b) на 1 та 8 дні циклу пацієнт 2 отримує від близько 10 до близько 400 мг/м карбоплатину; та (c) на 1, 4, 8 та 11 дні циклу пацієнт отримує від близько 10 до близько 100 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, на 1 та 8 дні циклу пацієнт отримує близько 2 100-2500 мг/м гемцитабіну та близько AUC 1-5 карбоплатину (від близько 10 до близько 400 2 мг/м карбоплатину); та на 1, 4, 8 та 11 дні циклу пацієнт отримує від близько 1 до близько 50 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, на 2 1 та 8 дні циклу пацієнт отримує близько 500-2000 мг/м гемцитабіну та від близько 50 до 2 близько 400 мг/м карбоплатину; та на 1, 4, 8 та 11 дні циклу пацієнт отримує від близько 1 до близько 50 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту метаболіту. У деяких 2 варіантах, на 1 та 8 дні циклу пацієнт отримує близько 1000 мг/м гемцитабіну та близько AUC 2 карбоплатину; та на 1, 4, 8 та 11 дні циклу пацієнт отримує близько 1, 2, 3, 4, 6, 8 чи 10, 12, 14, 16, 18 чи 20 мг/кг 4-йодо-3-нітробензаміду. Деякі варіанти описані у цій заявці, передбачають спосіб лікування раку молочної залози у пацієнта, який має тричі негативний рак молочної залози, з циклом лікування тривалістю 21 день, при цьому на 1, 4, 8 та 11 дні циклу пацієнт призначається від близько 10 до близько 100 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, 4йодо-3-нітробензамід призначається перорально чи шляхом внутрішньовенного вливання. Деякі варіанти передбачають спосіб лікування раку молочної залози у пацієнта, який має 8 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 тричі негативний рак молочної залози, з циклом лікування тривалістю 21 день: (a) на 1 та 8 дні 2 циклу пацієнту призначають близько 100-2000 мг/м гемцитабіну; (b) на 1 та 8 дні циклу пацієнту 2 призначають AUC 0.1-10 карбоплатину (від близько 10 до 400 мг/м карбоплатину); та (c) на 1, 4, 8 та 11 дні циклу пацієнту призначають від близько 10 до близько 100 мг/кг 4-йодо-3нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, гемцитабін вводиться шляхом внутрішньовенного вливання. У деяких варіантах, карбоплатин вводиться шляхом внутрішньовенного вливання. У деяких варіантах, 4-йодо-3-нітробензамід призначається перорально чи шляхом внутрішньовенного вливання. У деяких варіантах, гемцитабін вводиться шляхом внутрішньовенного вливання. У деяких варіантах, карбоплатин вводиться шляхом внутрішньовенного вливання. У деяких варіантах, 4-йодо-3-нітробензамід вводиться перорально чи шляхом внутрішньовенного вливання. Деякі варіанти, описані у цій заявці, передбачають спосіб лікування раку молочної залози у пацієнта, який має тричі негативний рак молочної залози, що включає: (a) визначення циклу лікування тривалістю від близько 10 до близько 30 днів; (b) протягом від 1 до 10 окремих днів циклу, призначення пацієнтові від близько 1 мг/кг до близько 50 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, 4-йодо-3-нітробензамід призначається перорально чи шляхом внутрішньовенного вливання. Деякі варіанти, описані у цій заявці, передбачають спосіб лікування раку молочної залози у пацієнта, який має тричі негативний рак молочної залози, що включає: (a) визначення циклу лікування тривалістю від близько 10 до близько 30 днів; (b) протягом від 1 до 5 окремих днів 2 циклу, призначення пацієнтові від близько 100 до близько 5000 мг/м гемцитабіну шляхом внутрішньовенного вливання; (c) протягом від 1 до 5 окремих днів циклу, призначення пацієнтові від AUC 1 до AUC 10 карбоплатину шляхом внутрішньовенного вливання (наприклад, 2 від близько 10 до близько 400 мг/м карбоплатину); та (d) протягом від 1 до 10 окремих днів циклу, призначення пацієнтові від близько 1 мг/кг до близько 50 мг/кг 4-йодо-3-нітробензаміду, чи молярного еквіваленту його метаболіту. У деяких варіантах, гемцитабін вводиться шляхом внутрішньовенного вливання. У деяких варіантах, карбоплатин вводиться шляхом внутрішньовенного вливання. У деяких варіантах, 4-йодо-3-нітробензамід призначається перорально чи шляхом внутрішньовенного вливання. Деякі варіанти включають спосіб лікування раку молочної залози у пацієнта, який потребує такого лікування, що включає: (a) отримання зразка від пацієнта; (b) дослідження зразка з метою визначення принаймні одного з наступних: (i) чи рак є ER-позитивним чи ER-негативним; (ii) чи рак є PR-позитивним чи PR-негативним; (iii) чи рак є HER2-позитивним чи HER2негативним; (c) якщо дослідження свідчить про те, що рак є ER-негативним, PR-негативним чи HER2-негативним, лікування пацієнта у поєднанні з терапевтичними агентами, де терапевтичні агенти включають принаймні один антиметаболіт, принаймні один комплекс платини та принаймні один інгібітор PARP; та (d) якщо дослідження не свідчить про те, що рак є ERнегативним, PR-негативним чи HER2-негативним, вибір іншого варіанту лікування. Деякі варіанти включають спосіб лікування раку молочної залози у пацієнта, який потребує такого лікування, що включає: (a) отримання зразка від пацієнта; (b) дослідження зразка з метою визначення принаймні одного з наступних: (i) чи рак є ER-позитивним чи ER-негативним; (ii) чи рак є PR-позитивним чи PR-негативним; (iii) чи рак є HER2-позитивним чи HER2негативним; (c) якщо дослідження свідчить про те, що рак є ER-негативним, PR-негативним чи HER2-негативним, лікування пацієнта принаймні одним інгібітором PARP; та (d) якщо дослідження не свідчить про те, що рак є ER-негативним, PR-негативним чи HER2-негативним, вибір іншого варіанту лікування. У деяких варіантах, досягається принаймні один терапевтичний ефект, при цьому зазначений принаймні один терапевтичний ефект проявляється у зменшенні розміру пухлини молочної залози, скороченні метастазу, повній ремісії, частковій ремісії, повній патоморфологічній регресії чи стабілізації хвороби. У деяких варіантах, отримано покращення показника клінічної ефективності (CBR = CR + PR + SD ≥ 6 місяців) порівняно з лікуванням без інгібітору PARP. У деяких варіантах, показник клінічної ефективності становить принаймні близько 30 %. У деяких варіантах, отримано покращення показника клінічної ефективності (CBR = CR + PR + SD ≥ 6 місяців) порівняно з лікуванням антиметаболітом та комплексом платини, але без інгібітору PARP. У деяких варіантах, показник клінічної ефективності становить принаймні близько 60 %. У деяких варіантах, інгібітор PARP є інгібітором PARP-1. У інших варіантах, інгібітор PARP є бензамідом чи його метаболітом. У деяких варіантах, бензамід є 4йодо-3-нітробензамідом чи його метаболітом. У деяких варіантах, комплекс платини обрано серед групи, що складається з цисплатину, карбоплатину, оксаплатину та оксаліплатину. У деяких варіантах, комплекс платини є карбоплатином. У деяких варіантах, антиметаболіт є 9 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 цитабіном. У деяких варіантах, антиметаболіт обрано серед групи, що складається з цитабіну, capeцитабіну, гемцитабіну та валопіцитабіну. У деяких варіантах, антиметаболіт є гемцитабіном. У деяких варіантах, спосіб також включає призначення пацієнтові таксану. У деяких варіантах, таксан є паклітакселом чи доцетакселом. У деяких варіантах, зразок є тканиною чи зразком рідини організму. У деяких варіантах, зразок є зразком пухлини, зразком крові, зразком плазми крові, зразком рідини черевної порожнини, ексудатом чи випотом. У деяких варіантах, рак молочної залози є метастатичним раком молочної залози. У деяких варіантах, рак молочної залози є ER-негативним метастатичним раком молочної залози. У деяких варіантах, рак молочної залози знаходиться на стадії I, II чи III. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2; та рак молочної залози є позитивним щодо принаймні одного з ER, PR чи HER2. У деяких варіантах, рак молочної залози є ER-негативним та PR-позитивним. У деяких варіантах, рак молочної залози є ER-негативним та HER2-позитивним. У деяких варіантах, рак молочної залози є ER-негативним, а також як PR-позитивним, так і HER2-позитивним. У деяких варіантах, рак молочної залози є PR-негативним метастатичним раком молочної залози. У деяких варіантах, рак молочної залози є PR-негативним та ER-позитивним. У деяких варіантах, рак молочної залози є PR-негативним та HER2-позитивним. У деяких варіантах, рак молочної залози є PR-негативним, а також як ERпозитивним, так і HER2-позитивним. У деяких варіантах, рак молочної залози є HER2негативним метастатичним раком молочної залози. У деяких варіантах, рак молочної залози є HER2-негативним та ER-позитивним. У деяких варіантах, рак молочної залози є HER2негативним та PR-позитивним. У деяких варіантах, рак молочної залози є HER2-негативним, а також як ER-позитивним, так і PR-позитивним. У деяких варіантах, рак молочної залози є ERнегативним та PR-негативним. У деяких варіантах, рак молочної залози є ER-негативним, PRнегативним та HER2-позитивним. У деяких варіантах, рак молочної залози є ER-негативним та HER2-негативним. У деяких варіантах, рак молочної залози є ER-негативним, HER2-негативним та PR-позитивним. У деяких варіантах, рак молочної залози є PR-негативним та HER2негативним. У деяких варіантах, рак молочної залози є PR-негативним, HER2-негативним та PR-позитивним. У деяких варіантах, рак молочної залози є ER-негативним, PR-негативним та HER2-негативним. Деякі варіанти винаходу передбачають спосіб лікування раку молочної залози у пацієнта, який потребує такого лікування, що включає: (a) отримання зразка від пацієнта; (b) дослідження зразка з метою визначення наступного: (i) чи рак є ER-позитивним чи - негативним; (ii) чи рак є PR-позитивним чи - негативним; (iii) чи рак є HER2-позитивним чи - негативним; (c) за наявності двох чи більше з наступних умов, лікування пацієнта принаймні одним інгібітором PARP: (i) рак є ER-негативним, (ii) рак є PR-негативним, чи (iii) рак є HER2-негативним; та (d) якщо принаймні наявні дві з вищезазначених умов, вибір іншого варіанту лікування. Деякі варіанти винаходу передбачають спосіб лікування раку молочної залози у пацієнта, який потребує такого лікування, що включає: (a) отримання зразка від пацієнта; (b) дослідження зразка з метою визначення наступного:(i) чи рак є ER-позитивним чи - негативним; (ii) чи рак є PR-позитивним чи - негативним; (iii) чи рак є HER2-позитивним чи - негативним; (c) за наявності двох чи більше з наступних умов, лікування пацієнта у поєднанні з терапевтичними агентами, де терапевтичні агенти включають принаймні один антиметаболіт, принаймні один комплекс платини та принаймні один інгібітор PARP: (i) рак є ER-негативним, (ii) рак є PR-негативним, чи (iii) рак є HER2-негативним; та (d) якщо принаймні наявні дві з вищезазначених умов, вибір іншого варіанту лікування. У деяких варіантах, досягається принаймні один терапевтичний ефект, при цьому зазначений принаймні один терапевтичний ефект проявляється у зменшенні розміру пухлини молочної залози, скороченні метастазу, повній ремісії, частковій ремісії, повній патоморфологічній регресії чи стабілізації хвороби. У деяких варіантах, досягається покращення показника клінічної ефективності (CBR = CR + PR + SD ≥ 6 місяців) порівняно з лікуванням без інгібітору PARP. У деяких варіантах, показник клінічної ефективності становить принаймні близько 30 %. У деяких варіантах, досягається покращення показника клінічної ефективності (CBR = CR + PR + SD ≥ 6 місяців) порівняно з лікуванням антиметаболітом та комплексом платини, але без інгібітору PARP. У деяких варіантах, показник клінічної ефективності становить принаймні близько 60 %. У деяких варіантах, зразок є тканиною чи зразком рідини організму. У деяких варіантах, зразок є зразком пухлини, зразком крові, зразком плазми крові, зразком рідини черевної порожнини, ексудатом чи випотом. У деяких варіантах, інгібітор PARP є інгібітором PARP-1. У інших варіантах, інгібітор PARP є бензамідом чи його метаболітом. У деяких варіантах, бензамід є 4-йодо-3-нітробензамідом чи його метаболітом. У деяких варіантах, комплекс платини обрано серед групи, що складається з цисплатину, 10 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 карбоплатину, оксаплатину та оксаліплатину. У деяких варіантах, комплекс платини є карбоплатином. У деяких варіантах, антиметаболіт є цитабіном. У деяких варіантах, антиметаболіт обрано серед групи, що складається з цитабіну, capeцитабіну, гемцитабіну та валопіцитабіну. У деяких варіантах, антиметаболіт є гемцитабіном. У деяких варіантах, спосіб також включає призначення пацієнтові таксану. У деяких варіантах, таксан є паклітакселом чи доцетакселом. У деяких варіантах, рак молочної залози є метастатичним раком молочної залози. У деяких варіантах, рак молочної залози знаходиться на стадії I, II чи III. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2; та рак молочної залози є позитивним щодо принаймні одного з ER, PR чи HER2. У деяких варіантах, рак молочної залози є ER-негативним метастатичним раком молочної залози. У деяких варіантах, рак молочної залози є PR-негативним метастатичним раком молочної залози. У деяких варіантах, рак молочної залози є HER2-негативним метастатичним раком молочної залози. У деяких варіантах, рак молочної залози є ER-негативним та PR-негативним. У деяких варіантах, рак молочної залози є ER-негативним та HER2-негативним. У деяких варіантах, рак молочної залози є PR-негативним та HER2-негативним. У деяких варіантах, рак молочної залози є ER-негативним, PR-негативним та HER2-негативним. У деяких варіантах, лікування передбачає вибір циклу лікування тривалістю принаймні 11 днів та: (a) на 1, 4, 8 та 11 дні цикл, пацієнт отримує від близько 10 до близько 100 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, 4-йодо-3-нітробензамід призначається перорально чи шляхом внутрішньовенного вливання. У деяких варіантах, лікування передбачає вибір циклу лікування принаймні 11 днів та: (a) на 1 та 8 дні циклу, пацієнт отримує близько 1002 2000 мг/м гемцитабіну; (b) на 1 та 8 дні циклу, пацієнт отримує від близько 10 до близько 400 2 мг/м карбоплатину; та (c) на 1, 4, 8 та 11 дні циклу пацієнт отримує від близько 10 до близько 100 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, гемцитабін вводиться шляхом внутрішньовенного вливання. У деяких варіантах, карбоплатин вводиться шляхом внутрішньовенного вливання. У деяких варіантах, 4-йодо-3нітробензамід вводиться перорально чи шляхом внутрішньовенного вливання. Деякі варіанти, що розкриваються у цій заявці, передбачають спосіб лікування раку молочної залози у пацієнта, який потребує такого лікування, що включає: (a) отримання зразка від пацієнта; (b) дослідження зразка з метою визначення наступного: (i) чи рак є ER-позитивним чи - негативним; (ii) чи рак є PR-позитивним чи - негативним; та (iii) чи рак є HER2-позитивним чи - негативним; (c) за наявності двох чи більше з наступних умов, лікування пацієнта принаймні одним інгібітором PARP: (i) рак є ER-негативним, (ii) рак є PR-негативним, чи (iii) рак є HER2негативним; та (d) за відсутності двох чи більше умов (i)-(iii), вибір іншого варіанту лікування. Деякі варіанти, описані у цій заявці, передбачають спосіб лікування ER-негативного, PRнегативного, HER-2 негативного метастатичного раку молочної залози у пацієнта, який потребує такого лікування, що включає призначення зазначеному пацієнтові принаймні одного інгібітору PARP. У деяких варіантах, досягається покращення показника клінічної ефективності (CBR = CR + PR + SD ≥ 6 місяців) порівняно з лікуванням без інгібітору PARP. У деяких варіантах, показник клінічної ефективності становить принаймні близько 30 %. У деяких варіантах, пацієнтові призначають дві чи більше терапевтичних сполуки у формі єдиної дози. У деяких варіантах, інгібітор PARP є інгібітором PARP-1. У інших варіантах, інгібітор PARP є бензамідом чи його метаболітом. У деяких варіантах, бензамід є 4-йодо-3-нітробензамідом чи його метаболітом. У деяких варіантах, рак молочної залози є метастатичним раком молочної залози. У деяких варіантах, рак молочної залози є ER-негативним метастатичним раком молочної залози. У деяких варіантах, рак молочної залози є PR-негативним метастатичним раком молочної залози. У деяких варіантах, рак молочної залози є HER2-негативним метастатичним раком молочної залози. У деяких варіантах, рак молочної залози є ER-негативним та PR-негативним. У деяких варіантах, рак молочної залози є ER-негативним та HER2-негативним. У деяких варіантах, рак молочної залози є PR-негативним та HER2-негативним. У деяких варіантах, рак молочної залози є ER-негативним, PR-негативним та HER2-негативним. У деяких варіантах, лікування передбачає цикл лікування тривалістю принаймні 11 днів та на 1, 4, 8 та 11 дні циклу пацієнт отримує від близько 10 до близько 100 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, 4-йодо-3-нітробензамід вводиться перорально чи шляхом внутрішньовенного вливання. Деякі варіанти передбачають спосіб лікування раку молочної залози у пацієнта, що включає: (a) дослідження зразка від пацієнта на предмет експресії PARP; та (b) якщо експресія PARP перевищує визначений рівень, призначення пацієнтові принаймні одного інгібітору PARP. У деяких варіантах, досягається принаймні один терапевтичний ефект, при цьому зазначений 11 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 принаймні один терапевтичний ефект проявляється у зменшенні розміру пухлини молочної залози, скороченні метастазу, повній ремісії, частковій ремісії, повній патоморфологічній регресії чи стабілізації хвороби. У деяких варіантах, досягається покращення показника клінічної ефективності (CBR = CR + PR + SD ≥ 6 місяців) порівняно з лікуванням без інгібітору PARP. У деяких варіантах, покращення показника клінічної ефективності становить принаймні близько 30 %. У деяких варіантах, інгібітор PARP є інгібітором PARP-1. У інших варіантах, інгібітор PARP є бензамідом чи його метаболітом. У деяких варіантах, бензамід є 4-йодо-3нітробензамідом чи його метаболітом. У деяких варіантах, рак молочної залози є метастатичним раком молочної залози. У деяких варіантах, спосіб також включає дослідження зразка від пацієнта на предмет експресії естрогенового рецептору, прогестеронового рецептору чи рецептору людського епідермального фактору росту 2. У деяких варіантах, рак молочної залози є HR-негативним раком молочної залози. У деяких варіантах, рак молочної залози є ER-негативним раком молочної залози. У деяких варіантах, рак молочної залози є PR-негативним раком молочної залози. У деяких варіантах, рак молочної залози є HER2-негативним раком молочної залози. У деяких варіантах, рак молочної залози є ER-негативним та PR-негативним. У деяких варіантах, рак молочної залози є ER-негативним та HER2-негативним. У деяких варіантах, рак молочної залози є PR-негативним та HER2-негативним. У деяких варіантах, рак молочної залози є ERнегативним, PR-негативним та HER2-негативним. У деяких варіантах, лікування передбачає вибір циклу лікування тривалістю принаймні 11 днів та на 1, 4, 8 та 11 дні циклу пацієнт отримує від близько 10 до близько 100 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, 4-йодо-3-нітробензамід вводиться перорально чи шляхом внутрішньовенного вливання. Деякі варіанти, що розкриваються у цій заявці, передбачають спосіб лікування раку молочної залози у пацієнта, який потребує такого лікування, що включає: (a) отримання зразка від пацієнта; (b) дослідження зразка з метою визначення наступного: (i) чи рак є ER-позитивним чи - негативним; (ii) чи рак є PR-позитивним чи - негативним; та (iii) чи рак є HER2-позитивним чи - негативним; (c) за наявності двох чи більше з наступних умов, лікування пацієнта у поєднанні з терапевтичними агентами, де терапевтичні агенти включають принаймні один антиметаболіт, принаймні один комплекс платини та принаймні один інгібітор PARP: (i) рак є ER-негативним, (ii) рак є PR-негативним, чи (iii) рак є HER2-негативним; та (d) за відсутності двох чи більше умов (i)-(iii), вибір іншого варіанту лікування. У деяких варіантах, гемцитабін вводиться шляхом внутрішньовенного вливання. У деяких варіантах, карбоплатин водиться шляхом внутрішньовенного вливання. У деяких варіантах, 4-йодо-3-нітробензамід водиться перорально чи шляхом внутрішньовенного вливання. Деякі варіанти, описані у цій заявці, передбачають спосіб лікування ER-негативного, PRнегативного, HER-2 негативного метастатичного раку молочної залози у пацієнта, який потребує такого лікування, що включає призначення зазначеному пацієнтові принаймні одного антиметаболіту, принаймні одного комплексу платини та принаймні одного інгібітору PARP. У деяких варіантах, досягається покращення показника клінічної ефективності (CBR = CR + PR + SD ≥ 6 місяців) порівняно з лікуванням антиметаболітом та комплексом платини, але без інгібітору PARP. У деяких варіантах, показник клінічної ефективності становить принаймні близько 60 %. У деяких варіантах, пацієнтові призначають дві чи більше терапевтичних сполуки у формі єдиної дози. У деяких варіантах, інгібітор PARP є бензамідом чи його метаболітом. У деяких варіантах, бензамід є 4-йодо-3-нітробензамідом чи його метаболітом. У деяких варіантах, комплекс платини обрано серед групи, що складається з цисплатину, карбоплатину, оксаплатину та оксаліплатину. У деяких варіантах, комплекс платини є карбоплатином. У деяких варіантах, антиметаболіт є цитабіном. У деяких варіантах, антиметаболіт обрано серед групи, що складається з цитабіну, capeцитабіну, гемцитабіну та валопіцитабіну. У деяких варіантах, антиметаболіт є гемцитабіном. У деяких варіантах, спосіб також включає призначення пацієнтові таксану. У деяких варіантах, таксан є паклітакселом чи доцетакселом. У деяких варіантах, рак молочної залози є метастатичним раком молочної залози. У деяких варіантах, рак молочної залози знаходиться на стадії I, II чи III. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2; та рак молочної залози є позитивним щодо принаймні одного з ER, PR чи HER2. У деяких варіантах, рак молочної залози є ERнегативним метастатичним раком молочної залози. У деяких варіантах, рак молочної залози є PR-негативним метастатичним раком молочної залози. У деяких варіантах, рак молочної залози є HER2-негативним метастатичним раком молочної залози. У деяких варіантах, рак молочної залози є ER-негативним та PR-негативним. У деяких варіантах, рак молочної залози є ER 12 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 негативним та HER2-негативним. У деяких варіантах, рак молочної залози є PR-негативним та HER2-негативним. У деяких варіантах, рак молочної залози є ER-негативним, PR-негативним та HER2-негативним. У деяких варіантах, лікування передбачає вибір циклу лікування тривалістю 2 принаймні 11 днів та: (a) на 1 та 8 дні циклу пацієнт отримує близько 100-2000 мг/м 2 гемцитабіну; (b) на 1 та 8 дні циклу пацієнт отримує від близько 10 до близько 400 мг/м карбоплатину; та (c) на 1, 4, 8 та 11 дні циклу пацієнт отримує від близько 10 до близько 100 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, гемцитабін водиться шляхом внутрішньовенного вливання. У деяких варіантах, карбоплатин водиться шляхом внутрішньовенного вливання. У деяких варіантах, 4-йодо-3-нітробензамід водиться перорально чи шляхом внутрішньовенного вливання. Деякі варіанти передбачають спосіб лікування раку молочної залози у пацієнта, що включає: (a) дослідження зразка від пацієнта на предмет експресії PARP; та (b) якщо експресія PARP перевищує визначений рівень, призначення пацієнтові принаймні одного антиметаболіту, принаймні одного комплексу платини та принаймні одного інгібітору PARP. У деяких варіантах, досягається принаймні один терапевтичний ефект, при цьому зазначений принаймні один терапевтичний ефект проявляється у зменшенні розмірів пухлини молочної залози, скороченні метастазу, повній ремісії, частковій ремісії, повній патоморфологічній регресії чи стабілізації хвороби. У деяких варіантах, досягається покращення показника клінічної ефективності (CBR = CR + PR + SD ≥ 6 місяців) порівняно з лікуванням антиметаболітом та комплексом платини, але без інгібітору PARP. У деяких варіантах, покращення показника клінічної ефективності становить принаймні близько 60 %. У деяких варіантах, інгібітор PARP є бензамідом чи його метаболітом. У деяких варіантах, бензамід є 4-йодо-3-нітробензамідом чи його метаболітом. У деяких варіантах, комплекс платини обрано серед групи, що складається з цисплатину, карбоплатину, оксаплатину та оксаліплатину. У деяких варіантах, комплекс платини є карбоплатином. У деяких варіантах, антиметаболіт є цитабіном. У деяких варіантах, антиметаболіт обрано серед групи, що складається з цитабіну, capeцитабіну, гемцитабіну та валопіцитабіну. У деяких варіантах, антиметаболіт є гемцитабіном. У деяких варіантах, спосіб також включає призначення пацієнтові таксану. У деяких варіантах, таксан є паклітакселом чи доцетакселом. У деяких варіантах, рак молочної залози є метастатичним раком молочної залози. У деяких варіантах, спосіб також включає дослідження зразка від пацієнта на предмет експресії естрогенового рецептору, прогестеронового рецептору чи рецептору людського епідермального фактору росту 2. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з: ER, PR чи HER2; та рак молочної залози є позитивним щодо принаймні одного з ER, PR чи HER2. У деяких варіантах, рак молочної залози є HR-негативним раком молочної залози. У деяких варіантах, рак молочної залози є ER-негативним раком молочної залози. У деяких варіантах, рак молочної залози є PR-негативним раком молочної залози. У деяких варіантах, рак молочної залози є HER2-негативним раком молочної залози. У деяких варіантах, рак молочної залози є ER-негативним та PR-негативним. У деяких варіантах, рак молочної залози є ER-негативним та HER2-негативним. У деяких варіантах, рак молочної залози є PR-негативним та HER2-негативним. У деяких варіантах, рак молочної залози є ERнегативним, PR-негативним та HER2-негативним. У деяких варіантах, лікування передбачає вибір циклу лікування тривалістю принаймні 11 днів та: (a) на 1 та 8 дні циклу пацієнт отримує 2 близько 100-2000 мг/м гемцитабіну; (b) на 1 та 8 дні циклу пацієнт отримує від близько 10 до 2 близько 400 мг/м карбоплатину; та (c) на 1, 4, 8 та 11 дні циклу пацієнт отримує від близько 10 до близько 100 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, гемцитабін водиться шляхом внутрішньовенного вливання. У деяких варіантах, карбоплатин водиться шляхом внутрішньовенного вливання. У деяких варіантах, 4йодо-3-нітробензамід водиться перорально чи шляхом внутрішньовенного вливання. Таким чином, варіанти, передбачені у цій заявці, включають лікування пацієнта принаймні трьома речовинами, що відрізняються за хімічним складом, однією з яких є антиметаболіт, однією з яких є комплекс, що містить платину, та однією з яких є інгібітор PARP. У деяких варіантах, одна чи більше з цих речовин має здатність бути представленою у різних фізичних формах - наприклад, вільна основа, солі (зокрема, фармацевтично прийнятні солі), гідрати, поліморфи, сольвати, метаболіти, тощо. Якщо інше не кваліфіковане у цій специфікації, використання хімічної назви має на меті охопити усі фізичні форми зазначеної хімічної речовини. Наприклад, наведення 4-йодо-3-нітробензаміду без подальшої кваліфікації має на меті у цілому охопити вільну основу, а також усі фармацевтично прийнятні солі, поліморфи, гідрати, метаболіти, тощо. Коли мається на меті обмежити розкриття чи пункти формули до конкретної фізичної форми, це буде чітко зрозуміло з контексту уривку чи пункту формули, у 13 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 яких з'являється посилання на сполуку. У деяких варіантах, дане розкриття передбачає спосіб лікування раку молочної залози, що включає призначення пацієнтові принаймні одного таксану, принаймні одного комплексу платини та принаймні одного інгібітору PARP. У деяких варіантах, досягається принаймні один терапевтичний ефект, при цьому зазначений принаймні один терапевтичний ефект проявляється у зменшенні розміру пухлини молочної залози, скорочення метастазу, повній ремісії, частковій ремісії, повній патоморфологічній регресії чи стабілізації хвороби. У деяких варіантах, інгібітор PARP є бензамідом чи його метаболітом. У деяких варіантах, бензамід є 4йодо-3-нітробензамідом чи його метаболітом. У деяких варіантах, комплекс платини обрано серед групи, що складається з цисплатину, карбоплатину, оксаплатину та оксаліплатину. У деяких варіантах, комплекс платини є карбоплатином. У деяких варіантах, таксан є паклітакселом чи доцетакселом. У деяких варіантах, таксан є паклітакселом. У деяких варіантах, спосіб передбачає цикл лікування тривалістю принаймні 11 днів: (a) на 1 день циклу 2 призначення пацієнтові близько 10-200 мг/м паклітакселу; (b) на 1 день циклу призначення 2 пацієнтові близько 10-400 мг/м карбоплатину; та (c) на 1 день та двічі на тиждень протягом циклу призначення пацієнтові близько 1-100 мг/кг 4-йодо-3-нітробензаміду чи молярного еквіваленту його метаболіту. У деяких варіантах, розкриття у цій специфікації передбачає спосіб лікування раку молочної залози у пацієнта, що включає: (a) отримання зразка від пацієнта; (b) дослідження зразка з метою визначення рівня експресії PARP у зразку; (c) визначення, чи експресія PARP перевищує визначений рівень, та в разі його перевищення, призначення пацієнтові принаймні одного таксану, принаймні одного комплексу платини та принаймні одного інгібітору PARP. У деяких варіантах, спосіб також включає необов’язково вибір іншого варіанту лікування, якщо експресія PARP у зразку не перевищує визначений рівень. У деяких варіантах, рак є раком молочної залози, що є негативним щодо одного чи більше рецепторів гормону. У деяких варіантах, рак є раком молочної залози, що є негативним щодо HER2. У деяких варіантах, рак є негативним щодо естрогенового рецептору (ER), прогестинового рецептору (PR) чи HER2. У деяких варіантах, рак є позитивним щодо принаймні одного рецептору гормону чи HER2. У деяких варіантах, таксан є цисплатином, карбоплатином, оксаплатином чи оксаліплатином. У деяких варіантах, таксан є паклітакселом. У деяких варіантах, комплекс платини є цисплатином чи карбоплатином. У деяких варіантах, комплекс платини є карбоплатином. У деяких варіантах, інгібітор PARP є бензамідом чи його метаболітом. У деяких варіантах, інгібітор PARP є 4-йодо-3нітробензамідом чи його метаболітом. У деяких варіантах, зразок є зрізом пухлини чи рідиною організму. Деякі варіанти, описані у цій заявці, передбачають спосіб лікування раку молочної залози у пацієнта, що включає цикл лікування тривалістю 21 день: (a) на 1 день циклу призначення 2 пацієнтові близько 750 мг/м паклітакселу; (b) на 1 день циклу призначення пацієнтові близько 2 10-400 мг/м карбоплатину; та (c) на 1 день циклу та далі двічі на тиждень призначення пацієнтові близько 1-100 мг/кг 4-йодо-3-нітробензаміду. У деяких варіантах, паклітаксел водиться шляхом внутрішньовенного вливання. У деяких варіантах, карбоплатин водиться шляхом внутрішньовенного вливання. У деяких варіантах, 4-йодо-3-нітробензамід водиться перорально чи шляхом внутрішньовенного вливання. Деякі варіанти, описані у цій заявці, передбачають спосіб лікування раку молочної залози у пацієнта, що включає: (a) визначення циклу лікування тривалістю від близько 10 до близько 30 днів; (b) протягом від 1 до 5 окремих днів циклу призначення пацієнтові від близько 100 до 2 близько 2000 мг/м паклітакселу шляхом внутрішньовенного вливання протягом від близько 10 до близько 300 хвилин; (c) протягом від 1 до 5 окремих днів циклу призначення пацієнтові 2 близько 10-400 мг/м карбоплатину шляхом внутрішньовенного вливання протягом від близько 10 до близько 300 хвилин; та (d) протягом від 1 до 10 окремих днів циклу призначення пацієнтові від близько 1 мг/кг до близько 8 мг/кг 4-йодо-3-нітробензаміду протягом від близько 10 до близько 300 хвилин. Таким чином, варіанти, передбачені у цій заявці, включають лікування пацієнта принаймні трьома речовинами, що відрізняються за хімічним складом, однією з яких є таксан (наприклад, паклітаксел чи доцетаксел), однією з яких є комплекс, що містить платину (наприклад, цисплатин чи карбоплатин, чи цисплатин), та однією з яких є інгібітор PARP (наприклад, BA чи його метаболіт). У деяких варіантах, одна чи більше з цих речовин має здатність бути представленою у різних фізичних формах - наприклад, вільна основа, солі (зокрема, фармацевтично прийнятні солі), гідрати, поліморфи, сольвати, метаболіти, тощо. Якщо інше не кваліфіковане у цій специфікації, використання хімічної назви має на меті охопити усі фізичні форми зазначеної хімічної речовини. Наприклад, наведення 4-йодо-3-нітробензаміду без 14 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 подальшої кваліфікації має на меті у цілому охопити вільну основу, а також усі фармацевтично прийнятні солі, поліморфи, гідрати, метаболіти, тощо. Коли мається на меті обмежити розкриття чи пункти формули до конкретної фізичної форми, це буде чітко зрозуміло з контексту уривку чи пункту формули, у яких з'являється посилання на сполуку. Терміни “ефективна кількість” чи “фармацевтично ефективна кількість” означають достатню кількість агенту для того, щоб забезпечити бажаний біологічний, терапевтичний та/чи профілактичний результат. Таким результатом може бути скорочення та/чи послаблення проявів, симптомів чи причин хвороби, чи будь-яка інша бажана зміна біологічної системи. Наприклад, “ефективною кількістю” для терапевтичного застосування є кількість сполуки нітробензаміду, яка розкривається у цій специфікації, самої по собі чи композиції, що включає сполуку нітробензаміду, потрібної відповідно до цієї специфікації для забезпечення клінічно суттєвого ослаблення хвороби. Відповідна ефективна кількість у кожному індивідуальному випадку може бути визначена спеціалістом зі звичайною кваліфікацією у даній галузі шляхом звичайного експерименту. Під “фармацевтично прийнятним” чи “фармакологічно прийнятним” мається на увазі матеріал, який не є біологічно чи в інший спосіб небажаним, тобто, матеріал може призначатися особі, не завдаючи значних небажаних біологічних ефектів чи не взаємодіючи у шкідливий спосіб з будь-якими компонентами композиції, до складу якої він входить. Термін “лікування” та його граматичні еквіваленти, у спосіб яким вони застосовуються в даній специфікації, включають досягнення терапевтичної користі та/чи профілактичної користі. Під терапевтичною користю мається на увазі знищення чи покращення розладів, що лежать в основі, та щодо яких здійснюється лікування. Наприклад, для пацієнта, хворого на рак, терапевтична користь передбачає знищення раку, що лежить в основі хвороби, чи покращення стану хворого. Також, терапевтична користь досягається шляхом знищення чи покращення одного чи більшої кількості фізіологічних симптомів, пов’язаних з розладом, що лежить в основі, у такий спосіб, що спостерігається покращення стану пацієнта, незважаючи на той факт, що пацієнт все ще може залишатися ураженим розладом, що лежить в основі. З метою профілактичної користі, спосіб відповідно до винаходу може бути застосовано, чи композиція відповідно до винаходу може бути призначена пацієнтові, якому загрожує розвиток раку, чи пацієнтові, у якого наявні прояви одного чи більшої кількості фізіологічних симптомів таких умов, навіть попри те, що діагностика стану могла не проводитися. Протипухлинні агенти Протипухлинні агенти, що можуть використовуватися у даному винаході включають, але не обмежуються, протипухлинні алкілувальні агенти, протипухлинні антиметаболіти, протипухлинні антибіотики, протипухлинні агенти рослинного походження, протипухлинний комплекс платини, протипухлинні похідні камптотецину, протипухлинні інгібітори тирозин кінази, моноклональні антитіла, інтерферони, модифікатори біологічного відгуку та інші агенти, що відзначаються протипухлинною активністю чи їх фармацевтично прийнятну сіль. У деяких варіантах, протипухлинний агент є алкілувальним агентом. Термін "алкілувальний агент" у цій специфікації загалом стосується агента, який утворює алкілову групу в реакції алкілування, під час якої атом водню органічної сполуки заміщується алкіловою групою. Приклади протипухлинних алкілувальних агентів включають, але не обмежуються, N-оксид азотистий іприт, циклофосфамід, іфосфамід, мелфалан, бусульфан, мітобронітол, карбоквон, тіотепа, ранімустін, німустін, темозоломід чи кармустін. У деяких варіантах, протипухлинний агент є антиметаболітом. Термін "антиметаболіт" у цій специфікації включає, у широкому сенсі, речовини, які порушують нормальний метаболізм, та речовини, які пригнічують систему перенесення електронів з метою запобігання утворенню макроергічних посередників, внаслідок їх структурних чи функціональних подібностей до метаболітів, які є важливими для живих організмів (такі як, вітаміни, коферменти, амінокислоти та сахариди). Приклади антиметаболітів, які відзначаються протипухлинною активністю, включають, але не обмежуються, метотрексат, 6-меркаптопурин рібозиду, меркаптопурин, 5фторурацил, тегафур, доксіфлурідин, кармур, цитарабін, окфосфат цитарабіну, еноцитабін, S-1, гемцитабін, флударабін чи пеметрексед двонатрієвий, при цьому перевага надається 5фторурацилу, S-1, гемцитабіну та їм подібним. У деяких варіантах, протипухлинний агент є протипухлинним антибіотиком. Приклади протипухлинних антибіотиків включають, але не обмежуються, актиноміцин D, доксорубіцин, даунорубіцин, неокарциностатин, блеоміцин, пепломіцин, мітоміцин C, акларубіцин, пірарубіцин, епірубіцин, зиностатін стімаламер, ідарубіцин, сіролімус чи валрубіцин. У деяких варіантах, протипухлинний агент є протипухлинним агентом рослинного походження. Приклади протипухлинних агентів рослинного походження включають, але не обмежуються, вінкрістин, 15 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 вінбластин, віндезін, етопозид, собузоксан, доцетаксел, паклітаксел та вінорелбін, при цьому перевага надається доцетакселу та паклітакселу. У деяких варіантах, протипухлинний агент є похідною камптотецину, яка відзначається протипухлинною активністю. Приклади протипухлинних похідних камптотецину включають, але не обмежуються, камптотецин, 10-гідроксилкамптотецин, Топотекан, іринотекан чи 9амінокамптотецин, при цьому перевага надається камптотецину, Топотекану та іринотекану. Крім того, іринотекан метаболізує in vivo та виявляє протипухлинний ефект як SN-38. Механізм дії та активність похідних камптотецину вважаються фактично такими ж як і самого камптотецину (наприклад, Нітта та інші, Ган ту Кагаку Ріохо, 14, 850-857 (1987)). У деяких варіантах, протипухлинний агент є органічною сполукою платини чи комплексом платини, який відзначається протипухлинною активністю. Органічна сполука платини у цій специфікації стосується сполуки, що містить платину, яка містить платину в іонній формі. Органічні сполуки платини, яким надається перевага, включають, але не обмежуються, цисплатин; цис-диамін-діакво-платина (II)-іон; хлор(диетилентриамін)-платина (II) хлорид; дихлор(етилендиамін)-платина (II); диамін(1,1-циклобутандикарбоксилато-) платина (II) (карбоплатин); спіроплатин; іпроплатин; диамін(2-етилмалонато-) платина (II); етилен-диамінмалонато-платина (II); аква(1,2-диаміно-дициклогексан-) сульфатоплатина (II); аква(1,2диамінодициклогексан-) малонато-платина (II); (1,2-диаміноциклогексан-) малонато-платина (II); (4-карбоксифталато) (1,2-диаміноциклогексан) платина (II); (1,2-диаміноциклогексан)(ізоцитрато-) платина (II); (1,2-диаміноциклогексан-) оксалато-платина (II); ормаплатин; тетраплатин; карбоплатин, недаплатин та оксаліплатин, при цьому перевага надається карбоплатину чи оксаліплатину. Крім того, інші протипухлинні органічні сполуки платини, що згадуються у специфікації, є відомими та наявними у продажу, та/чи можуть бути виготовлені спеціалістом зі звичайною кваліфікацією у даній галузі з використанням традиційних способів. У деяких варіантах, протипухлинний агент є протипухлинним інгібітором тирозин кінази. Термін "інгібітор тирозин кінази" у цій специфікації стосується хімічної речовини, яка інгібує "тирозин кіназу", що передає λ-фосфатну групу ATP до гідроксилової групи специфічного тирозину в білку. Приклади протипухлинних інгібіторів тирозин кінази включають, але не обмежуються, гефітиніб, іматиніб, ерлотиніб, Сутент, Нексавар, Рецентин, ABT-869, та Акситиніб. У деяких варіантах, протипухлинний агент є антитілом чи зв’язаною часткою антитіла, які відзначаються протипухлинною активністю. У деяких варіантах, протипухлинний агент є моноклональним антитілом. Приклади у даній специфікації включають, але не обмежуються, абциксімаб, адалімумаб, алемтузумаб, базіліксімаб, бевацизумаб, цетуксімаб, даклізумаб, екулізумаб, ефалізумаб, ібрітумомаб, тіуксетан, інфліксімаб, муромонаб-CD3, наталізумаб, омалізумаб, палівізумаб, панітумумаб, ранібізумаб, гемтузумаб озогаміцин, рітуксімаб, тосітумомаб, трастузумаб, чи будь-які фрагменти антитіла, притаманні антигенам. У деяких варіантах, протипухлинний агент є інтерфероном. Такий інтерферон має протипухлинну активність, та є глікопротеїном, який виробляється та секретується більшістю тваринних клітин на вірусну інфекцію. Він має не тільки ефект, що пригнічує вірусне зростання, але також різні імунні ефекторні механізми, включаючи пригнічення росту клітин (зокрема, пухлинних клітин) та покращення активності природних клітин-кілерів, відповідно позначених як один з видів цитокіну. Приклади протипухлинних інтерферонів включають, але не обмежуються, інтерферон α, інтерферон α-2a, інтерферон α-2b, інтерферон β, інтерферон -1a та інтерферон -n1. У деяких варіантах, протипухлинний агент є модифікатором біологічного відгуку. Він зазвичай є родовим терміном для речовин чи ліків для модифікації захисних механізмів живих організмів чи біологічних відгуків, таких як виживання, ріст чи диференціація тканинних клітин, з метою їх спрямування на користь для людини проти пухлини, інфекції чи інших хвороб. Приклади модифікаторів біологічного відгуку включають, але не обмежуються, крестин, лентинан, сізіран, піцибаніл та убенімекс. У деяких варіантах, протипухлинні агенти включають, але не обмежуються, мітоксантрон, Lаспарагіназа, прокарбазин, дакарбазин, гідроксилкарбамід, пентостатин, третиноїн, алефацепт, дарбепоетин альфа, анастрозол, екземестан, бікалутамід, лейпрорелін, флутамід, фулвестрант, пегаптаніб октанатрій, денілейкін діфтітокс, алдеслейкін, тіротропін альфа, триоксид миш'яку, бортезоміб, capeцитабін та гозерелін. Вищеописані терміни "протипухлинний алкілувальний агент", "протипухлинний антиметаболіт", "протипухлинний антибіотик", "протипухлинний агент рослинного походження", "протипухлинний комплекс платини", "протипухлинна похідна камптотецину", "протипухлинний інгібітор тирозин кінази", "моноклональне антитіло", "інтерферон", "модифікатор біологічного 16 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 відгуку" та "інші протипухлинні агенти" є усі відомими та є або наявними у продажу, чи можуть бути виготовлені спеціалістом зі звичайною кваліфікацією у даній галузі у по суті відомі способи, чи добре відомі, чи традиційні способи. Спосіб приготування гефітинібу описано, наприклад, у патенті США № 5,770,599; спосіб приготування цетуксімабу описано, наприклад, у патенті WO 96/40210; спосіб приготування бевацизумабу описано, наприклад, у патенті WO 94/10202; спосіб приготування оксаліплатину описано, наприклад, у патенті США №№ 5,420,319 та 5,959,133; спосіб приготування гемцитабіну описано, наприклад, у патенті США №№ 5,434,254 та 5,223,608; та спосіб приготування камптотецину описано у патенті США №№ 5,162,532, 5,247,089, 5,191,082, 5,200,524, 5,243,050 та 5,321,140; спосіб приготування іринотекану описано, наприклад, у патенті США № 4,604,463; спосіб приготування Топотекану описано, наприклад, у патенті США № 5,734,056; спосіб приготування темозоломіду описано, наприклад, у патенті JP-B № 4-5029; та спосіб приготування рітуксімабу описано, наприклад, у патенті JP-W № 2-503143. Вищезгадані протипухлинні алкілувальні агенти є наявним у продажу, де представлені наступними прикладами: N-оксид азотистий іприт виробництва "Mitsubishi Pharma Corp." під назвою Нітрорін (торгова назва); циклофосфамід виробництва "Shionogi & Co., Ltd." під назвою Ендоксан (торгова назва); іфосфамід виробництва "Shionogi & Co., Ltd." під назвою Іфомід (торгова назва); мелфалан виробництва "GlaxoSmithKline Corp." під назвою Алкеран (торгова назва); бусульфан виробництва "Takeda Pharmaceutical Co., Ltd." під назвою Маблін (торгова назва); мітобронітол виробництва "Kyorin Pharmaceutical Co., Ltd." під назвою Мієброл (торгова назва); карбоквон виробництва "Sankyo Co., Ltd." під назвою Есквінон (торгова назва); тіотепа виробництва "Sumitomo Pharmaceutical Co., Ltd." під назвою Теспамін (торгова назва); ранімустін виробництва "Mitsubishi Pharma Corp." під назвою Цимерін (торгова назва); німустін виробництва "Sankyo Co., Ltd." під назвою Нідран (торгова назва); темозоломід виробництва "Schering Corp." під назвою Темодар (торгова назва); та кармустін виробництва "Guilford Pharmaceuticals Inc." під назвою Вафлі Гліадел (торгова назва). Вищезгадані протипухлинні антиметаболіти є наявними у продажу та представлені наступними прикладами: метотрексат виробництва "Takeda Pharmaceutical Co., Ltd." під назвою Метотрексат (торгова назва); 6-меркаптопурин рібозида виробництва "Aventis Corp." під назвою Тіоінозин (торгова назва); меркаптопурин виробництва "Takeda Pharmaceutical Co., Ltd." під назвою Лейкерин (торгова назва); 5-фторурацил виробництва "Kyowa Hakko Kogyo Co., Ltd." під назвою 5-FU (торгова назва); тегафур виробництва "Taiho Pharmaceutical Co., Ltd." під назвою Футрафул (торгова назва); доксифлурідин виробництва "Nippon Roche Co., Ltd." під назвою Фурутулон (торгова назва); кармур виробництва "Yamanouchi Pharmaceutical Co., Ltd." під назвою Ямафур (торгова назва); цитарабін виробництва "Nippon Shinyaku Co., Ltd." під назвою Цилоцид (торгова назва); цитарабін окфосфат виробництва "Nippon Kayaku Co., Ltd." під назвою Стразид (торгова назва); еноцитабін виробництва "Asahi Kasei Corp." під назвою Санрабін (торгова назва); S-1 виробництва "Taiho Pharmaceutical Co., Ltd." під назвою TS-1 (торгова назва); гемцитабін виробництва "Eli Lilly & Co." під назвою Гемзар (торгова назва); флударабін виробництва "Nippon Schering Co., Ltd." під назвою Флудара (торгова назва); та пеметрексед двонатрієвий виробництва "Eli Lilly & Co." під назвою Алімта (торгова назва). Вищезгадані протипухлинні антибіотики є наявними у продажу та представлені наступними прикладами: актиноміцин D виробництва "Banyu Pharmaceutical Co., Ltd." під назвою Космеген (торгова назва); доксорубіцин виробництва "Kyowa Hakko Kogyo Co., Ltd." під назвою адріацин (торгова назва); даунорубіцин виробництва "Meiji Seika Kaisha Ltd." під назвою Дауноміцин; неокарциностатин виробництва "Yamanouchi Pharmaceutical Co., Ltd." під назвою Неокарциностатин (торгова назва); блеоміцин виробництва "Nippon Kayaku Co., Ltd." під назвою Блео (торгова назва); пепроміцин виробництва "Nippon Kayaku Co, Ltd." під назвою Пепро (торгова назва); мітоміцин C виробництва "Kyowa Hakko Kogyo Co., Ltd." під назвою Мітоміцин (торгова назва); акларубіцин виробництва "Yamanouchi Pharmaceutical Co., Ltd." під назвою Аклацинон (торгова назва); пірарубіцин виробництва "Nippon Kayaku Co., Ltd." під назвою Пінорубіцин (торгова назва); епірубіцин виробництва "Pharmacia Corp." під назвою Фарморубіцин (торгова назва); зиностатін стімаламер виробництва "Yamanouchi Pharmaceutical Co., Ltd." під назвою Сманкс (торгова назва); ідарубіцин виробництва "Pharmacia Corp." під назвою Ідаміцин (торгова назва); сіролімус виробництва "Wyeth Corp." під назвою Рапамун (торгова назва); та валрубіцин виробництва "Anthra Pharmaceuticals Inc." під назвою Валстар (торгова назва). Вищезгадані протипухлинні агенти рослинного походження є наявними у продажу та представлені наступними прикладами: вінкрістин виробництва "Shionogi & Co., Ltd." під назвою Онковін (торгова назва); вінбластин виробництва "Kyorin Pharmaceutical Co., Ltd." під назвою 17 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 Вінбластин (торгова назва); віндезін виробництва "Shionogi & Co., Ltd." під назвою Філдезин (торгова назва); етопозид виробництва "Nippon Kayaku Co., Ltd." під назвою Ластет (торгова назва); собузоксан виробництва "Zenyaku Kogyo Co., Ltd." під назвою Перазолін (торгова назва); доцетаксел виробництва "Aventis Corp." під назвою Таксотер (торгова назва); паклітаксел виробництва "Bristol-Myers Squibb Co." під назвою Таксол (торгова назва); та вінорелбін виробництва "Kyowa Hakko Kogyo Co., Ltd." під назвою Навелбін (торгова назва). Вищезгадані протипухлинні комплекси платини є наявними у продажу та представлені наступними прикладами: цисплатин виробництва "Nippon Kayaku Co., Ltd." під назвою Ранда (торгова назва); карбоплатин виробництва "Bristol-Myers Squibb Co." під назвою Параплатин (торгова назва); недаплатин виробництва "Shionogi & Co., Ltd." під назвою Акупла (торгова назва); та оксаліплатин виробництва "Sani-Synthelabo Co." під назвою Елоксатин (торгова назва). Вищезгадані протипухлинні похідні камптотецину є наявними у продажу та представлені наступними прикладами: іринотекан виробництва "Yakult Honsha Co., Ltd." під назвою Кампто (торгова назва); Топотекан виробництва "GlaxoSmithKline Corp." під назвою Гікамтин (торгова назва); та камптотецин виробництва "Aldrich Хімічн Co., Inc.", США. Вищезгадані протипухлинні інгібітори тирозин кінази є наявними у продажу та представлені наступними прикладами: гефітиніб виробництва "AstraZeneca Corp." під назвою Іресса (торгова назва); іматиніб виробництва "Novartis AG" під назвою Глівек (торгова назва); та ерлотиніб виробництва "OSI Pharmaceuticals Inc." під назвою Тарцева (торгова назва). Вищезгадані моноклональні антитіла є наявними у продажу та представлені наступними прикладами: цетуксімаб виробництва "Bristol-Myers Squibb Co." під назвою Ербітукс (торгова назва); бевацизумаб виробництва "Genentech, Inc." під назвою Авастин (торгова назва); рітуксімаб виробництва "Biogen Idec Inc." під назвою Рітуксан (торгова назва); алемтузумаб виробництва "Berlex Inc." під назвою Кемпас (торгова назва); та трастузумаб виробництва "Chugai Pharmaceutical Co., Ltd." під назвою Герцептин (торгова назва). Вищезгадані інтерферони є наявними у продажу та представлені наступними прикладами: інтерферон α виробництва "Sumitomo Pharmaceutical Co., Ltd." під назвою Суміферон (торгова назва); інтерферон α-2a виробництва "Takeda Pharmaceutical Co., Ltd." під назвою Канферон-A (торгова назва); інтерферон α-2b виробництва "Schering-Plough Corp." під назвою Інтрон A (торгова назва); інтерферон β виробництва "Mochida Pharmaceutical Co., Ltd." під назвою IFN.бета. (торгова назва); інтерферон -1a виробництва "Shionogi & Co., Ltd." під назвою Імуномакс- (торгова назва); та інтерферон -n1 виробництва "Otsuka Pharmaceutical Co., Ltd." під назвою Oгамма (торгова назва). Вищезгадані модифікатори біологічного відгуку є наявними у продажу та представлені наступними прикладами: крестин виробництва "Sankyo Co., Ltd." під назвою крестин (торгова назва); лентинан виробництва "Aventis Corp." під назвою Лентинан (торгова назва); сізіран виробництва "Kaken Seiyaku Co., Ltd." під назвою Соніфіран (торгова назва); піцибаніл виробництва "Chugai Pharmaceutical Co., Ltd." під назвою Піцибаніл (торгова назва); та убенімекс виробництва "Nippon Kayaku Co., Ltd." під назвою Бестатин (торгова назва). Вищезгадані інші протипухлинні агенти є наявними у продажу та представлені наступними прикладами: мітоксантрон виробництва "Wyeth Lederle Japan, Ltd." під назвою Новантрон (торгова назва); L-аспарагіназа виробництва "Kyowa Hakko Kogyo Co., Ltd." під назвою Лейназа (торгова назва); прокарбазин виробництва "Nippon Roche Co., Ltd." під назвою Натулан (торгова назва); дакарбазин виробництва "Kyowa Hakko Kogyo Co., Ltd." під назвою Дакарбазин (торгова назва); гідроксилкарбамід виробництва "Bristol-Myers Squibb Co." під назвою Гідреа (торгова назва); пентостатин виробництва "Kagaku Oyobi Kessei Ryoho Kenkyusho" під назвою Корін (торгова назва); третиноїн виробництва "Nippon Roche Co., Ltd." під назвою Везаноїд (торгова назва); алефацепт виробництва "Biogen Idec Inc." під назвою Амевів (торгова назва); дарбепоетин альфа виробництва "Amgen Inc." під назвою Аранесп (торгова назва); анастрозол виробництва "AstraZeneca Corp." під назвою Арімідекс (торгова назва); екземестан виробництва "Pfizer Inc." під назвою Аромазин (торгова назва); бікалутамід виробництва "AstraZeneca Corp." під назвою Казодекс (торгова назва); лейпрорелін виробництва "Takeda Pharmaceutical Co., Ltd." під назвою Лейплін (торгова назва); флутамід виробництва "Schering-Plough Corp." під назвою Еулексін (торгова назва); фулвестрант виробництва "AstraZeneca Corp." під назвою Фаслодекс (торгова назва); пегаптаніб октанатрій виробництва "Gilead Sciences, Inc." під назвою Макуген (торгова назва); денілейкін діфтітокс виробництва "Ліганд Pharmaceuticals Inc." під назвою Онтак (торгова назва); алдеслейкін виробництва "Chiron Corp." під назвою Пролейкін (торгова назва); тіротропін альфа виробництва "Genzyme Corp." під назвою Тіроген (торгова назва); триоксид миш'яку виробництва "Клітина Therapeutics, Inc." під назвою Тризенокс (торгова 18 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 назва); бортезоміб виробництва "Millennium Pharmaceuticals, Inc." під назвою Велкад (торгова назва); capeцитабін виробництва "Hfmann-La Roche, Ltd." під назвою Кселода (торгова назва); та гозерелін виробництва "AstraZeneca Corp." під назвою Золадекс (торгова назва). Термін "протипухлинний агент", у тому сенсі, в якому використовується у специфікації, включає вищеописані протипухлинний алкілувальний агент, протипухлинний антиметаболіт, протипухлинний антибіотик, протипухлинний агент рослинного походження, протипухлинний комплексом платини, протипухлинну похідну камптотецину, протипухлинний інгібітор тирозин кінази, моноклональне антитіло, інтерферон, модифікатор біологічного відгуку, та інші протипухлинні агенти. Інші протипухлинні агенти чи протинеопластичні агенти можуть застосовуватися у поєднанні зі сполуками бензопірону. Такі придатні протипухлинні агенти чи протинеопластичні агенти включають, але не обмежуються, 13-цис-Ретиноєва кислота, 2-CdA, 2-Хлордеоксиаденозин, 5Азацитідін, 5-Фторурацил, 5-FU, 6-Меркаптопурин, 6-MP, 6-TG, 6-Тиогуанін, Абраксан, Аккутан, Актиноміцин-D, Адріаміцин, Адруцил, Агрилін, Ала-Корт, Алдеслейкін, Алемтузумаб, АЛІМТА, Алітретиноїн, Алкабан-AQ, Алкеран, повністю трансретиноєва кислота, Альфа Інтерферон, Альтретамін, Аметоптерін, Амифостин, Аміноглутетімід, Анагрелід, Анандрон, Анастрозол, Арабіносілцитозин, Ара-C, Аранесп, Аредіа, Арімідекс, Аромазин, Арранон, Триоксид миш'яку, Аспарагіназа, ATRA, Авастин, Азацитідін, BCG, BCNU, Бендамустін, Бевацизумаб, Бексаротен, БЕКСАР, Бікалутамід, БиКНУ, Бленоксан, Блеоміцин, Бортезоміб, Бусульфан, Бусульфекс, C225, Кальцій Лейковорин, Кемпас, Камптозар, Камптотецин-11, Capeцитабін, Карак, Карбоплатин, Кармустін, Вафлі Кармустін, Казодекс, CC-5013, CCI-779, CCNU, CDDP, СииНУ, Церубідін, Цетуксімаб, Хлорамбуцил, Цисплатин, Цитроворум-фактор, Кладрібін, Кортизон, Космеген, CPT-11, Циклофосфамід, Цитадрен, Цитарабін, Цитарабін Ліпозомал, Цитозар-U, Цитоксан, Дакарбазин, Дакоген, Dактиноміцин, Дарбепоетин Альфа, Дазатиніб, Дауноміцин, Даунорубіцин, Даунорубіцин Гідрохлорид, Даунорубіцин Ліпозомал, ДауноКсом, Декадрон, Deцитабін, Дельта-Кортеф, Дельтазон, Денілейкін Діфтітокс, ДепоЦит™, Дексаметазон, Дексаметазон Ацетат, Дексаметазон фосфат натрію, Дексазон, Дексразоксан, DHAD, DIC, Діодекс, Доцетаксел, Доксіл, Доксорубіцин, Доксорубіцин Ліпозомал, Дроксіа™, DTIC, DTIC-Дом, Дуралон, Ефудекс, Елігард, Елленс, Елоксатин, Елспар, Емцит, Епірубіцин, Епоетин Альфа, Ербітукс, Ерлотиніб, Ервінія L-аспарагіназа, Естрамустин, Етіол, Етопофос, Етопозид, фосфат Етопозиду, Еулексін, Евіста, Екземестан, Фарестон, Фаслодекс, Фемара, Філграстим, Флоксурідин, Флудара, Флударабін, Флюороплекс, Фторурацил, Фторурацил (крем), Флюоксіместерон, Флутамід, Фолієва кислота, FUDR, Фулвестрант, G-CSF, Гефітиніб, Гемцитабін, Гемтузумаб озогаміцин, Гемзар & Гемзар побічні ефекти - хіміотерапевтичні ліки, Глівек, Вафлі Гліадель, GM-CSF, Гозерелін, Гранулоцит - фактор, що стимулює колонії, Гранулоцит фактор, що стимулює колонії макрофагів, Галотестин, Герцептин, Гексадрол, Гексален, Hexaметилмеламін, HMM, Гікамтин, Гідреа, Гідрокорт ацетат, Гідрокортизон, Гідрокортизон фосфат натрію, Гідрокортизон сукцинат натрію, фосфат Гідрокортону, Гідроксилкарбамід, Ібрітумомаб, Ібрітумомаб Тіуксетан, Ідаміцин, Ідарубіцин, Іфекс , IFN-альфа, Іфосфамід, IL-11, IL-2, Іматиніб мезілат, Імідазол Карбоксамід, Інтерферон альфа, Інтерферон Альфа-2b (PEG кон’югат), Інтерлейкін - 2, Інтерлейкін-11, Інтрон A (інтерферон альфа-2b), Іпекка, Іринотекан, Ізотретиноїн, Іксабепілон, Іксемпра, Кідролаза (t), Ланакорт, Лапатиніб, Lаспарагіназа, LCR, Леналідомід, Летрозол, Лейковорин, Лейкеран, Лейкін, Лейпролід, Лейрокрістин, Лейстатин, Ліпозомал Ара-C, Ліквід пред, Ломустин, L-PAM, L-Сарколізин, Лупрон, Лупрон Депот, Матулан, Максідекс, Мехлоретамін, гідрохлорид Мехлоретаміну, Медралон, Медрол, Мегас, Мегестрол, ацетат Мегестролу, Мелфалан, Меркаптопурин, Месна, Меснекс, Метотрексат, Метотрексат натрій, Метилпреднізолон, Метікортен, Мітоміцин, Мітоміцин-C, Мітоксантрон, M-Преднізол, MTC, MTX, Мустарген, Мустін, Мутаміцин, Мілеран, Мілоцел, Мілотарг, Навелбін, Неларабін, Неозар, Ньюласта, Ньюмега, Ньюпоген, Нексавар, Ніландрон, Нілутамід, Ніпент, азотистий іприт, Новалдекс, Новантрон, Октреотид, Октреотид ацетат, Онкоспар, Онковін, Онтак, Онксал, Опревелкін, Орапред, Оразон, Оксаліплатин, Паклітаксел, Паклітаксел зі зв’язаним білком, Памідронат, Панітумумаб, Панретин, Параплатин, Педіапред, PEG Інтерферон, Пегаспагаза, Пегфілграстим, PEG-ІНТРОН, PEG-L-аспарагіназа, ПЕМЕТРЕКСЕД, Пентостатин, Фенілаланін мустард, Платінол, Платінол-AQ, Преднізолон, Преднізон, Прелон, Прокарбазин, ПРОКРІТ, Пролейкін, Проліфепроспан 20 з Кармустін імплантантом, Пурінетол, Ралоксифен, Ревлімід, Реуматрекс, Рітуксан, Рітуксімаб, Рерон-A (Інтерферон Альфа-2a), Рубекс, гідрохлорид Рубідоміцину, Сандостатин, Сандостатин LAR, Сарграмостім, Солу-Кортеф, Солу-Medrol, Сорафеніб, СПРАЙСЕЛ, STI-571, Стрептозоцин, SU11248, Сунітиніб, Сутент, Тамоксифен, Тарцева, Таргретин, Таксол, Таксотер, Темодар, Темозоломід, Темсіролімус, Теніпозид, ТЕСПА, Талідомід, Таломід, ТераЦис, Тиогуанін, 19 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 Тиогуанін Таблоїд, Тіофосфоамід, Тіоплекс, Тіотепа, TICE, Топозар, Топотекан, Тореміфен, Торісел, Тосітумомаб, Трастузумаб, Третиноїн, Трексалл™, Тризенокс, TSPA, TYKERB, VCR, Вектібікс, Вектібікс, Велбан, Велкад, ВеПезід, Везаноїд, Віадур, Відаза, Вінбластин, Вінбластин сульфат, Вінказар Pfs, Вінкрістин, Вінорелбін, Вінорелбін тартрат, VLB, VM-26, Воріностат, VP16, Вумон, Кселода, Занозар, Зевалін, Зінекард, Золадекс, Золедронова кислота, Золінза, Зомета. Антиметаболіти: Антиметаболіти є ліками, що впливають на нормальні метаболічні процеси клітин. Оскільки раку клітини швидко відтворюються, втручання у клітинний метаболізм впливає на раку клітини в більшому ступені ніж на клітини господаря. Гемцитабін (4-аміно-1-[3,3-дифтор-4-гідроксил-5® (гідроксилметил) тетрагідруран-2-іл]- 1H-пірімідин- 2-один; що є у продажу під назвою ГЕМЗАР виробництва "Eli Lilly and Company") є аналогом нуклеозиду, який взаємодіє з клітинним поділом, блокуючи синтез ДНК, що, таким чином, призводить до некрозу клітин, очевидно через апоптичний механізм. Дозування гемцитабіну має уточнюватися для конкретного пацієнта. Для дорослих, дозування гемцитабіну, що застосовується у поєднанні з агентом платини та 2 2 інгібітором PARP, буде в межах від близько 100 мг/м до близько 5000 мг/м , у межах від 2 2 2 близько 100 мг/м до близько 2000 мг/м , у межах від близько 750 до близько 1500 мг/м , від 2 2 2 близько 900 до близько 1400 мг/м чи близько 1250 мг/м . Величини мг/м стосуються кількості 2 гемцитабін у міліграмах (мг) на одиницю площини поверхні пацієнту у квадратних метрах (м ). Гемцитабін може вводитися шляхом внутрішньовенного (IV) вливання, наприклад, протягом періоду від близько 10 до близько 300 хвилин, від близько 15 до близько 180 хвилин, від близько 20 до близько 60 хвилин чи близько 10 хвилин. Термін “близько” у цьому контексті вказує на звичайне вживання слова "приблизно"; та у деяких варіантах вказує на допуск ± 10 % чи ± 5 %. Комплекси платини: Комплекси платини є фармацевтичними композиціями, що застосовуються для лікування раку, які містять принаймні один платиновий центр у комплексі з принаймні однією органічною групою. Карбоплатин ((SP-4-2)-Диамін[1,1-циклобутандикарбоксилато(2-)-O,O’ платина), такий як цисплатин та оксаліплатин, є ДНК алкілувальним агентом. Дозування карбоплатину визначається шляхом розрахунку площини на кривій зміни концентрації плазми крові (AUC) y способи, відомі спеціалістам у галузі хіміотерапії раку, беручи до уваги кліренс креатиніну пацієнта. У деяких варіантах, дозування карбоплатину для комбінованого лікування разом з антиметаболітом (наприклад, гемцитабіном) та інгібітором PARP (наприклад, 4-йодо-3нітробензамідом) розраховується таким чином, щоб забезпечити AUC близько 0.1-6 мг/мл на . . хвилину, близько 1-3 мг/мл на хвилину, від близько 1.5 до близько 2.5 мг/мл на хвилину, від . . близько 1.75 до близько 2.25 мг/мл на хвилину чи близько 2 мг/мл на хвилину (AUC 2, . наприклад, є умовним позначенням для 2 мг/мл на хвилину). У деяких варіантах, дозування карбоплатину для комбінованого лікування разом з таксаном (наприклад, паклітакселом чи доцетакселом), та інгібітором PARP (наприклад, 4-йодо-3-нітробензамідом) розраховується . . таким чином, щоб забезпечити AUC близько 0.1-6 мг/мл на хвилину, близько 1-3 мг/мл на . хвилину, від близько 1.5 до близько 2.5 мг/мл на хвилину, від близько 1.75 до близько 2.25 . . мг/мл на хвилину чи близько 2 мг/мл на хвилину (AUC 2, наприклад, умовним позначенням для 2 . мг/мл на хвилину). У деяких варіантах, відповідна доза карбоплатину становить від близько 10 2 2 до близько 400 мг/м , наприклад, близько 360 мг/м . Комплекси платини, такі як карбоплатин, зазвичай уводяться внутрішньовенно (IV) протягом періоду від близько 10 до близько 300 хвилин, від близько 30 до близько 180 хвилин, від близько 45 до близько 120 хвилин чи близько 60 хвилин. У цьому контексті, термін “близько” має своє звичне значення "приблизно". У деяких варіантах, близько означає ± 10 % чи ± 5 %. Інгібітори топоізомерази У деяких варіантах, способи відповідно до винаходу можуть включати призначення пацієнтові, хворому на рак молочної залози, ефективної кількості інгібітору PARP у поєднанні з інгібітором топоізомерази, наприклад, іринотеканом чи Топотеканом. Інгібітори топоізомерази є агентами, створеними для впливу на дію ферментів топоізомерази (топоізомерази I та II), що є ферментами, які контролюють зміни у структурі ДНК шляхом каталізування розриву та з'єднання фосфодиефірної основи ланцюгів ДНК під час нормального клітинного циклу. Топоізомерази набули популярності у якості цілей при лікуванні раку хіміотерапією. Вважається, що інгібітори топоізомерази блокують етап лігірування клітинного циклу, генеруючи одноланцюгові та дволанцюгові розриви, що порушують цілісність геному. Введення цих розривів зрештою призводить до апоптозу та некрозу клітин. Інгібітори топоізомерази часто поділяються за типом ферменту, який вони інгібують. Топоізомераза I, тип 20 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 топоізомерази, що найчастіше зустрічається в еукаріотах, представлена топотеканом, іринотеканом, луртотеканом та екзатеканом, кожен з яких є наявним у продажу. Топотекан ® виготовляється "GlaxoSmithKline" під торговою назвою Гікамтим . Іринотекан виготовляється ® "Pfizer" під торговою назвою Камптозар . Луртотекан може бути отриманий як препарат ліпозомал виробництва "Gilead Sciences Inc." Інгібітори топоізомерази мають призначатися в ефективній дозі. У деяких варіантах ефективна доза для лікування людини буде в межах від 2 близько 0.01 до близько 10 мг/м /на день. Лікування може повторюватися на щоденній, двотижневій, півтижневій, тижневій чи місячній основі. У деяких варіантах, період лікування може супроводжуватися перервою від одного до кількох днів, чи від одного до кількох тижнів. У поєднанні з інгібітором PARP-1, прийом інгібітору PARP-1 та інгібітору топоізомерази може призначатися в один день чи в окремі дні. Сполуки, що представляють тип II топоізомерази поділяються на два основні класи: топоізомерази отрути, які націлені на комплекс топоізомерази-ДНК, та топоізомерази інгібітори, які розривають каталітичний цикл. Топоізомерази отрути II включають, але не обмежуються, еукаріотичні інгібітори топоізомерази II типу (топо- II): амсакрин, етопозид, фосфат етопозиду, теніпозид та доксорубіцин. Ці препарати належать до протиракових терапевтичних засобів. Приклади інгібіторів топоізомерази включають ICRF-193. Ці інгібітори націлені на N-кінцевий домен ATPази топо- II та перешкоджають обороту топо- II. Структура цієї сполуки, зв’язаної з доменом ATPази, була визначена Классеном (Вісті Національної академії наук, 2004 р.), який показав, що препарат зв’язує у неконкурентний спосіб та обмежує можливості димеризації домену ATPази. Протиангіогенні агенти У деяких варіантах, способи відповідно до винаходу можуть включати призначення пацієнтові, хворому на рак молочної залози, ефективної кількості інгібітору PARP у поєднанні з протиангіогенним агентом. Інгібітор ангіогенезу є речовиною, яка інгібує ангіогенез (ріст нових кровоносних судин). Кожна солідна пухлина (на відміну від лейкемії) має потребу в утворенні кровоносних судин для підтримання її життєздатності при досягненні певного розміру. Пухлини можуть зростати тільки, якщо вони формують нові кровоносні судини. Зазвичай, кровоносні судини не утворюються деінде в тілі дорослої людини, якщо не відбувається активного процесу репарації тканини. Ангіостатичний агент ендостатин та пов’язані хімічні речовини можуть пригнічувати утворення кровоносних судин, перешкоджаючи необмеженому зростанню раку. Дослідження на пацієнтах засвідчило, що пухлина втрачала активність та залишалася такою навіть після припинення лікування ендостатином. Лікування має дуже незначну кількість побічних ефектів, але має дуже обмежену селективність. Інші ангіостатичні агенти, такі як талідомід та природні речовини на рослинній основі активно досліджуються. Відомі інгібітори включають препарат бевацизумаб (Авастин), який зв’язує судинний ендотеліальний фактору росту (VEGF), пригнічуючи його зв’язування з рецепторами, які сприяють ангіогенезу. Інші протиангіогенні агенти включають, але не обмежуються, карбоксиамідотриазол, TNF-470, CM101, IFN-альфа, IL-12, тромбоцитарний фактор-4, сурамін, SU5416, тромбоспондин, ангіостатичні стероїди + гепарин, інгібіторний фактор ангіогенезу хрящового походження, інгібітори матричної металопротеїнази, ангіостатин, ендостатин, 2метоксиестрадіол, текогалан, тромбоспондин, пролактин, αVβ3 інгібітори та ліномід. Her-2 націлена терапія У деяких варіантах, способи відповідно до винаходу можуть включати призначення пацієнтові, хворому на HER2 позитивний рак молочної залози, ефективної кількості інгібітору PARP у поєднанні з Герцептином. Герцептин (трастузумаб) є націленим терапевтичним засобом для застосування на ранній стадії HER2-позитивного раку молочної залози. Герцептин схвалено для ад'ювантного лікування HER2-гіперекспресивного, з позитивними лімфовузлами чи негативними лімфовузлами (ER/PRнегативним чи тільки однією ознакою високого ризику) раку молочної залози. Герцептин може застосовуватися у декілька різних способів: як частина курсу лікування, що включає доксорубіцин, циклофосфамід, та або паклітаксел, або доцетаксел; з доцетакселом та карбоплатином; чи як окремий агент, що застосовується після комплексної терапії на основі антрацикліну. Герцептин у поєднанні з паклітакселом схвалено для першочергового лікування HER2-гіперекспресивного метастатичного раку молочної залози. Герцептин у якості окремого агенту схвалено для лікування HER2-гіперекспресивного раку молочної залози у пацієнтів, які отримали один чи більше курсів хіміотерапії метастатичної хвороби. Лапатиніб чи лапатиніб дитосілат є перорально активним хіміотерапевтичним препаратом для лікування солідних пухлин, таких як рак молочної залози. Під час розробки він був відомий 21 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 як дрібна молекула GW572016. Пацієнтам, які відповідали специфічним індикативним критеріям, могли призначати лапатиніб у якості компоненту комплексної терапії раку молочної залози. Фармакологічно, лапатиніб є інгібітором подвійної тирозин кінази, який перешкоджає клітинним сигналам, що спричиняють рак. Лапатиніб застосовується для лікування раку молочної залози у жінок-пацієнтів, які мають HER2-позитивний прогресуючий рак молочної залози, що прогресував після попереднього лікування іншими хіміотерапевтичними агентами, такими як антрациклін, препарати на основі таксану, чи трастузумаб (Герцептин виробництва "Genentech"). Гормональна терапія У деяких варіантах, способи відповідно до винаходу можуть включати призначення пацієнтові, хворому на рак молочної залози, ефективної кількості інгібітору PARP у поєднанні з гормональною терапією. Існує ряд гормонів, які можуть приєднуватися до ракових клітин та можуть впливати на їх здатність до розмноження. Ціль гормональної терапії полягає у приєднанні, блокуванні чи усуненні гормонів. При раку молочної залози, жіночі гормони естроген та прогестерон можуть стимулювати ріст деяких клітин раку молочної залози. Таким чином, щодо цих пацієнтів застосовується гормональна терапія для блокування естрогену, що виникає в організмі природнім шляхом, та для перешкоджання росту раку. Існує два види гормональної терапії раку молочної залози: препарати, що інгібують естроген та прогестерон з метою запобігання стимулюванню росту клітин раку молочної залози, та препарати чи хірургія для зупинки продукування гормонів яєчником. Препарати загальної гормональної терапії, що застосовуються для лікування раку молочної залози, включають, але не обмежуються, Тамоксифен, Фарестон, Арімідекс, Аромазин, Фемара та Золадекс. Тамоксифен - антагоніст гормону Тамоксифен (наявний у продажу під назвою Нолвадекс) зменшує шанси рецидиву раку молочної залози на деяких ранніх стадіях та може запобігти розвитку раку в молочній залозі, що не була уражена. Тамоксифен також уповільнює чи зупиняє ріст ракових клітин, наявних в організмі. Крім того, тамоксифен може являти собою альтернативу обережного очікування чи профілактичної (превентивної) мастектомії у жінок з високим ризиком розвитку раку молочної залози. Тамоксифен належить до виду препаратів, які називають селективним модулятором естрогенових рецепторів (SERM). У молочній залозі він функціонує як антиестроген. Естроген стимулює ріст клітин раку молочної залози, а тамоксифен блокує приєднання естрогену до естрогенових рецепторів у цих клітинах. Діючи у такий спосіб, вважається, що ріст клітин раку молочної залози буде зупинено. Тамоксифен часто застосовується разом з хіміотерапією та іншими видами лікування раку молочної залози. Він розглядається як один з можливих варіантів у наступних випадках: лікування внутрішньопротокової карциноми in situ (DCIS) разом з реконструктивною хірургією молочної залози чи мастектомією; ад'ювантне лікування лобулярної карциноми in situ (LCIS) з метою зменшення ризику розвитку прогресуючого раку молочної залози; ад'ювантне лікування метастатичного раку молочної залози у чоловіків та жінок, хворих на рак, позитивний щодо естрогенового рецептору; лікування рецидиву раку молочної залози; профілактика раку молочної залози у жінок з високим ризиком розвитку раку молочної залози. Стероїдний та нестероїдний інгібітор ароматази Інгібітори ароматази (AI) належать до класу препаратів, які застосовуються для лікування раку молочної залози та раку яєчника у жінок постменопаузального віку, що блокують фермент ароматази. Інгібітори ароматази зменшують кількість естрогену у жінок постменопаузального віку, які мають рак молочної залози, позитивний щодо рецепторів гормону. За умови зниження естрогену в організмі, рецептори гормону отримують меншу кількість сигналів росту, а розвиток раку може бути уповільнений чи зупинений. Медичні препарати інгібітору ароматази включають Арімідекс (хімічна назва: анастрозол), Аромазин (хімічна назва: екземестан), та Фемару (хімічна назва: летрозол). Кожен з яких приймається по таблетці раз на день, до п'яти років. Але жінки з прогресуючою (метастатичною) хворобою, продовжують приймати препарат до тих пір, допоки він добре допомагає. AI класифікуються за двома типами: необоротні стероїдні інгібітори, такі як екземестан, що утворюють постійний зв'язок з комплексом ферменту ароматази; та нестероїдні інгібітори (такі як анастрозол, летрозол), що інгібують фермент шляхом оборотної конкуренції. Фулвестрант, також відомий як ICI 182,780, та "Фаслодекс" застосовуються для медикаментозного лікування метастатичного раку молочної залози, що є позитивним на рецептор гормону, у жінок постменопаузального віку, у яких хвороба прогресує після протиестрогенової терапії. Це антагоніст естрогенового рецептору без ефекту агоніста, який діє 22 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 як шляхом понижуючої регуляції, так і шляхом деградування естрогенового рецептору. Препарат вводиться шляхом разової місячної ін’єкції. Націлена терапія У деяких варіантах, способи відповідно до винаходу можуть включати призначення пацієнтові, хворому на рак молочної залози, ефективної кількості інгібітору PARP у поєднанні з інгібітором, націленим на рецептор фактору росту, включаючи, але не обмежуючись, рецептор епідермального фактору росту (EGFR) та рецептор інсуліноподібного фактору росту 1 (IGF1R). EGFR є гіперекспресивним у клітинах певних типів людських карцином, включаючи, але не обмежуючись, рак легенів та рак молочної залози. Високопроліферовані, інвазивні клітини раку молочної залози часто відзначаються патологічно високими рівнями EGFR, що як відомо контролюють як поділ клітин, так і їх міграцію. Інтерес до EGFR також посилюється наявністю та схваленням FDA (Управління контролю за продуктами и ліками (США)) специфічних інгібіторів тирозин кінази EGFR, наприклад, Гефітинібу. Інгібування EGFR є важливим протираковим лікуванням. Приклади інгібіторів EGFR включають, але не обмежуються, цетуксімаб, який є a химерним моноклональним антитілом, що вводиться шляхом внутрішньовенної ін'єкції для лікування раку, включаючи, але не обмежуючись, метастатичний колоректальний рак та рак голови та шиї. Панітумімаб є іншим прикладом інгібітору EGFR. Він є гуманізованим моноклональним антитілом проти EGFR. Панітумімаб проявив себе корисним та кращим за підтримуюче лікування, коли застосовується окремо у пацієнтів з прогресуючим раком товстої кишки та був схвалений FDA для такого застосування. Активація рецептору інсуліноподібного фактору росту (IGF1R) 1 типу стимулює проліферацію та інгібує апоптоз у різних типах клітин. У трансгенних мишей, у яких проявлявся конститутивно-активний IGF1R чи IGF-1, розвивалися пухлини молочної залози та спостерігалися підвищені рівні IGF1R на стадії первинного раку молочної залози (Яночко та інші. Дослідження раку молочної залози 2006 р.). Також зазначалося, що рецептор інсуліноподібного фактору росту I (IGF1R) та HER2 відзначаються важливими сигнальними взаємодіями при раку молочної залози. Специфічні інгібітори одного з цих рецепторів можуть перехресно інгібувати активність інших. Націленість на обидва рецептори забезпечує максимальне інгібування їх позаклітинної сигнально регульованої та направленої вниз кінази 1/2 та сигнальних шляхів AKT. Таким чином, подібні комбінації препаратів можуть бути клінічно корисними та можуть мати користь навіть у пухлинах, в яких препарати окремо є неактивними, та представлені наступними прикладами дії комбінації інгібіторів HER2/IGF1R на HER2 негіперекспресивні клітини MCF7 (Чакраборті AK, та інші, Дослідження раку, 1 березня 2008 р.; 68(5):1538-45). Одним з прикладів інгібітору IGF1R є CP-751871. CP-751871 є людським моноклональним антитілом, що селективно зв’язується з IGF1R, перешкоджаючи зв’язуванню IGF1 з рецептором та подальшому автофосфорилюванню рецептору. Інгібування автофосфорилювання IGF1R може призводити до скорочення експресії рецептору у клітинах пухлини, в яких проявляється IGF1R, до скорочення протиапоптичного ефекту IGF та інгібування росту пухлини. IGF1R є рецептором з тирозин кіназою, що проявляється у більшості пухлинних клітин, та є задіяним у мітогенезі, ангіогенезі та виживанні пухлинних клітин. Шлях PI3K/mTOR Дерегуляція шляху фосфатиділінозитол-3-кінази (PI3K) є поширеним явищем у раку людини, або шляхом інактивації супресор фосфатази пухлини та тензин гомолога, видаленого з хромосоми 10, або шляхом активації мутації p110-α. Ці мутації "гарячих точок" призводять до онкогенної активності ферменту та сприяють терапевтичному опору трастузумабу анти-HER2 антитіла. Шлях PI3K є, таким чином, привабливою ціллю для терапії раку. NVP-BEZ235, подвійний інгібітор PI3K та націлений на ссавців рапаміцин (mTOR) засвідчили інгібування активації направлених униз ефектoрів Akt, S6 рібозомал білку та 4EBP1 у клітинах раку молочної залози. NVP-BEZ235 інгібує вісь PI3K/mTOR та призводить до протипроліферативної та протипухлинної активності у ракових клітинах як з немутованим, так і з мутованим p110-α (Віолетта Серра, та інші. Дослідження раку 68, 8022-8030, 1 жовтня 2008 р.). Інгібітори Hsp90 Ці препарати націлені на білки теплового шоку 90 (hsp90). Hsp90 належать до одного з класів білків-шаперонів, звичайною функцією яких є допомога іншим білкам у набутті та підтримці форми, необхідної для цих білків, щоб виконувати свої функції. Шаперони функціонують, будучи у фізичному контакті з іншими білками. Hsp90 також може забезпечити виживання ракових клітин та навіть їх буйне розростання, незважаючи на генетичні дефекти, які зазвичай спричиняють відмирання таких клітин. Таким чином, блокування функції HSP90 та пов’язаних білків-шаперонів може спричиняти відмирання ракових клітини, особливо якщо функція блокування шаперонів комбінується з іншими стратегіями з метою блокування 23 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 виживання ракових клітин. Інгібітори тубуліну Тубуліни є білками, які формують мікротрубочки, що є ключовими компонентами клітинного цитоскелету (структурної мережі). Мікротрубочки потрібні для поділу клітин (мітозу), структури клітини, транспорту, сигналізації та рухливості. Враховуючи їх першочергове значення для мітозу, мікротрубочки стали важливою ціллю для протиракових препаратів - які часто визначаються як антимітотичні препарати, інгібітори тубуліну та агенти, націлені на мікротрубочки. Ці сполуки зв’язуються з тубуліном у мікротрубочках та перешкоджають проліферації ракових клітин, шляхом втручання у формування мікротрубочкок, що потрібні для поділу клітин. Таке втручання блокує послідовність клітинного циклу, яка веде до апоптозу. Інгібітори апоптозу Інгібітори апоптозу (IAP) належать до родини функціонально та структурно пов’язаних білків, спочатку охарактеризованих у Бакуловірусі, які виконують роль ендогенних інгібіторів апоптозу. Родина людських IAP складається з принаймні 6 членів, а гомологи IAP були ідентифіковані у чисельних організмів. 10058-F4 є c-Myc інгібітором, який спричиняє зупинку клітинного циклу та апоптозу. Він є проникаючим у клітину тіазолідіноном, який зокрема інгібує c-Myc - Max взаємодію та перешкоджає трансактивації c-Myc націленої генної експресії. 10058-F4 інгібує ріст клітин пухлини у c-Myc-залежний спосіб як in vitro, так і in vivo. BI-6C9 є tBid інгібітором та протиапоптичним. GNF-2 належить до нового класу Bcr-abl інгібіторів. GNF-2 має властивості до зв’язування з мірістоїл-зв'язуючою кишенею, алостеричною ділянкою, яка знаходиться на відстані від активної ділянки, що стабілізує неактивну форму кінази. Він інгібує Bcr-abl фосфориляцію з IC50 267 nM, але не інгібує панель 63 інших кіназ, включаючи природжений cAbl, та відзначається повною відсутністю токсичності щодо клітин, які не проявляють Bcr-Abl. GNF-2 засвідчує значний потенціал для нового класу інгібіторів стосовно дослідження активності Bcr-abl та лікування резистивної хронічної мієлогенної лейкемії (CML), що спричинена Bcr-Abl онкопротеїном. Піфітрин-α є оборотним інгібітором p53-опосередкованого апоптозу та p53-залежної генної транскрипції, таких як циклін G, p21/waf1, та mdm2 експресія. Піфітрин-α покращує виживання клітин після генотоксичного стресу, такого як УФ опромінення та лікування цитотоксичними сполуками, включаючи доксорубіцин, етопоксид, паклітаксел та цитозин-β-D-арабінуранозід. Піфітрин-α захищає мишей від летального -опромінення усього організму без підвищення захворюваності на рак. Інгібітори PARP: У деяких варіантах, даний винахід передбачає спосіб лікування раку молочної залози, що є негативним щодо принаймні одного з ER, PR чи HER2, шляхом призначення суб’єктові, який цього потребує, принаймні одного інгібітору PARP. У інших варіантах, даний винахід передбачає спосіб лікування раку молочної залози шляхом призначення суб’єктові, який цього потребує, принаймні одного інгібітору PARP у поєднанні з принаймні одним протипухлинним агентом, описаним у цій специфікації. Не маючи на увазі обмеження будь-яким конкретним механізмом дії, сполуки, описані у цій специфікації, вважаються такими, що мають протираку властивості завдяки модуляції активності полі- (ADP-рібози) полімерази (PARP). Цей механізм дії стосується здатності інгібіторів PARP зв’язувати PARP та зменшувати її активність. PARP каталізує конверсію βнікотинамід аденін динуклеотиду (NAD+) у нікотинамід та полі-ADP-рібозу (PAR). Як полі (ADPрібоза), так і PARP зв’язуються з регулюванням транскрипції, проліферацією клітин, геномною стабільністю та канцерогенезом (Бушар В.Ж. та інші Експериментальна Гематологія, Том 31, номер 6, червень 2003 р., стор. 446-454(9); Герцег З.; Ванг З.-К. Дослідження мутації / Основи та молекулярні механізми Мутагенезу, Том 477, Номер 1, 2 червень 2001, стор. 97-110(14)). Полі(ADP-рібоза) полімераза 1 (PARP1) є ключовою молекулою у репарації одноланцюгових розривів ДНК (SSB) (Де Мурсія Ж, та інші 1997, Вісник Національної академії наук США 94:73037307; Шрайбер В, Данцер Ф, Аме ЖК, Де Мурсія Ж (2006) Національний вісник з молекулярної клітинної біології 7:517-528; Ванг ЗО, та інші (1997) Генні дослідження, 11:2347-2358). Нокаут репарації SSB шляхом інгібування функції PARP1 стимулює дволанцюгові розриви ДНК (DSB), що може запускати синтетичну летальність ракових клітин з дефектною гомологічнонаправленою репарацією DSB (Брайант ХЕ, та інші (2005) Природа 434:913-917; Фармер Х, та інші (2005) Природа 434:917-921). BRCA1 та BRCA2 діють як невід'ємний компонент механіки гомологічної рекомбінації (HR) (Народ СA, Фоулкес ВД (2004) Національний вісник з раку 4:665-676; Гудмундсдотір K, Ашворт A (2006) Онкоген 25:5864-5874). Клітини, що є дефектними на BRCA1 чи BRCA2, мають дефект репарації дволанцюгових розривів (DSB) механізмом гомологічної рекомбінації (HR) шляхом генної конверсії (Фармер Х, 24 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 60 та інші (2005) Природа 434:917-921; Народ СA, Фоулкес ВД (2004) Національний вісник з раку 4:665-676; Гудмундсдотір K, Ашворт A (2006) Онкоген 25:5864-5874; Хелледей T, та інші (2008) Національний вісник з раку 8:193-204). Дефіцит або на білки BRCA1, або BRCA2, що є вразливими до раку молочної залози, спричиняє глибоку клітинну чутливість до інгібування активності полі(ADP-рібоза) полімерази (PARP), що призводить до зупинки клітинного циклу та апоптозу. Відзначалося, що критична роль BRCA1 та BRCA2 у репарації дволанцюгових розривів шляхом гомологічної рекомбінації (HR) є причиною, що лежить в основі цієї чутливості, а дефіцит RAD51, RAD54, DSS1, RPA1, NBS1, ATR, ATM, CHK1, CHK2, FANCD2, FANCA чи FANCC спричиняє таку чутливість (МакКабе Н. та інші "Дефіцит репарації пошкодження ДНК шляхом гомологічної рекомбінації та чутливість до інгібування полі(ADP-рібоза) полімерази", Дослідження раку 2006 р., том 66,8109-8115). Пропонувалося, що інгібування PARP1 може розглядатися як спеціальна терапія раку з дефектами у BRCA1/2 чи інших компонентів шляху HR (Хелледей T, та інші (2008) Національний вісник з раку 8:193-204). Тричі негативні пухлини становлять 15 % від усього раку молочної залози та часто містять у собі дефекти репарації дволанцюгових розривів ДНК шляхом гомологічної рекомбінації (HR), такі як дисфункція BRCA1 (Роттенберг С, та інші, Вісник Національної академії наук США, 4 листопада 2008 р.; 105(44):17079-84). Інгібування активності молекули PARP включає зниження активності цих молекул. Термін “інгібує” та його граматичні дієвідміни, такі як “інгібуючий” не має на меті вимагати повного зниження активності PARP. У деяких варіантах, таке зниження становить принаймні близько 50 %, принаймні близько 75 %, принаймні близько 90 %, чи принаймні близько 95 % від активності молекули за відсутності інгібуючого ефекту, наприклад, за відсутності інгібітору, такого як сполука нітробензаміду відповідно до винаходу. У деяких варіантах, інгібування стосується зниження активності, що піддається спостеріганню чи вимірюванню. У лікуванні за певними сценаріями, інгібування є достатнім для спричинення терапевтичної та/чи профілактичної користі стосовно стану, відносно якого застосовується лікування. Фраза “не інгібує” та її граматичні дієвідміни не потребують повної відсутності ефекту активності. Наприклад, вона стосується ситуацій, коли спостерігається менше ніж близько 20 %, менше ніж близько 10 %, та переважно менше ніж близько 5 % скорочення активності PARP у присутності інгібітору, такого як сполука нітробензаміду відповідно до винаходу. Полі (ADP-рібоза) полімераза (PARP) є необхідним ферментом у репарації ДНК, таким чином, відіграючи потенціальну роль в опорі хіміотерапії. Націленість на PARP потенційно вважається такою, що перериває репарацію ДНК, таким чином, покращуючи таксан опосередковану, антиметаболіт опосередковану, інгібітор топоізомерази опосередковану та інгібітор рецептору фактору росту, наприклад, інгібітор IGF1R опосередковану, та/чи комплекс платини опосередковану реплікацію та/чи репарацію ДНК у ракових клітинах. Інгібітори PARP також можуть бути дуже активними проти раку молочної залози з порушенням функції BRCA 1 та BRCA2, чи у пацієнтів з іншими дефектами шляху репарації ДНК. ER, PR, HER2-негативний первинний рак молочної залози демонструє підвищену функціональну активність PARP. Цей підтип раку молочної залози має у 9 разів підвищений ризик мутації BRCA-1 та може мати додаткові дефекти у шляхів репарації ДНК при анемії Фанконі. 4-йодо-3-нітробензамід (BA) є невеликою молекулою, що діє на клітини пухлини без виявлення токсичних ефектів у нормальних клітинах. Вважається, що BA досягає свого протинеопластичного ефекту шляхом інгібування PARP. BA є дуже ліпофільним та швидко поширюється у тканинах, включаючи мозок та цереброспінальну рідину (CSF). Він діє активно проти широкого діапазону ракових клітин in vitro, включаючи проти клітинних ліній з опором дії ліків. Спеціалісту у даній галузі визнає, що BA може вводитися у будь-якій фармацевтично прийнятній формі, наприклад, фармацевтично прийнятній формі солі, сольвату чи комплексу. Крім того, BA є здатним до таутомеризування у розчині, при цьому таутомерична форма BA також вважається такою, що підпадає під термін BA (чи еквівалент 4-йодо-3-нітробензаміду), разом із солями, сольватами чи комплексами. У деяких варіантах, BA може призначатися у поєднанні з циклодекстрином, таким як гідроксилпропілбетациклодекстрин. Проте, спеціаліст даної галузі визнає, що інші активні та неактивні агенти можуть комбінуватися з BA; та наведення BA, якщо інше не зазначене, включає усі його фармацевтично прийнятні форми. Базально-подібний рак молочної залози має високу схильність до метастазування у мозок; а BA є відомим як такий, що перетинає гемоенцефалітичний бар’єр. Не прив’язуючись до якоїсь конкретної теорії, вважається, що BA досягає свого протинеопластичного ефекту, інгібуючи функцію PARP. У деяких варіантах, BA може застосовуватися у лікуванні тричі негативних метастатичних пухлин молочної залози. У деяких варіантах, BA може застосовуватися у лікуванні пухлин молочної залози, у яких принаймні один з ER, PR та Her2 є негативним. У 25 UA 99934 C2 5 10 15 20 25 30 35 40 45 50 55 деяких варіантах, BA може застосовуватися у лікуванні пухлин молочної залози, у яких принаймні два ER, PR та Her2 є негативними, наприклад, ER-негативний, PR-негативний та Her2 позитивний; чи ER-позитивний, PR-негативний та Her-2 негативний; чи ER-негативний, PRпозитивний та Her-2 негативний. У деяких варіантах, BA може застосовуватися у лікуванні пухлин молочної залози у поєднанні з протипухлинним агентом. У деяких варіантах, протипухлинний агент є протипухлинним алкілувальним агентом, протипухлинним антиметаболіт, протипухлинними антибіотиками, протипухлинним агентом рослинного походження, протипухлинним комплексом платини, протипухлинною похідною камптотецину, протипухлинним інгібітором тирозин кінази, моноклональним антитілом, інтерфероном, модифікатором біологічного відгуку, гормональним протипухлинним агентом, протипухлинним вірусним агентом, інгібітором ангіогенезу, диференціюючим агентом чи іншим агентом, який відзначається протипухлинною активністю, чи їх фармацевтично прийнятною сіллю. У інших варіантах, BA може застосовуватися у лікуванні пухлин молочної залози у поєднанні з антиметаболітом, таким як гемцитабін, та комплексом платини, таким як карбоплатин. У ще інших варіантах, BA може застосовуватися у лікуванні метастатичних пухлин молочної залози у поєднанні з таксаном, таким як паклітаксел, та комплексом платини, таким як карбоплатин. У інших варіантах, BA може застосовуватися у лікуванні пухлин молочної залози у поєднанні з антиметаболітом, таким як гемцитабін, та комплексом платини, таким як карбоплатин. У ще інших варіантах, BA може застосовуватися у лікуванні метастатичних пухлин молочної залози у поєднанні з таксаном, таким як паклітаксел, та комплексом платини, таким як карбоплатин. У інших варіантах, BA може застосовуватися у лікуванні пухлин молочної залози у поєднанні з протиангіогенним агентом. У ще інших варіантах, BA може застосовуватися у лікуванні пухлин молочної залози у поєднанні з інгібітором топоізомерази, таким як іринотекан чи топотекан. У інших варіантах, BA може застосовуватися у лікуванні пухлин молочної залози у поєднанні з гормональною терапією. У ще інших варіантах, BA може застосовуватися у лікуванні пухлин молочної залози у поєднанні з інгібітором рецептору фактору росту, включаючи, але не обмежуючись, інгібітори EGFR чи IGF1R. У деяких варіантах, рак молочної залози є метастатичним тричі негативним раком молочної залози. У деяких варіантах, рак молочної залози є негативним щодо принаймні одного з ER, PR чи Her-2. У деяких варіантах, рак молочної залози є негативним щодо принаймні двох з ER, PR чи Her-2. У інших варіантах, рак молочної залози є негативним щодо принаймні одного з ER, PR чи Her-2, та позитивним щодо принаймні одного з ER, PR чи Her-2. У деяких варіантах, рак молочної залози є негативним щодо принаймні двох з ER, PR чи Her2, наприклад, ERнегативним, PR-негативним та Her-2 позитивним; чи ER-позитивним, PR-негативним та Her-2 негативним; чи ER-негативним, PR-позитивним та Her-2 негативним. Дозування інгібітору PARP може змінюватися залежно від віку, зросту, ваги, загального стану пацієнта, тощо. У деяких варіантах, дозування BA є у межах від близько 1 мг/кг до близько 100 мг/кг, від близько 2 мг/кг до близько 50 мг/кг, близько 2 мг/кг, близько 4 мг/кг, близько 6 мг/кг, близько 8 мг/кг, близько 10 мг/кг, близько 12 мг/кг, близько 15 мг/кг, близько 20 мг/кг, близько 25 мг/кг, близько 30 мг/кг, близько 35 мг/кг, близько 40 мг/кг, близько 50 мг/кг, близько 60 мг/кг, близько 75 мг/кг, близько 90 мг/кг, від близько 1 до близько 25 мг/кг, від близько 2 до близько 70 мг/кг, від близько 4 до близько 100 мг, від близько 4 до близько 25 мг/кг, від близько 4 до близько 20 мг/кг, від близько 50 до близько 100 мг/кг чи від близько 25 до близько 75 мг/кг. BA може вводитися внутрішньовенно, наприклад шляхом вливання IV протягом від близько 10 до близько 300 хвилин, від близько 30 до близько 180 хвилин, від близько 45 до близько 120 хвилин чи близько 60 хвилин (тобто, близько 1 години). У деяких варіантах, BA може вводитися альтернативно перорально. У цьому контексті, термін “близько” має звичне значення "приблизно". У деяких варіантах, близько означає ± 10 % чи ± 5 %. Синтез BA (4-йодо-3-нітробензамід) описано у патенті Сполучених Штатів № 5,464,871, що включено у повному об’ємі до цієї специфікації шляхом посилання. BA може бути приготовано у концентраціях 10 мг/мл та може бути упаковано у зручній формі, наприклад у 10 мл флаконах. Метаболіти BA: У тому значенні, в якому вживається у даній специфікації, “BA” означає 4-йодо-3нітробензамід; “BNO” означає 4-йодо-3-нітроsoбензамід; “BNHOH” означає 4-йодо-3гідроксиламінобензамід. Сполуки-попередники, корисні для даного винаходу мають Формулу (Ia) 26 UA 99934 C2 O C NH2 R5 R1 (Ia) R4 R2 R3 5 10 де R1, R2, R3, R4 та R5 незалежно обрані серед групи, що складається з водню, гідроксилу, аміно-, нітро-, йодо-, (C1-C6) алкілу, (C1-C6) алкоксилу, (C3-C7) циклоалкілу та фенілу, де принаймні два з п'яти замісників R1, R2, R3, R4 та R5 є завжди воднем, принаймні один з п'яти замісників є завжди нітро-, та принаймні один з замісників, розміщених суміжно до нітро-, є завжди йодо-, та їх фармацевтично прийнятних солей, сольватів, ізомерів, таутомерів, метаболітів, аналогів чи проліків. R1, R2, R3, R4 та R5 також можуть бути галоїдом, таким як хлор, фтор, чи бромо- замісники. Сполукою-попередником, якій надається перевага, формули Ia є: Деякі метаболіти, що є корисними для даного винаходу, мають Формулу (IIa): 15 O C R5 NH2 R1 (IIa) R4 R2 R3 20 де або: (1) принаймні один із замісників R1, R2, R3, R4 та R5 є завжди замісником, що містить сірку, та решта замісників R1, R2, R3, R4 та R5 незалежно обрані серед групи, що складається з водню, гідроксилу, аміно-, нітро-, йодо-, бромо-, фтор-, хлор-, (C1-C6) алкілу, (C1-C6) алкоксилу, (C3-C7) циклоалкілу та фенілу, де принаймні два з п'яти замісників R1, R2, R3, R4 та R5 є завжди воднем; чи (2) принаймні один з замісників R1, R2, R3, R4 та R5 не є замісником, що містить сірку, та принаймні однин з п'яти замісників R1, R2, R3, R4 та R5 є завжди йодо-, та де зазначений йодоє завжди суміжним з групою R1, R2, R3, R4, чи R5, що є або нітро-, нітрозо-, гідроксиламіновою, 27 UA 99934 C2 5 гідроксиловою чи аміновою групою; та їх фармацевтично прийнятною сіллю, сольватами, ізомерами, таутомерами, метаболітами, аналогами чи проліками. У деяких варіантах, сполуки (2) є такими, що йодова група є завжди суміжною з групою R 1, R2, R3, R4 чи R5, що є нітрозо-, гідроксиламіновою, гідроксиловою чи аміновою групою. У деяких варіантах, сполуки (2) є такими, що йодова група є завжди суміжною з групою R1, R2, R3, R4 чи R5, що є нітрозо-, гідроксиламіновою чи аміновою групою. Наступні композиції є сполуками метаболіту, яким надається перевага, кожна з яких представлена хімічною формулою: H2N H2N O O O OH N S N O S O I O HN O HN HN O HN O H2N H2N O O HO 10 OH OH HO O O MS601 MS472 H2N O O N O S O NH OH O MS328 28
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod of treating breast cancer with use of 4-iodo-3-nitrobenzamide in combination with anti-tumor agents
Автори англійськоюSherman, Barry, M., Bradley, Charles, Ossovskaya, Valeria, S.
Назва патенту російськоюЛечение рака молочной железы с помощью соединения 4-йодо-3-нитробензамида в комбинации с противоопухолевыми средствами
Автори російськоюШерман Барри М., Бредли Чарльз, Оссовская Валерия С.
МПК / Мітки
МПК: A61K 31/7068, A61K 31/282, A61K 31/166, A61P 35/00
Мітки: 4-йодо-3-нітробензаміду, сполуки, лікування, залози, допомогою, комбінації, молочної, протипухлинними, засобами, раку
Код посилання
<a href="https://ua.patents.su/76-99934-likuvannya-raku-molochno-zalozi-za-dopomogoyu-spoluki-4-jjodo-3-nitrobenzamidu-v-kombinaci-z-protipukhlinnimi-zasobami.html" target="_blank" rel="follow" title="База патентів України">Лікування раку молочної залози за допомогою сполуки 4-йодо-3-нітробензаміду в комбінації з протипухлинними засобами</a>
Попередній патент: Лікування аутоімунних захворювань у пацієнта з неадекватною відповіддю на інгібітор tnf-альфа
Наступний патент: Класифікація точок доступу з використанням пілот-ідентифікаторів
Випадковий патент: Спосіб лікування пухлинних утворень