Антрациклінові дисахариди, спосіб їх одержання та фармацевтичні композиції, які їх містять
Номер патенту: 41951
Опубліковано: 15.10.2001
Автори: Аркамоне Федеріко Марія, Аніматі Фабіо, Чіполлоне Амалія, Ломбарді Паоло
Формула / Реферат
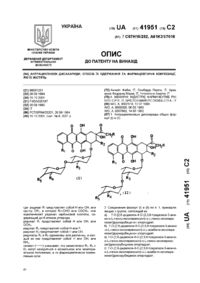
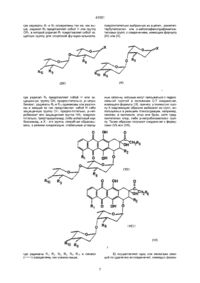
1. Антрациклиновые дисахариды общих формул (I) и (II):
где:
радикал R представляет собой Н или ОН, или группу OR7, в которой R7=СНО или СОСН3, или ациклический радикал карбоновой кислоты, содержащий до 6 атомов углерода;
радикал R1 представляет собой Н или ОН, или ОСН3;a
радикал R2 представляет собой Н или F;
радикал R3 представляет собой Н или ОН;
радикалы R4 и R5 одинаковы или различны, и каждый из них представляет собой Н или ОН, или NH2;
символ (~~~~) указывает, что заместители R3, R4 и R5 могут находиться в аксиальном или экваториальном положении, и их фармацевтически приемлемые соли.
2. Соединения формул (I) и (II) по п. 1, принадлежащие к группе, состоящей из:
а) 7-O-[2,6-дидеокси-4-O-(2,3,6-тридеокси-3-амино-a-L-ликсо-эксопиранозил)-a-L-ликсо-эксопиранозил]даунорубицинон хлоргидрат;
б) 7-O-[2,6-дидеокси-4-O-(2,3,6-тридеокси-3-амино-a-L-ликсо-эксопиранозил)-a-L-арабино-эксопиранозил]даунорубицинон хлоргидрат;
в) 7-O-[2,6-дидеокси-4-O-(2,3,6-тридеокси-3-амино-a-L-ликсо-эксопиранозил)-a-L-ликсо-эксопиранозил]доксорубицинон хлоргидрат;
г) 7-O-[2,6-дидеокси-4-O-(2,3,6-тридеокси-3-амино-a-L-ликсо-эксопиранозил)-a-L-арабино-эксопиранозил]доксорубицинон хлоргидрат;
д) 7-O-[2,6-дидеокси-4-O-(2,3,6-тридеокси-3-амино-a-L-ликсо-эксопиранозил)-a-L-арабино-эксопиранозил]-4-деметокси-даунорубицинон хлоргидрат;
е) 7-O-[2,6-дидеокси-4-O-(2,3,6-тридеокси-3-амино-a-L-ликсо-эксопиранозил)-a-L-ликсо-эксопиранозил]-4-деметокси-даунорубицинон хлоргидрат;
ж) 7-O-[2,6-дидеокси-4-O-(2,3,6-тридеокси-3-амино-a-L-ликсо-эксопиранозил)-a-L-ликсо-эксопиранозил]-4-деметокси-доксорубицинон хлоргидрат;
з) 7-O-[2,6-дидеокси-4-O-(2,3,6-тридеокси-3-амино-a-L-ликсо-эксопиранозил)-a-L-арабино-эксопиранозил]-4-деметокси-доксорубицинон хлоргидрат;
и) 7-O-[2,6-дидеокси-4-O-(2,3,4,6-тетрадеокси-4-амино-a-L-эритро-эксопиранозил)-a-L-ликсо-эксопиранозил]даунорубицинон хлоргидрат;
к) 7-O-[2,6-дидеокси-4-O-(2,3,4,6-тетрадеокси-4-амино-a-L-эритро-эксопиранозил)-a-L-ликсо-эксопиранозил]-4-деметокси-даунорубицинон хлоргидрат;
л) 7-O-[2,6-дидеокси-4-O-(2,3,4,6-тетрадеокси-4-амино-a-L-эритро-эксопиранозил)-a-L-ликсо-эксопиранозил]доксорубицинон хлоргидрат;
м) 7-O-H,6-дидеокси-4-O-(2,3,4,6-тетрадеокси-4-амино-a-L-эритро-эксопиранозил)-a-L-ликсо-эксопиранозил]-4-деметокси-доксорубицинон хлоргидрат;
н) 7-O-[2,б-дидеокси-4-O-(2,3,6-тридеокси-3-амино-a-L-ликсо-эксопиранозил)-a-L-ликсо-эксопиранозил]-4-деметокси-8-фтордаунорубицинон хлоргидрат;
о) 7-O-[2,6-дидеокси-4-O-(2,3,6-тридеокси-3-амино-a-L-ликсо-эксопиранозил)-a-L-ликсо-эксопиранозил]-4-деметокси-8-фтордоксорубицинон хлоргидрат.
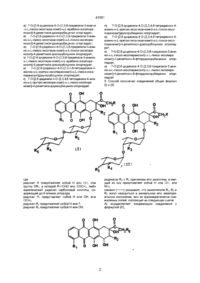
3. Способ получения соединений общих формул (I) и (II):
где:
радикал R представляет собой Н или ОН, или группу OR7, в которой R7=CHO или СОСН3, либо ациклический радикал карбоновой кислоты, содержащий до 6 атомов углерода;
радикал R1 представляет собой Н или ОН, или ОСН3;
радикал R2 представляет собой Н или F;
радикал R3 представляет собой Н или ОН;
радикалы R4 и R5 одинаковы или различны, и каждый из них представляет собой Н или ОН, или NH2;
символ (~~~~) указывает, что заместители R3, R4 и R5 могут находиться в аксиальном или экваториальном положении, или их фармацевтически приемлемых солей, состоящий из следующих шагов:
А) осуществляют конденсацию соединения с формулой (III),
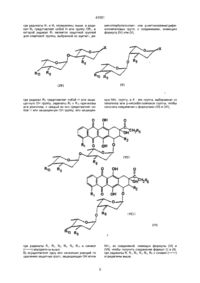
где радикалы R1 и R2 определены выше, а радикал R6 представляет собой Н или группу OR7, в которой радикал R7 является защитной группой для спиртовой группы, выбранной из ацетил-, диметилтербутилсилил- или р-метоксифенилдифенилметиловых групп, с соединением, имеющим формулу (IV) или (V),
где радикал R8 представляет собой Н или защищенную ОН группу, радикалы R9 и R10 одинаковы или различны, и каждый из них представляет собой Н или защищенную ОН группу, или защищенную NH группу, а Х - это группа, выбираемая из галогенов или р-нитробензоилокси группы, чтобы получить соединения с формулами (VI) и (VII),
где радикалы R1, R2, R6, R8, R9, R10 и символ (~~~~) определены выше;
Б) осуществляют одну или несколько реакций по удалению защитных групп, защищающих ОН и/или NH2, из соединений, имеющих формулы (VI) и (VII), чтобы получить соединения формул (I) и (II), где радикалы R, R1, R2, R3, R4, R5 и символ (~~~~) определены выше;
В) осуществляют, если возможно, превращение соединений, формул (I) и (II) в их фармацевтически приемлемые соли.
4. Способ получения соединений формулы (I) и (II) по п. 1, где R1, R2, R3, R4, R5 определены выше, а радикал R представляет собой группу ОН, или их фармацевтически приемлемых солей, состоящий из следующих шагов:
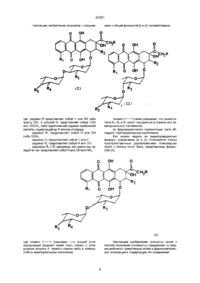
А) осуществляют бромирование углерода, находящегося в положении 14 в соединениях формул (I) и (II), или в их фармацевтически приемлемых солях, где радикалы R1, R2, R3, R4, R5 и символ (~~~~) определены выше, а радикал R представляет собой Н;
Б) осуществляют гидролиз полученных 14-бромпроизводных для получения соединений формул (I) и (II), где радикалы R1, R2, R3, R4, R5 определены выше, а радикал R представляет собой группу ОН.
5. Способ по п. 3, отличающийся тем, что в соединениях формул (IV) или (V), в стадии А) радикал R8 представляет собой Н или защищенную ОН группу, например, р-нитробензоат, радикалы R9 и R10 одинаковы или различны, и каждый из них представляет собой Н или защищенную группу ОН, например, р-нитробензоил- или группу NH2, защищенную посредством трифторацетил- или аллиловой оксикарбонильной группы.
6. Способ по п. 3, отличающийся тем, что стадию А) осуществляют в присутствии конденсирующего средства, выбранного из группы, состоящей из трифлата серебра, перхлората серебра, смеси окиси ртути и бромида ртути, триметилсилилтрифлата, р-толуолсульфокислоты, трифторуксусной кислоты, галоидных соединений бора, четыреххлористого олова, четыреххлористого титана или ионообменных смол, типа Amberlite®.
7. Способ по п. 3 или 6, отличающийся тем, что соединение, имеющее формулу (III), растворяют в инертном органическом растворителе, а конденсацию осуществляют в присутствии активированного цеолита в качестве дегидратирующего вещества.
8. Способ по п. 6 или 7, отличающийся тем, что в реакционную смесь в процессе конденсации добавляют органическое основание, выбранное из группы, состоящей из пиридина, коллидина, N,N-диметиламинопиридина, триэтиламина или 1,8-бис-(диметиламино)-нафталина.
9. Способ по п. 3, отличающийся тем, что галогеном, упомянутым на стадии А), является хлор или бром.
10. Способ по п. 3, отличающийся тем, что на стадии Б) трифторацетильную группу, которая защищает группу NH2, и/или р-нитробензоил- и/или ацетильную группы, которые защищают группы ОН, удаляют, воздействуя неорганическим основанием, выбранным из группы, состоящей из гидроокисей и карбонатов натрия, калия, лития или бария.
11. Способ по п. 3, отличающийся тем, что на стадии Б) удаляют аллиловую оксикарбонильную группу, защищающую группу NH2, оказывая воздействие органическими комплексами никеля или палладия.
12. Способ по п. 3, отличающийся тем, что на стадии Б) удаляют метоксифенилдифенилметильную группу, защищающую группу ОН, оказывая воздействие органической кислотой.
13. Способ по п. 12, отличающийся тем, что упомянутой органической кислотой является уксусная кислота.
14. Способ по п. 3, отличающийся тем, что на стадии Б) удаляют диметилтербутилсилиловую группу, защищающую группу ОН, в присутствии фторида тетрабутиламмония.
15. Способ по п. 3, отличающийся тем, что на стадии В) соединения формул (I) и (ІІ) превращают в фармацевтически приемлемые хлоргидраты.
16. Способ по п. 4, отличающийся тем, что на стадии А) осуществляют бромирование бромом в хлороформе.
17. Способ по п. 4, отличающийся тем, что на стадии Б) осуществляют гидролиз посредством муравьинокислого натрия.
18. Фармацевтическая композиция, содержащая в качестве активного ингредиента, по меньшей мере одно соединение по любому из пп. 1 или 2, или их фармацевтически приемлемые соли, в сочетании с фармацевтически приемлемьми носителем или растворителем.
19. Соединения по любому из пп. 1 или 2, или их фармацевтически приемлемые соли в качестве противораковых препаратов.
20. Фармацевтическая композиция, применяемая в качестве противоракового средства, содержащая в качестве активного ингредиента, по меньшей мере одно соединение по любому из пп. 1 или 2, или его фармацевтически приемлемую соль, в сочетании с фармацевтически приемлемым носителем или растворителем.
Текст
1 Антрацит и новые дисахариды общих формул (I) и (II) (21)96031231 (22)26 09 1994 (24)15 10 2001 (31)FI93A000187 (32)30 09 1993 (33) IT (86) РСТ/ЕР94/03201, 26 09 1994 (46) 15 10 2001, Бюл № 9, 2001 р о он О О о где радикал R представляет собой Н или ОН, или группу OR7, в которой R7=CHO или СОСНз, или ациклический радикал карбоновой кислоты, содержащий до 6 атомов углерода, радикал Ri представляет собой Н или ОН, или ОСНз, радикал R2 представляет собой Н или F, радикал R3 представляет собой Н или ОН, радикалы R4 и Rs одинаковы или различны, и каждый из них представляет собой Н или ОН, или NH2, символ ( ) указывает, что заместители R3, R4 и Rs могут находиться в аксиальном или экваториальном положении, и их фармацевтически приемлемые соли ю 2 Соединения формул (I) и (II) по п 1, принадлежащие к группе, состоящей из а) 7-О-[2,6-дидеокси-4-О-(2,3,6-тридеокси-3-амино-а-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]даунорубицинон хлоргидрат, б) 7-О-[2,6-дидеокси-4-О-(2,3,6-тридеокси-3-амино -а-Ь-ликсо-эксопиранозилЭ-а-Ьарабино-эксопиранозил]даунорубицинон хлоргидрат, в) 7-О-[2,6-дидеокси-4-О-(2,3,6-тридеокси-3-аминоа-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]доксорубицинон хлоргидрат, г) 7-О-[2,6-дидеокси-4-О-(2,3,6-тридеокси-3-аминоа-Ьликсо-эксопиранозилЭ-а-Ьарабино-эксопиранозил]доксорубицинон хлоргидрат, ю 41951 д) 7-О-[2,6-дидеокси-4-О-(2,3,6-тридеокси-3-амино -а-Ь-ликсо-эксопиранозилЭ-а-Ьарабино-эксопиранозил]-4-деметокси-даунорубицинон хлоргидрат, е) 7-О-[2,6-дидеокси-4-О-(2,3,6-тридеокси-3-амино-а-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]-4-деметокси-даунорубицинон хлоргидрат, ж) 7-О-[2,6-дидеокси-4-О-(2,3,6-тридеокси-3-амино-а-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]-4-деметокси-доксорубицинон хлоргидрат, з) 7-О-[2,6-дидеокси-4-О-(2,3,6-тридеокси-3-аминоа-Ьликсо-эксопиранозилЭ-а-Ьарабино-эксопиранозил]-4-деметокси-доксорубицинон хлоргидрат, и) 7-О-[2,6-дидеокси-4-О-(2,3,4,6-тетрадеокси-4амино-а-Ьэритро-эксопиранозилЭ-а-Ьликсо-эксопиранозил]даунорубицинон хлоргидрат, к) 7-О-[2,6-дидеокси-4-О-(2,3,4,6-тетрадеокси-4-амино-а-1-эритро-эксопиранозил)-а-Ьликсо-эксопиранозил]-4-демєтокси-даунорубицинон хлоргидрат, л) 7-О-[2,6-дидеокси-4-О-(2,3,4,6-тетрадеокси-4амино-а-Ьэритро-эксопиранозилЭ-а-Ьликсо-эксопиранозил]доксорубицинон хлоргидрат, м) 7-О-[2,6-дидеокси-4-О-(2,3,4,6-тетрадеокси-4амино-а-Ьэритро-эксопиранозилЭ-а-Ьликсо-эксопиранозил]-4-деметокси-доксорубицинон хлоргидрат, н) 7-О-[2,6-дидеокси-4-О-(2,3,6-тридеокси-3-амино-а-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]-4-деметокси-8-фтордаунорубицинон хлоргидрат, о) 7-О-[2,6-дидеокси-4-О-(2,3,6-тридеокси-3-амино-а-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]-4-деметокси-8-фтордоксорубицинон хлоргидрат 3 Способ получения соединений общих формул (I) и (II) он ii) где радикал R представляет собой Н или ОН, или группу OR7, в которой R7=CHO или СОСНз, либо ациклический радикал карбоновой кислоты, содержащий до 6 атомов углерода, радикал Ri представляет собой Н или ОН, или ОСНз, радикал R2 представляет собой Н или F, радикал R3 представляет собой Н или ОН, о радикалы R4 и Rs одинаковы или различны, и каждый из них представляет собой Н или ОН, или NH2, символ ( ) указывает, что заместители R3, R4 и Rs могут находиться в аксиальном или экваториальном положении, или их фармацевтически приемлемых солей, состоящий из следующих шагов А) осуществляют конденсацию соединения с формулой (III), он он он 41951 где радикалы Ri и F 2 определены выше, а ради? кал F 6 представляет собой Н или группу OR7, в ? которой радикал R7 является защитной группой для спиртовой группы, выбранной из ацетил-, ди метилтербутилсилил- или р-метоксифенилдифенилметиловых групп, с соединением, имеющим формулу (IV) или (V), где радикал Rs представляет собой Н или защищенную ОН группу, радикалы Rg и R-ю одинаковы или различны, и каждый из них представляет собой Н или защищенную ОН группу, или защищен ную NH2 группу, а X - это группа, выбираемая из галогенов или р-нитробензоилокси группы, чтобы получить соединения с формулами (VI) и (VII), (VII) где радикалы Ri, R2, R6, Rs, R9, R10 и символ ( ) определены выше, Б) осуществляют одну или несколько реакций по удалению защитных групп, защищающих ОН и/или NH2, из соединений, имеющих формулы (VI) и (VII), чтобы получить соединения формул (I) и (II), где радикалы R, Ri, R2, R3, R4, R5 и символ ( ) определены выше, 41951 В) осуществляют, если возможно, превращение соединений, формул (I) и (II) в их фармацевтически приемлемые соли 4 Способ получения соединений формулы (I) и (II) по п 1, где R-i, F?2, R3, F?4, R5 определены выше, а радикал R представляет собой группу ОН, или их фармацевтически приемлемых солей, состоящий из следующих шагов А) осуществляют бромирование углерода, находящегося в положении 14 в соединениях формул (I) и (II), или в их фармацевтически приемлемых солях, где радикалы Ri, R2, R3, R4, R5 и символ ( ) определены выше, а радикал R представляет собой Н, Б) осуществляют гидролиз полученных 14бромпроизводных для получения соединений формул (I) и (II), где радикалы Ri, R2, R3, R4, R5 определены выше, а радикал R представляет собой группу ОН 5 Способ по п 3, отличающийся тем, что в соединениях формул (IV) или (V), в стадии А) радикал Rs представляет собой Н или защищенную ОН группу, например, р-нитробензоат, радикалы Rg и R-т одинаковы или различны, и каждый из них представляет собой Н или защищенную группу ОН, например, р-нитробензоилили группу NH2, защищенную посредством трифторацетил- или аллиловой оксикарбонильной группы 6 Способ по п 3, отличающийся тем, что стадию А) осуществляют в присутствии конденсирующего средства, выбранного из группы, состоящей из трифлата серебра, перхлората серебра, смеси окиси ртути и бромида ртути, триметилсилилтрифлата, р-толуолсульфокислоты, трифторуксусной кислоты, галоидных соединений бора, четыреххлористого олова, четыреххлористого титана или ионообменных смол, типа Amberhte® 7 Способ по п 3 или 6, отличающийся тем, что соединение, имеющее формулу (III), растворяют в инертном органическом растворителе, а конденсацию осуществляют в присутствии активированного цеолита в качестве дегидратирующего вещества 8 Способ по п 6 или 7, отличающийся тем, что в реакционную смесь в процессе конденсации добавляют органическое основание, выбранное из группы, состоящей из пиридина, коллидина, N,Nдиметиламинопиридина, триэтиламина или 1,8бис-(диметиламино)-нафталина 9 Способ по п 3, отличающийся тем, что галогеном, упомянутым на стадии А), является хлор или бром 10 Способ по п 3, отличающийся тем, что на стадии Б) трифторацетильную группу, которая защищает группу NH2, и/или р-нитробензоил- и/или ацетильную группы, которые защищают группы ОН, удаляют, воздействуя неорганическим основанием, выбранным из группы, состоящей из гидроокисей и карбонатов натрия, калия, лития или бария 11 Способ по п 3, отличающийся тем, что на стадии Б) удаляют аллиловую оксикарбонильную группу, защищающую группу NH2, оказывая воздействие органическими комплексами никеля или палладия 12 Способ по п 3, отличающийся тем, что на стадии Б) удаляют метоксифенилдифенилметильную группу, защищающую группу ОН, оказывая воздействие органической кислотой 13 Способ по п 12, отличающийся тем, что упомянутой органической кислотой является уксусная кислота 14 Способ по п 3, отличающийся тем, что на стадии Б) удаляют диметилтербутилсилиловую группу, защищающую группу ОН, в присутствии фторида тетрабутиламмония 15 Способ по п 3, отличающийся тем, что на стадии В) соединения формул (I) и (II) превращают в фармацевтически приемлемые хлоргидраты 16 Способ по п 4, отличающийся тем, что на стадии А) осуществляют бромирование бромом в хлороформе 17 Способ по п 4, отличающийся тем, что на стадии Б) осуществляют гидролиз посредством муравьинокислого натрия 18 Фармацевтическая композиция, содержащая в качестве активного ингредиента, по меньшей мере одно соединение по любому из пп 1 или 2, или их фармацевтически приемлемые соли, в сочетании с фармацевтически приемлемыми носителем или растворителем 19 Соединения по любому из пп 1 или 2 или их фармацевтически приемлемые соли в качестве противораковых препаратов 20 Фармацевтическая композиция, применяемая в качестве противоракового средства, содержащая в качестве активного ингредиента по меньшей мере одно соединение по любому из пп 1 или 2 или его фармацевтически приемлемую соль, в сочетании с фармацевтически приемлемым носителем или растворителем 41951 Настоящее изобретение относится к соедине ниям с общей формулой (I) и (II) соответственно, где радикал R представляет собой Н или ОН либо группу OR7, в которой R7 представляет собой СОН или СОСНз, либо ациклический радикал карбоновой кислоты, содержащий до 6 атомов углерода, радикал Ri представляет собой Н или ОН либо ОСНз, радикал R2 представляет собой Н или F, радикал R3 представляет собой Н или ОН, радикалы R4 и Rs одинаковы или различны, каждый из них представляет собой Н или ОН или NH2, символ ( ) связи указывает, что заместители R3, R4 и Rs могут находиться в осевом или экваториальном положениях, их фармацевтически приемлемые соли обладают противораковыми свойствами Как можно видеть из вышеприведенных формул, соединения (I) и (II) отличаются только пространственным расположением гликозидных групп и потому могут быть представлены формулой (А), о (А) где символ ( ) указывает, что второй углеводородный радикал может быть связан с углеродным атомом 4' первого сахара либо в осевом, либо в экваториальном положении Настоящее изобретение относится также к способу получения упомянутых соединений, их фармацевтически приемлемым солям и фармацевтическим композициям, содержащим эти соединения 41951 Состояние техники Даунорубицин и доксорубицин являются широко известными антибиотиками, используемыми в настоящее время в клинической практике для лечения различных плотных опухолей и лейкемии (Ф Аркамон в публикации "Дексорубицин противораковые антибиотики", А Ч Сарторелли, Издательство "Академик пресс", Нью-Йорк, 1981) В европейском патенте № 0457215 описаны продукты, структура которых подобна структуре продуктов, приведенных в данной заявке, но имеющих только одну гликозидную группу Однако, как известно, сильное побочное действие, оказываемое противораковыми препаратами, используемыми в настоящее время, накладывает ограничения на их применение для большого числа пациентов, которые в противном случае могли бы извлечь пользу из лечения Более того, нужен серьезный прогресс при лечении некоторых распространенных плотных опухолей, например, в легочной и овариальной областях, которые не поддаются адекватно лечению современными методами Из сказанного следует, что существует неотложная потребность в появлении на рынке лекарств, обладающих высокой избирательностью при оказании подавляющего воздействия на разрастание больных и нормальных клеток Подробное описание изобретения Цель данного изобретения заключается в создании новых противораковых соединений, в частности, аналогов антрациклина, в которых углеводородная часть состоит из дисахаридного радикала Несколько неожиданным оказался тот установленный факт, что заявленные антрациклиновые дисахариды, у которых сахар, непосредственно связанный с аглюконом, не содержит аминогрупп, проявляют более высокие противораковую активность и избирательность, чем известный ранее антрациклин Следует отметить, что в известных антрациклинах, имеющих аналогичную структуру и содержащих два углеводородных радикала, сахар, связанный с аглюконом, всегда содержит свободную или замещенную аминогруппу Соединения, отвечающие настоящему изобретению, - это соединения, которые имеют общую формулу (I) и (II), упомянутую выше, а также их фармацевтически приемлемые соли, где присутствуют радикалы R, Ri, R2, R3, R4 и Rs, описанные ранее Настоящее изобретение относится также к фармацевтическим композициям, содержащим упомянутые соединения, или их солям, образованным с фармацевтически приемлемыми кислотами, предпочтительно соляной кислотой Особенно предпочтительны следующие соединения а) 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3амино-а-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]даунорубицинон хлоргидрат, б) 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3амино-а-Ьликсо-эксопиранозилЭ-а-Ьарабино-эксопиранозил]даунорубицинон хлоргидрат, в) 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3амино-а-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]доксорубицинон хлоргидрат, г) 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3амино-а-Ьликсо-эксопиранозилЭ-а-Ьарабино-эксопиранозил]доксорубицинон хлоргидрат, д) 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3амино-а-Ьликсо-эксопиранозилЭ-а-Ьарабино-эксо-пиранозил]-4-деметокси-даунорубицинон хлоргидрат, е) 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3амино-а-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]-4-деметокси-даунорубицинон хлоргидрат, ж) 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3амино-а-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]-4-деметокси-доксорубицинон хлоргидрат, з) 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3амино-а-Ьликсо-эксопиранозилЭ-а-Ьарабино-эксопиранозил]-4-деметокси-доксорубицинон хлоргидрат, и) 7-0-[2,6-дидеокси-4-0-(2,3,4,6-тетрадеокси-4-амино-а-1-эритро-эксопиранозил)-а-1-ликсоэксопиранозил]даунорубицинон хлоргидрат, к) 7-0-[2,6-дидеокси-4-0-(2,3,4,6-тетрадеокси-4амино-а-Ьэритро-эксопиранозилЭ-а-Ьликсо-эксопиранозил]-4-деметокси-даунорубицинон хлоргидрат, л) 7-0-[2,6-дидеокси-4-0-(2,3,4,6-тетрадеокси-4-амино-а-1-эритро-эксопиранозил)-а-1-ликсоэксопиранозил]доксорубицинон хлоргидрат, м) 7-0-[2,6-дидеокси-4-0-(2,3,4,6-тетрадеокси4-амино-а-1_-эритроэксопиранозил)-а-1_-ликсо-эксопиранозил]-4-деметокси-доксорубицинон хлоргидрат, н) 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3амино-а-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]-4-деметокси-8-фтордаунорубицинон хлоргидрат, о) 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3амино-а-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]-4-деметокси-8-фтордоксорубицинон хлоргидрат, Соединения с общей формулой (I) и (II) могут быть получены посредством процесса, состоящего из следующих шагов А) осуществляют конденсацию соединения, имеющего формулу (III), он он (III) 41951 где радикалы Ri и F 2 определены так же, как вы? ше, радикал F 6 представляет собой Н или группу ? OR7, в которой радикал R7 представляет собой защитную группу для спиртовой функциональности, предпочтительно выбранную из ацетил-, диметилтербутилсилил- или р-метоксифенилдифенилметиловых групп, с соединением, имеющим формулу (IV) или (V), где радикал Rs представляет собой Н или защищенную группу ОН, предпочтительно, р-нитробензоат, радикалы Rg и R-ю одинаковы или различны и каждый из них представляет собой Н либо защищенную группу ОН, предпочтительно, р-нитробензоат или защищенная группа NH2, предпочтительно, трифторацетамид, либо аллиловый карбоксиамид, а X - это группа, способная образовывать, в режиме конденсации, стабильные углерод ные катионы, которые могут связываться с гидроксильной группой в положении С-7 соединения, имеющего формулу (III), причем, упомянутую группу X надлежащим образом выбирают из групп, используемых в реакциях гликозидиации, например, галоген, в частности, хлор или бром, хотя предпочтителен хлор, либо р-нитробензоилокси группу Таким образом получают соединения с формулами (VI) или (VII), (VII) где радикалы Ri, R2, R6, Rs, R9, R10 и символ ( ) определены, как указано выше, Б) осуществляют одну или несколько реакций по удалению из соединений, имеющих форму 41951 лы (VI) и (VII), защитных групп для функциональности ОН и/или Nbb, с целью получения соединений с формулами (I) и (II), где радикалы R, Ri, R2, R3, R4, R5 и символ ( ) определены, как указано выше, В) осуществляют превращение, если таковое возможно, вышеупомянутых гликозидов, входящих в формулы (I) и (II), в их фармацевтически приемлемые соли, предпочтительно, хлоргидраты Условия проведения реакции гликозидиации соединения, имеющего формулу (III), с соединениями, имеющими формулы (IV) или (V), с целью получения соединений, имеющих формулы (VI) или (VII), могут варьироваться в зависимости от типа заместителей, присутствующих в соединениях с формулами (IV) или (V) Гликозидиацию выполняют в инертном органическом растворителе, в присутствии конденсирующего вещества В качестве конденсирующих веществ используют, в частности, трифторметансульфонат серебра, перхлорат серебра, смеси окиси ртути с бромидом ртути, галоидные соединения бора, четыреххлористый титан или олово, либо ионообменные смолы, например, амберлит Гликозидиацию предпочтительно осуществляют в инертном органическом растворителе с молярным отношением в пределах от 1 1 до 1 3, например, бензоле, толуоле, этиловом эфире, тетрагидрофуране, диоксане, хлороформе, метиленхлориде или дихлорэтане, либо их смесях Диапазон температур, в котором протекает реакция, лежит от -40°С до 40°С, хотя предпочтительнее, от -20°С до 20°С, а время реакции составляет от 15 минут до 3 часов Реакционная смесь может включать в себя дегидратирующее вещество, например, активированный цеолит В процессе или в конце реакции к реакционной смеси можно добавить органическое основание, например, пиридин, коллидин, N.N-диметиламинопиридин, триэтиламин или 1,8-тетраметиламинонафгалин В соответствии с настоящим изобретением удаление из соединений, имеющих формулы (VI) и (VII), защитных групп для функциональностей ОН и/или NH2, с целью получения соединений, имеющих формулу (I), может быть осуществлено при различных условиях, зависящих от типа используемых защитных групп Когда радикалы Rg и/или R-ю одинаковы или различны, и каждый из них представляет собой защищенную группу NH2, например, как трифторацетамид, или защищенную группу ОН, например, как р-нитробензоат, и/или радикал Rs представляет собой защищенную группу ОН, например, как р-нитробензоат, и/или радикал R6 представляет защищенную группу ОН, например, как ацетат, реакцию по удалению защиты выполняют в полярном растворителе, например, воде, метаноле, этаноле, пиридине, диметилформамиде или их смесях в присутствии неорганических оснований, взятых в стехиометрическом соотношении, либо свыше стехиометрического соотношения, например, гидроокисей натрия, калия, лития или бария, либо карбоната Диапазон температур, в котором протекает реакция может лежать от 0°С до 50°С, а время реакции - от 3 до 48 часов Когда каждый из радикалов Rg и/или R-ю представляет собой защищенную группу NH2, например, какаллиловый карбоксиамид, удаление защиты осуществляют в инертном растворителе в присутствии комплексного соединения металла, например, тетракис(трифенилфосфин) палладия, как описано, например, в "Тетрагедрон Леттерз", 1989, т 30, с 3773, или тетракарбонильный никель, как описано, например, в 'Журнале органической химии", 1973, т 38, с 3233 Когда радикал R6 представляет собой защищенную группу ОН, например, как диметилтербутилсилиловый эфир, снятие защиты осуществляют в инертном растворителе в присутствии фторида тетрабутиламмония, как описано в 'Журнале по антибиотикам", 1984, т 37, с 853 Когда радикал R6 представляет собой защищенную группу ОН, например, как р-метоксифенилдифенилметиловый эфир, снятие защиты осуществляют в кислой среде, например, водном растворе уксусной кислоты, как описано, например, в 'Журнале органической химии", 1977, т 42, с 3653 Соединения с формулой (III) либо известны, либо могут быть получены в соответствии с методами и процессами, известными в органической химии, как описано, например, в "Химической газете Италии", 1984, т 114, с 517, в "Бюллетене химической Ассоциации Японии", 1986, т 59, с 423 и в упомянутой ранее итальянской заявке на патент, поданной заявителем, раскрытие сущности которой приведено здесь в качестве ссылочного материала Соединения, имеющие формулы (IV) или (V), либо известны, либо могут быть получены согласно методам и процессам, известным в органической химии для синтеза дисахаридов ('Журнал химии углеводов", 1991, т 10, с 833, "Исследование углеводов", 1979, т 74, с 199, "Исследование углеводов", 1980, т 208, с 111, "Тетрагедрон", 1990, т 46, с 103) В качестве альтернативы, при желании, антрациклиновые гликозиды с формулами (I) и (II), где радикалы Ri, R2, R3, R4, R5 определены, как указано выше, а радикал R представляет собой группу ОН, могут быть получены из гликозидов с формулами (I) и (II) или из их фармацевтически приемлемых солей, где радикалы Ri, R2, R3, R4, R5 и символ ( ) определены, как указано выше, а радикал R представляет собой Н, путем бромирования углерода, находящегося в положении 14, посредством брома в хлороформе, с последующим гидролизом при комнатной температуре в течение 48 часов полученных 14-бромпроизводных посредством муравьинокислого натрия При желании гликозиды с формулами (I) и (II) могут быть превращены в их фармацевтически приемлемые соли, например, хлоргидраты, путем обработки соляной кислотой в метиловом спирте Настоящее изобретение относится также к фармацевтическим композициям, содержащим в качестве активного ингредиента соединение, имеющее формулы (I) или (II), либо его фармацев 41951 тически приемлемую соль в сочетании с фармацевтически приемлемым растворителем или носителем В соответствии с настоящим изобретением терапевтически эффективную дозу соединения, имеющего формулы (I) или (II), сочетают с инертным носителем Композиции могут быть составлены обычным образом с использованием общепринятых носителей Заявленные соединения полезны для терапевтического воздействия на людей и других млекопитающих В частности, упомянутые соединения являются хорошими противораковыми препаратами при их применении в терапевтически эффективных дозах Нижеследующие примеры иллюстрируют более детально настоящее изобретение Пример 1 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3-амино-а-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]-4-деметокси-даунорубицинон хлоргидрат (соединение с формулой (II), R=Ri=R2=H, R3=R5=OH, R4=NH2) Смесь 4-деметоксидаунорубицинона (соединение с формулой (III), Ri=R2=R6-H) (300 мг, 0,81 ммоль) и 2,6-дидеокси-4-0-(2,3,6-тридеокси-40-р-нитробензоил-3-трифтор-ацетомидо-а-І_-ликсо-эксопиранозил)-3-0-р-нитро-бензоил-а-1_-ликсоэксопиранозил-р-нитробензоата (соединение с формулой (IV), R3=R5-p-HHTpo6eH3onn-OKCH-, R4=тpифтopaцeтoмидo-, Х=р-нитробензоилокси-) (600 мг, 0,72 ммоль) в хлористом метиле (72 мл) и этиловом эфире (24 мл), в присутствии активированного цеолита (А4), при температуре -20°С обработана триметилсилилтрифлатом (266 мкл, 1,44 ммоль) Реакционную смесь перемешивали в течение 1 часа, после чего она была разбавлена хлористым метилом, промыта насыщенным раствором бикарбоната натрия и высушена путем испарения Остаток был отделен путем хроматографии на силикагеле (растворитель для элюирования CH2CI2 - ЕЮН, 99/1), при этом получен выход в количестве 360 мг 7-0-[2,6-дидеокси-4-0-(2,3,6тридеокси-4-0-р-нитробензоил-3-фторацетомидо-а1_-ликсо-эксопиранозил)-3-0-р-нитробензоил-а-1_ликсо-эксопиранозил]-4-деметоксидаунорубици нона (соединение с формулой (VII), Ri=R2=R6=H, Rs= =Rio=p-HHTpo6eH3onnoKCH-, R9=тpифтopaцeтoмидo-) Суспензия защищенных гликозидов, представляющих собой соединение с формулой (VII) (Ri=R2=R6=H, Rs^Rio-p-нитробензоилокси-, Rg=Tpnфгорацетомидо-) (120 мг, 0,117 ммоль), в 17,6 мл 0,1 М раствора Ва(ОН)2 в Н2О/МеОН, 1/1, была подвергнута перемешиванию при комнатной температуре в течение 3 часов Реакционная смесь была нейтрализована посредством 0,2 М раствора бисульфата калия и извлечена с помощью хлороформа, органические вытяжки собраны вместе, высушены на безводном сульфате натрия, выпарены досуха и поглощены 0,002 М раствором HCI Водный раствор кислоты обработан хлороформом и высушен путем замораживания, при этом получено 62 мг нужного продукта (состав с формулой (II), R=Ri=R2=H, R3=R5=OH, R4=NH2) Выход - 39% Данные ЯМР приведены ниже 1 H-NMR (DMSO-d6), 5 1,05 (d, ЗН), 1/15 (d, ЗН), 1,5-1,95 (m, 4H), 2,1 (m, 2H), 2,25 (s, ЗН), 2,95 (dd, 2H), 3,55 (s, 2H), 3,8 (m, 1H), 3,95 (m, 1H), 4,15 (q, 1H), 4,35 (q, 1H), 4,6 (d, 1H), 4,9 (bs, 2H), 5,25 (bs, 1H), 5,35 (d, 1H), 5,55 (s, 1H), 7,95 (bs, 2H), 8,25 (bs, 2H) Согласно аналогичному процессу были получены также следующие соединения, имеющие формулы (I) и (II) 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3-амино-а-1_-ликсо-эксопиранозил)-а-1_-ликсо-эксопиранозил]даунорубицинон хлоргидрат (соединение с формулой (II), R=R2=H, Ri=OCH3, R3=R5=OH, R4=NH2) 1H-NMR(DMSO-d6), 5 1,05 (d, 3H), 1,15 (d, 3H), 1,35-2,15 (m, 6H), 2,25 (s, 3H), 2,95 (dd, 2H), 3,55 (bs, 2H), 3,8 (m, 1H), 3,95 (s, 3H), 4,05-4,2 (m+q, 2H), 4,35 (q, 1H), 4,9 (bs, 2H), 5,25 (d, 1H), 7,65 (m, 1H), 7,9 (d, 2H) 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3-амино-а-1_-ликсо-эксопиранозил)-а-1_-арабино-эксопиранозил]даунорубицинон хлоргидрат (соединение с формулой (I), R=R2=H, Ri=OCH3, R3=R5=OH, R4=NH2) 1H-NMR (DMSO-d6), 5 1,13 (d, 3H), 1,15 (d, 3H), 1,45-1,85 (m, 4H), 2,05 (m, 2H), 2,15 (s, 3H), 2,87 (dd, 2H), 2,98 (m, 1H), 3,6 (m, 1H), 3,85 (q, 1H), 3,9 (q, 1H), 3,9 (s, 3H), 4,84 (m, 2H), 5,13 (bs, 1H), 5,28 (s, 1H), 5,32 (d, 1H), 5,55 (s, 1H), 7,55 (m, 1H), 7,8 (m, 2H) 7-0-[2,6-дидеокси-4-0-(2,3,6-тридеокси-3-амино-а-1_-ликсо-эксопиранозил)-а-1_-арабино-эксопира~ нозил]-4-деметокси-даунорубицинон хлоргидрат (соединение с формулой (I), R=Ri=R2=H, R3=Rs= ОН, R4=NH2) 1H-NMR (DMSO-d6), 5 1,1 (d, ЗН), 1,2 (d, ЗН), 1,5-1,95 (m, 4H), 2,05-2,2 (m, 2H), 2,25 (s, 3H), 2,95 (dd, 2H), 3,1 (t, 1H), 3,4 (m, 1H), 3,6 (bs, 1H), 3,65 (m,1H), 3,85-4,00 (q+q, 2H), 3,9 (m, 1H), 4,95 (d, 1H), 5,2 (d, 1H), 5,4 (bs, 2H), 5,7 (s, 1H), 7,95 (m, 2H), 8,25 (m, 2H) Тираж 50 екз Відкрите акціонерне товариство «Патент» Україна, 88000, м Ужгород, вул Гагаріна, 101 (03122) 3 - 7 2 - 8 9 (03122) 2 - 5 7 - 0 3
ДивитисяДодаткова інформація
Назва патенту англійськоюAnthracycline disaccharides, a process for the preparation thereof and pharmaceutical compositions containing them
Автори англійськоюAnimati Fabio, Lombardi Paolo, Arcamone Federico, Cipollone Amalia
Назва патенту російськоюАнтрациклиновые дисахариды, способ их получения и фармацевтические композиции, их содержащие
Автори російськоюАнимати Фабио, Ломбарди Паоло, Аркамоне Федерико, Чиполлоне Амалия
МПК / Мітки
МПК: A61K 31/7034, A61K 31/70, A61K 31/7028, A61K 31/704, A61P 35/00, C07H 15/252
Мітки: антрациклінові, фармацевтичні, дисахариди, одержання, містять, композиції, спосіб
Код посилання
<a href="https://ua.patents.su/9-41951-antraciklinovi-disakharidi-sposib-kh-oderzhannya-ta-farmacevtichni-kompozici-yaki-kh-mistyat.html" target="_blank" rel="follow" title="База патентів України">Антрациклінові дисахариди, спосіб їх одержання та фармацевтичні композиції, які їх містять</a>
Попередній патент: Пристрій для визначення місця спалаху блискавки
Наступний патент: Похідні аміну, фармацевтична композиція на їх основі та спосіб лікування психозів і шизофренії
Випадковий патент: Спосіб визначення числа ароматоутворюючих сполук