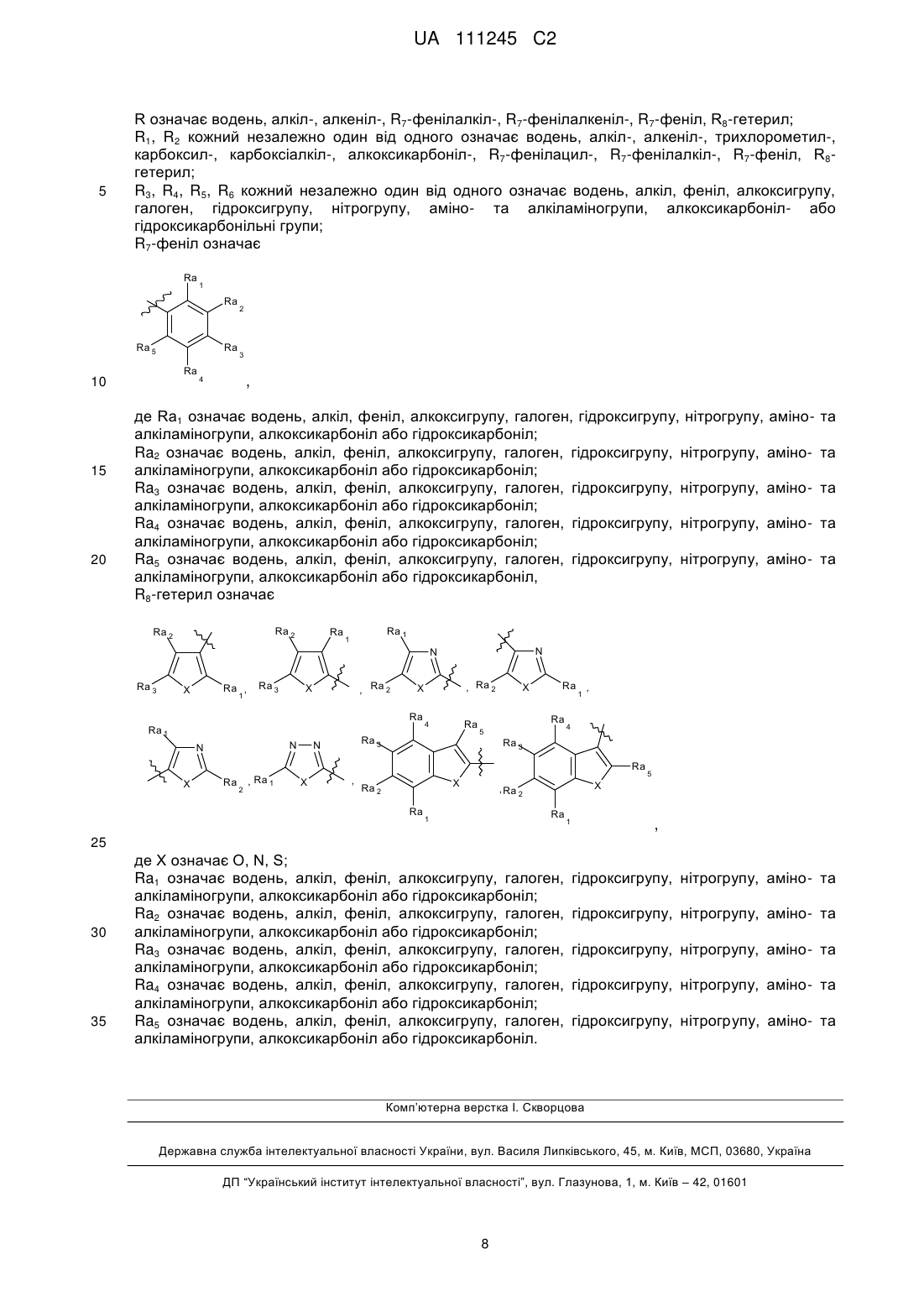
6-моно- та 6,6-дизаміщені 3-r-8-r3-9-r4-10-r5-11-r6-6,7-дигідро-2н-[1,2,4]триазино[2,3-с]хіназолін-2-они
Номер патенту: 111245
Опубліковано: 11.04.2016
Автори: Коломоєць Олександра Сергіївна, Пальчиков Віталій Олександрович, Берест Галина Григорівна, Коваленко Сергій Іванович, Воскобойник Олексій Юрійович, Оковитий Сергій Іванович, Холодняк Сергій Валерійович, Сергеєва Тетяна Юріївна
Формула / Реферат
6-Моно- та 6,6-дизаміщені 3-R-8-R3-9-R4-10-R5-11-R6-6,7-дигідро-2H-[1,2,4]триазино[2,3-с]хіназолін-2-они формули:
 ,
,
в якій
R означає водень, алкіл-, алкеніл-, R7-фенілалкіл-, R7-фенілалкеніл-, R7-феніл, R8-гетерил;
R1, R2 кожний незалежно один від одного означає водень, алкіл-, алкеніл-, трихлорометил-, карбоксил-, карбоксіалкіл-, алкоксикарбоніл-, R7-фенілацил-, R7-фенілалкіл-, R7-феніл, R8-гетерил;
R3, R4, R5, R6 кожний незалежно один від одного означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл- або гідроксикарбонільні групи;
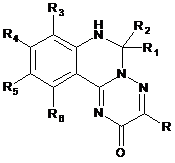
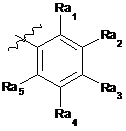
R7-феніл означає
 ,
,
де Ra1 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл;
Ra2 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл;
Ra3 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл;
Ra4 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл;
Ra5 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл,
R8-гетерил означає
 ,
,
де X означає О, N, S;
Ra1 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл;
Ra2 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл;
Ra3 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл;
Ra4 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл;
Ra5 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл.
Текст
Реферат: UA 111245 C2 (12) UA 111245 C2 Винахід стосується 6-моно- та 6,6-дизаміщених 3-R-8-R3-9-R4-10-R5-11-R6-6,7-дигідро-2H[1,2,4]триазино[2,3-с]хіназолін-2-онів формули R3 R4 H N R2 R1 N R5 R6 N N R O . Ці сполуки можуть бути отримані в умовах вітчизняних промислових хіміко-фармацевтичних підприємств з використанням стандартного обладнання, синтезовані з доступних вихідних реагентів, мають низьку токсичність і використані у спрямованому пошуку біологічно активних речовин як перспективних лікарських засобів. R3 R4 H N R2 R1 N R5 R6 N N R O UA 111245 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід належить до нових 3-R-8-R3-9-R4-10-R5-11-R6-6,7-дигідро-2Н[1,2,4]триазино[2,3-с]хіназолін-2-онів, які можуть бути використані у хіміко-фармацевтичній промисловості для спрямованому пошуку біологічно активних речовин як перспективних лікарських засобів. Синтез органічних сполук, що містять конденсовані по ребру [с] піримідиновий та 1,2,4триазиновий цикли, було описано у спеціалізованій літературі. Так, реакцією 1-R-3-(2'амінофеніл)-1,4,5,6-тетрагідро[1,2,4]триазинів з хлорангідридами карбонових кислот у хлористому метилені в присутності органічної основи синтезовані ацильні похідні, які термолізом перетворені у 6-R1-2-алкіл-3,4-дигідро-2Н-[1,2,4]триазино[4,3-с]хіназоліни. 1-R-3-(2'амінофеніл)-1,4,5,6-тетрагідро[1,2,4]триазини також легко взаємодіють з арилізоціанатами, утворюючи відповідні сечовини, які при термолізі елімінують ароматичний амін та гетероциклізуються у відповідні 2-алкіл-2,3,4,7-тетрагідро-6Н-[1,2,4]триазино[4,3-с]хіназолін-6они [Trepanier D.L., Sunder S., Braun W.H. // J. Heterocycl. Chem. - 1974, - Vol. 11, № 5. - P. 747750; Trepanier D.L. Sunder S. // J. Heterocycl. Chem. - 1975. - Vol. 12, № 2. - P. 321-326]. 3-алкіл(алкарил-, арил-, гетерил)-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-они та методи їх одержання описані, наприклад, в HETEROCYCLES (O.V. Karpenko, S.I. Kovalenko, O.O. Chekotylo et al. // HETEROCYCLES. - 2007. - Vol. 71, Issue 3, P. 619-626], в Журналі органічної та фармацевтичної хімії [С.І. Коваленко, О.Ю. Воскобойнік, О.В. Карпенко та інші // Журнал органічної та фармацевтичної хімії. - 2008, - Т. 6. - Випуск 1(21). - С. 25-32; О. Yu. Voskoboynik, О. V. Karpenko, T. Yu. Sergeieva, S. I. Kovalenko, S. I. Okovytyy. // Журнал органічної та фармацевтичної хімії. - 2013. - Т. 11, Вип. 1(41). - С. 37-44]; в Віснику Національного університету "Львівська політехніка" [О. Ю. Воскобойнік, С. І. Коваленко // Вісник Національного університету "Львівська політехніка": „Хімія, технологія речовин та їх застосування". - 2008, - № 622. - С. 18-21]; в Tetrahedron [A.V. Karpenko, S.I. Kovalenko O.V. Shishkin // Tetrahedron. - 2009. Vol.65, № 31. - P. 5964-5972]. Зазначені методи одержання 3-алкіл(алкарил-, арил-, гетерил)-2Н[1,2,4]триазино[2,3-с]-хіназолін-2-онів зводяться до прямого апелювання s-триазинонового циклу до хіназоліну, і полягають у взаємодії заміщених 4-гідразинохіназоліну з естерами кетокарбонових та естерами , -діоксо--арил(гетерил-)карбонових кислот в льодяній оцтовій кислоті; а також гетероциклізації естерів 2-R-2-{[3H-хіназолін-4-іліден]гідразоно}оцтових та 4оксо-4-арил-2-{[3H-хіназолін-4-іліден]гідразоно}бутанових кислот у льодяній оцтовій кислоті, ДМФА або термолізом. В 2009 році Коваленко С.І. зі співавторами описали інший підхід до синтезу піримідинотриазинових систем [Патент України №40484, МПК (2009), C07D 253/00. // Коваленко С.І., Кривошей О.В., Карпенко О.В. (UA). - Заявл. 17.11.2008; Опубл. 10.04.2009. - Бюл. № 7]. Авторами синтезовано (3-оксо-3,4-дигідро-2Н-[1,2,4]триазино[4,3-с]хіназолін-4-іл)оцтові кислоти взаємодією заміщених 4-гідразинохіназоліну з малеїновим ангідридом. Крім того, 2010 р. 1 Коваленко С.І. зі співавторами описав синтез 3-R-6-R -тіо-6,7-дигідро-2H-[1,2,4]. триазино[2,3с]хіназолін-2-онів та їх заміщених, які отримані циклізацією 3-(2-амінофеніл)-6-R-2H[1,2,4]триазин-5-онів з калію О-алкіл карбонодитіонатами [Патент України на винахід № 90982 МПК C07D 487/04 (2006.01). // С.І. Коваленко, П.І. Степанюк, Г.Г. Берестта ін. - Заявл. 18.09.2009; Опубл. 10.06.2010. - Бюл. № 11]. В 2012 році Коваленко С.І. зі співавторами розробили оригінальний метод синтезу (3-R-8-R1-9-R2-10-R3-11-R4-2-охо-2H-[1,2,4]триазино[2,3с]хіназолін-6-іл)алкілкарбонових кислот, взаємодією 3-(2-амінофеніл)-6-R-2H-[1,2,4]триазин-5онів з ангідридами та хлорангідридами аліфатичних дикарбонових кислот [Патент України на винахід №97586 МПК (2009) C07D 253/00 (2006/01), C07D 253/10 (2006/01). // Коваленко СІ., Степанюк ГЛ., Скорина Д.Ю. та ін. - Заявл. 12.11.2010; Опубл. 20.02.2012.- Бюл. № 4]. Найбільш близькими до сполук, що заявляються, є 6-моно- та 6-дизаміщені 2-алкіл-3,4,6,7тетрагідро-2H-[1,2,4]триазино[4,3-с]хіназоліни, які запропоновані Trepanier D.L. зі співавторами в 1975 році [Pat. 3919216 USA, C07D 253/08. / Trepanier D. L., Sunder S.; The Dow Chemical Company; заявл. 04.11.74; опубл. 11.11.75 // Chem. Abstr.-1975. - Vol. 84.-121903; Pat. 3919219 USA, C07D 253/08. / Trepanier D. L., Sunder S.; The Dow Chemical Company; заявл. 04.11.74; опубл. 11.11.75 // Chem. Abstr. - 1975. - Vol. 84. - 121906; Pat. 3919220 USA, C07D 253/08. / Trepanier D. L., Sunder S.; The Dow Chemical Company; заявл. 04.11.1974; опубл. 11.11.1975 // Chem. Abstr. - 1975. - Vol. 84.- 121907]. За даним методом взаємодія 1-R-3-(2'-амінофеніл)1,4,5,6-тетрагідро[1,2,4]триазинів з аліфатичними, ароматичними та гетероциклічними альдегідами або кетонами приводить до відповідних 6-моно- та 6,6-дизаміщених 2-алкіл-3,4,6,7тетрагідро-2H-[1,2,4]триазино[4,3-с]хіназолінів. Спільною суттєвою ознакою прототипу та винаходу є те, що сполуки за прототипом та винаходом можна віднести до похідних [1,2,4]триазино[с]хіназоліну. Проте винахід у відмінності від прототипу конденсований по ребру [с] за положеннями 2 та 3 і, крім того, у положенні 2 1 UA 111245 C2 5 містить карбонільну групу, а у положенні 3 - різноманітні функціональні групи. Тим більше, вихідна сполука дозволяє ввести у молекулу [1,2,4]триазино[2,3-с]хіназоліну за положеннями 8, 9, 10 та 11 різноманітні замісники. Виходячи із зазначеного, в основу винаходу поставлено задачу створення нових 6-моно- та 6,6-дизаміщених 3-R-8-R3-9-R4-10-R5-11-R6-6,7-дигідро-2H-[1,2,4]триазино[2,3-с]хіназолін-2-онів, які можуть бути використані у хіміко-фармацевтичній промисловості для спрямованого пошуку біологічно активних речовин як перспективних лікарських засобів. У відповідності з цим у винаході пропонуються нові сполуки - 6-моно- та 6,6-дизаміщені 3-R8-R3-9-R4-10-R5-11-R6-6,7-дипдро-2H-[1,2,4]триазино[2,3-с]хіназолін-2-они формули: 10 R3 H N R4 R2 R1 N R5 N N R6 R O 15 , в якій R означає водень, алкіл-, алкеніл-, R7-фенілалкіл-, R7-фенілалкеніл-, R7-феніл, R8гетерил; R1, R2 кожний незалежно один від одного означає водень, алкіл-, алкеніл-, трихлорометил-, карбоксил-, карбоксіалкіл-, алкоксикарбоніл-, R7-фенілацил-, R7-фенілалкіл-, R7-феніл, R8-гетерил; R3, R4, R5, R6 кожний незалежно один від одного означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл- або гідроксикарбонільні групи; R7-феніл означає 20 Ra 1 Ra Ra 5 Ra 2 3 Ra 25 30 4 , де Ra1 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra 2 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra3 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra 4 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra 5 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл, R8 гетерил означає: 2 UA 111245 C2 Ra 2 Ra 2 Ra Ra 1 1 N N Ra 3 Ra X 1 , Ra 3 , Ra 2 X X Ra Ra 1 N N , Ra 4 Ra 3 N Ra 2 X Ra Ra 5 1, 4 Ra 3 Ra X Ra , Ra 1 2 X , X Ra 2 Ra 5 10 15 20 25 30 35 40 45 1 5 X , Ra 2 Ra 1 , де X означає О, N, S; Ra1 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra 2 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra 3 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra4 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra 5 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл. Винахід ілюструється прикладами 1 та 2 отримання сполук, що заявляються. Приклад 1. Загальний метод синтезу 6-монозаміщених 3-R-8-R3-9-R4-10-R5-11-R6-6,7дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-ону До суспензії 0,005 моль 3-(2-аміно-3-R-8-R3-9-R4-10-R5-11-R6-феніл)-6-R-1,2,4-триазин5(2Н)ону у оцтовій кислоті додають 0,005 моль відповідного аліфатичного, ароматичного, коричного або гетероциклічного альдегіду та кип'ятять протягом 3 годин, розчинник видаляють в вакуумі, додають 30 мл пропанолу-2, перемішують, осад, що утворився відфільтровують та сушать. 3-(4-Ізопропілфеніл)-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (1.1). Вихід: 44,3 %, 1 Т. пл.: 233-235 °C Н ЯМР (400 MHz, dmso-d6) 8,10 (d, J=8,0 Hz, 2H, 3 Ph H-2,6), 8,02 (d, J=7,7 Hz, 1H, H-11), 7,39 (t, J=7,4 Hz, 1H, H-9), 7,28 (d, J=8,1 Hz, 2H, 3 Ph H-3,5), 6,98-6,81 (m, 1H, H-8, 10), 5,30 (s, 2H, CH2), 3,02 - 2,87 (m, 1H, CH(CH3)), 1,30 (d, J=6,8 Hz, 6H, СН(СН3))- ЖХ-МС (XI), + m/z=319 (MH ), Розраховано для C19H18N4O: С - 71,68 %; H - 5,70 %; N - 17,60 %. Визначено: С 71,69 %; Н - 5,73 %; N - 17,61 %. 3-(4-Метоксифеніл)-6-ізопропіл-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (1.2). 1 Вихід: 65,8 %, Т. пл.: 181-183 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 8,21 (d, J=8,9 Hz, 2H, 3 Ph H2,6), 7,95 (d, J-7,1 Hz, 1H, H-11), 7,60 (d, J=2,6 Hz, 1H, NH), 7,35 (t, J=6,9 Hz, 1H, H-9), 6,95 (d, J8,9 Hz, 2H, 3Ph H-3,5), 6,90 (d, J=8,1 Hz, 1H, H-8),6,80 (t, J=7,3 Hz, 1H, H-10), 5,24 (dd, J=6,9, 3,3 Hz, 1H, CHp), 3,86 (s, 3H, OCH3), 2,40-2,18 (m, J=13,3, 6,5 Hz, 1H, CH(CH3)), 0,96 (dd, J-10,0, 6,8 + Hz, 6H, СН(СН3))- ЖХ-МС (XI), m/z=349 (MH ), Розраховано для C20H20N4O2: С - 68,95 %; H 5,79 %; N - 16,08 %. Визначено: С - 68,97 %; Н - 5,81 %; N - 16,12 %. 3-(4-Метилфеніл)-6-ізобутил-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (1.3). Вихід: 1 50,0 %, Т. пл.: 196-198 °C Н ЯМР (400 MHz, DMSO) 8,07 (d, J=8,0 Hz, 2H, 3 Ph H-2,6), 7,94 (d, J=7,8 Hz, 1H, H-11), 7,62 (s, 1H, NH), 7,44 (t, J=7,5 Hz, 1H, H-9), 7,30 (d, J=8,0 Hz, 2H, 3 Ph H-3,5), 6,94 (d, J=8,2 Hz, 1H, H-8), 6,88 (t, J=7,5 Hz, 1H, H-10), 5,64 (s, 1H, CH), 3,36 (s, 2H, CH2CH(CH3)2), 2,37 (s, 3H, CH3Ph), 1,13-0.99 (m, 1H, CH2CH(CH3)2), 0.93 (s, 6H, СН2СH(СН3)2). 13 С ЯМР (101 MHz, DMSO) 161,16, 151,45, 147,34, 144,89, 140.13, 135,58, 135,04, 129,76, 129,48, 128,72, 128,55, 126,84, 118,59, 115,72, 112,13, 72,32, 41,77, 23,36, 22.54, 21,96, 21,05, + ЖХ-МС (XI), m/z=347 (MH ), Розраховано для C21H22N4O: С - 72,81 %; H - 6,40 %; N - 16,17 %. Визначено: С - 72,86 %; Н - 6,44 %; N - 16,18 %. 3-(4-Флуорофеніл)-6-ізобутил-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (1.4). Вихід: 1 40.9 %, Т. пл.: 209-211 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 8,34-8,16 (m, 2Н, 3 Ph H-2,6), 7,99 (d, J=7,3 Hz, 1H, H-11), 7,52 (s, 1H, NH), 7,38 (t, J=6,9 Hz, 1H, H-9), 7,19 (t, J=8,7 Hz, 2H, 3 Ph H3,5), 6,95-6,75 (m, 2H, H-8,10), 5,57 (s, 1H, CH), 1,89-1,62 (m, 3Н, СН2СН(СН3)2), 0.98 (d, J=5,8 Hz, 3 UA 111245 C2 + 5 10 15 20 25 30 35 40 45 50 55 60 6H, СН2СН(СН3)2)- ЖХ-МС (XI), m/z=351 (MH ), Розраховано для C20H19FN4O: С - 68,56 %; Н 5,47 %; N - 15,99 %. Визначено: С - 68,59 %; Н - 5,50 %; N - 16,03 %. 3-(4-Ізопропілфеніл)-6-(хлорометил)-6,7-дигідро-2Н-[1,2,4]триазино[2,3-хіназолін-2-он (1.5). 1 Вихід: 76,82 %, Т. пл.: 245-248 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 8,12 (d, J=8,0 Hz, 1H, 3 Ph H2,6), 8,00 (d, J=1,1 Hz, 1H, H-11), 7,77 (s, 1H, NH), 7,39 (t, J=7,5 Hz, 1H, H-9), 7,30 (d, J=8,1 Hz, 2H, 3 Ph H-3,5), 6,92 (d, J=8,1 Hz, 1H, H-8), 6,85 (t, J=7,5 Hz, 1H, H-10), 5,84 (s, 1H, CH), 3,94 (ddd, J=16,0, 11,7, 5,1 Hz, 2H, CH2Cl), 2,98 (dt, J=13,6, 6,8 Hz, 1H, CH(CH3)2), 1,30 (d, J=6,8 Hz, 6H, + СН(СН3)2)- ЖХ-МС (XI), m/z-367 (MH ), Розраховано для C20H19ClN40: С - 65,48 %; H - 5,22 %; N 15,27 %. Визначено: С - 65,52 %; Н - 5,25 %; N - 15,29 %. 3-Феніл-6-(хлорметил)-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (1.6). Вихід: 1 53,75 %, Т. пл.: 205-207 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 8,18 (d, J=5,6 Hz, 2H, 3 Ph H-2,6), 8,00 (d, J=7,5 Hz, 1H, H-11), 7,80 (s, 1H, NH), 7,58-7,26 (m, 4H, H-9, 3 Ph H-3,4,5), 6,93 (d, J=8,0 Hz, 1H, H-8), 6,86 (t, J=7,4 Hz, 1H, H-10), 5,86 (s, 1H, CH), 3,94 (ddd, J=16,0, 11,7, 5,1 Hz, 2H, CH2Cl). ЖХ-МС (XI), m/z=326 (MH+), Розраховано для C17H13C1N4O: С - 62,87 %; H - 4,03 %; N - 17,25 %. Визначено: С - 62,89 %; Н - 4,07 %; N - 17,29 %. (Е)-3-(4-метилфеніл)-6-стиріл-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (1.7). Вихід: 1 92,0 %, Т. пл.: 257-260 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 8,10 (d, J-8,0 Hz, 2H, 3 Ph H-2,6), 8,02 (d, J=7,5 Hz, 1H, H-11), 7,78 (s, 1H, NH), 7,41 (m, 5H, H-9, 6 Ph H-2,6), 7,25 (m, 5H, 3 Ph H3,5, 6 Ph H-3,4,5), 6,96 (d, J=8,1 Hz, 1H, H-8), 6,87 (t, J=7,3 Hz, 1H, H-10), 6,77 (d, J=15,8 Hz, 1H, CH=CHPh), 6,48 (dd, J-15,7, 6,4 Hz, 1H, CH=CHPh), 6,17 (s, 1H, CH), 2,41 (s, 3Н, СН3). ЖХ-МС + (XI), m/z=393 (MH ), Розраховано для C25H20N4O: С - 76,51 %; Н - 5,14 %; N - 14,28 %. Визначено: С - 76,54 %; Н - 5,19 %; N - 14,32 %. (Е)-3-(4-флуорфеніл)-6-стиріл-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (1.8). Вихід: 1 78,4 %, Т. пл.: 269-271 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 8,29 (t, 2Н, 3 Ph H-2,6), 8,02 (d, J=7,8 Hz, 1H, H-11), 7,80 (s, 1H, NH), 7,42 (m, 3H, H-9, 6 Ph H-2,6), 7,34-7,11 (m, 5H, 3 Ph H-3,5, 6 Ph H3,4,5), 6,96 (d, J=7,9 Hz, 1H, H-10), 6,88 (t, J=7,1 Hz, 1H, H-8), 6,77 (d, J=15,8 Hz, 1H, CH=CHPh), + 6,48 (dd, J=15,7, 6,3 Hz, 1H, CH=CHPh), 6,18 (s, 1H, CH). ЖХ-МС (XI), m/z=397 (MH ), Розраховано для C24H17FN4O: С - 72,72 %; Н - 4,79 %; N - 14,13 %. Визначено: С - 72,75 %; Н 4,84 %; N - 14,17 %. (Е)-3-(4-флуорофеніл)-6-(1-фенілпроп-1-ен-2-іл)-6,7-дигідро-2Н-[1,2,4]триазино[2,31 с]хіназолін-2-он (1.9). Вихід: 50.8 %, Т. пл.: 210-217 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 8,28 (t, 2Н, 3 Ph H-2,6), 8,00 (d, J=7,7 Hz, 1H, H-11), 7,77 (s, 1H, NH), 7,43-7,21 (m, 6H, H-9, 6 Ph H-2, 3, 4, 5, 6), 7,18 (t, J=8,7 Hz, 2H, 3 Ph H-3,5), 6,93 (d, J=8,0 Hz, 1H, H-8), 6,83 (t, J=7,2 Hz, 1H, H-10), 6,61 (s, 1H, C(CH3)=CHPh), 6,11 (s, 1H, C(CH 3)=CHPh), 1,95 (s, 3Н, СН3). ЖХ-МС (XI), m/z=411 + (MH ), Розраховано для C25H19FN4O: С - 73,16 %; H - 4,67 %; N - 13,65 %. Визначено: С 73,19 %; Н - 4,72 %; N - 13,68 %. (Е)-3-(4-метилфеніл)-6-(1-хлор-2-(4-нітрофеніл)вініл)-6,7-дигідро-2Н-[1,2,4]триазино[2,31 с]хіназолін-2-он (1.10). Вихід: 69,5 %, Т. пл.: 217-219 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 8,22 (d, J=8,7 Hz, 2H, 6 Ph H-3,5), 8,14-8,04 (m, J=8,4 Hz, 3H, NH, 3 Ph H-2,6), 8,01 (d, J=7,8 Hz, 1H, H11), 7,89 (d, J=8,7 Hz, 2H, 6 Ph H-2,6), 7,39 (t, J=7,1 Hz, 1H, H-9), 7,29 (s, 1H, С(Сl)=СH) 7,23 (d, J=7,9 Hz, 2H, 3 Ph H-3,5), 6,93 (d, J=8,1 Hz, 1H, H-8), 6,84 (t, J=7,6 Hz, 1H, H-10), 6,57 (s, 1H, CH), + 2,41 (s, 3H, CH3). ЖХ-МС (XI), m/z=473 (MH ), Розраховано для C25H18CIN5O3: С - 63,63 %; H 3,84 %; N - 14,84 %. Визначено: С - 63,65 %; Н - 3,87 %; N - 14,85 %. (Е)-6-(1-хлор-2-(4-нітрофеніл)вініл)-3-(4-флуорфеніл)-6,7-дигідро-2Н-[1,2,4]триазино[2,31 с]хіназолін-2-он (1.11). Вихід: 88,3 %, Т. пл.: 264-267 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 8,27 (t, 2H, 3 Ph H-2,6), 8,22 (d, J=8,7 Hz, 2H, 6 Ph H-3,5), 8,09 (s, 1H, NH), 8,01 (d, J=7,4 Hz, 1H, H-11), 7,89 (d, J=8,7 Hz, 2H, 6 Ph H-2,6), 7,40 (t, J=7,0 Hz, 1H, H-9), 7,30 (s, 1H, C(Cl)=CH), 7,19 (t, J= 8,7 Hz, 2H, 3 Ph H-3,5), 6,93 (d, J=8,1 Hz, 1H, H-8), 6,85 (t, J=12 Hz, 1H, H-10), 6,59 (s, 1H, CH). ЖХ+ МС (XI), m/z=467 (MH ), Розраховано для C24H15CIFN5O3: С – 60,58 %; H - 3,18 %; N - 14,72 %. Визначено: С - 60,60 %; Н - 3,22 %; N - 14,77 %. 3-(4-Флуорофеніл)-6-(2-метоксифеніл)-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он 1 (1.12). Вихід: 90,6 %, Т. пл.: 215-218 °C, Н ЯМР (400 MHz, dmso-d6+ccl4) 8,16 (dd, J=7,4, 6,1 Hz, 1H, 3 Ph H-2, 6), 8,04 (d, J=7,9 Hz, 1H, H-11), 7,65 (s, 1H, 3 Ph NH), 7,34 (m, 2H, H-9, 6 Ph H6), 7,20-7,00 (m, 3H, 3 Ph H-3,5, 6 Ph H-4), 6,97-6,78 (m, 3H, CH, 6 Ph H-3,5), 3,88 (s, 3Н, ОСН3). ЖХ-МС (XI), m/z=399 (MH+), Розраховано для C 23H17FN4O2: С - 68,99 %; H - 4,28 %; N - 13,99 %. Визначено: С - 69,03 %; Н - 4,31 %; N - 14,01 %. 3-(4-Фторфеніл)-6-(4-метоксіфеніл)-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (1.13). 1 Вихід: 99,2 %, Т. пл.: 268-269 °C Н ЯМР (400 MHz, DMSO) 8,23-8,13 (м, J=6,8 Hz, 3Н, NH, 3 Ph Н-2,6), 7,94 (д, J=7,9 Hz, 1Н, H-11), 7,46 (m, J=7,6 Hz, 1H, H-9), 7,38-7,26 (м, J=7,8 Hz, 4H, 3 Ph H3,5, 6 Ph H-2,6), 6,98 (д, J=8,2 Hz, 1H, H-8), 6,94 (д, J=8,5 Hz, 2H, 6 Ph H-3,5), 6,88 (m, J=7,5 Hz, 4 UA 111245 C2 13 5 10 15 20 25 30 35 40 45 50 55 1Н, H-10), 6,74 (c, 1H, CH), 3,72 (c, 3Н, СН3). С ЯМР (100 MHz, DMSO) 5 162,11, 160.89, 159,71, 152,11, 145,47, 135,28, 131,13, 131,05, 130.48, 128,94, 128,91, 127,80, 126,86, 118,83, 115,45, + 115,27, 115,06, 114,10, 112,07, 74,26, 55,16; ЖХ-МС (XI), m/z=399 (MH ), Розраховано для C23H17FN4O2: С - 68,99 %; H - 4,74 %; N - 13,99 %. Визначено: С - 69,03 %; Н - 4,80 %; N 14,03 %. 6-(3,4-Диметоксифеніл)-3-(4-ізопропілфеніл)-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2он (1.14). Вихід: 87,3,2 %, Т. пл.: 243-245 °C 'Н ЯМР (400 MHz, dmso-d6+ccl4) 5 8,08 (d, J=8,3 Hz, 2H, 3 Ph H-2,6), 8,01 (s, 1H, NH), 7,98 (d, J=7,9 Hz, 1H, H-11), 7,39 (t, J=7,3 Hz, 1H, H-9), 7,27 (d, J=8,2 Hz, 2H, 3 Ph H-3,5), 7,03 (s, 1H, 6 Ph H-2), 6,96 (d, J=7,9 Hz, 1H, H-8), 6,89-6,73 (m, J=17,8, 8,0 Hz, 3H, H-10, 6 Ph H-5,6), 6,58 (s, 1H, CH), 3,74 (s, 1H, 4-OCH3), 3,72 (s, 1H, 3-OCH3), 3,01+ 2,91 (m, 1H, CH(CH3)), 1,28 (d, J=6,9 Hz, 3Н, СН(СН3)). ЖХ-МС (XI), m/z=456 (MH ), Розраховано для C27H26N4O3: С - 71,35 %; H - 5,77 %; N - 12,33 %. Визначено: С - 71,37 %; Н - 5,79 %; N 12,33 %. 6-(2,3-Диіхлорфеніл)-3-(4-метоксифеніл)-6,7-дигідро-2Н-[1,2,4]триазино-[2,3-с]хіназолін-2-он 1 (1.15). Вихід: 99,8 %, Т. пл.: 291-293 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 8,06 (d, J=8,4 Hz, 2H, 3 Ph), 7,90 (d, 1H, H-11), 7,60 (bs, 1H, NH), 7,44-7,22 (m, 1H, H-9, 6 Ph H-4,5), 6,99 (s, 1H, CH), 6,93+ 6,78 (m, 3Н, 3 Ph H-3,5, 6 Ph H-6), 3,83 (s, 3Н, ОСН3). ЖХ-МС (XI), m/z=452 (MH ), Розраховано для C23H16Cl2N4O2: С - 61,21 %; Н - 3,57 %; N - 12,41 %. Визначено: С - 61,24 %; Н - 3,59 %; N 12,46 % 4-(8-Метил-2-оксо-3-фенил-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-6-іл)бензойна 1 кислота (1.16). Вихід: 92,7 %, Т. пл.: 342-344 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 12,67 (s, 1H, СООН), 8,21 (d, J-6,8 Hz, 2H, 3 Ph H-3,5), 7,92-7,87 (m, 3Н, H-11, 3 Ph H-2,6), 7,60 (d, J=4,2 Hz, 1H, NH), 7,52-7,36 (m, 5H, 3 Ph H-3,4,5, 6 Ph 2,6), 7,30 (d, J=1A Hz, 1H, H-9), 6,83 (d, J=7,5 Hz, 1H, + H-10), 6,75 (d, J=4,3 Hz, 1H, CH), 2,31 (s, 3Н, СН3). ЖХ-МС (XI), m/z-411 (MH ), Розраховано для C24H18N4O3: С - 70,23 %; H - 4,42 %; N - 13,65 %. Визначено: С - 70,25 %; Н - 4,43 %; N - 13,63 %. 4-(10-Бромо-2-оксо-3-феніл-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-6-іл)бензойна 1 кислота (1.17). Вихід: 94,3 %, Т. пл.: 344-346 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 12,72 (s, 1H, СООН), 8,37 (s, 1Н, H-11), 8,13 (d, J=6,6 Hz, 2H, 6 Ph H-3,5), 8,06 (s, 1H, NH), 7,95 (d, J=8,1 Hz, 2H, 3 Ph H-2,6), 7,54-7,36 (m, 6H, H-9, 3 Ph H-3,4,5 6 Ph 2,6), 6,95 (d, J=8,7 Hz, 1H, H-8), 6,82 (s, + 1H, CH) ЖХ-МС (XI), m/z=476 (MH ), Розраховано для C23H15BrN4O3: С - 58,12 %; H - 3,18 %; N 11,79 %. Визначено: С - 58,17 %; Н - 3,21 %; N - 11,83 %. 4-(10-Бром-3-(4-флуорфеніл)-2-оксо-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-61 іл)бензойна кислота(1.18). Вихід: 80,4 %, Т. пл.: 336-338 °C Н ЯМР (400 MHz, dmso-d6+CCl4) 12,73 (s, 1H, COOH), 8,37 (s, 1H, H-11), 8,24 (dd, J=7,7, 6,1 Hz, 2H, 3 Ph H-2,6), 8,06 (s, 1H, NH), 7,95 (d, J=8,0 Hz, 2H, 6 Ph H-3,5), 7,55-7,39 (m, 3H, H-9, 6 Ph H-2,6), 7,18 (t, J=8,6 Hz, 2H, 3 Ph H+ 3,5), 6,95 (d, J=8,7 Hz, 1H, H-8), 6,82 (s, 1H, CH). ЖХ-МС (XI), m/z=494 (MH ), Розраховано для C23H14BrFN4O3: С - 56,00 %; H - 2,86 %; N - 11,36 %. Визначено: С - 56,02 %; Н - 2,89 %; N 11,37 %. Приклад 2. Загальний метод синтезу 6, 6-дизаміщених 3-R-8-R3-9-R4-10-R5-11-R6-6,7-дигідро2H-[1,2,4]триазино[2,3-с]хіназолін-2-онів. До суспензії 0.005 моль 3-(2-аміно-3-R3-4-R4-5-R5-6-R5-11-R6-феніл)-6R-1,2,4-триазин5(2Н)ону у оцтовій кислоті додають 0.005 моль кетону, суміш кип'ятять протягом 3 годин, розчин охолоджують, осад, що утворився відфільтровують, промивають 15 мл. пропанолу-2 та висушують. 3,6,6-Триметил-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2.1). Вихід: 81,1 %, Т. пл.: 1 271-273 °C Н ЯМР (400 MHz, dmso-d6+CCl4) 7,95 (d, J=7,5 Hz, 1H, H-11), 7,35 (t, J=7,5 Hz, 1H, 13 H-9), 7,30 (s, 1H, NH), 6,81 (m, 2H, H-8, 9), 2,23 (s, 3H, CH3), 1,67 (s, 6H, (CH3)2). C ЯМР (100 MHz, DMSO) 8 161,58, 152,42, 150.92, 144,75, 134,16, 126,66, 117,96, 114,86, 112,38, 95,49, + 75,74, 26,10, 17,24; ЖХ-МС (XI), m/z=243 (MH ), Розраховано для C13H14N4O: С - 64,45 %; H 5,82 %; N - 23,13 %. Визначено: С - 64,46 %; Н - 5,84 %; N - 23,15 %. 6,6-Диметил-3-феніл-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2.2). Вихід: 93,0 %, 1 Т. пл.: 291-292 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 8,18 (d, J=8,0 Hz, 2H, 3-Ph H-2,6), 8,00 (d, J7,8 Hz, 1H, H-11), 7,54-7,20 (m, 4H, H-9, 3 Ph H-3,4,5), 6,84 (m, 2H, H-8, 10), 1,78 (s, 6H, (CH3)2). + ЖХ-МС (XI), m/z=305 (MH ), Розраховано для C18H16N4O: С - 71,04 %; H - 5,30 %; N - 18,41 %. Визначено: С - 71,09 %; Н - 5,33 %; N - 18,44 %. 3-(4-Етоксифеніл)-6,6-диметил-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2,3). 1 Вихід: 88,8 %, Т. пл.: 262-263 °C Н ЯМР (400 MHz, dmso_d6+ccl4) 8,22 (d, J=8,4 Hz, 2H, 3 Ph H-2,6), 7,99 (d, J=7,8 Hz, 1H, H-11), 7,42-7,28 (m, 2H, H-9, NH), 6,94 (d, J=8,4 Hz, 2H, 3 Ph H-3,5), 6,88-6,69 (m, J=7,1 Hz, 2H, H-8, 10), 4,11 (dd, J=13,2, 6,4 Hz, 2H, ОСН2СН3), 1,77 (s, 6H, (CH3)2), 5 UA 111245 C2 + 5 10 15 20 25 30 35 40 45 50 55 60 1,43 (t, J=6,7 Hz, 3H, ОСН2СН3). ЖХ-МС (XI), m/z=349 (MH ), Розраховано для C20H20N4O2: С 68,95 %; H - 5,79 %; N - 16,08 %. Визначено: С - 68,99 %; Н - 5,81 %; N - 16,11 %. 3-(4-Флуорофеніл)-6,6-диметил-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2.4). 1 Вихід: 81,5 %, Т. пл.: 268-270 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 8,29 (t, 2Н, 3 Ph H-2,6), 7,99 (d, J=7,6 Hz, 1H, H-11), 7,42 (s, 1H, NH2), 7,39 (t, 1H, H-9), 7,21 (t, J=8,4 Hz, 2H, 3 Ph H-3,5), 6,88+ 6,71 (m, 2H, 3 Ph H-8, 10), 1,77 (s, 6H, (CH3)2). ЖХ-МС (XI), m/z=323 (MH ), Розраховано для C18H15FN4O: С - 67,07 %; H - 4,69 %; N - 17,38 %. Визначено: С - 67,11 %; Н - 4,71 %; N - 17,39 %. 6,6-Диметил-3-(тіофен-2-іл)-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2.5). Вихід: 1 98,4 %, Т. пл.: 277-278 °C Н ЯМР (400 MHz, dmso-d6+ccl4) 8,23 (s, 1H, тіофен Н-3), 7,99 (d, J=1,1 Hz, 1H, H-11), 7,67 (d, J=4,4 Hz, 1H, тіофен H-5), 7,42 (s, 1H, NH), 7,38 (t, 1H), 7,17 (t, 1H, + тіофен H-4), 6,84 (m, 2H, H-8,10), 1,77 (s, 6H, (CH3)2). ЖХ-МС (XI), m/z=311 (MH ), Розраховано для C16H14N4OS: С - 61,92 %; H - 4,55 %; N - 18,05 %. Визначено: С - 61,98 %; Н - 4,57 %; N 18,08 %. 6-Етил-3,6-диметил-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2.6). Вихід 51,5 %, Т. 1 пл.: 268-269 °C Н ЯМР (400 MHz, dmso_d6+ccl4) 7,93 (d, J=7,7 Hz, 1H, H-11), 7,30 (t, J=7,5 Hz, 1H, H-9), 7,18 (s, 1H, NH), 6,82-6,71 (m, 2H, H-8, 10), 2,22 (s, 3Н, 3-СН3), 2,18 (dd, J=14,0, 7,1 Hz, 1H, СН2СН3), 1,79 (dd, J=14,0, 7,1 Hz, 1H, CH2CH3), 1,66 (s, 3H, 6-CH3), 0.92 (t, J=7,0 Hz, 1H, 13 СН2СН3). С ЯМР (100 MHz, DMSO) 8 161,40, 152,86, 150.83, 144,86, 134,05, 126,69, 117,60, + 114,56, 111,99, 78,35, 31,16, 24,68, 17,21, 7,74,ЖХ-МС (XI), m/z-256 (MH ), Розраховано для C14H16N4O: С - 65,61 %; H - 6,29 %; N - 21,86 %. Визначено: С - 65,64 %; Н - 6,32 %; N - 21,89 %. 6-Етил-6-метил-3-(р-толіл)-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2.7). Вихід: 1 91,9 %, Т. пл.: 263-266 °C Н ЯМР (400 MHz, dmso_d6+ccl4) 8,09 (d, J=7,3 Hz, 2H, 3 Ph H-2, 6), 7,98 (d, J=7,6 Hz, 1H, H-11), 7,33 (t, 1H, H-9), 7,28 (s, 1H, NH), 7,22 (d, J=7,4 Hz, 2H, 3 Ph H-3,5), 6,88-6,68 (m, 2H, H-8, H-10), 2,42 (s, 3H, CH3), 2,28 (dd, J=13,7, 6,9 Hz, 1H, 6-СН2СНз), 1,89 (dd, J = 13,8, 6,8 Hz, 1H, 6-CH2CH3), 1,76 (s, 3Н, 6-СН3), 0.98 (t, J=6,4 Hz, 3Н, 6-СН2СН3). ЖХ-МС (XI), + m/z=333 (MH ), Розраховано для C20H20N4O: С - 72,27 %; H - 6,06 %; N - 16,86 %. Визначено: С 72,29 %; Н - 6,10 %; N - 16,87 %. 6-Етил-3-(4-ізопропілфеніл)-6-метил-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2.8). 1 Вихід: 71,7 %, Т. пл.: 268-269 °C Н ЯМР (400 MHz, dmso_d6+ccl4) 8,10 (d, J=7,9 Hz, 1H, 3 Ph H2,6), 7,98 (d, J=7,7 Hz, 1H, H-11, 7,33 (t, 1H, H-9), 7,29 (d, 3H, NH, 3 Ph H-3,5), 6,92-6,63 (m, 2H, H8, 10), 2,96 (dd, J = 13,6, 6,8 Hz, 1H, CH(CH3)2), 2,28 (dt, J=13,3, 6,7 Hz, 1H, 6-CH2CH3), 1,90 (td, J = 13,7, 6,6 Hz, 1H, 6-CH2CH3), 1,76 (s, 3H, 6-CH3), 1,29 (d, J=6,7 Hz, 6H, СH2СН3)), 0.98 (t, J=7,0 + Hz, 3Н, 6-СН2СН3)). ЖХ-МС (XI), m/z=361 (MH ), Розраховано для C22H24N4O: С - 73,31 %; H 6,71 %; N - 15,54 %. Визначено: С - 73,34 %; Н - 6,73 %; N - 15,57 %. 3-(3,4-Диметилфеніл)-6-етил-6-метил-6,7-дигідро-2Н-[1,2,4]триазино[2,3-хіназолін-2-он (2.9). 1 Вихід: 86,1 %, Т. пл.: 268-269 °C Н ЯМР (400 MHz, dmso_d6+ccl4) 7,98 (d, J=7,8 Hz, 1Н, H-11), 7,94 (s, 1H 3 Ph H-2), 7,88 (d, J=7,8 Hz, 1H, 3 Ph H-6), 7,33 (t, J=7,5 Hz, 1H, H-9), 7,27 (s, 1H, NH), 7,16 (d, J=7,7 Hz, 1H, 3 Ph H-5), 6,88-6,71 (m, 2H, H-8, 10), 2,34 (s, 3H, 4-CH3), 2,32 (s, 3H, 3-CH3), 2,30-2,20 (dd, J=14,0, 6,8 Hz, 1H, 6-CH2CH3), 1,89 (dd, J=14,0, 6,8 Hz, 1H, 6-СНзСНз), 1,76 (s, 3H, + 6-CH3), 0.98 (t, J=6,9~Hz, 1H, 6-СН2СН3). ЖХ-МС (XI), m/z-399~(MH ), Розраховано для C21H22N4O: С - 72,81 %; H - 6,40 %; N - 16,17 %. Визначено: С - 72,84 %; Н - 6,41 %; N - 16,18 %. 3-(4-Етоксифеніл)-6-етил-6-метил-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2.10). 1 Вихід: 99,2 %, Т. пл.: 235-238 °C Н ЯМР (400 MHz, dmso_d6+ccl4) 8,20 (d, J=8,0 Hz, 2H, 3 Ph H2,6), 7,97 (d, J=7,7 Hz, 1H, H-11), 7,32 (t, J=7,4 Hz, 1H, H-9), 7,26 (s, 1H, NH), 6,91 (d, J=8,0 Hz, 2H, 3 Ph H-3, 5), 6,86-6,70 (m, J=17,0, 8,0 Hz, 2H, H-8, 10), 4,10 (dd, J=12,9, 6,2 Hz, 2H, OCH2CH3), 2,28 (dd, J=14,1, 7,0 Hz, 1H, 6-CH2CH3), 1,87 (dd, J-14,1, 7,0 Hz, 1H, 6-CH2CH3), 1,76 (s, 3Н, 6СН3), 1,43 (X, J=6,3 Hz, 3Н, ОСН2СН3), 0.98 (t, J=6,7 Hz, 3H, -6-СН2СН3). ЖХ-МС (XI), m/z=363 + (MH ), Розраховано для C21Н22N4O2: С - 69,59 %; H - 6,12 %; N - 15,46 %. Визначено: С - 69,62 %; Н - 6,15 %; N - 15,49 %. 6-Етил-6-метил-3-(тіофен-2-іл)-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2.11). 1 Вихід: 86,6 %, Т. пл.: 246-247 °C Н ЯМР (400 MHz, dmso_d6+ccl4) 8,22 (d, J=2,1 Hz, 1H, тіофен H-3), 7,98 (d, J=7,7 Hz, 1H, H-11), 7,59 (d, J=4,5 Hz, 1H, тіофен H-5), 7,32 (m, 2H, H-9, NH), 7,14 (t, 1H, H-4), 6,80 m, 2H, H-8, H-10), 2,28 (dd, J=14,0, 7,1 Hz, 1H, 6-CH2CH3), 1,88 (dd, J=14,0, 7,1 Hz, + 1H, 6-СН2СН3), 1,76 (s, 3Н, 6-СН3), 0.97 (t, J=6,9 Hz, 3Н, 6-СН2СН3)- ЖХ-МС (XI), m/z=325 (MH ), Розраховано для C17H16OS: С - 62,94 %; Н - 4,97 %; N - 17,27 %. Визначено: С - 62,96 %; Н 4,98 %; N - 17,29 %. 6-Гексил-3,6-диметил-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2.12). Вихід: 1 44,9 %, Т. пл.: 143-147 °C Н ЯМР (400 MHz, dmso_d6+ccl4) 7,93 (d, J=7,5 Hz, 1H, H-11), 7,29 (t, J=6,9 Hz, 1H, H-9), 7,17 (s, 1H, NH), 6,84-6,69 (m, 2H, H-8, 10), 2,22 (s, 3H, CH3), 2,18-2,01 (m, 1H, CH2CH2CH2CH2CH2CH3), 1,85-1,60 (m, 4H, CH2CH2CH2CH2CH2CH3 6-CH3), "1,45 1,08 (m, 8H, 6 UA 111245 C2 CH2CH2CH2CH2CH2CH3), 0.85 (t, 3Н, СН3). С ЯМР (100 MHz, DMSO) 152,76, 150.82, 144,81, 134,19, 126,67, 126,66, 117,61, 114,56, 111,93, 99,41, 78,05, 38,12, 30.96, 28,54, 25,04, 22,73, + 21,93, 17,24, 13,71; ЖХ-МС (XI), m/z=313 (MH ), Розраховано для C18H24N4O: С - 69,20 %; H 7,74 %; N - 17,93 %. Визначено: С - 69,25 %; Н - 7,76 %; N - 17,97 %. 6-Гексил-6-метил-3-феніл-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2.13). Вихід: 1 60.6 %, Т. пл.: 169-190 °C Н ЯМР (400 MHz, dmso_d6+ccl4) 8,17 (d, J-6,9 Hz, 1H, 3 Ph H-2, 6), 7,99 (d, J=7,7 Hz, 1H, H-11), 7,53-7,38 (m, J=15,7 Hz, 3H, H-3, 4, 5), 7,34 (t, J=7,6 Hz, 1H, H-9), 7,29 (s, 1H, NH), 6,89-6,67 (m, 2H, H-8, 10), 2,23 (t, J=12,5 Hz, 1H, CH2CH2CH2CH2CH2CH3), 1,83 (t, J12,5 Hz, 1H, CH2CH2CH2CH2CH2CH3), 1,76 (s, - 3Н, 6-СН3), 1,51-1,32 (m, 1H, CH2CH2CH2CH2CH2CH3), 1,24 (s, 6H, CH2CH2CH2CH2CH2CH3), 0.84 (t, 3H, + СН2СН2СН2СН2СН2СН3). ЖХ-МС (XI), m/z=375 (MH ), Розраховано для C23H26N4O: С - 73,77 %; H - 7,00 %; N - 14,96 %. Визначено: С - 73,80 %; Н - 7,04 %; N - 15,01 %. 6-Гексил-6-метил-3-(р-толіл)-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2.14). Вихід: 1 67,9 %, Т. пл.: 173-174 °C Н ЯМР (400 MHz, dmso_d6+ccl4) 8,09 (d, J=7,7 Hz, 2H, 3 Ph H-2,6), 7,98 (d, J=7,7 Hz, 1H, H-11), 7,33 (t, J=7,5 Hz, 1H, H-9), 7,27 (s, 1H, NH), 7,22 (d, J=7,7 Hz, 2H, 3 Ph H-3,5), 6,88-6,70 (m, J=11,6, 7,9 Hz, 2H, H-8, 9), 2,42 (s, 3H, CH3), 2,23 (m, 1H, CH2CH2CH2CH2CH2CH3, 1,87-1,77 (m, 1H, CH2CH2CH2CH2CH2CH3), 1,75 (s, 1H, 6-CH3), 1,48-1,31 (m, 2H, CH2CH2CH2CH2CH2CH3), 1,24 (s, 3Н, CH2CH2CH2CH2CH2CH3), 0.84 (t, 3H, + CH2CH2CH2CH2CH2CH3). ЖХ-МС (XI), m/z=389 (MH ), Розраховано для C24H28N4O: С - 74,2 %; H 7,26 %; N - 14,42 %. Визначено: С - 74,23 %; Н - 7,30 %; N - 14,45. 3-(4-Флуорфеніл)-6-гексил-6-метил-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2,15). 1 Вихід: 61,1 %, Т. пл.: 268-269 °C Н ЯМР (400 MHz, dmso_d6+ccl4) 8,34-8,18 (m, 2Н, 3 Ph H-2,6), 7,98 (d, J=1,1 Hz, 1H, H-11), 7,41-7,22 (m, 2H, H-9, NH), 7,16 (t, J=8,2 Hz, 2H, 3 Ph H-3,5), 6,886,71 (m, 2H, H-8, 10), 2,21 (t, J=12,3 Hz, 1H, CH2CH2CH2CH2CH2CH3), 1,82 (t, J=12,3 Hz, 1H, CH2CH2CH2CH2CH2CH3), 1,76 (s, 3H, 6-CH3), 1,51-1,32 (m, 2H, CH2CH2CH2CH2CH2CH3), 1,24 (s, + 6H, CH2CH2CH2CH2CH2CH3), 0.83 (s, 3H, CH2CH2CH2CH2CH2CH3). ЖХ-МС (XI), m/z=393 (MH ), Розраховано для C23H25FN4O: С – 70,39 % Н - 6,42 %; N - 14,28 %. Визначено: С - 70,43 %; Н 6,47 %; N - 14,32 %. 6-Гексил-6-метил-3-(тіофен-2-іл)-6,7-дигідро-2Н-[1,2,4]триазино[2,3-с]хіназолін-2-он (2.16). 1 Вихід: 39,8 %, Т. пл.: 170-172 °C Н ЯМР (400 MHz, dmso_d6+ccl4) 8,22 (s, 1Н, тіофен H-3), 7,98 (d, J=7,5 Hz, 1H, H-11), 7,59 (d, J=4,3 Hz, 1H, тіофен H-5), 7,33 (m, 1H, H-9), 7,29 (s, 1H, NH), 7,14 (t, 1H, тіофен Н-4), 6,86-6,70 (m, 1H, H-8, 10), 2,24 (t, J=12,1 Hz, 1H, CH2CH2CH2CH2CH2CH3), 1,82 (t, J=12,3 Hz, 1H, CH2CH2CH2CH2CH2CH3), 1,74 (s, 1H, 6-CH3), 1,50-1,33 (m, 2H, CH2CH2CH2CH2CH2CH3), 1,33-1,09 (m, 6H, CH2CH2CH2CH2CH2CH3), 0,84 (t, 3Н, + CH2CH2CH2CH2CH2CH3). ЖХ-МС (XI), m/z=381 (МН ), Розраховано для C21H24N4OS: С - 66,29 %, Н - 6,36 %; N - 14,72 %. Визначено: С - 66,32 %; Н - 6,39 %; N - 14,74 %. Таким чином, заявлено нові 6-моно- та 6,6-дизаміщені 3-R-8-R3-9-R4-10-R5-11-R6-6,7-дигідро2Н-[1,2,4]триазино[2,3-с]хіназолін-2-они, які можуть бути відтворені в умовах вітчизняних промислових хіміко-фармацевтичних підприємств з використанням стандартного обладнання, синтезовані з доступних вихідних реагентів та використані у спрямованому пошуку біологічно активних речовин як перспективних лікарських засобів. 13 5 10 15 20 25 30 35 40 ФОРМУЛА ВИНАХОДУ 45 6-Монота 6,6-дизаміщені с]хіназолін-2-они формули: R3 R4 H N R2 R1 N R5 R6 N N R O 50 3-R-8-R3-9-R4-10-R5-11-R6-6,7-дигідро-2H-[1,2,4]триазино[2,3 , в якій 7 UA 111245 C2 5 R означає водень, алкіл-, алкеніл-, R7-фенілалкіл-, R7-фенілалкеніл-, R7-феніл, R8-гетерил; R1, R2 кожний незалежно один від одного означає водень, алкіл-, алкеніл-, трихлорометил-, карбоксил-, карбоксіалкіл-, алкоксикарбоніл-, R7-фенілацил-, R7-фенілалкіл-, R7-феніл, R8гетерил; R3, R4, R5, R6 кожний незалежно один від одного означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміно- та алкіламіногрупи, алкоксикарбоніл- або гідроксикарбонільні групи; R7-феніл означає Ra 1 Ra Ra 5 Ra Ra 10 15 20 2 3 4 , де Ra1 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміноалкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra2 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміноалкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra3 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміноалкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra4 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміноалкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra5 означає водень, алкіл, феніл, алкоксигрупу, галоген, гідроксигрупу, нітрогрупу, аміноалкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл, R8-гетерил означає Ra 2 Ra 2 Ra Ra , X 1 Ra 3 , Ra 2 X N , Ra 2 Ra 4 Ra 3 N X Ra , Ra 1 2 X та та Ra , 1 Ra 5 4 Ra 3 Ra X та N X Ra Ra 1 N та Ra 1 1 N Ra 3 та , X Ra 2 Ra Ra 1 5 X , Ra 2 1 , 25 30 35 де X означає О, N, S; Ra1 означає водень, алкіл, феніл, алкоксигрупу, галоген, алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra2 означає водень, алкіл, феніл, алкоксигрупу, галоген, алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra3 означає водень, алкіл, феніл, алкоксигрупу, галоген, алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra4 означає водень, алкіл, феніл, алкоксигрупу, галоген, алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл; Ra5 означає водень, алкіл, феніл, алкоксигрупу, галоген, алкіламіногрупи, алкоксикарбоніл або гідроксикарбоніл. гідроксигрупу, нітрогрупу, аміно- та гідроксигрупу, нітрогрупу, аміно- та гідроксигрупу, нітрогрупу, аміно- та гідроксигрупу, нітрогрупу, аміно- та гідроксигрупу, нітрогрупу, аміно- та Комп’ютерна верстка І. Скворцова Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 8
ДивитисяДодаткова інформація
Назва патенту англійською6-mono- and 6,6-disubstituted 3-r-8-r3-9-r4-10-r5-11-r6-6,7-dihydro-2h-[1,2,4]triazino[2,3-c]quinazolin-2-ones
Автори англійськоюVoskoboinik Oleksii Yuriiovych, Kolomoiets Oleksandra Serhiivna, Kovalenko Serhii Ivanovych, Berest Halyna Hryhorivna, Kholodniak Serhii Valeriiovych, Serheieva Tetiana Yuriivna, Okovytyi Serhii Ivanovych, Palchikov Vitalii Oleksandrovych
Назва патенту російською6-моно- и 6,6-дизамещенные 3-r-8-r3-9-r4-10-r5-11-r6-6,7-дигидро-2н-[1,2,4]триазино[2,3-с]хиназолин-2-оны
Автори російськоюВоскобойник Алексей Юрьевич, Коломоец Александра Сергеевна, Коваленко Сергей Иванович, Берест Галина Григорьевна, Холодняк Сергей Валерьевич, Сергеева Татьяна Юрьевна, Оковитый Сергей Иванович, Пальчиков Виталий Александрович
МПК / Мітки
МПК: C07D 253/06, C07D 487/04, C07D 239/72, C07D 253/10
Мітки: 6-моно, 6,6-дизаміщені, 3-r-8-r3-9-r4-10-r5-11-r6-6,7-дигідро-2н-[1,2,4]триазино[2,3-с]хіназолін-2-они
Код посилання
<a href="https://ua.patents.su/10-111245-6-mono-ta-66-dizamishheni-3-r-8-r3-9-r4-10-r5-11-r6-67-digidro-2n-124triazino23-skhinazolin-2-oni.html" target="_blank" rel="follow" title="База патентів України">6-моно- та 6,6-дизаміщені 3-r-8-r3-9-r4-10-r5-11-r6-6,7-дигідро-2н-[1,2,4]триазино[2,3-с]хіназолін-2-они</a>
Попередній патент: Вироби із волоконних джгутів з високим деньє елементарної нитки і низьким загальним деньє
Наступний патент: Прогресивне кодування позиції останнього значущого коефіцієнта
Випадковий патент: Спосіб отримання екстрактів з насіння озимої і ярої форм ріпаку методом холодного пресування за допомогою преса шнекового