Спосіб підвищення вмісту 1r-транс s-, 1s-транс r-, 1r-цис s- та 1s-цис r-ізомерів кристалізуємого піретроіда
Формула / Реферат
Способ повышения содержания 1R-транс S-, 1S-транс R-, 1R цис S- и 1S-цис R-изомеров кристаллизуемого пиретроида общей формулы
где R1- дигалоидвинил;
R2 - фенокси при n=1 или R2 - фенокси и фтор при n=2, проявляющею высокую инсектицидную активность, путем образования суспензии исходной смеси кристаллизуемого пиротроида, имеющею асимметрический атом углерода, к которому присоединяется эпимеризуемый протон, в жидкой среде - алифатическом углеводороде, контактирования суспензии с основанием о присутствии катализатора в жидкой среде - алифатическом углеводороде, в которой целевые изомеры не растворяются, затем полученные кристаллические изомеры выделяют из жидкой среды, отличающийся тем, что обработку ведут в среде углеводорода с 5-8 атомами углерода при массовом соотношении исходная смесь:углеводород:основание:катализатор 1:1-4,0,05-0,1:0,01-0,1, используют катализатор -четвертичные аммонийные соединения или краун эфир, растворимый в жидкой среде, реакционную смесь перемешивают в течение 2-24 ч при 5-35°С.
Текст
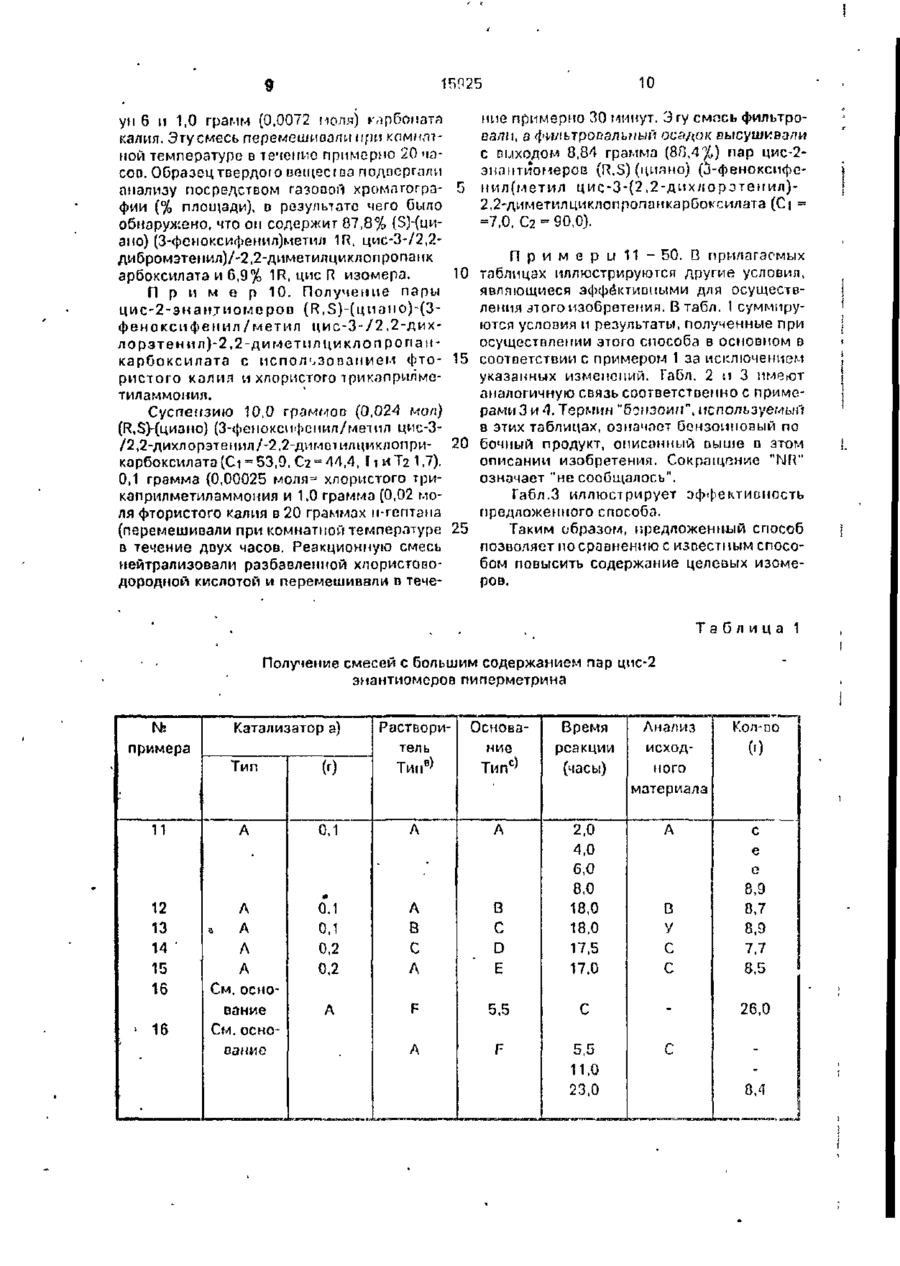
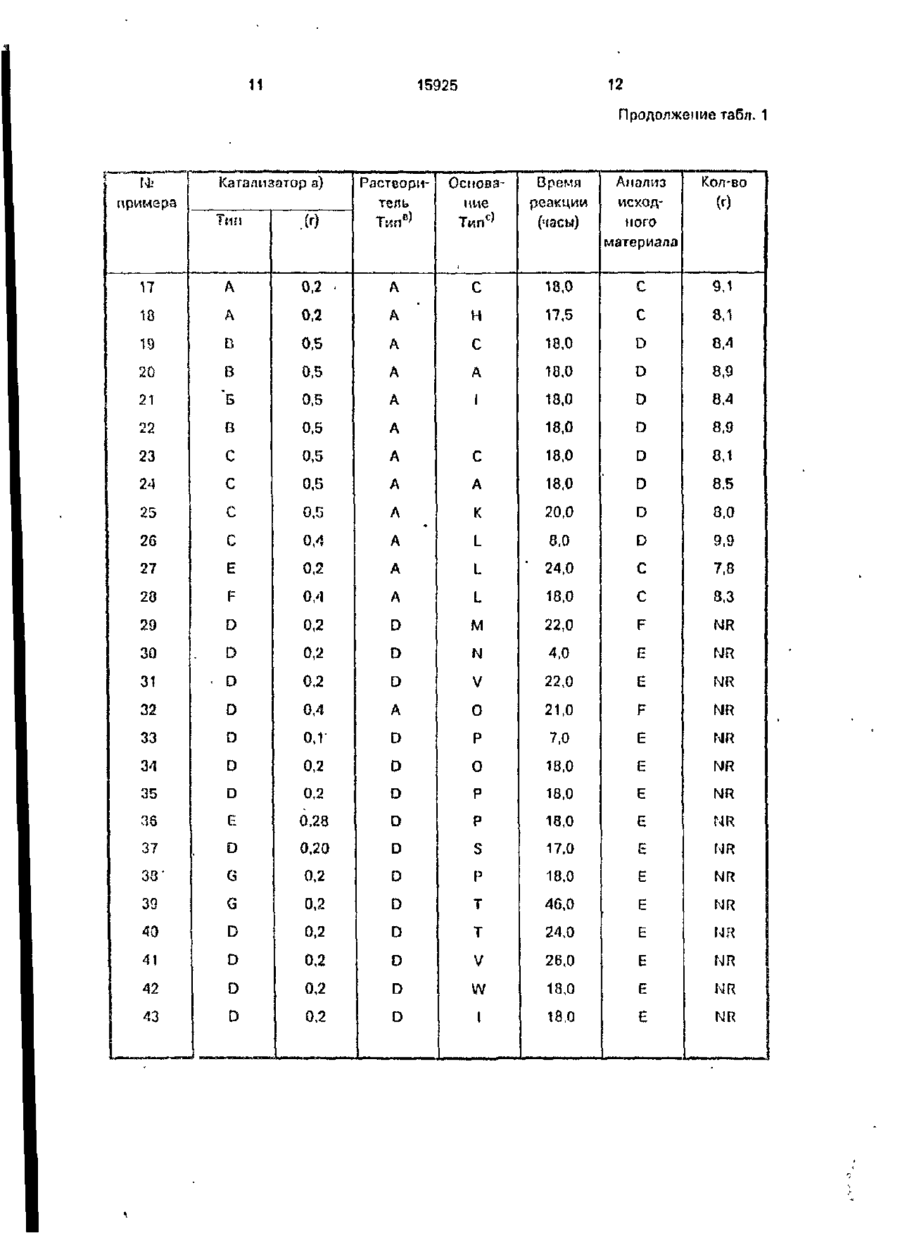
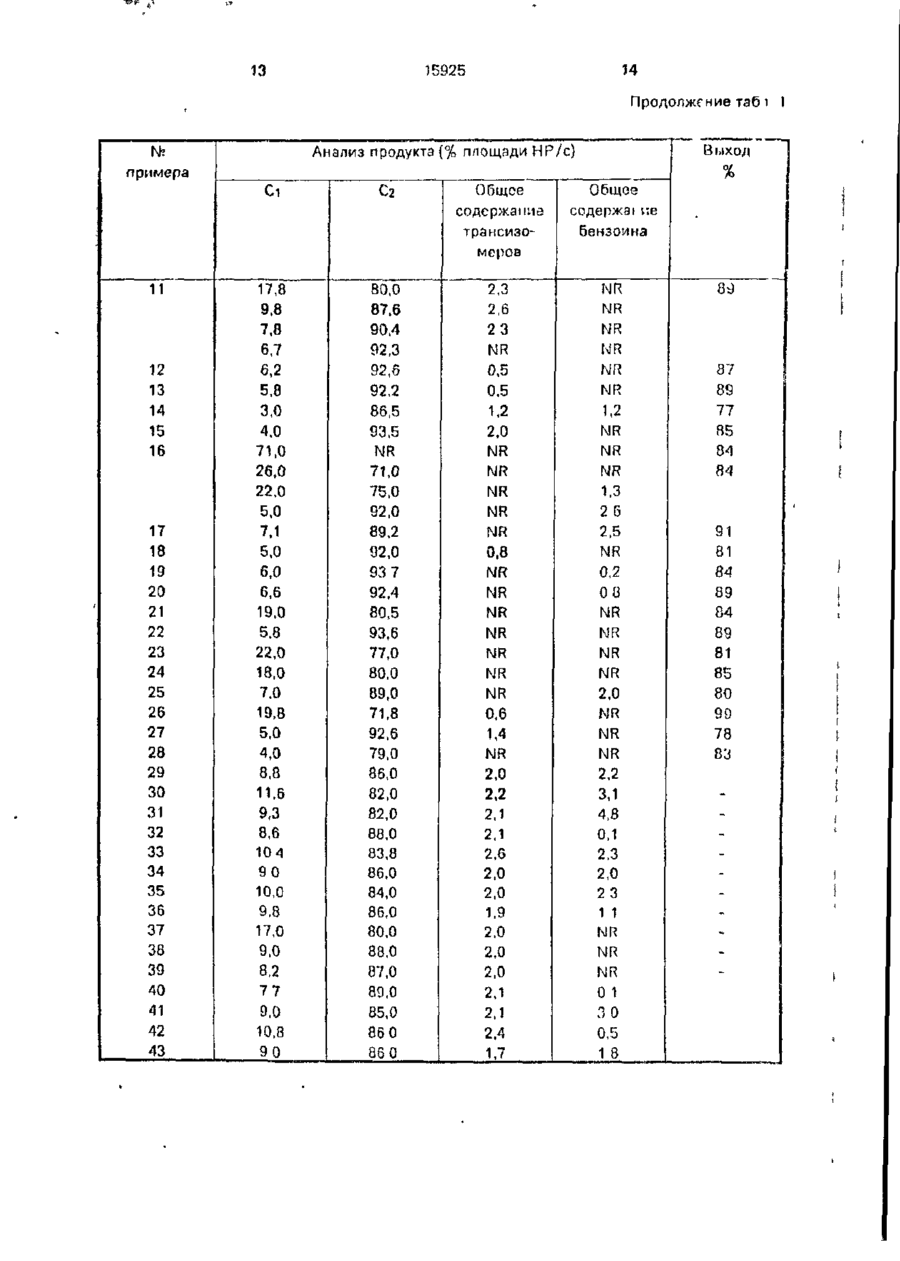
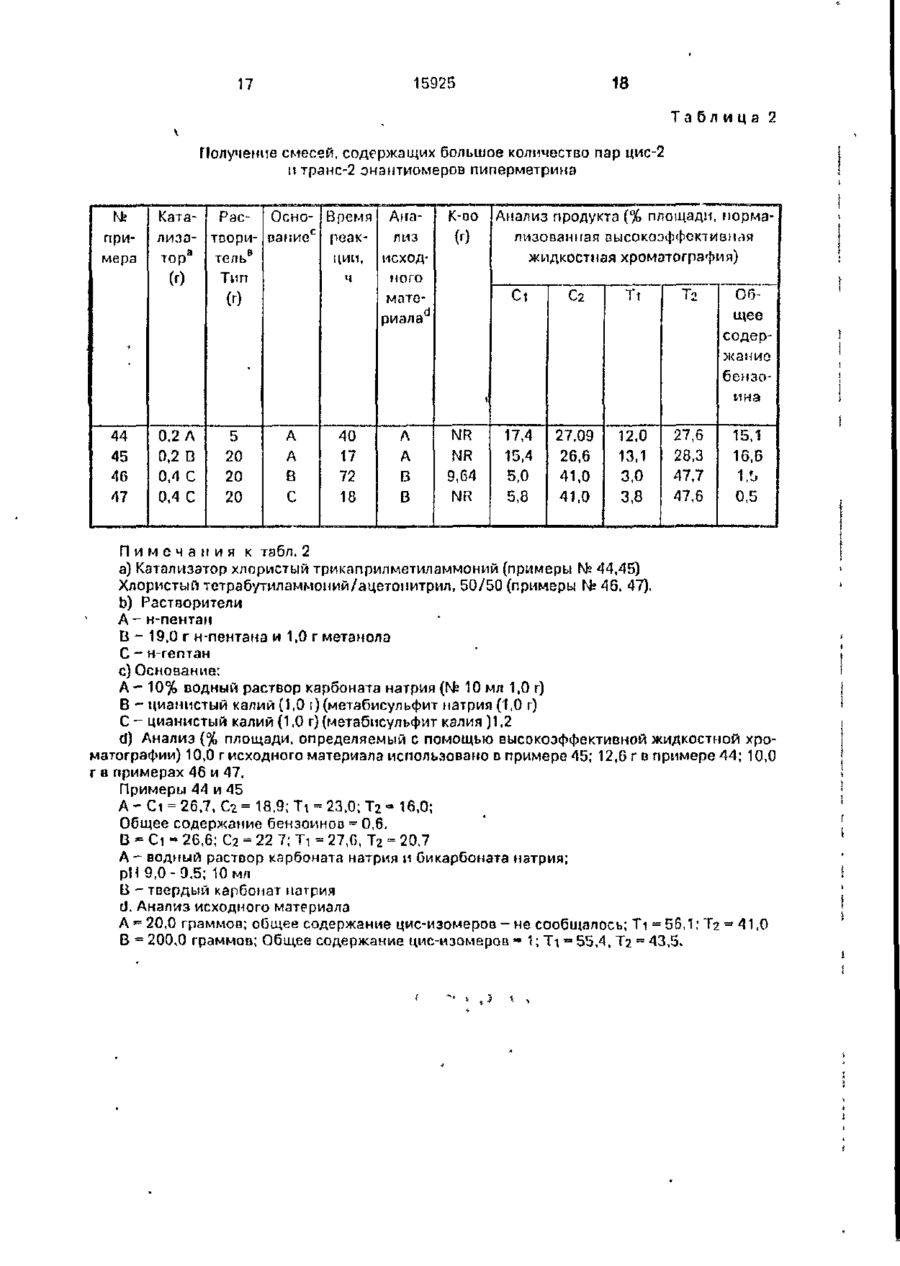
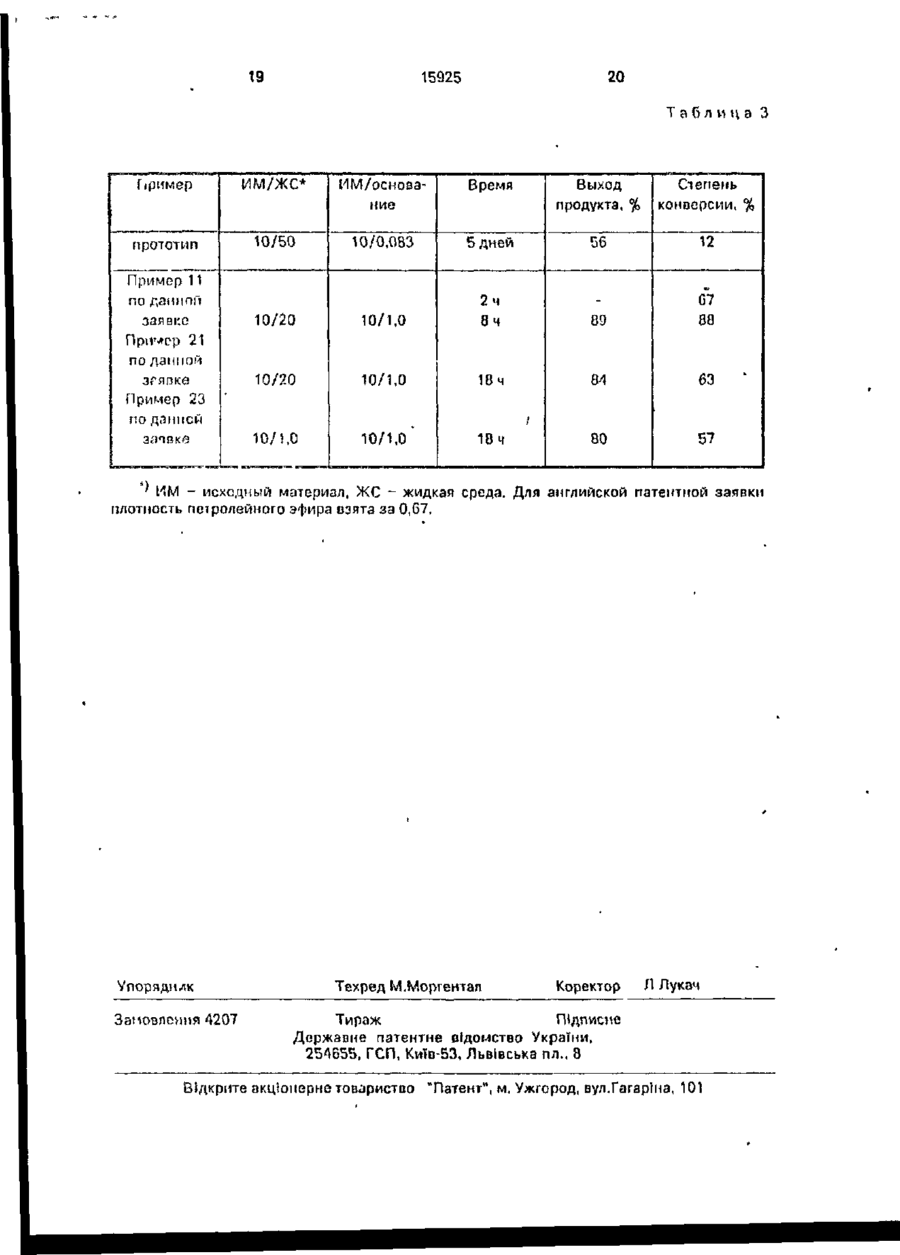
УКРЛЇІ-ІЛ ДСРЖЛВНЕ ПАТЕНТНЕ ВІДОМСТВО 5 O9R ilt) ~ІА ВИНАХІД (54) СПОСІБ ПІДВИЩЕННЯ ВМІСТУ 1П-ТРЛМС S-, 1S-TPAMC R-, IR-ЦИС S- ГА 15-ЦИС R-ІЗОМЕРІВ КРИСТАЛІЗУЄМСЯ О ПІРЕТРОІДА 1 (20)95320209, 15.10 93 (21)4742720/SU (22) 14 12 89 (24)30 00.97 {31)87062274 (32) 15.06 87 (33) US (46)30.06.97, Бгал. Г* 3 2 (50) Патент Великобритании №2064528, кл. С 07 С 121/75. 1981. (72) Джон ВІмфрІд Ейджер (US) (73) ФМК Корпорейшн (US) (57) Способ повышения содержания 1Rтранс S-, lS-трапс R-, 1R цис S- и IS-цис R-изомєров кристаллизуемого пиретроида общем формулы сн 3 где Ri - дигалоидвинил; R2 - феноксм при п = 1 или ЇІ2 ~ фемокси и фтор при п = 2, проявляющею высокую имсекіиі^ідпую актиомость, путем образосамия суспензии исходной смеси кристаллизуемого пиротроида. имеющею асимметри'юсш'і атом углерода, к которому присоединяется эпимеризуемый протон, в жидкой среде - алифаі ичсском углеводороде, контактиропанич суспгмоии с основанием о присутствии катализатора в жилкой средо - алифатическом углеводороде, в кото Изобретете ОТНОСИТСЯ к области пиретроидов, в частности, к уговершемствовэиному способу повыиюнич содержания lR-транс S, 13-транс R, lR-цис S и 15-цис R изомеров кристаллизуемого пирегроида, проявляющего пысокую инсектицидную активность, общей формулы ( рой целевые изомеры не растворяются, затем попучеиные кристаллические изомеры выделяют из жидкой среды, о т л и ч а ю щ и й с я тем, что обработку ведут п средоут леводородл с 5*8 атомами углерода при массопом соотношении исходная смссь:углеводород.оспование.катализатор 1 1-4,0,050,1 "0,01-0,1, используют катализатор четвертичные аммонийные соединонит или краун эфир, растооримый в жидкой среде, реакционную смесь перомешиззют в течение 2-2^ ч приБ-35°С V о ел 15925 где Rj - ДШЙПОИДОМКИЛ; R2 ~ фенокси при п^1 или R2 ~ фепокси и фтор при п=2, которые используют в сельском хозяйстве. Известен способ повышении содержания изомеров формулы I путем образования суспензии исходной смеси кристаллизусмою ппретроидз, имеющего асимметрический аюм уїлерода, к которому присоединяется зпимеризуемый протон, в жидкой среде алифатическом углеводороде, контактирования суспензии с основанием D присутствии к а т а л и з а т о р а в ж и д к о й среде алифатическом углеводороде, и в которой целевые изомеры нс растворяются, затем полученные кристаллические изомеры выделяют из жидкой среди, отличительной особенностью которого является то, что обработку ведут о среде углеводорода с 5-8 атомами углерода при массовом соотношении исходпии смеси, углеподород:осиование; к а т а л и з а т о р , р а в н о м 1:(1-4) : (0,050,1);(0,01-0,1), используют катализатор-четвертичные аммонийные соединения или крауюфир,' растворимые в жидкой среде, реакционную смесь перемешивают в течение; 2-24 часов при температуре 5-35°С. Смесь изомеров, где Пі - дигалоидвинил, R2-фтор и фенокси называется цифлубрин, где Ri - дигомоидвил, п = 1, R2 ~ Фонокси, - пнперметрин. Пипермстрин включает четыре цис/ - в четыре трапсизомера, обозначенные I-VIII следующим образом: Цис-изомеры 1.(5) (а-циано) (З-феноксифемил)метил 1R, цис-3-(2,2-дижлорзтенил)-2,2-диметилциклопропаикарбоксилат (сокращенно 1R,цис S) П. (R) (а-циано) (З-феноксифенил)метил 1S, цис-3-{212-дихлорэтил)-2,2-диметилциклопропанкарбоксилат (сокращенно 1S, цис R). III. (S) (а циамо) (З-феноксифеиил)метил 1S, цис-3-(2,2-д''1хлорэтенил)-2,2-дпметилциклопроппикарСоксилат (сокращенно IS, цис S). 5 10 15 20 25 30 35 40 ^5 IV. (Р}(а-циапо)о(3-феноксифєиил)мєтил 1R, цис-3(2,2-дихлорзгснил) 2,2-дихлорэтенпл) 2,2-диметилциклопропанкарбоксилат 50 (сокращенно 1П, цисЯ) Транс-изомеры V. Транс-изомер соединения I (сокращенно IR транс S) VI. Транс-изомер соединения 1 (сокра- 55 1 щено 1S, транс R). VII. Транс-изомер соединения Мі) сокращенно 1S. транс S). VIII. Транс-изомер соединения IV (сокращенно i n , трапе R) 4 Цифлутрин и другие гшретроиды, к которым относится 5то изобретение, представляют аналогичные смеси изомеров. Известно, что наибольшей инсектицидной активностью из вышеуказанных восьми изомеров обладают изомеры I и V и что пары эпаитиомеров 1(11) сокращенно цис-2/ и V(V1) сокращенно трамс-2/ являются более активными в инсектицидном отношении, чем пары знантстомеров III (IV) сокращенно цис-1) и V1I/VIII) сокращенно транс-1). Чрезвычайно трудно и экономически невыгодно отделять более активные изомеры, такие как I и V, от сложных смесей изомеров, полученных в результате обычного синтеза пиретроидов. Поэтому усилия, направленные на создание более активных а пестицидном отношении пиретроидов, были сосредоточены на методах превращений менееактмппых изомеров в процессе синтеза целевых смесей в более активные изомеры, т.е. на обогащении смесей изомеров в отношении более активных изомеров, что позволяет избежать сложных процедур разделения и потерь, связанных с уничтожением менее активных изомеров. Тем не менее, даже в тех случаях, когда смеси изомеров обогащались, а не разделялись, процедуры превращения оставались экономически невыгодными из-за низкого выхода, обычно из-за образования нежелательного побочного продукта, обычно часто включающего столько же изомеров, что и целевой продукт, и из-за многочисленных этапов, требующих большой затраты времени, высоких температур и/или необходимости регенерации дорогостоящих реагентоо. В случае циперметрина основным побочным продуктом является ( S )-2-оксо-1,2-бис-(3феноксифенил)этил цис- и транс-3-(2,2-дихлорэтенил)-2,2-диметилциклопропанкарбок- силат, причем эту смесь, содержащую восемь изомеров, обычно называют "бензоиновым побочным продуктом". Аналогичные побочные продукты встречаются при синтезе других пиретроидов, таких как цифлутрин. Следующие примеры далее иллюстрируют это изобретение. В этих примерах термины цис, транс, цис-1, цис-2,транс-1 итранс-2 относятся к изомерам и парам энантиомеров пиперметрина или цифлутрина, описанным выше в соответствии с данным случаем. В каждом случае название соединения с последующим указанием результатов анализа, выполненного с помощью жидкостной хроматографии (процентное значение площади), далее сокращается следующим образом: Сі = пара цис-1 энантиомеров; Сг = пара цис-2 энэнтиомероэ; 15925 Ті = пара трамс-1 энапнюмеров: Тг *• паратранс-2 энантиомероо; Ві = пара цис-1 онантиомеровбензоиновых побочных продуктов; В? = пара цис-2 энамтиомеров бензоино- 5 вых побочных продуктов; В з = пара транс-1 эиантиомеров бензоиновых побочных продуктов, и В/] = пара транс-2 энаитиомеров бензоиновых побоч10 ных продуктов П р и м е р ! . Получение с помощью водного раствора МагСОз смеси, содержащей большое количество пар цис-2 энаитиомеров пиперметрина К перемешанной смеси 10,0 граммов 15 (0,024 моля) (R, БМциано) (3-феноксифенил)мстил цис-3-(2,2-ди-хлорэгенил)'2,2-дпметилциклопропанкэрбоксилата (Сі - 53,8, Сг = 42,0, Ті - 2,8 и Т = 1,2) в 20 г н-гепгапа добавляли 0,1 грамма (0,00025 моля) хлори- 20 стого трикаприлметиламмония (Аликвот ® 336, Элдрич кемикал компани) и 10 мл 10% водного раствора карбоната натрия. Эту смесь перемешивали при комнатной температуре о течение пяти часов Затем добавля- 25 ли еще 0,1-граммэ хлористого трикаприлметиламмония, после чего эту смесь перемешивали при комнатной температуре в течение 13 часов. Эту реакционную смесь фідльтровали с выходам 8,37 граммов 30 (83,7%) пары цис-2 энантиомеров (Я,Б)-(циано)(3-феноксифепил) метил цис-3-(2,2-дихлорэтенилУ2,2-диметилциклопропанкарбокси лата в виде твердого вещества (Сі = 4,0, Сг = 94,0, Ві = 1,1 иВ2=-0,6) 35 П р и м е р 2. Получение с помощью твердого №2СОз смеси, содержащей большое количество пар цис-2 энангиомеров пиперметрина. Раствор сырой реакционной смеси анализировали с помощью жидкостной хроматографии, которая позволила установить наличие 30,88% (R,S) (циано)(3-феноксифенил) метил-цис-3-(2,2-дихлорэтемил)2,2-диметилциклопропачкарбоксилата в смеси гептаиоо. Раствор смеси гептанов удаляли из 32.4 граммового образца раствора с выходом 9,96 граммов цис-изомероо пиперметрина, который анализировали посредством жидкостной хроматографии, позволившей установить наличие следующих изомеров- Ci = 52.56, С2 = 41,56, T-j- 2,6 и Тг= 2,7. В другой 32,4 граммовый образец этого раствора вносили затрпвку в виде кристаллов пиперметрина с высоким содержанием цис-изомера (по крайней мере 50%) и перемешивали при комнатной температуре в течение 18 часов до кристаллизации. Эту смесь обрабатывали 0,1 грамма (0,00025 моля) хлористого трикаприлметиламмония и 40 45 50 55 0,5 грамма твердого карбона га натрия. Эту смесь перемешивали при комнатной температуре в течение четырех часоа, причем па протяжении этого времени добавляли еще 0,1 грамма хлористого трикаприлметиламмония. Реакционную суспензию перемешивали еще в течение 3,0 чзеоо при комнатной температуре Реакционную смесь разОпвляли 15 мл водного раствора, содержащего 2,0 грамма концентрированной, хлористоводородной кислоты для нейтрализации NagCCh и перемешивали в течение 10 минут. Эту смесь фильтровали с выходом 7,06 граммоп (71%) пары цис-2-энэнтиомероо (S)-(HMOно)(3-фемоксифенил)-метил цис-3 (2,2-дихЛОрЭТОНИЛ)2,2-ДИМетИЛЦИКЛОПрОП,"3,ЧКЛрбОК силата в виде твердого вещества (Сі ^ 4,0, Сг *• 95 0,Т2 = 0,6, В 2 -0,3) П р и м е р З . Получение смеси, содержащей большое количество пар цис-2 и транс-2 энантиомеров пиперметрина Перемешанную смесь 10,0 ірлммов мгептана и 10,0 граммов 10% водного растиора карбоната натрия охлаждали до 10°С. К этой смеси добавляли затравочные кристаллы (R, S) (циэмо) (З-феноксифенпл)-метил цис/3-(2,2-дихлорзтенил)-2,2-димеіилциклопропанкарбоксилата(Сі = 54, Сг = 42, Ті = З, Ї2 = 1) При поддержании температуры, равной 10°С, к этой смеси по каплям добавляли в течение 12 часов раствор, состоящий из 10.0 граммов (0,024 моля) (R.S) (циано) (3-феноксифенил) метил, цис, тракс-3(2,2дихлорэтенил)-2,2'Димстилциклог,ропапкарбоксилата (Сі =26,7, С2 = 18,9, Ті = 23,0, Т2 = 15 и В2 * 0,6) и 0,2 грамма (0.005 моля) хлористого трикаприлметиламмония в 10,0 граммах н-гептана до образования суспензии. После окончания добавления эту суспензию перемешивали при температуре 10°С еще в течение 18 часов. Эту смесь фильтровали с выходом 7,5 граммов (75%) пар цис-2 и транс-2 энантиомеров (R 3)-(и и зно)(3-феноксифенил/метил цис, транс 3/2,2дихлорэтенил-2 2-диметилциклопропан карСюксипата в виде твердого вещоства (Сі = 7, О2 = 41,Ті = 7.Т2 = 32 В1-4.С, В 2 = 2 5 и Вз - 3 8J. П р и м е р 4. Получение смеси, содержащ^й Оопьшое количесг[ю пар транс-2-энантиомеров пиперметрина. Суспензию 10 0 rpaMN-on (0,024 моля; и (П,Г)-(циано-)(3 фоноксифенил) метил трзис3-/2 2-дихлорэтенил/-2,2 диметилцигпо'пропанкарбоксилата ( С И С? = 1,1. Ті =55,4 и Т2.= 43.5) 0,1 грамма (0,00025 моля) хлористого трикаприлметиламмония и 1.0 грамма карбоната н.чтрия в 20 граммах н-гєпіана перемешивали при комнатной температуре в течение трех часов В отусуспензи.о добав 15925 ляли еще 0,1 грамма хлористого трикаприлметиламмоппя, после чего эту смесь перемешивали oiu.f в течение трех часов. Реакционную смесь разбавляли 10 мл воды и перемешивали в течение 15 минут. Пол- 5 ученную смесь фильтровали. Фильтровальным осадок промывали п-гептаиом с выходом 9,17 граммов (91,7%) пар транс-2энантиомеров (R.S) (3-фспоксифепил/метил траис-3-/2,2-дихлорэтенил/-2,2-диметил- 10 циклопропанкарбоксилата (Ті = 1,7 и Тг • = 97,5). П р и м е р 5. Получение с помощью твердого К2СО3 смеси, содержащей большоо количество пар цпс-2 знантиомеров пи- 15 по| матрица. Суспензию 10,0 граммов (0,024 моля} твердого {n.S) (цЬаио)-(3-фемоксифелил)меtvn цис-3-/2,2-диу-лоротенил-/-2,2-диметилциклопропанкарбоксилата (Сі = 51,7, Сг = 20 • 40,0 и Ті t- T2 = 1,5), 0,25 грамма (0,00095) 18-крлуп-С и 1,0 грамма (0,0072 молл)карбоната калип в 20,0 граммах н-гептана перемешивали мри комнатной температуре а течение примерно 18 часов. К реакционной 2Г) смеси добавляли разбавлемнуп хлористоводородную кислоту для централизации карбоната кзлип. Эту смесь перемешивали при комнат ной температуре о течение двух дней. Эту смесь фильтровали, а фильтровальный 30 осадок высушивали с выходом 8,72 граммов (87,2%) пар цис-2эмэнтиомеров(К,5) (циана) (3-фєноксифенил) метил цис-3-/2,2-дихларзтет'л/-2,2-диметилциклопропанкарбокси лата (Ci-3,8 u Сг = 94,9). 35 і! р и м е р G. Получение смеси, содержащей большое количество пар цис-2 знантиомеров цпфлурина. Суспензию 5,0 граммов (0,012 моля) твердою (н\5)-(циано)-Л1-фтор-3-фепоксифенип/метил цис-3-/2,2-дихлорэтеиил/-2,2диметилцпклопропанкэр5оксилата (Сі = 49.2 и С,2 7 5 0 ' 8 ) - °-5 грамма 0,0047 моля) карбоната натрия и 0,05 грамма (0,00012 моля) хлористого трпкаприлметиламмония в 10,0 граммах и-гептана перемешивали при комнатной температуре в течение четырех часов. К этой суспензии добавляли еще 0,05 грамма хлористого трикаприлметиламмомил, после чего эту суспензию перемешивали при комнатной температуре еще в течение 13 часов. Основную реакционную смесь нейтрализовали разбавленной хлористоводородной кислотой, а затем перемешивали о течение примерно 30 минут. Эту смесь фильтровали, а фильтровальный осадок высушивали с выходом 4,45 граммов (89%) пар цис-2 эиантиомероо (R,S)-(nnaно)(4-фтор-3-феноксифенил/метил цис-3 40 45 50 55 8 /2,2-дихлорэтенил)-2.2-диметш1Циклопроп анкарбоксилата (Сі = 0,1 и Сг = 0,08). П р и м е р 7. Получение с помощью триэтиламипа смеси, содержащей большое количество пар цис-2 знантиомеров пиперметринз. Суспензию 10,0 граммов (0,024 моля) (R.SHunano) (З-феноксифенил)метил цис-3(2,2-дихлорэтепил)-2,2-диметил-циклопропанкарбоксилата (Сі - 53,8, Сг = 42,0, Ті = 2,8, • Тг = 1,2), 0,1 грамма (0,00025 моля) хлористого трикэпри-пметиламмония и 8,0 граммов (0,079 моля) триэтиламина D 20 граммах нгексапа перемешивали при комнатной температуре в течение 5,5 часов. К этой суспензии добавляли еще 0,1 грамма хлористого трикаприлметиламмония, после чего эту смесь перемешивали еще в течение 17 часов. Эту суспензию фильтровали, а фильтровальный осадок промывали н-гептамом. Фильтровальный осадок промывали с выходом 7,78 граммов (77 8%) пэр цис-2-аиантиомеровв (Р,Б)-(циано) (3-феноксифенил) метил цис-3-(2,2-дихлорзтенил)-2,2-диметилциклопропанкарбоксилэта (Сі = 3,6, С2 = 92,0, Т = 0,9). П р и м е р 8 . Получение смеси, содержащей большое количество пар транс-2 энантиомеров цифлутрина. Суспензию 5,0 граммов (0,012 моля) твердого (Рї,5)-(циано)-4-фтор-3-феноксифенил) транс-3-/2,2-дихлорэтенил)-2,2-диметилциклопропанкарбоксилата (Ті = 7 ї , 0 , Тг = 28,0), 0,5 грамма (0,0036 моля) карбоната калия и 0,05 грамма (0,00012) моля) хлористого трикаприлметиламмония в 10,0 граммах н-гептана перемешивали при комнатной температуре в течение примерно 17 часов. Основную смесь нейтрализовали разбавленной хлористоводородной кислотой и перемешивали в течение примерно 30 минут. Эту смесь фильтровали, а фильтровальный осадок высушивали с выходом 4,82 граммов (96,4%) пар транс-2 энамтиомеров (1?,5)-(циано-)(4-фтор-3-феноксифенил) метил транс-3*(2,2-дихлорэтенил)-2,2-диметилциклопропанкарбоксилата (Ті = 4,6, Тг 94,0) П р и м с р 9. Получение смеси, содержащей большое количество 1И,цис бромсодержащего аналога изомера 1 пиперметрина, полученного из смеси диастереомеров. Раствор 9,4 грамма (0,018 моля) (R.S)(циана) (3-феноксифенил/метил 1, цис-3/2,2-дибромэтен ил/-2,2-димети л циклопропан карбоксилата(1Р, цис S = 46,0%, 1R, цис R = 52,0%) в 18 граммах н-гептана перемешивали при комнатной температуре до образования суспензии. К этой суспензии добавляли 0,2 грамма (0.00076 моля) 18-кра 10 1ВП25 ун 6 и 1,0 грамм (0,0072 поля) клрбомата калия. Этусмесь перемешивали при камчтиой температуре в течение примерно 20 часов. Образец твердою вещества подвергали анализу посредством газовой хромагографии (% площади), в результате чего было обнаружено, что он содержит 87,8% (Э)-(циано) (З-феноксифенил)метил 1ГС, цис-3-/2,2дибромэтепил)/-2,2-диметилциклопропаик арбоксилата и 6,9% 1R,цисR изомера. П р и м е р 10. Получение пары ц и с - 2 - э н а м т и о м е р о в (R,S)-(miatio)-(3фенокси фе п и л / м е т и л цис-3-/2,2-дихл орэтен и л)-2,2-диметпл ц и к л о п р о п а н карбоксилата с использованием фтористого калия и хлористого трикзлрилмстиламмония. Суспензию 10,0 граммов (0,024 мол) (R.SHnnano) (3-фемоксифспил/меіпл цис-3/2,2-дихлорэтенил/-2,2-диметилциклоприкарбоксилата (Сі« 53,0, С2-44 А ї і и Т г 1,7). 0,1 грамма (0,00025 моля- хлористого трикаприлметиламмония и 1,0 грамма (0,02 моля фтористого калия в 20 граммах п-гептаиа (перемешивали при комнатной температуре в течение двух часов. Реакционную смесь нейтрализовали разбавленной хлористоводородной кислотой и перемешивали в тече Г) ние примерно 30 минут. 3 гу смось фильтровали, а фильтровальный оеддок высушивали с виходом 8,84 грамма (8Я,4%) пар цис-2энантиомеров (K.S) (циано) (j-феноксифсни л (метил цис-3-(2.2-дихлорэтемил)2,2-диметилциклопропанкарбоксилата(Сі = =7,0, С2 = 90,0). П р и м е р ы 1 1 - 50. В прилагаемых 10 таблицах иллюстрируются другие условия, являющиеся эффективными для осуществления л о г о изобретения. В табл. 1 суммируются условия и результаты, полученные при осуществлении этого способа в основном в 15 соответствии с примером 1 за исключением указанных изменений. Габл. 2 и 3 имеют аналогичную связь соответственно с примерами 3 и А. Термин "бепзоші", используемый в этих таблицах, означает бензоиновый по 20 бочный продукт, описанный выше в этом описании изобретения. Сокращение "NR" означает "не сообщалось". Габл.З иллюстрирует эффективность предложенного способа. 25 Таким образом, предложенный способ позволяет по сравнению с известным способом повысить содержание целевых изомеров, Таблица 1 Получение смесей с большим содержанием пар цис-2 энантиомеров пиперметрина Тип tsfe примера 11 12 13 14 15 16 > 16 (г) Растворитель Тип в ) А 0.1 А Катализатор а) Л » Л Л А См. основание См. основание Основание Тип с ) Время реакции (часы) Анализ исходного материала Кол-во А А с е с с 8,9 0,7 8,9 7,7 8,5 (0 0.1 0,1 0,2 0,2 А В С А В С D Е 2,0 4,0 6,0 8,0 18,0 18.0 17,5 17.0 А F 5,5 С 26,0 А F 5,5 11.0 23,0 с 8,4 G В У 11 12 15925 Продолжение табл. 1 —-JJ-— Катализатор а) примера Тип .М Растворитель Тип в ) Основание Тип с ) Время реакции (часы) Анализ исходного материала Кол-во (г) 17 А 0,2 • А С 18,0 С 9,1 13 А 0,2 А Н 17,5 С 8,1 19 В 0,5 А С 18,0 D 8.4 20 В 0,5 А А 18,0 D 8.9 21 "Б 0,5 А 1 18,0 D 8,4 22 В 0,5 А 18,0 D 8.9 23 С 0,5 А С 18.0 D 8,1 24 С 0,5 А А 18.0 D 8,5 25 С 0,0 Л К 20,0 D 8,0 26 С 0,4 А L 8,0 D 9,9 27 Е 0.2 А L " 24,0 С 7,8 28 F о,
ДивитисяДодаткова інформація
МПК / Мітки
МПК: C07C 255/14, A01N 27/00, A01P 7/02, C07C 69/743
Мітки: спосіб, підвищення, r-ізомерів, вмісту, кристалізуємого, піретроіда, 1r-транс, 1s-цис, 1s-транс, 1r-цис
Код посилання
<a href="https://ua.patents.su/10-15925-sposib-pidvishhennya-vmistu-1r-trans-s-1s-trans-r-1r-cis-s-ta-1s-cis-r-izomeriv-kristalizuehmogo-piretroida.html" target="_blank" rel="follow" title="База патентів України">Спосіб підвищення вмісту 1r-транс s-, 1s-транс r-, 1r-цис s- та 1s-цис r-ізомерів кристалізуємого піретроіда</a>
Попередній патент: Комплекс по виготуванню субстрату для вирощування грибів
Наступний патент: Ведуче колесо гусеничного транспортного засобу
Випадковий патент: Спосіб створення бінарних посівів в системі органічного землеробства