Спосіб одержання димеру лізоциму
Формула / Реферат
1. Способ получения димера лизоцима, предусматривающий приготовление раствора лизоцима путем добавления мономера лизоцима к буферному раствору, димеризацию мономера лизоцима в растворе, pH которого поддерживают на требуемом уровне, добавление суберимидата, остановку реакции димеризации в заданный момент, очистку полученного раствора димеризованного лизоцима посредством ионообменной хроматографии через колонку с декстрановой матрицей, элюирование и сбор очищенного продукта димерного лизоцима, отличающийся тем, что pH буферного раствора устанавливают по меньшей мере равным 9 и поддерживают по меньшей мере на этом уровне в течение процесса димеризации, а димеризацию останавливают посредством снижения pH до примерно 7,0, при этом полученный раствор димеризованного лизоцима предварительно очищают ионообменной хроматографией через колонку с агарозной матрицей, элюируют и собирают фракции, существенно содержащие димерную форму лизоцима.
2. Способ по п.1, отличающийся тем, что pH раствора мономера лизоцима доводят и/или поддерживают на уровне примерно 10.
3. Способ по п.2, отличающийся тем, что pH устанавливают и/или поддерживают посредством добавления NaOH.
4. Способ по п.1, отличающийся тем, что буферный раствор получают из дигидрата динатрийфосфата.
5. Способ по п.1, отличающийся тем, что добавляют суберимидат в количестве 4 - 6г.
6. Способ по п.1, отличающийся тем, что димеризацию проводят при комнатной температуре.
7. Способ по п.1, отличающийся тем, что димеризацию проводят при непрерывном перемешивании раствора.
8. Способ по п.1 отличающийся тем, что реакцию димеризации прекращают путем добавления ингредиента, выбранного из группы, включающей в себя HCl, раствор ацетата аммония или их комбинацию.
9. Способ по п.1, отличающийся тем, что осуществляют фильтрацию нерастворенных после димеризации частиц с помощью пористого фильтра.
10. Способ по п.1, отличающийся тем, что размер пор фильтра составляет примерно 0,4 - 0,5мкм.
11. Способ по п.1, отличающийся тем, что приготавливают раствор мономера лизоцима, содержащий 40 - 60г мономера лизоцима, 4 - 6л буфера и 4 - 6г суберимидата.
12. Способ по п.1, отличающийся тем, что элюирование проводят в катионообменной колонке, заполненной S-сефарозой FF.
13. Способ по п.1, отличающийся тем, что элюирование проводят в ионообменной колонке, заполненной сефадексом G 50 F.
14. Способ по п.1, отличающийся тем, что фракции, собранные после элюирования в катионообменнике, анализируют на содержание лизоцима гель-электрофорезом.
15. Способ по п.13, отличающийся тем, что фракции, собранные после элюирования в ионообменнике, анализируют на содержание лизоцима гель-электрофорезом.
16. Способ по п.1, отличающийся тем, что фракции, собранные после элюирования в катионообменной колонке, концентрируют с помощью системы с тангенциальным потоком.
17. Способ по п.1, отличающийся тем, что фракции, собранные после элюирования в ионообменной колонке, концентрируют с помощью системы с тангенциальным потоком.
18. Способ по п.1, отличающийся тем, что очищенный димер лизоцима, собранный после элюирования на ионообменнике, лиофилизируют.
19. Способ по п.1, отличающийся тем, что после димеризации недимеризованные мономеры лизоцима собирают и возвращают в повторный цикл процесса димеризации.
Текст
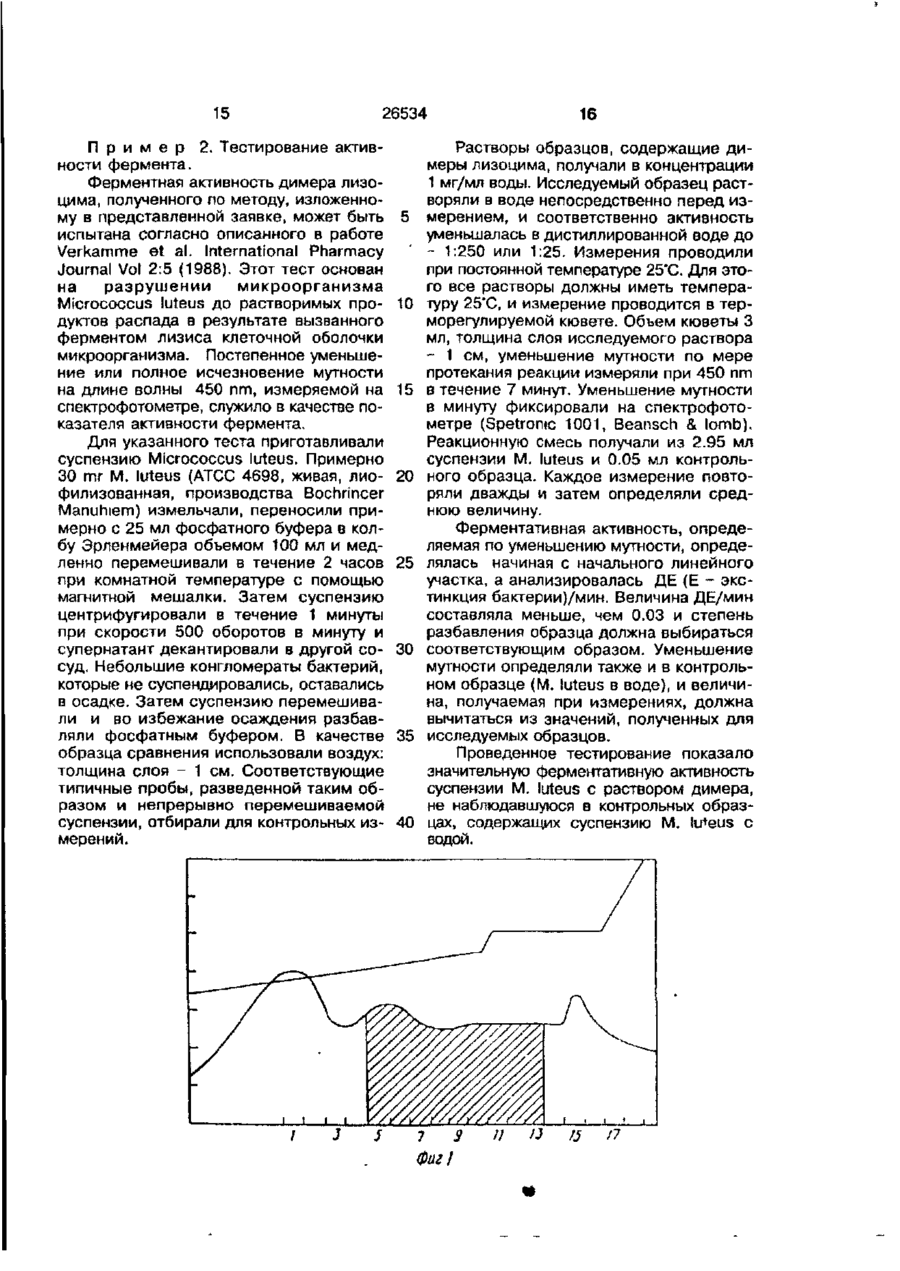
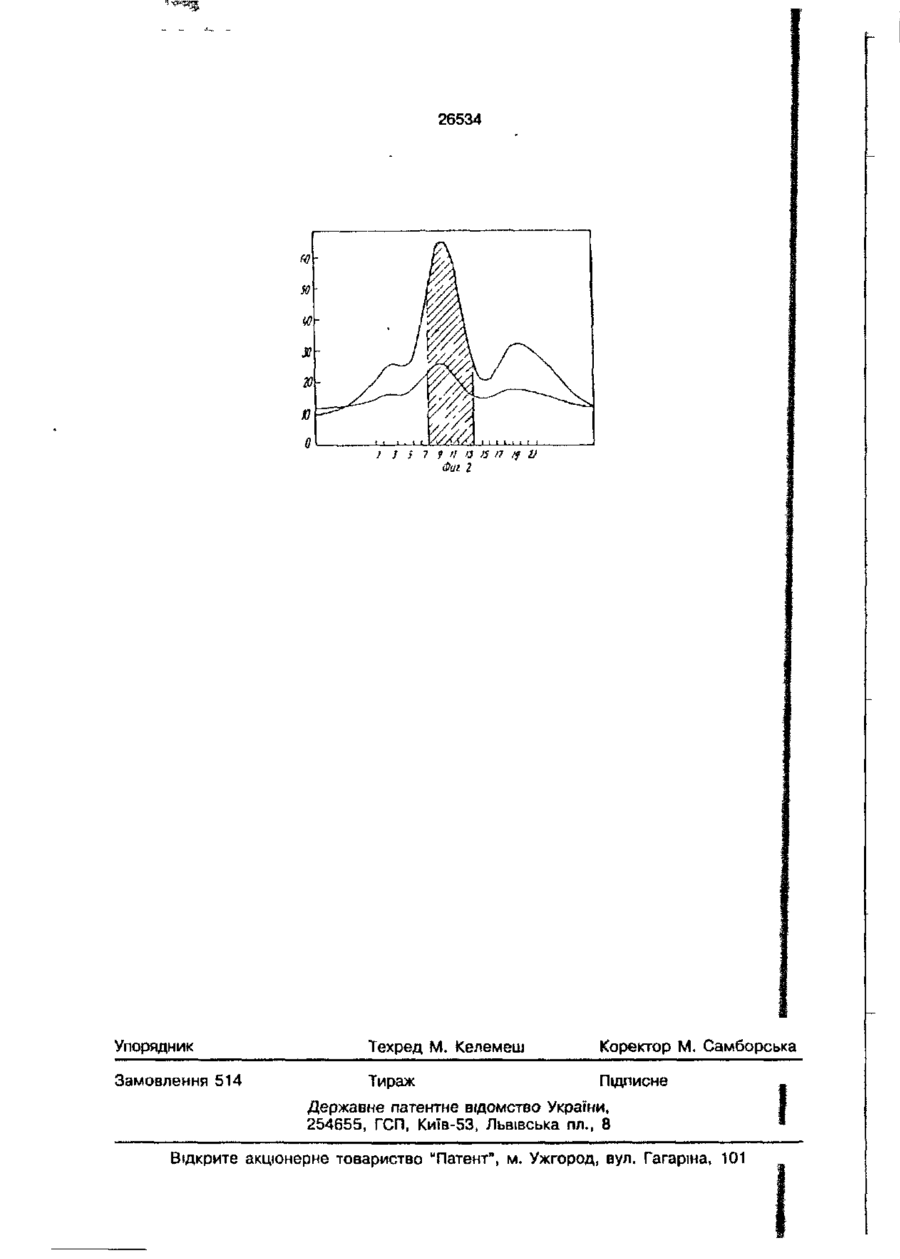
1. Способ получения димера лизоцима, предусматривающий приготовление раствора лизоцима путем добавления мономера лизоцима к буферному раствору, димеризацию мономера лизоцима в растворе, рН которого поддерживают на требуемом уровне, добавление суберимидата, остановку реакции димеризации а заданный момент, очистку полученного раствора димеризованного лизоцима посредством ионообменной хроматографии через колонку с декстрановой матрицей, элюирование и сбор очищенного продукта димерного лизоцима, о т л и ч а ю щ и й с я тем, что рН буферного раствора устанавливают по меньшей мере равным 9 и поддерживают по меньшей мере на этом уровне в течение процесса димеризации, а димеризацию останавливают посредством снижения рН до примерно 7,0, при этом полученный раствор димеризованного лизоцима предварительно очищают ионообменной хроматографией через колонку с агарозной матрицей, элюируют и собирают фракции, существенно содержащие димерную форму лизоцима. 2. Способ по п.1, о т л и ч а ю щ и й с я тем, что рН раствора мономера лизоцима доводят и/или поддерживают на уровне примерно 10. 3. Способ по п.2, о т л и ч а ю щ и й с я тем, что рН устанавливают и/ /или поддерживают посредством добавления NaOH. 4. Способ по п.1, о т л и ч а ю щ и й с я тем, что буферный раствор получают из дигидрата динатрийфосфата. 5. Способ по п.1, о т л и ч а ю щ и й с я тем, что добавляют суберимидат в количестве 4 - 6 г. 6. Способ по п.1, о т л и ч а ю щ и й с я тем, что димеризацию проводят при комнатной температуре. 7. Способ по п.1, о т л и ч а ю щ и й с я тем, что димеризацию проводят при непрерывном перемешивании раствора. 8. Способ по п. 1 о т л и ч а ю щ и й с я тем, что реакцию димеризации прекращают путем добавления ингредиента, выбранного из группы, включающей в себя НС1, раствор ацетата аммония или их комбинацию. 9. Способ по п.1, о т л и ч а ю щ и й с я тем, что осуществляют фильтрацию нерастворенных после димеризации частиц с помощью пористого фильтра. 10. Способ по п.1, о т л и ч а ю щ и й с я тем, что размер пор фильтра составляет примерно 0,4 - 0,5 мкм. 11. Способ по п.1 о т л и ч а ю щ и й с я тем, что приготавливают раствор мономера лизоцима, содержащий 40 - 60 г мономера лизоцима, 4 6 л буфера и 4 - 6 г суберимидата. 12. Способ по п.1, о т л и ч а ю щ и й с я тем, что элюирование проводят в катионообменной колонке, заполненной S-сефарозой FF. 13. Способ по п.1, о т л и ч а ю щ и й с я тем, что элюирование проводят в ионообменной колонке, заполненной сефадексом G 50 F. Os о 26534 14 Способ по п.1, о т л и ч а ю щ и й с я тем, что фракции, собранные после элюирования в катионообменнике, анализируют на содержание лизоцима гель-электрофорезом. 15. Способ по п. 13, о т л и ч а ю щ и й с я тем, что фракции, собранные после элюирования в ионообменнике, анализируют на содержание лизоцима гель-электрофорезом. 16. Способ по п.1, о т л и ч а ю щ и й с я тем, что фракции, собранные после элюирования в катионообменной колонке, концентрируют с помощью системы с тангенциальным потоком. 17. Способ по п.1, о т л и ч а ю щ и й с я тем, что фракции, собранные после элюирования в ионообменной колонке, концентрируют с помощью системы с тангенциальным потоком. 18. Способ по п.1, о т л и ч а ю щ и й с я тем, что очищенный димер лизоцима, собранный после элюирования на ионообменнике, лиофилизируют. Изобретение относится к способам приготовления и очистки димера лизоцима, которые могут, в частности, использоваться для лечения вирусных и бактериальных инфекций. Непрерывный рост числа бактериальных штаммов и вирусных заболеваний, устойчивых к антибиотикам, обуславливает необходимость разработки новых лекарств для лечения человека и животных. Среди множества современных средств для лечения различных заболеваний используются ферменты в мономерной форме. Ферменты являются каталитически активными белками, ответственными почти за все основные жизненные процессы в организме. Так, многие ферменты, взятые как отдельно, так и в определенных комбинациях, были выделены на основании их физиохимического, физиологического или биологического действия. В настоящее время показано, что лизоцим, известный с 1922 года, наряду с другими ферментами, обладающими лечебным действием, может быть использован для лечения различных заболеваний, требующих физиологического и биологического воздействия. Было обнаружено, что лизоцим обладает различными терапевтическими свойствами, такими, как антивирусное, антибактериальное, противовоспалительное и антигистаминное действие. Антибактериальное действие лизоцима, по-видимому, обусловлено гидролизом бета-1-4-гликозидной связи между н-ацетилмураминовой кислотой и н-ацетилглюкозамином, находящимися в бактериальной оболочке. К сожалению, огромный потенциал возможного лечебного действия лизоцима при его использовании не реализуется прежде всего из-за заметного цитотоксического эффекта, присущего мономерной форме этого фермента. Так, в опытах с культурами фибробластов наблюдалось заметное цитотоксическое действие лизоцима в мономерной форме даже в очень маленьких дозах. Таким образом, приобретает актуальность поиск возможной максимизации потенциального лечебного действия с помощью разработки эффективного способа ограничения цитотоксических свойств мономера. Недавно было обнаружено, что антивирусные или антибактериальные препараты, не обладающие цитотоксическим действием, могут быть изготовлены на основе лизоцима, т.е. посредством получения композиции, содержащей димерную форму фермента. Использование димера лизоцима позволяет создать препарат, пригодный для лечения ряда инфекционных заболеваний и не обладающий сильными цитотоксическим и свойствами, обычно ассоциирующимися с мономером лизоцима. Использование димера лизоцима в различных терапевтических препаратах раскрывается в одновременно рассматриваемой заявке РСТ Application us 88/01785. Хотя способы получения димерной формы лизоцима из мономера известны, однако потребность в недорогом и эффективном производстве больших количеств димера лизоцима остается актуальной. Таким образом, крайне желательна разработка технологии изготовления и анали 19. Способ по п.1, о т л и ч а ю щ и й с я тем, что после димеризации недимеризованные мономеры лизоцима собирают и возвращают в повторный цикл процесса димеризации. 5 10 15 20 25 30 35 26534 за больших количеств очищенного димера лизоцима, не содержащего мономерной или полимерной форм фермента или других загрязнений. Краткое содержание изобретения. В соответствии с настоящим изобретением предлагается эффективный метод изготовления очищенного димера лизоцима, состоящий из следующих стадий: a) приготовление раствора лизоцима путем добавления мономера лизоцима к буферному раствору, имеющему рН по меньшей мере около 9; b) добавление сшивающего реагента - суберимидата, такого как диметилсуберимидат, для димеризации мономеров лизоцима в растворе, рН которого поддерживается на уровне 9 и выше; c) снижение рН до значения, близкого к 7, для прекращения реакции димеризации в заданный момент времени; d) очистка раствора димеризованного лизоцима с помощью первой стадии элюирования, при проведении которого раствор пропускают через ионообменную колонку и собирают фракции, содержащие преимущественно димерную форму лизоцима; e) фильтрование фракций, собранных в первой стадии очистки, путем проведения вторичного элюирования, при котором собранные фракции снова пропускают через ионообменную колонку; f) сбор высокоочищенного димера лизоцима, полученного на второй стадии выделения. С помощью описанного выше метода можно получать значительные количества очищенного димера лизоцима, который может быть использован при лечении ряда вирусных и бактериальных заболеваний. Краткое описание прилагаемых фигур. На фиг. 1 представлен профиль элюции, полученный на первой стадии элюцирования, проведенного в соответствии с настоящим изобретением. На фиг. 2 представлен профиль элюции, полученный на второй стадии элюцироеания, проведенного в соответствии с настоящим изобретением. Подробное описание предпочтительного" осуществления способа. При получении димеров лизоцима в соответствии с настоящим изобретением в качестве исходного сырья могут быть использованы любые подходящие для этой цели мономеры. В представленном изобретении лизоцим в форме мономера по 5 10 15 20 25 ЗО 6 лучали от Serva Feine Biochemicsa. GmbH Heidelberg, каталожный номер N 28260. Перед добавлением сшивающего реагента к мономеру, раствор лизоцима получали в мензурке, растворяя мономер в растворе фосфатного буфера при комнатной температуре, и непрерывно перемешивая при этом в течение по меньшей мере двух часов. Используемый фосфатио-буферный раствор состоит предпочтительно из 0.1 М раствора дигидрата двузамещенного фосфорнокислого натрия. Указанный буферный раствор получали путем растворения 70 г дигидрата двузамещенного фосфорнокислого натрия в 1000 мл Н2О. Хотя реальные количества реагентов и растворителей, используемых в предложенном изобретении, могут варьироваться, реакцию димеризации, осуществленную в соответствии с настоящим изобретением, проводили с использованием примерно от 40 до 60 г мономера лизоцима, растворенного в химическом стакане с 5 л буферного раствора дигидрата двузамещенного фосфорнокислого натрия. Необходимо также, чтобы рН раствора мономера был доведен, по меньшей мере, до 9, а лучше всего - до 10. Для регулировки рН может быть использован раствор основания, например, 1 Н NaOH. Реакцию димеризации осуществляли путем добавления подходящего сшивающего реагента - суберимидата - в соответствующих пропорциях к мономеру лизоцима, поддерживая при этом рН на уров35 не 9 или выше. В соответствии с настоящим изобретением, предпочтительно использовать диметилсуберимидат. К раствору, приготовленному как описано выше, 40 добавляли 4-6 г диметилсуберимидата, при этом растворение происходит в течение примерно одной минуты. Реакция полимеризации происходит в течение 60 минут при комнатной температуре (25±5°С) 45 при непрерывном перемешивании с помощью магнитной или другой мешалки. Реакция димеризации может быть остановлена в заданный момент путем понижения рН до 7 (±0.2}, осуществляемом 50 добавлением 1 М HCI и/или 0.2 М раствора ацетата аммония (примерно 250 мл). Соответствующий раствор ацетата аммония получали путем растворения 15 г вещества в 1000 мл Н20. Как правило, реак55 ция димеризации протекает в течение 1 часа, хотя этот период может быть больше или меньше в зависимости от точного количества вводимых веществ и от природы использованных реагентов и растворов. 26534 На этой стадии необходимо, чтобы вся реакционная смесь, обладающая значительной мутностью, как правило, была бы пропущена через мембранный фильтр для отделения нерастворенных частиц. Обычно это является необходимой операцией, так как раствор на этой стадии содержит примесь нерастворимых полимеров. Для отделения полимеров и других нерастворенных частиц необходимо использовать фильтры с размерами пор примерно 0.40.5 ц т . Были проведены гель-электрофорезные исследования образцов, взятых через различные промежутки времени после добавления сшивающего реагента к раствору мономера лизоцима. Исследования показали, что хотя мономерная форма четко видна в почти каждой проанализированной фракции, полоса, соответствующая димерной форме лизоцима, становится различима через 10 минут после начала реакции и по мере развития реакции увеличивается. Молекулярный вес лизоцима примерно 14000, а полоса димера соответствует молекулярному весу, равному 30000. Как показали электрофоретические исследования, имеет место также образование полимерных форм. Для получения значительных количеств очищенного димера лизоцима предпочтительно чтобы раствор прошел , по крайней мере, две дополнительные стадии очистки для выделения димеризованного лизоцима и удаления мономеров лизоцима или других примесей. В представленном изобретении предполагается, что удаленные недимеризованные мономеры лизоцима могут быть собраны и рециклированы для максимизации эффективности производства димера лизоцима. Первая стадия очистки производится с помощью ионообменной хроматографии. На этом этапе раствор димера лизоцима, полученный в результате процесса димеризации так, как описано выше, вводится в колонку с ионообменной смолой, представляющую собой Сефарозу или другие катиониты. В предпочтительном варианте колонка диаметром примерно 10 см и высотой 25 см заполняется S-Сефарозой FF (Pharmacia) объемом около 2.1 л, уравновешенной 4.2 л 50 мм раствора К-фосфатного буфера с рН равным 7. Примерно 5 литров димеризованного раствора пропускают через ионообменную колонку и элюирование происходит с предпочтительной скоростью элюирования около 60 мл/мин. Желательно, чтобы элюирование происходило с использованием солевого 5 10 15 20 25 30 35 40 45 50 55 8 градиента - 1.5-1 М NaCI в 50 mM Kфосфатном буфере. На этой стадии фракции собирали с помощью коллектора фракций {марки LKB 2211 Suprec) и хранили в стерильных колбах. Профиль элюции регистрировали, используя самописец LKB 2210, работающий на скорости 1 mM в минуту, и полученный профиль элюции может быть использован при определении точного состава собранных фракций. Поглощение собранных растворов предпочтительно измерять при 280 nm с помощью прибора LKB 2238 UV1COR S11. Точное содержание белка в каждой фракции, собранной на первой стадии элюции, описанной выше, анализируется главным образом, с помощью гель-электрофореза, например, в полиакриламидном геле с ДСН (ДСН - ПААГ), описанного Thomas et al. PNAS 72, 2626 (1979). При электрофоретическом исследовании предпочтительно около 50 мкл каждой фракции смешивают с 50 мкл буфера для сенсибилизации, и смесь нагревают 10 минут при около 95°С. Затем 25 мкл этой смеси вносят в ячейку с гелем. После проведения электрофореза в течение примерно около 4 часов при токе 20-35 тА полосы белка разделяются и становятся видимыми при подкрашивании таким красителем, как кумасси голубой (Coomascie-Biue R250 (Мегк.)). Используя гель-электрофорез на ДСН можно разделить мономеры, димеры и полимеры лизоцима. Электрофоретический анализ может быть использован для идентификации собранных фракций, которые содержат, главным образом, димерные формы лизоцима. Фракции, состоящие, в основном, из димеров лизоцима, собирают и предпочтительно концентрируют до получения около 800 мл в системе с тангенциальным потоком. На этой стадии, для дальнейшей очистки димерного продукта целесообразно провести следующий этап фильтрации. В предпочтительном варианте собранные от первой стадии элюции продукты лизоцима концентрируют с использованием тангенциального потока и снова пропускают через ионообменную колонку. Предполагается, что в данном случае будет использована колонка с Сефадексом Sephadex G 50 F (Pharmacia), размером, приблизительно 25 см в диаметре и 120 см высотой. Колонка уравновешивается объемом около 60 литров 5 mM буферного раствора ацетата аммония, который способствует поддержанию рН, равным при 26534 мерно 5. Соответствующий буферный раствор ацетата аммония был приготовлен из 4 г ацетата аммония, растворенного в 1000 мл воды с рН, доведенным до 5 с помощью раствора 3 г уксусной кислоты в около 1000 мл дистиллированной воды. Раствор димера лизоцима, собранный после первой стадии элюирования и концентрированный в системе в тангенциальном потоке, пропускают через ионообменную колонку при скорости элюции в уравновешивающем буфере около 70 мл в минуту. Как и в случае первого элюирования, фракции собирают и накапливают и примерно 50 мл каждой фракции анализируют путем ДСН-электрофореза в ПААГ, описанного выше. Кроме того, профиль элюции опять регистрируют на самописце, работающем при скорости примерно 0.5 мм/мин. Поглощение также измеряется при 280 nm. Профиль элюции, полученный для фракций, взятых после второго этапа очистки, имеет три пика, но, в основном, профиль состоит из среднего пика, представляющего фракцию димера лизоцима. На этом этапе остаются только минимальные количества полимерных и мономерных форм лизоцима. Димерные фракции с высокой степенью чистоты, как это видно из средних пиков профиля элюции, собирают и снова концентрируют в системе с тангенциальным потоком. В конечном счете, очищенный димер лиофилизуют и сохраняют до использования. Весь этот процесс может быть повторен столько раз, сколько необходимо для получения соответствующего количества димерного продукта. Отдельные серии димеров посте очистки могут быть растворены в дистиллированной воде, а затем лиофилизованы. Таким путем можно получать гомогенные партии лизоцима, которые могут быть эффективно использованы при лечении многих вирусных и бактериальных заболеваний. В дополнение к антивирусным и антибактериальным свойствам, лизоцим в димерной форме обладает и другими терапевтическими действиями такими как, противовоспалительные и антигистаминные, причем он не обнаруживает цитотоксического действия, характерного для мономерной формы лизоцима. Таким образом, представленный способ может быть использован для эффективного производства больших количеств очищенного полезного продукта - димера лизоцима. Благодаря способности димерного продукта, полученного методом, предложенным в настоящем 5 10 15 20 25 30 35 40 45 50 55 10 изобретении разрушать бактерии можно проверив его эффективность путем введения димера в суспензию микроорганизмов с последующим наблюдением за уменьшением количества микроорганизмов после введения димера фермента (с помощью спектрофотометра). Испытания, проведенные описанным способом, показали, что димер лизоцима, полученный способом, изложенным в настоящем изобретении, обладает ценными свойствами, которые могут быть использованы для лечения вирусных и бактериальных заболеваний. В качестве иллюстрации настоящего изобретения представляются следующие примеры, которые, однако, не ограничивают объема настоящего изобретения. П р и м е р 1. Приготовление димера лизоцима. 50 г мономера лизоцима (Serva Feine, каталожный номер N 28260) растворяли в закрытом сосуде с использованием 5 л в 0.1 М буферного раствора дигидрата двузамещенного фосфорнокислого натрия при непрерывном помешивании в течение 2 часов при 25°С Фосфатный буфер получали из 70.98 г дигидрата двузамещенного фосфорнокислого натрия • 2Н20 (МепЧ. Р.А.), растворенного в 1000 мл Н2. рН раствора был доведен до 10 с помощью 1 Н NaOH. Затем к раствору белка добавляли 5 г сшивающего реагента - диметилсубе рими дата (Sioma), и рН раствора постоянно поддерживали равным 10. Реагент полностью растворялся в течение 1 минуты, а реакция димеризации протекала в течение 60 минут при комнатной температуре
ДивитисяДодаткова інформація
МПК / Мітки
МПК: C12N 9/96, C12N 9/36, C12N 15/56
Мітки: лізоциму, одержання, спосіб, димеру
Код посилання
<a href="https://ua.patents.su/10-26534-sposib-oderzhannya-dimeru-lizocimu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання димеру лізоциму</a>
Попередній патент: Теплоізоляційна маса
Наступний патент: Спосіб факсимільного зв’язку,система зв’язку селективного виклику і система факсимільної передачі
Випадковий патент: Привод клапана зливного приладу залізничної цистерни для розплавлених продуктів