Спосіб одержання 4-амінодифеніламіну
Номер патенту: 56354
Опубліковано: 15.05.2003
Автори: Ф'єдлєр Кароль, Пінтер Йозеф, Бешка Емануель, Томан Петер, Гронєц Мілан
Формула / Реферат
1. Спосіб одержання 4-амінодифеніламіну (4-АДФА) через одержання проміжної сполуки 4-нітродифеніламіну і/або 4-нітрозодифеніламіну, і/або їх солей взаємодією аніліну і нітробензолу в рідкому середовищі при температурі від 50 до 130°С, атмосферному або зниженому тиску, в атмосфері інертного газу або в присутності кисню повітря з наступним гідруванням проміжної сполуки 4-нітродифеніламіну і/або 4-нітрозодифеніламіну та побічних продуктів і виділенням 4-амінодифеніламіну та побічних продуктів, і рецикл неперетворених матеріалів, який відрізняється тим, що
взаємодію аніліну з нітробензолом здійснюють у реакційній системі, що включає розчин солей цвітеріонів з гідроксидами загальної формули
HO-/(R1R2R3)N+-CHR4-(CH2)x-Y-/Z+,
де
R1 і R2 представляють радикал від метилу до додецилу,
R3 означає метил, етил, феніл, бензил,
R4 означає водень або метил,
х означає ціле число від 0 до 5,
Y- означає СO2-, SO3- і
Z+ означає катіон лужного металу Na, К, Cs або тетразаміщений катіон четвертинного амонію, такого як тетраметиламоній, або їхні взаємні поєднання, у яких кількість як солі цвітер-іона, так і гідроксиду дорівнює щонайменше еквімолярній кількості відносно кількості нітробензолу в реакційній системі, де утворюються 4-нітрозодифеніламін і/або 4-нітродифеніламін, які після гідрування дають 4-АДФА, і після реакції рециркулюють щонайменше половину реакційної середи.
2. Спосіб за п. 1, який відрізняється тим, що реакцію проводять у присутності розчину солей цвітер-іонів з гідроксидами загальної формули, де R1, R2 і R3 означають метил, R4 означає водень, х означає 0, Y- означає СO2-, а Z+ означає катіон калію і/або тетразаміщений катіон четвертинного амонію.
3. Спосіб за п. 1 або 2, який відрізняється тим, що Z+ означає катіон калію і/або тетраалкіламонію з кількістю атомів вуглецю в алкілі від 1 до 4.
4. Спосіб за будь-яким із пп. 1-3, який відрізняється тим, що реакційне середовище одержують окремо і/або його утворюють in situ у реакційній системі з вихідних матеріалів.
5. Спосіб за будь-яким із пп. 1-4, який відрізняється тим, що рідке середовище для взаємодії аніліну з нітробензолом одержують змішуванням з водою і/або щонайменше однією органічною сполукою, яку вибирають з аніліну, піридину, толуолу, ксилолу, циклогексану та аліфатичних спиртів, що містять в молекулі від 1 до 4 атомів вуглецю.
Текст
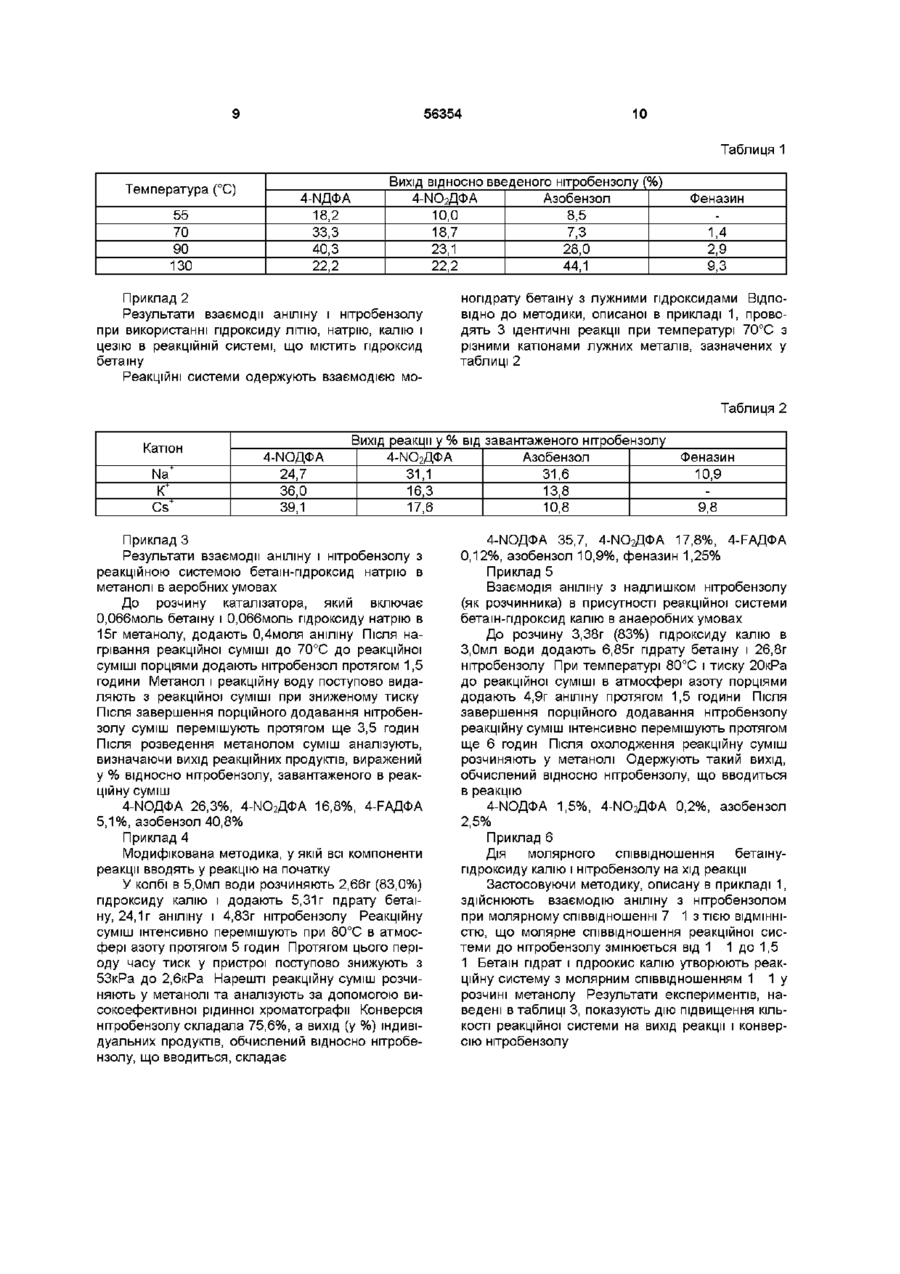
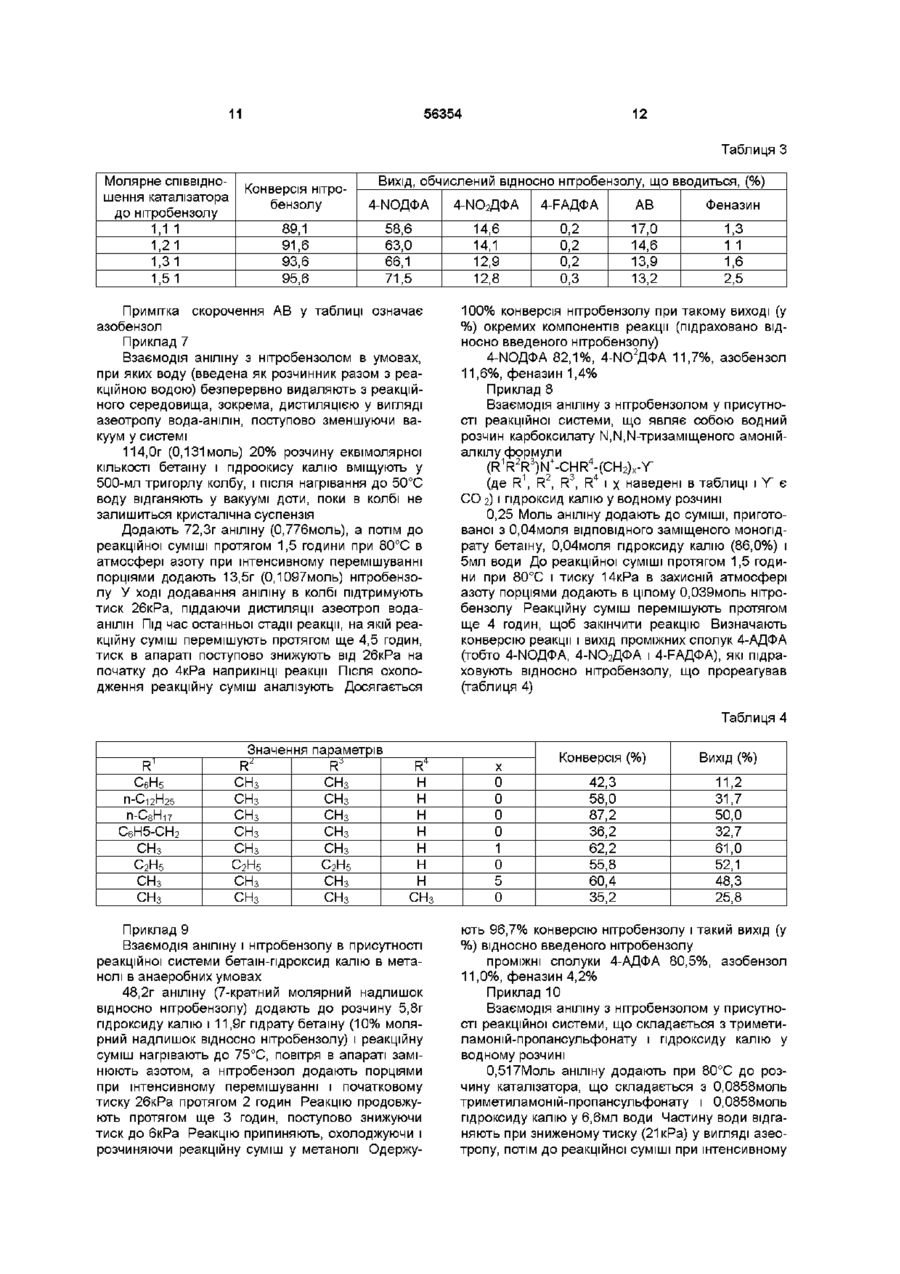
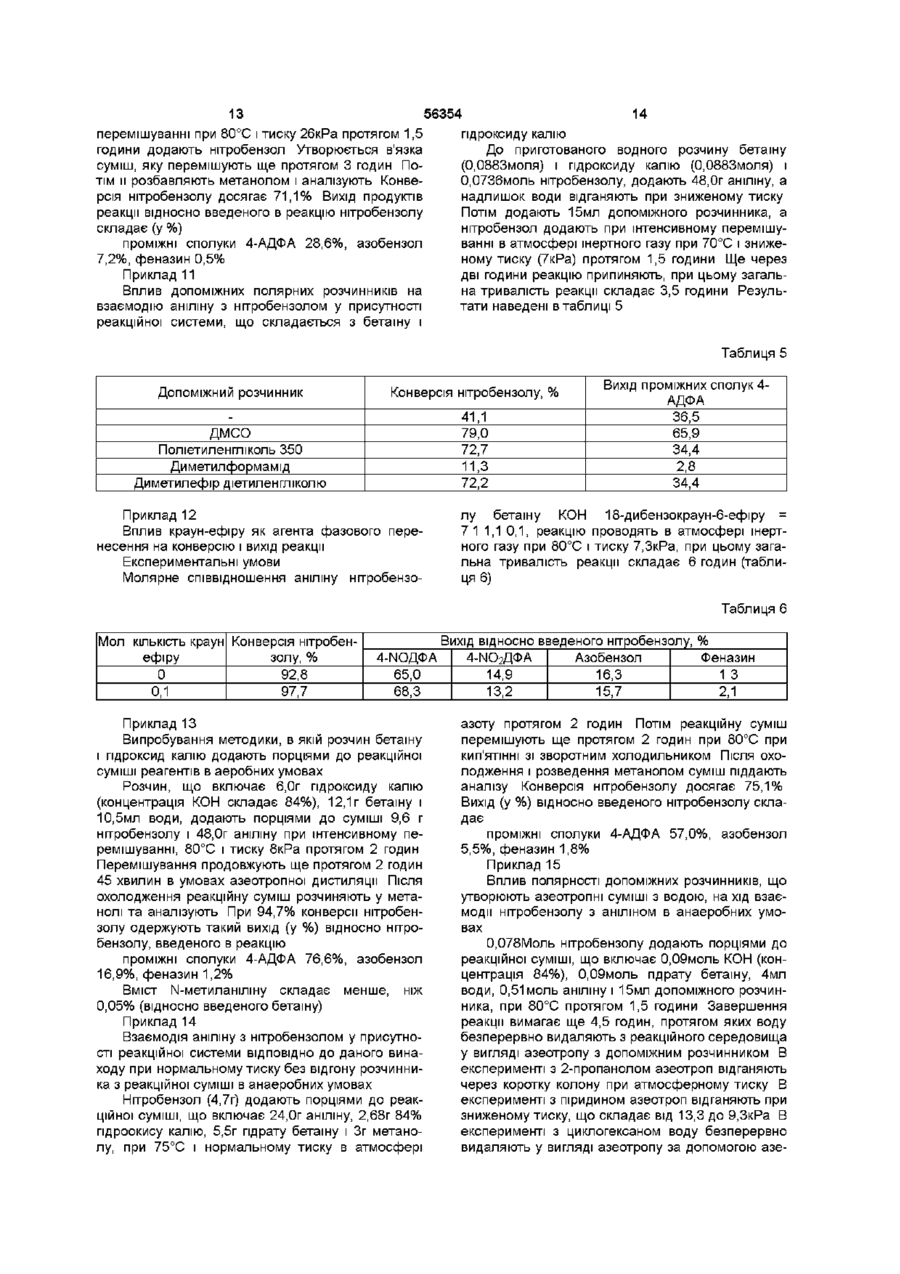
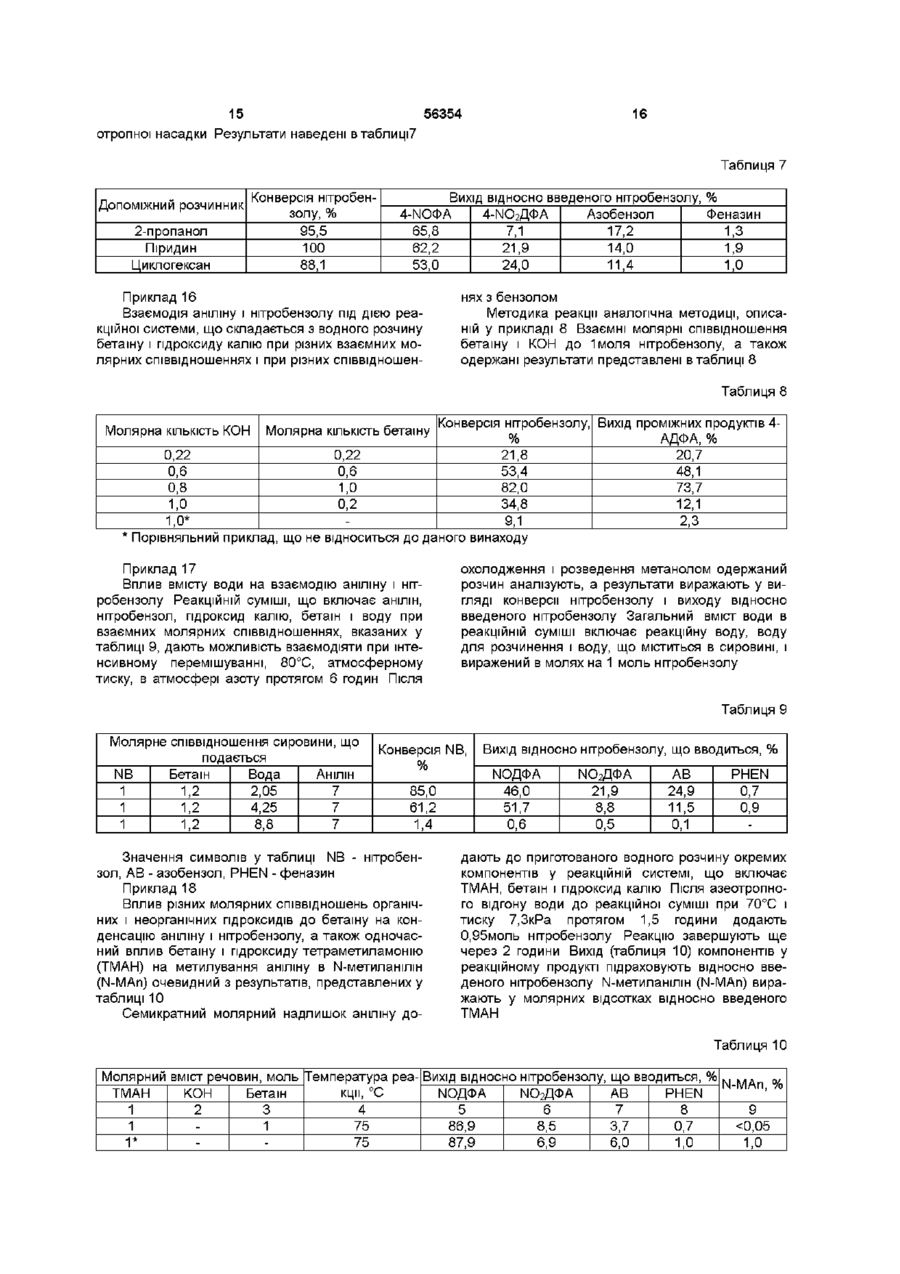
1 Спосіб одержання 4-амінодифеніламшу (4АДФА) через одержання проміжної сполуки 4нітродифеніламшу і/або 4-нітрозодифеніламшу, і/або їх солей взаємодією аніліну і нітробензолу в рідкому середовищі при температурі від 50 до 130°С, атмосферному або зниженому тиску, в атмосфері інертного газу або в присутності кисню повітря з наступним гідруванням проміжної сполуки 4-нітродифеніламіну і/або 4нітрозодифеніламіну та побічних продуктів і виділенням 4-амінодифеніламшу та побічних продуктів, і рецикл неперетворених матеріалів, який відрізняється тим, що R означає метил, етил, феніл, бензил, R4 означає водень або метил, х означає ціле число від 0 до 5, Y~ означає СОг , SO3 і Z+ означає катіон лужного металу Na, K, Cs або тетразаміщений катіон четвертинного амонію, такого як тетраметиламоній, або їхні взаємні поєднання, у яких КІЛЬКІСТЬ як солі цвітер-юна, так і гідроксиду дорівнює щонайменше еквімолярній КІЛЬКОСТІ відносно КІЛЬКОСТІ нітробензолу в реак R1 і R2 представляють радикал від метилу до додецилу, ційній системі, де утворюються 4нітрозодифеніламін і/або 4-нітродифеніламш, які після гідрування дають 4-АДФА, і після реакції рециркулюють щонайменше половину реакційної середи 2 Спосіб за п 1, який відрізняється тим, що реакцію проводять у присутності розчину солей цвітер-юнів з гідроксидами загальної формули, де R1, R2 і R3 означають метил, R4 означає водень, х означає 0, Y~ означає СО2, a Z+ означає катіон калію і/або тетразаміщений катіон четвертинного амонію 3 Спосіб за п 1 або 2, який відрізняється тим, що Z+ означає катіон калію і/або тетраалкіламонію 3 КІЛЬКІСТЮ атомів вуглецю в алкілі від 1 до 4 4 Спосіб за будь-яким із пп 1-3, який відрізняється тим, що реакційне середовище одержують окремо і/або його утворюють in situ у реакційній системі з вихідних матеріалів 5 Спосіб за будь-яким із пп 1-4, який відрізняється тим, що рідке середовище для взаємодії аніліну з нітробензолом одержують змішуванням з водою і/або щонайменше однією органічною сполукою, яку вибирають з аніліну, піридину, толуолу, ксилолу, циклогексану та аліфатичних спиртів, що містять в молекулі від 1 до 4 атомів вуглецю Даний винахід відноситься до способу одержання 4-амінодифеніламшу (4-АДФА) через одер жання проміжної сполуки 4-нітродифеніламшу і/або 4-нітрозодифеніламіну, і/або їхніх солей, у взаємодію аніліну з нітробензолом здійснюють у реакційній системі, що включає розчин солей цвітерюнів з гідроксидами загальної формули HO7(R1R2RJ)N+-CHR4-(CH2)x-WZ+, О ю со (О ю 56354 якому анілін взаємодіє з нітробензолом у рідкому Відоме одержання 4-АДФА окисленням аніліну середовищі, з утворенням попередників 4-АДФА, фериціанідом у сильнолужному середовищі (патобто 4-нітрозодифеніламшу (4-ІЧОДФА), 4тент США 4760186 і патент Великобританії нітродифеніламшу (4-І\ІО2ДФА) і/або їхніх солей, 1440767), у якому здійснюють з'єднання "головаякі після гідрування дають 4-АДФА хвіст" двох анілінових молекул 4-Амінодифеніламш (4-АДФА) широко застоПатент США 5574187 описує одержання 4совують як проміжний продукт при одержанні алкіАДФА заміщенням фенілгідроксиламіну аніліном у лованих похідних, що виявляють прекрасні власприсутності кислотного каталізатора Вихід продутивості при використанні як антиозонантів, кту є середнім (макс 51,2%) антиоксидантів і стабілізаторів Суть способу, описаного в наступному патенті США 5420354, полягає в реакції нітробензолу з ВІДОМІ способи промислового одержання 4аніліном у присутності водню, каталізатора гідруАДФА починають з гідрування проміжних сполук, вання, кислотного каталізатора та шпбітора гідрутобто 4-ЫОДФА або 4-І\ІО2ДФА Однак одержання вання, яка безпосередньо призводить до одерданих проміжних сполук, яке включає декілька жання 4-АДФА, але з порівняно низьким виходом технологічно складних стадій, супроводжується (макс 12%) і низькою селективністю реакцмодержанням ряду побічних продуктів, органічних і подібно іншим вищезгаданим методикам неорганічних ВІДХОДІВ, ЯКІ підлягають знищенню, що є однією з найсерйозніших проблем даного У заявці ЕР 566783, на ім'я AKZO N V , описаспособу одержання ний спосіб одержання 4-нітродифеніламшу реакцією нітробензолу з аніліном у середовищі полярноЕкологічно та економічно кращі альтернативні го апротонного розчинника, зокрема, способи одержання проміжних сполук 4-АДФА диметилсульфоксиду і третинного бутанолу, у сивключають пряму взаємодію аніліну і нітробензольнолужній реакційній системі, у якій гідроксиди лу Така реакція ІНІЦІЮЄТЬСЯ основами, що утволужних і лужноземельних металів, алкоксиди, амірюють в результаті реакції аніон аніліду, який згоди і гідриди лужних металів використовують як дом заміщає водень у нітробензолі за механізмом основи, нарешті, у присутності каталізатора фазореакції нуклеофільного приєднання ((A Wohl et al , вого перенесення, такого як кислий сірчанокислий Вег 34- 2442-2450, 1901, і A Wohl, Ber 36, 4135тетрабутиламоній Був досягнутий порівняно висо4138, 1903), при цьому при використанні як основи кий вихід, однак селективність реакції недостатня твердого гідроксиду калію одержують головним Тому виникає необхідність відділення продукту чином феназин і • оксид феназину, при викорис(ІЧОгДФА) від побічних продуктів кристалізацією танні гідроксиду натрію одержують також 4Більш ТОГО, у процесі виділення продуктів одержуЫОДФА ють солі, таким чином додатково збільшуючи варВ п'ятидесяті роки багато вчених досліджували тість їхньої обробки Також виникає питання про та описали механізм нуклеофільної реакції Wohlекономічне рециркулювання основ і сумішей розAue аніліну та його похідних з ароматичними нітчинника назад у процес росполуками під впливом основ (NaOH, KOH, навіть NaNbb) у середовищі бензолу, толуолу і ксилолу з одержанням похідних феназину Крім них, у цей же час були також виділені та описані ІНШІ продукти реакції, такі як 4-нітрозодифеніламін, 4нітрозаміщені дифеніламіни, азобензоли, азоксибензоли (Е І Abramova et al, Zhur Obshchei Khim 22, 502-509, 1953, S B Serebryanyi, Uspekhi Khimn 24, 313-345, 1955, S B Serebryanyi, Ukrain Khim Zhur 21, 350-360, 1955, V P Chernetskn et al , Zhur Obshchei Khim 25,2161-2170,1955) Відомо (N R Ayyangar et al , Tetrahedron Letters 31, 3217-3220, 1990), що 4-ШДФА і 4-ЫО2ДФА одержують у результаті реакції нітробензолу з ацетанілідом у присутності диполярного апротонного розчинника, диметилсульфоксиду (ДМСО) під дією гідроксиду натрію і карбонату калію, а також (A A Primer et al , J Org Chem 48, 1700-1705, 1983), що 4-І\ІО2ДФА одержують з виходом до 24% у результаті реакції аніліну з нітробензолом у присутності основ, застосовуючи в даному випадку бутилат або перекис калію в середовищі бензолу та у присутності краун-ефіру Подібним чином (D J Stuehretal, J Org Chem 50, 694-696, 1985), у результаті реакції аніліну і Nметиланіліну в ДМСО з перекисом калію разом з 18-краун-6-ефіром, а також третинним бушлатом калію, як реакційний продукт була одержана суміш 4-ІЧОДФА, Ч-МОгДФА, 4-АДФА, азобензолу, 4фенілазодифеніламшу і фенілформаміду (вихід не зазначений) Інший спосіб одержання 4-АДФА, в якому не використовують галогени, включає реакцію аніліну з 4-фенілазодифеніламшом у присутності сильних основ, таких як третинний бутилат калію з краунефірами або з четвертинними гідроксидами амонію (патенти США 5382691, 5633407, 5618979 і 5451702) Наступне перетворення 4-РАДФА в 4АДФА може бути здійснено або каталітичним гідруванням ВІДПОВІДНО до патенту США 5451702, або реакцією нуклеофільного заміщення 4-РАДФА аміном у присутності сильних основ (патенти США 5382691, 5633407 і 5618979) 4-АДФА може бути також одержаний (див патенти США 5618979 і 5633407, а також роботу М К Stern et al , J Org Chem 59, 5627-5632, 1994) в одну стадію безпосередньо реакцією азобензолу, зокрема азоксибензолу, з аніліном у присутності сильнолужних каталізаторів Однак у всіх вищевказаних методиках вихідною сировиною є азобензол, який технічно являє собою більш важкодоступну сировину і повинен бути одержаний заздалегідь Крім того, виникає велика КІЛЬКІСТЬ ВІДХОДІВ, ЯКІ ПОВИННІ бути обов'язково оброблені або знищені У ряді патентів на ім'я компанії Monsanto (патенти США 5117063, 5453451, 5608111, 5623088) описаний спосіб одержання проміжних продуктів 4АДТА прямою реакцією аніліну з нітробензолом в апротонному розчиннику з контрольованою КІЛЬКІСТЮ протонного розчинника під впливом основ, що включають лужні гідроксиди, алкоголяти, гідриди і 56354 четвертинні гідроксиди амонію з алкіл-, арил- і аралкілзамісниками, а також алкілзаміщені гідроксиди діамонію Проте високий вихід реакційних продуктів і висока селективність можуть бути досягнуті тільки при використанні четвертинних гідроксидів амонію Механізм реакції описаний у (М К Stern e t a l , J Am Chem Soe 114, 9237-9238, 1992 і New J Chem 20, 259-268, 1996) У результаті порівняння ВІДПОВІДНИХ ОСНОВ, описаних у вищенаведених патентах і роботах, що застосовуються у реакції аніліну з нітробензолом, стає зрозуміло, що лужні гідроксиди забезпечують низький вихід проміжних сполук 4-АДФА Вихід істотно збільшується при використанні лужних гідроксидів разом із краун-ефірами Проте, беручи до уваги їх технічно складне одержання, їхнє промислове застосування не дуже можливе Реакція в присутності бушлату калію і ДМСО також дає низьку селективність На противагу цьому, при використанні в реакції як основи четвертинних гідроксидів амонію досягаються як висока селективність, так і високий вихід Проте їхнім недоліком є низька стабільність, вони розкладаються в концентрованому виді, тому вони повинні зберігатися тільки в розведених водних розчинах Іншим недоліком є також їхня низька термостійкість, вони легко розкладаються при високих температурах (A Cope et al , Org Reactions, Vol XI, p 317, 1960, Hellman H , Angew Chem 65, 475-485, 1953, F Moller, Methoden der Orgamschen Chemie, Houben-Weyl XI/1, p 961-967, 262, 1957, і XI/2, p 623, 631-640, 1958) Внаслідок дії четвертинних гідроксидів амонію на первинні аміни також має місце їх легке алкілування Наприклад, гідроксид тетраметиламонію (ТМАН) взаємодіє з аніліном, даючи N-метиланілш у КІЛЬКОСТІ, що залежить від вибраних умов реакції (патент США 5687691) Одержаний N-метиланілш може бути складно ВІДДІЛИТИ ВІД аніліну, але це повинно бути зроблене перед рециркуляцією аніліну назад у подальший реакційний цикл, щоб уникнути утворення небажаних домішок метильованих похідних 4-АДФА Недоліком четвертинних гідроксидів амонію per se також є висока вартість Тому в кожному циклі виникає необхідність виділення і рециркуляції четвертинних амонієвих основ для наступного виробничого циклу, що не може бути зроблене без зниження їхньої активності Метою даного винаходу є розробка способу, що використовує переваги відомих розчинів і усуває їхні недоліки Метою даного винаходу є спосіб одержання 4амінодифеніламшу через одержання проміжної сполуки 4-нітродифеніламшу і/або 4нітрозодифеніламіну, і/або їхніх солей взаємодією аніліну і нітробензолу в рідкому середовищі при температурі від 50 до 130°С, атмосферному або зниженому тиску, атмосфері інертного газу або в присутності кисню повітря з наступним гідруванням проміжної сполуки 4-нітродифеніламіну і/або нітрозодифеніламіну та побічних продуктів, і виділенням 4-амінодифеніламшута побічних продуктів і рециклом неконвертованої сировини Суть даного винаходу полягає в тому, що реакцію аніліну з нітробензолом здійснюють у реакційній системі, яка включає розчин цвітерюнної солі з гідроксидами загальної формули 1 3 + + HO/(R FrR )N -CHR4-(CH2)x-WZ 1 де R і R2 позначають радикал від метилу до додецилу, R позначає метил, етил, феніл, бензил, 4 R позначає водень або метил, х означає ціле число від 0 до 5, Y~ означає СО 2, SO з, і + Z позначає катіон лужного металу Na, К, Cs або чотиризаміщений катіон четвертинного амонію, такого як тетраметиламоній, або їхні взаємні поєднання, в яких КІЛЬКІСТЬ ЯК СОЛІ цвітерюна, так і гідроксиду знаходитсья, щонайменше, у еквімолярному співвідношенні з КІЛЬКІСТЮ нітробензолу, що прореагував у реакції, з утворенням 4нітрозодифеніламіну і/або 4-нітродифеніламіну, які після гідрування дають 4-АДФА, і після реакції рециркулюють, щонайменше, половину реакційної системи Встановлено, що краще проводити реакцію в присутності розчину солі цвітерюна з гідроксидами загальної формули, де R1, R2 і R3 представляють метил, R4 представляє водень, х представляє 0, Y~ представляє CO 2, a Z+ представляє катіон калію і/або чотиризаміщений катіон четвертинного амонію, більш переважно Z+ представляє катіон, калію і/або катіон тетраалкіламонію з КІЛЬКІСТЮ атомів вуглецю в алкільному ланцюгу від 1 до 4 Реакційне середовище може бути одержане окремо і/або воно може бути одержане in situ у реакційній системі з вихідної сировини Рідке середовище для реакції аніліну з нітробензолом одержують змішуванням з водою і/або щонайменше однією органічною сполукою, такою як анілін, піридин, толуол, ксилол, циклогексан та аліфатичні спирти, що мають у молекулі від 1 до 4 атомів вуглецю Перевага даного способу, що включає реакцію аніліну з нітробензолом, головним чином полягає у використанні реакційної системи ВІДПОВІДНО ДО даного винаходу Вона технічно більш легкодоступна і більш стійка, ніж самі четвертинні гідроксиди амонію та алкілдіамонію, у той час як реакція аніліну з нітробензолом є досить селективною для одержання проміжних сполук 4-АДФА (із селективністю, яка складає, щонайменше, 50% 4нітродифеніламшу і нітрозодифеніламіну), при цьому вихід одержуваного продукту є високим Однією З переваг способу ВІДПОВІДНО ДО даного винаходу є також технічно доступний широкий діапазон як біполярних, так і багатополярних органічних сполук, що містять у молекулі щонайменше один катіон азоту, а також їх стабільність, не тільки термальна, але і стабільність при гідруванні, і той факт, що реакційна система може бути регенерована З літератури (М Rabmowitz et a l , Angew Chem 98, 958-968, 1986) відомо, що багато органічних реакцій, ініційованих гідроксидами, протікають в умовах системи КФП/ОН , тобто в присутності каталізаторів фазового перенесення (КФП) Звичайнозастосовувані КФП являють собою четвертинні іони амонію Також відоме застосування цвітерюнних солей у деяких реакціях як каталізаторів фазового перенесення, проте у даному ви 56354 падку імовірний механізм дм ВІДМІННИЙ, ОСКІЛЬКИ З біполярної внутрішньої солі цвітерюна і гідроксиду утворюється біс-юнна пара (G Starks et al , Phase Transfer Catalysts Principles and Technique, N Y Acad Press 1978, p 67, 127, 365, Yu Sh Goldberg etal, Dokl Akad Nauk SSSR 294, 1387-1391, 1987, Yu Sh Goldberg et al, Zhur Org Khim, 23, 15611563, 1987, Yu Sh Goldberg et al Tetrahedron 46, 1911-1922,1990) Під цвітерюнами розуміють сполуки, які містять у своїх молекулах, крім карбоксильної групи, пералкіловану аміногрупу, при цьому дані групи взаємно утворюють внутрішні солі Такі сполуки не містять рухомого водню, а містять групу четвертинного амонію У способах, відомих з літератури, цвітерюнні солі застосовують як каталізатори фазового перенесення в каталітичній КІЛЬКОСТІ, а саме, у КІЛЬКОСТІ ВІД 1 до 5%мол У, даний час встановлено, що при використанні способу одержання проміжних сполук 4-АДФА ВІДПОВІДНО до даного винаходу може бути досягнута повна конверсія нітробензолу з аніліном при проведенні реакції з щонайменше еквімолярною КІЛЬКІСТЮ цвітерюнної солі і гідроксиду відносно КІЛЬКОСТІ нітробензолу, присутнього в реакції, що вказує на інший хід реакції Цвітерюнні солі, також ВІДОМІ ЯК бетаїни або, зокрема, сульфобеташи, випускаються промисловістю у вигляді внутрішньомолекулярних солей або пдратованих форм, або можуть бути одержані ВІДПОВІДНО до способів, відомих з літератури (Methoden der Organischen Chemie (Houben-Weyl), XI/2, p 627-650, 1958, Ullmans Enzyklopadie der Techmschen Chemie, Vol 2, p 497-498, Verlag Chemie 1982, Goldberg Yu Sh et al, Tetrahedron 46, 1911-1922, 1990, Goldberg Yu Sh et al , Dokl Akad Nauk SSSR297, 1387-1391, 1987, Willstatter R , Ber, 35, 584-620, 1907, патент США 4672077 і бельгійський патент 903785) Реакційна система для конденсації аніліну з нітробензолом може бути одержана в такий спосіб одержують розчин гідроксиду в протонному розчиннику (у воді, метанолі або 2-пропанолі), додають до нього кристалічну цвітерюнну сіль, можливо, у вигляді гідрату, а потім вводять ВІДПОВІДНИЙ розчинник, наприклад, анілін Можна вчинити також у такий спосіб анілін додають до розчину гідроксиду в протонному розчиннику і до такої суміші додають цвітерюнну сіль, При одержанні реакційної системи, що складається з суміші гідроксидів, можна також вчинити у такий спосіб до розведеного водного розчину гідроксиду четвертинного амонію додають кристалічну цвітерюнну сіль і після її розчинення твердий гідроксид лужного металу, і, нарешті, додають анілін Також може бути одержаний розчин метилату розчиненням лужного металу, його оксиду або гідроксиду в метанолі і додаванням розчину цвітерюнної солі в аніліні Взаємне співвідношення реакційних компонентів може змінюватися в широкому діапазоні таким чином, щоб компонентом, який лімітує, була або цвітерюнна сіль, або нітробензол, або анілін, їхнє 8 взаємне співвідношення може бути вибране таким чином, щоб реакція проходила в оптимальних умовах Реакція може бути здійснена в широкому діапазоні температур від 50 до 130°С Реакція також може бути проведена в атмосфері інертного газу або в аеробних умовах, при атмосферному або зниженому тиску, у той час як вихід, конверсія і селективність реакції залежать від умов реакції В реакції також можуть бути використані ДОПОМІЖНІ протонні та апротонні розчинники, такі як третинний бутиловий спирт, ДМСО, диметиловий ефір діетиленгліколю, монометиловий ефір етиленгліколю, толуол, ксилол, циклогексан і т д Основними продуктами, одержуваними в результаті реакції, є 4-ІЧОДФА і 4-І\ІО2ДФА, які присутні у реакційній суміші у вільному вигляді або у вигляді солей Реакційна суміш, крім цих сполук і реакційної води, може додатково включати такі речовини, як 4-фенілазодифеніламш, азобензол, азоксибензол, 2-нітродифеніламш, феназин або окис феназину Це залежить від молярного співвідношення реакційних компонентів системи, а також від типу цвітерюнів, їх солей, протонного розчинника, можливо, від допоміжного розчинника і їх концентрації в реакційній суміші, температури, тривалості реакції і міри конверсії нітробензолу Дані факти добре ВІДОМІ фахівцям у даній галузі 4-АДФА одержують із суміші 4-І\ІОДФА, 4ІЧОгДФА і 4-фенілазодифеніламіну або їх солей відомими способами каталітичного гідрування після розведення реакційної суміші розчинником Наступні приклади ілюструють, але ніяким чином не обмежують обсяг формули винаходу Приклад 1 Результати реакції аніліну з нітробензолом в анаеробних умовах, коли реакційна система являє собою розчин бетаїну і гідроксиду калію в метанолі при різних температурах в інтервалі від 55 до 130°С Реакцію проводять в апаратах, що складаються з 100-мл 3-горлоі колби, обладнаної магнітною мішалкою, термометром, краплинною лійкою і насадкою для азеотропної перегонки Апарати з'єднані з водоструминним насосом, 3,5г (84,02%) гідроксиду калію (0,052моля) розчиняють у 6г метанолу Додають 6,1г бетаїну (0,052моля), і після нагрівання до 50°С додають 37,0г аніліну (0,49молів) Повітря в апараті заміняють азотом і після нагрівання до реакційної температури спочатку відганяють метанол при тиску 5,2кРа, а потім при інтенсивному перемішуванні протягом 1,5 години порціями додають нітробензол, у цілому 6,4г (0,052моля) Реакційну суміш залишають взаємодіяти протягом ще 3 годин, потім її охолоджують, розбавляють метанолом і аналізують з використанням високоефективної рідинної хроматографії Вихід реакційних компонентів визначають відносно КІЛЬКОСТІ нітробензолу, що вводиться в реакцію Інші реакційні умови та одержані результати представлені в таблиці 1 56354 10 Таблиця 1 Температура (°С) 55 70 90 130 4-ЫДФА 18,2 33,3 40,3 22,2 Вихід ВІДНОСНО введеного нітробензолу (%) 4-Ш 2 ДФА Азобензол 10,0 8,5 18,7 7,3 23,1 28,0 22,2 44,1 Приклад 2 Результати взаємодії аніліну і нітробензолу при використанні гідроксиду ЛІТІЮ, натрію, калію і цезію в реакційній системі, що містить гідроксид бетаїну Реакційні системи одержують взаємодією мо Феназин 1,4 2,9 9,3 ногідрату бетаїну з лужними гідроксидами ВІДПОВІДНО до методики, описаної в прикладі 1, проводять 3 ідентичні реакції при температурі 70°С з різними катіонами лужних металів, зазначених у таблиці 2 Таблиця 2 Катіон Na+ К+ Cs+ 4-ШДФА 24,7 36,0 39,1 Вихід реакції у % від завантаженого нітробензолу 4-Ш 2 ДФА Азобензол 31,1 31,6 16,3 13,8 17,6 10,8 Приклад З Результати взаємодії аніліну і нітробензолу з реакційною системою беташ-пдроксид натрію в метанолі в аеробних умовах До розчину каталізатора, який включає 0,066моль бетаїну і 0,066моль гідроксиду натрію в 15г метанолу, додають 0,4моля аніліну Після нагрівання реакційної суміші до 70°С до реакційної суміші порціями додають нітробензол протягом 1,5 години Метанол і реакційну воду поступово видаляють з реакційної суміші при зниженому тиску Після завершення порційного додавання нітробензолу суміш перемішують протягом ще 3,5 годин Після розведення метанолом суміш аналізують, визначаючи вихід реакційних продуктів, виражений у % відносно нітробензолу, завантаженого в реакційну суміш 4-ШДФА 26,3%, 4-Ш 2 ДФА 16,8%, 4-РАДФА 5,1%, азобензол 40,8% Приклад 4 Модифікована методика, у якій всі компоненти реакції вводять у реакцію на початку У колбі в 5,0мл води розчиняють 2,66г (83,0%) гідроксиду калію і додають 5,31г гідрату бетаїну, 24,1г аніліну і 4,83г нітробензолу Реакційну суміш інтенсивно перемішують при 80°С в атмосфері азоту протягом 5 годин Протягом цього періоду часу тиск у пристрої поступово знижують з 53кРа до 2,6кРа Нарешті реакційну суміш розчиняють у метанолі та аналізують за допомогою високоефективної рідинної хроматографії Конверсія нітробензолу складала 75,6%, а вихід (у %) індивідуальних продуктів, обчислений відносно нітробензолу, що вводиться, складає Феназин 10,9 9,8 4-ШДФА 35,7, 4-Ш 2 ДФА 17,8%, 4-РАДФА 0,12%, азобензол 10,9%, феназин 1,25% Приклад 5 Взаємодія аніліну з надлишком нітробензолу (як розчинника) в присутності реакційної системи беташ-пдроксид калію в анаеробних умовах До розчину 3,38г (83%) гідроксиду калію в 3,0мл води додають 6,85г гідрату бетаїну і 26,8г нітробензолу При температурі 80°С і тиску 20кРа до реакційної суміші в атмосфері азоту порціями додають 4,9г аніліну протягом 1,5 години Після завершення порційного додавання нітробензолу реакційну суміш інтенсивно перемішують протягом ще 6 годин Після охолодження реакційну суміш розчиняють у метанолі Одержують такий вихід, обчислений відносно нітробензолу, що вводиться в реакцію 4-ЫОДФА 1,5%, 4-Ш 2 ДФА 0,2%, азобензол 2,5% Приклад 6 Дія молярного співвідношення бетаїнупдроксиду калію і нітробензолу на хід реакції Застосовуючи методику, описану в прикладі 1, здійснюють взаємодію аніліну з нітробензолом при молярному співвідношенні 7 1 з тією ВІДМІННІСТЮ, що молярне співвідношення реакційної системи до нітробензолу змінюється від 1 1 до 1,5 1 Бетаїн гідрат і гідроокис калію утворюють реакційну систему з молярним співвідношенням 1 1 у розчині метанолу Результати експериментів, наведені в таблиці 3, показують дію підвищення КІЛЬКОСТІ реакційної системи на вихід реакції і конверсію нітробензолу 11 56354 12 Таблиця З Молярне співвідношення каталізатора до нітробензолу 1,1 1 1,21 1,31 1,51 Вихід, обчислений відносно нітробензолу, що вводиться, (%) Конверсія нітробензолу 4-ШДФА 4-Ш2ДФА 4-FAfl
ДивитисяДодаткова інформація
Назва патенту англійськоюA method of preparation of 4-aminodiphеnylamine
Назва патенту російськоюСпособ получения 4-аминодифениламина
МПК / Мітки
МПК: C07C 209/38, C07C 209/36, C07C 211/52, C07C 209/68, C07B 61/00, C07C 211/50, C07C 209/60
Мітки: спосіб, одержання, 4-амінодифеніламіну
Код посилання
<a href="https://ua.patents.su/10-56354-sposib-oderzhannya-4-aminodifenilaminu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 4-амінодифеніламіну</a>
Попередній патент: Навісний оборотний плуг із змінною шириною захвату
Наступний патент: Спосіб обробки фільтрувальної тканини
Випадковий патент: Абсорбер роторний