1,3-дизаміщені сечовини та спосіб їх одержання
Номер патенту: 61125
Опубліковано: 17.11.2003
Автори: Какалік Іван, Оремус Владімір, Земанек Маріан, Шмаховскі Венделін, Фаберова Вєра, Шмідтова Людміла
Формула / Реферат
1. 1,3-Дизаміщені сечовини загальної формули І
, I
де
X = O, S,
R2 = NO2, NH2,
якщо R1 означає 2-фторфеніл, 2,4-дифторфеніл, 2,5-дифторфеніл, 2,6-дифторфеніл, 2-хлорфеніл, 2,3-дихлорфеніл, 2,6-дихлорфеніл, 3,5-дихлорфеніл, 2-метилфеніл, 4-метилфеніл, 2,4-диметилфеніл, 2,6-диметилфеніл, 3,5-диметилфеніл, 2,6-ди(метилетил)феніл, 2-трифторметилфеніл, 3-трифторметилфеніл, 4-трифторметилфеніл, 2-піридил, 3-піридил, 4-піридил, 1-нафтил, 2-нафтил, 1-адамантил, то R2 означає нітрогрупу, і Х=О,
якщо R1 означає 4-нітрофеніл, 2-фторфеніл, 4-фторфеніл, 2,4-дифторфеніл, 2,5-дифторфеніл, 2,6-дифторфеніл, 2-хлорфеніл, 4-хлорфеніл, 2,3-дихлорфеніл, 2,4-дихлорфеніл, 2,6-дихлорфеніл, 3,4-дихлорфеніл, 3,5-дихлорфеніл, 2-метилфеніл, 4-метилфеніл, 2,4-диметилфеніл, 2,6-диметилфеніл, 3,5-диметилфеніл, 2,6-ди(метилетил)феніл, 2-трифторметилфеніл, 3-трифторметилфеніл, 4-трифторметилфеніл, 2-піридил, 3-піридил, 4-піридил, 1-нафтил, 2-нафтил, 1-адамантил, то R2 означає нітрогрупу, і Х=S,
і якщо R1 означає 2,4-дифторфеніл, 2,3-дихлорфеніл, 2,6-диметилфеніл, 2,6-ди(метилетил)феніл, R2 означає аміногрупу, то Х=О, S.
2. 1,3-Дизаміщені сечовини згідно з п. 1, які відрізняються тим, що їм властива інгібуюча активність відносно ферменту ацил-КоА: холестерол-ацилтрансферази (АСАТ).
3. Спосіб одержання 1,3-дизаміщених сечовин загальної формули І
, І
де
X=O, S,
R2=NO2, NH2,
якщо R1 означає 2-фторфеніл, 2,4-дифторфеніл, 2,5-дифторфеніл, 2,6-дифторфеніл, 2-хлорфеніл, 2,3-дихлорфеніл, 2,6-дихлорфеніл, 3,5-дихлорфеніл, 2-метилфеніл, 4-метилфеніл, 2,4-диметилфеніл, 2,6-диметилфеніл, 3,5-диметилфеніл, 2,6-ди(метилетил)феніл, 2-трифторметилфеніл, 3-трифторметилфеніл, 4-трифторметилфеніл, 2-піридил, 3-піридил, 4-піридил, 1-нафтил, 2-нафтил, 1-адамантил, то R2 означає нітрогрупу, і Х=О,
якщо R1 означає 4-нітрофеніл, 2-фторфеніл, 4-фторфеніл, 2,4-дифторфеніл, 2,5-дифторфеніл, 2,6-дифторфеніл, 2-хлорфеніл, 4-хлорфеніл, 2,3-дихлорфеніл, 2,4-дихлорфеніл, 2,6-дихлорфеніл, 3,4-дихлорфеніл, 3,5-дихлорфеніл, 2-метилфеніл, 4-метилфеніл, 2,4-диметилфеніл, 2,6-диметилфеніл, 3,5-диметилфеніл, 2,6-ди(метилетил)феніл, 2-трифторметилфеніл, 3-трифторметилфеніл, 4-трифторметилфеніл, 2-піридил, 3-піридил, 4-піридил, 1-нафтил, 2-нафтил, 1-адамантил, то R2 означає нітрогрупу, і Х=S,
і якщо R1 означає 2,4-дифторфеніл, 2,3-дихлорфеніл, 2,6-диметилфеніл, 2,6-ди(метилетил)феніл, R2 означає аміногрупу, то Х=О, S,
який відрізняється тим, що амін загальної формули II
, ІІ
в якій R2 і Х мають вищевказані значення, вводять у взаємодію з ізоціанатом загальної формули III
R1-N=С=O, (III)
в якій R1 має вищевказані значення, причому ізоціанат необов'язково одержують in situ з відповідних реагентів.
4. Спосіб згідно з п. 3, який відрізняється тим, що при одержанні ізоціанату in situ реакцію проводять у толуолі при температурі приблизно 80°С.
5. Спосіб згідно з будь-яким з пп. 3-4, який відрізняється тим, що одержану 1,3-дизаміщену сечовину загальної формули І, в якій R2 означає нітрогрупу, обробляють воднем у присутності паладієвого каталізатора, внаслідок чого нітрогрупа відновлюється до аміногрупи.
Текст
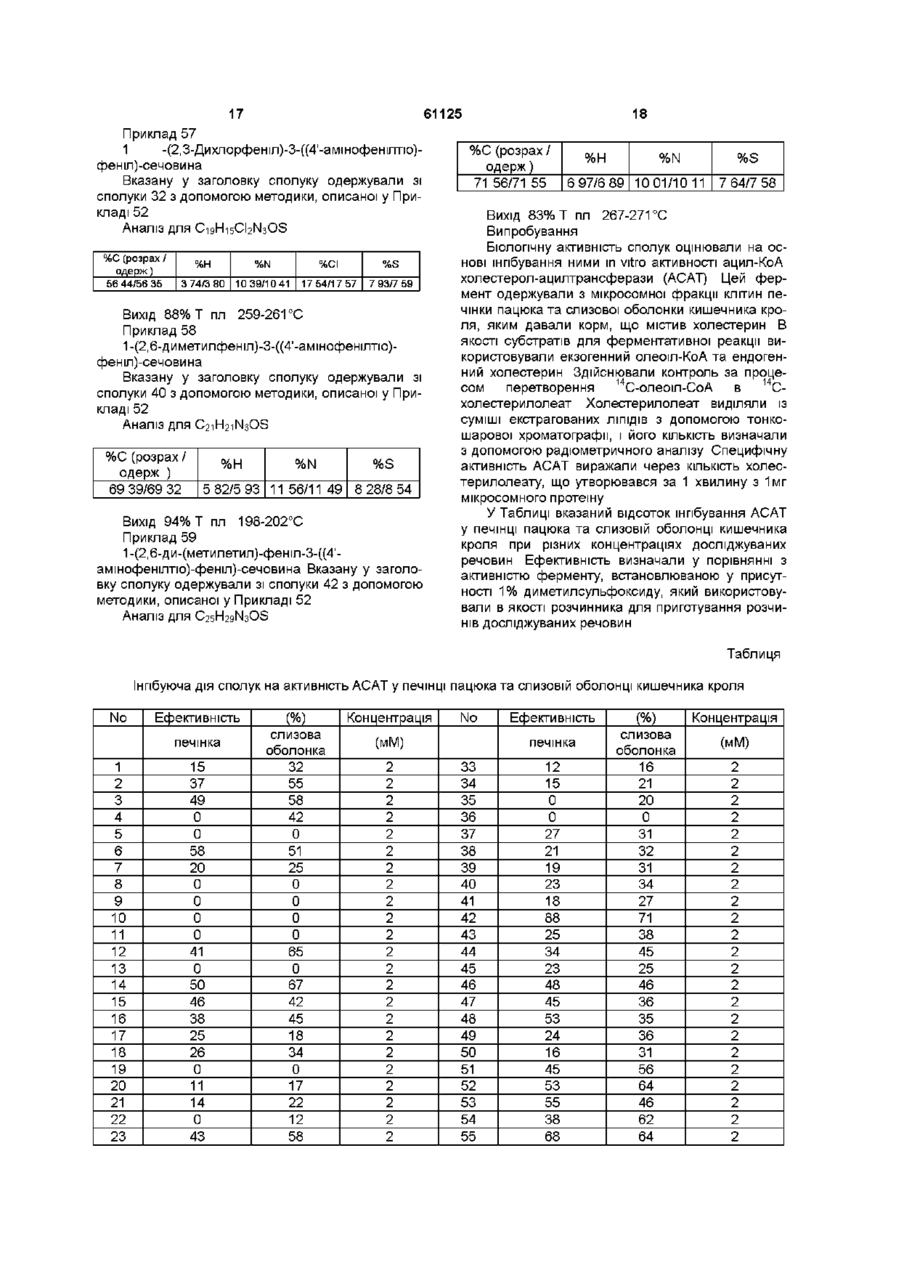
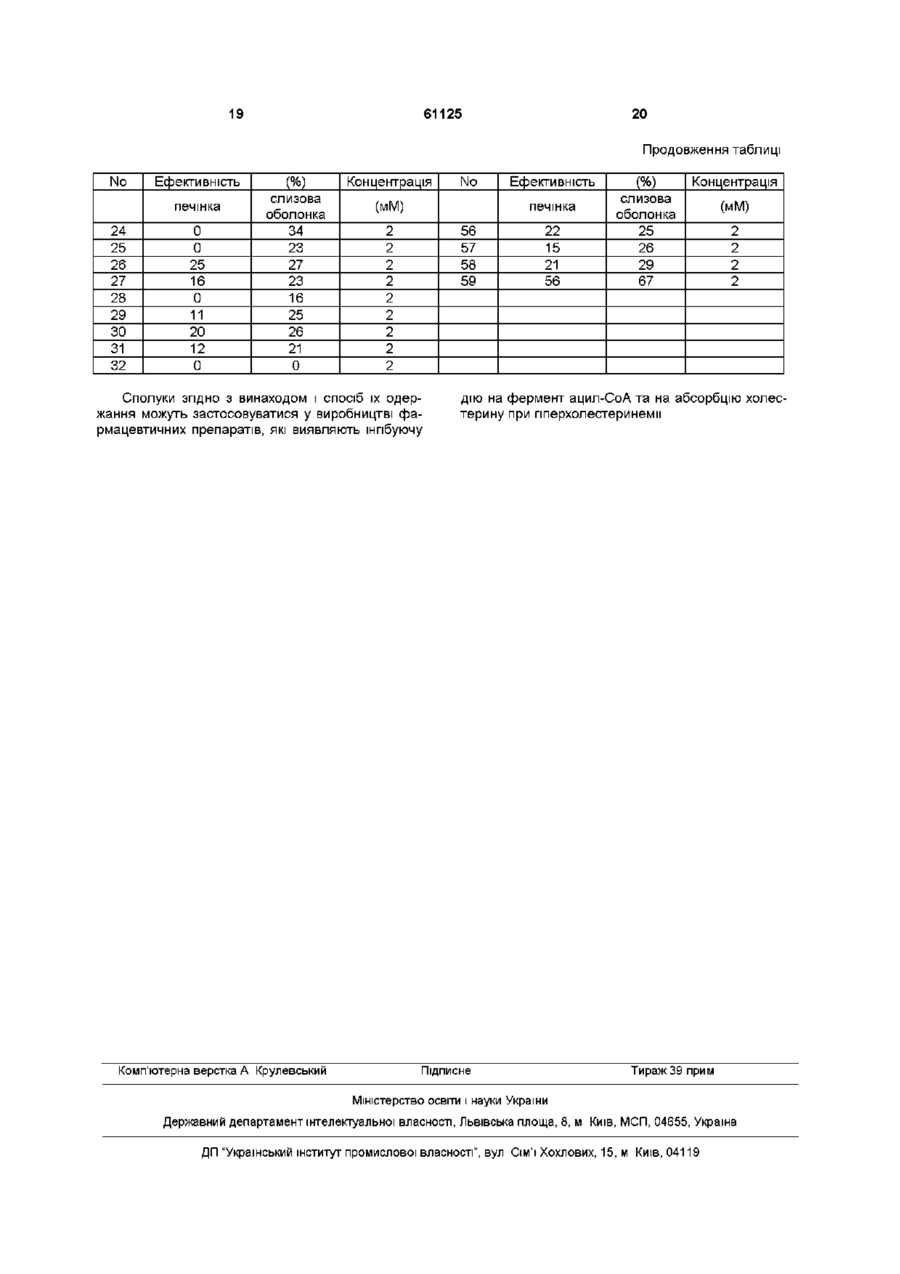
1 1,3-Дизаміщені сечовини загальної формули І 1 і якщо R означає 2,4-дифторфеніл, 2,3дихлорфеніл, 2,6-диметилфеніл, 2,62 ди(метилетил)феніл, R означає аміногрупу, то Х=О, S 2 1,3-Дизаміщені сечовини згідно з п 1, які відрізняються тим, що їм властива інгібуюча активність відносно ферменту ацил-КоА холестеролацилтрансферази (АСАТ) 3 Спосіб одержання 1,3-дизаміщених сечовин загальної формули І R\ Де х=о, s, R2=NO2, NH2, NH Де х 2= о, s, R = NO2, NH2, якщо R1 означає 2-фторфеніл, 2,4-дифторфеніл, 2,5-дифторфеніл, 2,6-дифторфеніл, 2-хлорфеніл, 2,3-дихлорфеніл, 2,6-дихлорфеніл, 3,5дихлорфеніл, 2-метилфеніл, 4-метилфеніл, 2,4диметилфеніл, 2,6-диметилфеніл, 3,5диметилфеніл, 2,6-ди(метилетил)феніл, 2трифторметилфеніл, 3-трифторметилфеніл 4трифторметилфеніл, 2-піридил, 3-піридил 4піридил, 1-нафтил, 2-нафтил, 1-адамантил, то R 2 означає нітрогрупу, і Х=О, якщо R1 означає 4-нітрофеніл 2-фторфеніл, 4фторфеніл, 2,4-дифторфеніл, 2,5-дифторфеніл, 2,6-дифторфеніл, 2-хлорфеніл, 4-хлорфеніл, 2,3дихлорфеніл, 2,4-дихлорфеніл, 2,6-дихлорфеніл, 3,4-дихлорфеніл, 3,5-дихлорфеніл, 2-метилфеніл, 4-метилфеніл, 2,4-диметилфеніл, 2,6диметилфеніл, 3,5-диметилфеніл, 2,6ди(метилетил)феніл, 2-трифторметилфеніл, 3трифторметилфеніл, 4-трифторметилфеніл, 2піридил, 3-піридил 4-піридил, 1-нафтил, 2-нафтил, 1-адамантил, то R означає нітрогрупу, і X=S, якщо R1 означає 2-фторфеніл, 2,4-дифторфеніл, 2,5-дифторфеніл, 2,6-дифторфеніл, 2-хлорфеніл, 2,3-дихлорфеніл, 2,6-дихлорфеніл, 3,5дихлорфеніл, 2-метилфеніл, 4-метилфеніл, 2,4диметилфеніл, 2,6-диметилфеніл, 3,5диметилфеніл, 2,6-ди(метилетил)феніл, 2трифторметилфеніл, 3-трифторметилфеніл 4трифторметилфеніл, 2-піридил, 3-піридил 4піридил, 1-нафтил, 2-нафтил, 1-адамантил, то R 2 означає нітрогрупу, і Х=О, якщо R1 означає 4-нітрофеніл 2-фторфеніл, 4фторфеніл, 2,4-дифторфеніл, 2,5-дифторфеніл, 2,6-дифторфеніл, 2-хлорфеніл, 4-хлорфеніл, 2,3дихлорфеніл, 2,4-дихлорфеніл, 2,6-дихлорфеніл, 3,4-дихлорфеніл, 3,5-дихлорфеніл, 2-метилфеніл, 4-метилфеніл, 2,4-диметилфеніл, 2,6диметилфеніл, 3,5-диметилфеніл, 2,6ди(метилетил)феніл, 2-трифторметилфеніл, 3трифторметилфеніл, 4-трифторметилфеніл, 2піридил, 3-піридил 4-піридил, 1-нафтил, 2-нафтил, 1-адамантил, то R означає нітрогрупу, і X=S, і якщо R1 означає 2,4-дифторфеніл, 2,3дихлорфеніл, 2,6-диметилфеніл, 2,6ди(метилетил)феніл, R2 означає аміногрупу, то х=о, s, який відрізняється тим, що амін загальної формули II О Ю (О 61125 в якій R і X мають вищевказані значення, вводять у взаємодію з ізоціанатом загальної формули III R1-N=C=O, (III) в якій R1 має вищевказані значення, причому ізоціанат необов'язково одержують in situ з ВІДПОВІД Винахід стосується сполук, основною властивістю яких є здатність інгібувати активність ферменту ацил-КоА холестерол-ацилтрансферази (АСАТ), та способу їх одержання Фермент ацил-КоА холестерол Оацилтрансфераза (ЕС 2 3 1 26) (АСАТ) відповідає за каталіз внутрішньоклітинної естерифікації холестерину АСАТ присутній у більшості тканин, таких як кишкова, печінкова тканини та тканина стінок артерії Вважається, що цей фермент бере участь у ряді процесів, які лежать в основі розвитку атеросклерозу, абсорбції холестерину харчового походження, накопичення складних ефірів холестерину, секреції печінкою складних ефірів холестерину у вигляді холестерину дуже низької густини в плазму крові Відомо, ЩО ряд речовин типу сечовини має властивості інгібіторів АСАТ Даний винахід стосується декількох нових прикладів 1,3-дизаміщених сечовин, що мають властивості інгібіторів ферменту АСАТ У патентах ЕР 506532, FR 2674522, JP 93097802, US 5219859 описані сечовини, молекули яких містять ПОХІДНІ індолу У патентах ЕР 665216, JP 95258199 А описане поєднання в молекулі ароматичної та аліфатичної частин Про введення у молекулу сечовини 1,3-дюксоланового кільця згадувалось в Bioorg Med Chem Lett 1995, 5(15) 1581 Незважаючи на той факт, що деякі з 1,3дизаміщених сечовин, які мають подібну структуру, були описані в патенті США №3284433 як анТИКОКЦИДІЙНІ агенти, і одна сполука подібної структури описана в заявці на європейський патент ЕР 0709225 як агент, що посилює забарвлення, 1,3дизаміщені сечовини згідно з винаходом досі не були описані в літературі Об'єктом винаходу є 1,3-дизаміщені сечовини загальної формули І x=o,s FT= N02, NH-2 НИХ реагентів 4 Спосіб згідно з п 3, який відрізняється тим, що при одержанні ізоціанату in situ реакцію проводять у толуолі при температурі приблизно 80°С 5 Спосіб згідно з будь-яким з пп 3-4, який відрізняється тим, що одержану 1,3-дизаміщену сечовину загальної формули І, в якій R2 означає нітрогрупу, обробляють воднем у присутності паладієвого каталізатора, внаслідок чого нітрогрупа відновлюється до аміногрупи в якій R1 означає 2-фторфеніл, 2,4дифторфеніл, 2,5-дифторфеніл, 2,6-дифторфеніл, 2-хлорфеніл, 2,3-дихлорфеніл, 2,6-дихлорфеніл, 3,5-дихлорфеніл, 2-метилфеніл, 4-метилфеніл, 2,4-диметилфеніл, 2,6-диметилфеніл, 3,5диметилфеніл, 2,6-ди(метилетил)феніл, 2трифторметил феніл, 3-трифторметилфеніл, 4трифторметилфеніл, 2-піридил, 3-піридил, 4піридил, 1-нафтил, 2-нафтил, 1-адамантил, a R2 означає нітро-групу, і X = О, в якій R1 означає 4-нітрофеніл, 2-фторфеніл, 4-фторфеніл, 2,4-дифторфеніл, 2,5-дифторфеніл, 2,6-дифторфеніл, 2-хлорфеніл, 4-хлорфеніл, 2,3дихлорфеніл, 2,4-дихлорфеніл, 2,6-дихлорфеніл, 3,4-дихлорфеніл, 3,5-дихлорфеніл, 2-метилфеніл, 4-метилфеніл, 2,4-диметилфеніл, 2,6диметилфеніл, 3,5-диметилфеніл, 2,6ди(метилетил)феніл, 2-трифторметилфеніл, 3трифторметилфеніл, 4-трифторметилфеніл, 2піридил, 3-піридил, 4-піридил, 1-нафтил, 2-нафтил, 1-адамантил, a R2 означає нітро-групу, і Х = S, і якщо R1 означає 2,4-дифторфеніл, 2,3дихлорфеніл, 2,6-диметилфеніл, 2,6ди(метилетил)-феніл, R означає аміно-групу, і Х=О, S Ще одним об'єктом винаходу є спосіб одержання вищезгаданих сполук згідно з винаходом, який полягає у тому, що ізоціанат (одержаний m situ або такий, що наявний на ринку) вводять у взаємодію з аміном, в результаті чого одержують сечовину, нітро-група якої може бути відновлена на наступному етапі до аміно-групи Одержані таким чином сечовини інгібують ацил-КоА холестерол-ацилтрансферазу (АСАТ) Приклади Приклад 1 1 -(2-Фторфеніл)-3-((4'-нітрофенокси)-феніл)сечовина До розчину 4'-нітрофеноксианілшу (2 30г, 0 01 моль) в суміші діетилового ефіру (20мл) і тетрапдрофурану (20мл) при кімнатній температурі по краплях додають розчин 2-фторфенілізоціанату (1,1 еквів) в діетиловому ефірі (20мл), і суміш перемішують протягом ночі Осад відсмоктують, промивають діетиловим ефіром (20мл) Неочищений продукт очищають хроматографією на силікагелі, елююючи сумішшю дихлорметан/метанол Аналіз для Ci 9 Hi 4 FN 3 O4 61125 %С (розрах /одерж) 62 11/62 09 %Н 3 84/3 88 %N 11 44/11 29 Вихід 48% Т ПЛ 253-255°С Приклад 2 1 -(2,4-Дифторфеніл)-3-((4'-нітрофенокси)феніл)-сечовина Вказану у заголовку сполуку одержували з 2,4дифторфенілізоціанату з допомогою методики; описаної у Прикладі 1 1 Н-ЯМР (CDCI3) 6 98-7 18(м, 5Н, Н-аром), 7 23-7 37(м, 1Н, Н-аром), 7 56(д, 2Н, Н-аром). 8 03-8 16(м, 1 Н, Н-аром), 8 24(д, 2Н, Н-аром). 8 50(с, 1Н, NH), 9 13(с, 1Н, NH) 13 С-ЯМР (CDCI3) 103 72(СН-аром), 110 96(СН-аром ), 116 73(СН-аром ), 119 88(СНаром ), 121 18(СН-аром ), 122 02(СН-аром ), 126 09(СН-аром), 136 94 14191, 148 48, 152 27. 154 49, 159 80(С-аром ), 163 46(С=О) Аналіз для C19H13F2N3O4 6 Вихід 75% Т ПЛ 231-232°С Приклад 5 1-(2-Хлорфеніл)-3-((4'-нітрофенокси)-феніл)сечовина Вказану у заголовку сполуку одержували з 2хлорфенілізоціанату з допомогою методики, описаної у Прикладі 1 Аналіз для C19H14CIN3O4 %С (розрах / одерж) 59 46/59 37 %Н %N %СІ 3 68/3 82 10 95/10 78 9 24/8 99 Вихід 63% Т ПЛ 195-197°С Приклад 6 1-(2,3-Дихлорфеніл)-3-((4'-нітрофенокси)феніл)-сечовина Вказану у заголовку сполуку одержували з 2,3дихлорфенілізоціанату з допомогою методики, описаної у Прикладі 1 Аналіз для C19H13CI2N3O4 %С(розрах /одерж) 59 22/59 20 %Н 3 40/3 53 %N 10 91/10 89 Вихід 85% Т ПЛ 223-224°С Приклад З 1-(2,5-Дифторфеніл)-3-((4'-нітрофенокси)феніл)-сечовина Вказану у заголовку сполуку одержували з 2,5дифторфенілізоціанату з допомогою методики, описаної у Прикладі 1 1 Н-ЯМР (CDCI3) 6 73-6 88(м, 1Н, Н-аром), 7 04-7 35(м, 5Н, Н-аром), 7 56(д, 2Н, Н-аром), 7 98-8 11 (м, 1 Н, Н-аром), 8 22(д, 2Н, Н-аром), 8 75-9 30(ш с , 2Н NH) 13 С-ЯМР (CDCI3) 106 56(СН-аром), 107 75(СН-аром ), 115 67(СН-аром ), 116 74(СНаром ), 120 03(СН-аром ), 121 21 (СН-аром ), 126 08(СН-аром), 128 82, 136 62 14195, 148 73, 151 95,155 65,160 38(С-аром), 163 42(С=О) Аналіз для C19H13F2N3O4 %С(розрах /одерж) 59 22/59 07 %Н 3 40/3 49 %N 10 91/10 83 Вихід 76% Т ПЛ 207-208°С Приклад 4 1 -(2,6-Дифторфеніл)-3-((4'-нітрофенокси)феніл)-сечовина Вказану у заголовку сполуку одержували з 2,6дифторфенілізоціанату з допомогою методики, описаної у Прикладі 1 1 Н-ЯМР (CDCI3) 6 95-7 26(м, 6Н, Н-аром), 7 42-7 56(м, 2Н, Н-аром), 8 01-8 23(м, ЗН Наром), 8 94-9 05(м, 2Н, NH) 13 С-ЯМР (CDCI3) 111 77(СН-аром), 116 82(СН-аром ), 120 06(СН-аром ), 121 18(СНаром), 12619(СН-аром), 12711 (СН-аром), 13731, 14199, 14849, 15261, 15565, 16057(Саром), 163 61(С=О) Аналіз для C19H13F2N3O4 %С (розрах /одерж) 59 22/59 10 %Н 3 40/3 55 %с (розрах/ одерж) 54 56/54 50 %Н %N %СІ 3 13/3 31 10 05/9 78 16 95/16 91 Вихід 74% Т ПЛ 199-201 °С Приклад 7 1-(2,6-Дихлорфеніл)-3-((4'-нітрофенокси)феніл)-сечовина Вказану у заголовку сполуку одержували з 2,6дихлорфенілізоціанату з допомогою методики, описаної у Прикладі 1 Аналіз для C19H13CI2N3O4 %С (розрах / %Н %N %СІ одерж) 54 56/54 39 3 13/3 20 10 05/9 92 16 95/16 81 Вихід 68% Т ПЛ 195-198°С Приклад 8 1 -(3,5-Дихлорфеніл)-3-((4'-нітрофенокси)феніл)-сечовина Вказану у заголовку сполуку одержували з 3,5дихлорфенілізоціанату з допомогою методики, описаної у Прикладі 1 Аналіз для C20H13CI2N3O4 %С (розрах / %Н %N %СІ одерж) 54 56/54 48 3 13/3 30 10 05/10 01 16 95/17 24 Вихід 56% Т ПЛ 213-216°С Приклад 9 1 -(2-Метилфеніл)-3-((4'-нітрофенокси)-феніл)сечовина Вказану у заголовку сполуку одержували з 2метилфенілізоціанату з допомогою методики, описаної у Прикладі 1 Аналіз дляC20H17N3O4 %N 10 91/10 78 %С (розрах /одерж) 60 11/65 96 %Н %N 4 72/4 89 11 56/11 48 61125 8 Н-ЯМР (CDCI3) 1 18(д, 6Н, 2хСН3), 3 22(гепт , 2Н, 2хСН), 7 06-7 30(м, 7Н, Н-аром ), 7 56(д, 2Н, Наром ), 7 63(с, 1Н, NH), 8 23(д, 2Н, Н-аром ), 8 78(с, 1Н, NH) 13 С-ЯМР (CDCI3) 23 31 (2хСН3), 27 86(2хСН), 116 58(СН-аром ), 119 44(СН-аром ), 120 86(СНаром ), 122 72(СН-аром ), 125 87(СН-аром ), 146 53(СН-аром), 127 08, 13214, 137 80, 14183, 147 89 154 10(С-аром), 163 46(С=О) 1 Вихід 59% Т ПЛ 112-116°С Приклад 10 1-(4-Метилфеніл)-3-((4'-нітрофенокси)-феніл)сечовина Вказану у заголовку сполуку одержували з 4метилфенілізоціанату з допомогою методики, описаної у Прикладі 1 Аналіз для C20H17N3O4 Аналіз для C25H27N3O4 %С (розрах /одерж) 66 11/66 02 %Н %N 4 72/4 87 1156/11 40 Вихід 64% Т ПЛ 168-170°С Приклад 11 1-(2,4-диметилфеніл)-3-((4'-нітрофенокси)феніл)-сечовина Вказану у заголовку сполуку одержували з 2,4диметилфенілізоціанату з допомогою методики, описаної у Прикладі 1 Аналіз для C21H19N3O4 %С (розрах /одерж) 66 83/66 87 %Н 5 07/5 10 %N 11 13/11 05 Вихід 73% Т ПЛ 165-169°С Приклад 12 1-(2,6-диметилфеніл)-3-((4'-нітрофенокси)феніл)-сечовина Вказану у заголовку сполуку одержували з 2,6диметилфенілізоціанату з допомогою методики, описаної у Прикладі 1 1 Н-ЯМР (CDCI3) 2 22(с, 6Н, СН3), 7 04-7 17(м, 7Н, Н-аром ), 7 57(м, 2Н Н-аром ), 7 74(с, 1Н, NH), 8 23(д, 2Н, Н-аром ), 8 87(с, 1Н, NH) 1 Х-ЯМР (CDCI3) 18 19(2х СН3), 116 61 (СНаром ), 119 54(СН-аром ), 121 08(СН-аром ), 126 07(СН-аром ), 127 67(СН-аром ), 135 53(СНаром), 125 93, 135 51, 137 95, 14182, 147 87,153 10(СН-аром ), 163 64(С=О) Аналіз для C21H19N3O4 %С (розрах /одерж) 66 83/66 67 %Н 5 07/5 18 %N 11 13/10 98 Аналіз для C21H19N3O4 %Н 5 07/5 22 %Н 6 28/6 34 %N 9 69/9 56 Вихід 88% Т ПЛ 208-210°С Приклад 15 1-(2-трифторметилфеніл)-3-((4'-нітрофенокси)феніл)-сечовина 4'-Нітрофеноксианілш (1 0г, 4 3 ммоль), трифосген (0 43г, 1 44 ммоль), триетиламш (0 бмл, 4 3 ммоль) нагрівають у толуолі (15мл) в трубі високого тиску при температурі 80°С протягом 20 годин Після ЦЬОГО додають 2-трифторметиланілш (0 53мл, 4 3 ммоль) і триетиламін (0 бмл, 4 З ммоль) у толуолі (Юмл) Суміш нагрівають при температурі 80°С протягом 4 годин, після чого концентрують, і одержаний продукт виділяють з допомогою хроматографії на силікагелі, елююючи сумішшю дихлорметану з метанолом Аналіз для C20H14F3N3O4 %С (розрах /одерж) 57 56/57 60 %Н 3 38/3 44 %N 10 07/9 89 Вихід 67% Т ПЛ 201-203°С Приклад 16 1-(3-трифторметилфеніл)-3-((4'-нітрофенокси)феніл)-сечовина Вказану у заголовку сполуку одержували з 3трифторметиланіліну з допомогою методики, описаної у Прикладі 15 Аналіз для C20H14F3N3O4 вихід 68% т пл 249-250°С Приклад 13 1-(3,5-диметилфеніл)-3-((4'-нітрофенокси)феніл)-сечовина Вказану у заголовку сполуку одержували з 3,5-диметилфенілізоціанату з допомогою методики, описаної у Прикладі 1 %С (розрах /одерж) 66 83/66 78 %С (розрах /одерж) 69 27/69 13 %С (розрах /одерж) 57 56/57 66 %Н 3 38/3 45 %N 10 07/9 96 Вихід 72% Т пл 208-211 °С Приклад 17 1-(4-трифторметилфеніл)-3-((4'-нітрофенокси)феніл)-сечовина Вказану у заголовку сполуку одержували з 4трифторметиланіліну з допомогою методики, описаної у Прикладі 15 Аналіз для C20H14F3N3O4 %N 11 13/11 06 Вихід 58% Т ПЛ 145-147°С Приклад 14 1-(2,6-ди-(метилетил)-феніл)-3-((4'нітрофенокси)-феніл)-сечовина Вказану у заголовку сполуку одержували з 2,6ди-(метилетил)фенілізоціанату з допомогою методики, описаної у Прикладі 1 %С (розрах /одерж) 57 56/57 48 %Н 3 38/3 41 %N 10 07/10 00 Вихід 45% Т ПЛ 185-189°С Приклад 18 1-(2-Піридил)-3-(4'-нітрофенокси)-феніл)сечовина Вказану у заголовку сполуку одержували з 2піридиламшу з допомогою методики, описаної у Прикладі 15 61125 Аналіз для C18H14N4O4 %С (розрах /одерж) 61 71/61 67 %Н 4 03/4 06 %N 15 99/15 79 Вихід 76% Т ПЛ 143-146°С Приклад 19 1-(3-Піридил)-3-(4'-нітрофенокси)-феніл)сечовина Вказану у заголовку сполуку одержували з 3піридиламшу з допомогою методики, описаної у Прикладі 15 Аналіз для C18H14N4O4 %С (розрах /одерж) 61 71/61 58 %Н 4 03/4 21 %N 15 99/15 87 Вихід 69% Т ПЛ 177-179°С Приклад 20 1-(4-Піридил)-3-(4'-нітрофенокси)-феніл)сечовина Вказану у заголовку сполуку одержували з 4піридиламшу з допомогою методики, описаної у Прикладі 15 Аналіз для C18H14N4O4 %С (розрах /одерж ) 61 71/61 66 %Н 4 03/4 11 %N 15 99/15 87 Вихід 72% Т ПЛ 126-127°С Приклад 21 1-(1 -Нафтил)-3-(4'-нітрофенокси)-феніл)сечовина Вказану у заголовку сполуку одержували з 1нафтилізоціанату з допомогою методики, описаної у Прикладі 1 Аналіз для C23H17N3O4 %С (розрах /одерж) 69 17/69 23 %Н 4 29/4 41 %N 10 52/10 46 Вихід 82% Т ПЛ 117-119°С Приклад 22 1 -(2-Нафтил)-3-(4'-нітрофенокси)-феніл)сечовина Вказану у заголовку сполуку одержували з 2нафтиламшу з допомогою методики, описаної у Прикладі 15 Аналіз для C23H17N3O4 %С (розрах /одерж) 69 17/69 09 %Н 4 29/4 36 %N 10 52/10 38 Вихід 69% Т ПЛ 103-106°С Приклад 23 1-(1 -Адамантил)-3-(4'-нітрофенокси)-феніл)сечовина Вказану у заголовку сполуку одержували з 1адамантиламшу з допомогою методики, описаної у Прикладі 15 Аналіз для C23H25N3O4 %С (розрах /одерж) 67 80/67 65 %Н 6 18/6 23 %N 1031/1016 10 Вихід 61% Т ПЛ 143-146°С Приклад 24 1-(4-Нітрофеніл)-3-((4'-нітрофенілтю)-феніл)сечовина Розчин 4-нітрофенілізоціанату в діетиловому ефірі (20мл) додають по краплях до розчину 4'нітрофенілтюанілшу (2 46г, 0 01 моль) в суміші діетилового ефіру (20мл) і тетрапдрофурану (20мл) при кімнатній температурі, і суміш перемішують протягом 16 годин Одержаний продукт відсмоктують, промивають діетиловим ефіром (20мл) Неочищений продукт очищають хроматографією на силікагелі, елююючи сумішшю дихлорметану і метанолу Аналіз для C19H14N4O5S %С (розрах /одерж) 55 61/55 52 %Н %N S% 3 44/3 49 13 65/13 59 7 81/7 67 Вихід 56% Т ПЛ 164-167°С Приклад 25 1-(2-Фторфеніл)-3-((4'-нітрофенілтю)-феніл)сечовина Вказану у заголовку сполуку одержували з 2фторфенілізоціанату з допомогою методики, описаної у Прикладі 24 Аналіз для C19H14FN3O3S %С (розрах /одерж) 59 52/59 41 %Н %N S% 3 68/3 77 10 96/11 04 8 36/8 41 Вихід 61% Т ПЛ 274-277°С Приклад 26 1-(4-Фторфеніл)-3-((4'-нітрофенілтю)-феніл)сечовина Вказану у заголовку сполуку одержували з 4фторфенілізоціанату з допомогою методики, описаної у Прикладі 24 Аналіз для C19H14FN3O3S %С (розрах /одерж) 59 52/59 46 %Н %N S% 3 68/3 71 10 96/10 87 8 36/8 18 Вихід 59% Т ПЛ 287-290°С Приклад 27 1-(2,4-Дифторфеніл)-3-((4'-нітрофенілтю)феніл)-сечовина Вказану у заголовку сполуку одержували з 2,4-дифторфенілізоціанату з допомогою методики, описаної у Прикладі 24 Аналіз для C19H13F2N3O3S %С (розрах / одерж) 56 86/56 78 %Н %N 3 26/3 39 10 47/10 41 S% 7 99/7 86 Вихід 57% Т ПЛ 268-271 °С Приклад 28 1-(2,5-Дифторфеніл)-3-((4'-нітрофенілтю)феніл)-сечовина 61125 12 11 Вказану у заголовку сполуку одержували з описаної у Прикладі 24 2,5-дифторфенілізоціанату з допомогою методики, Аналіз для C19H13CI2N3O3S описаної у Прикладі 24 %С (розрах / Аналіз для C19H13F2N3O3S ЛіН %N %С (розрах / одерж) 56 86/56 76 одерж ) 52 55/52 57 %Н %N 3 26/3 37 10 47/10 35 7 99/8 05 Аналіз для C19H13F2N3O3S %Н %N S% 3 26/3 34 10 47/10 43 7 99/7 81 Вихід 68% Т пл 263-265°С Приклад ЗО 1-(2-Хлорфеніл)-3-((4'-нітрофенілтю)-феніл)сечовина Вказану у заголовку сполуку одержували з 2хлорфенілізоціанату з допомогою методики, описаної у Прикладі 24 Аналіз для C19H14CIN3O3S %С (розрах / одерж) 57 07/57 01 ЛіН 3 53/3 6 2 %СІ %N 10 51/11 46 8 Лі 8 87/8 65 8 02Я 95 Вихід 65% Т ПЛ 231-233°С Приклад 31 1-(4-Хлорфеніл)-3-((4'-нітрофенілтю)-феніл)сечовина Вказану у заголовку сполуку одержували з 4хлорфенілізоціанату з допомогою методики, описаної у Прикладі 24 Аналіз для C19H14CIN3O3S %С (розрах / одерж) 57 07/56 97 ЛіН %N %СІ S Лі 3 53/3 5 7 10 51/10 4 5 8 87/8 81 8 02Я 86 Вихід 63% Т пл 206-209°С Приклад 32 1-(2,3-Дихлорфеніл)-3-((4'-нітрофенілтю)феніл)-сечовина Вказану у заголовку сполуку одержували з 2,3-дихлорфенілізоціанату з допомогою методики, описаної у Прикладі 24 Аналіз для C19H13CI2N3O3S %С (розрах / одерж) 52 55/52 46 9 68/9 5 4 %СІ S Лі 16 33/16 35 7 38Я 28 S% Вихід 64% Т ПЛ 259-261 °С Приклад 29 1-(2,6-Дифторфеніл)-3-((4'-нітрофенілтю)феніл)-сечовина Вказану у заголовку сполуку одержували з 2,6дифторфенілізоціанату з допомогою методики, описаної у Прикладі 24 %С (розрах / одерж ) 56 86/56 69 3 02/3 21 ЛіН %N %СІ S Лі 3 02/3 0 7 9 68/9 6 2 16 33/16 27 7 38Я 50 Вихід 75% Т ПЛ 157-159°С Приклад 33 1-(2,4-Дихлорфеніл)-3-((4'-нітрофенілтю)феніл)-сечовина Вказану у заголовку сполуку одержували з 2,4дихлорфенілізоціанату з допомогою методики, Вихід 57% Т ПЛ 174-178°С Приклад 34 1-(2,6-Дихлорфеніл)-3-((4'-нітрофенілтю)феніл)-сечовина Вказану у заголовку сполуку одержували з 2,6-дихлорфенілізоціанату з допомогою методики, описаної у Прикладі 24 Аналіз для C19H13CI2N3O3S %С (розрах / одерж) 52 55/52 51 ЛіН %N %СІ S Лі 3 02/3 0 7 9 68/9 7 3 16 33/16 25 7 38Я 19 Вихід 83% Т ПЛ 164-167°С Приклад 35 1-(3,4-Дихлорфеніл)-3-((4'-нітрофенілтю)феніл)-сечовина Вказану у заголовку сполуку одержували з 3,4-дихлорфенілізоціанату з допомогою методики, описаної у Прикладі 24 Аналіз для C19H13CI2N3O3S %С (розрах / одерж) 52 55/52 47 ЛіН %N %СІ S Лі 3 02/3 14 9 68/9 5 7 16 33/16 09 7 38Я 24 Вихід 57% Т ПЛ 238-240°С Приклад 36 1-(3,5-Дихлорфеніл)-3-((4'-нітрофенілтю)феніл)-сечовина Вказану у заголовку сполуку одержували з 3,5дихлорфенілізоціанату з допомогою методики, описаної у Прикладі 24 Аналіз для C19H13CI2N3O3S %С (розрах / одерж) 52 55/52 47 ЛіН %N %СІ S Лі 3 02/3 11 9 68/9 5 9 16 33/16 21 7 38Я 41 Вихід 67% Т ПЛ 185-188°С Приклад 37 1-(2-Метилфеніл)-3-((4'-нітрофенілтю)-феніл)сечовина Вказану у заголовку сполуку одержували з 2метилфенілізоціанату з допомогою методики, описаної у Прикладі 24 Аналіз для C20H17N3O3S %С (розрах / одерж) 63 31/63 22 %Н %N S% 4 52/4 66 11 07/10 79 8 45/8 34 Вихід 78% Т ПЛ 229-234°С Приклад 38 1-(4-Метилфеніл)-3-((4'-нітрофенілтю)-феніл)сечовина Вказану у заголовку сполуку одержували з 4метилфенілізоціанату з допомогою методики, описаної у Прикладі 24 Аналіз для C20H17N3O3S 61125 13 %С (розрах / одерж) 63 31/63 25 %н 4 % N S % 52/4 63 1107/11 12 845/8 35 Вихід 73% Т ПЛ 163-166°С Приклад 39 1-(2,4-диметилфеніл)-3-((4'-нітрофенілтю)феніл)-сечовина Вказану у заголовку сполуку одержували з 2,4диметилфенілізоціанату з допомогою методики, описаної у Прикладі 24 Аналіз для C21H19N3O3S %С (розрах / одерж) 64 11/64 08 %Н %N S% 4 87/4 83 10 68/10 59 8 15/7 95 Вихід 65% Т ПЛ 209-213°С Приклад 40 1-(2,6-диметилфеніл)-3-((4'-нітрофенілтю)феніл)-сечовина Вказану у заголовку сполуку одержувализ 2,6диметилфенілізоціанату з допомогою методики, описаної у Прикладі 24 14 трифторметиланіліну (0 53мл, 4 3 ммоль) і триетиламіну (0 бмл, 4 3 ммоль) в толуолі (Юмл) Суміш нагрівають при температурі 80°С протягом 4 годин, після цього концентрують, і продукт ВІДДІЛЯЮТЬ хроматографією на силікагелі, елююючи сумішшю дихлорметан/метанол Аналіз для C20H14F3N3O3S %С (розрах / одерж) 55 43/55 38 %Н %N 3 26/3 39 9 70/9 71 S% 7 40/7 35 Вихід 52% Т ПЛ 257-261 °С Приклад 44 1-(3-трифторметилфеніл)-3-((4'-нітрофенілтю)феніл)-сечовина Вказану у заголовку сполуку одержували з 3трифторфенілізоціанату з допомогою методики, описаної у Прикладі 43 Аналіз для C20H14F3N3O3S %С (розрах / одерж) 55 43/55 21 %Н %N 3 26/3 38 9 70/9 53 S% 7 40/7 31 Аналіз для C21H19N3O3S %С (розрах / одерж) 64 11/63 97 %Н %N S% 4 87/4 83 10 68/10 47 8 15/8 01 Вихід 72% Т ПЛ 264-267°С Приклад 41 1-(3,5-диметилфеніл)-3-((4'-нітрофенілтю)феніл)-сечовина Вказану у заголовку сполуку одержували з 3,5диметилфенілізоціанату з допомогою методики, описаної у Прикладі 24 Вихід 65% Т ПЛ 241-244°С Приклад 45 1-(4-трифторметилфеніл)-3-((4'нітрофенілтю)-феніл)-сечовина Вказану у заголовку сполуку одержували з 4трифторфенілізоціанату з допомогою методики, описаної у Прикладі 43 Аналіз для C20H14F3N3O3S %С (розрах / одерж) 55 43/55 37 %Н %N 3 26/3 33 9 70/9 81 S% 7 40/7 28 Аналіз для C21H19N3O3S %С (розрах / одерж) 64 11/64 04 %Н %N S% 4 87/4 99 10 68/10 63 8 15/8 01 Вихід 68% Т ПЛ 194-196°С Приклад 42 1-(2,6-ди-(метилетил)-феніл-((4'нітрофенілтю)-феніл)-сечовина Вказану у заголовку сполуку одержували з 2,6(метилетил)-фенілізоціанату з допомогою методики, описаної у Прикладі 24 Вихід 51% Т ПЛ 254-257°С Приклад 46 1-(2-Піридил)-3-((4'-нітрофенілтю)-феніл)сечовина Вказану у заголовку сполуку одержували з 2піридиламшу з допомогою методики, описаної у Прикладі 43 Аналіз для C18H14N4O3S %С (розрах / одерж ) 59 01/58 86 %Н %N S% 3 85/3 91 15 29/15 23 8 75/8 80 Аналіз для C25H27N3O3S %С (розрах / одерж) 66 79/66 72 %Н %N S% 6 06/6 17 9 35/9 27 7 12/6 96 Вихід 72% Т ПЛ 175-177°С Приклад 43 1-(2-трифторметилфеніл)-3-((4'-нітрофенілтю)феніл)-сечовина Розчин 4'-нітрофенілтюанілшу (1 06г, 4 З ммоль), трифосгену (0 43г, 1 44 ммоль), триетиламіну (0 6г, 4 3 ммоль) в толуолі (15мл) нагрівають в трубі високого тиску при температурі 80°С протягом 20 годин Після цього додають розчин 2 Вихід 48% Т ПЛ 278-281 °С Приклад 47 1-(3-Піридил)-3-((4'-нітрофенілтю)-феніл)сечовина Вказану у заголовку сполуку одержували з 3піридиламшу з допомогою методики, описаної у Прикладі 43 Аналіз для C18H14N4O3S %С (розрах / одерж) 59 01/58 99 %Н %N S% 3 85/3 99 15 29/15 25 8 75/8 49 Вихід 63% Т ПЛ 261-264°С 16 15 61125 Приклад 48 1-(4-Піридил)-3-((4'-нітрофенілтю)-феніл)%С (розрах /одерж) %Н %N сечовина 64 22/64 09 4 25/4 29 11 83/12 01 Вказану у заголовку сполуку одержували з 4піридиламшу з допомогою методики, описаної у Вихід 88% Т ПЛ 248-251 °С Прикладі 43 Приклад 53 Аналіз для C18H14N4O3S 1-(2,3-Дихлорфеніл)-3-((4'-амшофенокси)феніл)-сечовина %С (розрах / Вказану у заголовку сполуку одержували зі %Н %N S% одерж) сполуки 6 з допомогою методики, описаної у При59 01/58 92 3 85/3 76 15 29/15 32 8 75/8 67 кладі 52 Вихід 69% Т ПЛ 190-192°С Приклад 49 1 -(1 -Нафтил)-3-((4'-нітрофенілтю)-феніл)сечовина Вказану у заголовку сполуку одержували з 1нафтилізоціанату з допомогою методики, описаної у Прикладі 24 Аналіз для C23H17N3O3F %С (розрах / одерж) 66 49/66 53 %Н %N S% 4 13/4 21 10 12/10 17 7 70/7 54 Вихід 56% Т ПЛ 164-168°С Приклад 50 1-(2-Нафтил)-3-((4'-нітрофенілтю)-феніл)сечовина Вказану у заголовку сполуку одержували з 2нафтиламшу з допомогою методики, описаної у Прикладі 43 Аналіз для C23H17N3O3S %С (розрах / одерж) 66 49/66 47 %Н %N S% 4 13/4 25 10 12/10 06 7 70/7 57 Вихід 69% Т ПЛ 142-147°С Приклад 51 1 -(1 -Адамантил)-3-((4'-нітрофенілтю)-феніл)сечовина Вказану у заголовку сполуку одержували з 1-адамантиламшу з допомогою методики, описаної у Прикладі 43 Аналіз для C23H25N3O3S Аналіз для C19H15CI2N3O3 %С (розрах / %Н %N %СІ одерж ) 58 78/58 45 3 89/3 94 10 82/10 78 18 26/18 11 Вихід 91% Т ПЛ 201-204°С Приклад 54 1-(2,6-диметилфеніл)-3-((4'-амшофенокси)феніл)-сечовина Вказану у заголовку сполуку одержували зі сполуки 12 з допомогою методики, описаної у Прикладі 52 Аналіз для C21H21N3O2 %С (розрах /одерж) 72 60/72 45 %Н 6 09/6 13 %N 12 10/12 02 Вихід 85% Т ПЛ 225-227°С Приклад 55 1-(2,6-ди(метилетил)-феніл)-3-((4'амшофенокси)-феніл)-сечовина Вказану у заголовку сполуку одержували зі сполуки 14 з допомогою методики, описаної у Прикладі 52 1 Н-ЯМР (CDCI3) 1 15(д, 6Н, 2хСН3), 3 15(гепт , 2Н, 2хСН), 4 86(с, 2Н, NH), 6 57(д, 2Н, Н-аром ), 6 72(д, 2Н, Н-аром), 6 81 (д, 2Н, Н-аром), 7 101 28(м, ЗН, Н-аром ), 7 36(д, 2Н, Н-аром ), 7 56(с, 1Н, HN), 8 58(шс, 1Н, NH) 13 С-ЯМР (CDCI3) 23 43(2хСН3), 27 93(2хСН), 114 63(СН-аром ), 117 55(СН-аром ), 119 09(СНаром ), 199 43(СН-аром ), 122 79(СН-аром ), 127 11(СН-аром), 12711 (СН-аром), 13240, 134 86, 144 77, 146 61, 146 89, 152 88(С-аром), 154 36(С=О) Аналіз для C25H29N3O2 %С (розрах / одерж) 65 22/65 17 %Н %N S% 5 95/6 03 9 93/10 02 7 56/7 38 Вихід 52% Т ПЛ 264-267°С Приклад 52 1-(2,4-Дифторфеніл)-3-((4'-амшофенокси)феніл)-сечовина Один грам сполуки 2 розчиняють у метанолі (20мл) і додають 0 1г 10% паладію на вугіллі Суміш перемішують в атмосфері водню (при атмосферному тиску) протягом 20 годин Після ЦЬОГО додають ЮОмл метанолу, і каталізатор відфільтровують Після ЦЬОГО концентруванням метанольного розчину одержують бажаний продукт Аналіз для C19H15F2N3O2 %С (розрах /одерж) 74 41/74 54 %Н 7 24/7 33 %N 10 41/10 34 Вихід 90% Т ПЛ 219-221 °С Приклад 56 1-(2,4-Дифторфеніл)-3-((4'-амшофенілтю)феніл)-сечовина Вказану у заголовку сполуку одержували зі сполуки 27 з допомогою методики, описаної у Прикладі 52 Аналіз для C19H15F2N3OS %С (розрах / одерж) 61 44/61 56 %Н %N %S 4 07/4 18 11 31/11 15 8 63/8 51 Вихід 79% Т пл вище 300°С 18 17 61125 Приклад 57 1 -(2,3-Дихлорфеніл)-3-((4'-амшофенілтю)%С (розрах / %Н %N %S феніл)-сечовина одерж) Вказану у заголовку сполуку одержували зі 71 56/71 55 6 97/6 89 1001/1011 7 64/7 58 сполуки 32 з допомогою методики, описаної у Прикладі 52 Вихід 83% Т ПЛ 267-271 °С Аналіз для C19H15CI2N3OS Випробування Біологічну активність сполук оцінювали на ос%С (розрах / нові інгібування ними in vitro активності ацил-КоА ЛіН %N %СІ AtS одерж) холестерол-ацилтрансферази (АСАТ) Цей фер56 44/56 35 3 74/3 8 0 10 3 9 / 1 0 4 1 17 54/17 57 7 93Я 59 мент одержували з мікросомної фракції клітин печінки пацюка та слизової оболонки кишечника кроВихід 88% Т ПЛ 259-261 °С ля, яким давали корм, що містив холестерин В Приклад 58 якості субстратів для ферментативної реакції ви1-(2,6-диметилфеніл)-3-((4'-амшофенілтю)користовували екзогенний олеоіл-КоА та ендогенфеніл)-сечовина ний холестерин Здійснювали контроль за процеВказану у заголовку сполуку одержували зі 14 сом перетворення С-олеоіл-СоА в 14Ссполуки 40 з допомогою методики, описаної у Прихол естери л олеат Хол естери л олеат виділяли із кладі 52 суміші екстрагованих ЛІПІДІВ З ДОПОМОГОЮ тонкоАналіз для C21H21N3OS шарової хроматографії, і його КІЛЬКІСТЬ визначали з допомогою радіометричного аналізу Специфічну %С (розрах / активність АСАТ виражали через КІЛЬКІСТЬ холес%Н %N %S одерж ) терилолеату, що утворювався за 1 хвилину з 1мг 69 39/69 32 5 82/5 93 11 56/11 49 8 28/8 54 мікросомного протеїну Вихід 94% Т ПЛ 198-202°С Приклад 59 1-(2,6-ди-(метилетил)-феніл-3-((4'амшофенілтю)-феніл)-сечовина Вказану у заголовку сполуку одержували зі сполуки 42 з допомогою методики, описаної у Прикладі 52 Аналіз для C25H29N3OS У Таблиці вказаний відсоток інгібування АСАТ у печінці пацюка та слизовій оболонці кишечника кроля при різних концентраціях досліджуваних речовин Ефективність визначали у порівнянні з активністю ферменту, встановлюваною у присутності 1% диметилсульфоксиду, який використовували в якості розчинника для приготування розчинів досліджуваних речовин Таблиця Інгібуюча дія сполук на активність АСАТ у печінці пацюка та слизовій оболонці кишечника кроля No Ефективність (%) Концентрація печінка 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 слизова оболонка (мМ) 15 37 49 0 0 58 20 0 0 0 0 41 0 50 46 38 25 26 0 11 14 0 43 32 55 58 42 0 51 25 0 0 0 0 65 0 67 42 45 18 34 0 17 22 12 58 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 No Ефективність печінка 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 12 15 0 0 27 21 19 23 18 88 25 34 23 48 45 53 24 16 45 53 55 38 68 (%) слизова оболонка 16 21 20 0 31 32 31 34 27 71 38 45 25 46 36 35 36 31 56 64 46 62 64 Концентрація (мМ) 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 19 20 61125 Продовження таблиці No Ефеїсгивність печінка 24 25 26 27 28 29 ЗО 31 32 0 0 25 16 0 11 20 12 0 (%) слизова оболонка 34 23 27 23 16 25 26 21 0 Концентрація (мМ) Ефективність печінка 2 2 2 2 2 2 2 2 2 56 57 58 59 Сполуки згідно з винаходом і спосіб їх одержання можуть застосовуватися у виробництві фармацевтичних препаратів, які виявляють інгібуючу Комп'ютерна верстка А Крулевський No 22 15 21 56 (%) слизова оболонка 25 26 29 67 Концентрація (мМ) 2 2 2 2 дію на фермент ацил-СоА та на абсорбцію холестерину при пперхолестеринемм Підписне Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ДП "Український інститут промислової власності", вул Сім'ї Хохлових, 15, м Київ, 04119
ДивитисяДодаткова інформація
Назва патенту англійською1,3-disubstituted ureas as inhibitors of acyl-coenzyme a: cholesterol acyltransferase and a method for preparing the same
Назва патенту російською1,3-дизамещенные мочевины в качестве ингибиторов фермента ацил-коа: холестерол-ацилтрансферазы и способ их получения
МПК / Мітки
МПК: A61P 43/00, A61K 31/4406, C07D 213/75, C07C 275/36, A61K 31/4409, C07D 213/74, A61K 31/17, A61K 31/4402, A61P 3/06, C07C 323/44
Мітки: спосіб, сечовини, одержання, 1,3-дизаміщені
Код посилання
<a href="https://ua.patents.su/10-61125-13-dizamishheni-sechovini-ta-sposib-kh-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">1,3-дизаміщені сечовини та спосіб їх одержання</a>
Попередній патент: Пентасахариди та фармацевтична композиція що їх містить
Наступний патент: Спосіб визначення вертикальної рефракції
Випадковий патент: Спосіб лікування менінгококцемії у дітей