Фармацевтична композиція, яка включає телмісартан, спосіб її одержання (варіанти), двошарова фармацевтична таблетка та спосіб її одержання
Номер патенту: 81781
Опубліковано: 11.02.2008
Автори: Тойошіма Кензо, Охкі Тошімітсу, Накатані Манабу, Такеші Савада
Формула / Реферат
1. Фармацевтична композиція, яка включає 3-50 мас. % телмісартану, диспергованого в розчинюючій матриці, яка включає:
(а) основний агент у молярному співвідношенні основний агент:телмісартан = 1:1 до 10:1,
(б) поверхнево-активну речовину або емульгатор у кількості від приблизно 1 до приблизно 20 мас. % від кінцевої композиції,
(в) 25-70 мас. % водорозчинного розріджувача і
(г) необов'язково 0-20 мас. % додаткових наповнювачів і/або допоміжних речовин, сума всіх компонентів становить 100 %.
2. Фармацевтична композиція за п. 1, де основний агент означає гідроксид металу, такий, як NaOH або КОН; або вибраний з NaHCO3, КНСОз, Na2CO3, К2СОз, Nа2НРО4, К2НРО4, з основних амінокислот, таких, як аргінін; і з меглюміну (N-метил-D-глюкаміну).
3. Фармацевтична композиція за п. 1, де поверхнево-активні речовини і емульгатори вибирають з полоксамерів або плюроніків, поліетиленгліколів, моноолеату поліетиленгліколю, полісорбатів, лаурилсульфату натрію, поліетоксилованої і гідрогенізованої рицинової олії.
4. Фармацевтична композиція за п. 1, де поверхнево-активні речовини і емульгатори вибирають з полоксамерів, які мають середню молекулярну масу від приблизно 2000 до приблизно 12000.
5. Фармацевтична композиція за п. 4, де полоксамер вибирають з полоксамеру 182LF, полоксамеру 331 і полоксамеру 188.
6. Фармацевтична композиція за п. 1, де водорозчинні розріджувачі вибирають з вуглеводів, таких, як моносахариди, як глюкоза; олігосахариди, як сахароза; і вуглеводні спирти, як еритрит, сорбіт, маніт, дульцит, рибіт і ксиліт.
7. Фармацевтична композиція за п. 1, де інші наповнювачі і/або допоміжні речовини вибирають із зв'язувальних речовин, носіїв, змащувальних речовин, агентів для регулювання потоку, агентів для уповільнення кристалізації, речовин, які сприяють розчиненню, і фарбувальних агентів.
8. Тверда пероральна фармацевтична лікарська форма, готова для застосування/проковтування, отримана з фармацевтичної композиції за будь-яким з пп. 1-7.
9. Лікарська форма за п. 8 у вигляді капсули або таблетки.
10. Лікарська форма за п. 8 або 9, яка включає стандартну дозу 10-160 мг телмісартану.
11. Двошарова фармацевтична таблетка, яка включає перший шар таблетки, що містить телмісартан, одержаний з фармацевтичної композиції за будь-яким з пп. 1-7, і другий шар таблетки, який містить діуретик у дезінтегруючій матриці таблетки.
12. Спосіб одержання фармацевтичної композиції за п. 1, що використовує методику грануляції в киплячому шарі (А), охарактеризований наступними етапами:
(і) одержання грануляційної рідини у вигляді водного розчину шляхом розчинення 3-50 мас. % телмісартану разом з наступними компонентами в воді або в суміші розчину етанолу і води:
(а) основний агент у молярному співвідношенні основний агент:телмісартан = 1:1 до 10:1,
(б) неіонний поверхнево-активний агент або емульгатор у кількості від приблизно 1 до приблизно 20 мас. %,
(іі) завантаження 25-70 мас. % водорозчинного розріджувача в гранулятор з киплячим шаром, необов'язково разом з 10-20 мас. % сухої сполучної речовини, включаючи етап попереднього змішування,
(ііі) проведення грануляції в киплячому шарі, використовуючи грануляційну рідину для розпилення на компоненти, поміщені в гранулятор,
(iv) після закінчення грануляції - висушування і необов'язкове просіювання отриманого гранулята,
(v) необов'язкове змішування гранулята з додатковими наповнювачами і/або допоміжними речовинами, щоб одержати кінцеву композицію, і
(vi) необов'язкове перемішування одержаного в такий спосіб гранулята, щоб одержати порошкоподібну композицію з визначеним розподілом частинок за розміром; де всі наведені процентні кількості стосуються кінцевої композиції, яка повинна бути отримана.
13. Спосіб одержання фармацевтичної композиції за п. 1, використовуючи методику висушування розпиленням (Б), що характеризується наступними етапами:
(і) одержання водного розчину для розпилення шляхом розчинення 3-50 мас. % телмісартану разом з наступними компонентами в воді або в суміші розчину етанолу і води:
(а) основний агент у молярному співвідношенні основний агент:телмісартан=1:1 до 10:1,
(б) неіонний поверхнево-активний агент або емульгатор у кількості від приблизно 1 до приблизно 20 мас. %,
(іі) висушування розпиленням згаданого розчину для розпилення, щоб одержати висушений розпиленням гранулят;
(ііі) змішування згаданого гранулята, висушеного розпиленням, з 25-70 мас. % водорозчинного розріджувача, щоб одержати попередню суміш;
(iv) необов'язкове змішування згаданої попередньої суміші із змащувальною речовиною;
(v) необов'язкове додавання додаткових наповнювачів і/або допоміжних речовин на кожному з етапів (i)-(iv), де всі наведені процентні кількості стосуються кінцевої композиції, яка повинна бути одержана.
14. Спосіб одержання двошарової таблетки за п. 11, що використовує наступні етапи:
(і) приготування композиції першого шару таблетки, що включає телмісартан, із
застосуванням способу за п. 12 або 13;
(іі) приготування композиції другого шару таблетки;
(а) змішування і/або грануляцію діуретику зі складовими частинами дезінтегруючої матриці таблетки і необов'язково додатковими наповнювачами і/або допоміжними речовинами;
(б) примішування змащувальної речовини, щоб одержати кінцеву суміш другого шару таблетки;
(ііі) введення композиції першого або другого шару таблетки в таблетковий прес;
(iv) пресування згаданої композиції шару таблетки для утворення таблеткового шару;
(v) введення композиції іншого шару таблетки в таблетковий прес; і
(vi) пресування обох композицій таблеткових шарів для утворення двошарової таблетки.
Текст
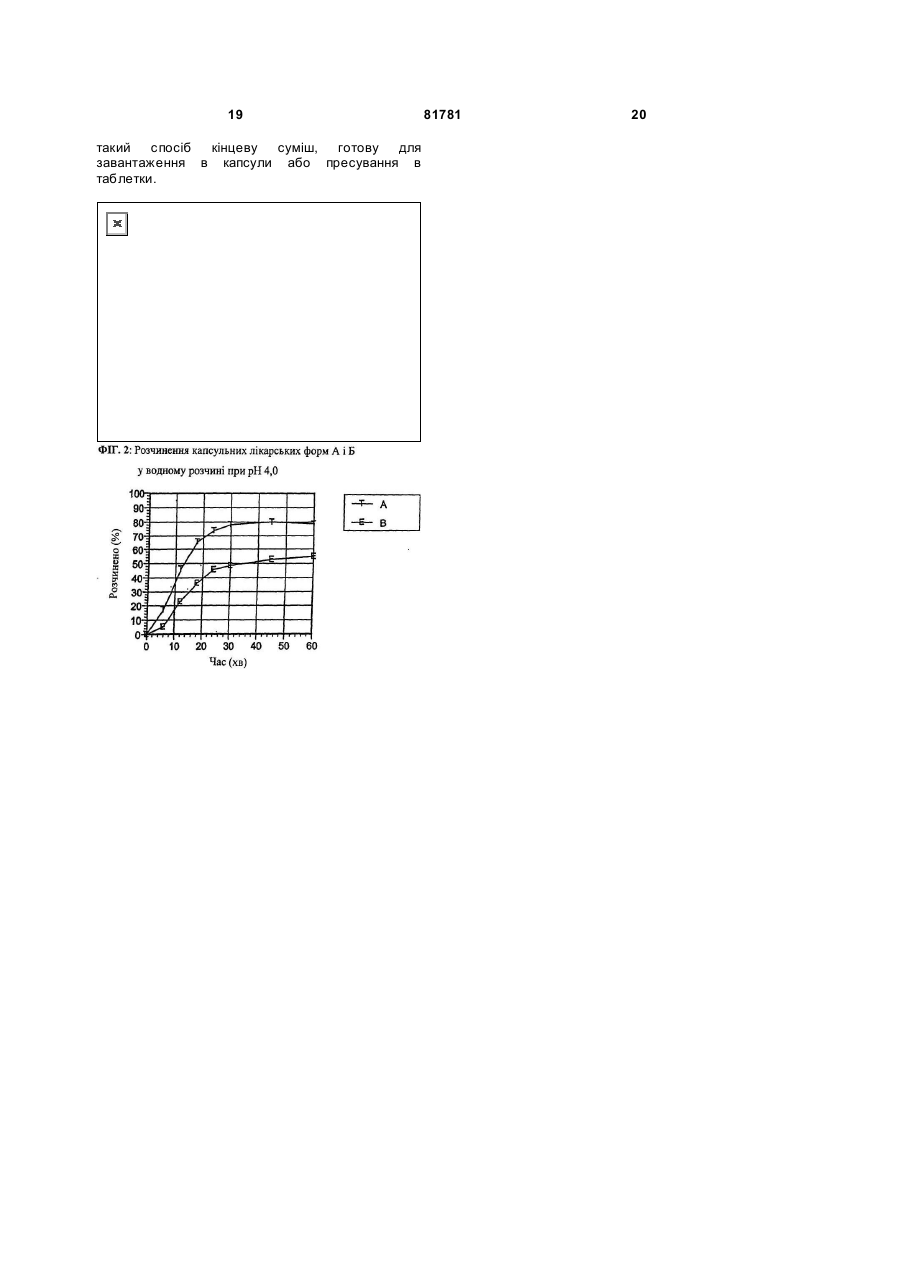
1. Фармацевтична композиція, яка включає 350 мас. % телмісартану, диспергованого в розчинюючій матриці, яка включає: (а) основний агент у молярному співвідношенні основний агент:телмісартан = 1:1 до 10:1, (б) поверхнево-активну речовину або емульгатор у кількості від приблизно 1 до приблизно 20 мас. % від кінцевої композиції, (в) 25-70 мас. % водорозчинного розріджувача і (г) необов'язково 0-20 мас. % додаткових наповнювачів і/або допоміжних речовин, сума всіх компонентів становить 100 %. 2. Фармацевтична композиція за п. 1, де основний агент означає гідроксид металу, такий, як NaOH або КОН; або вибраний з NaHCO3, КНСОз, Na2CO3, К2СОз, Nа2НРО4, К2НРО4, з основних амінокислот, таких, як аргінін; і з меглюміну (Nметил-D-глюкаміну). 3. Фармацевтична композиція за п. 1, де поверхнево-активні речовини і емульгатори вибирають з полоксамерів або плюроніків, поліетиленгліколів, моноолеату поліетиленгліколю, полісорбатів, лаурилсульфату натрію, поліетоксилованої і гідрогенізованої рицинової олії. 4. Фармацевтична композиція за п. 1, де поверхнево-активні речовини і емульгатори вибирають з полоксамерів, які мають середню молекулярну масу від приблизно 2000 до приблизно 12000. 2 (19) 1 3 81781 4 необов'язково разом з 10-20 мас. % сухої сполучної речовини, включаючи етап попереднього змішування, (ііі) проведення грануляції в киплячому шарі, використовуючи грануляційну рідину для розпилення на компоненти, поміщені в гранулятор, (iv) після закінчення грануляції - висушування і необов'язкове просіювання отриманого гранулята, (v) необов'язкове змішування гранулята з додатковими наповнювачами і/або допоміжними речовинами, щоб одержати кінцеву композицію, і (vi) необов'язкове перемішування одержаного в такий спосіб гранулята, щоб одержати порошкоподібну композицію з визначеним розподілом частинок за розміром; де всі наведені процентні кількості стосуються кінцевої композиції, яка повинна бути отримана. 13. Спосіб одержання фармацевтичної композиції за п. 1, використовуючи методику висушування розпиленням (Б), що характеризується наступними етапами: (і) одержання водного розчину для розпилення шляхом розчинення 3-50 мас. % телмісартану разом з наступними компонентами в воді або в суміші розчину етанолу і води: (а) основний агент у молярному співвідношенні основний агент:телмісартан=1:1 до 10:1, (б) неіонний поверхнево-активний агент або емульгатор у кількості від приблизно 1 до приблизно 20 мас. %, (іі) висушування розпиленням згаданого розчину для розпилення, щоб одержати висушений розпиленням гранулят; (ііі) змішування згаданого гранулята, висушеного розпиленням, з 25-70 мас. % водорозчинного розріджувача, щоб одержати попередню суміш; (iv) необов'язкове змішування згаданої попередньої суміші із змащувальною речовиною; (v) необов'язкове додавання додаткових наповнювачів і/або допоміжних речовин на кожному з етапів (i)-(iv), де всі наведені процентні кількості стосуються кінцевої композиції, яка повинна бути одержана. 14. Спосіб одержання двошарової таблетки за п. 11, що використовує наступні етапи: (і) приготування композиції першого шару таблетки, що включає телмісартан, із застосуванням способу за п. 12 або 13; (іі) приготування композиції другого шару таблетки; (а) змішування і/або грануляцію діуретику зі складовими частинами дезінтегруючої матриці таблетки і необов'язково додатковими наповнювачами і/або допоміжними речовинами; (б) примішування змащувальної речовини, щоб одержати кінцеву суміш другого шару таблетки; (ііі) введення композиції першого або другого шару таблетки в таблетковий прес; (iv) пресування згаданої композиції шару таблетки для утворення таблеткового шару; (v) введення композиції іншого шару таблетки в таблетковий прес; і (vi) пресування обох композицій таблеткових шарів для утворення двошарової таблетки. Даний винахід стосується нових твердих фармацевтичних композицій, які включають антагоніст рецептора ангіотензину II телмісартан, наприклад, у формі гранул або у формі порошку, а також твердих пероральних лікарських форм, які готові для застосування/проковтування, наприклад, капсульних і таблеткових лікарських форм, отриманих із згаданих фармацевтичних композицій. Даний винахід забезпечує також способи одержання згаданих композицій і лікарських форм. Телмісартан INN є антагоністом рецептора ангіотензину II, створеним для лікування гіпертензії та інших медичних показань, як розкрито [в патенті ЕР-А-502314]. Його хімічна назва 4'-[2-н-пропіл-4-метил-6-(1метилбензимідазол-2-іл)бензимідазол-1илметил]біфеніл-2-карбонова кислота, яка має наступну структуру: Телмісартан звичайно виробляється і постачається у формі вільної кислоти. Як розкрито [в WO 00/43370], кристалічний телмісартан існує в двох поліморфних формах, які мають різні точки плавлення. Під впливом тепла і вологості поліморф Б, який більш низько плавиться, незворотньо перетворюється в поліморф А, який більш високо плавиться. Обидві форми характеризуються дуже поганою розчинністю у водних системах у фізіологічному інтервалі рН шлунково-кишкового тракту, що знаходиться між рН1 до рН7. Телмісартан доступний у продажі під торговою назвою мікардіс®. Виходячи з форми вільної кислоти, введеної в продаж, телмісартан виробляється із застосуванням дорогого способу висушування розпиленням. Через погану розчинність форми вільної кислоти одержання альтернативної лікарської форми телмісартану утруднено. Існує явна необхідність у забезпеченні альтернативної твердої пероральної лікарської форми телмісартану, яка може бути отримана з використанням менш складних і дорогих методик і відповідати усім вимогам фармацевтичного застосування, тобто тривалої стійкості лікарської форми при різних кліматичних умовах і достатній 5 розчинності активної речовини для достатнього поглинання в шлунково-кишковому тракті в діапазоні слабокислих і нейтральних значень рН. Перший об'єкт за винаходом полягає в забезпеченні згаданих альтернативних твердих фармацевтичних композицій, які включають телмісартан, наприклад, у формі гранул або порошку, у формі, яка допускає, що активна сполука вивільняється із згаданих композицій і лікарських форм із достатньою розчинністю для поглинання в шлунково-кишковому тракті в діапазоні слабокислих і нейтральних значень рН. Переважно лікарські форми повинні мати властивості негайного вивільнення і розчинення, не виявляючи істотної залежності від рН у межах фізіологічного характерного інтервалу рН шлунково-кишкового тракту. Другий об'єкт за винаходом полягає в забезпеченні додаткових твердих пероральних лікарських форм, готових для застосування/проковтування, наприклад, капсульних і таблеткових лікарських форм, приготовлених із згаданих фармацевтичних композицій, названих у першому аспекті за винаходом. Третій об'єкт за винаходом стосується способів одержання згаданих композицій і лікарських форм, названих вище. Перший об'єкт за винаходом (фармацевтична композиція) Несподівано було виявлено, що розчинність телмісартану може бути збільшена з коефіцієнтом у декілька сотень разів за допомогою фармацевтичної композиції, яка включає 350мас.% телмісартану, диспергованого в розчинюючій матриці, що включає (а) основний агент у молярному співвідношенні молярний агент:телмісартан=1:1 до 10:1, (б) поверхнево-активний агент або емульгатор у кількості приблизно 1-20мас.% від кінцевої композиції, (в) 25-70мас.% водорозчинного розріджувача і (г) необов'язково 0-20мас.% додаткових наповнювачів і/або допоміжних речовин, сума всіх компонентів становить 100%. Термін «розчинююча матриця таблетки» стосується готової форми фармацевтичної матриці таблетки, яка має властивості негайного вивільнення (швидкого розчинення), яка легко розчиняється у фізіологічному водному середовищі. Специфічними прикладами відповідних основних агентів є гідроксиди лужних металів, такі, як NaOH і КОН; крім того, NaHCO3, KНСО3, Na2CO3, K2СО3, Na2HPO4, K2НРО4; основні амінокислоти, такі, як аргінін; і меглюмін (N-метилО-глюкамін). Поверхнево-активні речовини і емульгатори можуть бути іонними і неіонними, останні є переважними. Специфічними прикладами поверхнево-активних речовин і емульгаторів є такі агенти, як полоксамери або плюроніки, поліетиленгліколі, моностеарат поліетиленгліколю, полісорбати, лаурилсульфат натрію, 81781 6 поліетоксилована і гідрогенізована рицинова олія і т.д. Що стосується полоксамерів або плюроніків, придатних як неіонні поверхнево-активні агенти і емульгатори, посилаються на визначення, наведене [в Merck Index, 12 видання, 1996p.], включене в даному описі у вигляді посилання. Відповідні полоксамери можуть мати середню молекулярну масу приблизно 2000-12000, переважно 4000-10000, більш переважно 600010000, найбільш переважно 8000-9000. Прикладами специфічних полоксамерів є полоксамер 182LF, полоксамер 331 і полоксамер 188. Специфічними прикладами відповідних водорозчинних розріджувачів є вуглеводи, такі, як моносахариди, як глюкоза; олігосахариди, як сахароза; і вуглеводні спирти, як еритрит, сорбіт, маніт, дульцит, рибіт і ксиліт. Маніт, еритрит, сорбіт і сахароза є переважними розріджувачами. Іншими наповнювачами і/або допоміжними речовинами є, наприклад, вибрані із зв'язувальних речовин, носіїв, змащувальних речовин, агентів, які регулюють плинність, сповільнювачів кристалізації, речовин, які сприяють розчиненню, і фарбувальних агентів. Зв'язувальна речовина може бути вибрана з групи сухих зв'язувальних речовин або зв'язувальних речовин, які застосовують при вологій грануляції, залежно від способу одержання, вибраного для фармацевтичної композиції. Відповідними сухими зв'язувальними речовинами є, наприклад, порошок целюлози, кристалічна целюлоза, мікрокристалічна целюлоза або неповністю безводна кремнієва кислота. Специфічними прикладами зв'язувальних речовин при вологій грануляції є кукурудзяний крохмаль, полівінілпіролідон (повідон), співполімер вінілпіролідону і вінілацетату (співповідон) і похідні целюлози, як гідроксиметилцелюлоза, гідроксіетилцелюлоза, гідроксипропілцелюлоза і гідроксипропілметилцелюлоза. Відповідними дезінтегрантами є, наприклад, модифікований гліколятом натрію крохмаль, кросповідон, кроскармеллоза, карбоксиметилцелюлоза в натрієвій формі і висушений кукурудзяний крохмаль. Іншими наповнювачами і допоміжними речовинами, якщо вони використовуються, є речовини, переважно вибрані з розріджувачів і носіїв, таких, як порошкоподібна целюлоза, кристалічна целюлоза або мікрокристалічна целюлоза, похідні целюлози, як гідроксиметилцелюлоза, гідроксіетилцелюлоза, гідроксипропілцелюлоза і гідроксипропілметилцелюлоза, двоосновний фосфат кальцію, кукурудзяний крохмаль, попередньо желатинізований крохмаль, полівінілпіролідон (повідон) і т.д.; змащувальні речовини, такі, як стеаринова кислота, стеарат магнію, стеарилфумарат натрію, трибегенат гліцерину і т.д.; агенти, які контролюють плинність, такі, як колоїдний кремній, неповністю безводна кремнієва кислота, кристалічна целюлоза, тальк і т.д.; сповільнювачі кристалізації, такі, як повідон і 7 т.д.; фарбувальні агенти, які включають барвники і пігменти, такі, як червоний або жовтий оксид заліза, діоксид титану, тальк і т.д.; і суміші двох або декількох цих наповнювачів і/або допоміжних речовин. Фармацевтичні композиції за даним винаходом забезпечують поліпшену розчинність погано розчинного у воді телмісартану до концентрації більше ніж 4,4мг/100мл, тим самим сприяючи розчиненню препарату при фізіологічному рівні рН, і також забезпечують негайне вивільнення із матриці, яка швидко розпадається. Присутність компонента (б), поверхневоактивної речовини або емульгатора, є істотним для досягнення значно поліпшеної розчинності активного інгредієнта, а також для застосування спрощеного способу одержання, такого, як грануляція в киплячому шарі замість висушування розпиленням, для приготування твердих фармацевтичних композицій за винаходом. У переважному варіанті втілення винаходу фармацевтична композиція за винаходом включає 10-35мас.% телмісартану, диспергованого в розчинюючій матриці, що включає (а) основний агент у молярному співвідношенні основний агент:телмісартан= 1,5:1 до 5:1, (б) неіонну поверхнево-активну речовину або емульгатор у кількості приблизно 1-Юмас.% від кінцевої композиції, (в) 35-60мас.% водорозчинного розріджувача і (г) необов'язково 0-20мас.% додаткових наповнювачів і/або допоміжних речовин, сума всіх компонентів становить 100%. Усі наведені в описі компоненти (а) і (б), згадані вище, можуть застосовуватися в переважному варіанті втілення, беручи до уваги, що переважними основними агентами є NaOH, KOH, аргінін і меглюмін, переважні неіонні поверхнево-активні речовини або емульгатори вибирають з полоксамерів, поліетиленгліколів і гідрогенізованої рицинової олії, переважні водорозчинні розріджувачі вибирають із сахарози, еритриту, сорбіту, маніту і ксиліту, і переважні необов'язкові додаткові наповнювачі і/або допоміжні речовини вибирають із кристалічної целюлози, неповністю безводної кремнієвої кислоти, гідроксиметилцелюлози, гідроксіетилцелюлози, гідроксипропілцелюлози, гідроксипропілметилцелюлози, стеарату магнію, кукурудзяного крохмалю, полівінілпіролідону, співполімеру вінілпіролідону і вінілацетату, стеаринової кислоти, стеарату магнію, стеарилфумарату натрію, колоїдного кремнію, тальку, повідону й фарбувальних агентів. У більш переважному варіанті втілення винаходу фармацевтична композиція за винаходом включає 15-25мас.% телмісартану, диспергованого в розчинюючій матриці, що включає (а) основний агент у молярному співвідношенні основний агент:телмісартан= 2:1 до 3:1, 81781 8 (б) неіонну поверхнево-активну речовину або емульгатор у кількості приблизно 2-7мас.% від кінцевої композиції, (в) 35-50мас.% водорозчинного розріджувача і (г) необов'язково 0-20% додаткових наповнювачів і/або допоміжних речовин, сума всіх компонентів становить 100%. Усі наведені в описі компоненти (а)-(д), згадані вище, можуть застосовуватися в більш переважному варіанті втілення, беручи до уваги, що найбільш переважним основним агентом є меглюмін, найбільш переважні неіонні поверхневоактивні речовини вибирають з полоксамерів, найбільш переважні водорозчинні розріджувачі вибирають з маніту, еритриту, сорбіту і сахарози, і найбільш переважні додаткові наповнювачі і/або допоміжні речовини вибирають із кристалічної целюлози, неповністю безводної кремнієвої кислоти і стеарату магнію. У будь-якому варіанті втілення за винаходом можуть бути присутні одна(ин) або декілька неіонних поверхнево-активних речовин або емульгаторів, водорозчинних розріджувачів і наповнювачів і/або допоміжних речовин. Другий об'єкт за винаходом (лікарська форма, готова для застосування/проковтування) Другий об'єкт за винаходом спрямований на тверді пероральні лікарські форми, готові для застосування/проковтування, наприклад, капсульні і таблеткові лікарські форми, приготовлені з фармацевтичних композицій, згаданих раніше. Капсульні лікарські форми можуть бути отримані просто завантаженням порошкоподібних або гранульованих фармацевтичних складів, згаданих вище, у звичайні капсули, наприклад, у жорсткі або м'які желатинові капсули. Лікарські форми у вигляді таблеток також можуть бути приготовлені за допомогою загальновідомих методик, наприклад, прямим пресуванням порошкоподібних або гранульованих фармацевтичних композицій, згаданих вище. Отримані в такий спосіб таблетки можуть бути оброблені далі з використанням звичайних прийомів, наприклад, можуть бути покриті, використовуючи відповідні покриття, відомі фахівцям у цій галузі, які не впливають негативно на властивості розчинення кінцевої лікарської форми. Наприклад, таблетки можуть бути мати верхніми водоізолювальним шаром для захисту від вологи шляхом плавлення поліетиленгліколю з високою молекулярною масою або будь-якого поліетиленгліколю, який є твердим на ядрах таблеток при кімнатній температурі (25°С). Навіть якщо полімер є водорозчинним, швидкість його розчинення досить низька, щоб надати ядрам таблеток захисту від вологи. Можуть застосовуватися також інші полімери, які виявляють подібну розчинність у воді і подібний ступінь захисту від вологи. Крім того, такі агенти, як бджолиний віск, шелак, ацетат-фталат целюлози, полівінілацетатфталат, зеїн, полімери, які утворюють плівку, такі, як гідроксипропілцелюлоза, етилцелюлоза і полімерні метакрилати, можуть бути розчинені у відповідному розчиннику і нанесені на таблетки за 9 умови, що покриття істотно не впливає на руйнування/розчинення лікарської форми і що лікарська форма з покриттям має стійкі фізикохімічні властивості. Після того, як лікарська форма закупорена, цукрове покриття може бути нанесене на герметизовану фармацевтичну лікарську форму. Цукрове покриття може включати сахарозу, декстрозу, сорбіт тощо або їх суміші. За необхідності до розчину цукру можуть бути додані барвники або опалесцентні речовини. Композиція лікарської форми як капсули, так і таблетки (ядра) переважно така ж, як згадано вище у відношенні фармацевтичних складів. Як альтернатива додаткові кількості необов'язкових наповнювачів і/або допоміжних речовин, згаданих вище, можуть бути додані перед завантаженням порошкоподібних або гранульованих фармацевтичних складів у капсули або пресуванням їх у таблетки, наприклад, щоб відрегулювати концентрацію активної сполуки до визначеного значення (наприклад, додаванням більшої кількості наповнювача), поліпшити сипкість порошкоподібних складів, поліпшити пресування (наприклад, додаванням більшої кількості змащувальної або зв'язувальної речовини), або використані інші рутинні способи оптимізації, відомі фахівцям. Тверді пероральні лікарські форми за даним винаходом, як правило, містять 10-160мг, переважно 20-80мг телмісартану. Переважні в даний час форми включають 20, 40 або 80мг телмісартану, відповідно. Наприклад, загальний склад капсульної або таблеткової лікарських форм за винаходом може змінюватися в межах наступних діапазонів за умови, що пропорційний склад, наведений вище у відношенні основних фармацевтичних композицій, дотримується: 10-160мг телмісартану; 10-160мг меглюміну або аргініну, або 2-33мг NaOH, або 3-46мг КОН, або 4-80мг NaHCO3, KHCO3, Na2CO3, K2CO3, Na2HPO4 або K2НРО4; 2-40мг неіонних поверхнево-активних речовин або емульгаторів; 20-200мг водорозчинних розріджувачів; і 0-80мг додаткових наповнювачів і/або допоміжних речовин; переважно 20-80мг телмісартану; 20-80мг меглюміну або 4-16мг NaOH, або 6-23мг KОН; 4-20мг неіонних поверхнево-активних речовин або емульгаторів, вибраних з полоксамерів, поліетиленгліколів, поліетоксилованої і гідрогенізованої рицинової олії, особливо переважними є полоксамери; 40-100мг водорозчинних розріджувачів, вибраних з глюкози, сахарози, еритриту, сорбіту, маніту і ксиліту; і 0,2-40мг додаткових наповнювачів і/або допоміжних речовин, вибраних із кристалічної целюлози, неповністю безводної кремнієвої 81781 10 кислоти, гідроксиметилцелюлози, гідроксіетилцелюлози, гідроксипропілцелюлози, гідроксипропілметилцелюлози, стеарату магнію, кукурудзяного крохмалю, полівінілпіролідону, співполімеру вінілпіролідону і вінілацетату, стеаринової кислота, стеарилфумарату натрію, колоїдного кремнію, тальку, повідону й фарбувальних агентів; найбільш переважно 35-45мг телмісартану; 35-45мг меглюміну; 6-10мг неіонних поверхнево-активних речовин або емульгаторів, вибраних з полоксамерів, особливо переважним є полоксамер 188; 70-90мг водорозчинних розріджувачів, вибраних з маніту, еритриту, сорбіту і сахарози; і 0,2-20мг додаткових наповнювачів і/або допоміжних речовин, вибраних із кристалічної целюлози, неповністю безводної кремнієвої кислоти і стеарату магнію. Слід розуміти, що для капсульних лікарських форм перевагою може бути додавання агента контролю плинності, такого, як колоїдний кремній, неповністю безводна кремнієва кислота, кристалічна целюлоза, перед заповненням капсули в машині для завантаження капсул порошкоподібною фармацевтичною композицією, щоб поліпшити властивості плинності композиції. Отже, у капсульних лікарських формах вміст додаткових наповнювачів і/або допоміжних речовин переважно буде знаходитися у верхньому діапазоні, наприклад, у діапазоні 10-20мас.% від усієї лікарської форми. На відміну від цього, агенти контролю плинності переважно не додаються при одержанні таблеткових лікарських форм за даним винаходом, оскільки дані агенти в сполученні з інтенсивними силами стискання, які застосовуються при виробництві таблеток, погіршують розчинення або розпад таблеток. Отже, у таблеткових лікарських формах вміст додаткових наповнювачів і/або допоміжних речовин переважно буде знаходитися в більш низькому діапазоні, наприклад, у діапазоні 0,15мас.%, переважно 0,3-2мас.% від кінцевої лікарської форми, оскільки повинні бути присутні лише малі кількості зв'язувальних речовин. Таблеткові лікарські форми за даним винаходом можуть також застосовуватися для приготування продуктів з комбінацією фіксованих доз, наприклад, разом з діуретиком як другим активним компонентом. Відповідними діуретиками є діуретики на основі тіазиду і його аналогів, як гідрохлортіазид (HCTZ), клопамід, ксипамід або хлороталідон, або які-небудь інші діуретики, придатні для лікування гіпертензії, як, наприклад, фуросемід і піретанід, і їх комбінації з амілоридом і триамтереном. Гідрохлортіазид несумісний з основними агентами, будучи компонентом таблеткової лікарської форми телмісартану за винаходом. Дана проблема може бути подолана за допомогою двошарової фармацевтичної таблетки, яка включає перший таблетковий шар, який містить телмісартан, отриманий з фармацевтичної композиції, згаданої вище в першому аспекті за винаходом, і другий 11 таблетковий шар, який містить діуретик у матриці таблетки, яка розпадається. Другий шар композиції таблетки, як правило, включає 1,5-35мас.%, переважно 2-15мас.% активного інгредієнта; 25-75мас.%, переважно 3565мас.% наповнювача; 10-40мас.%, переважно 1535мас.% сухого зв'язувального речовини; 0,55мас.%, переважно 1-4мас.% зв'язувального речовини вологої грануляції; і 1-10мас.%, переважно 2-8мас.% дезінтегратора. Інші наповнювачі і допоміжні речовини, як правило, застосовуються в тій же кількості, що й у першому шарі композиції таблетки. Наповнювач може бути вибраний з безводної лактози, висушеної розпиленням лактози і моногідрату лактози. Таблетки за даним винаходом мають тенденцію до прояву дуже низької гігроскопічності і можуть бути упаковані, використовуючи блістери з полівінілхлориду (ПВХ), блістери з полівініліденхлориду (ПВДХ) або стійкого до вологи пакувального матеріалу, такого, як блістерні упаковки з алюмінієвої фольги, поліпропіленові пробірки, скляні флакони і флакони з поліетилену високої густини (ПЕВГ). Третій об'єкт за винаходом (спосіб одержання фармацевтичних композицій і кінцевих лікарських форм) Третій об'єкт за винаходом спрямований на способи одержання твердих фармацевтичних композицій, згаданих вище. Композиції за винаходом, які включають телмісартан, можуть бути отримані будь-яким придатним способом, відомим фахівцям у даній галузі, наприклад, ліофілізацією водних розчинів, нанесенням частинок носія в псевдозрідженому шарі й осадженням з розчинника на цукрові гранули або інші носії. Однак переважно фармацевтичні композиції одержують, використовуючи спосіб грануляції, наприклад, спосіб грануляції в киплячому шарі (А) або як альтернатива спосіб висушування розпиленням (Б), описаний конкретно нижче. Переважним є менш складний і більш дешевий спосіб грануляції в киплячому шарі (А). Оскільки в процесі наступної обробки телмісартан звичайно розчиняється і перетворюється в основному аморфну форму, його вихідна кристалічна структура і розмір частинок мало важливі для фізичних і біофармацевтичних властивостей отриманої фармацевтичної композиції. У першому варіанті втілення винаходу спосіб грануляції в киплячому шарі (А) може бути використаний для одержання фармацевтичних композицій за винаходом, який характеризується наступними етапами: (і) приготування грануляційної рідини у вигляді водного розчину шляхом розчинення 3-50мас.% телмісартану разом з наступними компонентами в воді або суміші розчину етанолу і води: (а) основний агент у молярному співвідношенні основний агент:телмісартан=1:1 до 10:1, (б) неіонна поверхнево-активна речовина або емульгатор у кількості приблизно 1-20мас.%, 81781 12 (іі) завантаження 25-70мас.% водорозчинного розріджувача в гранулятор з киплячим шаром, необов'язково разом з 10-20мас.% сухої сполучної речовини, включаючи етап попереднього змішування, (ііі) здійснення грануляції в киплячому шарі, використовуючи грануляційну рідину для розбризкування на компоненти, завантажені в гранулятор, (iv) після завершення грануляції сушіння і необов'язково просіювання отриманого гранулята, (ν) необов'язкове змішування гранулята з додатковими наповнювачами і/або допоміжними речовинами, щоб одержати кінцеву композицію, і (vi) необов'язкове подрібнення отриманого в такий спосіб гранулята, щоб одержати порошкоподібну композицію з визначеним розподілом розмірів частинок; де всі наведені процентні кількості стосуються кінцевої композиції, яка повинна бути отримана. Переважні варіанти втілення способу у відношенні специфічних компонентів і пропорційних кількостей повністю відповідають таким варіантам, які розкриті вище у відношенні першого аспекту винаходу. На стадії попередньої суміші етапу (іі) може застосовуватися температура вхідного повітря приблизно 60-120°С. На етапі грануляції може застосовуватися температура вхідного повітря приблизно 80-100°С. Швидкість розпилення значно залежить від типу використовуваного гранулятора, а також від обсягу партії і може регулюватися фахівцем за допомогою рутинної операції. Наприклад, тільки швидкість розпилення 400-1000мл/хв. може бути придатною для партії гранулята 200кг. Можуть застосовуватися також більш низькі або більш високі швидкості розпилення. На стадії сушіння етапу (iv) може застосовуватися температура вхідного повітря приблизно 60-120°С і тривалість сушіння приблизно 1-30хв. На етапі просіювання придатним може бути сито з розміром комірки 0,53мм. Необов'язковий етап подрібнення (vi) звичайно може здійснюватися фахівцем у цій галузі. В другому варіанті втілення спосіб висушування розпиленням (Б) може застосовуватися для одержання фармацевтичних композицій за винаходом, які характеризується наступними етапами: (і) приготування водного розчину для розпилення шляхом розчинення 3-50мас.% телмісартану разом з наступними компонентами в воді або суміші розчину етанолу і води: (а) основний агент у молярному співвідношенні основний агент:телмісартан= 1:1 до 10:1, (б) неіонна поверхнево-активна речовина або емульгатор у кількості приблизно 1-20мас.%, (іі) розпилювальне сушіння згаданого водного розчину для розпилення, щоб одержати висушений розпиленням гранулят; (ііі) змішування згаданого висушеного розпиленням гранулята з 25-70мас.% 13 водорозчинного розріджувача, щоб одержати попередню суміш; (iv) необов'язкове перемішування згаданої попередньої суміші з змащувальною речовиною; (ν) необов'язкове додавання додаткових наповнювачів і/або допоміжних речовин на кожному з етапів (i)-(iv), де всі наведені процентні кількості стосуються кінцевої композиції, яка повинна бути отримана. Якщо необхідно відрегулювати особливий розподіл розмірів частинок в отриманій в такий спосіб порошкоподібної композиції, може бути використаний етап звичайного подрібнення, переважно перед необов'язковим додаванням змащувальної речовини відповідно до етапу (iv). Крім того, порошкоподібна композиція може бути перетворена в гранулярну композицію, застосовуючи звичайні методики грануляції. Переважні варіанти втілення способу у відношенні специфічних компонентів і пропорційних кількостей повністю відповідають таким варіантам, які розкриті вище у відношенні першого аспекту за винаходом. У переважному варіанті втілення способу (Б) водний лужний розчин телмісартану одержують розчиненням активного інгредієнта в воді або суміші етанолу і води за допомогою одного або декількох основних агентів, як гідроксид натрію або меглюмін. Необов'язково може бути доданий сповільнювач перекристалізації. Вміст сухої речовини в початковому водному розчині, як правило, становить 10-40мас.%, переважно 2030мас.%. Водний розчин потім сушать розпиленням при кімнатній температурі або переважно при підвищених температурах, наприклад, між 50 і 100°С в умовах прямоточного або протитечійного апарата для сушіння розпиленням при тиску розпилення, наприклад, 1-4бар. Загалом, умови висушування розпиленням переважно вибирають таким чином, що висушений розпиленням гранулят, який має залишкову вологість £5мас.%, переважно £3,5мас.%, виходить у розділовій ділянці низького тиску. До цього моменту температура вихідного повітря апарата для сушіння з розпиленням підтримується при значенні між 80 і 90°С, тоді як інші параметри способу, такі, як тиск розпилення, швидкість розпилення, температура вхідного повітря і т.д., встановлюються відповідно. Отриманий висушений розпиленням гранулят переважно є тонкоподрібненим порошком, який має наступний розподіл частинок за розмірами: d10: £20мкм, переважно £10мкм d10: £80мкм, переважно 20-55мкм d10: £350мкм, переважно 50-150мкм Після висушування розпиленням активний інгредієнт (телмісартан), а також наповнювачі, які містяться у висушеному розпиленням грануляті, знаходяться в основному в аморфному стані, без кристалічності, яка піддається визначенню. З фізичної точки зору, висушений розпиленням гранулят є затверділим розчином або склом, що має температуру склування Tg переважно >50°С, більш переважно >80°С. 81781 14 Змащувальну речовину, як правило, додають до попередньої суміші в кількості 0,1-5мас.%, переважно 0,3-2мас.% у розрахунку на масу кінцевої композиції. Змішування проводять у два етапи, тобто на першому етапі змішування висушений розпиленням гранулят і розріджувач змішують, використовуючи, наприклад, міксер з великим зсувним зусиллям або гравітаційний змішувач, і на другому етапі змішування змащувальна речовина змішується з попередньою сумішшю, переважно також в умовах великого зсувного зусилля. Однак спосіб за винаходом не обмежується даними методиками змішування, і, як правило, альтернативні методики змішування можуть застосовуватися на будь-якому етапі способу, включаючи методики змішування, такі, як, наприклад, контейнерне змішування з проміжним просіюванням. Партії гранул різного складу, отримані способом (А) або (Б), можуть бути змішані разом, щоб відрегулювати цільову композицію, і можуть бути додатково змішані з новими наповнювачами і/або допоміжними речовинами, такими, як змащувальні речовини, якщо потрібно для відрегулювання кінцевої композиції з метою подальшої обробки в заключну лікарську форму, готову для застосування/проковтування, наприклад, для завантаження в капсули, використовуючи відповідну машину для заповнення капсул, або для безпосереднього пресування таблеток, використовуючи відповідний роторний таблетковий прес. Кінцева композиція для безпосереднього стискання може бути отримана шляхом сухого змішування складових компонентів, наприклад, за допомогою високоінтенсивного міксера або гравітаційного змішувача. Альтернативно кінцева композиція може бути отримана, використовуючи методику вологої грануляції, де водний розчин або зв'язувальну речовину вологої грануляції додають до попередньої суміші і згодом отриманий вологий гранулят сушать, наприклад, в апараті для сушіння в псевдозрідженому шарі або в сушильній камері. Висушену суміш просіюють і потім підмішують змащувальну речовину, використовуючи, наприклад, барабанний міксер або гравітаційний змішувач, після чого композиція готова для пресування. Двошарова таблетка, згадана в другому аспекті винаходу, може бути отримана в такий спосіб: (і) забезпечення композиції першого шару таблетки, що включає телмісартан, із застосуванням методики грануляції в киплячому шарі (А) або методики висушування розпиленням (Б), описаної вище, (іі) забезпечення композиції другого шару таблетки шляхом (а) змішування і/або гранулювання діуретику зі складовими частинами дезінтегрувальної таблеткової матриці і необов'язково додатковими наповнювачами і/або допоміжними речовинами; 15 (б) примішування змащувальної речовини, щоб одержати кінцеву суміш для другого шару таблетки; (ііі) введення першого або другого шару композиції таблетки в таблетковий прес; (iv) стискання композиції згаданого таблеткового шару, щоб утворити шар таблетки; (ν) введення іншого шару композиції таблетки в таблетковий прес; і (vi) стискання обох композицій таблеткових шарів, щоб утворити двошарову таблетку. Для одержання двошарової таблетки за даним винаходом композиції першого і другого таблеткових шарів можуть бути стиснуті звичайним способом у двошаровому таблетковому пресі, наприклад, високошвидкісному роторному пресі в режимі двошарового таблетування. Однак слід дотримуватися обережності, щоб не застосовувати надмірну силу стискання для першого шару таблетки. Переважне відношення сили стискання, яка застосовується в процесі пресування першого шару таблетки, до сили стискання, яка застосовується в процесі пресування як першого, так і другого таблеткових шарів, знаходиться в діапазоні від 1:10 до 1:2. Наприклад, перший таблетковий шар може бути стиснутий при помірній силі 4-8 кН, тоді як основний стиск шару перший плюс другий здійснюється при силі 10-20кН. При стисканні двошарової таблетки досягається відповідне утворення зв'язків між двома шарами за допомогою сил дистанційного притягання (міжмолекулярних сил) і механічного зчеплення між частинками. Для того щоб уникнути якого-небудь перехресного забруднення між першим і другим шарами таблетки (які могли привести до розкладання гідрохлортіазиду), будь-які залишки гранулята повинні були бути ретельно видалені в процесі таблетування шляхом інтенсивного відсмоктування залишків матриці всередині таблетувальної камери. Вивчення вивільнення активного інгредієнта Тверді пероральні лікарські форми за даним винаходом вивільняють активний інгредієнт телмісартан швидко і з незначною залежністю від рН. Звичайно принаймні 70% і типово принаймні 80% лікарського навантаження розчиняються через 30хв, і вивільнення основної фракції відбувається менш ніж за 20хв. Таблиця 1 представляє типову капсульну лікарську форму, яка містить фармацевтичну композицію за винаходом, позначену лікарською формою А, яка містить як неіонну поверхневоактивну речовину або емульгатор 8мг полоксамеру 188 (полюксіетилен[160]поліоксипропілен[30]гліколю), і відповідну стандартну лікарську форму, позначену лікарська форма Б, яка містить замість полоксамерного компонента додаткові 8мг Dманіту. Розчинення даних капсульних лікарських форм оцінювали у водних розчинах із рН 1,2 і 4,0 відповідно до Японської фармакопеї (JP), способом з лопатевою мішалкою, 100об/хв., 81781 16 900мл, 37°С, розчинне середовище: рН1,2, JP, перша рідина, ацетатний буфер, рН4,0; визначення: УФ/296нм. Отримані результати можна бачити на Фіг.1 і 2, які демонструють вивільнення активного інгредієнта телмісартану, наведене як «% розчинення». Вивільнення телмісартану було істотно швидше в присутності полоксамеру 188. Таблиця 1 Композиція досліджених капсульних лікарських форм Лікарська форма А Телмісартан 40мг Меглюмін 40мг Полоксамер 188 8мг D-Маніт 81мг Кристалічна целюлоза 30мг (авіцель РН101) Стеарат магнію 1мг Загальна кількість 200мг/кап. Б 40мг 40мг 0мг 89мг 30мг 1мг 200мг/кап. Короткий опис фігур Фіг.1 показує профіль вивільнення активного інгредієнта телмісартану з капсульної лікарської форми А за винаходом в порівнянні з відповідною капсульною лікарською формою Б без компонента полоксамер 188 у водному досліджуваному розчині (JP, перша рідина) при рН1,2. Фіг.2 показує профіль вивільнення телмісартану з лікарської форми А в порівнянні з лікарською формою Б в водному ацетатному буфері при рН4,0. Для того щоб ілюструвати далі даний винахід, наведені наступні приклади, які його не обмежують. Наступна таблиця представляє тверді фармацевтичні композиції за винаходом. Лікарські форми В, Г, Д, Ε і Є є гранулярними лікарськими формами, які можуть бути завантажені в капсули, лікарські форми Г, Д, Ε і Є можуть також бути стиснуті з утворенням таблеток. Усі лікарські форми містять 40мг телмісартану, тоді як альтернативні капсульні і таблеткові лікарські форми, що містять 20 або 80мг телмісартану, є гомологічними лікарськими формами. Лікарська форма Телмісартан Меглюмін Полоксамер 188 D-Маніт Еритрит Сорбіт Сахароза Кристалічна целюлоза Неповністю безводна кремнієва кислота Стеарат магнію Загальна кількість Виробництво В 40,0мг 40,0мг 8,0мг 81,5мг 30,0мг Г 40,0мг 40,0мг 8,0мг 80,6мг 0,5мг 200,0мг 1,4мг 170,0мг 17 1. Грануляційна рідина або розчин для розпилення Відміряють 90кг очищеної води у відповідній ємкості з нержавіючої сталі при температурі між 20-40°С. Послідовно розчиняють 8кг полоксамеру 188 (поліоксіетилен[160]поліоксипропілен[30]гліколю), 40мг меглюміну і 40кг телмісартану (суміш поліморфів А і Б) в очищеній воді при інтенсивному перемішуванні до одержання фактично прозорого розчину. Загальний об'єм приблизно 160л. 2. Грануляція Варіант (а) для одержання лікарської форми В У гранулятор з киплячим шаром завантажують 81,5кг D-маніту і 30кг кристалічної целюлози (наприклад, авіцелю РН101 або 302), недовго попередньо перемішують і розпилюють з 178кг грануляційної рідини (яка містить 88кг сухої маси). Потім розпилюють з 2л очищеної води з наступним етапом висушування й етапом просіювання. Варіант (б) для одержання лікарської форми Г У гранулятор з киплячим шаром завантажують 81,5кг D-маніту і розпилюють з 178кг грануляційної рідини (яка містить 88кг сухої маси). Потім розпилюють з 2л очищеної води з наступним етапом висушування й етапом просіювання. Варіант (в) для одержання лікарської форми Д У гранулятор з киплячим шаром завантажують 80,5кг еритриту і 0,1кг неповністю безводної кремнієвої кислоти і розпилюють з 178кг грануляційної рідини (яка містить 88кг сухої маси). Потім розпилюють з 2л очищеної води з наступним етапом висушування й етапом просіювання. Варіант (г) для одержання лікарської форми Ε У гранулятор з киплячим шаром завантажують 70,6кг еритриту і 10кг сорбіту і розпилюють з 178кг грануляційної рідини (яка містить 88кг сухої маси). Потім розпилюють з 2л очищеної води з наступним етапом висушування й етапом просіювання. Варіант (д) для одержання лікарської форми Є У гранулятор з киплячим шаром завантажують 80,6кг сахарози і розпилюють з 178кг грануляційної рідини (яка містить 88кг сухої маси). Потім розпилюють з 2л очищеної води з наступним етапом висушування й етапом просіювання. Параметри способу попереднього готування суміші Температура вхідного повітря 80-100°С. Кінець попереднього приготування суміші. Температура підігріву 55°С. Параметри способу грануляції Температура вхідного повітря 80-100°С. Швидкість розпилення 500-900мл/хв. Параметри способу етапу висушування Температура вхідного повітря 80-100°С. Кінець висушування. Температура підігріву більше ніж 70°С. Тривалість висушування приблизно 5хв. Параметри способу етапу просіювання Гранулят просіюють, використовуючи, наприклад, вібратор або машину Comil для просіювання з розміром отвору 1,5мм. 3. Кінцева суміш для одержання капсульної лікарської форми 81781 18 Два завантаження по 199,5 кг просіяних гранул, отриманих відповідно до варіанта грануляції (а), змішували, використовуючи відповідний змішувач з обертанням 10об/хв. протягом 20хв., що приводило до 399кг перемішаного завантаження, яке на закінчення змішували з 1кг стеарату магнію, використовуючи відповідний змішувач з обертанням 10об/хв. протягом приблизно 15хв., одержуючи в такий спосіб кінцеву суміш. Кінцева суміш для одержання таблеткової лікарської форми Два завантаження по 199,5кг просіяних гранул, отриманих відповідно до варіанта грануляції (б), (в), (г) або (д), змішували, використовуючи відповідний змішувач з обертанням 10об/хв. протягом 10-20хв., що приводило до 399кг перемішаного завантаження, яке на закінчення змішували з 1кг стеаратом магнію, використовуючи відповідний змішувач з обертанням 10об/хв. протягом приблизно 15хв., одержуючи в такий спосіб кінцеву суміш. 5. Заповнення капсул Кінцеву суміш для капсульної лікарської форми завантажували в капсули, використовуючи відповідну машину для заповнення капсул (100, 200 або 400мг на капсулу). 6. Пресування таблеток Використовуючи відповідний ротаційний таблетковий прес, кінцеву суміш для стиску в таблетки пресували у вигляді таблеток. Контрольна маса 85, 170 або 340мг. Параметри способу таблетування Таблетковий прес Fette 3090 Швидкість 100000 (80000-120000) таблетування таблеток/год Швидкість лопатевої Приблизно 30об/хв. мішалки Сила стискання 7(5-10)кН Твердість таблетки може бути відрегульована зміною основної сили стискання. 8. Одержання висушеної розпиленням лікарської форми Розчин для розпилення, описаний вище, розпилювали у відповідному розпилювальному сушильному апараті, наприклад, Niro P 6,3, обладнаному форсунками Schlick діаметром 1,0мм, із проточним нагрівальним змійовиком, встановленим проти потоку сушильного апарата, і сушили, одержуючи білий до не зовсім білий дрібний гранулят. Тип розпилення протитечійний при тиску розпилення приблизно 3 бари, температурі вхідного повітря близько 125°С і швидкості розпилення приблизно 11кг/год., у такий спосіб приводячи до температури вихідного повітря приблизно 85°С. Температура проточної нагрівальної змієвикової водної бані встановлюється при значенні приблизно 80°С. Змішували 88кг висушених розпиленням гранул з 80,6кг порошкоподібного D-маніту, використовуючи відповідний міксер з обертанням 10об/хв. протягом приблизно 15хв., і на закінчення змішували з 1,4кг стеарату магнії, одержуючи в 19 такий спосіб кінцеву суміш, готову для завантаження в капсули або пресування в таблетки. 81781 20
ДивитисяДодаткова інформація
Назва патенту англійськоюPharmaceutical formulation comprising telmisartan, process for preparing thereof (variants), bilayer pharmaceutical tablet and process for preparing thereof
Автори англійськоюNakatani Manabu, Ohki Toshimitsu, Takeshi Sawada, Toyoshima Kenzo
Назва патенту російськоюФармацевтическая композиция, которая включает телмисартан, способ ее получения (варианты), двухслойная фармацевтическая таблетка и способ ее получения
Автори російськоюНакатани Манабу, Охки Тошимитсу, Такеши Савада, Тойошима Кензо
МПК / Мітки
МПК: A61K 9/20, A61P 9/12, A61K 31/4184, A61K 9/16
Мітки: композиція, таблетка, яка, фармацевтична, варіанти, телмісартан, двошарова, спосіб, включає, одержання
Код посилання
<a href="https://ua.patents.su/10-81781-farmacevtichna-kompoziciya-yaka-vklyuchaeh-telmisartan-sposib-oderzhannya-varianti-dvosharova-farmacevtichna-tabletka-ta-sposib-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Фармацевтична композиція, яка включає телмісартан, спосіб її одержання (варіанти), двошарова фармацевтична таблетка та спосіб її одержання</a>
Попередній патент: Спосіб перетворення теплової енергії в механічну роботу з утилізацією теплоти продуктів згоряння
Наступний патент: Застосування пристрою з подвійним перехресним видавлюючим шнеком для обробки матеріалу в піролітичних умовах та спосіб обробки вугілля в піролітичних умовах
Випадковий патент: Спосіб виготовлення суспензій і установка для його здійснення