Спосіб одержання літієвої батареї
Номер патенту: 72728
Опубліковано: 15.03.2005
Автори: Калінушкін Євген Павлович, Балакін Олександр Анатольєвич, Новак Петро Якович, Маркевич Олександр Васильович, Шембель Олена Мойсеївна
Формула / Реферат
1. Спосіб отримання літієвої батареї, що складається з активної катодної маси, нанесеної на струмознімач, анода, сепаратора і неводного електроліту, який відрізняється тим, що катодна маса містить 100 % електрохімічного активного матеріалу, за який використовують оксиди або сульфіди металів у вигляді компактного осаду, при цьому щільність катодної маси становить 2,6-4,9 г/см3, а товщину активного шару катоду вибирають в межах від 0,5 мкм до 3 мм.
2. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що як анодний матеріал використовують літій, літієві сплави, вуглець або будь-які інші сполуки, оборотні по катіонах літію.
3. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що катод забезпечує вигин без порушення контакту між активною масою і струмознімачем в діапазоні радіуса вигину від 0,4 мм до 3,9 мм при товщині шару активного катодного матеріалу від 0,5 мкм до 440 мкм.
4. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що активний матеріал катода отримують у вигляді компактного осаду, що складається з триоксиду молібдену (МоО3).
5. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що активний матеріал катода отримують у вигляді компактного осаду, що складається з сульфідів заліза.
6. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що щільність шару активного матеріалу катода і його структуру змінюють у напрямі від межі поділу струмознімач/активний матеріал катода до межі поділу активний матеріал катода/неводний електроліт таким чином, що на межі поділу струмознімач/активний матеріал катода щільність активного матеріалу вища, ніж на межі поділу активний матеріал/рідкий електроліт, при цьому щільність може змінюватися на величину 2 г/см3 по товщині електрохімічного активного шару оксиду металу до 1,4 мм.
7. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що активний матеріал катода наносять на поверхню струмознімача методом термовакуумної конденсації-солідифікації.
8. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що у процесі одержання катода використовують молібденовий випарник.
9. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що як катодний струмознімач використовують нержавіючу сталь, алюміній або титан.
10. Спосіб отримання літієвої батареї за п.4, який відрізняється тим, що в процесі нанесення МоО3 температура катодного струмознімача складає від 210 до 250°С при швидкості охолодження шару від 18 до 22°С/сек.
11. Спосіб отримання літієвої батареї за п. 10, який відрізняється тим, що виготовлений катод використовують в первинних та вторинних джерелах струму.
12. Спосіб отримання літієвої батареї за п.5, який відрізняється тим, що в процесі нанесення FeS2 у присутності пари сірки температура катодного струмознімача складає від 20 до 60°С.
13. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що як катодний струмознімач використовують метал з розвиненою поверхнею.
14. Спосіб отримання літієвої батареї за п.11, який відрізняється тим, що в процесі нанесення МоО3 температура катодного струмознімача складає від 230 до 270°С при швидкості охолодження шару 2-4°С/сек.
15. Спосіб отримання літієвої батареї за п.14, який відрізняється тим, що виготовлений катод використовують в первинних джерелах струму.
16. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що як неводний електроліт використовують рідкий електроліт.
17. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що як неводний електроліт використовують полімерний електроліт з провідністю по катіонах літію.
18. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що як неводний електроліт використовують твердий неорганічний електроліт з провідністю по катіонах літію.
19. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що поверхня катода покрита шаром твердого електроліту.
20. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що на стадії переходу матеріалу твердого електроліту з газової фази в рідку електроліт проникає в пори катодного матеріалу і рівномірно розподіляється по об'єму електрода.
21. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що товщина шару твердого електроліту становить 2-10 мкм, а процес нанесення твердого електроліту реалізують шляхом складного ступеневого випарювання матеріалу з наступним ступеневим охолодженням осаду.
22. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що між шаром твердого електроліту, що покриває поверхню катода, і анодом знаходиться сепаратор, просочений рідким неводним електролітом.
23. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що між шаром твердого електроліту, що покриває поверхню катода, і анодом знаходиться полімерний електроліт з провідністю по катіонах літію.
24. Спосіб отримання літієвої батареї за п.1, який відрізняється тим, що між шаром полімерного електроліту, що покриває поверхню катода, і літієвим анодом знаходиться сепаратор, що просочений рідким неводним електролітом.
Текст
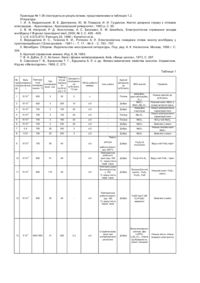
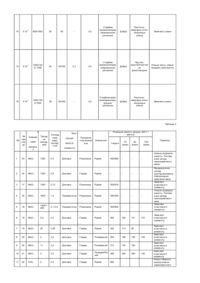
Винахід відноситься до хімічних джерел струму, зокрема, до хімічних джерел струму з анодом на основі літію, неводним електролітом, і катодом, у якому в якості активної катодної речовини використовуються оксиди або сульфіди металів. Від властивостей катоду у значній мірі залежать питомі розрядні характеристики літієвих джерел струму з твердофазним катодом, зокрема, його питомої розрядної ємності на одиницю ваги і одиницю об'єму. Як правило, до складу катодної маси літієвих джерел струму входять: активна речовина, електропровідна добавка, наприклад, графіт і/чи сажа, та сполучне. Катодн у масу готують з ви хідних порошків цих компонентів [1]. Електрохімічне активною з перерахованих компонентів катодної маси є тільки активна речовина. Достатню електронну провідність в об'ємі катодної маси забезпечує електропровідна добавка. Ме ханічну міцність катодної маси забезпечує сполучне. Слід зазначити, що механічна міцність необхідна не тільки при складанні джерела струму, але і в процесі його роботи. Це пов'язано з тим, що при розряді об'єм катодної маси збільшується, а при заряді зменшується. В результаті можуть виникати механічні напруги, що приводять до руйнування електрода. Забезпечити механічну міцність катода на всіх стадіях його роботи повинно сполучне. До недоліків даного способу варто віднести те, що при механічному змішуванні дисперсних часток і компонентів катодного матеріалу дуже складно одержати однорідну за розподілом суміш. Крім того, у значній мірі знижує питомі електричні характеристики джерела струму наявність баластового електрохімічне пасивного матеріалу в складі активної маси позитивного електроду (електропровідна і сполучна добавки). Відомий спосіб виготовлення безбаластового катоду на основі оксидів молібдену нестехіометричної сполуки, призначеного для роботи в низькотемпературних літієви х акумуляторах. Спосіб полягає в тому, що катодне висадження оксидів молібдену на стр умознімач здійснюється з розчинів молібдату амонію [2]. До недоліків даного способу варто віднести необхідність жорсткого контролю параметрів режиму електролізу, складу електроліту, низьку швидкість одержання електрохімічне активної катодної речовини необхідного шару та неможливість отримання товстих шарів (біля 1 мм) оксидів молібдену. Крім того, перед складанням джерела струму з катодом, виготовленим за цим способом, виникає необхідність його тривалої термічної обробки з метою видалення з електродної структури залишків води. Відомий спосіб виготовлення безбаластового катоду на основі дисульфіда титана. У цьому способі формування катодного шару здійснюється з газової фази. У свою чергу, у газовій фазі протікає хімічна реакція між хлоридом титана і сірководнем. Продукт взаємодії (дисульфід титана) осаджується на струмознімач у вигляді тонкої плівки, товщиною від 1 до 10 мкм [3]. До недоліків даного способу варто віднести високу токсичність сірководню, що служить одним з реагентів для синтезу катодного матеріалу. Крім того, даний технологічний процес не дозволяє одержувати плівки катодного матеріалу товщиною до 1 мм, що значно звужує область застосування і можливості конструкційного виконання хімічного джерела струму. Найбільш близьким до запропонованого авторами технічного рішення є спосіб одержання безбаластного активного катодного матеріалу на основі МоО3 шляхом анодування листового молібдену високої чистоти (99,98 %) в електроліті, що містить 1 М розчин виннокислого натрію, 0,13 М винної кислоти і 0,01 М розчин вуглекислого натрію при щільності струму 2,4 мА/см 2 і кімнатній температурі [4]. До недоліків прототипу варто віднести високу вартість молібдену високої чистоти, низьку швидкість одержання і невизначеність основних фізичних параметрів електрохімічне активного катодного шару (товщина, питома вага, і т.д.) та неможливість отримання товстих шарів (біля 1 мм) МoО3. Крім того, перед складанням джерела струму з катодом, виготовленим за цим способом, виникає необхідність його тривалої термічної обробки з метою видалення з електродної структури залишків води. Задачею даного винаходу є створення такого джерела струму, у якому досягається підвищення питомих енергетичних характеристик за рахунок додаткової кількості електрохімічне активної маси, що заміняє сполучне і електропровідну добавку. Вирішення поставленої задачі досягається за рахунок того, що в способі одержання літієвої батареї, що складається з активної катодної маси, нанесеної на струмознімач, анода, сепаратора і неводного електроліту, відповідно до винаходу, катодна маса містить 100 % електрохімічного активного матеріалу, в якості якого використовують оксиди або сульфіди металів у вигляді компактного осаду, при цьому щільність катодної маси становить 2,6 - 4,9 г/см 3, а товщину активного шару катоду обирають в межах 0,5 мкм до 3 мм. У якості анодного матеріалу використовують літій, літієві сплави, вуглець або будь-які інші сполуки, оборотні по катіонах літію. Активний матеріал катода отримують у вигляді компактного осаду, що складається, в одному випадку, з оксидів, наприклад, з триоксиду молібдену (МоО3), а в др угому випадку, з сульфідів, наприклад, FeS2-піріту. При цьому катод забезпечує вигин без порушення контакту між активною масою і струмознімачем в діапазоні радіуса вигину від 0,4 мм до 3,9 мм при товщині шару активного катодного матеріалу від 0,5 мкм до 440 мкм. Крім того, нові корисні властивості додаються до винаходу, коли питому вагу шару активного матеріалу катоду і його структур у змінюють у напрямі від межі розділу струмознімач/активний матеріал катоду до межі розділу активний матеріал катоду/неводний електроліт таким чином, що на межі розділу струмознімач/активний матеріал катоду щільність активного матеріалу вище, ніж на межі розділу активний матеріал/рідкий електроліт, при цьому щільність може змінюватися на величину 2 г/см 3 по товщині електрохімічного активного шару оксиду металу до 1,4 мм. Зменшення питомої ваги активного матеріалу в напрямку до межі розподілу електрод/електроліт сприяє збільшенню пористості і питомої поверхні матеріалу на межі електрод/електроліт. Цей факт додає об'єкту новий корисний ефект, який полягає у тому, що при одній і тій же геометричній щільності струму реальна щільність струму на межі розподілу електрод/електроліт зменшується, тобто електрохімічний процес протікає в об'ємі катоду. Це означає, що електрод може ефективно працювати при підвищених геометричних щільностях розрядного струму. Збільшення пористості катодного матеріалу на межі з електролітом сприяє також оптимізації структури електрод/твердий електроліт. Твердий неорганічний електроліт наносять на електрод з використанням методу, який включає стадії переходу матеріалу з газової фази в рідку і потім у тверду. На стадії переходу матеріалу твердого електроліту з газової фази в рідку електроліт проникає в пори катодного матеріалу і рівномірно розподіляється по об'єму електрода. При цьому додатковою позитивною властивістю структури, що утворюється, є також висока механічна міцність межі розподілу електрод/електроліт. В якості катодного струмознімача використовують метал з розвиненою поверхнею. Матеріал струмознімача нержавіюча сталь, алюміній або титан. В процесі нанесення МоО3 температура катодного струмознімача складає від 210 до 250°С при швидкості охолодження шару від 18 до 22°С/сек. В процесі нанесення FeS2 у присутності пари сірки температура катодного струмознімача складає від 20 до 60°С. Виготовлений таким чином оксидний або сульфідний катод використовується в первинних та вторинних джерелах стр уму. В процесі нанесення товстих (більше 80 мкм) шарів МоО3 для первинних джерел струму температура катодного струмознімача складає від 230 до 270 °С при швидкості охолодження шару 2-4°С/сек. При цьому в якості катодного струмознімача використовують метал з розвиненою поверхнею. Наприклад, це може бути металева фольга, на поверхню якої нанесений порошок того ж самого металу різного ступеня дисперсності. Перелік фігур: Фіг. 1. Зміна питомої ємності катоду на основі FeS2 від кількості заряд-розрядних циклів. Крива з трикутними крапками відповідає розряду. Крива з круглими крапками відповідає заряду. Фіг. 2. Залежність питомої розрядної ємності від товщини катодного матеріалу. Лінія з прозорими крапками відповідає щільності розрядного струму до 0,8 мА/см 2. Лінія з чорними крапками відповідає щільності розрядного струму 5 мА/см 2. Фіг. 3. Схема зразка мікробатареі дискової конструкції з катодом на основі МоО3, отриманим методом термовакумної конденсації-солідифікації. Фіг. 4. С хема зразка мікробатареї призматичної конструкції з катодом на основі МоО3, отриманим методом термовакумної конденсації-солідифікації. Фіг. 5. Дослідження механічної міцності, адгезії і когезії електродів на основі оксидів молібдену. Фіг. 6. Залежність аморфизованності структури МоО 3 від товщини електрода. Фіг. 7. Зміна питомої ваги МоО3 по товщині катоду, отриманого методом термовакуумної конденсаціїсолідифікації. Фіг. 8. Зміна питомої електронної провідності шару МоО 3 від ступеня розряду електрода. В літієвій батареї в якості неводного електроліту використовують: 1. Рідкий електроліт. 2. Полімерний електроліт. 3. Твердий неорганічний електроліт. Усі електроліти мають провідність по катіонах літію. В другому випадку, між шаром полімерного електроліту, що покриває поверхню катоду, і літієвим анодом знаходиться сепаратор, що просочений рідким неводним електролітом. У третьому випадку, поверхня катоду, покрита шаром твердого електроліту, товщина якого становить 2-10 мкм. Це поєднання забезпечує об'єкту нові корисні властивості, такі, як підвищення питомої ємності в процесі електрохімічного циклування. Нанесення твердого електроліту реалізують шляхом складного східчастого випару матеріалу з наступним східчастим охолодженням осаду. Між шаром твердого електроліту, що покриває поверхню катоду, і анодом знаходиться сепаратор, просочений рідким неводним електролітом, або полімерний електроліт. Модифікацію поверхні позитивного електроду шаром твердого електроліту використовують для виготовлення вторинних хімічних джерел струму. При модифікації поверхні позитивного электроду шаром твердого електроліту підвищуються оборотні електрохімічні характеристики електродів, у яких товщина активної маси знаходиться в межах від 0,5 до 80 мкм. Зазначені характеристики досягаються тим, що для виготовлення електроду застосовують метод термовакумної конденсації-солідифікації з оптимальним режимом нанесення активної маси позитивного електроду і твердого електроліту. Вибір МoО3, як катодного матеріалу в хімічних джерелах струму, у даній заявці обумовлений тим, що цей оксид при нагріванні вище 600 °С має властивість переходити в пароподібний стан без зміни свого хімічного складу [5]. Цією властивістю не володіють більшість інших оксидів, що широко використовуються в літієвих джерелах струм у, що перезаряджаються, та первинних елементах. Так, наприклад, марганцю диоксид (МnO2) при нагріванні вище 535°С, до переходу у газоподібний стан, розкладається до Мn2О3 . Пентаоксид ванадію (V2O5) розкладається при нагріванні вище 1750°С, також до переходу у газоподібний стан [6]. Схильність до хімічної деструкції при нагріванні до високих температур виявляють і більшість сульфідів металів. Одержання у вигляді тонкої плівки феррум дисульфіду (FeS2), так само представленого в даній заявці як катодного матеріалу для літієвих хімічних джерел струму, стало можливим завдяки проведення процесу термовакуумного напилювання в присутності в робочій камері парів сірки. При термічному випарі FeS2 у газоподібний стан переходять продукти розкладання феррум дисульфіду. При цьому сполуки заліза, що випаровуються і переходять в об'єм камери, збіднюються по сірці. Проведення процесу напилювання FeS2 у присутності пари сірки, що вводяться додатково в об'єм робочої камери, зміщує хімічну рівновагу убік утворення феррум дисульфіду. FeS2 , який утворився внаслідок цього процесу, осаджується на підкладку, формуючи плівку електродного матеріалу. Заявлені граничні характеристики обумовлені наступним: 1. При питомій вазі активної маси позитивного електроду менш ніж 2,7 г/см 3 зменшуються об'ємні питомі розрядні характеристики катода і джерела струму в цілому. 2. Товщина шару активної маси позитивного електроду менш ніж 0,5 мкм не дозволяє одержати рівномірний шар МoО3 по всій поверхні струмознімача. При цьому також погіршується матеріальний баланс батареї, оскільки виникає необхідність значного зменшення ваги та товщини стр умознімача. 3. Для вторинного джерела струму товщина активної маси позитивного електроду не повинна перевищувати 80 мкм, оскільки більша товщина шар у не дозволяє одержувати високі оборотні питомі електрохімічні характеристики в рідкому і полімерному електролітах. 4. У випадку вторинного джерела струму позитивний електрод, поверхня якого не модифікована шаром твердого електроліту, характеризується зниженими оборотними питомими електрохімічними характеристиками, що негативним чином позначається на заряд-розрядних характеристиках джерела струму в цілому. 5. У випадку первинного джерела струму товщина електродів, що не містять сполучного та електропровідної добавки, досягає 3 мм. Використання товсти х електродів дозволяє значно підвищити питомі характеристики джерела струму. Це обумовлено тим, що значно покращується матеріальний баланс элементу, який характеризується співвідношенням активних матеріалів джерела струму і конструкційних матеріалів. В якості прикладу в даному винаході запропоновані катоди на основі МоО3 і FeS2 з високою питомою вагою, які одержують методом термовакуумної конденсації-солідифікації. Висока питома вага катодної маси забезпечує високі питомі електричні характеристики літієвого джерела струму. Корисні переваги цього методу і катоду, отриманого на його основі наступні: - після отримання катоду і збереження його в сухій атмосфері, він не потребує термічної обробки з метою видалення з електродної структури залишків води. - швидкість отримання катодів на основі МоО3 методом термовакумної конденсації-солідифікації (1-30 мкм/с) значно перевищує швидкість отримання катодів, описаних в аналогах і прототипі. - отримані катоди володіють високою механічною міцністю, незважаючи на те, що до складу катодної маси не входить сполучне. Це обумовленно тим, що між катодним матеріалом і струмознімачем висока адгезія, а між частками катодного матеріалу висока когезія. Отримані катоди на основі оксидів молібдену мають таку корисну властивість , як низький опір, незважаючи на те, що до складу катодної маси не входить електропровідна добавка. Це пояснюється тим, що отримана структура оксиду молібдену має високу електронну провідність. Високу електронну провідність електродним шарам МоО3, отриманим методом термрвакуумної конденсації-солидификації, забезпечують іони металів, що присутні в структурі осаду у вигляді незначних домішок [7]. У даному випадку висока електронна провідність забезпечується іонами молібдену більш низьких ступенів окислювання [8]. Впровадження таких іонів у катодну структур у забезпечують в момент випару МоО3. У якості матеріалу випарника був використаний металевий молібден. У момент випару невелика частина МоО3 за реакцією диспропорціанування взаємодіє з металевим молібденом з утворенням нижчих оксидів, молекули яких містять іони молібдену більш низьких ступенів окислювання. Частково відновлені іони молібдену з газової фази осаджуються на підкладку-стр умознімач і вбудовуються в кристалічну структур у основної речовини (МоО3) у вигляді домішки, забезпечуючи високу електронну провідність катодного осаду. Основними факторами, що впливають на якість шару електродного матеріалу, є кількість матеріалу, що випаровується, температура випару, час випару, температура субстрату, швидкість охолодження субстрату, об'єм робочої камери. Наступні приклади характеризують новизну та промислову придатність винаходу, який заявляється. Приклад 1 У вакуумній установці для осадження матеріалів в умові конденсації-кристалізації розміщують підкладку з нержавіючої сталі діаметром 20 мм. Поверхню підкладки піддають піскоструминній обробці з глибиною рельєфу 3-4 мкм і наступному іонному очищенню при напрузі на аноді 1,5 кв. Після відкачки робочої камери до залишкового тиску 10-5 TORR порошок МоО3 у кількості 10 мг переводять в пароподібний стан і осаджують на підкладці. Аналіз отриманого покриття показав його низьку адгезію до підкладки, про що свідчили численні ділянки відшарування і розтріскування (табл. 1 п. 1). Приклад 2 В установці, описаній в Прикладі 1, кількість речовини, що випаровується, було збільшено до 15 мг, а об'єм робочої камери зменшений у 2 рази. Випар вихідної речовини проводився при температурі 620°С. Температура підкладки була збільшена до 200°С. Час напилювання -3 секунди. Таким чином, були створені умови для конденсації речовини на підкладці у ви гляді рідкої фази. Рідкий шар МоО3 кристалізувався за допомогою примусового охолодження струменем аргону. Швидкість охолодження складала 10°С/сек. Аналіз отриманого покриття показав, що при товщині 8-10 мкм воно має гарну адгезію до підкладки. Адгезивна міцність визначалася за мінімальним радіусом вигину зразка, при якому на його поверхні виявилися мікротріщини, що доходять до підкладки. Аналіз розтріскування зразка проводився за допомогою растрового електронного мікроскопа. Значення радіуса вигину складало 1,2 мм. Рентгено-структурний аналіз (XRD) отриманого зразка виявив у ньому наявність фаз МоО 2, МоО3, Мо4О 11 (табл. 1 п. 2). Приклад 3 В установці, описаній в Прикладі 2, температура випару речовини була збільшена до 700°С. Температура підкладки складала 100°С. Швидкість охолодження після конденсації рідкого шару була збільшена до 20°С/сек. Аналіз отриманого покриття показав, що за товщиною і адгезивною міцністю воно відповідає аналогічному, описаному в прикладі 2, однак за результатами XRD аналізу має аморфну стр уктур у (табл. 1 п. 3). Приклад 4 В установці, описаній в Прикладі 3, було отримане покриття з вихідного МоО3 при температурі підкладки 130°С. Аналіз отриманого покриття показав, що воно представлено сполукою Мо40ц (табл. 1 п. 4). Приклад 5 В установці, описаній в Прикладі 3, було отримане покриття з вихідного МоО3 при температурі підкладки 160°С. XRD аналіз показав, що склад шару відповідає стехіометрії МоО2 (табл.1 п. 5). Приклад 6 В установці, описаній в Прикладі 3, було отримане покриття з вихідної речовини МоО3 при температурі підкладки 230°С. Товщина шару покриття становить від 0,5 до 430 мкм. Аналіз отриманого покриття показав, що воно .має тонкодиференційовану пластинчасту структур у і відповідає сте хіометрії МоО3 (табл. 1 п. 6). Приклад 7 В установці, описаній в Прикладі 3, було отримане покриття з вихідної речовини МоО3 при температурі підкладки 300°С. Час осадження - 20 секунд. При цьому зразок охолоджувався з боку підкладки зі швидкістю 3°С/сек. Таким чином, був отриманий зразок з товщиною покриття 1,32 мм із пластинчастою структурою МоО3. Середня питома вага отриманого шару МоО3 становила 2,3 г/см . (табл. 1 п. 7). Приклад 8 В установці, описаній в Прикладі 7, було отримане покриття з вихідної речовини МоО3 при температурі підкладки 250 °С. Таким чином, був отриманий зразок з товщиною покриття 1,3 мм із пластинчастою структурою МоО3 . Середня питома вага отриманого шару МоО3 становила 2,73 г/см 3, (табл. 1 п. 8). Приклад 9 В установці, описаній в Прикладі 3, було отримане покриття з вихідної речовини FeS2 при температурі підкладки 40°С. Робочий простір розігрівають до температури 500°С. Вихідну речовину випаровують при 750°С і осаджують на підкладку за 50 секунд. Маса шару складала 1 мг при задовільній адгезії до підкладки. Фазова сполука покриття: Fe9S8 + S monoclinic (табл. 1 п. 9). Приклад 10 В установці, описаній в Прикладі 9, було отримане покриття з вихідної речовини FeS2 при температурі підкладки 40°С. Однак з використанням додаткового випарника в робочий простір подавали пару сірки при температурі 240°С. Випарювання FeS2 проводилося при 800°С. Загальний час напилювання - 51 сек. Маса напиленого шару складала 1,4 мг. Фазовий аналіз дозволяє виявити в напиленому шарі наступні складові: Рез84 - основа, Fe7S8 - до 5 % (табл.1 п. 10). Приклад 11 В установці, описаній в Прикладі 10, було отримане покриття з вихідної речовини FeS2 при температурі підкладки 40°С. Пару сірки вводять при температурі 150°С. Загальний час напилювання - 110 секунд. Маса напиленого шару - 4 мг. Фазовий аналіз покриття показав наступне: Сірка (моноклінна) - 50 %, FeS2 - 5%, Fe3S4 7%, FeS - 30%, S орторомбічна - 8 % (табл.1 п. 11). Приклад 12 В установці, описаній в Прикладі 11, було отримане покриття з вихідної речовини FeS2 при температурі підкладки 40°С. Пару сірки вводять при температурі 190°С. Загальний час напилювання - 50 секунд. Маса покриття - 1,8 мг. Фазова сполука покриття - FeS2 (пірит) -95%, FeS2 (марказит) 5% (табл. 1 п. 12). Приклад 13 На тонку плівку МоО3 , отриману за режимом Прикладу 6 за допомогою вакуумної установки, що припускає конденсацію пароподібної фази з утворенням тонкого шару рідини і її наступну кристалізацію, аналогічно, описаному в прикладі 3, проводили осадження твердого неорганічного електроліту, до складу якого входять оксиди літію, вольфраму та бора. Осадження вели за наступним режимом: вихідний матеріал нагрівають до 900°С за 21 сек і витримують при цій температурі протягом 4-х сек. Надалі температуру піднімають до 1500°С за 4сек. і проводять ізотермічну витримку протягом 2-х сек. При цьому спостерігають повне випарювання вихідної речовини масою 5 мг. Після конденсації речовини у вигляді рідкої плівки на поверхні оксиду молібдену, за допомогою примусового обдування інертним газом протягом 30сек., рідина кристалізується. У процесі охолодження температуру електрода знижують з 200°С до 100°С. Аналіз отриманого на оксиді молібдену покриття товщиною 3 мкм, показав наявність кристалічних фаз Li2WО4, Lі4B10O 17. Стр уктура плівки грубозерниста і характеризується різною товщиною, розкид якої сягає більш ніж 30 %. (табл. 1 п. 13). Приклад 14 На тонку плівку МоО3 , отриману за режимом Прикладу 6 за допомогою вакуумної установки, що припускає конденсацію пароподібної фази з утворенням тонкого шару рідини і її наступну кристалізацію, аналогічно, описаному в прикладі 3, проводилось осадження твердого неорганічного електроліту, до складу якого входять оксиди літію, вольфрама та бора. Осадження проводилось за режимом прикладу 13 з наступними змінами. Вихідну речовину нагрівають до 800°С за 15 сек. і витримують при цій температурі протягом 10 сек. Надалі температура випарника підвищувалася до 1000°С зі швидкістю 45°С/сек. Ізотермічна витримка при цій температурі складала 20 сек. Температура поверхні МоО3 підтримувалася на рівні 40 °С. Аналіз отриманої плівки твердого електроліту, проведений методом рентгеноструктурного і металографічного аналізів, показав його оптичну прозорість і рентгеноаморфну структур у (табл.1 п. 14). Приклад 15 На тонку плівку FeS2, отриману за режимом Прикладу 12 за допомогою вакуумної установки, що припускає конденсацію пароподібної фази з утворенням тонкого шару рідини і її наступну кристалізацію, аналогічно, описаному в прикладі 3, проводилось осадження твердого неорганічного електроліту, до складу якого входять оксиди літію, вольфраму та бора. Осадження проводилось за наступним режимом. Вихідну речовину нагрівають до 1000°С за 10 сек. і витримують при цій температурі протягом 5 сек. Далі температур у випарника підвищують до 1200°С за 2 сек. з наступною ізотермічною витримкою протягом 13 сек. Після її закінчення речовину нагрівають до 1500°С за 10 сек. і витримують при цій температурі 3 сек. Таким чином, загальний час напилення складав 43 сек. За цей час температура поверхні FeS2 лінійно збільшувалася від 20°С до 300°С. Охолодження утвореної на поверхні FeS2 плівки проводилось аналогічно Прикладу 13. Аналіз отриманого покриття показав, що воно має крупнокристалічну стр уктур у з фазовою складом і різнотовщинністю, аналогічно Прикладу 13 (табл.1 п. 15). Приклад 16 На тонку плівку FeS2, отриману за режимом Прикладу 12 за допомогою вакуумної установки, що припускає конденсацію пароподібної фази з утворенням тонкого шару рідини і її наступну кристалізацію, аналогічну, описаній в прикладі 3, проводили осадження твердого неорганічного електроліту, до складу якого входять оксиди літію, вольфраму та бора. Осадження проводили за режимом Прикладу 15 з наступними змінами. Нагрівання вихідної речовини у випарнику проводили в такий спосіб: температуру підвищували до 1000°С за 10 секунд і надалі, після 5-ти секундної ізотермічної витримки, до 1200°С - за 5 секунд. Ізотермічна витримка при цій температурі складала 15 секунд, після чого температур у стрибкоподібне піднімали до 1500°С, при якій матеріал витримали протягом 3-х секунд. Таким чином, загальний час напилювання складав 38 секунд. За цей час температура поверхні FeS2 лінійно зростала з 20 до 300°С. Охолодження утвореної на поверхні FeS2 плівки проводили аналогічно Прикладу 15. Аналіз отриманої плівки твердого електроліту, проведений методом рентгеноструктурного і металографічного аналізів, показав його оптичну прозорість і рентгеноаморфну стр уктур у. Товщина покриття складала 4 мкм (табл. 1 п. 16). Приклад 17 Отриманий у прикладі 8 електрод поміщають у корпус джерела струму дискової конструкції, що містить літієвий негативний електрод і рідкий апротонний електроліт. При цьому поверхня струмознімача, на яку нанесений катодний матеріал, розвинена. Герметизують джерело струму і проводять його випробування вимірюють його розрядну ємність. При розряді елемента питома розрядна ємність на одиницю ваги катода досягає 300 мА.г/г. Це становить 819 мА.г/см 3 катода. Товщина шару такого електрода становить 1,3 мм (табл. 2 п. 3). Приклад 18 Два електрода, які отримані по режиму прикладу 8, розміщують у корпусі джерела струму призматичної конструкції з ламінованої алюмінієвої фольги, що містить літієвий негативний електрод і рідкий апротонний електроліт. Товщина шару одного такого электрода становить 1,4 мм. Питома вага МоО3 зменшується в напрямку від струмознімача, на який наноситься шар оксиду, до зовнішньої поверхні оксиду молібдену. У реальному джерелі струму зовнішня межа МоО3 граничить з електролітом. Питома вага оксиду молібдену зменшується від 3,9 г/см 3 на межі зі струмознімачем до 2,1 г/см 3 на зовнішній поверхні МоО3. Герметизують джерело струму і проводять його випробування - вимірюють його розрядну ємність. При розряді питома об'ємна ємність елементу складає 466 мА.г/см 3. При цьому розрядна ємність катоду на одиницю ваги МоО 3 досягає 300 мА.г/г. Це становить 800 мА.г/см 3 катода, (табл. 2 п. 5). Приклад 19 Отриманий у прикладі 6 електрод розміщують у корпусі дискового чи призматичного джерела струму з ламінованої алюмінієвої фольги, що містить літієвий негативний електрод і неводний електроліт. Герметизують джерело струму і проводять його випробування - вимірюють його розрядну ємність. При розряді елемента розрядна ємність електрода на першому циклі складає 260 - 300 мА.г/г катода. При розряді на другому і наступному циклах (до 95 заряд-розрядних циклів) питома ємність складає від 230 до 90 мА.г/г. катода. Товщина шару катода при цьому становить від 0,5 до 80 мкм (табл. 2 п. 6, 7). Приклад 20 На поверхнюотриманого в прикладі 6 електрода виливають розчин полімерного електроліту. Видаленням легкокипучого розчинника формують на поверхні електрода плівку полімерного електроліту. Змочивши поверхню негативного електрода і полімерного електроліту рідким апротонним електролітом, складають електродну структур у. Електродну структур у розміщують у корпусі елемента і герметизують. Проводять випробування виготовленого елементу - вимірюють його розрядну ємність. При розряді елемента розрядна ємність електрода на першому циклі складає 280 - 300 мА.г/г катода. При розряді на другому і наступному циклах (до 120 зарядрозрядних циклів) питома ємність складає від 230 до 100 мА.г/г. Товщина шару катода при цьому становить від 0,5 до 80 мкм (табл. 2 п. 8, 9). Приклад 21 Електрод, виготовлений за прикладом 14, розміщують у корпусі елемента. На поверхню плівки твердого електроліту накладають сепаратора просочений рідким електролітом. Збирання електродної структури завершують негативним літієвим електродом, після чого елемент герметизують. Проводять випробування виготовленого елементу - вимірюють його розрядну ємність. При розряді елемента розрядна ємність електрода на першому циклі складає 390 мА.г/г катода. При розряді на другому і наступному циклах (до 500 зарядрозрядних циклів) питома ємність складає від 300 до 140 мА.г/г катода. Товщина шару катода при цьому становить 2 мкм (табл. 2 п. 10). Приклад 22 Отриманий у прикладі 12 електрод розміщують у корпусі дискового чи призматичного джерела струму з ламінованої алюмінієвої фольги, що містить літієвий негативний електрод і неводний електроліт. Герметизують джерело струму і проводять його випробування - вимірюють його розрядну ємність. При розряді елемента розрядна ємність електрода на першому циклі складає 850 мА.г/г катоду. При розряді на другому і наступному циклах електрод електрохімічної активності не виявляв (табл. 2 п. 11). Приклад 23 На поверхню отриманого в прикладі 12 електрода виливають розчин полімерного електроліту. Видаленням легкокипучого розчинника формують на поверхні електрода плівку полімерного електроліту. Змочивши поверхню негативного електрода і полімерного електроліту рідким апротонним електролітом, складають електродну структур у. Електродну структур у розміщують у корпусі елементу і герметизують. Проводять випробування виготовленого елементу - вимірюють його розрядну ємність. При розряді елементу розрядна ємність електрода на першому циклі складає 850 мА.г/г катоду. При розряді на другому і наступному циклах електрод електрохімічної активності не виявляв (табл. 2 п. 12). Приклад 24 Електрод, виготовлений за прикладом 16, розміщують у корпусі елемента. На поверхню плівки твердого електроліту накладають сепаратор, просичений рідким електролітом. Складання електродної структури завершують негативним літієвим електродом, після чого елемент герметизують. Проводять випробування виготовленого елементу - вимірюють його розрядну ємність. При розряді елемента розрядна ємність електрода на першому циклі складає 850 мА.г/г катода. При розряді на другому і наступному циклах (до 60 заряд-розрядних циклів) питома ємність складає від 450 до 300 мА.г/г. Зміна питомої ємності від кількості заряд-розрядних циклів, де представлена система FeS2 (2 мкм) - твердий електроліт ( 4 мкм) - рідкий електроліт - Li, наведена на фіг. 1. (табл. 2 п. 13). Приклад 25 Для катода на основі оксиду молібдену, отриманого за описаним вище методом, розрядна ємність не залежить від товщини катодного матеріалу в діапазоні товщин МоО3 від 2 до 1330 мкм. Питома розрядна ємність зменшується тільки на 20% при збільшенні щільності струму в шість разів від 0,8 мА/см 2 до 5,0 мА/см 2, як це наведено на фіг. 2. Приклад 26 На декілька струмознімачів наносять шари МоО3 різної товщини. Потім досліджують адгезивну міцність катодного шару до поверхні струмознімача. Адгезивна міцність визначалася за мінімальним радіусом вигину зразка, при якому на його поверхні виявилися мікротріщини, що доходять до підкладки. Аналіз розтріскування зразка проводився за допомогою растрового електронного мікроскопа. Видно, що при товщині, катодного покриття більше 430 мкм радіус вигину електрода при збереженні його механічних властивостей складає усього 3,9 мм. Ці результати отримані для електродів, що не містять сполучного в складі катодного матеріалу. Результати дослідження механічної міцності, адгезії і когезії електродів на основі оксиду молибдена, отриманих за прикладом 6 показано на фіг. 5. Приклад 27 На декілька струмознімачів наносять шари МоО3 різної товщини. Методом морфологічного аналізу за результатами дослідженнь на скануючому електронному мікроскопі виявили залежність аморфизованності структури оксиду при збільшені товщини електрода. Збільшення товщини електрода супроводжується зменшенням аморфизованності структури МоО3 . Це видно з фіг. 6. Приклад 28 При збільшенні товщини МоО3, щільність шару активного матеріалу катоду і його структура змінюються у напрямі від межі розділу струмознімач/активний матеріал катоду до межі розділу активний матеріал катоду/неводний електроліт таким чином, що на межі розділу струмознімач/активний матеріал катоду щільність активного матеріалу вище, ніж на межі розділу активний матеріал/рідкий електроліт. При цьому щільність може змінюватися на величину 2 г/см 3 по товщині електрохімічне активного шару МоО3 до 1,4 мм. Зміна питомої ваги МоО3 по товщині катоду, отриманого методом термовакуумної конденсації-солідифікації представлена на фіг. 7. Приклад 29 Два електрода, які отримані за режимом прикладу 8, розміщують у корпусі джерела струму призматичної конструкції з ламінованої алюмінієвої фольги, що містить літієвий негативний електрод і рідкий апротонний електроліт. Товщина шару одного такого електрода становить 1,3 мм. Питома вага МоО3 зменшується в напрямку від струмознімача, на який наноситься шар оксиду, до зовнішньої поверхні оксиду молібдену. У реальному джерелі струму зовнішня межа МоО3 граничить з електролітом. Питома вага оксиду молібдену зменшується від 3,9 г/см 3 на межі зі струмознімачем до 2,1 г/см 3 на зовнішній поверхні МоО3. Герметизують джерело струму і проводять його випробування - розряджають на 10 % від номінальної розрядної ємності током, при якому катодна щільність струму складає 0,45 мА/см 2, витримують у вимкненому стані протягом 1 доби, після чого досліджують його імпедансні характеристики за допомогою метода електродного імпеданса. Зі спектру, представленого в координатах R -1/w.C, вираховують електронну компоненту, опір якої майже повністю відноситься до катодного шару МоО 3. Було встановлено, що питома електронна провідність (Ge) електродного шару на основі МоО3, лінійно зростає в першій третині розрядної ємності з 3,5.10-3 Ом -1.см-1 до 1,2.10-2 0м -1•см -1, після чого мало залежить від ступеню розряду. Зміна питомої електронної провідності шару МоО 3 від ступеня розряду електрода проставлена на фіг. 8. Приклад 30 Зразок джерела струму виготовлений у такий спосіб. Катод на основі оксиду молібдену отримай методом термовакумної конденсації-солідифікації, описаним у прикладі 6. Товщина шару МоО3 від 30 до 170 мкм. Питома вага шару МоО3 від 3,0 до 3,6 г/см 3. Оксид молібдену нанесен на струмознімач з алюмінієвої фольги товщиною 20 мкм. Катод покритий шаром твердого неорганічного електроліту, отриманого за прикладом 13. Товщина твердого електроліту 4 мкм. Літієвий анод також виготовлений методом термовакумної конденсації-солідифікації. Товщина літієвого анода до 55 мкм. Струмознімачем для літієвого анода служить мідна фольга товщиною 10 мкм. Розрядна ємність катода до 360 мА.г/г. Робочий діапазон щільності струму до 5 мА/см 2(табл. 2 п. 14). Приклад 31 Зразок призматичного первинного літієвого джерела струму з рідким електролітом виготовлений на основі МоО3 , отриманого за прикладом 8. Елемент містить наступні компоненти: два катоди на основі МоО3, отримані методом конденсації-солідифікації. Середня питома вага катодного матеріалу - 2,66 г/см 3. То вщина катодного матеріалу на одному МоО3-електроді складає 1,25 мм. Геометричні розміри електродів - 2 х (1,5 х 1,5) см. Катодний струмознімач - алюмінієва фольга з розвиненою поверхнею і товщиною 20 мкм. Товщина сепаратора 25 мкм. Струм розряду - 2 мА. Перед тестуванням джерело струму зберігалося протягом 4 місяців. Розрядна ємність елемента - 475 мАт. Питома розрядна ємність катода -317 мА.г/г. Це становить 843 мА.г/см 3. Питома енергія на об'єм електродної структури 1307 Вт.г/л (табл. 2 п. 15). Приклад 32 Зразок призматичного вторинного джерела струму на основі МоО3, отриманого за прикладом 8. Джерело струму містить наступні компоненти: два катоди на основі оксиду молібдену, отриманного методом конденсаціїсолідифікації. Середня питома вага катодного матеріалу становить 3,66 г/см 3. Товщина шару МоО 3 на катоді - 85 мкм. Геометричні розміри електрода: 2 х (1,2 х 1,2) см. Катодний струмознімач - алюмінієва фольга товщиною 20 мкм. Катод покритий шаром твердого неорганічного електроліту товщиною 5 мкм. Твердий неорганічний електроліт має питому електропровідність по катіонах літію 10-5 См/см при кімнатній температурі. Твердий неорганічний електроліт був нанесений методом термовакуумної конденсації-солідифікації за прикладом 14. Сепаратор, товщиною 25 мкм, просочений рідким неводним електролітом. Металевий літій як анод. Елемент був випробуваний у наступному режимі: струм розряду - 0,3 мА; струм заряду - 0,15 мА. Перед тестуванням елемент зберігався два місяці. Результати тестування елемента: розрядна ємність -27 мАт; питома ємність катода - 305 мА.г/г. Питома об'ємна ємність катода становить 1116 мА.г/дм 3. Питома об'ємна енергія на електродну структуру 870 Вт.г/см 3. (табл. 2 п. 16). Приклад 33 Отриманий у прикладі 7 електрод поміщають у корпус джерела струму дискової конструкції, що містить літієвий негативний електрод і рідкий апротонний електроліт. При цьому поверхня струмознімача, на яку нанесений катодний матеріал, розвинена. Герметизують джерело струму і проводять його випробування вимірюють його розрядну ємність. При розряді елемента розрядна ємність катода досягає 300 мА.г/г. Це становить 690 мА.г/см 3 катода. Товщина шару такого МоО 3-електрода становить 1,32 мм (табл. 2 п. 1). Приклад 34 Отриманий у прикладі 8 електрод поміщають у корпус джерела струму дискової конструкції, що містить літієвий негативний електрод і рідкий апротонний електроліт. При цьому поверхня струмознімача, на яку нанесен катодний матеріал, гладка. Товщина шару такого електрода становить 1,3 мм. МоО3 відшаровувався від гладкої поверхні струмознімача навіть після незначного струсу (табл. 2 п. 2). Приклад 35 Два електрода, які отримані за режимом прикладу 7, розміщують у корпусі джерела струму призматичної конструкції з ламінованої алюмінієвої фольги, що містить літієвий негативний електрод і рідкий апротонний електроліт. Товщина шару одного електроду становить 0,9 мм, другого електроду становить 1,0 мм. Середня питома вага МоО3-катода складає 1,5 г/см 3. Герметизують джерело струму і проводять його випробування вимірюють його розрядну ємність. При розряді елемента питома розрядна ємність катода складає 300 мА.г/г. При цьому питома об'ємна ємність катода складає 450 мА.г/см 3 (табл. 2 п. 4). Як доказ корисності та промислової придатності запропонованого винаходу є наведені на фіг. 3 та 4 конструкції батарей. Батарея дискової конструкції (фіг. 3), складається з 1 - Корпус елементу. 2 - Струмовивід катоду. 3 - Катод. 4 - Струмовивід аноду. 5 - Анод (металевий літій). 6 - Сепаратор. 7 - Кришка. 8 Поліпропіленова прокладка. Батарея призматичної конструкції, яка приведена на фіг. 4, складається з 1 - Корпус елементу. 2 – Стр умовивід катоду. 3 - Катод. 4 - С трумовивід аноду. 5 - Анод (металевий літій). 6 - Сепаратор. 7 Зварювальні шви. Приклади № 1-35 ілюструються результатами, представленими в таблицях 1,2. Література: 1. И. А. Кедринський, В. Е. Дмитренко, Ю. М. Поваров, И. И. Гр удянов. Хімічні джерела струму з літієвим електродом. - Красноярськ.: Красноярський університет., 1983 р, С. 95. 2. В. М. Нагірний, Р. Д. Апостолова, А. С. Баскевич, Е. М. Шембель. Електролітичне отримання оксидів молібдену // Журнал прикладної хімії, 2000, № 3, С. 406 - 409. 3. U.S. 4,572,873 / February 25, 1986 /. Kanehori et al. 4. Верещагина И. С., Ти хонов К. И., Ротинян А. Л. Електрохімічна поведінка плівок окислу молібдену у пропіленкарбонаті // Електрохімія. - 1981 г. - Т. 17. - № 5. - С. 783 - 787. 5. Молибден. Сборник. Издательство иностранной литературы. Под. ред. А. К. Натансона. Москва, 1959 г. С. 304. 6. Краткий справочник химика. Изд. 6, М, 1963. 7. В. А. Дубок, Е. С. Ко тенко. Хімія і фізика напівпровідників. Київ, «Вища школа», 1973, С. 287. 8. Самсонов Г. В., Буланкова Т. Г., Бурыкина А. Л. и др. Физико-химические свойства окислов. Справочник. Изд-во «Маталлургия», 1969, С. 273. Таблиця 1 Темп ер Шв идкість Темп ера № Вага ату ра Час охолодж ен ту ра при в ипареної підкла д в ипаровув ня ки кла речов ини, в ипарову су бстрату , ання, сек. ду г в ання, °С (су бстр °С/сек ату ) °С Об'єм робочо ї камери, Інші у мов и Адге зія матеріалу до су бстрату XRD-ана ліз амор фнокристалічна( Мо 4 О11) МоО 2, МоО 3,Мо4 О11 Амор фна стру кту ра Примітка Низька адге зія до су бстрату 1 10 10 . -3 650 3 20 2 х 2 15 10 . -3 620 3 200 10 х/2 Добра 3 15 10 . -3 700 3 100 20 х/2 Добра 4 15 10 . -3 700 3 130 20 х/2 Погана Мо4 О11 5 . 15 10 -3 700 3 160 20 х/2 Погана МоО 2 Вітсу тній МоО3 6 15 10 . -3 700 3 230 20 х/2 Добра МоО 3 Заяв лені у мов и 7 0,9 700 20 300 3 х/2 Добра МоО 3 8 0.91 700 20 250 3 х/2 Добра МоО 3 Добра Fe9S8+S monoclinic Відсу тній FеS2-пірит Добра Fe3S4+Fe7 S8 Відсу тній FeS2 - пірит Добра Smonoclinic+ort oromb., FeS2, Fе3S4, FeS Низький в міст FeS2піриту Добра FeS2-nipi T (95 %)+FeS2марказ ит Заяв лені у мов и Добра Включеннякр ист алічних фаз Li2WО4, Li4B1 0O17, плів ка гру бозерниста, різної тов щини Низька якість плів ки тв ердого елек троліту Погана Низький в міст МоО3 у складі актив ної маси. Низькі електрохі мічні характеристик и Низькі електрохі мічні характеристик и Низька питома в ага МоО 3 Заяв лені у мов и Темп е 9 . -3 15 10 750 50 40 х/2 10 15 10 . -3 800 51 40 х/2 11 15 10 . -3 800 110 40 х/2 12 . -3 13 15 10 . -3 5 10 800 900/1500 50 31 40 200 3,3 рату ра рабочогопрост ору 500°С Темп ерату ра робочого простору 240 °С, прису тність парів сірки Темп ерату раро бочогопр остор у 150 °С,прису тність парів сірки х/2 Темп ерату ра робочогопрост ору 190 °С,прису тність паров сірки х/2 Стадійнен агрів ання при в ипаровув анні речов ини . -3 800/1000 50 40 х/2 Стадійне нагрів анняприв ипаровув анні речов ини Добра Рентге ноамор фна,оптич нопрозора плів ка Заяв лені у мов и . -3 1000/120 0/ 1500 43 20/300 3,3 х/2 Стадійне нагрів анняприв ипаровув анні речов ини Добра Кру пнокристалічнап лів ка різноїтов щини Низька якість плів ки тв ердого елек троліту . -3 1000/120 0/1500 38 20/300 х/2 Стадійнен агрів анняприв ипаро вув анні речов ини Добра Рентге ноамор фна,оптич нопрозора плів ка Заяв лені у мов и 14 5 10 15 5 10 16 5 10 Таблиця 2 . В № 1 № при кла ду 33 ипарову ємий матеріа л МоО 3 Тов щи на катода, мкм 1320 Питома в ага шару катода, 3 г/см 2,3 Розрядна ємність катода, мАг /г / 3 мАг/см Конс тру кція корпу су Пов ерхня стру мознім ача Електр оліт 1-йцик л 10йцикл 30йцикл 100йцикл Примітка елеме нта Д исков а Розв инена Рідкий 300/690 2 34 МоО 3 1300 2,8 Д исков а Гладка Рідкий 3 17 МоО 3 1300 2,73 Д исков а Розв инена Рідкий 300/819 4 35 МоО 3 1900 1.5 Призматична Розв инена Рідкий 300/450 5 18 МоО 3 1400/1 400 2,1-3,9 Призматична Розв инена Рідкий 300/800 6 19 МоО 3 2,5 3,2 Д исков а Гладка Рідкий 260 182 151 121 7 19 МоО 3 25 3,28 Д исков а Гладка Рідкий 300 113 90 8 20 МоО 3 2 3,2 Д исков а Гладка Полімерн ий 284 166 126 100 9 20 МоО 3 11 3,2 Д исков а Гладка Полімерн ий 313 134 100 10 21 МоО 3 2 3,2 Д исков а Гладка Тв ердий/Рід кий 390 240 200 140 11 22 FeS2 2 4,5 Д исков а Гладка Рідкий 850 Низька розрядна ємність. Питома в ага катоду нижчезаяв лено ї межи. Відша рув ання катоду в ідстру мознімача Нев иконання заяв леної ме жі. Заяв лені в ластив ості елеме нту . Низька розрядна ємність. Питома в ага катоду нижчезаяв лено ї межі. Заяв лені в ластив ості елеме нту . Заяв лені в ластив ості елеме нту . Заяв лені в ластив ості елеме нту . Заяв лені в ластив ості елеме нту . Заяв лені в ластив ості елеме нту . Заяв лені в ластив ості елеме нту . Низькі оборотні електр охімічні характеристик и 12 23 FeS2 2 4,5 Д исков а Гладка Полімерн ий 850 13 24 FeS2 2 4,5 Д исков а Гладка Тв ердий/Рід кий 850 328 322 175 14 30 МоО 3 30-170 3,0-3,6 Призматична Гладка Тв ердий/Рід кий 360 15 31 МоО 3 1250 2,66 Призматична Розв инена Рідкий 317/843 16 32 МоО 3 85 3,66 Призматична Гладка Тв ердий/Рід кий 305/111 6 Низькі оборотні електр охімічні характеристик и Заяв лені в ластив ості елеме нту . Заяв лені в ластив ості елеме нту . Заяв лені в ластив ості елеме нту . Заяв лені в ластив ості елеме нту .
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for producing a lithium battery
Автори англійськоюShembel' Olena Moiseivna, Novak Petro Yakovych
Назва патенту російськоюСпособ изготовления литиевой батареи
Автори російськоюШембель Елена Мойсеевна, Новак Петр Яковлевич
МПК / Мітки
МПК: H01M 4/06
Мітки: літієвої, батареї, одержання, спосіб
Код посилання
<a href="https://ua.patents.su/11-72728-sposib-oderzhannya-litiehvo-batare.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання літієвої батареї</a>
Попередній патент: Пристрій запалення пальної суміші у циліндрах двигуна внутрішнього згорання
Наступний патент: Спосіб одержання фтороапатиту
Випадковий патент: Спосіб запобігання раптових викидів вугілля та газу