Спосіб роботи низькотемпературного банку біологічних об’єктів
Номер патенту: 49759
Опубліковано: 16.09.2002
Автори: Лобинцева Галина Степанівна, Гладких Юрий Васильович, Гладких Володимир Юрьович, Лобинцев Дмитро Валерьйович
Формула / Реферат
Композиція вуглеводневого палива на основі бензину марки А-76, що містить метил-трет-бутиловий ефір, яка відрізняється тим, що вона додатково містить антидетонаційну добавку на основі ароматичних амінів, добавку етанольну паливну і компонент моторного палива ароматичний або сольвент нафтовий при нижчезазначеному співвідношенні компонентів, мас. %:
антидетонаційна добавка на основі ароматичних амінів
0,4-1,0
добавка етанольна паливна
4,0-7,0
компонент моторного палива ароматичний або сольвент нафтовий
5,0-10,0
метил-трет-бутиловий ефір
3,0-5,0
бензин марки А-76
до 100
Текст
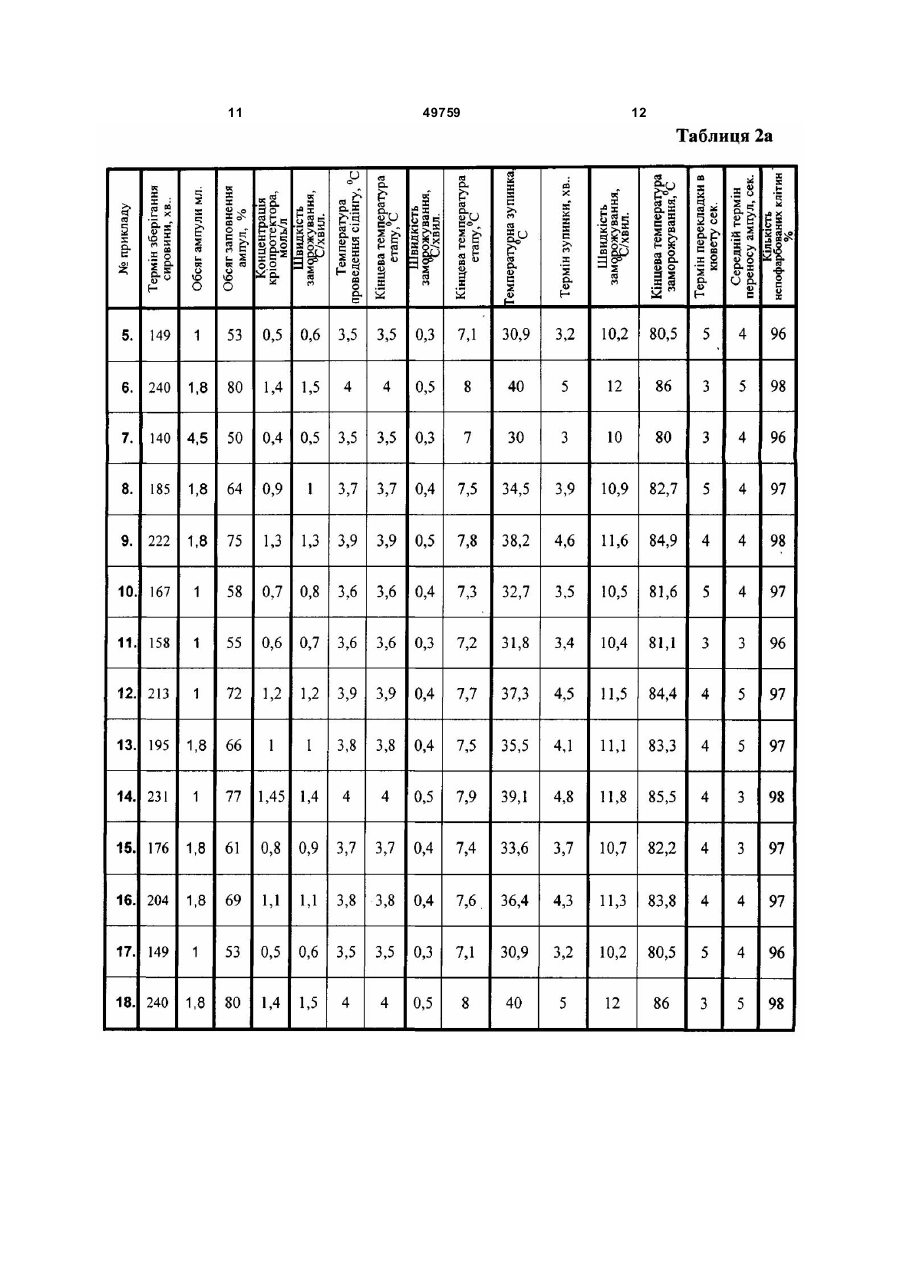
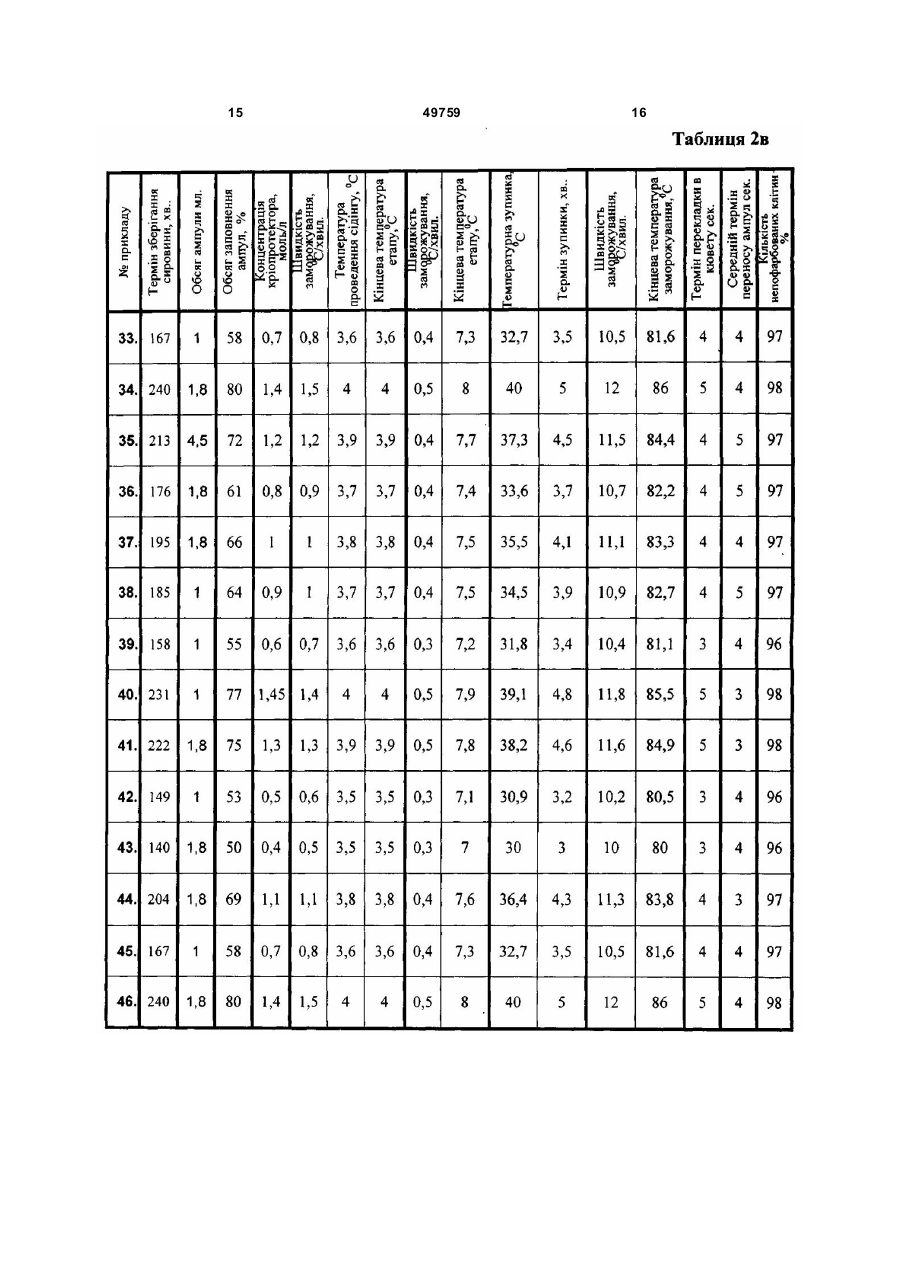
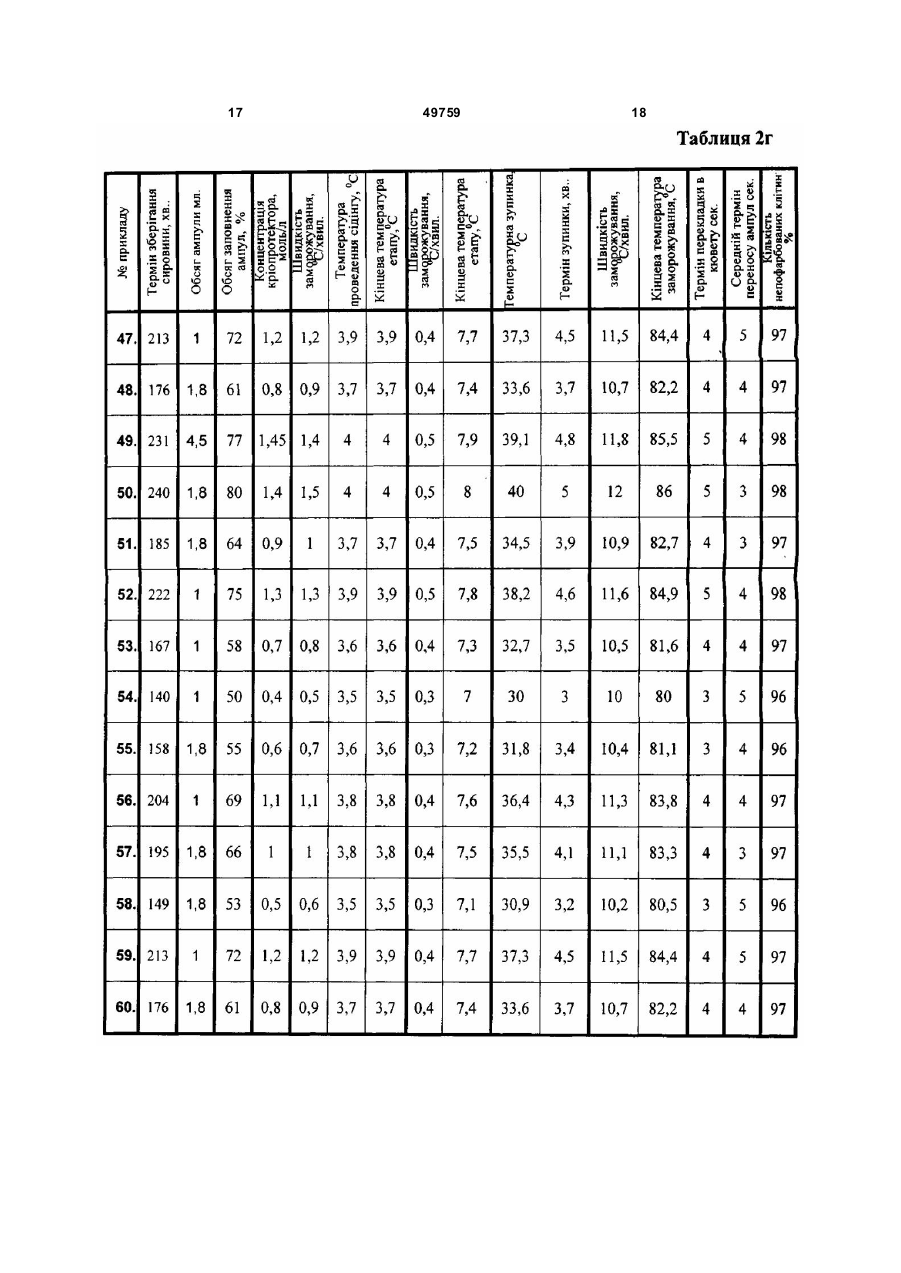
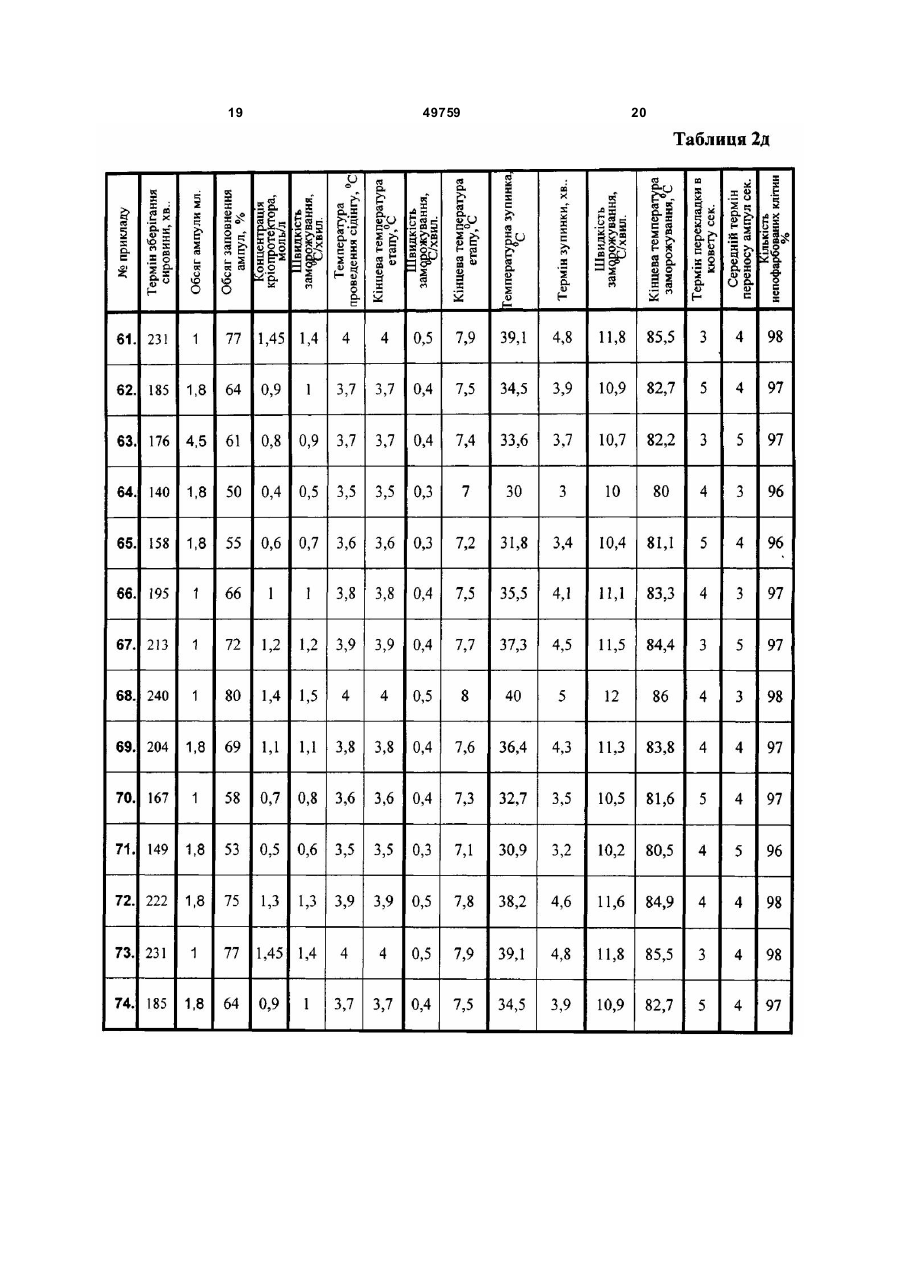
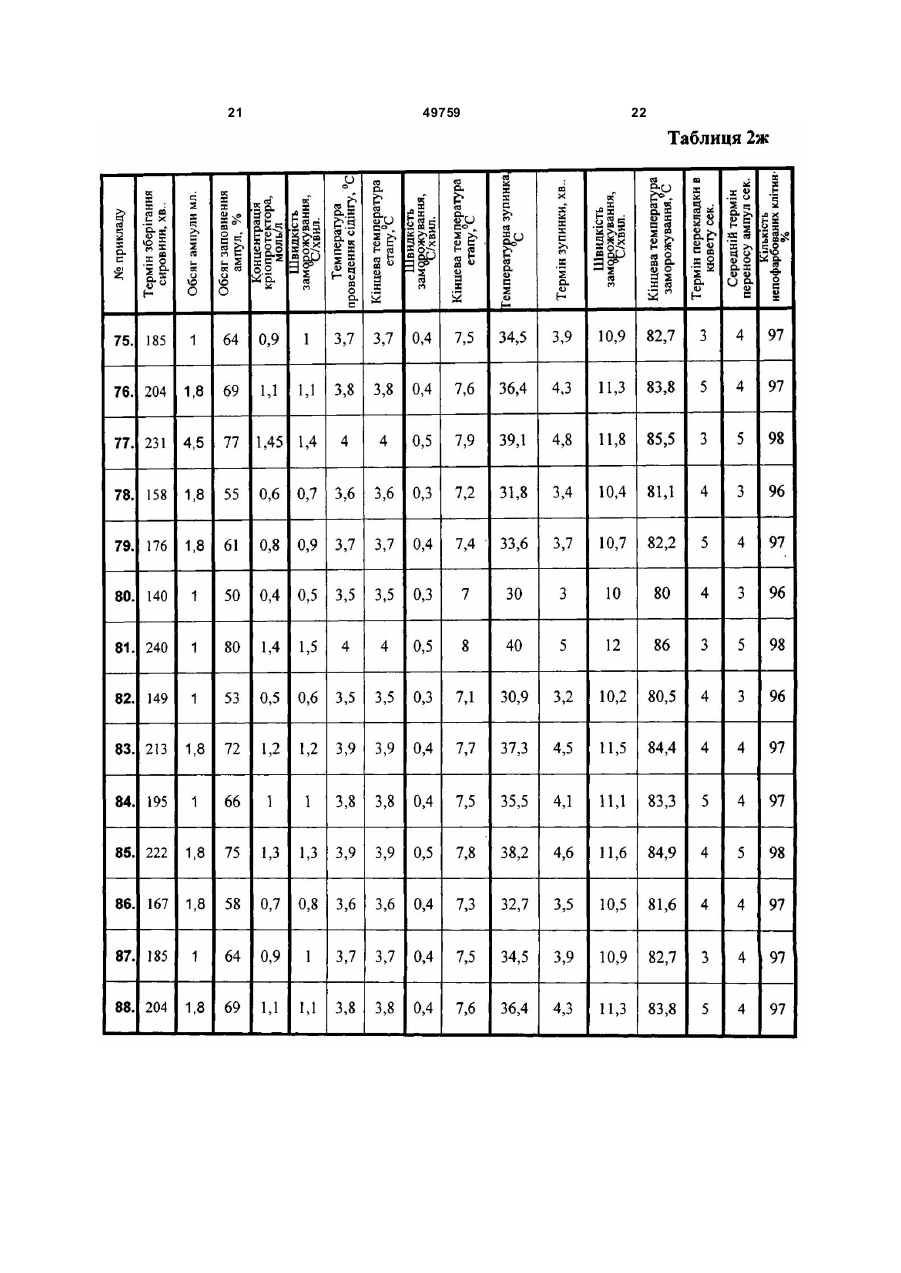
Спосіб роботи банку кріоконсервованих біологічних об'єктів, який передбачає розміщення зразка біологічних середовищ у спеціальній ємності, додавання кріоконсерванту, розфасування зависі клітин в контейнери (ампули), програмне заморожування середовища в контейнері, розміщення контейнера з замороженим середовищем у сховищі, збереження контейнера із середовищем при низькій температурі, вилучення контейнера зі схови ща, розморожування середовища в контейнері для наступного використання, який відрізняє ться тим, що для збереження в банку застосовують отримані в клінічних установах біооб'єкти, які поміщають у стерильний фізіологічний розчин з антибіотиком і зберігають при кімнатній температурі не більш 4 годин із моменту одержання до кріоконсервування в банку, а як ємність для збереження використовують ампули об’ємом 1,8 - 4,5 мл, ампули заповнюють на 50 - 80 % і вставляють в касети для A 2 49759 1 3 49759 4 мембрани, заморожування середовища в суспензій при температурі рідкого азоту практично контейнері, розміщення контейнера з не здійснює додаткової пошкоджуючої на них дії, замороженим середовищем у сховище, однак у роботі банку заморожені біооб'єкти не збереження контейнера із середовищем при можуть постійно зберігатися до моменту низькій температурі, вилучення контейнера зі використання без виконання в банку над ними схови ща, розморожування середовища в ряду технологічних операцій, наприклад по контейнері, часткове видалення рідкого розморожуванню зразків для бактеріологічного середовища з контейнера з використанням контролю, для вірусного та мікоплазмового електроосмотичної мембрани, для наступного контролю, для культивування, вилучення зразків використання залишку середовища. для клінічного використання . Недоліком зазначеного способу є те, що його Внаслідок цих дій не тільки вибраний операції вузькоспецифічні для збереження крові і контейнер а і вся укладка частково при використанні в способі інших біооб'єктів не розморожується. При цьому навіть короткочасне забезпечується необхідні якісні характеристики (протягом 1-2хвил.) перебування матеріалу при після завершення процесу їх збереження в банку. кімнатній температурі викликає нагрівання Недоліком зазначеного способу є те, що контейнера до температури - 100°С і вище. При застосований у ньому одноетапний режим даній температурі в замороженій системі із заморожування травматичний для інших більшістю кріопротекторів, вже відбуваються біооб'єктів людини тому що швидке зниження фазові переходи, і чим скоріше протікає фазовий температур викликає швидкий зріст великих перехід, тим сильніше система відходить від кристалів які порушують оболонки клітин. рівноважного стана. У цей період у зразках Відсутність контролю за процесом розвиваються фізичні явища, що призводять до кристалізації не забезпечує стабільності рекристалізації, утворення мікро - і макро тріщин, характеристик біооб'єктів, які зберігаються в банку. появі нескомпенсованих зарядів і електричних Спосіб передбачає використання в якості полів, що викликають механічні й електричні кріопротектора гліцерину що ускладнює процедуру ушкодження клітинних мембран об'єктів що клінічного застосування, тому що потребує його зберігаються. видалення, наприклад, перед уведенням клітин У такому способі зазначені технологічні пацієнту. процеси роботи банку повинні бути організовані Найбільш близьким до заявленого за певним чином для того, щоб виключити зазначені ознаками є спосіб роботи банку кріоконсервованої процеси, які істотно знижують життєздатність крові (див. заявку Росії 99126524/14, МПК об'єктів, що зберігаються в банку. A01N1/02, дата публ. заявки: 2001.08.27) який Завданням винаходу є створення способу передбачає видалення надлишку плазми роботи низькотемпературного банку біологічних центрифугуванням і наступним ресуспендуванням об'єктів у якому шляхом зміни знайдених суспензії і додаванням кріопротектора, при цьому емпіричним шляхом режимів роботи банку, підготовку до консервування здійснюють у використовуваної сировини, допоміжних речовин, полімерному контейнері, який поміщають у пенал обладнання, та дій з його використанням холдер у вигляді гофрованого алюмінієвого забезпечується покращення умов збереження контейнера, заморожування проводять при середовищ, збільшення періоду збереження та температурі -80°, збереження здійснюють у цій же підвищення кількості життєздатних клітин тарі, вилучення контейнера зі сховища, середовищ, що зберігаються після періоду розморожування середовища в контейнері, збереження. часткове видалення рідкого середовища з Спосіб роботи низькотемпературного банку контейнера, для наступного використання залишку біологічних об'єктів передбачає розміщення зразка середовища. біологічних середовищ у спеціальну ємність, Недоліком зазначеного способу є те, що його додавання кріоконсерванту, розфасування операції вузькоспецифічні для збереження крові і біологічних середовищ в контейнери, при використанні в способі інших біооб'єктів не заморожування середовища в контейнері, забезпечуються необхідні якісні характеристики розміщення контейнера з замороженим після завершення процесу їх збереження в банку. середовищем у схови ще, збереження контейнера Недоліком зазначеного способу є те, що із середовищем при низькій температурі, застосований у ньому одноетапний режим вилучення контейнера зі сховища і заморожування травматичний для інших розморожування середовища в контейнері. біооб'єктів людини тому, що швидке зниження Новим в способі є те, що для збереження в температур викликає швидкий зріст великих банку застосовують отримані в клінічних установах кристалів які порушують оболонки клітин. біооб'єкти, які поміщають у стерильний Відсутність контролю за процесом фізиологічний розчин з антибіотиком і зберігають кристалізації не забезпечує стабільності при кімнатній температурі не більше 4 годин із характеристик біооб'єктів, які зберігаються в банку. моменту одержання до кріоконсервування в банку, Спосіб передбачає використання 5% в якості ємності для збереження (контейнера) концентрації кріопротектора диметилацетамида і використовують ампули обсягом 1,8÷4,5мл., потребує збільшених розмірів контейнерів та ампули заповнюють на 50÷80% і вставляють в схови щ банку і ускладнює наступне використання касети для заморожування, застосовують збережених біооб'єктів. концентрації кріопротектора диметилсульфоксиду Довготривале збереження біологічних (далі ДМСО) 0,4÷1,45моль/л, заморожування 5 49759 6 здійснюють у три етапи, при цьому на першому запропонованим способом здійснювали однаково. етапі з швидкістю 0,5÷1,5°С/хв. до -3,5÷-4°С, з Використовували в прикладах суспензії клітин, застосуванням сідінгу при температурі -3,5÷-4°С, що містять ядро, а саме, суспензії клітин плодових на другому етапі зі швидкістю 0,3÷0,5°С/хв. до -7÷тестисів, суспензії нервових клітин, суспензії клітин 8°С, після цього етапу здійснюють температурну гепатоцитів, суспензії клітин кардиоміоцитів, зупинку при -30÷-40°С протягом 3÷5хв., а на суспензії клітин підшлункової залози, суспензії третьому етапі - зі швидкістю 10÷12°С/хв. до -80÷гемопоетичних клітин крові. 86°С, після заморожування касету з ампулами Отримані в клінічних установах біооб'єкти витягають з камери для заморожування і поміщали у стерильний фізіологічний розчин з переносять (протягом 3÷5сек.) в кювету з рідким антибіотиком (гентамицин, канамицин) і зберігали азотом, в яку попередньо занурюють іншу касету при кімнатній температурі не більш 4 годин із для збереження ампул і, послідовно, переносять моменту одержання до кріоконсервування в банку, кожну ампулу протягом 3÷5сек. в касету для В Таблиці 1 зазначені режими виконання збереження ампул, касету для збереження прикладів 1-4 за прототипом. переносять у схови ще біологічних продуктів , В прикладах за прототипом не вставляють в укладку і занурюють у рідкий азот, використовували суспензії клітин плодових процес вилучення зразків об'єктів для визначення тестисів, суспензії нервових клітин, суспензії клітин якісних характеристик об'єктів, що зберігаються, кардиоміоцитів тому, що без досліджень зрозуміло здійснюють шляхом вилучення касети з що зазначений спосіб роботи необхідною партією ампул і занурення її в кювету з низькотемпературного банку непридатний для цих рідким азотом, наступного вилучення окремих клітин внаслідок того, що дуже малі обсяги ампул з касети, для перевірки якості, після чого суспензій (1-5мл), навіть при використанні касету знову вставляють в сховище, по найменшого контейнеру за способом для їх результатах перевірки якості касети з клітинами, збереження в 50мл., після технологічних операцій які мають вірусне чи мікоплазмове забруднення, в банку по перевірці їх якісних характеристик вилучають зі сховища. продукт в контейнері, який отримано від одного Внаслідок використання зазначеного способу донора вже непридатний для подальшого його операції прийнятні для збереження широкого зберігання в банку. переліку біооб'єктів і при цьому забезпечується їх В прикладах за прототипом в зв'язку з необхідні якісні характеристики після завершення відсутністю відповідної регламентації не процесу їх збереження в банку. витримували зазначений в розробленому способі Перевагою способу є те, що застосований у режим збереження сировини (не більше 4 годин). ньому режим заморожування не травматичний для В якості кріоконсерванта використовували 5% клітин біооб'єктів тому, що емпірично підібране диметилацетамид. трьохетапне зниження температур та гарантоване Отриману завісь клітин, що призначені для за певних умов ініціювання процесу кристалізації збереження в банку поміщали в контейнери не викликає швидкий зріст великих кристалів, які об'ємом 50мл., контейнери заповнювали в порушують оболонки клітин, що забезпечує середньому на 20÷30мл., видушували з стабільність характеристик біооб'єктів, які контейнера повітря і запаювали отвори. зберігаються в банку. Контейнери поміщали у пенал - холдер у вигляді Спосіб передбачає використання зменшеної гофрованого алюмінієвого контейнера, концентрації кріопротектора що зменшує заморожування проводили в один етап в необхідний розмір сховищ банку та спрощує холодильнику VXS 380 фірми JOUAN при наступне використання збережених біооб'єктів. температурі -80°. Розроблені технологічні операції по Збереження здійснювали у цій же тарі, для розморожуванню зразків для бактеріологічного чого холдер вкладали в паперовий пакет з контролю, для вірусного та мікоплазмового відповідними відмітками, і вставляли в касету для контролю, для культивування і для визначення збереження в схови щі в рідкому азоті. кількості клітин-попередників не викликають Розморожуванню зразків для критичного нагрівання всього контейнера і система бактеріологічного контролю, для вірусного та не відходить від урівноваженого стану. Внаслідок мікоплазмового контролю, для культивування цього не виникає рекристалізація, не утворюються здійснювали шляхом вилучення касети з холдером мікро - і макро тріщини, як наслідок не і контейнером зі сховища, відбору по напису на ушкоджуються клітини мембрани об'єктів що пакеті необхідного контейнера, виймання зберігаються. контейнера з пакета, розморожування середовища У такому способі зазначені технологічні в контейнері, розкривання контейнеру і відбору процеси роботи банку емпірично підібрані таким проби необхідного обсягу. чином, що виключаються процеси, які істотно Середній термін виконання сукупності знижують життєздатність об'єктів, що зберігаються зазначених дій вказано в Таблиці 1. в банку. Якісні характеристики збережених в банку Для порівняння прототипу та запропонованого клітин, а саме життєздатність визначали за способу здійснювали спосіб за прототипом та відомим способом, шляхом фарбування зразків запропонованим на зазначених нижче прикладах трипаневим синім, за яким пошкоджені клітини 1-88. В прикладах здійснювали такі дії. фарбувалися, після чого підраховували кількість Незалежно від джерела одержання, пофарбованих та непофарбованих клітин на 100 приготування клітинної суспензії за прототипом та клітин. Кількість непофарбованих клітин 7 49759 8 отриманих в прикладах вказано в Таблиці 1. одного боку контейнера із клітинною суспензією, В таблиці 2 зазначені режими виконання шляхом разового пропускання через нього рідкого прикладів 5-88 за пропонованим способом. азоту, завдяки чому, при відповідній температурі В прикладах 5-18, Таблиця 2а автоматично відбувалася ініціація використовували суспензії клітин плодових кристалоутворення. тестисів, в прикладах 19-32, Таблиця 26 суспензії На другому етапі зі швидкістю 0,3÷0,5°С/хв. до нервових клітин, в прикладах 33-46, Таблиця 2в -7÷-8°С, після цього етапу здійснюють суспензії клітин гепатоцитів, в прикладах 47-60, температурну зупинку при -30÷-40°С протягом 3Таблиця 2г суспензії клітин кардиомиоцитів, в 5хв., а на третьому етапі зі швидкістю 10÷12°С/хв. прикладах 61-74, Таблиця 2д суспензії клітин до -80÷-86°С. Конкретні режими в прикладах підшлункової залози, в прикладах 75-88, Таблиця зазначені в Таблиці 2. 2ж суспензії гемопоетичних клітин крові. Концентрація кріопротектора складала 0,4Підготовка клітин до низькотемпературного 1,45моль/л. консервування за запропонованим способом. Після замороження контейнери за допомогою Кріопротектор ДМСО - 7,0мол/л концентрації лещат вилучали із укладки і переносили в рідкий розводили до 0,8 і 2,9мол/л концентрації. В азот в сховище біологічних продуктів (марки СБотриману завісь клітин, що призначені для 0,5), обладнане чарунками зі змінними касетами. кріоконсервування, через ін'єкційну голку по Зберігали кріоконсервовані клітини в краплині додавали 1:1 розчин ДМСО до низькотемпературному сховищі при мінус 130одержання 0,4-1,45мол/л кінцевих концентрацій 196°С протягом трьох місяців. при легкому перемішуванні завісі шляхом Процес вилучення зразків об'єктів для похитування пробірки. визначення якісних характеристик об'єктів, що За допомогою шприцу через ін'єкційну голку зберігаються здійснювали шляхом вилучення гемопоетичні клітини розливали по 1мл в касети з необхідною партією ампул і занурення її в поліетиленові кріоампули об'ємом 1-4,5мл фірми кювету з рідким азотом, наступного вилучення Nunc (CryoStore Boxes). Використовувані ампули окремих ампул з касети, для перевірки якості, та обсяг їх заповнення зазначені в Таблиці 2. після чого касету знов вставляли в сховище. Кріоампули герметично закривали кришками і Терміни роботи з ампулами та касетами зазначені маркували. в Таблиці 2. Заморожування гемопоетичніх клітин Оцінку якісних характеристик збережених виконували за допомогою програмного клітин, а саме життєздатність визначали за заморожувача, який дозволяє варіювати швидкість відомим способом, шляхом фарбування зразків зниження температури на різних етапах трипаневим синім, за яким пошкоджені клітини кріоконсервування і автоматично здійснювати фарбувалися, після чого підраховували кількість ініціювання процесу кристалізації (сідінг) за певної пофарбованих та непофарбованих клітин на 100 температури, шля хом разового пропуску рідкого клітин. Кількість непофарбованих клітин азоту через відповідну трубку. отриманих в прикладах вказано в Таблиці 2. При заморожуванні клітинної суспензії в Результати досліджень показують що клітини, ампулах використовували спеціальні укладки, в які які зберігалися за способом роботи банку, по вставляли ампули (контейнери) вертикально і програмі, описаної в прототипі, мали низьку укладку розміщували в теплообмінну камеру життєздатність після розморожування, крім того, заморожувача на відповідному пристрої, що за таким способом роботи банку можна зберігати виконує ініціацію кристалоутворення. не усі види клітинних суспензій, а тільки ті, що Заморожування клітин виконували за одержують у великих обсягах. трьохетапною програмою. На першому етапі від Клітинні суспензії, що заморожені по кімнатної температури (20±4°С) зі швидкістю запропонованому способу роботи банку і 0,5÷1,5°С/хв. до -3,5÷-4°С, Протягом першого зберігались в банку по описаній вище технології, етапу заморожування, при досягненні температури показали високий процент життєздатних клітин -3,5÷-4°С здійснювали захолоджування (сідінг) після збереження протягом 3-х місяців. 9 49759 10 11 49759 12 13 49759 14 15 49759 16 17 49759 18 19 49759 20 21 49759 22 23 49759 ДП «Український інститут промислов ої в ласності» (Укрпатент) вул. Сім’ї Хохлов их, 15, м. Київ , 04119, Україна (044) 456 – 20 – 90 ТОВ “Міжнародний науков ий коміт ет” вул. Артема, 77, м. Київ , 04050, Україна (044) 216 – 32 – 71 24
ДивитисяДодаткова інформація
Назва патенту англійськоюActivity of bank for storing cryopreserved biological objects
Автори англійськоюLobyntseva Halyna Stepanivna
Назва патенту російськоюСпособ работы банка криоконсервированных биологических объектов
Автори російськоюЛобинцева Галина Степановна
МПК / Мітки
МПК: A61J 1/05, A01N 1/02, A01N 1/00
Мітки: низькотемпературного, спосіб, роботи, об'єктів, банку, біологічних
Код посилання
<a href="https://ua.patents.su/12-49759-sposib-roboti-nizkotemperaturnogo-banku-biologichnikh-obehktiv.html" target="_blank" rel="follow" title="База патентів України">Спосіб роботи низькотемпературного банку біологічних об’єктів</a>
Попередній патент: Технологія переробки томатів
Наступний патент: Спосіб корекції системних порушень в перименопаузі
Випадковий патент: Пристрій для очищення рідини