Спосіб одержання cu/zn/al-каталізатора, каталізатор та його застосування
Номер патенту: 91547
Опубліковано: 10.08.2010
Автори: Хіке Мартін, Полір Зігфрід (помер), Хінце Дітер
Формула / Реферат
1. Спосіб одержання Cu/Zn/Al-каталізатора, який відрізняється тим, що
- одержують перший водний розчин, який містить щонайменше форміат міді і форміат цинку,
- одержують другий розчин, який містить осаджувач,
- причому перший розчин і/або другий розчин містить суміш золю/гелю гідроксиду алюмінію,
- на стадії осадження перший розчин і другий розчин з'єднують, і одержують осад,
- осад відділяють від водної фази, яка утворює відпрацьовану воду, і
- осад промивають доти, доки вміст лугу, з розрахунку на прожарений при 600 °С каталізатор, не стане меншим 500 частин/млн., і
- потім осад сушать.
2. Спосіб за п. 1, який відрізняється тим, що перший розчин одержують шляхом
- одержання водного розчину форміату міді, в якому розчинена сполука, що містить мідь, без залишку шляхом додавання мурашиної кислоти,
- одержання водної дисперсії або розчину сполуки, що містить цинк,
- одержання водного розчину солі алюмінію, і
- з'єднування розчину форміату міді, дисперсії або розчину сполуки, що містить цинк, і розчину солі алюмінію.
3. Спосіб за п. 2, де розчин форміату міді має значення рН нижче 3, переважно нижче 2,5.
4. Спосіб за одним з пп. 2 або 3, де розчин або дисперсію сполуки, що містить цинк, з'єднують з розчином форміату міді з утворенням мідно-цинкового розчину, причому одержаний мідно-цинковий розчин має рН в інтервалі від 3,0 до 4,0, переважно від 3,5 до 3,7, і до мідно-цинкового розчину додають розчин солі алюмінію.
5. Спосіб за п. 4, де розчин солі алюмінію додають декількома розчинами, причому щонайменше першу частину розчину солі алюмінію одержують так, що щонайменше першу частину солі алюмінію розчиняють у воді при додаванні мурашиної кислоти.
6. Спосіб за п. 4 або 5, де другу частину розчину солі алюмінію одержують так, що другу частину солі алюмінію розчиняють у воді і для одержання першого розчину першу частину розчину солі алюмінію і другу частину розчину солі алюмінію додають до мідно-цинкового розчину, переважно рознесеними за часом.
7. Спосіб за одним з пп. з 2 по 6, який відрізняється тим, що водний розчин солі алюмінію, першу частину розчину солі алюмінію і/або другу частину розчину солі алюмінію перед осадженням нагрівають до температури максимум 40 °С, зокрема максимум 30 °С.
8. Спосіб за одним з попередніх пунктів, де під час стадії осадження рН підтримують в діапазоні від 3,5 до 7,5, переважно від 6,0 до 7,0, зокрема переважно 6,5±0,1.
9. Спосіб за одним з попередніх пунктів, який відрізняється тим, що як сполуки, що містить мідь, вибирають з CuO, Cu(OH)2 і Cu(OH)2xCuCO3.
10. Спосіб за одним з попередніх пунктів, який відрізняється тим, що як сполуку, що містить цинк, вибирають ZnO.
11. Спосіб за одним з попередніх пунктів, де осаджувач є лужною основою, переважно лужним карбонатом.
12. Спосіб за одним з пп. з 1 по 10, де осаджувач є пероксидом водню.
13. Спосіб за одним з попередніх пунктів, який відрізняється тим, що осад після осадження піддають дозріванню.
14. Спосіб за п. 13, який відрізняється тим, що дозрівання проводять протягом від 10 хвилин до 10 годин, переважно від 1 до 5 годин.
15. Спосіб за п. 13 або 14, який відрізняється тим, що дозрівання проводять при температурі вище 60 °С, зокрема в інтервалі від 65 до 80 °С.
16. Спосіб за одним з попередніх пунктів, який відрізняється тим, що стадію осадження проводять як безперервне осадження.
17. Спосіб за одним з попередніх пунктів, який відрізняється тим, що перший розчин містить мідь і цинк у співвідношенні, вибраному від 1:99 до 99:1.
18. Спосіб за одним з попередніх пунктів, який відрізняється тим, що осад після сушіння прожарюють.
19. Спосіб за п. 18, де осад прожарюють при температурах в інтервалі 140-1000 °С, переважно 170-350 °С, протягом щонайменше 0,1 секунди, переважно від 20 хвилин до 8 годин, зокрема переважно від 30 хвилин до 4 годин.
20. Спосіб за одним з попередніх пунктів, який відрізняється тим, що відпрацьована вода містить форміатні іони і тим, що відпрацьовану воду, що містить форміати, піддають окислювальній обробці, причому форміатні іони окислюються в основному до карбонату, гідрокарбонату, діоксиду вуглецю і води.
21. Спосіб за п. 20, який відрізняється тим, що для окислювальної обробки у відпрацьовану воду, що містить форміати, додають пероксид водню.
22. Спосіб за п. 20 або 21, який відрізняється тим, що окислювальну обробку відпрацьованої води, що містить форміати, проводять перед відділенням осаду.
23. Спосіб за одним з пп. 20-22, який відрізняється тим, що окислювальну обробку проводять шляхом біологічної обробки відпрацьованої води, що містить форміати.
24. Каталізатор, одержаний способом за одним з пп. 1-23, містить форміат, з розрахунку на оксидний каталізатор, менше 5 мас. %.
25. Каталізатор за п. 24, який відрізняється тим, що частка мезопор з радіусом 3,75-7,0 нм складає більше 30 % від повного об'єму пор.
26. Каталізатор за п. 24 або 25, який відрізняється тим, що вміст міді, розрахований на оксид міді і віднесений до маси оксидного каталізатора, вибирають між 55 і 69 мас. %.
27. Каталізатор за одним з пп. 24-26, який відрізняється тим, що вміст цинку, розрахований на оксид цинку і віднесений до маси оксидного каталізатора, вибирають між 20 і 33 мас. %.
28. Каталізатор за одним з пп. 24-27, який відрізняється тим, що вміст алюмінію, розрахований на оксид алюмінію і віднесений до ваги оксидного каталізатора, вибирають між 5 і 20 мас. %.
29. Каталізатор за одним з пп. 24-28, який відрізняється тим, що оксидний каталізатор має вміст лужних іонів менше 500 частин/млн.
30. Застосування каталізатора за одним з пп. 24-29 для синтезу метанолу.
31. Застосування каталізатора за одним з пп. 24-29 для риформінгу метанолу.
32. Застосування каталізатора за одним з пп. 24-29 для низькотемпературної конверсії моноксиду вуглецю в діоксид вуглецю.
Текст
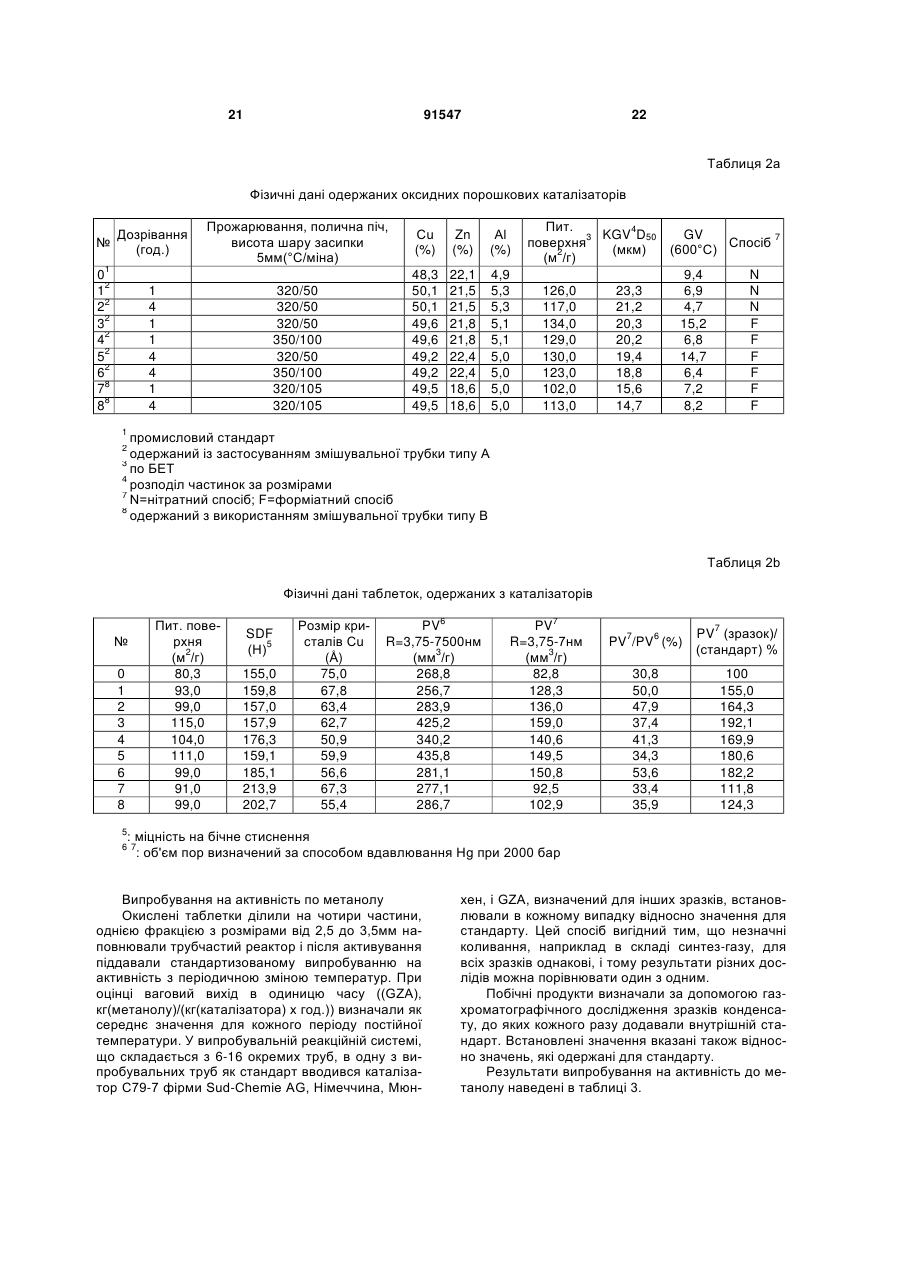
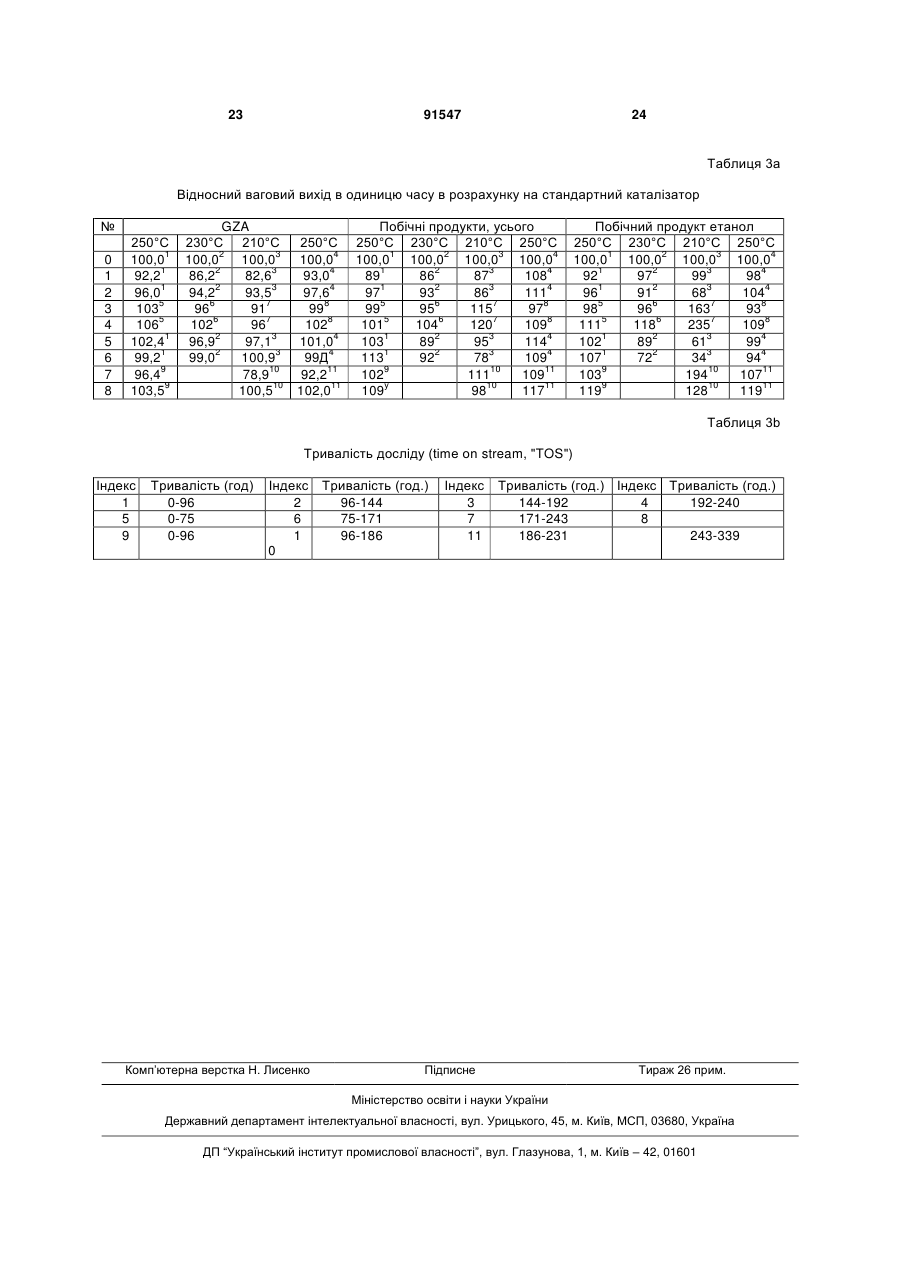
1. Спосіб одержання Cu/Zn/Al-каталізатора, який відрізняється тим, що - одержують перший водний розчин, який містить щонайменше форміат міді і форміат цинку, - одержують другий розчин, який містить осаджувач, - причому перший розчин і/або другий розчин містить суміш золю/гелю гідроксиду алюмінію, - на стадії осадження перший розчин і другий розчин з'єднують, і одержують осад, - осад відділяють від водної фази, яка утворює відпрацьовану воду, і - осад промивають доти, доки вміст лугу, з розрахунку на прожарений при 600°С каталізатор, не стане меншим 500 частин/млн., і - потім осад сушать. 2. Спосіб за п.1, який відрізняється тим, що перший розчин одержують шляхом - одержання водного розчину форміату міді, в якому розчинена сполука, що містить мідь, без залишку шляхом додавання мурашиної кислоти, - одержання водної дисперсії або розчину сполуки, що містить цинк, - одержання водного розчину солі алюмінію, і - з'єднування розчину форміату міді, дисперсії або розчину сполуки, що містить цинк, і розчину солі алюмінію. 3. Спосіб за п.2, де розчин форміату міді має значення рН нижче 3, переважно нижче 2,5. 2 (19) 1 3 91547 4 13. Спосіб за одним з попередніх пунктів, який відрізняється тим, що осад після осадження піддають дозріванню. 14. Спосіб за п.13, який відрізняється тим, що дозрівання проводять протягом від 10 хвилин до 10 годин, переважно від 1 до 5 годин. 15. Спосіб за п.13 або 14, який відрізняється тим, що дозрівання проводять при температурі вище 60°С, зокрема в інтервалі від 65 до 80°С. 16. Спосіб за одним з попередніх пунктів, який відрізняється тим, що стадію осадження проводять як безперервне осадження. 17. Спосіб за одним з попередніх пунктів, який відрізняється тим, що перший розчин містить мідь і цинк у співвідношенні, вибраному від 1:99 до 99:1. 18. Спосіб за одним з попередніх пунктів, який відрізняється тим, що осад після сушіння прожарюють. 19. Спосіб за п.18, де осад прожарюють при температурах в інтервалі 140-1000°С, переважно 170350°С, протягом щонайменше 0,1 секунди, переважно від 20 хвилин до 8 годин, зокрема переважно від 30 хвилин до 4 годин. 20. Спосіб за одним з попередніх пунктів, який відрізняється тим, що відпрацьована вода містить форміатні іони і тим, що відпрацьовану воду, що містить форміати, піддають окислювальній обробці, причому форміатні іони окислюються в основному до карбонату, гідрокарбонату, діоксиду вуглецю і води. 21. Спосіб за п.20, який відрізняється тим, що для окислювальної обробки у відпрацьовану воду, що містить форміати, додають пероксид водню. 22. Спосіб за п.20 або 21, який відрізняється тим, що окислювальну обробку відпрацьованої води, що містить форміати, проводять перед відділенням осаду. 23. Спосіб за одним з пп.20-22, який відрізняється тим, що окислювальну обробку проводять шляхом біологічної обробки відпрацьованої води, що містить форміати. 24. Каталізатор, одержаний способом за одним з пп.1-23, містить форміат, з розрахунку на оксидний каталізатор, менше 5мас.%. 25. Каталізатор за п.24, який відрізняється тим, що частка мезопор з радіусом 3,75-7,0нм складає більше 30 % від повного об'єму пор. 26. Каталізатор за п.24 або 25, який відрізняється тим, що вміст міді, розрахований на оксид міді і віднесений до маси оксидного каталізатора, вибирають між 55 і 69мас.%. 27. Каталізатор за одним з пп.24-26, який відрізняється тим, що вміст цинку, розрахований на оксид цинку і віднесений до маси оксидного каталізатора, вибирають між 20 і 33мас.%. 28. Каталізатор за одним з пп.24-27, який відрізняється тим, що вміст алюмінію, розрахований на оксид алюмінію і віднесений до ваги оксидного каталізатора, вибирають між 5 і 20мас.%. 29. Каталізатор за одним з пп.24-28, який відрізняється тим, що оксидний каталізатор має вміст лужних іонів менше 500 частин/млн. 30. Застосування каталізатора за одним з пп.24-29 для синтезу метанолу. 31. Застосування каталізатора за одним з пп.24-29 для риформінгу метанолу. 32. Застосування каталізатора за одним з пп.24-29 для низькотемпературної конверсії моноксиду вуглецю в діоксид вуглецю. Винахід належить до способу одержання Cu/Zn/Al-каталізатор, до каталізатора, який може бути одержаний цим способом, а також до його застосування для синтезу метанолу і риформінгу метанолу і для низькотемпературної конверсії моноксиду вуглецю. Cu/Zn/Al-каталізатори, які каталізують перетворення CO, CO2 і Н2 на метанол, відомі давно. Атомне співвідношення між міддю і цинком може у цих відомих каталізаторах мінятися, причому звичайно мідь все ж присутня в надлишку. Крім того, частина цинкового компонента може бути замінена на кальцій, магній і/або марганець. Оксид алюмінію, що застосовується як термостабілізуюча речовина, також може бути частково замінений на оксид хрому. Так, наприклад, з документа DE 1 965 007 відомий каталізатор для низькотемпературного синтезу метанолу. Для одержання каталізатора спочатку з розчину придатних солей цинку і міді додаванням карбонатів лужних металів висаджують відповідний основний карбонат. Його відділяють від водної фази, сушать і прожарюють, щоб одержати відповідні оксиди. Потім оксиди цинку і міді змішують з оксидом алюмінію, причому вихо дить суспензія оксидів, яка містить не більше 20% твердої фази. її потім гомогенізують, причому гомогенізація триває стільки, щоб дисперговані оксиди не осаджувалися протягом 2 годин. Після гомогенізації суміш сушать, таблетують і прожарюють. Щоб перетворити оксидну форму на каталізатор, її додатково відновлюють в потоці водню. З документа DE 2 302 658 А відомий спосіб одержання попередника каталізатора, який може застосовуватися для синтезу метанолу. Для одержання попередника каталізатора спочатку одержують перший осад, який містить двовалентний метал, наприклад, цинк, а також тривалентний метал, наприклад, алюміній, в формі якої-небудь сполуки, яку можна розкласти термічно до відповідних оксидів. Відповідними сполуками є, наприклад, карбонати або бікарбонати. Далі одержують другий осад, який містить сполуки міді, які можна розкласти термічно до оксидів. Обидва осади змішують. За цим безпосередньо ідуть звичайні етапи сушіння і прожарювання, щоб одержати з металевих сполук оксиди і, по можливості, викликати утворення шишельної структури. Потім тверду фазу таблетують. Щоб перевести попередник в 5 активний каталізатор, таблетки відновлюють в потоці водню. У документі DE 2 056 612 А описаний спосіб одержання метанолу, в якому реакція іде на каталізаторі, що містить цинк, мідь і алюміній. Каталізатор належить до ряду змішаних кристалів формули (СuхZnу)АІ2(ОН)16 СО3 4Н2О, в якій х і у можуть приймати чисельні значення від 0,5 до 5,5, а сума х і у дорівнює 6. Сполуку зі змішаними кристалами осаджують з водного розчину, який містить солі міді, цинку і алюмінію, при додаванні лужного карбонату, лужного бікарбонату або їх суміші. Атомне відношення суми двовалентних металів міді і цинку до тривалентного алюмінію в ряді змішаних кристалів постійне і становить 6:2. Для одержання мідь, цинк і алюміній в формі придатних солей, переважно нітрату, розчиняють у воді, і притому в кількісному співвідношенні, яке відповідає бажаному складу каталізатора. Цей розчин нагрівають до температури від 50 до 100°С, переважно від 70 до 100°С, і обробляють відповідним нагрітим водним розчином осаджувача, наприклад, карбонатом лужного металу. Виникаючий осад відфільтровують, миють і сушать. Висушену сполуку прожарюють при температурах в інтервалі від 200 до 500°С протягом 12-24 годин. Прожарений продукт формують в таблетки і потім шляхом відновлення в потоці водню переводять в активну форму каталізатора. У документі US 4,279,781 описаний каталізатор для синтезу метанолу, який включає оксид міді і цинку, а також оксид металу для термічної стабілізації, наприклад, оксид алюмінію. Відношення оксиду міді до оксиду цинку з розрахунку на вагу металу складає від 2:1 до 3,5:1. Одержання каталізатора відбувається через загальне осадження розчинених солей цинку, міді і алюмінію, наприклад, нітрату. Цим досягається ретельне перемішування компонентів каталізатора. Щоб одержати активну форму, попередник каталізатора відновлюють в потоці водню. З документа ЕР 0 125 689 А2 відомий каталізатор для синтезу метанолу, який як каталітично активні речовини містить оксид міді і оксид цинку, а як термостабілізуючу речовину - оксид алюмінію. Каталізатор відрізняється визначеним розподілом пор по радіусу, причому частка пор з діаметром від 20 до 75Д (мезопори) складає щонайменше 20%, а частка пор з діаметром більше 75Д (макропори) становить саме більше 80%. Бажаний розподіл пор по радіусу може бути досягнутий тим, що при одержанні каталізатора використовується колоїдально диспергований оксид або гідроксид алюмінію. Для одержання цих каталізаторів каталітично активні компоненти оксид міді і оксид цинку осаджують з водних розчинів відповідних солей, наприклад, нітратів, сульфатів, хлоридів, ацетатів, за допомогою лужних речовин в присутності колоїдально диспергованого оксиду або гідроксиду алюмінію. Продукт осадження можна потім висушити, прожарити, пресувати в формований виріб і при необхідності відновити. З документа ЕР 0 152 809 А2 відомий каталізатор для синтезу метанолу і спиртової суміші, що містить вищі спирти, який у вигляді оксидного по 91547 6 передника містить оксид міді і оксид цинку, які шляхом відновлення щонайменше частини оксиду міді можуть бути перетворені на каталітично діючі компоненти, а також оксид алюмінію як термостабілізуючу речовину і щонайменше один лужний карбонат або лужний оксид. Частка пор з діаметром від 14 до 7,5нм в оксидному попередникові складає від 20 до 70% від повного об'єму. Вміст лугу складає від 13 до 130 10-6 грам-атомів лужного металу на грам оксидного попередника. Компонент оксид алюмінію одержували з колоїдально диспергованого гідроксиду алюмінію. Для одержання каталізатора звичайно застосовують розчини нітрату міді і цинку і осадження проводять переважно водним розчином К2СО3. Концентрація розчину складає переважно від 5 до 20ваг.%. Замість нітрату можна також виходити з відповідних форміатів або ацетатів металів. Осадження можна здійснювати також за допомогою розчину гідрокарбонату калію. Осадження може проводитися періодично або безперервно. Переважно осадження проводиться шляхом безперервного з'єднування розчину нітрату міді і цинку, який містить колоїдально диспергований гідроксид алюмінію, з водним розчином К2СО3. Відразу після осадження промитий осад каталізатора прожарюють і підлуговують шляхом обробки розчином сполуки лужного металу. Підлугований попередник каталізатора після сушіння пресують способом, який сам по собі відомий, з утворенням формованого тіла, причому може додаватися мастило, як графіт. Щоб перевести попередник каталізатора в активну форму, його відновлюють воднем. З документа WO 03/053569 А1 відомий каталізатор для синтезу метанолу, який містить оксид міді і оксид цинку як каталітично діючі речовини, а також оксид алюмінію як термостабілізуючу речовину. Для одержання каталізатора з розчину, який містить солі Сu і Zn, а також частину солі Аl, за допомогою розчину лужного карбонату або лужного алюмінату осаджують відповідні гідроксокарбонати або гідроксиди. Або розчин солей Сu і Zn, або розчин лужного карбонату або лужного алюмінату містить золь гідроксиду алюмінію. Одержаний осад відділяють від розчину, в якому відбувалося осадження, миють, сушать і при необхідності прожарюють. При одержанні каталізатора виходять переважно з нітрату міді і цинку, які осаджуються переважно карбонатом натрію або алюмінатом натрію. У документі JP 2001-144779 описаний мідноцинковий каталізатор для реакції моноксиду вуглецю і води з отриманням діоксиду вуглецю і води, який одержують тим, що розчин, що містить форміат міді і форміат цинку, змішують з водним розчином лужного матеріалу. Осад, що утворюється при цьому, потім фільтрують, миють, сушать і прожарюють. Прожарену тверду речовину скаламучують додаванням води і наносять на поверхню підкладки зі структурою стільників. Як зв'язуюче може застосовуватися золь оксиду алюмінію або золь оксиду цирконію. Вони можуть додаватися у завись прожареного осаду. При цьому оксид алюмінію розподілений в каталізаторі неоднорідно, а знаходиться тільки між частинками каталізатора. 7 Таким чином, його задачею є діяти тільки як зв'язуюче між частинками каталізатора, що містять мідь і цинк, а також підкладки з стільниковою структурою, і він не є активним компонентом каталізатора. Для одержання Cu/Zn/Al-каталізаторів для синтезу метанолу в способі, що технічно реалізовується, застосовуються в основному нітрат цинку і міді завдяки своїй хорошій розчинності у воді. При цьому при осадженні накопичується відпрацьована вода, яка містить великі кількості нітрату натрію. При скиданні в поверхневі води це привело б до надмірної концентрації добрив. Тому перед скиданням в поверхневі води вміст водорозчинного азоту у відпрацьованих водах, що накопичуються при одержанні каталізаторів синтезу метанолу, повинен бути суттєво зменшений. Тому задачею винаходу є розробити спосіб одержання Cu/Zn/Al-каталізаторів, який, з одного боку, дозволяє помітно зменшити вміст у відпрацьованій воді солі, зокрема нітрату лужного металу, і який, з іншого боку, надає каталізатори для синтезу метанолу, активність яких щонайменше порівнянна з активністю каталізатора, одержуваного з нітрату металу. Ця задача вирішена способом з відмітними ознаками пункту 1 формули винаходу. Вигідні форми реалізації способу є об'єктом залежних пунктів. У способі одержання Cu/Zn/Al-каталізаторів згідно з винаходом спочатку одержують перший водний розчин, що містить щонайменше форміат міді і форміат цинку. Далі одержують другий розчин, який містить осаджувач. При цьому під осаджувачем розуміється реагент, який, прямо або непрямо, виробляє іони, наприклад, гідроксильні іони і/або карбонатні іони, за допомогою яких можна осадити метали, зокрема, мідь, цинк і алюміній. Перший розчин і/або другий розчин містить золь/гель суміш гідроксиду алюмінію. При цьому під золем гідроксиду алюмінію розуміється тонкодисперсний розподіл гідроксиду алюмінію у воді, в якій вже були утворені полікислоти шляхом конденсації гідроксиду алюмінію, однак при цьому у водній фазі неозброєним оком не видно ніяких частинок, так що розчин є прозорим. Під гелем гідроксиду алюмінію розуміється дисперсія гідроксиду алюмінію у воді, причому вже утворені великі агломерати з полікислот, так що навіть неозброєним оком можна розрізнити частинки, наприклад, як помутніння водної фази. На стадії осадження перший розчин і другий розчин з'єднують, причому виходить осад. Осад відділяють від водної фази, причому водна фаза утворює відпрацьовану воду, яку проводять на переробку. Осад миють, поки вміст в ньому лугу не складе менше 500 частин/млн. з розрахунку на прожарений при 600°С каталізатор. Потім осад сушать, при необхідності прожарюють і мелють. У способі згідно з винаходом відпрацьованої води, що містить нітрат, не 1 утворюється. Завдяки використанню форміату міді і форміату цинку як водорозчинних солей міді і цинку відпрацьована вода містить форміатні іони, які можуть бути пере 91547 8 роблені більш простим шляхом. Завдяки застосуванню форміатів навантаження відпрацьованої води органічним матеріалом зберігається відносно низьким. Це є перевагою в порівнянні із застосуванням вищих карбонових кислот, таких як оцтова кислота, оскільки вони через більш високе число зв'язків С-Н підвищують навантаження відпрацьованої води органікою. Іншою перевагою є економічно вигідне одержання мурашиної кислоти, яка необхідна для одержання форміатів міді і цинку, так що спосіб згідно з винаходом вигідний також з економічної точки зору. Для способу згідно з винаходом суттєво, щоб щонайменше частина алюмінію вводилася в розчин, де проводиться осадження, в формі золю гідроксиду алюмінію, а інша частина - як гель гідроксиду алюмінію. При відмові від додавання золь/гель суміші гідроксиду алюмінію в розчин солей металів падає вихід продукту по вазі в одиницю часу (GZA, [кг метанолу/{кг каталізатора х год.}]). Осад після відділення ретельно промивають, так щоб вміст в ньому лугу, розрахований на прожарений при 600°С оксидний каталізатор, впав до значень менше 500 частин/млн., переважно менше 400 частин/млн., зокрема до значень в інтервалі від 100 до 300 частин/млн. Промивальну воду, що накопичується при цьому, можна об'єднати з відпрацьованою водою, яка містить форміат, і при необхідності переробити. Після промивання, сушіння і при необхідності прожарювання оксидна форма каталізатора ще виявляє залишковий вміст форміату менше 5ваг.%, переважно від 0,5 до 4ваг.%, зокрема переважно 1-2ваг.%. Вміст форміату можна визначити, наприклад, окислювальним титруванням або кількісним хроматографічним аналізом, наприклад, ВЕРХ. Крім форміату міді і форміату цинку, перший водний розчин може також містити звичайні промотори, як, наприклад, кальцій, магній, марганець, церій, лантан, а також рутеній або паладій. Крім названих промоторів можуть також використовуватися і інші промотори. Промотори вводяться переважно також в формі своїх форміатів перевалено в перший водний розчин. їх частка в оксидній формі каталізатора, розрахована на оксид, складає переважно менше 10ваг.%, зокрема менше 5ваг.%. Якщо як промотори використовуються благородні метали, як рутеній або паладій, то вони переважно містяться в кількості менше 1ваг.%. Як вже згадувалося, в способі згідно з винаходом перший і/або другий розчин містить золь/гель суміш гідроксиду алюмінію. Як вихідний продукт для золь/гель суміші гідроксиду алюмінію може, наприклад, використовуватися продукт, що є в продажу. Однак золь/гель суміш гідроксиду алюмінію можна також одержати тим, що до розбавленого розчину солі алюмінію додають небагато гідроксиду амонію, причому нагрівання уникають, щоб перешкодити перетворенню на великодисперсні гідроксопохідні. Згідно з іншим варіантом, можна до розчину лужного алюмінату додати незначну кількість кислоти, причому утворюється золь/гель гідроксиду алюмінію. Переважно золь/гель гідроксиду алюмінію міститься в першо 9 му водному розчині. Продукти, що утворюються із золь/гель гідроксиду алюмінію на наступних стадіях, служать як підкладкою, так і термостабілізуючою речовиною. Не прив'язуючись до цієї теорії, автори винаходу передбачають, що при нагріванні із золь/гель суміші гідроксиду алюмінію утворюється тривимірна сітка, у вільних об'ємах якої розташовуються кристали міді, що належать до активних компонентів, які виходять після відновлення. Через це ускладнюється подальше зрощення кристалів міді при синтезі метанолу, що підвищує стабільність каталізатора і його термін служби в технологічних процесах. Вважається, що оксид цинку, по-перше, впливає сильний чином на утворення активних компонентів, а по-друге, завдяки своїй частково голчатій структурі, сприяє стабільності каталізатора. Крім того, оксид цинку діє як пастка для отруйних речовин, реагуючи зі сполуками сірки, які можуть випадково попадатися. Присутні у відомих випадках як промотори оксиди кальцію, магнію, марганцю, церію і лантану також діють стабілізуюче. Перший розчин, який містить суміш різних солей металів, одержують переважно тим, що - одержують водний розчин форміату міді, повністю розчиняючи сіль міді шляхом додавання мурашиної кислоти, - одержують водну дисперсію або розчин солі цинку, - одержують водний розчин солі алюмінію, і - розчин форміату міді, дисперсію або розчин солі цинку і розчин солі алюмінію з'єднують. Якщо Cu/Zn/Al-каталізатор повинен ще модифікуватися промоторами, їх можна вводити, наприклад, в перший розчин. Промотори можуть додаватися у формі придатних солей, наприклад, як карбонати, оксиди або гідроксиди. Самі по собі ці солі можуть додаватися в будь-який момент часу, тобто в розчин форміату міді, в дисперсію або розчин солі цинку, або також після з'єднування розчину форміату міді і дисперсії або розчину солі цинку. Особливо дорогі промотори, як благородні метали, додаються до суспензії переважно на більш пізньому етапі процесу, наприклад, перед розпилювальним сушінням, або напилюються тонкоподрібненими на сухий порошок після розпилювального сушіння. При одержанні розчину форміату міді і цинку переважно додається стільки мурашиної кислоти, щоб з розрахунку на використовувану кількість солі міді і цинку, з урахуванням стехіометрії, мурашина кислота знаходилася в надлишку щонайменше на 10 моль %, переважно від 10 до 20 моль %, зокрема переважно від 14 до 16 моль %. Значення рН розчину форміату міді після додавання мурашиної кислоти переважно складає менше 3, переважно менше 2,5. У переважному варіанті реалізації способу розчин або дисперсію солі цинку з'єднують з розчином форміату міді. Після з'єднання розчину або дисперсії форміату міді і солі цинку як мідь, так і цинк знаходяться в розчині в формі їх форміату. Одержаний розчин має переважно значення рН в діапазоні від 3,0 до 4,0, зокрема переважно від 3,5 91547 10 до 3,7. Потім до розчину міді з цинком додають розчин солі алюмінію. Розчин солі алюмінію переважно вводять в мідно-цинковий розчин декількома частинами. При цьому щонайменше першу частину розчину солі алюмінію одержують так, щоб щонайменше перша частка солі алюмінію розчинялася у воді при додаванні мурашиної кислоти. При одержанні першої частини розчину солі алюмінію переважно діють так, що, наприклад, спочатку розчиняють у воді алюмінат натрію, а потім додають стільки мурашиної кислоти, щоб значення рН складало менше 5, переважно від 4,5 до 2, зокрема від 4 до 3. Переважно додають стільки мурашиної кислоти, щоб одержати прозорий розчин. Далі, другу частину розчину солі алюмінію одержують переважно тим, що розчиняють у воді другу частину солі алюмінію. При цьому у другу частину розчину солі алюмінію мурашину кислоту не додають. Для приготування першого розчину, який містить суміш всіх солей металів перед осадженням, в цьому випадку у водний мідноцинковий розчин переважно вводять першу частину розчину солі алюмінію і другу частину розчину солі алюмінію, переважно рознесеними за часом. Другу частину розчину солі алюмінію одержують, наприклад, тим, що NaAlO2 розчиняють у воді. Значення рН водного розчину NaAlO2 складає, в залежності від надлишку лугу у вихідному матеріалі, від 11 до 14, переважно від 12 до 13. Частки першої і другої частин розчину солі алюмінію можуть знаходитися, з розрахунку на вміст алюмінію, в діапазоні від 0:100 до 100:0, переважно від 1:99 до 99:1, особливо переважно від 30:70 до 70:30 і, зокрема, переважно вибираються близько приблизно 50:50. Одержання розчинів солі алюмінію проводиться переважно при температурах нижче 40°С, зокрема переважно нижче 30°С. Цю температуру також не можна перевищувати, коли розчин солі алюмінію вводиться в мідно-цинковий розчин або в розчин форміату міді або в дисперсію, або розчин солі цинку. Цим пригнічується утворення великодисперсних полімерних сполук алюмінію. Під великодисперсними полімерними сполуками алюмінію розуміються комплексні гідроксосполуки алюмінію, які утворюють помітні оком частинки, що опускаються відносно швидко. Тому одержання розчинів проводиться переважно в котлі, який оснащений відповідним пристроєм охолоджування. Солями алюмінію, придатними для застосування в способі згідно з винаходом, є, наприклад, ди- і триформіат алюмінію, гідрат Al(NO3)3 або NaAlO2. Розчини солі алюмінію мають переважно концентрацію алюмінію в інтервалі від приблизно 0,4 до приблизно 1,1 моль/л, зокрема переважно від приблизно 0,9 до 1,1 моль/л. При цьому верхні значення вказаних інтервалів визначаються межами розчинності солі алюмінію, тоді як нижні межі виходять з економічних міркувань. Як солі міді переважно застосовуються такі солі, аніони яких є оксидами, гідроксидами і карбонатом або їх одержуваними відновленням похі 11 дними і які в першому розчині або в оксидній формі каталізатора більше не повинні виявлятися індивідуально серед помітних елементів. Переважно сіль міді вибирається з CuO, Cu(OH)2 і Cu(OH)2 CuCO3. Як сіль цинку переважно вибирають також сполуку цинку, аніон якого в першому розчині або в оксидному попередникові каталізатора більше не виявляється як такий, що заважає, переважно як помітний елемент. Переважно як сіль цинку вибирається ZnO. Концентрація розчину форміату міді переважно вибирається так, щоб після з'єднування розчину форміату міді і розчину або дисперсії солі цинку концентрація міді встановлювалася в інтервалі від приблизно 0,1 до приблизно 0,5, зокрема переважно від 0,3 до приблизно 0,5 моль/л. Верхнє значення при цьому визначається межею розчинності солі міді, а нижня межа виходить з економічних міркувань, оскільки обробка розбавлених розчинів приводить до підвищених об'ємів, що, наприклад, впливає на визначення розмірів пристрою, в якому реалізовується спосіб згідно з винаходом. Концентрація солі цинку переважно вибирається так, щоб після з'єднування розчину форміату міді і розчину або суспензії солі цинку концентрація цинку переважно лежала в інтервалі від приблизно 0,1 до приблизно 0,2 моль/л, переважно від 0,15 до приблизно 0,2 моль/л. Тут також верхня межа виходить з розчинності солі цинку, а нижня межа - з економічних міркувань. Розчин солі алюмінію переважно вводять в мідно-цинковий розчин. Значення рН першого розчину, який переважно містить повну кількість Cu, Zn і Аl, при цьому переважно встановлюється на значення в інтервалі від 4,0 до 5,0, особливо переважно від 4,2 до 4,4. Як осаджувач переважно застосовуються основи лужних металів. Як основи лужного металу використовуються переважно карбонати лужних металів, гідрокарбонати лужних металів або алюмінати лужних металів. Як лужний метал переважно застосовується натрій. Якщо, наприклад, як осаджувач використовується розчин соди, то концентрація содового розчину складає переважно від 80г/л до 200г/л, переважно від 170 до 180г/л. Згідно з іншою формою реалізації способу згідно з винаходом як осаджувач використовується пероксид водню. Пероксид водню вводиться в перший розчин або дисперсію, що містить мідь, цинк і алюміній в формі їх форміатів або гідроксоформіатів. Завдяки пероксиду водню форміат окислюється на карбонат, так що в осад випадають метали в формі їх гідроксокарбонатів, карбонатів або гідроксидів. При окисленні форміат-аніонів спочатку утворюються аніони гідрокарбонату, а потім, при зростаючому значенні рН, аніони карбонату. Використовувані аніони металів осаджуються послідовно в ряду Al-Cu-Zn як | гідроксокарбонати. Таким чином, можна відмовитися від використання карбонатвмісного лужного розчину. Крім пероксиду водню можуть застосовуватися також інші придатні окислювачі, наприклад, озон. Для одержання оксидних попередників каталізаторів спочатку з'єднують перший і другий роз 91547 12 чин, причому одержують осад. Осадження переважно проводять так, щоб під час осадження значення рН утримувалося в діапазоні від 3,5 до 7,5, переважно від 6,0 до 7,0 зокрема переважно 6,5±0,1. Температуру при осадженні утримують переважно в діапазоні від 25 до 95°С, зокрема переважно від 50 до 75°С. Після змішування утворений осад переважно піддають дозріванню. Для цього можна, наприклад, перевести суспензію, що утворилася при змішуванні першого і другого розчину, в резервуар для дозрівання, в якому суспензію можна обертати, наприклад, придатною мішалкою. Дозрівання проводиться переважно протягом періоду від 10 хвилин до 10 годин, зокрема переважно від 1 до 5 годин. При дозріванні суспензію переважно витримують при підвищеній температурі, причому дозрівання відбувається, зокрема, при температурі більше 60°С, зокрема переважно в діапазоні від 65 до 80°С. З'єднування першого і другого розчинів переважно проводять так, що розчини вводять паралельно в змішувальний резервуар і там перемішують. У цьому резервуарі проводиться грубе перемішування, наприклад, за допомогою придатної мішалки. Однак переважно, щоб осадження здійснювалося як безперервне осадження. Для цього передбачений змішувальний резервуар, що має відповідні розміри, в який безперервно подають перший і другий розчин і одержувану суміш безперервно відводять. Переважно об'єм змішувального резервуара вибирають так, щоб можна було здійснити безперервне підведення першого і другого розчинів в змішувальний резервуар і безперервне відведення суміші, причому час перебування суміші складає переважно від приблизно 0,1 секунди до 10 хвилин, особливо переважно від приблизно 1 до 120 секунд, зокрема переважно від 1 до 20 секунд. Час перебування суміші в змішувальному резервуарі сильно залежить від розмірів змішувального резервуара і швидкості потоку. Відповідні придатні розміри змішувального резервуара, а також швидкості підведення і відведення розчинів або суспензії можуть бути вибрані фахівцем. Після осадження і проведеного при необхідності етапу дозрівання осад відділяють від водної фази, для чого можуть застосовуватися звичайні способи, наприклад фільтрація. Осад потім промивають і сушать. Переважно після сушіння осад прожарюють. Прожарювання проводиться, в залежності від використовуваного способу, при температурах переважно від 140°С до 1000°С, зокрема переважно від 170°С до 350°С, протягом щонайменше 0,1 секунди, переважно щонайменше 4 хвилин, особливо переважно від 20 хвилин до 8 годин, зокрема переважно від 30 хвилин до 4 годин. У залежності від вибраних умов прожарювання форміат, що залишився в осіданні на фільтрі, при кальцинуванні видаляють по суті весь окисленням на повітрі або шляхом внутрішньомолекулярної окислювально-відновної 13 реакції в інертному газі. У останньому випадку Сu(НСО2)2 Н2О ймовірно спочатку розкладається до Н2 і СuС2О2. Потім оксалат міді реагує до утворення СО2 і елементарної міді. Прожарювання може проводитися в звичайних пристроях. У промисловому виробництві через краще теплоперенесення застосовуються як пульсаційні реактори, так і реактори з псевдозрідженим шаром каталізатора як переважні з точки зору вартості обертової печі. Пульсаційна сушарка робить можливим дуже короткочасне сушіння, в межах менше 1 секунди, звичайно в діапазоні від 0,1 секунди до 4 хвилин, причому можуть застосовуватися дуже високі температури до 1000°С. Прожарений порошок можна при необхідності розмолоти і потім за допомогою звичайних інструментів переробити, наприклад, на таблетки або екструдати. Однак можна також скаламутити порошок, розмолоти до дуже маленьких розмірів зерна і нанести одержану суспензію на придатну підкладку, наприклад, стільники. Для цього можна використовувати звичайні способи. При цьому придатний розмір зерна встановлюють так, щоб середній розмір зерна D50 складав від 10нм до 10мкм, зокрема переважно від 100нм до 5мкм. Середній розмір зерна можна визначити, наприклад, лазерною дифракцією. Придатні каталізатори можуть бути одержані, наприклад, з розміром зерна, при якому значення D50 знаходиться в інтервалі приблизно 2-3мкм. Особлива перевага способу згідно з винаходом полягає в тому, що відпрацьована вода, що накопичується після відділення осаду, яка містить форміати, може бути оброблена порівняно простими засобами. Для цього відпрацьовану воду, яка містить форміати, переважно піддають окислювальній обробці, причому форміатні іони окисляють у водному розчині, в залежності від рН, в основному до карбонату, гідрокарбонату, діоксиду вуглецю і води. Вміст форміатів, наприклад, у вигляді форміату натрію, у відпрацьованій воді знаходиться при технічній реалізації способу згідно з винаходом в інтервалі від 0,2 до 1,5 моль/л, зокрема переважно від 0,8 до 1,0 моль/л, але можуть також бути присутніми більш високі або більш низькі концентрації форміату. Шляхом окислювальної обробки відпрацьованої води можна знизити концентрацію форміату до значень менше 0,1 моль/л, переважно від 0,01 до 0,075 моль/л, зокрема переважно від 0,02 до 0,04 моль/л. Це відповідає зниженню кількості форміату, що міститься у відпрацьованій воді, більше ніж на 95%. Згідно з переважною формою реалізації для окислювальної обробки до відпрацьованої води, що містить форміати, додають пероксид водню. Пероксид водню в відпрацьовану воду, що містить форміати, додають переважно в формі розчину, концентрація пероксиду водню в якому лежить в діапазоні приблизно від 9 до 20 моль/л (приблизно до 60ваг.%). Для випадку, коли потрібно дотримуватися особливих правил перевезення, концентрацію використовуваного розчину пероксиду водню можна підвищити до більше ніж 90ваг.%. Переважно пероксид водню додають в надлишку, причому додана кількість в розрахунку на форміат, 91547 14 що міститься у відпрацьованій воді, вибирається в інтервалі від 160 до 200 моль %, зокрема переважно від 160 до 170 моль %. Крім пероксиду водню, можуть також використовуватися інші окислювачі, наприклад, озон або розчин гіпохлориту натрію. При виборі окислювача грає роль, наприклад, собівартість і законодавство про навколишнє середовище. У залежності від законодавчих обмежень і додаткових доступних рівнів очищення при відомих умовах не потрібно окисляти всю кількість форміатних іонів. Суттєве зниження концентрації форміатних іонів хімічною окислювальною обробкою може виявитися вже достатнім, і оброблена таким способом відпрацьована вода при необхідності може направлятися, наприклад, на рівень біологічного прояснення. Обробку пероксидом водню відпрацьованої води, що містить форміати, проводять переважно при 20-95°С, зокрема переважно при 50-80°С, в діапазоні рН 4-8, зокрема переважно від 5,0 до 6,5. Згідно з однією формою реалізації способу за винаходом окислювальна обробка відпрацьованої води, що містить форміати, проводиться вже перед відділенням осаду. Для цього можна, наприклад, після етапу дозрівання додати в суспензію придатну кількість пероксиду водню і відділяти осад тільки після суттєвого окислювального розщеплення форміатних іонів. У альтернативній послідовності технологічних стадій можна провести додавання розчину пероксиду водню вже до розчину форміату, що містить Cu, Zn, Al, причому осаджувач (карбонатні іони) виходить шляхом окислення з форміатних іонів. Окислювальну обробку відпрацьованої води шляхом додавання придатного окислювача, як пероксиду водню, дуже просто провести технічно, і вона дозволяє також обробити відпрацьовану воду, яка містить відносно високу концентрацію форміатних іонів. Однак можливо також, щоб окислювальна обробка проводилася виключно біологічною обробкою відпрацьованої води, яка містить форміати. При цьому відпрацьована вода, що містить форміати, може при необхідності розбавлятися до придатної концентрації. Окислювальна обробка відпрацьованої води, що містить форміати, проводиться переважно так, щоб концентрація форміату у відпрацьованій воді після окислювальної обробки була меншою 0,1ваг.%. Якщо порівнювати Cu/Zn/Al-каталізатор, одержаний із застосуванням форміату, з каталізаторами, які були одержані, виходячи з нітрату, то у каталізатора, одержаного способом згідно з винаходом, виявляється краща або порівнянна активність і порівнянна селективність. Також, довготривала стабільність каталізатора, одержаного із застосуванням форміату, визначена при 250°С в тесті на синтез метанолу, є трохи кращою або щонайменше порівнянною зі стабільністю каталізатора, який був одержаний, виходячи з нітрату металів. Тому об'єктом винаходу є також каталізатор, який може бути одержаний вищеописаним способом. Каталізатор згідно з винаходом в своїй оксидній формі містить менше 5ваг.%, переважно від 15 0,5 до 4ваг.%, зокрема переважно від 1 до 2ваг.%, форміату, який розраховується як мурашина кислота. Завдяки прожарюванню в м'яких умовах можна зберегти структуру форміату, яка, згідно з правилом "ключа і замка", що часто зустрічається в каталізі, може грати важливу роль в досягненні високої активності. При прожарюванні в щадних умовах при приблизно 170°С протягом 4 хвилин утворюється каталізатор, який має дуже високу активність при 250°С. Каталізатор згідно з винаходом відрізняється високим об'ємом мезопор. При цьому частка мезопор з радіусом від 3,75 до 7,0нм складає переважно більше 30%, переважно від 30 до 80% від всього об'єму пор. Повний об'єм пор включає об'єми пор з радіусом від 3,75 до 7500нм. Об'єм пор може бути визначений за методом вдавлювання ртуті. Переважно, повний об'єм пор, визначений для таблеток розміром 6 4мм, становить 100мм3/г-700мм3/г, переважно 250мм3/г-450мм3/г. Вміст міді, розрахований як CuO і віднесений до ваги оксидної форми каталізатора, з урахуванням втрати при прожарюванні при 600°С, вибирається переважно між 55 і 69ваг.%, зокрема переважно між 60 і 63ваг.%. Вміст цинку, розрахований як ZnO і віднесений до ваги оксидної форми каталізатора, з урахуванням втрати при прожарюванні при 600°С, вибирається переважно між 20 і 33ваг.%, зокрема переважно між 25 і 31ваг.%. Вміст алюмінію, розрахований як Аl2О3 і віднесений до ваги оксидної форми каталізатора, переважно вибирається між 5 і 20ваг.%, зокрема переважно між 8 і 11ваг.%. Процентні дані для вмісту міді, цинку і алюмінію розраховані на каталізатор, прожарений три години при 600°С. Крім того, каталізатор згідно з винаходом має в оксидній формі вміст лужних іонів, зокрема іонів натрію, переважно менше 500 частин/млн., зокрема переважно менше 300 частин/млн., зокрема від 100 частин/млн. до 300 частин/млн У своїй оксидній формі каталізатор згідно з винаходом має питому поверхню переважно більше 90м2/г, зокрема переважно більше 100м2/г. Каталізатор згідно з винаходом може бути виконаний як формоване тіло довільного вигляду. Наприклад, він може бути виконаний у вигляді кілець, формованих тіл з 3-20 отворами, таблеток з гладкою або хвилястою зовнішньою поверхнею або як стільники. Розмір формованого тіла відповідає звичайним значенням. Для одержання формовок порошковий каталізатор пресують, при необхідності з додаванням мастила, як графіт, наприклад, в таблетки, наприклад, розміром 6 4мм. Перед застосуванням каталізатор переводять з оксидної форми в активну форму. Для цього оксид міді щонайменше частково відновлюють до елементарної міді. Крім того, оксидну форму каталізатора згідно з винаходом переважно відновлюють в потоці водню. Активування можна провести безпосередньо в реакторі синтезу і переважно воно здійснюється тим, що спочатку проводять відновлення за допомогою інертного газу, такого 91547 16 як азот, що містить невелику кількість водню. Азот спочатку містить звичайно приблизно 2,0об.% Н2. При цьому температуру підвищують, наприклад, з 100 до 235°С протягом 16 годин. Потім вміст водню підвищують, причому, наприклад, відновлення ведуть з 2,0об.% Н2 (інше N2) протягом 3 годин в інтервалі температур від 235 до 270°С. Завершення відновної обробки може проводитися з 99,9%ним Н2 протягом приблизно 3 годин при температурі від 270°С до 300°С. Звичайно каталізатор активують при об'ємній швидкості приблизно від 3000 до 4000 літрів відновлювального газу в годину на літр каталізатора. У відновленому стані розмір кристалів міді дорівнює переважно приблизно 4-12нм, переважно 5-7нм. Каталізатор згідно з винаходом придатний, зокрема, для застосування в синтезі метанолу. Тому об'єктом винаходу є застосування вищеописаного каталізатора для синтезу метанолу з CO, CO2 і Н2. Синтез звичайно проводиться при температурі приблизно від 200 до 320°С, переважно від 210°С до 280°С, при тиску приблизно від 40 до 150 бар, переважно приблизно від 60 до 100 бар, і при об'ємній швидкості від приблизно 2000 до 22000, переважно від 8000 до 12000 літрів синтез-газу в годину на літр каталізатора, причому синтез-газ може містити приблизно від 5 до 25, переважно від 6 до 12об.% CO, приблизно від 4 до 10об.% СО2, приблизно від 10 до 30об.% N2 плюс СН4 (інертні гази) і як інше - Н2. Далі, каталізатор згідно з винаходом придатний для застосування в риформінгу метанолу, а також в низькотемпературній конверсії моноксиду вуглецю в діоксид вуглецю. Остання реакція, звана також низькотемпературним зсувом (LTS), проходить при температурах в діапазоні приблизно від 175 до 250°С, переважно від 205 до 215°С і відношеннях пар/газ в діапазоні приблизно від 0,4 до 1,5 (норм, л/норм. л). Типові сировинні газові суміші містять приблизно 3об.% CO, 17об.% СО2, 2об.% N2 і 78об.% Н2, які проводяться через реактор з об'ємною швидкістю приблизно від 2000 до 12000л сухого газу (тобто без води) на літр каталізатора в годину. З хорошими каталізаторами при об'ємній швидкості 11200год.-1 і відношенні пари до газу приблизно 1,5 досягаються міри перетворення CO від 70 до 85%. Далі винахід детальніше пояснюється на прикладах. Приклад (а) Одержання розчину міді 5054г суспензії Cu(OH)2 CuCO3 (вміст Сu: 27,7ваг.%, що відповідає 1400г Сu) диспергують в 10-літровій хімічній склянці і порціями змішують з 85%-ною мурашиною кислотою (D=1,1856г/см3), всього 2,399мл, поки не припиниться виділення СО2. Розчин міді має рН 2,35 і температуру 55°С. (b) Одержання розчину Cu/Zn (попередник першого розчину) У 5-літровій хімічній склянці з 781г ZnO і 4000мл Н2О одержують дисперсію ZnO. Дисперсію з'єднують з розчином міді, одержаним згідно з (а). При диспергуванні, що продовжується, порціями додають наступні 890мл мурашиної кислоти і 33,6 17 л демінералізованої води. Блакитний, спочатку злегка каламутний розчин перемішують доти, поки він не стане зовсім прозорим. (с) Одержання розчину карбонату натрію (другий розчин) Одержують 24000мл розчину Na2CO3, який має концентрацію приблизно 180г СО3/100мл, і розчин нагрівають до 70°С. (d) Одержання розчину І алюмінію У 5-літрову мішалку, обладнану пристроєм охолоджування, в якій знаходиться 2193мл м'якої води, додають 246,7г NaAlO2. Розчин нагрівають до температури максимум 30°С і потім порціями додають 350мл мурашиної кислоти. Молочного кольору розчин має рН приблизно 4,0. (є) Одержання розчину II алюмінію У мішалку, обладнану пристроєм охолоджування, в якій знаходиться 2,193мл води, порціями додають 246,7г NaAlO2. При цьому стежать за тим, щоб температура розчину не перевищувала 30°С. Суміш перемішують доти, поки не вийде прозорий розчин. (f) Осадження Розчин, одержаний згідно з (b), переводять в перший накопичувальний бак змішувального пристрою. Потім розчин І алюмінію, одержаний згідно з (d), вводять в бак і там перемішують при кімнатній температурі доти, поки з'єднані розчини не стануть повністю прозорими. При необхідності можна додати воду, щоб усунути опалесцентність розчину. Перед початком осадження розчин нагрівають до 70°С. Приблизно за 30 хвилин до початку осадження одержаний згідно з (є) розчин II алюмінію переводять в бак, причому утворюється молочна, блідо-голуба суспензія. Другий накопичувальний бак наповнюють одержаним згідно з (с) розчином Na2CO3 і нагрівають до 70°С. Розчини, що містяться в першому і другому баках, одночасно подають в змішувальний пристрій і після витримування протягом приблизно 20 с проводять звідти в перепускний бак. Швидкості закачування встановлюються так, що рН при осадженні становить 6,5±0,1. Зі змішувального пристрою суміш поступає в перепускний бак. З перепускного бака одержана суспензія проводиться в резервуар для дозрівання, де вона витримується при перемішуванні при приблизно 65°С. Осадження закінчується приблизно через 35 хвилин. Потім установку промивають приблизно 600мл зм'якшеної води і температуру в резервуарі для дозрівання підвищують до 70°С. По закінченні процесу промивання суспензію витримують при перемішуванні. Початок процесу дозрівання визначається кінцем процесу промивання. Використані в прикладах тривалості дозрівання вказані в таблиці 2. По закінченні дозрівання суспензію фільтрують, промивають зм'якшеною водою доти, поки залишковий вміст натрію в осаді на фільтрі не знизиться до менше ніж 350 частин/млн., і одержану тверду фазу сушать в протитечії шляхом розпилювального сушіння з використанням однокомпонентної форсунки Як подачу встановлюють суспензію із вмістом сухих речовин 30ваг.%. Температура гарячого газу на вході становить 330350°С, температура продукту на виході - 110 91547 18 120°С. Висушений порошок потім прожарюють 50 хвилин при приблизно 320°С або в фарфоровій чашці в поличній печі, або в працюючій періодично лабораторній обертовій трубчастій печі. (g) Обробка відпрацьованої води Відпрацьовану воду, що накопичилася при фільтрації і промиванні, обробляють пероксидом водню, причому за допомогою сірчаної кислоти рН утримують на рівні від 5 до 6,5, а температуру відпрацьованої води утримують на рівні 70°С. При цьому концентрацію форміату у відпрацьованій воді встановлюють на значеннях від 2,8ваг.% до 0,09ваг.%. Селективність, що визначається як число молів форміату, що прореагував, віднесене до числа молів пероксиду водню, що використовується, становить приблизно 60%. Порівняльний приклад (a) Одержання розчину нітрату міді/цинку До 9,79 кг розчину нітрату міді, який містить 1400г міді, додають 781,25г оксиду цинку. Потім додають 2077г азотної кислоти (58%-ної) і суміш перемішують доти, поки тверда фаза повністю не розчиниться. (b) Одержання розчину нітрату алюмінію У 1,5л повністю зм'якшеної води розчиняють 246,7г Na2AlO2. Потім додають 1365г азотної кислоти (58%) і перемішують доти, поки розчин не стане прозорим. Одержаний розчин нітрату алюмінію додають до розчину нітрату міді і цинку і розчин Cu/Zn/Al нагрівають до 60°С. (с) Одержання золю алюмінію У 1,5л повністю зм'якшеної води протягом 30 хвилин при перемішуванні розчиняють 246,7г Na2AlO2. Одержаний розчин додають до розчину Cu/Zn/Al і суміш нагрівають до 60°С. (d) Осадження У перший накопичувальний бак змішувального пристрою наливають суміш, одержану згідно з (с). У другий накопичувальний бак змішувального пристрою наливають 25л водного розчину, які містять 172г Na2CO3 на літр. Обидва розчини одночасно закачують в змішувальний резервуар і звідти суміш направляють в резервуар для дозрівання. По закінченні осадження змішувальний резервуар промивають повністю зм'якшеною водою, температуру в резервуарі для дозрівання підвищують до 70°С і осад витримують від 1 до 4 годин. По закінчення дозрівання суспензію фільтрують, промивають демінералізованою водою доти, поки залишковий вміст натрію в осаді на фільтрі не складе менше 350 частин/млн., і одержану тверду фазу сушать розпилювальним сушінням із застосуванням однокомпонентної насадки в протитечії. Вхідна температура гарячого газу становить 330350°С, температура продукту на виході - 110120°С. Потім висушений порошок прожарюють 50 хвилин при приблизно 320°С або в фарфоровій чашці в поличній печі, або в працюючій в періодичному режимі лабораторній обертовій трубчастій печі. Здійснені приклади осадження, а також наведені далі умови прожарювання зведені в таблицях 2а і 2b. У цих таблицях наведені також хімічні склади і фізичні параметри одержаних попередників оксидних каталізаторів. 19 Визначення фізичних параметрів проводилося таким чином: Визначення розмірів кристалів Сu: Розміри кристалів Сu визначають за допомогою рентгенівської дифракції порошків (XRD). Рефлекс Сu (III) вимірюють в діапазоні -43,3° (2 ). Півширина і інтегральна інтенсивність рефлексу розраховуються по функції псевдо-Фойгта. Розмір кристала Сu розраховується за допомогою функції Шеррера на основі розрахованої півширини. Для підготовки до рентгенографічного визначення розміру кристала оксидні каталізатори відновлюють таким чином: 2-5г таблеток розміром 6 4мм нагрівають в трубчастому реакторі з відновлювальним газом (98% N2, 2% Н2) від кімнатної температури до максимальної температури при швидкості нагрівання 2°С/хв. Каталізатори, які були одержані з форміатів, нагрівають до максимальної температури 80120°С. Каталізатори, які були одержані з використанням нітрату, гріють спочатку протягом ночі при 175°С. Потім протягом менше 2 годин встановлюють максимальну температуру: а) 180°С для каталізаторів, одержаних форміатним/карбонатним шляхом; b) 240°С для одержаних нітратно/карбонатним шляхом. При утриманні максимальної температури вміст водню в відновлювальному газі підвищують в кінці до 100% протягом години і потім зразок відновлюють ще 3 години. Визначення питомої поверхні Поверхня по БЕТ для порошкового оксидного каталізатора, а також для таблеток розміром 6 4мм визначають за одноточковим методом адсорбції азоту, згідно зі стандартом DIN 66132. Визначення втрати при прожарюванні Якщо треба визначити втрату при прожарюванні для таблеток, то їх спочатку розмелюють в порошок. Досліджуваний зразок зважують у зваженому фарфоровому тиглі, який до цього нагрівали 3 години при 600°С в муфельній печі і потім охолоджували в ексикаторі до кімнатної температури. Тигель нагрівали З години в муфельній печі до 600°С і потім охолоджували в ексикаторі до кімнатної температури. Охолоджений тигель знов зважували і з різниці визначали втрату при прожарюванні при 600°С. Визначення міцності на бічне стиснення Міцність на бічне стиснення визначали згідно зі стандартом DIN EN 1094-5, видання 1995-09, вогнестійкі вироби, призначене для ізоляції - частина 5: Визначення межі міцності на стиснення формованих виробів в холодному стані. Визначення проводилося на стандартному приладі, як Schleuninger 6-D або ERWEKA ТВН 310 MD, згідно з вказівками виробника приладу. Для репрезентативної кількості проби в 100 таблеток у випробуванні на опір продавлюванню визначався тиск пресування, що прикладається до їх циліндричної оболонки, і за допомогою статистичної програми, що є в приладі, розраховувалося середнє значення, стандартне відхилення, а також мінімальна і максимальна твердість. Розподіл таблеток по твердості (N) представлявся графічно. Визначення об'єму пор 91547 20 Об'єм пор для порошкових оксидних каталізаторів, а також таблеток розміром 6 4мм визначають по методу вдавлювання ртуті, додержуючись стандарту DIN 66133. Визначення вмісту форміату Приблизно 10-20г прожареного порошку каталізатора вводять в 300-мілілітровій колбі ЕрленМейера в (25+х)мл H2SO4 (25%) і розчиняють при нагріванні до приблизно 70°С. Кількість х мл H2SO4 (25%) визначається з мінімально необхідної додаткової кількості сірчаної кислоти, необхідної щоб досягнути повного розчинення наважки. Колбу наповнюють дистильованою водою до приблизно 100мл. Додаванням приблизно від 2,5 до 25мл NaOH (30%) встановлюють значення рН розчину 8-10. Потім розчин нагрівають щонайменше ще 5 хвилин при 70°С. Після цього додають 20мл розчину КМnО4 (0,2н) і розчин нагрівають до легкого кипіння щонайменше 30хв. Гарячий розчин підкисляють H2SO4 (25-50мл) і додають 20мл щавлевої кислоти (0,2н), щоб відновити діоксин марганцю і надмірний КМnО4 до Мn+2. Розчин щавлевої кислоти, що додається, повинен точно відповідати по кількості відновних еквівалентів окислювальному еквіваленту розчину перманганату. Нарешті, прозорий розчин титрують 0,2 н КМnО4, поки не з'явиться легке рожеве забарвлення. Розрахунок: Кожний мл витраченого 0,2н розчину КМnО4 відповідає 4,5мг форміату. Процентний вміст в зразку форміату виходить з: [% форміату]=[(мл витраченого 0,2н розчину КМnO4) (4,5мг форміату/мл 0,2н розчину КМnО4) 100)/(наважка кількості зразка в мг]. Спосіб дає надійні результати для концентрацій форміату в титрованому розчині від 0,08 до 0,5ваг.% з похибками
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for producing cu/zn/al catalyst, catalyst and its use
Автори англійськоюPolier Siegfried, DE); Hieke Martin, Hinze Dieter
Назва патенту російськоюСпособ получения cu/zn/al-катализатора, катализатор и его применение
Автори російськоюПолир Зигфиид (умер), Хике Мартин, Хинце Дитер
МПК / Мітки
МПК: C01B 3/16, C07C 29/154, B01J 37/03, C01B 3/32, B01J 23/80
Мітки: застосування, одержання, спосіб, каталізатор
Код посилання
<a href="https://ua.patents.su/12-91547-sposib-oderzhannya-cu-zn-al-katalizatora-katalizator-ta-jjogo-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання cu/zn/al-каталізатора, каталізатор та його застосування</a>
Наступний патент: Сенсорний пристрій
Випадковий патент: Генератор високочастотного переключення