Спосіб одержання суміші ізомерів синтетичних піретроїдів
Номер патенту: 19064
Опубліковано: 25.12.1997
Автори: Дьордь Хідаші, Тамаш Саболчі, Ержбет Радвані, Шандор Ботар, Антал Гайарі, Агнеш Хегедюш, Єва Шомфаі, Ласло Пап, Лайош Надь, Рудольф Шоош, Шандор Золтан, Іштван Секелі, Бела Барток
Формула / Реферат
1. Способ получения смеси изомеров синтетических пиретроидов общей формулы I
где X - хлор или бром, содержащих по меньшей мере 95 мас.% энантиомерных пар IR цис S, IS цис R и IR транс S, IS транс R в массовом соотношении от 55:45 до 25:75, отличающийся тем, что в расплав или в насыщенный раствор смеси энантиомерных пар IR цис S, IS цис R(1a), IR транс S, IS транс R(1b), IR цис R, IS цис S(1c), IR транс R, IS транс S(1d) в низшем спирте или его смеси с низшим галоидуглеводородом и/или низшем алкиловом эфире, таком как диизопропиловый эфир, или в углеводороде, таком, как петролейный эфир или гексан, добавляют затравленный кристалл, состоящий из смеси энантиомерной пары 1а и 1b в соотношении от 55:45 до 25:75, и осуществляют кристаллизацию при температуре от +30 до -10°С с последующим отделением при указанной температуре кристаллов энантиомерной пары, содержащей 1а и 1b.
2, Способ по п.1, οτличающийся тем, что процесс ведут в присутствии гидроксида калия и антиоксиданта, такого, как 2,6-дитретбутил-4-метилфенола.
Текст
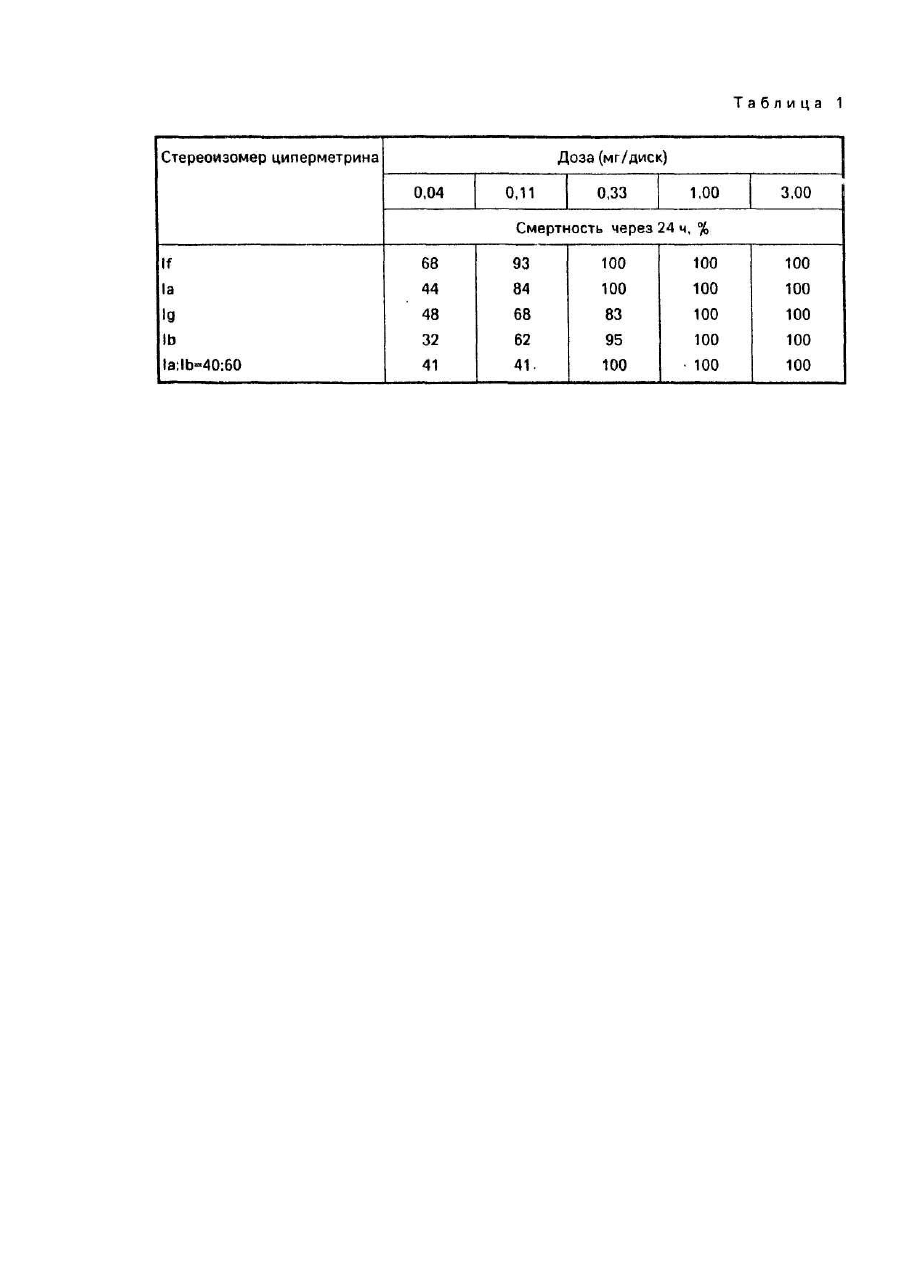
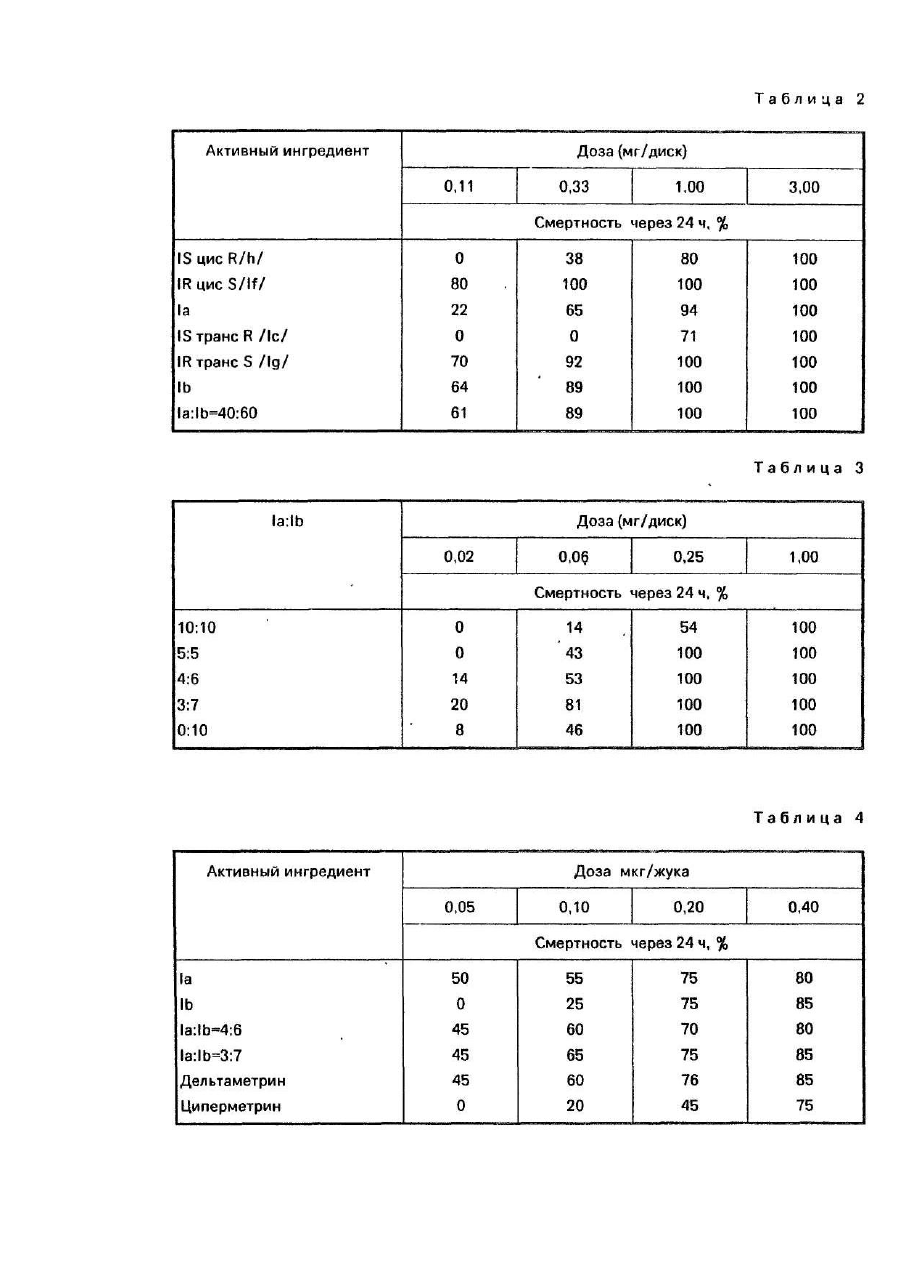
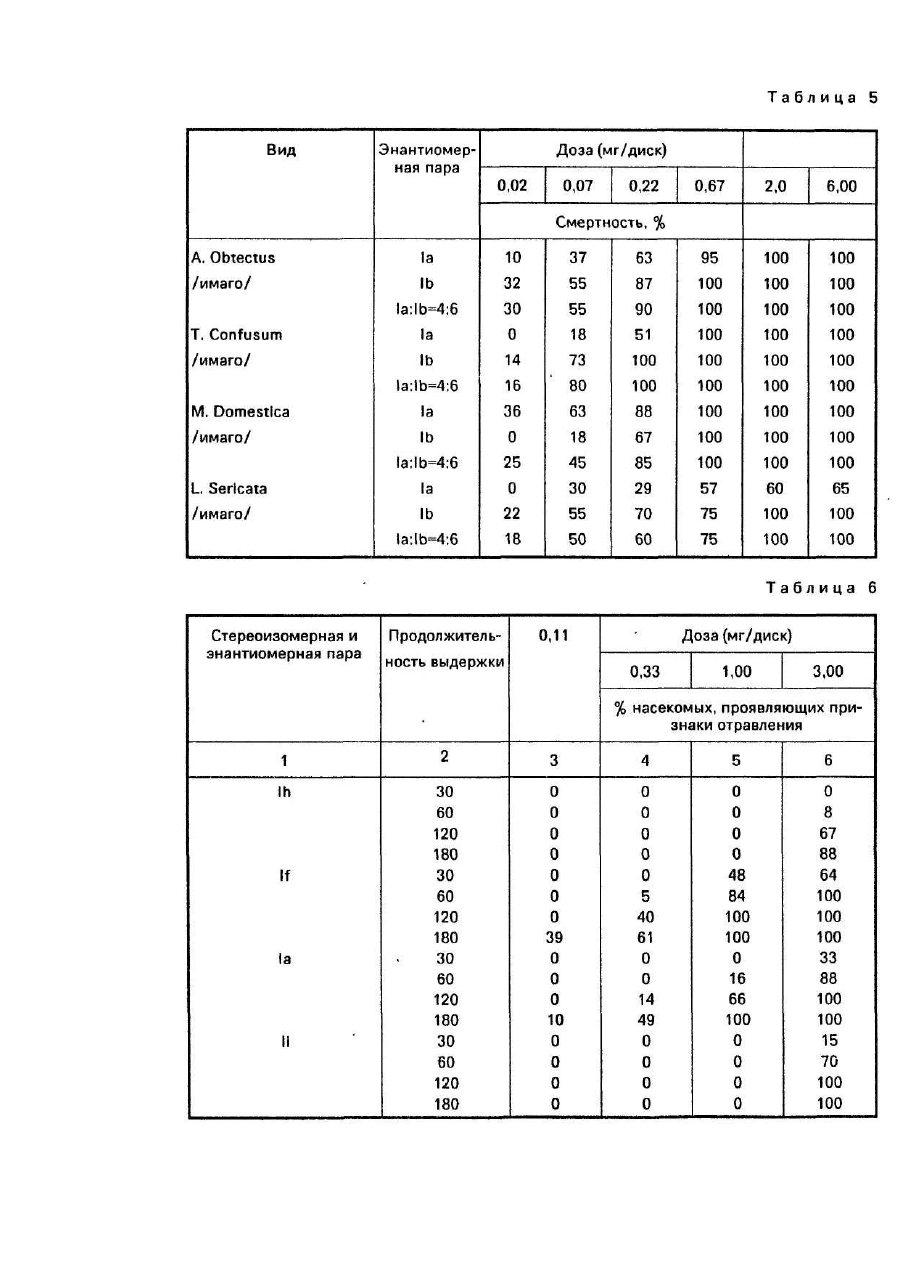
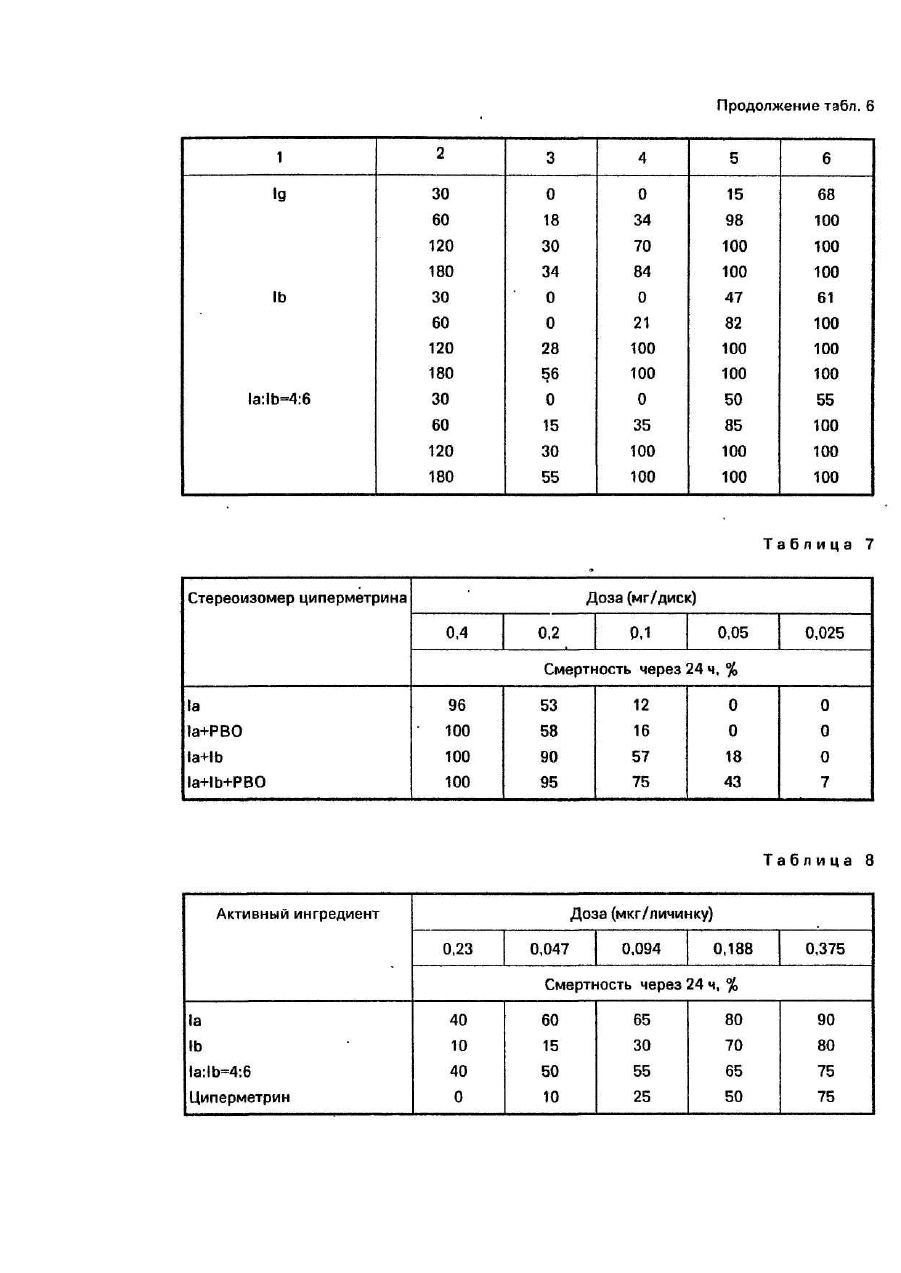
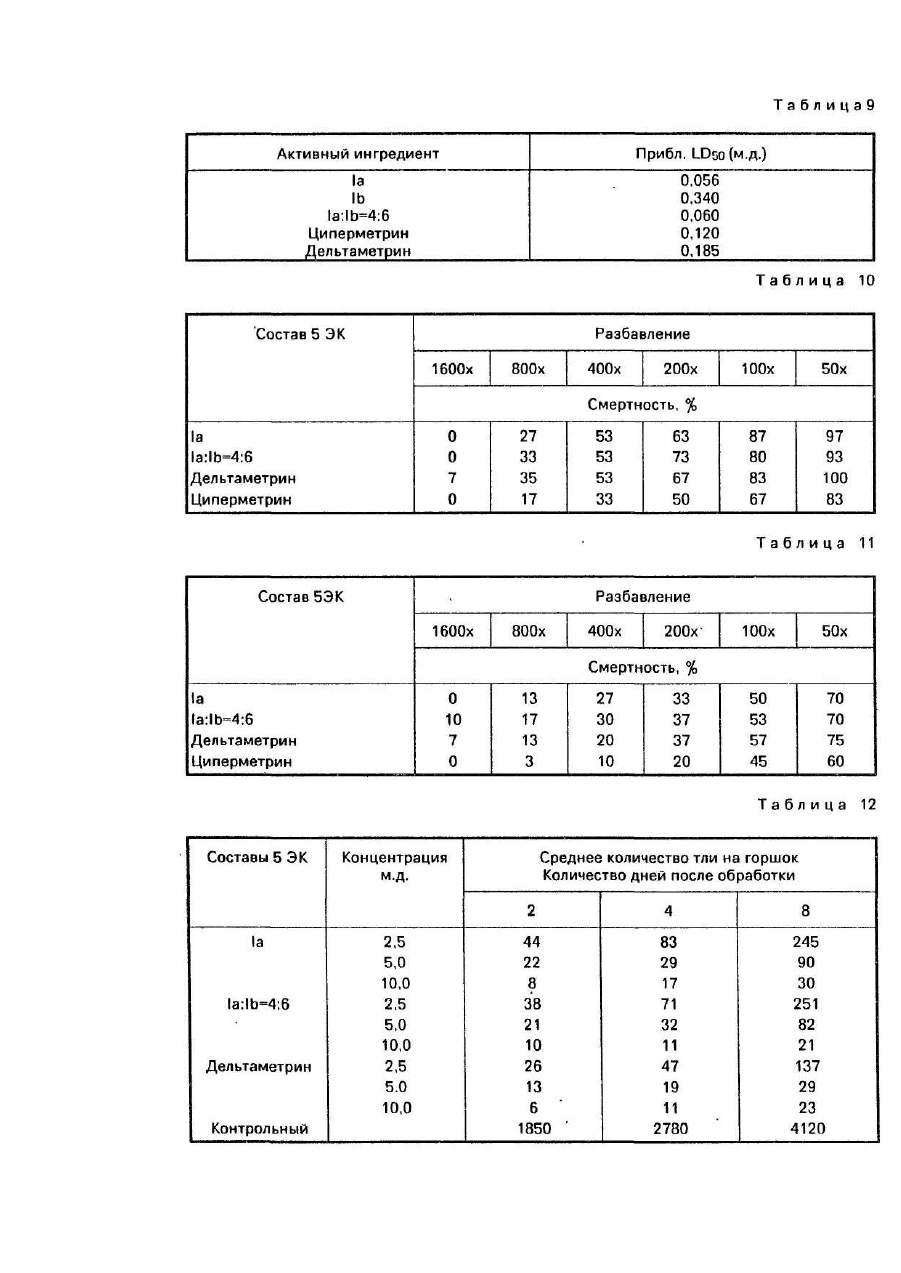
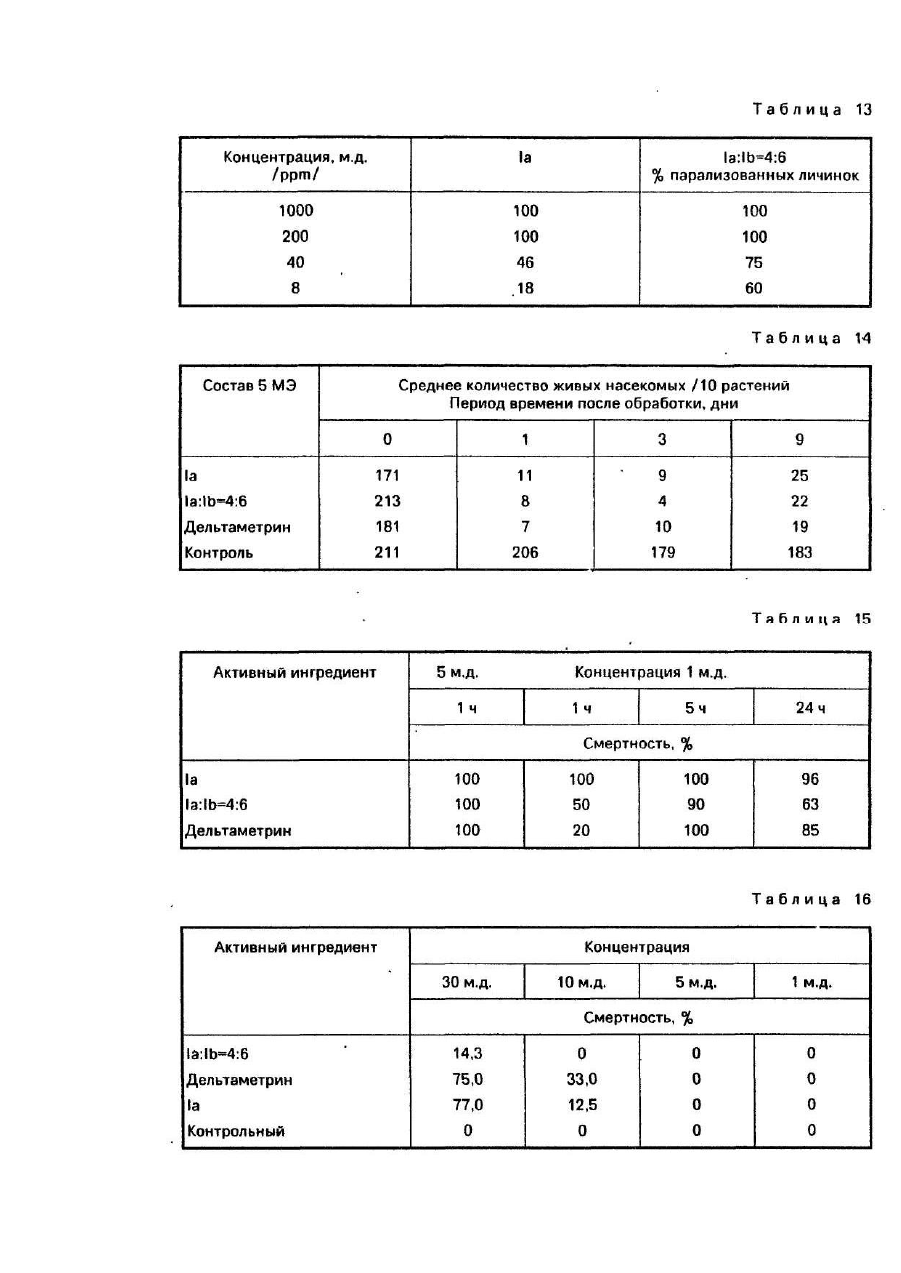
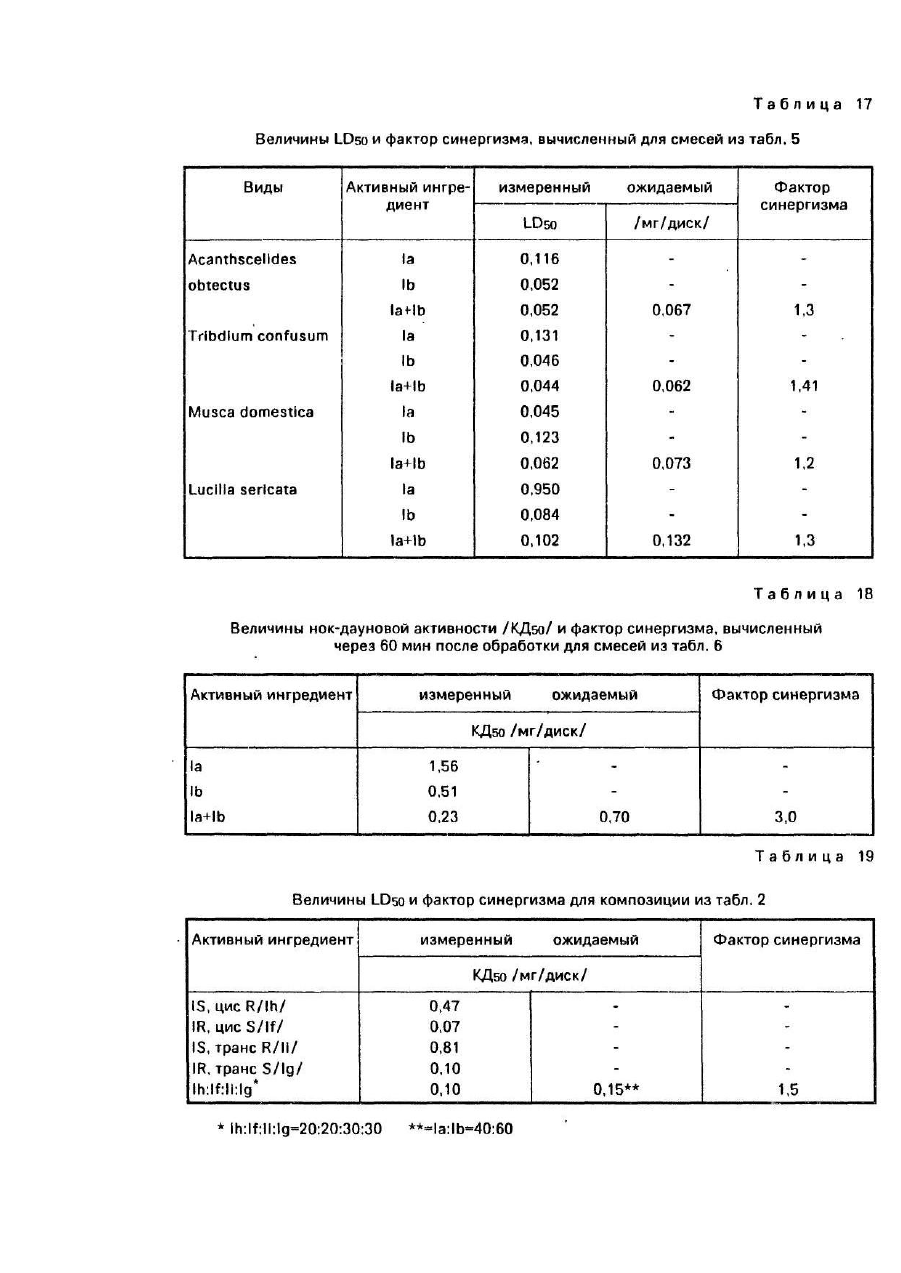
Изобретение относится -к способу получения изомеров синтетических пиретроидов общей формулы где X - хлор или бром, содержащих по меньшей мере 95 вес % энантиомерных пар IR цис S, IS и IR транс S, IS транс R в весовом соотношении от 55:45 до 25;75, которые могут быть использованы в сельском хозяйстве в качестве инсектицидов. В настоящем описании пространственная конфигурация заместителей, связанных с хиральным атомом углерода, обозначенная α, характеризуется "S" и "R" соответственно. Обозначения "цис" и "транс" соответственно указывают положение заместителей, связанных с атомом углерода "3" циклопропанового кольца, относящегося к пространственной конфигурации заместителей атома углерода "1". Абсолютная пространственная конфигурация заместителя, связанного с атомом углерода "Г обозначена символом "IR" и "IS" соотве тственно. Различные энантиомеры и энантиомерные пары обозначены при помощи следующи х сокращений: 1а - смесь IR цис S и IS цис R 1Ь - смесь IR транс S и IS транс R 1с - смесь IR цис R и IS цис S 1d - смесь IR транс R b IS транс S 1f- IR цис S 1g - IR транс S 1h-IS цис R 1i-IS трансR Из соединений общей формулы I известны следующие "Циперметрин" формулы II включая все изомеры. "Альфаметрин" формулы II, включая только изомеры IR цис S и IS цис R. "Дельтаметрин" формулы III включая только изомер IR цис S Выбор возможных изомеров по инсектицидному действию основан на экспериментально установленном факте, что в особенности согласно опытам, проведенным на домашней мухе (Muscadomestlca) -некоторые изомеры проявляют себя как высоко токсичные вещества по отношению к некоторым насекомым. Известно, что пиретроид формулы II (известный под родовым названием "циперметрин") относится к ценному семейству синтетических пиретроидов и использован в качестве инсектицида. Циперметрин получают взаимодействием м-феноксибензальдегидциангидрида с хлорангидридом циклопропанкарбоновой кислоты в присутствии основания и, как указано выше, состоит из восьми стереоизоме-ров (четыре энантиомерные пары). Если применяют смесь в весовом отношении 60:40 хлорангидридов транс и цис-цикло-пропанкарбоновой кислоты, то целевой продукт представляет смесь 1819% энантиомерной пары 1а 21-22% энантиомерной пары, 1с 26-27%-энантиомерной пары 1Ь и 33-34% энантиомерной пары 1d. В соответствии с известным уровнем сте-реоизомеры циперметрина проявляют различную биологическую активность. Вообще принято считать, что активность молекул, включающих в себя цисциклопропанкарбоновые кислоты, выше активности соответствующи х транс-производных. Сравнительные испытания, включая стероизомерные пары циперметрина, проведены на видах домашней мухи (Musca domestica) и Phaedon cochlerial Fab. Для хлорпроизводных, транс-изомеров IR транс S(lg) и IR транс R, сравнительные данные показывают, что, в то время изомер IR транс S обладает высокой активностью; изомер IR транс R проявляет значительно меньшую активность (в соответствии с опытом активность относящаяся к биоресметрину (100), достигает 1400 и 81 соответственно для домашней мухи и 2200 и 110 соответственно для Phaedon cochlearial. Далее показано, что активность смеси обоих испытанных изомеров ниже расчетного значения, изомеры проявляют антагонизм и степень антагонизма составляет 1,42 и 1,46 для домашней мухи и Mustard Beetle, соответственно. В результате указанных испытаний и публикаций активности транс-изомерам и их смесям был потерян биологический интерес и исследования были сконцентрированы вокруг активных цис-производных и их смесей. Поэтому стали разрабатывать смеси, обогащенные цис-изомерами. Так известно получение смеси, обогащенной цис-изомером, в основном смесь 1:1 изомеров IR цис S и IS цис R, которая может быть выделена из смеси, содержащей также другие цис-изомеры путем кристаллизации из растворов с применением подходящих растворителей. Целью изобретения является разработка способа получения новой смеси изомеров синтетических пиретроидов , которые являются более активными, Поставленная цель достигается способом получения смеси изомеров синтетических пиретроидов общей формулы 1, отличительная способность которой состоит в том, что в расплав или в ненасыщенный раствор смеси энантиомерных пар IR цис S, IS цис R(1a) и IR транс S, IS транс R(1b) и IR цис R, IS цис S(1c), IR транс R, IS транс S(1d) в низшем спирте или его смеси с низшим галоидуглеводородом и/или в низшем алкиловом эфире, таком как диизопрапиловый эфир, или в углеводороде, таком как петро-лейный эфир или гексан, добавляют затравочный кристалл, состоящий из смеси энантиомерной пары 1а и 1Ь в соотношении от 55:45 до 25:75 и осуществляют кристаллизацию при температуре от (+)30 до (-} 10°С с последующим отделением кристаллов энантиомерной пары, содержащей 1а и 1Ь, в количестве достаточном для получения целевого продукта в требуемом весовом соотношении при указанной выше температуре. Предпочтительно процесс вести в присутствии антиоксиданта, такого как 2,6 ди-третбутил-40метилфенола и гидроксида калия. Смеси изомеров, полученные согласно данному изобретению обладают синергиче-ским эффектом. Кроме того, смеси изомеров, полученные согласно предложенного способа менее токсичны по отношению к млекопитающим, чем известные композиции, обладающие сходной эффективностью. Изобретение иллюстрируется примерами. Пример 1/1. 100 г циперметрина {состоящего, согласно результатам анализа методом газовой хроматографии, из смеси 18,2%, 1a 21,8% 1с, 26,8% (1b) и 33,2% (1d) 0,2 г едкого калия и 0,2 г 2,6дитретбутил-4-метилфенола растворяют в 2000 мл изопропанола при постоянном перемешивании при температуре 45,0°С. Раствор медленно охлаждают до температуры 30°С, осветляют активированным углем и фильтруют при температуре 30°С. В бесцветный раствор вводят затравочный кристалл, состоящий из 60% 1Ьи40% 1аи смесь перемешивают при температуре -10°С в течение 24 часов. Выпавший в осадок продукт отфильтровывают, промывают изопропанолом и сушат в вакууме. Таким образом, получают 36,02 г белоснежного кристаллического продукта. Т.пл. 62-65°С (не скорректированное значение). Согласно анализам методами газовой и тонкослойной хроматографии продукт содержит 37% изомеров 1а и 58% изомеров 1Ь. Выход 76% (в расчете на содержание изомеров 1а+1Ь в исходном материале пиперметрине). Изомер 1aRf = 0,25, изомер 1b Rf = 0,20. После кристаллизации из изопропанола получено 32 г продукта в виде первой культуры. Т.пл. 63,565,0°С, продукт состоит из 39,5% 1а и 59,5% 1b, 0,5% - изомеры 1с и 1d. ИК/KBr с ν С = 0: 1730, 1735 см"1. ЯМР(СОСl3) d (м.д.): 1,05-2,45т(8Н),5,6 d. J = 8 Гц. (=СН транс 0,6Н), 6,14 d. J = 8 Гц (=СН цис 0,4Н), 6,35 d (1 Η), 6,85-7,60 m (9H). Пример 1/2, 100 г циперметрина (27,8% 1а, 21,8 1b, 32,1% 1еи18,2% 1d),0,2r гидроксида калия и 0,2 г 2,6дитретбутил-4-метилфенола растворяют в 2000 мл изолропанола при перемешивании при температуре 45°С. Раствор осветляют активированным углем и фильтруют при температуре 30°С. В бесцветный раствор вводят затравочный кристалл, состоящий из 20% 1Ь и 80% 1а и перемешивают при температуре -10°С в течение 36 часов. Выпавший в осадок продукт отфильтровывают, промывают изопропанолом и высушивают в вакууме. Таким образом получают белоснежный кристаллический продукт. Т.пл. 66-73°С. В соответствии с результатами анализа методом газовой хроматографии продукт содержит 77% 1а + 19% 1Ь, чистота 96% (тонкослойная хроматография, см. пример 1). После перекристаллизации из изопропанола в качестве первого поколения получено 26,5 г белоснежного кристаллического продукта, т.пл, 70-73°С, содержание 81,5% 1а +18% 1Ь (анализ методом газовой хроматографии). ИК(КВr) ν С = 0: 1730 см -1. ЯМР CDCI3) d (м.д.); 1,05-2,45 т(8Н), 5,60 d, J = 8 Гц. (=СН транс 0,2Н), 6,14 d, J = 8 Гц (=СН цис 0.8Н), 6,35 й (АгС 1Н), 6,85-7,60 m (9Н). Пример 1/3. В 100 г бесцветного прозрачного маслянистого циперметрина (18,2% 1а. 21,8% 1с, 26,8% 1b и 32,2% 1d) вводят затравочный кристалл, состоящий из 60% 1b и 40% 1а, и расплав оставляют кристаллизоваться при температуре 7°С в течение недели. Смесь суспендируют в 100 мл смеси изопропанол/диизопропиловый эфир 1:1 и фильтруют при температуре -15°С. Кристаллы промывают изопропанолом и высушивают в вакууме. Таким образом получают 40,1 г белого кристаллического продукта, содержащего 37,5% 1а и 59% 1b, т.пл. 62,5-65°С. Выход 86%, После перекристаллизации из изопропанола получают в виде первого поколения 36 г белоснежного кристаллического продукта с температурой плавления 63,5-65°С, состоящего из 40% 1а и 60% 1b (газовая хроматография), ИК и ЯМР идентичны приведенным в примере 1. Пример 1/4. 100 г циперметрина (18,2% 1а, 21,8% 1с, 26,8% 1Ь, 33,2 1d)n0,05r 2,6-дитретбутил-4метилфенола растворяют в 100 мл диизопропилового эфира при постоянном перемешивании при температуре 0°С. Раствор осветляют активированным углем (2 г), фильтруют и при температуре 15°С вводят затравочный кристалл, состоящий из 60% 1 b и 40% 1а. Смесь оставляют кристаллизоваться в течение 72 часов, кристаллы отфильтровывают, промывают диизопропиловым эфиром и изопропанолом и сушат. Таким образом получают 38 г белоснежного кристаллического продукта, т.пл, 62-65°С, состоящего из 37,5% 1а и 58% 1b. Выход 80,6%. После перекристаллизации из изопропанола в качестве первого поколения получают 35 г белоснежного кристаллического продукта, т.пл. 63,5-65°С, соотношение изомеров 1 а: 1 b составляет 40:60. Физические константы идентичны приведенным в примере 1. Пример 1/5. Юг образцов продукта, полученного согласно примеру 2 (соотношение изомеров 1а:1b равно 4:1) смешивают с 4,60 г, 6 г, 10 г, 16,67 г и 22,0 г чистых затравочных кристаллов 1b соответственно. Полученные таким образом смеси перекристаллизовывают, как описано в примере 1, из десятикратного количества изопропанола каждую. Состав и температуры плавления полученных таким образом продуктов следующие: Пример 1/6. 10 г образцов чистой кристаллической пары изомеров 1а смешивают с 8,20 г, 10,00 г и 15,00 г чистой кристаллической пары изомеров 1b соответственно. Смеси гомогенизируют. Получены таким образом кристаллические смеси, содержащие вещества 1а + 1b в соотношении 55:45, 50:50 и 40:60 соответственно, т.пл. 62,5-64°С, 60,5-62°С и 63,5-65°С, соответственно. Пример 1/7. 10 г образцов чистой кристаллической пары изомеров 1а растворяют в десятикратном количестве изопропанола и к каждому образцу добавляют 23,43 г и 30,0 г чистой кристаллической пары изомеров 1Ь соответственно. Растворы кристаллизуются. Выпавшие в осадок белые кристаллические продукты (т.пл. 65-68°С и 67-71,5°С соответственно) содержат изомеры 1а:1b в соотношении 30:70 и 25:75 соответственно. Полученный таким образом продукт может быть использован в качестве активного инсекционного ингредиента. Пример 1/8. В смеси 1900 мл изопро-пилового спирта и 100 мл четыреххлористо-го углерода при постоянном перемешивании при 45°С растворяются 100 г циперметрина состоящего согласно газовой хроматографии из смеси 18,2% 1а, 26,8% 1b, 21,6% 1с и 33,2% 1d, 0,2 г гидроокиси калия и 0,2 г 2,6дитретбутил-4-метилфенола. Раствор медленно охлаждается до 30°С и очищается с помощью 2-5 г активированного древесного угля и фильтруется быстро при 30°С. Полученный бесцветный раствор подвергается затравке с помощью затравочного кристалла, состоящего из 60% 1b и 40% 1а и постепенно охлаждается до -15°С. Смесь перемешивается при -15°С в течение 6 часов и оставляют нагреваться до комнатной температуры. Смесь перемешивается при комнатной температуре в течение 2 часов и постепенно охлаждается до -12°С, а затем оставляют кристаллизоваться в течение дополнительных 4 часов. Выпавший в осадок продукт реакции фильтруется, дважды промывается с помощью 50 мл холодного изопропилового спирта и высушивается в вакууме. Таким образом получается кристаллический продукт снежно-белого вида (36,0 г). Т.пл. 62-65,5°С (неисправленное значение). Согласно ГХ - анализа продукт содержит 30% 1а и 57,5% 1Ь изомеров. Выход: 76,4% (относительно содержания 1а + 1b изомеров в исходном циперметрине). После перекристаллизации из 360 мл изопропилового спирта получается как первая фракция 31,5 г снежно-белого кристаллического продукта (содержащего 39,5% 1а и 59,5% 1b изомеров (по ГХ-анализу). Т.пл., 63,5-65,0°С. Данные ИК- и ЯМР-спектроскопии являются идентичными с таковыми, раскрытыми в примере 4. Пример 1/9. 100 г бесцветного, прозрачно-чистого маслянистого циперметрина (состоящего по данным газовой хроматографии из смеси 18,2% 1а, 26,8% 1b, 21,8% 1с и 38,2% Id) оставляют кристаллизоваться при 11°С в течение двух недель. Вязкая смесь суспендируется в 100 мл смеси 1:1 изопропилового спирта и диизопропилового эфира при -15°С, а затем быстро фильтруется. Полученные кристаллы промывают дважды с помощью 50 мл изопропилового спирта и высушиваются в вакууме. Таким образом получается 38 г снежно-белого кристаллического продукта, т.пл.: 62,0-65,5°С, содержащего 38% 1а и 59% 1b изомеров (по ГХ-анализу). Выход: 81,5% относительно содержания 1а+1b изомеров в исходном циперметрине. Продукт перекристаллизовывается из 380 мл изопропилового спирта и получается как первая фракция 32,0 г снежно-белого кристаллического продукта. Т.пл. 63,5-65°С, содержащий 40% 1а и 60% 1Ь изомеров (по ГХ-анализу). Данные ИК- и ЯМР-спектроскопии являются идентичными с таковыми, показанными в примере 4. Пример 1/10. 100г(3-)21.21-дибром-винил(2,2-диметил-циклопропанкарбоксил-ат-(a-циан-м-феноксибензила состоящего, согласно результатам анализа методом газовой хроматографии, из смеси 20% 1а, 20% 1с, 30,0% 1b и 30,0% 1d), 0,2 г едкого кали и 0,2 г 2,6-дитретбутил-4-метилфенола растворяют в 2000 мл изопропанола при постоянном перемешивании при температуре 45,0°С. Раствор медленно охлаждают до температуры 30°С, оставляют активированным углем и фильтруют при температуре 30°С. В бесцветный раствор вводят затравочный кристалл, состоящий из 60% 1b и 40% 1а и смесь перемешивают при температуре -10°С в течение 24 часов. Выпавший в осадок продукт отфильтровывают, промывают изопропанолом и сушат в вакууме. Таким образом получают 30 г белоснежного кристаллического продукта. Т.пл. 69-73°С. Согласно анализам методами газовой и тонкослойной хроматорафии продукт содержит 38% изомеров 1а и 58% изомеров 1b. Выход 76% (в расчете на содержание изомеров 1а+1b в исходном материале циперметрине). Изомер 1а Rf = 0,4, изомер 1b Rf = 0,37 на силикагелевой пластинке G60 с элюентом-смесью гексан:диэтиловый эфир = 6:1). ЯМР (CDCl3 d (м.д.): 1,20-2,25 m (8H), 6,17 d (=СН транс, 0,6Н); 6,70, d (=CH цис, 0,4Н), 6,38, d (1H). 6,857,60 m (9H). После перекристаллизации из изопропанола получено 26 г продукта в виде белых кристалликов. Т.пл. 7075°С, продукт состоит из 39,0% 1а и 60-0% 1b. Пример 1/11.100 г сложного (a-циа-но-м-феноксибензилового) эфира 3 (2 ,21 дибромвинил)-2,2-диметилциклопропан-карбоновой кислоты, содержащей 20,0%, 1а, 30,0% 1b, 20,0% 1с и 30,0% 1d),0,2 г гидроксида калия и 0,2 г 2,6-дитретбутил-4-метил-фенола растворяют в 2000 мл изопропанола при перемешивании при температуре 45°С. Раствор осветляют активированным углем и фильтруют при температуре 30°С. В бесцветный раствор вводят затворочный кристалл, состоящий из 20% 1b и 80% 1а и перемешивают при температуре -10°С в течение 36 часов. Выпавший в осадок продукт отфильтровывают, промывают изопропанолом и высушивают в вакууме. Таким образом получают 18 г белоснежного кристаллического продукта, т.пл. 80-85°С. В соответствии с результатами анализа методом газовой хроматографии продукт содержит 78% 1а + 19% 1b. После перекристаллизации из изопропанола получено 16,0 г белоснежного кристаллического продукта, т.пл. 82-85°С, содержание 81,5% 1а+18% 1Ь (анализ методом газовой хроматографии). Пример 1/12. 100 г циперметрина, содержащего, согласно газовой хроматографии, смесь из 18,2% 1а, 26,8% 1Ь, 21,6% 1сиЗЗ,2% 1dn 0,2 г 2,6-ди-третичныйбутил-4-метил-фенола растворяют в 750 мл нефтеэфира с точкой кипения от 70 до 100°С или гексана при постоянном перемешивании при 45°С. Раствор медленно охлаждают до 30°С, быстро осветляют древесным углем 0,5 г и фильтруют при 30°С. Полученный бесцветный раствор засевают затравочным кристаллом, содержащим 55% 1b и 45% 1а и постепенно охлаждают до 20°С. Смесь перемешивают 2 дня, а затем постепенно охлаждают до 5-10°С. После перемешивания в течение 1 дня суспензию постепенно нагревают до комнатной температуры, и так охлаждение и нагревание повторяют несколько раз. Осажденный продукт отфильтровывают, дважды промывают 50 мл нефтеэфира и сушат под вакуумом, таким образом получают 30 г снежно-белого кристаллического продукта. Точка плавления 63,5°С. Чистота 93%. Соотношение изомеров 1а:1b = 45:55. Примеры приготовления составов. Пример 2/1. К 166,2 г перлита (dmax = 120 мкм) добавляют 0,8 г синтетической кремниевой кислоты (Аэросил 300) в скоростной мешалке кипящего слоя. Затем добавляют 20 г циперметриновой смеси энантиомерных пар 1а:1Ь = 4:6 и 2 г простого эфира спирта жирного ряда и полигликоля, так что смесь равномерно гомогенизирована. Порошкообразную смесь измельчают сначала в механической мельнице, затем в пневматической, после чего в скоростной мешалке добавляют 5 г олкоктилфенолполигликолевого эфира (ЕО = 20) и 2 г сульфосукцината. Полученную таким образом смачивающуюся порошкообразную смесь (СП) испытывают на суспензионную стойкость, Продолжительность смачивания = 23 секунды, текучесть = 99% (стандартный метод WHD). Пример2/2. К 3г смеси циперметри-новых энантиомерных пар 1а:1b = 3:7 и 0,3 г спирт жирного ряда полигликолевого эфира добавляют в гомогенизаторе тальк (-dmax = 15 мкм), доведенной до значения рН = 6,5 при помощи буфера 0,8 г синтетической кремниевой кислоты (Аэрозил 200) и 193,9 г фосфата калия и натрия. К смеси при перемешивании добавляют 1 г диоктилсульфосукцината и 1 г сульфоната спирт жирного ряда полигликолевого эфира и смесь измельчают до среднего размера частиц 20 мкм. Таким образом получают тонкий текучий порошок. Пример 2/3. Растворяют при медленном перемешивании 5 г смеси циперметриновых энантиомерных пар 1а:1b - 55:45 в смеси 21,25 г ксилола и 42,5 г н-пропанола. К раствору добавляют при перемешивании смесь 4 г этоксилированного алкилфенола + кальциевая соль линейного алкилзрилсульфоната и смесь 6 н этоксилированного амина + соль щелочного металла линейного алкиларилсульфоната до полного растворения всех ве ществ, после чего добавляют 21,25 г воды. Таким образом, получают прозрачный раствор, сохраняющий свои свойства в течение длительного периода времени в температурном интервале 050°С. Раствор необязательно может быть разбавлен водой в любом соотношении с образованием эмульсии с размерами частиц 0,8-1,5 мкм. Пример 2/4. Растворяют 5 г смеси циперметриновых энантиомерных пар 1а:1b = 25:75 в смеси 75 г ксилола и 10 г алифатического масла, после чего добавляют при медленном перемешивании смесь (7,5 г) этоксилированного алкилфенола + кальциевая соль линейного алкиларилсуль-фоната, а также смесь (2,5 г) этоксилированной жирной кислоты + соль линейного алкиларилсульфоната. Испытания по методу CJPAC показали стойкость эмульсионного концентрата после 170 часов. Пример 2/5. Смешивают в механическом грануляторе смесь 50:50 циперметриновых энэнтиомерных пар 1а и 1b с 1500 г щелочной соли поликарбоксилата, 500 г додецибензолсульфоната натрия, 500 г сахарозы и 7200 г каолина. Порошкообразную смесь смешивают с 8300 мл воды в мешалке с большой силой сдвига (ν = 10 мкс) и сушат распыливанием. Распределение размеров частиц следующее: 0,1-0,4 мм 95%. Текучесть 98% (по методу НО). Пример 2/6. Приготовлены эмульгирующиеся концентраты (ЭК) путем смешения следующи х компонентов: Примеры на биологическую активность. Пример 3/1.В табл.1 представлена активность различных стереоизомеров циперметрина по отношению к домашней мухе (Muscadomestica). Испытание проведено следующим образом. Активный ингредиент растворяют в смеси масла и ацетона 1:2, пропитывают фильтровальные бумажные диски (Whatman № 1, диаметр 9 см) растворами соответствующи х стереоизомеров и энантиомерных пар соответственно. Добавляют ацетон для испарения, после чего насекомых кладут на фильтровальные бумажные диски, помещенные на чашки Петри. Для каждой дозы проводят три параллельных опыта и в каждую чашку Петри кладут по 15 насекомых. Процент смертности определяют через 24 ч. Корректированный процент смертности вычислен по формуле Аббота. Согласно этому испытанию активность смеси 1а:1b соответствует активности чистого изомера 1а. Пример 3/2. Из табл.2 видно, что повышенная активность, проявившаяся в примере 14, обусловлена синергическим действием трансизомеров. В примере 18 показано на других вида х насекомых, что энантиомерная пара 1b согласно настоящему изобретению более активна, чем 1а. Повышенная активность проявляется не только в смертности через 24 часа, но также и в факте, что токсическое действие проявляется быстрее. Пример 3/3. В табл.3 инсектицидное действие смесей энантиомерных пар 1а и 1b в различных соотношениях показано на хрущаке малом мучном (Tribollum confum). Методика испытания описана в примере 14. Приведенные данные доказывают синергизм энантиомерных пар 1а и 1b. Пример 3/4. Согласно настоящему изобретению, если смеси энантиомерных пар 1а и 1b сочетают с обычными пиретроидными синергистами (например, пиперонилбутоксидом, ΝΙΑ 16388 и т.д.), активность повышается до значения, превышающего обычное значение (см. пример III/4). В табл.4 представлена активность по отношению к колорадскому картофельному жуку. Методика испытания заключается в следующем. Испытуемый материал растворяют в 2-этоксиэтаноле (целлозоле Cellosolve). Одну каплю раствора объемом 0,3мкл наносят на брюшинн'о-грудную область имаго. Для каждой дозы проводят две параллельные обработки и для каждой обработки применяют 10 насекомых. Смертность определяют через 48 ч. Наблюдается синергизм между знанти-омерными парами 1а и 1b, хотя по отношению к имаго колорадского картофельного жука 1а более активна, чем 1Ь. Смеси энантиомерных пар 1а и 1b проявляют такую же активность, как дельтаметрин. Пример 3/5. Проведены сравнительные испытания 1а, 1b и 40:60 смеси 1а:1b на зерновые фасольной Acanthoscelides obtectus), хрущаке, малом мучном (Fribollum confusum), домашней Myxe(Musca domestica) и мухе падальной (Lucilla Scricate). Применена методика, описанная в примере III/1. Результаты представлены в табл.5. Пример 3/6. Активность циперметриновых стереоизомерных пар в зависимости от продолжительности выдержки испытана на хрущаке малом мучном (Tribolium confusum). Имаго хрущака малого мучного (Trlbllum confusum) выдерживают в чашках Петри по методике, описанной в примере 14. Для каждой дозы проводят три параллельных опыта и для каждого параллельного опыта применяют по 15 насекомых. Для каждого момента времени подсчитывают количество насекомых, лежащих на спине, и результаты в процентах сведены в табл.6. Пример 3/7. Имаго хрущака малого мучного (T.confusum) обрабатывают по способу, аналогичному описанному в примере H1/1. В качестве синергиста применяют пиперонилбутоксид в дозе 0,5 мг/диск. Можно видеть, что смесь энантиомеров 1а и 1Ь испытывают больший синергизм, чем энантиомер 1а (1а:1b = 4:6). Пример 3/8. Активные ингредиенты растворены в 2-этоксиэтане и растворы нанесены в виде капелек объемом 0,2 мкл на спинки гусениц американской белой бабочки (Hyphantria cunea) в стадии L7-L8. Обработанные гусеницы помещают на листья земляники в чашки Петри. Для каждой дозы проводят два параллельных опыта с применением 10 насекомых. Через 24 ч подсчитывают количество мертвых гусениц и вычисляют процент смертности. Результаты представлены в табл.8. Пример 3/9. Опыляют листья, зараженные клещем паутинным (Tetranychues witicae). Через 24 ч сравнивают смертность на обработанных листьях со смертностью на контрольных листьях. Пример 3/10. Пять составов эмульгирующихся концентратов (ЭК), приготовленных по методу, описанному в примере 13, разбавляют водой 50х, ЮОх, 200х, 400х, 800х и 1 600х и дозы по 0,5 мл напрыскивают на стеклянные пластины. После сушки на каждую стеклянную пластину помещают 10 имаго. Ldecemlineata и пластину закрывают чашкой Петри. Исследования проводят путем применения 6 доз и 3 параллельных опытов для каждой дозы. Количество мертвых насекомых подсчитывают через 48 ч. Результаты приведены в табл.10. Пример 3/11. На стеклянные пластины напрыскивают составы 5 ЭК (эмульгирующиеся концентраты), приготовленные в соответствии с примером 13 аналогично примеру 23. После сушки на каждую пластину помещают 10 имаго зерновки фасольной (Acanthascelides obtectus) и насекомых накрывают чашками Петри. Через 24 ч подсчитывают количество мертвых насекомых. Исследование проводят с 6 дозами, применяя три параллельных опыта для каждой дозы. Результаты приведены в табл.11. Πримеры 3/12. 15 бобовых растений, зараженных тлей, персиковой зеленой (Myzus persicae) в 6-дневном возрасте, выращивают в каждом горшке. В возрасте 12 дней отбирают сильно и равномерно зараженные растения и опрыскивают их до стекания свежеприготовленной эмульсией состава согласно примеру 13. Обработку проводят тремя дозами (содержание активного ингредиента 2,5, 5 и 10 м.д.) и проводят четыре параллельных опыта (один горшок на каждый параллельный опыт). На второй, четвертый и восьмой день после обработки тлю сметают с растений на белую бумагу тонкой кистью и подсчитывают количество живых насекомых. Результаты приведены в табл.12. Пример 3/13. Томаты, предварительно выращенные в горшках, опрыскивают суспензией, активного ингредиента, приготовленной со смесью ацетона и воды. Обработанные растения помещают в изоляторы и заражают личинками Leptinotarsa decemlireara на стадии L3. Через 6 часов определяют процентное отношение парализованных личинок, которые падают с растений. Результаты приведены в табл.13. Пример 3/14. Обработку производят на делянке 25 м , сильно зараженной колорадским картофельным жуком. На каждой делянке специально отмечены 10 растений, на которых предварительно было подсчитано количество колорадских картофельных жуков. При оценке количества вредителей принимались во внимание только взрослые насекомые второго летнего поколения, так как в период испытаний количество личинок на стадиях L3 и L4 было мало. На каждую делянку 25 м 2 обработку проводят дозой 10 г активного ингредиента на 1 га водной суспензии составов согласно примеру 10, причем проводят три параллельных опыта. Оценку производят путем подсчета живых насекомых на отмеченных растениях. Средние значения трех параллельных опытов приведены в табл.14. Пример 3/15. Исследование остаточного контакта на взрослых Aphidinus matricarial. Взрослых A matricarial подвергают действию остатков активного ингредиента, свеженанесенных на стеклянные пластины, образующие клетки, затем подсчитывают количество выживших насекомых. Обработка: испытуемый(е) продукт(ы) и контрольные, обработанные водой. Повторение: по меньшей мере 3. Размер сети: 1 клетка. Применяют паразитов известного возраста (24 ч). Продукты наносят концентрацией 5,1 м.д. на каждую из стеклянных пластин. Десять самок A.matricarial помещают в каждую клетку и в качестве пищи им дают мед. Количество самок, оставши хся в живых после выдержки, определяют через 1,5 и 24 часа в независимых опытах. Вычисляют для каждой клетки общее количество выживших. Результаты приведены в табл.15. Пример 3/16. Исследование прямого контакта на куколках A.matricarial. Зрелые куколки A. matricarial на листьях перца подвергают в чашках Петри прямому опрыскиванию активными ингредиентами. Применяют листья перца с куколками паразитов за два дня до вылупления. Листья кладут на увлажненную фильтровальную бумагу в пластмассовую чашку Петри. Обработка: см. пример 28. Кусочки листьев помещают после обработки на дно чистой чашки Петри. Поддоны укладывают в климатическую камеру при температуре 20°С, относительной влажности 70% и цикле свет-ночь 16-8 часов. Выжившие куколки вылупляются через 2-3 дня. Подсчитывают количество вылупившихся и мертвых куколок. Результаты приведены в табл.16. Положительное влияние отдельных компонентов смеси иллюстрирует фактор синергизма, который представляет отношение ожидаемых и измеренных величины LD50, если отношение 1, имеет место положительный синергический эффект. В табл.17-19 представлены данные по фактору синергизма для смесей, приведенных в табл.2,5,6. Синергизм означает положительное взаимное воздействие компонентов смеси, т.е. когда активность смесипревышает сумму активности отдельных компонентов их. Мерой указанного взаимного воздействия является фактор синергизма, а именно отношение ожидаемых и измеренных LD 50 величин. Если это отношение превышает 1, это означает положительный синергетический эффект.
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for producing mixture of isomers of synthetic pyrethroids
Автори англійськоюGiyorugii Hidashi, Istvan Szekely, Bela Bertok, Sandooru Zorutan, Antaru Gayari, SOMFAI EVA, Agunesu Hegejiyuusu, Pap Laslo, Rudolf Soos, Erzsebet Radvany, Sandooru Botaru, Tamasu Suzaborukushi
Назва патенту російськоюСпособ получения смеси изомеров синтетических пиретроидов
Автори російськоюДьордь Хидаши, Иштван Секели, Белла Барток, Шандор Золтан, Антал Гайари, Ева Шомфаи, Агнеш Хегедюш, Ласло Пап, Рудольф Шоош, Ержбет Радвани, Шандор Ботар, Тамаш Саболчи
МПК / Мітки
МПК: C07C 255/37, A01N 37/34, C07B 63/00
Мітки: ізомерів, піретроїдів, синтетичних, спосіб, суміші, одержання
Код посилання
<a href="https://ua.patents.su/13-19064-sposib-oderzhannya-sumishi-izomeriv-sintetichnikh-piretrodiv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання суміші ізомерів синтетичних піретроїдів</a>
Попередній патент: Спосіб кислотної обробки пласта
Наступний патент: Спосіб приготування в’язкопружної композиції
Випадковий патент: Ковпак для диска автомобільного колеса