Композиція та спосіб одержання кетону
Формула / Реферат
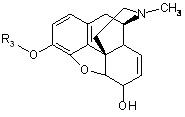
1. Композиція, одержувана шляхом комбінування сполуки формули R1SR2, трихлорізоціанурової кислоти і основи з вторинним спиртом формули (І)
 , (І)
, (І)
де R3 є захисною групою, або одержувана шляхом додавання вторинного спирту формули (І) до суміші, що містить сполуку формули R1SR2 і трихлорізоціанурову кислоту з наступним додаванням основи, де R1 і R2 є кожен незалежно (С1-С20)-алкіл, (С3-С8)-циклоалкіл або феніл.
2. Композиція за п. 1, в якій R1 є -СН3 і R2 є (С1-С20)-алкіл і переважно R1 є -СН3 і R2 є С12-алкіл.
3. Композиція за п. 1, в якій кількість сполуки формули R1SR2 знаходиться в інтервалі від приблизно 1,0 до приблизно 9,0, від приблизно 2,0 до приблизно 5,0 або від приблизно 2,5 до приблизно 3,5 молярних еквівалентів на молярний еквівалент трихлорізоціанурової кислоти.
4. Композиція за п. 1, в якій основою є органічний амін і переважно є триетиламін, діізопропілетиламін, піридин, диметилпіридин або диметиламінопіридин і більш переважним є триетиламін.
5. Композиція за п. 1, в якій кількість основи знаходиться в інтервалі від приблизно 1,0 до приблизно 15,0, від приблизно 2,0 до приблизно 10,0, або від приблизно 2,5 до приблизно 7,0 молярних еквівалентів на молярний еквівалент трихлорізоціанурової кислоти.
6. Композиція за п. 1, в якій кількість спирту знаходиться в інтервалі від приблизно 1,0 до приблизно 9,0, від приблизно 2,0 до приблизно 5,0 або від приблизно 2,0 до приблизно 4,0 молярних еквівалентів на молярний еквівалент трихлорізоціанурової кислоти.
7. Композиція за п. 1, яка додатково містить органічний розчинник і органічним розчинником є переважно бензол, толуол, ксилен, мезитилен, хлорбензол, дихлорметан, хлороформ, тетрахлорид вуглецю, дихлоретан, діетиловий етер, дипропіловий етер, дибутиловий етер, метил-трет-бутиловий етер, тетрагідрофуран, метилтетрагідрофуран, етилацетат або будь-яка їх комбінація і більш переважним є дихлорметан.
8. Спосіб одержання кетону, в якому вторинний спирт формули (І)
 , (І)
, (І)
де R3 є захисною групою, піддають взаємодії із сумішшю сполуки формули R1SR2, трихлорізоціануровою кислотою і основою за умов, достатніх для одержання кетону, де R1 і R2 є кожен незалежно (С1-С20)-алкіл, (С3-С8)-циклоалкіл або феніл.
9. Спосіб за п. 8, в якому R1 є СН3 і R2 є (С1-С20)-алкіл, і переважно R1 є СН3 і R2 є С12-алкіл.
10. Спосіб за п. 8, в якому кількість сполуки формули R1SR2 знаходиться в інтервалі від приблизно 1,0 до приблизно 9,0, від приблизно 2,0 до приблизно 5,0 або від приблизно 2,5 до приблизно 3,5 молярних еквівалентів на молярний еквівалент трихлорізоціанурової кислоти.
11. Спосіб за п. 8, в якому кількість основи знаходиться в інтервалі від приблизно 1,0 до приблизно 15,0, від приблизно 2,0 до приблизно 10,0 або від приблизно 2,5 до приблизно 7,0 молярних еквівалентів на молярний еквівалент трихлорізоціанурової кислоти.
Текст
1. Композиція, одержувана шляхом комбінування сполуки формули R1SR2, трихлорізоціанурової кислоти і основи з вторинним спиртом формули (І) CH3 N C2 2 87833 1 3 87833 4 молярних еквівалентів на молярний еквівалент 15,0, від приблизно 2,0 до приблизно 10,0 або від трихлорізоціанурової кислоти. приблизно 2,5 до приблизно 7,0 молярних еквіва11. Спосіб за п. 8, в якому кількість основи знахолентів на молярний еквівалент трихлорізоціануродиться в інтервалі від приблизно 1,0 до приблизно вої кислоти. 1. Галузь винаходу Представлений винахід стосується способів одержання 3-О-захищених морфінонів і 3-Озахищених морфінондієнолкарбоксилатів. Представлений винахід також стосується способів одержання альдегідів і кетонів з відповідних первинних і вторинних спиртів, відповідно. 2. Передумови створення винаходу Морфін і структурні аналоги морфіну ("морфінові алкалоїди") такі як кодеїн, гідрокодон, гідроморфон, налоксон, налтрексон, оксикодон і оксиморфон використовуються як анальгетичні рецептурні лікарські засоби. Інші аналоги морфіну, наприклад, тебаїн, корисні як вихідні матеріали для одержання аналогетичних морфінових алкалоїдів. Однак, тебаїн є другорядним компонентом морфінових алкалоїдів, що виділяють з насіння маку, а синтетичні способи одержання тебаїну є відносно дорогими (дивіться патент US 6,262,266 В1, Chiu et al). Кодеїнондієнолацетат, який є 3-О-метильним похідним морфінондієнолацетату, є морфіновим алкалоїдом корисним при одержанні анальгетичних і антагоністичних морфінових алкалоїдів, таких як налоксон, налтрексон і оксикодон (дивіться, наприклад, патент US 6,013,796, Huang et al). Кодеїнондієнолацетат можна одержати шляхом окислення кодеїну у кодеїнону з наступним ацилюванням (дивіться, наприклад, патент US 6,013,796, Huang et al). Відомі інші 3-О-захищеніморфінондієнолкарбоксилати і їх загалом одержують шляхом окислення відповідного 3-Озахищеного-морфіну з наступним ацилюванням. Ряд цих 3-О-захищенихморфінондієнолкарбоксилатів використовується для одержання інших корисних морфінових алкалоїдів. Наступні параграфи стосуються способів одержання 3-О-захищених морфінонів шляхом окислення відповідних 3-О-захищених морфінів. Кодеїн є 3-О-метилморфіном і кодеїнон є 3-Ометилморфіноном. Патент US 2,654,75, Homeyer et al., описує реакцію кодеїну з три(трет-бутоксидом)алюмінію і метоксициклогексаноном в толуолі з утворенням кодеїнону, де вихід кодеїнону складав менше ніж 50%. Ninan et al, Tetrahedron 48:6709-6716 (1992) описує реакцію 3-О-диметил-т-бутилсилілморфіну з діоксидом марганцю в хлороформі при 25°С з утворенням 3-0-диметил-т-бутилсилілморфінону. Ninan et al. також описує реакцію 3-О-диметилт-бутилсилілморфіну з перутенатом тетрапропіламонію і N-метилморфолін-н-оксидом в дихлорметані при нечітко встановлений температурі з утво ренням 3-О-диметил-т-бутилсилілморфінону з виходом 86%. Патент US 6,013,796, Huang et al., описує реакцію 3-О-ацетилморфіну з комплексом утвореним диметилсульфоксидом ("ДМСО") і оксалілхлоридом в присутності основи ("спосіб окислення Сверна") при -78°С з одержанням відповідного 3ацетилморфінону з виходом 73%. Патент US 6,013,796 також описує реакцію 3-0бензилморфіну за подібних умов з одержанням 3О-бензилморфінону з виходом 65%. Однак, описаний спосіб потребує, принаймні, 2,5 молярних еквівалентів ДМСО на моль морфіну і одержання смердючого диметилсульфіду, як побічного продукту. Недивлячись на ці описані способи, існує потреба в кращих способах одержання 3-Озахищених морфінонів. Дослідження були спрямовані на спосіб окислення Сверна описаний вище, оскільки в ньому не використовується агресивні неорганічні окисники, такі як МnО2, і він особливо корисний для окислення первинних і вторинних спиртів у альдегіди і кетони, відповідно. Наприклад, De Luca et al., J. Org. Chem. 66:7907-7909 (2001) описує реакцію первинних або вторинних спиртів з комплексом утвореним ДМСО і трихлорциануровою кислотою ("ТХЦК") в тетрагідрофурані ("ТГФ") при -30°С в присутності триетиламіну з одержанням відповідних альдегідів і кетонів, відповідно. Однак, в ході реакції утворюється смердючий диметилсульфід, як побічний продукт. Відповідно, було зроблено багато спроб по модифікуванню способу окислення Сверна або розробки більш прийнятних альтернатив. Наступні параграфи стосуються відомих модифікацій і альтернатив способів окислення Сверна. Nishide et al, Tetrahedron. Lett. 43:5177-5179 (2002) описує низькоароматний спосіб окислення Сверна з використанням додецилметилсульфоксиду, як сульфоксидного реагенту. Harris et al, J. Org. Chem. 63:2407-2409 (1998) описує низькоароматний спосіб окислення Сверна з використанням полімерзв'язаної 6(метилсульфініл)гексанової кислоти як сульфоксидного реагенту, і сульфоксидний реагент можна регенерувати використовуючи реакцію сульфідного побічного продукту з NalO4. Альтернатива реакції Сверна описується Corey et al., J. Am. Chem. Soc. 94:7586-7587 (1972), де первинний або вторинний спирт взаємодіє з комплексом утвореним диметилсульфідом і Nхлорсукцинамід ("NCS") або СІ2 при -25°С в присутності основи ("окислення Корі-Кіма") з утворенням відповідного альдегіду і кетону, відповідно. Однак, Корі описує, що реакція 2-циклогексенолу з утво 5 87833 6 ренням хлорциклогексену більш переважна ніж 2R1 і R2 є кожен, незалежно, -(С1-С20)алкіл, -(С3циклогексенону. Крім того, описаний спосіб передС8)циклоалкіл або -феніл; і бачає використання диметилсульфіду як реагенту. R3 є захисна група. Ohsugi et al., Tetrahedron 59:8393-8398 (1992) Представлений винахід також стосується споописує низько ароматне окислення Корі-Кіма, де собів одержання 3-О-захищених похідних дієнолпервинний або вторинний спирт реагує з карбоксилату морфінону. CH3S(C12H25) і NCS в присутності триетиламіну при В одному з втілень, представлений винахід -40°С, але описаний спосіб використовує, принайстосується способів одержання сполуки формули мні, 3-кратний надлишок сульфіду і NCS на моль (III): спирту. Недивлячись на ці описані способи, залишається потреба в удосконалених способах окислення первинних або вторинних спиртів у відповідні альдегіди або кетони. Цитування будь-яких посилань в Розділі 2 цієї заявки не слід трактувати як посилання на попередній рівень техніки винаходу. 3. Короткий опис суті винаходу Представлений винахід стосується способів одержання альдегідів або кетонів з відповідного первинного або вторинного спирту, відповідно. В одному з втілень, винахід стосується способів одержання кетону, в яких вторинний спирт взав яких: ємодіє з сполукою формули R1SR2, трихлорізоци(а) сполука формули (І): ануровою кислотою і основою за умов достатніх для одержання кетону, де R1 і R2 є кожен, незалежно, -(C1-С20)алкіл, -(С3-С8)циклоалкіл або -феніл. В іншому втіленні, представлений винахід стосується способів одержання альдегіду, в яких первинний спирт взаємодіє з сполукою формули R1SR2, трихлорізоциануровою кислотою і основою за умов достатніх для одержання альдегіду, де R1 і R2 є кожен, незалежно, -(С1-С20)алкіл, -(С3С8)циклоалкіл або -феніл. Представлений винахід також стосується способів одержання 3-О-захищених морфінонів. В одному з втілень, винахід стосується способів одержання сполуки формули (II): взаємодіє з сполукою формули R1SR2 і хлорвмісним реагентом за умов достатніх для одержання суміші, що містить сполуку формули (II): в яких сполука формули (І): взаємодіє з сполукою формули R1SR2 і хлорвмісним реагентом за умов достатніх для одержання сполуки формули (II), де: і (б) сполука формули (II) взаємодіє з першою основою і ацилюючим агентом формули R4C(O)OC(O)R4 або R4C(O)X за умов достатніх для одержання сполуки формули (III), де: R1 і R2 є кожен, незалежно, -(С1-С20)алкіл, -(С3С8)циклоалкіл або -феніл; R3 є захисна група; і R4 є -(С1-С10)алкіл; і X є -СІ, -Вr або -І. Представлений винахід також стосується нових композицій корисних для окислення первинного або вторинного спирту у альдегід або кетон, відповідно. 7 87833 8 В одному з втілень, представлений винахід в якій R3 є захисна група. стосується композицій, що містять сполуку форСполука формули (На) має структуру: мули R1SR2, трихлорізоцианурову кислоту і основу, де R1 і R2 є кожен, незалежно, -(С1-С20)алкіл або -(С3-С8)циклоалкіл або -феніл. Представлений винахід також стосується нових похідних 3-О-захищених дієнолкарбоксилатів морфінону. В одному з втілень, представлений винахід стосується сполук формули (III), де: R3 є -Sі((С1-С10)алкіл)3, -Sі(арил)((С1-С10)алкіл)2 або -Sі(арил)2((С1-С10)алкіл); і R4 є -(С1-С10)алкіл. Представлений винахід можна зрозуміти більш повно з посиланням на наступний детальв якій R3 є захисна група. ний опис і ілюстративні приклади, які є ілюстратиЯк тут використовується, генерична фраза "3вними не обмежуючими втіленнями винаходу. О-захищений морфінондієнолкарбоксилат" стосу4. Детальний опис винаходу ється сполуки, що має структуру формули (III): 4,1. Визначення Як тут використовується, генерична фраза "3О-захищений морфін" стосується сполуки, що має структуру формули (І): в якій R3 є захисна група, і R4 є -(С1-С10)алкіл. Сполука формули (ІІІа) має структуру: в якій R3 є захисна група. Сполука формули (Іа) має структуру в якій R3 є захисна група. Як тут використовується, генерична фраза "3О-захищений морфінон" стосується сполуки, що має структуру формули (II): в якій R3 є захисна група, і R4 є -(С1-С10)алкіл. Як тут використовується, термін "гало" стосується -F, -СІ, -Вr або -І. Як тут використовується, термін "-(С1С10)алкіл" означає насичений нерозгалужений або розгалужений вуглеводень, що має від 1 до 10 атомів вуглецю Характерними насиченими нерозгалуженими (С1-С10)алкілами є -метил, -етил, -нпропіл, -н-бутил, -н-пентил, -н-гексил, -н-гептил, -ноктил, -н-ноніл і -н-децил. Характерними насиченими розгалуженими -(С1-С10)алкілами є ізопропіл, -втор-бутил, -ізобутил, -трет-бутил і їм подібні. Як тут використовується, термін "-(С1С20)алкіл" означає насичений нерозгалужений або розгалужений вуглеводень, що має від 1 до 20 9 87833 10 атомів вуглецю. Характерними насиченими нерозпентанол, 4,4-диметил-2-пентанол, 3-гептанол, 2галуженими (С1-С20)алкілами є -метил, -етил, -нметил-3-гептанол, 4-метил-3-гептанол, 5-метил-3пропіл, -н-бутил, -н-пентил, -н-гексил, -н-гептил, -нгептанол, 2,2-диметил-3-пентанол, 2,4-диметил-3октил, -н-ноніл, -н-децил, -н-ундецил, -н-додецил, пентанол, 2-етил-3-пентанол, 4-етил-3-пентанол, н-тридецил, -н-тетрадецил, -н-пентадецил, -н4-гептанол, і їм подібні; циклічні вторинні спирти, гексадецил, -н-гептадецил, -н-октадецил, -нтакі як циклогексанол; сполуки формули (І) або нонадецил, і -н-ейкозил. Необмежуючими прикла(Іа), де R3 є захисна група; алкіларилвторинні дами насичених розгалужених -(С1-С20)алкілів є спирти, такі як 1-феніл-1-етанол, 1-феніл-1ізопропіл, -втор-бутил, -ізо-бутил, -трет-бутил і їм пропанол, 1-феніл-1-пропанол і їм подібні; діалкілподібні. вторинні спирти, такі як дифенілметанол; олігомеЯк тут використовується, фраза "захисна грурні і полімерні спирти, такі як олігомери і полімери па" означає групу іншу ніж -Н, яка є корисною для полівінілового спирту; і їм подібні. захисту 3-О-положення морфіну, морфінону і В одному з втілень, спосіб одержання карбоніморфінондієнолкарбоксилату від небажаних реаклу включає використання сполуки формули (І), де цій. Захисна група може, при бажанні, бути заміR3 є захисна група. нена -Н або іншою групою після одержання сполуВ одному з втілень, спосіб одержання карбоніки формули (III). лу включає використання вторинного спирту форЯк тут використовується, фраза "безводний", мули (Іа). коли використовується з посиланням на органічНеобмежуючими прикладами захисних груп ний розчинник, якщо тут не вказано інше, означає корисних в способі одержання карбонілу сполуки органічний розчинник, що має вміст води менше формули (І) є -(С1-С10)алкіл; -бензил; ацили, такі як ніж приблизно 0,01ваг.% від загальної кількості -С(О)(С1-С10)алкіл і -С(О)С6Н5; карбонати, такі як води і органічного розчинника. С(О)О((С1-С10)алкіл); силіли, такі як -Sі((С1Як тут використовується, фраза "хлор-вмісний С10)алкіл)3, -Sі(арил)((С1-С10)алкіл)2 і реагент", коли використовується з посиланням на Sі(арил)2((С1-С10)алкіл); фосфіноксиди, такі як спосіб одержання морфінону або стадії одержання Р(О)(СН3)2; фосфінсульфіди, такі як -P(S)(CH3)2; і морфінону, стосується сполуки або комплексу, що арилсульфонати, такі як -S(O)OC6H4-n-CH3. має реактивний хлор, що є корисним для промоВ одному з втілень, спосіб одержання карбонічування утворення сполуки формули (II) з сполуки лу включає використання сполуки формули (І), в формули (І) якій R3 є -(С1-С10)алкіл, -бензил, -С(О)(С1-С10)алкіл, Як тут використовується, термін "виділення", -С(О)О((С1-С10)алкіл),-Sі((С1-С10)алкіл)3, коли використовується з посиланням на суміш, що Sі(арил)((С1-С10)алкіл)2, -Sі(арил)2((С1-С10)алкіл), містить сполуку формули (II) або (III), означає віР(O)((С1-С10)алкіл)2, -P(S)((C1-C10)aлкіл)2 або докремлення сполуки формули (II) або (III) від орS(O)OC6H4-n-CH3. ганічного розчинника, коли присутній, і воли, коли В одному з втілень, спосіб одержання карбоніприсутня. лу включає використання сполуки формули (І), в 4,2. Способи окислення Первинних або Втоякій R3 є -СН3. ринних Спиртів В іншому втіленні, спосіб одержання карбонілу Як визначено вище, представлений винахід включає використання сполуки формули (І), в якій стосується способів окислення первинного або R3 є -Si((С1-С10)алкіл)3, -Sі(арил)((С1-С10)алкіл)2 вторинного спирту з утворенням альдегіду або або -Si(aрил)2((C1-С10)алкіл). кетон, відповідно ("спосіб одержання карбонілу"). В іншому втіленні, спосіб одержання карбонілу Порівнюючи з відомими способами, представлені включає використання сполуки формули (І), в якій способи окислення первинних або вторинних R3 є -Sі((С1-С10)алкіл)3. спиртів можуть бути здійснені за м'якших умов В іншому втіленні, спосіб одержання карбонілу і/або з більш ефективним використанням реагенвключає використання сполуки формули (І), в якій тів, ніж у випадку звичайних способів. R3 є -Si(CH3)2(C(CH3)3). В одному з втілень, спосіб одержання карбоніВ іншому втіленні, представлений винахід столу включає використання низькоароматного спосується способу одержання альдегіду, в якому собу окислення. первинний спирт взаємодіє з сполукою формули В одному з втілень, представлений винахід R1SR2, трихлорізоциануровою кислотою і основою стосується способу одержання кетону, в якому за умов достатніх для одержання альдегіду, де R1 і вторинний спирт взаємодіє з сполукою формули R2 є кожен, незалежно, -(С1-С20)алкіл, -(С3R1SR2, трихлорізоциануровою кислотою і основою С8)циклоалкіл або -феніл. за умов достатніх для одержання кетону, де R1 і R2 Необмежуючими прикладами первинних спирє кожен, незалежно, -( С1-С20)алкіл, -(С3тів корисних в способі одержання карбонілу є, але С8)циклоалкіл або -феніл. не обмежується, нерозгалужені і розгалужені алкіНеобмежуючими прикладами корисних втольні, алкенільні і алкінільні первинні спирти, такі як ринних спиртів є нерозгалужений і розгалужений метанол, етанол, н-пропанол, н-бутанол, 2алкільні, алкенільні і алкінільні первинні спирти метилпропанол, н-пентанол, 2-метилбутанол, 3включаючи 2-пропанол, 2-бутанол, 2-пентанол, 3метилбутанол, н-гексанол, 2-метилпентанол, 3метилбутан-2-ол, 2-гексанол, 3-метил-2-пентанол, метилпентанол, 4-метилпентанол, 2,24-метил-2-пентанол, 3-гексанол, 2-метил-3диметилбутанол, 2,3-диметилбутанол, 3,3пентанол, 2-гептанол, 3-метил-2-гексанол, 4диметилбутанол, 2-етилбутанол, н-гептанол, нметил-2-гексанол, 5-метил-2-гексанол, 3-етил-2октанол, н-нонанол, н-деканол і їм подібні. пентанол, 3,3-диметил-2-пентанол, 3,4-диметил-2 11 87833 12 В одному з втілень, спосіб одержання карбоніходиться в інтервалі від приблизно 2,0 до приблилу включає використання сполуки формули R1SR2, зно 4,0 молярних еквівалентів на молярний в якій R1 є -метил і R2 є -(С1-С20)алкіл, -(С3еквівалент трихлорізоцианурової кислоти. С8)циклоалкіл або -феніл. В одному з втілень, кількість сполуки формули В іншому втіленні, спосіб одержання карбонілу R1SR2 використовуваної в способі одержання карвключає використання сполуки формули R1SR2, в бонілу знаходиться в інтервалі від приблизно 1,0 якій R1 є -СН3 і R2 є -(С1-С20)алкіл. до приблизно 9,0 молярних еквівалентів на моляВ іншому втіленні, спосіб одержання карбонілу рний еквівалент трихлорізоцианурової кислоти; в включає використання сполуки формули R1SR2, в іншому втіленні, кількість сполуки формули R1SR2 якій R1 є -СН3 і R2 є -(С12)алкіл. використовуваної в способі одержання карбонілу Основою є органічна основа або неорганічна знаходиться в інтервалі від приблизно 2,0 до приоснова. Необмежуючими прикладами органічних близно 5,0 молярних еквівалентів на молярний основ корисних в способі одержання карбонілу є, еквівалент трихлорізоцианурової кислоти; і в інале не обмежується, органічні аміни, такі як, нашому втіленні, кількість сполуки формули R1SR2 приклад, триалкіламіни, такі як триметиламін, тривикористовуваної в способі одержання карбонілу етиламін, три-н-пропіламін, три-н-бутиламін, діезнаходиться в інтервалі від приблизно 2,5 до притилметиламін, диметилетиламін, близно 3,5 молярних еквівалентів на молярний діізопропілетиламін і їм подібні; арилдіалкіламіни, еквівалент трихлорізоцианурової кислоти. такі як диметилфеніламін і діетилфеніламін; піриВ одному з втілень, кількість основи викорисдин і піридин заміщений одним або декількома товуваної в способі одержання карбонілу знахо(С1-С4)алкілами, такими як 2-метилпіридин, 3диться в інтервалі від приблизно 1,0 до приблизно метилпіридин, 4-метилпіридин, 2,315,0 молярних еквівалентів на молярний еквівадиметилпіридин, 2,4-диметилпіридин, 2,5лент трихлорізоцианурової кислоти; в іншому втідиметилпіридин, 3,4-диметилпіридин, 3,5ленні, кількість основи використовуваної в способі диметилпіридин, 2,3,4-триметилпіридин, 2,3,5одержання карбонілу знаходиться в інтервалі від триметилпіридин, 2,4,5-триметилпіридин, 3,4,5приблизно 2,0 до приблизно 10,0 молярних еквітриметилпіридин і їм подібні; піридин заміщений валентів на молярний еквівалент трихлорізоциадіалкіламіногрупами, такими як пара-N,Nнурової кислоти; і в іншому втіленні, кількість осдиметиламінопіридин; солі лужних металів слабих нови використовуваної в способі одержання кислот, такі як, наприклад, карбоксилати літію, карбонілу знаходиться в інтервалі від приблизно натрію; калію, рубідію і цезію; і будь-яка їх комбі2,5 до приблизно 7,0 молярних еквівалентів на нація. молярний еквівалент трихлорізоцианурової кислоНеобмежуючими прикладами неорганічних ости. нов корисних в способі одержання карбонілу є В одному з втілень, спосіб одержання карбонігідроксиди лужних металів, таких як літій, натрій, лу проводять в присутності органічного розчинникалій, рубідій і цезій. ка. Необмежуючими прикладами органічних розВ одному з втілень, основою є органічна осночинників, що корисні в способі одержання ва. В іншому втіленні, органічною основою є оргакарбонілу є, але не обмежується, ароматичні вугнічний амін. В іншому втіленні, органічним аміном леводні, такі як бензол, толуол, ксилен, мезитиє триетиламін, діізопропілетиламін, піридин, димелен, хлорбензол; (С1-С4)галогеновані вуглеводні, тилпіридин або диметиламінопіридин. В іншому такі як дихлорметан, хлороформ, тетрахлорид втіленні, органічним аміном є триетиламін. вуглецю і дихлоретан; етери, такі як діетиловий В іншому втіленні, основою є неорганічна осетер, дипропіловий етер, дибутиловий етер, менова. тил-трет-бутиловий етер, тетрагідрофуран, метилСполуки формули (І) і (Іа) є комерційно достутетрагідрофуран; і етилацетат. пними або можна одержати за способами описаВ одному з втілень, органічним розчинником ними в Розділі 4.3. використовуваним в способі одержання карбонілу Трихлорізоцианурову кислоту одержували від є бензол, толуол, ксилен, мезитилен, хлорбензол, Aldrich Chemical Co., Milwaukee, Wl. дихлорметан, хлороформ, тетрахлорид вуглецю, Сполуки формули R1SR2 є комерційно доступдихлоретан, діетиловий етер, дипропіловий етер, ними від Lancaster Synthesis, Windham, NH, або дибутиловий етер, метил-трет-бутиловий етер, можна одержати внаслідок реакції сполуки фортетрагідрофуран, етилацетат, або будь-яка їх коммули R1SH з К2СО3 і R2I в диметилформаміді, як бінація. описано Ohsugi et al., Tetrahedron 59:8393-8398 В іншому втіленні, органічним розчинником ви(2003). користовуваним в способі одержання карбонілу є В одному з втілень, кількість спирту викорисабо включає дихлорметан. товуваного в способі одержання карбонілу знахоВ іншому втіленні, органічним розчинником є диться в інтервалі від приблизно 1,0 до приблизно або включає толуол. 9,0 молярних еквівалентів на молярний еквівалент В одному з втілень, органічний розчинник витрихлорізоцианурової кислоти; в іншому втіленні, користовуваний в способі одержання карбонілу кількість спирту використовуваного в способі одеприсутній в кількості в інтервалі від приблизно 0,1 ржання карбонілу знаходиться в інтервалі від привагових частин до приблизно 50 вагових частин близно 2,0 до приблизно 5,0 молярних еквіваленвиходячи з ваги сполуки формули R1SR2. В іншому тів на молярний еквівалент трихлорізоцианурової втіленні, органічний розчинник використовуваний в кислоти; і в іншому втіленні, кількість спирту викоспособі одержання карбонілу присутній в кількості ристовуваного в способі одержання карбонілу знав інтервалі від приблизно 0,1 вагових частин до 13 87833 14 приблизно 25 вагових частин виходячи з ваги споржання карбонілу проводять при атмосферному луки формули R1SR2. В іншому втіленні, органічтиску. ний розчинник використовуваний в способі одерВ іншому втіленні, стадію одержання карбоніжання карбонілу присутній в кількості в інтервалі лу проводять в інертній атмосфері, такій як, навід приблизно 0,1 вагових частин до приблизно 10 приклад, N2, He, Ne, Аr, Кr, Хе, або будь-яка їх вагових частин виходячи з ваги сполуки формули комбінація. В одному з втілень, стадію одержання R1SR2. карбонілу проводять в атмосфері N2. В одному з втілень, органічний розчинник виПорядок додавання сполуки формули R1SR2, користовуваний в способі одержання карбонілу є трихлорізоцианурової кислоти, первинного або безводним. Безводні органічні розчинники є комевторинного спирту, основи і органічного розчиннирційно доступними або можна одержати контактуку, якщо це має місце, може змінюватись. Далі ванням органічного розчинника з придатним дегідприведені приклади. ратуючим агентом, таким як, наприклад, В одному з необмежуючих втілень, спосіб молекулярні сита; реактивні метали, такі як Li, Na одержання карбонілу проводять шляхом додаванабо К, і їх суміші; гідриди металів, такі як СаН або ня первинного або вторинного спирту, необов'язLІАІН4; і оксиди металів або металоїдів, такі як ково, в присутності органічного розчинника, до ВаО, СаО і Р2О5 (дивіться Amarego et al., Purificaсуміші, що містить сполуку формули R1SR2, трихtion of Laboratory Chemicals (4th ed. 1996); і Gordan лорізоцианурову кислоту і основу, необов'язково, в et al., The Chemist's Companion 445-447 (1972)). присутності органічного розчинника. Кількість води в органічному розчиннику можна В іншому необмежуючому втіленні, спосіб визначити, наприклад, титруванням Карла-Фішера одержання карбонілу проводять шляхом додаван(дивіться ASTM ЕІ 064-00 і ASTME2O3-O1). ня суміші, що містить сполуку формули R1SR2, Спосіб одержання карбонілу проводять за трихлорізоцианурову кислоту і основу, необов'язумов достатніх для одержання альдегіду або кетоково, в присутності органічного розчинника, до ну. В одному з втілень, спосіб одержання карбоніпервинного або вторинного спирту, необов'язково, лу проводять доки, принаймні, приблизно 80 мов присутності органічного розчинника. лярних відсотків спирту не перетворяться у В іншому необмежуючому втіленні, спосіб альдегід або кетон; в іншому втіленні, спосіб одеодержання карбонілу проводять шляхом додаванржання карбонілу проводять доки, принаймні, приня основи, необов'язково, в присутності органічноблизно 95 молярних відсотків спирту не перетвого розчинника, до суміші, що містить сполуку форряться у альдегід або кетон; і в іншому втіленні, мули R1SR2 і трихлорізоцианурову кислоту, спосіб одержання карбонілу проводять доки, принеобов'язково, в присутності органічного розчиннаймні, приблизно 99 молярних відсотків спирту не ника, з наступним додаванням первинного або перетворяться у альдегід або кетон. вторинного спирту, необов'язково, в присутності Протікання способу одержання карбонілу моорганічного розчинника. жна контролювати використовуючи стандартні В іншому необмежуючому втіленні, спосіб аналітичні методики, включаючи, але не обмежуодержання карбонілу проводять шляхом додаванється, тонкошарова хроматографія ("ТШХ"), висоня суміші, що містить сполуку формули R1SR2 і коефективна рідинна хроматографія ("ВЕРХ"), трихлорізоцианурову кислоту, необов'язково, в газова хроматографія ("ГХ"), газорідинна хроматоприсутності органічного розчинника, до основи, графія ("ГРХ"), інфрачервона спектроскопія ("ІЧ") і необов'язково, в присутності органічного розчинядерний магнітний резонанс ("ЯМР"), такий як 1Н ника, з наступним додаванням первинного або або 13С ЯМР. вторинного спирту, необов'язково, в присутності Типово, час достатній для проведення способу органічного розчинника. одержання карбонілу знаходиться в інтервалі від В іншому необмежуючому втіленні, спосіб приблизно 0,25 годин до приблизно 20 годин; в одержання карбонілу проводять шляхом додаваніншому втіленні, час достатній для проведення ня первинного або вторинного спирту, необов'язспособу одержання карбонілу знаходиться в інково, в присутності органічного розчинника, до тервалі від приблизно 0,5 годин до приблизно 10 суміші, що містить сполуку формули R1SR2 і трихгодин; і в іншому втіленні, час достатній для пролорізоцианурову кислоту, необов'язково, в присутведення способу одержання карбонілу знаходитьності органічного розчинника, з наступним додася в інтервалі від приблизно 1 години до приблизванням основи, необов'язково, в присутності но 5 годин. органічного розчинника. Типово, температура достатня для проведенВ іншому необмежуючому втіленні, спосіб ня способу одержання карбонілу знаходиться в одержання карбонілу проводять шляхом додаванінтервалі від приблизно -78°С до приблизно 130°С; ня сполуки формули (І), необов'язково, в присутв іншому втіленні, температура достатня для проності органічного розчинника, до суміші, що місведення способу одержання карбонілу знаходитьтить сполуку формули R1SR2 і ся в інтервалі від приблизно -50°С до приблизно трихлорізоцианурову кислоту, необов'язково, в 50°С; і в іншому втіленні, температура достатня присутності органічного розчинника, з наступним для проведення способу одержання карбонілу додаванням основи, необов'язково, в присутності знаходиться в інтервалі від приблизно -40°С до органічного розчинника. приблизно 50°С. В іншому необмежуючому втіленні, спосіб Спосіб одержання карбонілу можна проводити одержання карбонілу проводять шляхом додаванпри пониженому тиску, атмосферному тиску або ня основи, необов'язково, в присутності органічнопідвищеному тиску В одному з втілень, спосіб одего розчинника, до суміші, що містить сполуку фор 15 87833 16 мули R1SR2 і трихлорізоцианурову кислоту, необоР(О)((С1-С10)алкіл)2, -Р(S)((С1-С10)алкіл)2, або в'язково, в присутності органічного розчинника, з S(O)OC6H4-n-CH3. наступним додаванням сполуки формули (І), неВ іншому втіленні, винахід стосується компообов'язково, в присутності органічного розчинника. зиції, що містить сполуку формули R1SR2, трихлоАльдегід або кетон одержаний в способі одеррізоцианурову кислоту, основу і сполуку формули жання карбонілу можна виділити і очистити за ме(І), в якій R3 є -Si((C1-С10)алкіл)3, -Sі(арил)((С1тодами відомими в цій галузі. Наприклад, реакційС10)алкіл)2 або -Sі(арил)2(С1-С10)алкіл. ну суміш, що містить альдегід або кетон, можна В іншому втіленні, винахід стосується компоочистити фракційною кристалізацією; хроматогзиції, що містить сполуку формули R1SR2, трихлорафією на силікагелі, оксиді алюмінію або різоцианурову кислоту, основу і сполуку формули FLORISIL™; і/або перекристалізацією. Де з реак(І), в якій R3 є -Si((C1- С10)алкіл)3. ційної суміші, що містить альдегід або кетон, а В іншому втіленні, винахід стосується компотакож містить органічний розчинник, весь або часзиції, що містить сполуку формули R1SR2, трихлотину органічного розчинника можна, необов'язкорізоцианурову кислоту, основу і сполуку формули во, видалити, типово шляхом упарювання, перед (І), в якій R3 є -Si(CH3)2(C(CH3)3). очисткою. В іншому втіленні, винахід стосується компоНеобмежуючими прикладами органічних роззиції, що містить сполуку формули R1SR2, трихлочинників корисних як хроматографічні елюенти є різоцианурову кислоту, основу і сполуку формули нерозгалужені і розгалужені аліфатичні (С4(І), в якій R3 є -СН3. С10)вуглеводні, такі як бутани, пентани, гексани, В іншому втіленні, композиції, що містять пергептани, октани, нонани і декани; аліфатичні циквинний або вторинний спирт, сполуку формули лічні (С4-С7)вуглеводні, такі як циклобутан, циклоR1SR2 і трихлорізоцианурову кислоту, також мопентан, циклогексан і циклогептан; ароматичні жуть включати органічний розчинник. Необмежуювуглеводні, такі як бензол, толуол і ксилен; кожен з чими прикладами органічних розчинників є та, що яких є заміщеним однією або декількома галогеописані для способу одержання карбонілу. нами. 4,3. Способи одержання Морфінонів Іншими необмежуючими прикладами органічВідносні молярні кількості первинного або втоних розчинників корисних як хроматографічні елюринного спирту, сполуки формули R1SR2, трихлоенти є (С1-С4)галогеновані вуглеводні, такі як хлорізоцианурової кислоти і основи, і відносна кільрметан, метиленхлорид, хлороформ і тетрахлорид кість органічного розчинника, коли присутній, є вуглецю; (С1-С10)аліфатичні спирти, такі як метатакими як описано вище для способу одержання нол, етанол, н-пропанол, ізопропанол, н-бутанол, карбонілу. втор-бутанол, ізобутанол, трет-бутанол, нВ іншому втіленні, представлений винахід стопентанол, н-гексанол, н-гептанол, н-октанол, нсується способів одержання сполуки формули (II) нонанол, н-деканол і їм подібні; діалкілові етери, ("спосіб одержання морфінону"), що включає взатакі як діетиловий етер, діізопропіловий етер, диємодію сполуки формули (І) з сполукою формули бутилові етери і метилбутилові етери; діарилові R1SR2 і хлор-вмісним реагентом за умов достатніх етери, такі як дифеніловий етер; циклічні етери, для одержання сполуки формули (II), в якій: такі як тетрагідрофуран і діоксан; гліми, такі як R1 і R2 є кожен, незалежно, -(С1-С20)алкіл, -(С3диметиловий етер етиленгліколю; етилацетат; С8)циклоалкіл або -феніл; і диметилсульфоксид; N-метилпіролідон; гексамеR3 є захисна група. тилфосфорамід; диметилформамід; і будь-яка їх В одному з втілень, сполукою формули (І) є суміш. сполука формули (Іа), і сполукою формули (II) є В одному з втілень, органічний розчинник висполука формули (IIа). користовуваний як хроматографічний елюент місВ одному з втілень, спосіб одержання морфітить аліфатичний вуглеводень і етер. нону включає використання сполуки формули (І), в Представлений винахід також стосується комякій R3 є -(С1-С10)алкіл, -бензил, -С(О)(С1-С10)алкіл, позицій, що містять первинний або вторинний -С(О)О((С1-С10)алкіл), -Sі((С1-С10)алкіл)3, спирт, сполуку формули R1SR2, як тут визначено, Sі(арил)((С1-С10)алкіл)2, -Sі(арил)2((С1-С10)алкіл), трихлорізоцианурову кислоту і основу. Ці композиР(О)((С1-С10)алкіл)2, -Р(S)((С1-С10)алкіл)2 або ції корисні при одержанні кетону або альдегіду, як S(O)OC6H4-n-CH3. описано вище. В іншому втіленні, спосіб одержання морфіноНеобмежуючими прикладами первинних або ну включає використання сполуки формули (І), в вторинних спиртів, сполук формули R1SR2, трихякій R3 є -Sі((С1-С10)алкіл)3, -Sі(арил)((С1лорізоцианурової кислоти і основ є ті, що описані С10)алкіл)2 або -Sі(арил)2((С1-С10)алкіл). вище для способу одержання карбонілу. В іншому втіленні, спосіб одержання морфіноВ іншому втіленні, винахід стосується компону включає використання сполуки формули (І), в зиції, що містить сполуку формули R1SR2, трихлоякій R3 є -Sі((С1-С10)алкіл)3. різоцианурову кислоту, основу і сполуку формули В іншому втіленні, спосіб одержання морфіно(І), в якій R3 є захисна група. ну включає використання сполуки формули (І), в В іншому втіленні, винахід стосується компоякій R3 є -Si(CH3)2(C(CH3)3). зиції, що містить сполуку формули R1SR2, трихлоВ іншому втіленні, спосіб одержання морфінорізоцианурову кислоту, основу і сполуку формули ну включає використання сполуки формули (І), в (І), в якій R3 є -(С1-С10)алкіл, -бензил, -С(О)(С1якій R3 є -СН3. С10)алкіл, -С(О)О((С1-С10)алкіл), -Sі((С1-С10)алкіл)3, Необмежуючими прикладами сполук формули -Sі(арил)((С1-С10)алкіл)2, -Sі(арил)2((С1-С10)алкіл), R1SR2 корисних в спосіб одержання морфінону є 17 87833 18 сполуки описані в Розділі 4.2 способу одержання формі і в присутності бікарбонату натрію при кикарбонілу. В одному з втілень, R1 є -СН3 і R2 є п'ятінні із зворотнім холодильником як описано в (С12)алкіл. патенті US 5,112,975, Wallace. Необмежуючими прикладами хлор-вмісних Трихлорізоцианурову кислоту, Nреагентів корисних в способі одержання морфінохлорсукцинімід, дихлорізоцианурат натрію, 1,3ну є N-хлораміни, такі як трихлорізоцианурова кидихлор-5,5-диметилгідантоїн і гіпохлорит кальцію слота, N-хлорсукцинімід, солі дихлорізоцианурової одержували від Aldrich Chemical Co., Milwaukee, кислоти, такі як дихлорізоцианурат натрію, 1,3Wl. дихлор-5,5-диметилгідантоїн; СІ2; і гіпохлорити, Коли Cl2 є хлор-вмісним реагентом, СІ2 можна такі як гіпохлорит кальцію. одержати у формі газу або розчину. СІ2 у формі В одному з втілень, хлор-вмісним реагентом газу одержували від Matheson, Montgomeryville, використовуваним в способі одержання морфінону PA, і можна додавати до реакційної суміші, наприє трихлорізоцианурова кислота, N-хлорсукцинімід, клад, шляхом барботування СІ2 в суміш. Швидкість дихлорізоцианурат натрію, 1,3-дихлор-5,5і кількість СІ2, що додається, можна контролювати диметилгідантоїн, СІ2, гіпохлорит кальцію, або за способами відомими в цій галузі, наприклад, будь-яка їх суміш. використовуючи регулятор газового потоку і/або В іншому втіленні, хлор-вмісним реагентом вивимірювачі. користовуваним в способі одержання морфінону є СІ2 у формі розчину можна одержати розчитрихлорізоцианурова кислота. ненням газоподібного СІ2 в придатному органічноВ іншому втіленні, хлор-вмісним реагентом виму розчиннику Концентрація СІ2 в розчині можна користовуваним в способі одержання морфінону є визначити за допомогою аналітичних методів віN-хлорсукцинімід. домих в цій галузі. В іншому втіленні, хлор-вмісним реагентом виБез обмеження теорією, заявник припускає, користовуваним в способі одержання морфінону є що хлор-вмісний реагент взаємодіє з сполукою СІ2. формули R1SR2 з утворенням сульфонієвого катіСполуки формули (І) можна одержати за доону: помогою відомих методів корисних для захисту фенольної гідроксигрупи {дивіться, наприклад, Greene et al., Protective Groups in Organic Synthesis 143-170 (1991), яка включена сюди як посилання). Сульфонієва сполука потім взаємодіє з гідроСполуки формули (І), де R3 є -(С1-С10)алкіл є ксильною групою первинного або вторинного комерційно доступними або можна одержати шляспирту з утворенням карбонільної групи. хом взаємодії морфіну з гало(С1-С10)алкілом в диВ одному з втілень, кількість сполуки фометоксиетані і в присутності фториду тетраетилармули (І) використовуваної в способі одержання монію при 20°С як описано Т.W. Greene et al., морфінону знаходиться в інтервалі від приблизно Protective Groups in Organic Synthesis 146 (1991) і в 1,0 до приблизно 9,0 молярних еквівалентів на опублікованій заявці на патент US № молярний еквівалент хлор-вмісного реагенту, в 2003/0073848 А1. іншому втіленні, кількість сполуки формули (І) виСполуки формули (І), де R3 є -Sі((С1користовуваної в способі одержання морфінону С10)алкіл)3, -Sі(арил)((С1-С10)алкіл)2 або знаходиться в інтервалі від приблизно 2,0 до приSі(арил)2((С1-С10)алкіл), можна одержати взаємоблизно 5,0 молярних еквівалентів на молярний дією морфіну з Na або бутиллітіем, і взаємодією еквівалент хлор-вмісного реагенту; і в іншому втіодержаного комплексу з СІSі((С1-С10)алкіл)3, ленні, кількість сполуки формули (І) використовуСІSі(арил)((С1-С10)алкіл)2 або СІSі(арил)2((С1ваної в способі одержання морфінону знаходиться С10)алкіл) як описано Ninan et al, Tetrahedron в інтервалі від приблизно 2,0 до приблизно 4,0 48:6709-6716 (1992) і в патенті US 6,046,313, молярних еквівалентів на молярний еквівалент Scheinmann et al., з одержанням 3-О-диметил-тхлор-вмісного реагенту. бутилсилілморфін. Альтернативно, 3-О-силільне В одному з втілень, кількість сполуки формули похідне морфіну можна одержати взаємодією R1SR2 використовуваної в способі одержання морфіну з СІSі((С1-С10)алкіл)3, СІSі(арил)((С1морфінону знаходиться в інтервалі від приблизно С10)алкіл)2 або СІSі(арил)2((С1-С10)алкіл) в поляр1,0 до приблизно 9,0 молярних еквівалентів на ному органічному розчиннику і в присутності осномолярний еквівалент хлор-вмісного реагенту; в ви як описано в Розділі 5.1 з утворенням сполуки іншому втіленні, кількість сполуки формули R1SR2 формули (І), де R3 є -Si(CH3)2(C(CH3)3). використовуваної в способі одержання морфінону Сполуки формули (І), де R3 є -С(0)(С1-С10)алкіл знаходиться в інтервалі від приблизно 2,0 до приможна одержати взаємодією гідрохлориду морфіблизно 5,0 молярних еквівалентів на молярний ну з сполукою формули (С1-С10)С(О)ОС(О)(С1-С10) еквівалент хлор-вмісного реагенту; і в іншому втіу водному бікарбонаті натрію як описано в патенті ленні, кількість сполуки формули R1SR2 викорисUS 5,908,846, Bundgaard et al. товуваної в способі одержання морфінону знахоСполуки формули (І), де R3 є -бензил, можна диться в інтервалі від приблизно 2,5 до приблизно одержати взаємодією морфіну з бензилбромідом і 3,5 молярних еквівалентів на молярний еквівалент NaOH у водному метанолі при 25°С, як описано в хлор-вмісного реагенту. патенті US 6,013,796, Huang et al. В одному з втілень, кількість хлор-вмісного реСполуки формули (І), де R3 є -С(О)О(С1агенту використовуваного в способі одержання С10)алкіл, можна одержати взаємодією морфіну з морфінону знаходиться в інтервалі від приблизно сполукою формули СІС(О)О(С1-С10)алкіл в хлоро 19 87833 20 1,0 до приблизно 9,0 молярних еквівалентів на ли (І) не перетворяться у сполуку формули (II); в молярний еквівалент сполуки формули (І); в іншоіншому необмежуючому втіленні, спосіб одержанму втіленні, кількість хлор-вмісного реагенту виконя морфінону проводять доки, принаймні, приблиристовуваного в способі одержання морфінону зно 95 молярних відсотків сполуки формули (І) не знаходиться в інтервалі від приблизно 2,0 до приперетворяться у сполуку формули (II); і в іншому близно 5,0 на молярний еквівалент сполуки форнеобмежуючому втіленні, спосіб одержання мормули (І); і в іншому втіленні, кількість хлор-вмісного фінону проводять доки, принаймні, приблизно 99 реагенту використовуваного в способі одержання молярних відсотків сполуки формули (І) не переморфінону знаходиться в інтервалі від приблизно творяться у сполуку формули (II). 2,0 до приблизно 4,0 на молярний еквівалент споПротікання одержання морфінону можна контлуки формули (І). ролювати використовуючи звичайні аналітичні В деяких втіленнях, спосіб одержання морфіметодики аналогічні тим, що описані в Розділі 42 нону також може включати використання основи. для контролювання одержання карбонілу. Необмежуючими прикладами корисних основ є Типово, час достатній для проведення способу органічні основи і неорганічні основи описані в одержання морфінону знаходиться в інтервалі від Розділі 4.2 способу одержання карбонілу. приблизно 0,25 годин до приблизно 50 годин; в В одному з втілень основою є органічна осноіншому втіленні, час достатній для проведення ва. В одному з втілень, органічною основою є триспособу одержання морфінону знаходиться в інетиламін або пapa-N.N-диметиламінопіридин. тервалі від приблизно 0,5 годин до приблизно 25 В іншому втіленні, основою є неорганічна осгодин; і в іншому втіленні, час достатній для пронова. ведення способу одержання морфінону знахоВ одному з втілень, кількість основи викорисдиться в інтервалі від приблизно 1 годин до притовуваної в способі одержання морфінону знахоблизно 10 годин. диться в інтервалі від приблизно 1,0 до приблизно Типово, температура достатня для проведен15,0 молярних еквівалентів на молярний еквіваня способу одержання морфінону знаходиться в лент хлор-вмісного реагенту; в іншому втіленні, інтервалі від приблизно -78°С до приблизно 130°С; кількість основи використовуваної в способі одерв іншому втіленні, температура достатня для прожання морфінону знаходиться в інтервалі від приведення способу одержання морфінону знахоблизно 2,0 до приблизно 10,0 молярних еквівалендиться в інтервалі від приблизно -50°С до приблитів на молярний еквівалент хлор-вмісного зно 50°С; і в іншому втіленні, температура реагенту; і в іншому втіленні, кількість основи видостатня для проведення способу одержання користовуваної в способі одержання морфінону морфінону знаходиться в інтервалі від приблизно знаходиться в інтервалі від приблизно 2,5 до при40°С до приблизно 50°С. близно 7,0 молярних еквівалентів на молярний Спосіб одержання морфінону можна проводиеквівалент хлор-вмісного реагенту. ти при пониженому тиску, атмосферному тиску або В деяких втіленнях, спосіб одержання морфіпідвищеному тиску. В одному з втілень, спосіб нону також може включати використання органічодержання морфінону проводять при атмосферного розчинника. Необмежуючими прикладами ному тиску. корисних органічних розчинників є розчинники заВ іншому втіленні, спосіб одержання морфінозначені вище в способі одержання карбонілу. В ну проводять в інертній атмосфері, такій як, наодному з втілень, органічним розчинником є дихприклад, N2, He, Ne, Аr, Кr, Хе, або будь-яка їх лорметан. комбінація. В одному з втілень, спосіб одержання В одному з втілень, органічний розчинник, коморфінону проводять в атмосфері N2. ли використовується в способі одержання морфіПредставлений винахід також стосується комнону, присутній в кількості в інтервалі від приблизпозицій, що містять сполуку формули (І), сполуку но 0,1 вагових частин до приблизно 50 вагових формули R1SR2 і хлор-вмісну сполуку; де R1 і R2 є частин виходячи з ваги сполуки формули (І); в інкожен, незалежно, -(С1-С20)алкіл, -(С3шому втіленні, органічний розчинник, коли викориС8)циклоалкіл або -феніл; і R3 є захисна група. Ці стовується в способі одержання морфінону, прикомпозиції є корисними при одержанні сполуки сутній в кількості в інтервалі від приблизно 0,1 формули (II). вагових частин до приблизно 25 вагових частин В іншому втіленні, винахід стосується комповиходячи з ваги сполуки формули (І); і в іншому зицій, що містять сполуку формули (І), сполуку втіленні, органічний розчинник, коли використовуформули R1SR2 і хлор-вмісну сполуку; де R1 і R2 є ється в способі одержання морфінону, присутній в кожен, незалежно, -(С1-С20)алкіл, -(С3кількості в інтервалі від приблизно 0,1 вагових чаС8)циклоалкіл або -феніл; R3 є захисна група; і стин до приблизно 10 вагових частин виходячи з хлор-вмісним реагентом є трихлорізоцианурова ваги сполуки формули (І). кислота, N-хлорсукцинімід, дихлорізоцианурат В одному з втілень, органічний розчинник є натрію, 1,3-дихлор-5,5-диметилгідантоїн, СІ2, гіпобезводним. Способи одержання безводних розхлорит кальцію або будь-яка їх суміш. чинників описуються в Розділі 4.2 способу одерВ іншому втіленні, винахід стосується компожання карбонілу. зицій, що містять сполуку формули (І), сполуку Спосіб одержання морфінону проводять за формули R1SR2 і хлор-вмісну сполуку; де R1 і R2 є умов прийнятних для одержання сполуки формули кожен, незалежно, -(С1-С20)алкіл, -(С3(II). В одному з необмежуючих втілень, спосіб одеС8)циклоалкіл або -феніл; R3 є захисна група; і ржання морфінону проводять доки, принаймні, хлор-вмісним реагентом є трихлорізоцианурова приблизно 80 молярних відсотків сполуки форму 21 87833 22 кислота, N-хлорсукцинімід, СІ2 або будь-яка їх суR4C(O)OC(O)R4 або R4C(O)X за умов достатніх міш. для одержання сполуки формули (III), в якій В іншому втіленні, винахід стосується компоR1 і R2 є кожен, незалежно, -(С1-С20)алкіл, -(С3зицій, що містять сполуку формули (І), сполуку С8)циклоалкіл або -феніл, формули R1SR2 і трихлорізоцианурову кислоту; де R3 є захисна група; R1 і R2 є кожен, незалежно, -(С1-С20)алкіл, -(С3R4 є -(С1-С10)алкіл; і С8)циклоалкіл або -феніл; і R3 є захисна група. X є -СІ, -Вr або -І. В одному з втілень, винахід стосується компоСтадію взаємодії сполуки формули (І) із сполузиції, що містить сполуку формули R1SR2, як тут кою формули R1SR2 і хлор-вмісним реагентом за визначено, хлор-вмісну сполуку і сполуку формули умов достатніх для одержання сполуки формули (І), де R3 є -(С1-С10)алкіл, -бензил, -С(О)(С1(II) ("стадія одержання морфінону") можна провоС10)алкіл, -С(О)О(С1-С10)алкіл), -Sі((С1-С10)алкіл)3, дити за методами описаними в Розділі 4,3 для Sі(арил)((С1-С10)алкіл)2, -Sі(арил)2((С1-С10)алкіл), способу одержання морфінону. Р(О)((С1-С10)алкіл)2, -Р(S)((С1-С10)алкіл)2 або В одному з втілень, стадію одержання морфіS(O)OC6H4-n-CH3. нону проводять в присутності основи ("друга осноВ іншому втіленні, винахід стосується компова"), як описано в Розділі 4,3, коли спосіб одерзиції, що містить сполуку формули R1SR2, хлоржання морфінону проводять в присутності основи. вмісний реагент і сполуку формули (І), в якій R3 є Необмежуючими прикладами корисних других осSі((С1-С10)алкіл)3, -Sі(арил)((С1-С10)алкіл)2 або нов є ті, що описані в Розділі 4.2 для способу одеSі(арил)2(С1-С10)алкіл. ржання карбонілу. Друга основа, коли використоВ іншому втіленні, винахід стосується комповується на стадії одержання морфінону, може бути зиції, що містить сполуку формули R1SR2, хлортакою ж самою або іншою ніж перша основа. В вмісний реагент і сполуку формули (І), де R3 є одному з втілень, перша основа і друга основа, Sі((С1-С10)алкіл)3. коли використовуються, є однаковими. В іншому втіленні, винахід стосується компоВ одному з втілень, другою основою, коли визиції, що містить сполуку формули R1SR2, хлоркористовується на стадії одержання морфінону, є вмісний реагент і сполуку формули (І), де R3 є триетиламін або пара-N,N-диметиламінопіридин. Si(CH3)2(C(CH3)3). В іншому втіленні, другою основою, коли викоВ іншому втіленні, винахід стосується компористовується на стадії одержання морфінону, є зиції, що містить сполуку формули R1SR2, хлортриетиламін. вмісний реагент і сполуку формули (І), де R3 є В одному з втілень, кількість другої основи, СН3. коли використовується на стадії одержання морВ іншому втіленні, винахід стосується компофінону, знаходиться в інтервалі від приблизно 1,0 зиції, що містить сполуку формули R1SR2, хлордо приблизно 15,0 молярних еквівалентів на мовмісний реагент і сполуку формули (Іа). лярний еквівалент хлор-вмісного реагенту, в інВ іншому втіленні, композиції містять сполуку шому втіленні, кількість другої основи, коли викоформули (І) або (Іа), сполуку формули R1SR2 і ристовується на стадії одержання морфінону, хлор-вмісний реагент і також містять основу. Незнаходиться в інтервалі від приблизно 2,0 до приобмежуючими прикладами основ є ті, що описані в близно 10,0 молярних еквівалентів на молярний Розділі 4.2 способу одержання карбонілу еквівалент хлор-вмісного реагенту; і в іншому втіВ іншому втіленні, композиції містять сполуку ленні, кількість другої основи, коли використовуформули (І) або (Іа), сполуку формули R1SR2 і ється на стадії одержання морфінону, знаходиться хлор-вмісний реагент, а також містять органічний в інтервалі від приблизно 2,5 до приблизно 7,0 розчинник. Необмежуючими прикладами органічмолярних еквівалентів на молярний еквівалент них розчинників є та, що описані в Розділі 4.2 для хлор-вмісного реагенту. способу одержання карбонілу. Стадію взаємодії сполуки формули (II) з перВідносні молярні кількості сполуки формули (І) шою основою і ацилюючим агентом формули або (Іа), сполуки формули R1SR2 хлор-вмісного R4C(O)OC(O)R4 або R4C(O)X за умов достатніх реагенту, основи, якщо це має місце, і органічного для одержання сполуки формули (III) ("стадія одерозчинника, якщо це має місце, є такими як описаржання морфінондієнолкарбоксилату") можна но вище для способу одержання морфінону. проводити за методами описаними нижче. 4.4. Способи одержання 3-О-Захищених МорВ одному з втілень, стадія одержання морфіфінондіенолкарбоксилатів нондієнолкарбоксилату включає використання Як зазначено вище, представлений винахід сполуки формули (II), в якій R3 є -(С1-С10)алкіл, також стосується способів одержання сполуки фобензил, -С(О)(С1-С10)алкіл, -С(О)О((С1-С10)алкіл), рмули (III). Sі((С1-С10)алкіл)3, -Sі(арил)((С1-С10)алкіл)2, В одному з втілень, представлений винахід Sі(арил)2((С1-С10)алкіл), -Р(О)((С1-С10)алкіл)2, стосується способу одержання сполуки формули P(S)((С1-С10)2алкіл) або -S(O)OC6H4-n-CH3. (III), що включає: В одному з втілень, стадія одержання морфі(а) взаємодію сполуки формули (І) в присутнонондієнолкарбоксилату включає використання сті сполуки формули R1SR2 і хлор-вмісного реагесполуки формули (II), в якій R3 є -СН3. нту за умов достатніх для одержання сполуки фоВ іншому втіленні, стадія одержання морфінормули (II); і ндієнолкарбоксилату включає використання спо(б) взаємодію сполуки формули (II) з першою луки формули (II), в якій R3 є -Sі((С1-С10)алкіл)3, основою і ацилюючим агентом формули Sі(арил)((С1-С10)алкіл)2, або -Sі(арил)2((С1С10)алкіл). 23 87833 24 В іншому втіленні, стадія одержання морфіноВ одному з втілень, стадію одержання морфіндієнолкарбоксилату включає використання спонондієнолкарбоксилату проводять в присутності луки формули (II), в якій R3 є -Sі((С1-С10)алкіл)3. органічного розчинника. Необмежуючими приклаВ іншому втіленні, стадія одержання морфінодами корисних органічних розчинників для стадії ндієнолкарбоксилату включає використання споодержання морфінондієнолкарбоксилату є ті, що луки формули (II), в якій R3 є -Sі(СН3)2(С(СН3)3). описані в Розділі 4.2 для способу одержання карВ іншому втіленні, стадія одержання морфінобонілу. ндієнолкарбоксилату включає використання ациВ одному з втілень, органічним розчинником, люючого агенту формули R4C(O)OC(O)R4. коли використовується на стадії одержання морВ іншому втіленні стадія одержання морфінофінондієнолкарбоксилату, є дихлорметан, тетрагіндієнолкарбоксилату включає використання ацидрофуран, метилтетрагідрофуран, толуол або люючого агенту формули СН3С(О)ОС(О)СН3. будь-яка їх суміш. В іншому втіленні, спосіб одержання морфіноВ одному з втілень, кількість органічного розндієнолкарбоксилату включає використання ацичинника, коли використовується на стадії одерлюючого агенту формули R4C(O)X. жання морфінондієнолкарбоксилату, знаходиться В іншому втіленні, стадія одержання морфінов інтервалі від приблизно 1 вагової частини до ндієнолкарбоксилату включає використання ациприблизно 100 вагових частин виходячи з ваги люючого агенту формули R4C(O)X, в якій X є -F, сполуки формули (II); в іншому втіленні, кількість СІ, -Вr або -І. органічного розчинника, коли використовується на В іншому втіленні, стадія одержання морфіностадії одержання морфінондієнолкарбоксилату, ндієнолкарбоксилату включає використанняацизнаходиться в інтервалі від приблизно 5 вагових люючого агенту формули СН3С(О)СІ. частин до приблизно 50 вагових частин виходячи з Необмежуючими прикладами перших основ ваги сполуки формули (II); і в іншому втіленні, кількорисних на стадії одержання морфінондієнолкаркість органічного розчинника, коли використовубоксилату є ті, що писані в Розділі 4.2 для способу ється на стадії одержання морфінондієнолкарбокодержання карбонілу. силату, знаходиться в інтервалі від приблизно 10 В одному з втілень, першою основою є триалвагових частин до приблизно 25 вагових частин кіламін, пара-N,N-диметилпіридин або карбоксивиходячи з ваги сполуки формули (II). лат лужного металу. В одному з втілень, органічний розчинник, коВ іншому втіленні, першою основою є триетили використовується на стадії одержання морфіламін нондієнолкарбоксилату, є безводним. Способи В іншому втіленні, першою основою є пapaодержання безводних органічних розчинників опиN,N-диметилпіридин. суються в Розділі 4.2 для способу одержання карАцилюючі агенти формули R4C(O)OC(O)R4 або бонілу. R4C(O)X є комерційно доступними або можна одеСтадію одержання морфінондієнолкарбоксиржати за допомогою відомих методів. лату проводять за умов достатніх для одержання В одному з втілень, кількість ацилюючого агеморфінондієнолкарбоксилату. В одному з необменту використовуваного на стадії одержання моржуючих втілень, стадію одержання морфінондієфінондієнолкарбоксилату знаходиться в інтервалі нолкарбоксилату проводять доки, принаймні, привід приблизно 1 до приблизно 15 молярних еквіваблизно 80 молярних відсотків сполуки формули (II) лентів на молярний еквівалент сполуки формули не перетворяться у сполуку формули (III); в іншо(II); в іншому втіленні, кількість ацилюючого агенту му необмежуючому втіленні, стадію одержання використовуваного на стадії одержання морфінонморфінондієнолкарбоксилату проводять доки, дієнолкарбоксилату знаходиться в інтервалі від принаймні, приблизно 95 молярних відсотків споприблизно 1 до приблизно 10 молярних еквіваленлуки формули (II) не перетворяться у сполуку фотів на молярний еквівалент сполуки формули (II); і рмули (III); і в іншому необмежуючому втіленні, в іншому втіленні, кількість ацилюючого агенту стадію одержання морфінондієнолкарбоксилату використовуваного на стадії одержання морфінонпроводять доки, принаймні, приблизно 99 молярдієнолкарбоксилату знаходиться в інтервалі від них відсотків сполуки формули (II) не перетворятьприблизно 2 до приблизно 7 молярних еквіваленся у сполуку формули (III). тів на молярний еквівалент сполуки формули (II). Протікання стадії одержання морфінондієнолВ одному з втілень, кількість першої основи карбоксилату можна контролювати використовуювикористовуваної на стадії одержання морфінончи звичайні аналітичні методики аналогічні тим, що дієнолкарбоксилату знаходиться в інтервалі від описані в Розділі 4.2 приблизно 1 до приблизно 15 молярних еквіваленСтадію одержання морфінондієнолкарбокситів на молярний еквівалент ацилюючого агенту; в лату проводять протягом часу і при температурі іншому втіленні, кількість першої основи викорисдостатній для одержання сполуки формули (III). В товуваної на стадії одержання морфінондієнолкаодному з втілень, час достатній для одержання рбоксилату знаходиться в інтервалі від приблизно сполуки формули (III) знаходиться в інтервалі від 2 до приблизно 7 молярних еквівалентів на моляприблизно 1г до приблизно 50г; в іншому втіленні, рний еквівалент ацилюючого агенту; і в іншому час достатній для одержання сполуки формули втіленні, кількість першої основи використовуваної (III) знаходиться в інтервалі від приблизно 5 г до на стадії одержання морфінондієнолкарбоксилату приблизно 30г; і в іншому втіленні, час достатній знаходиться в інтервалі від приблизно 3 до придля одержання сполуки формули (III) знаходиться близно 6 молярних еквівалентів на молярний еквів інтервалі від приблизно 5г до приблизно 25г. валент ацилюючого агенту. 25 87833 26 В одному з втілень, температура достатня для карбоксилату, і ацилюючий агент і першу основу одержання сполуки формули (III) знаходиться в додають до сполуки формули (II), тобто, "однореаінтервалі від приблизно -78°С до приблизно темкторний" метод. ператури кипіння органічного розчинника, якщо В іншому втіленні, сполуку формули (II) не вивикористовується; в іншому втіленні, температура діляють після стадії одержання морфінону, і ацидостатня для одержання сполуки формули (III) люючий агент і першу основу додають одночасно знаходиться в інтервалі від приблизно -78°С до до сполуки формули (II). приблизно 130°С; в іншому втіленні, температура В іншому втіленні, сполуку формули (II) не видостатня для одержання сполуки формули (III) діляють після стадії одержання морфінону, і ацизнаходиться в інтервалі від приблизно 0°С до прилюючий агент додають першим до сполуки форблизно 100°С; і в іншому втіленні, температура мули (II) з наступним додаванням першої основи. достатня для одержання сполуки формули (III) В іншому втіленні, сполуку формули (II) не визнаходиться в інтервалі від приблизно 20°С до діляють після стадії одержання морфінону, і першу приблизно 75°С. основу є додають першою до сполуки формули (II) Стадію одержання морфінондієнолкарбоксиз наступним додаванням ацилюючого агенту. лату можна проводити при пониженому тиску, атВ іншому втіленні, стадія одержання морфіномосферному тиску або підвищеному тиску. В одну також включає другу основу; сполуку формули ному з втілень, стадію одержання (II) не виділяють після стадії одержання морфіноморфінондієнолкарбоксилату проводять при атмону; і ацилюючий агент додають до сполуки формусферному тиску. ли (II) з наступним додаванням першої основи. В одному з втілень, стадію одержання морфіВ іншому втіленні, стадія одержання морфінонондієнолкарбоксилату проводять в інертній атмону також включає другу основу; сполуку формули сфері, такій як, наприклад, N2, Не, Ne, Аr, Кr, Хе, (II) не виділяють після стадії одержання морфіноабо будь-яка їх комбінація. В іншому втіленні, стану; і ацилюючий агент і першу основу додають дію одержання морфінондієнолкарбоксилату проодночасно до сполуки формули (II); де друга основодять в атмосфері N2. ва і перша основа є однаковими. На стадії одержання морфінондієнолкарбокВ одному з втілень, сполуку формули (II) не силату, порядок додавання сполуки формули (II), виділяють після стадії одержання морфінону, і ацилюючого агенту, першої основи і органічного стадія одержання морфінону включає використанрозчинника, коли присутній, може змінюватись. ня першу основу і другу основу. Коли стадія одерВ одному з необмежуючих втілень, стадію жання морфінону включає використання першої одержання морфінондієнолкарбоксилату провооснови і другої основи, перша основа і друга оснодять шляхом додавання сполуки формули (II), нева можуть бути однаковими або різними. В одному обов'язково, в присутності органічного розчинника, з втілень, перша основа і друга основа є однакодо суміші, що містить ацилюючий агент і першу вими. В іншому втіленні, першою основою і другою основу, необов'язково, в присутності органічного основою є триетиламін. розчинника. В іншому втіленні, сполуку формули (II) видіВ іншому необмежуючому втіленні, стадію ляють перед її використанням на стадії одержання одержання морфінондієнолкарбоксилату провоморфінондієнолкарбоксилату. Способи виділення дять шляхом додавання суміші, що містить ацисполуки формули (II) є такими як обговорювалось люючий агент і першу основу, необов'язково, в в Розділі 4.2 для одержання кетонів або альдегідів присутності органічного розчинника, до сполуки в способі одержання карбонілу. формули (II), необов'язково, в присутності органічПри бажанні, сполуку формули (III) можна виного розчинника. ділити і очистити за методами аналогічними обгоВ іншому необмежуючому втіленні, стадію вореним в Розділі 4.2 для виділення і очистки одеодержання морфінондієнолкарбоксилату проворжаних кетонів або альдегідів в способі одержання дять шляхом додавання першої основи, необов'якарбонілу і/або за методами описаними нижче. зково, в присутності органічного розчинника, до В одному з втілень, спосіб виділення сполуки суміші, що містить сполуку формули (II), необов'яформули (III) включає контактування сполуки фозково, в присутності органічного розчинника, з нармули (III) з органічним розчинником і водою. ступним додаванням ацилюючого агенту, необоНаприклад, сполуку формули (III) можна видів'язково, в присутності органічного розчинника. лити шляхом контактування суміші ("стадія контакВ іншому необмежуючому втіленні, стадію тування"), що включає сполуку формули (III) і ородержання морфінондієнолкарбоксилату провоганічний розчинник з водою, що необов'язково дять шляхом додавання ацилюючого агенту, непідкислена. Коли вода, що використовується на обов'язково, в присутності органічного розчинника, стадії контактування не є підкисленою, органічну до суміші, що містить сполуку формули (II), необофазу збирають, водна фазу може надалі контактув'язково, в присутності органічного розчинника, з вати з органічним розчинником, і одержану біфазнаступним додаванням першої основи, необов'язну суміш можна необов'язково надалі обробити ково, в присутності органічного розчинника. основою, такою як 25% водний NaOH для підвиВ одному з втілень, сполуку формули (II) одещення рН водної фази в інтервалі від приблизно ржують використовуючи стадію одержання морфі7,0 до приблизно 9,0. нону і не виділяючи використовують на стадії одеКоли вода, що використовується на стадії конржання морфінондіенолкарбоксилату. тактування, є підкисленою, водну фазу збирають; В іншому втіленні, сполуку формули (II) не виводна фаза контактує з органічною фазою; одерділяють після стадії одержання морфінондієнолжану біфазну суміш потім обробляють основою, 27 87833 28 такою як 25% водний NaOH для підвищення рН люючим агентом за умов достатніх для одержання водної фази до значення в інтервалі від приблизно сполуки формули (III), як описано вище. 7,0 до приблизно 9,0; і органічну фазу збирають. Наступні приклади приведені для кращого роОб'єднані органічні фази концентрують до зазуміння винаходу і не обмежують описаний виналишку при пониженому тиску, і одержаний залихід і пункти формули винаходу. Такі варіації винашок можна потім відокремити і очистити за метоходу, включаючи заміну всіх еквівалентів відомих дами аналогічними тим, що описані в Розділі 4.2, зараз або розроблених потім, які будуть попадати такі як, наприклад, перегонка, кристалізація і/або в межі знань спеціаліста в цій галузі, і зміни рецепхроматографія. тур або незначні зміни в експериментальних метоНеобмежуючими прикладами корисних органідиках, попадають в межі рамок представленого чних розчинників для контактування сполуки форвинаходу. мули (III) з водою є органічні розчинники, що не 5. Приклади змішуються з водою, такі як нерозгалужені і розга5.1. Приклад 1: Синтез 3-О-Біс(диметил-тлужені аліфатичні (С4-С10)вуглеводні, такі як бутабутил)силілморфіну ни, пентани, гексани, гептани, октани, нонани, деРозчин диметил-т-бутилсилілхлориду (0,115г, кани; циклічні аліфатичні (С4-С7)вуглеводні, такі як 0,76 ммоль) в тетрагідрофурані (76мл) (Aldrich) циклобутан, циклопентан, циклогексан і циклогепдодавали протягом приблизно 5хв до розчину тан; ароматичні вуглеводні, такі як бензол, толуол морфіну (20,38г, 71ммоль), імідазолу (14,59г; 214 і ксилен, кожен з яких може бути заміщений одним ммоль) і диметилформаміду ("ДМФА") (100мл) при або декількома -гало або -гідроксигрупами; (С125°С в атмосфері N2. Одержаний зелений розчин С3)вуглеводні заміщені двома або більше галогеперемішували при 25°С протягом 24г і концентрунами, такі як дихлорметан, хлороформ і тетрахловали при пониженому тиску і при 40°С. Одержану рид вуглецю; діалкілові етери, такі як діетиловий в'язку суміш додавали до деіонізованої води (500г) етер, діізопропіловий етер, дибутилові етери і мепри 25°С і одержаний білий осад збирали фільттилбутилові етери; етилацетат; і будь-яка їх суміш. руванням. Тверду речовину розчиняли в дихлорВ одному з втілень, органічним розчинником є диметані (100мл) і одержану органічну фазу збирали. хлорметан. Органічну фазу сушили над сульфатом натрію, Сполуки формули (III) корисні для одержання фільтрували і фільтрат концентрували при пониморфінових алкалоїдів, таких як налоксон, налтреженому тиску при 40°С. Одержаний залишок перексон і оксикодон за допомогою методів добре вікристалізували з гептану, що кипить (75мл), одердомих в цій галузі (дивіться, наприклад, патент US жуючи 3-О-біс(диметил-т-бутил)силілморфін як 6,013,796, Huang et al). білі кристали. Вихід: 13,60г (34 ммоль, 48%). При бажанні, R3 захисну групу сполуки форму5.2. Приклад 2: Однореакторний синтез кодеїли (III) можна видалити і замінити групою, такою як нондіенолацетату -Н ("стадія зняття захисту"). Типово, стадію зняття Одержання кодеїнону: Трихлорізоцианурову захисту не проводять до завершення інших хімічкислоту (2,30г, 3,8 ммоль) завантажували у 100мл них реакцій, що можуть несприятливо впливати на круглодонну колбу споряджену дистиляційною присутню гідроксигрупу на бензольному кільці насадкою і вміст колби охолоджували до -30°С в морфінового алкалоїду. Способи видалення спеатмосфері N2. У колбу додавали безводний дихцифічних захисних груп в морфінових алкалоїдах лорметан (15мл) і одержану суспензію перемішуописуються, наприклад, в патенті US 4,472,253, вали протягом 30хв при -30°С. По краплям протяSchwartz (де R3 є -алкіл); патенті US 5,112,975, гом 5 хвилин до суспензії додавали розчин кодеїну Wallace (де R3 є - карбонат); і патенті US (2,97г, 9,9ммоль) в безводному дихлорметані 6,008,355, Huang et al. (де R3 є -ацил); або за до(15мл.) і вміст колби перемішували протягом припомогою способів відомих в цій галузі для захисту близно 30хв при -30°С. Одержану молокоподібну фенолів (дивіться, наприклад, Greene et al., Proсуспензію витримували при -30°С і по краплям tective Groups in Organic Synthesis 143-170 (1991), протягом приблизно 10 хвилин додавали триетикожен з яких включений сюди як посилання). ламін (6,91мл, 50 ммоль). Одержану світлоЯк зазначено вище, представлений винахід коричневу суспензію нагрівали до 10°С і залишали також стосується нових сполук формули (III), де R3 на 2г і за цей час завершувалось перетворення є -Sі((С1-С10)алкіл)3, -Sі(арил)((С1-С10)алкіл)2 або кодеїну у кодеїнон. Sі(арил)2(С1-С10)алкіл; і R4 є -(С1-С10)алкіл. Одержання кодеїнондієнолацетату: Коричневу В одному з втілень, представлений винахід суспензію описану вище залишали нагріватись до стосується нових сполук формули (III), де R3 є кімнатної температури і додавали оцтовий ангідSі((С1-С10)алкіл)3. рид (4,68мл, 50 ммоль). Вміст колби нагрівали до В іншому втіленні, представлений винахід таприблизно 50°С і приблизно 90% дихлорметану кож стосується нових сполук формули (ІІІ), де R3 євидаляли перегонкою. Одержану суспензію залиSі(СН3)2(С(СН3)3). шали охолоджуватись до приблизно 25°С і переВ іншому втіленні, представлений винахід тамішували протягом 17г при 25°С і за цей час завекож стосується нових сполук формули (III), дe R4 є ршувалось перетворення кодеїнону у -CH3. кодеїнондієнолацетат. Нові сполуки формули (III) можна одержати Дихлорметан (20мл) додавали до реакційної взаємодією сполуки формули (II), де R3 є -Sі((С1суміші і суміш охолоджували до 0°С. До охолоС10)алкіл)3, -Sі(арил)((С1-С10)алкіл)2 або дженої суміші додавали розчин 3мл 88% (в/в) муSі(арил)2((С1-С10)алкіл), з першою основою і ацирашиної кислоти в 20мл води охолодженої приблизно до 0°С і біфазну суміш перемішували 29 87833 30 протягом 5хв при 0°С Одержану органічну фазу Представлений винахід не обмежується рамзбирали і промивали розчином 1мл 88% (в/в) муками специфічних втілень описаних в прикладах, рашиної кислоти в 20мл води. Водні шари об'єднуякі призначені для ілюстрації деяких аспектів вивали і охолоджували до приблизно 0°С. Додавали находу і будь-які втілення, що функціонально еквідихлорметан (20мл), потім 25% (в/в) водний гідровалентні, знаходяться в межах цього винаходу. ксид натрію до рН водної фази 8,75. Водний шар Насправді, різні модифікації винаходу на додаток збирали і екстрагували з дихлорметаном (20мл) до тут показаних і описаних будуть очевидні спеціОб'єднані органічні шари сушили над сульфатом алістам в цій галузі і попадають в рамки приведенатрію, фільтрували і концентрували при понижених далі пунктів формули винаходу. ному тиску при 30°С Одержаний масляний залиРяд посилань приведених тут, повні описи шок сушили при 40 Торр при 30°С одержуючи кояких включені сюди як посилання. деїнондієнолацетат як світло-коричневу тверду речовину. Вихід 2,82г (83 ммоль; 84%). Комп’ютерна верстка В. Мацело Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюComposition and process for the preparation of ketone
Автори англійськоюStumpf Andreas
Назва патенту російськоюКомпозиция и способ получения кетона
Автори російськоюШтумпф Андреас
МПК / Мітки
МПК: C07D 489/00, C07F 7/08
Мітки: спосіб, одержання, кетону, композиція
Код посилання
<a href="https://ua.patents.su/15-87833-kompoziciya-ta-sposib-oderzhannya-ketonu.html" target="_blank" rel="follow" title="База патентів України">Композиція та спосіб одержання кетону</a>
Попередній патент: Стереоселективний синтез аналогів вітаміну д
Наступний патент: Лопатеве колесо шахтної турбомашини
Випадковий патент: Двостаторний вітроелектрогенератор з дисковим зіставним ротором і постійними магнітами збудження












