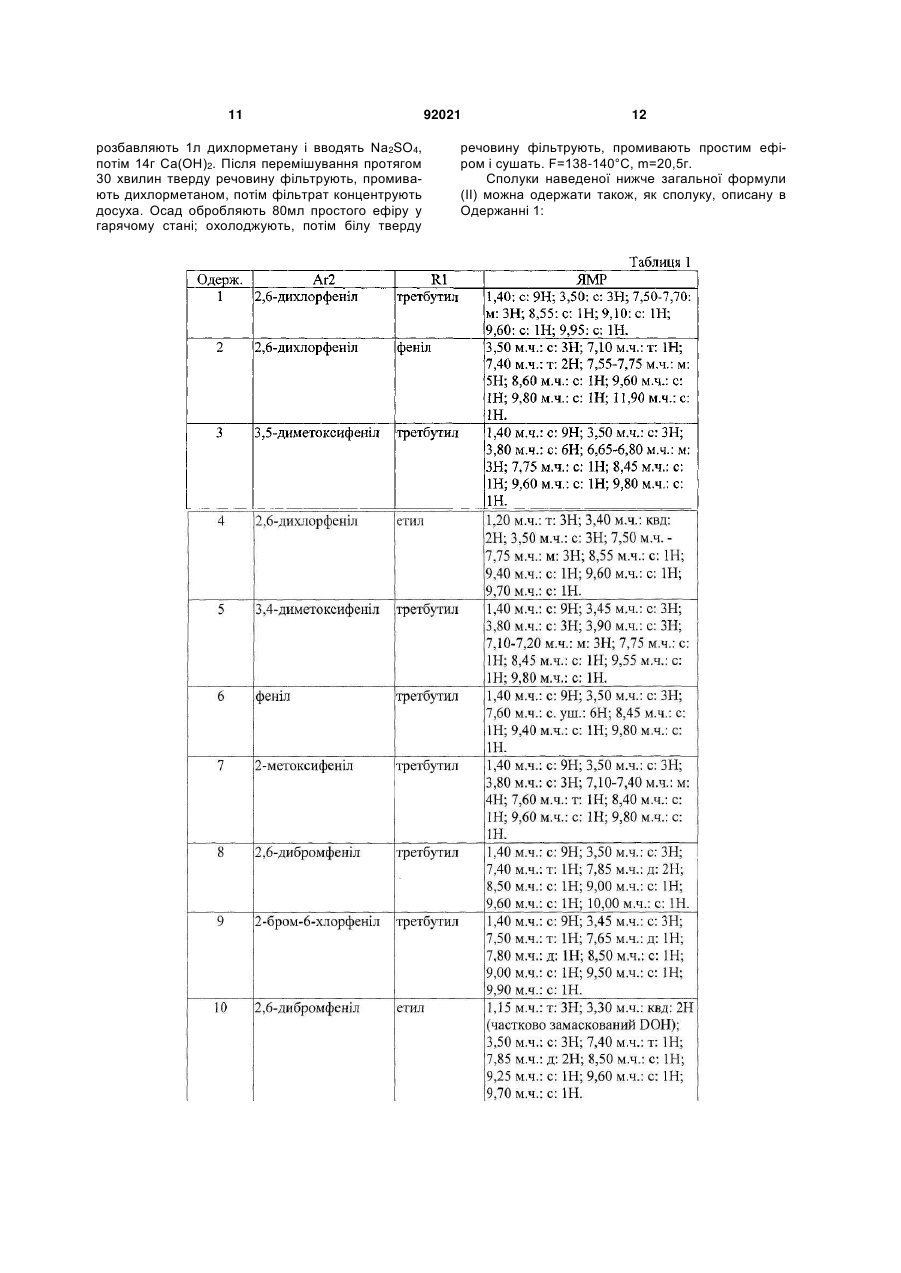
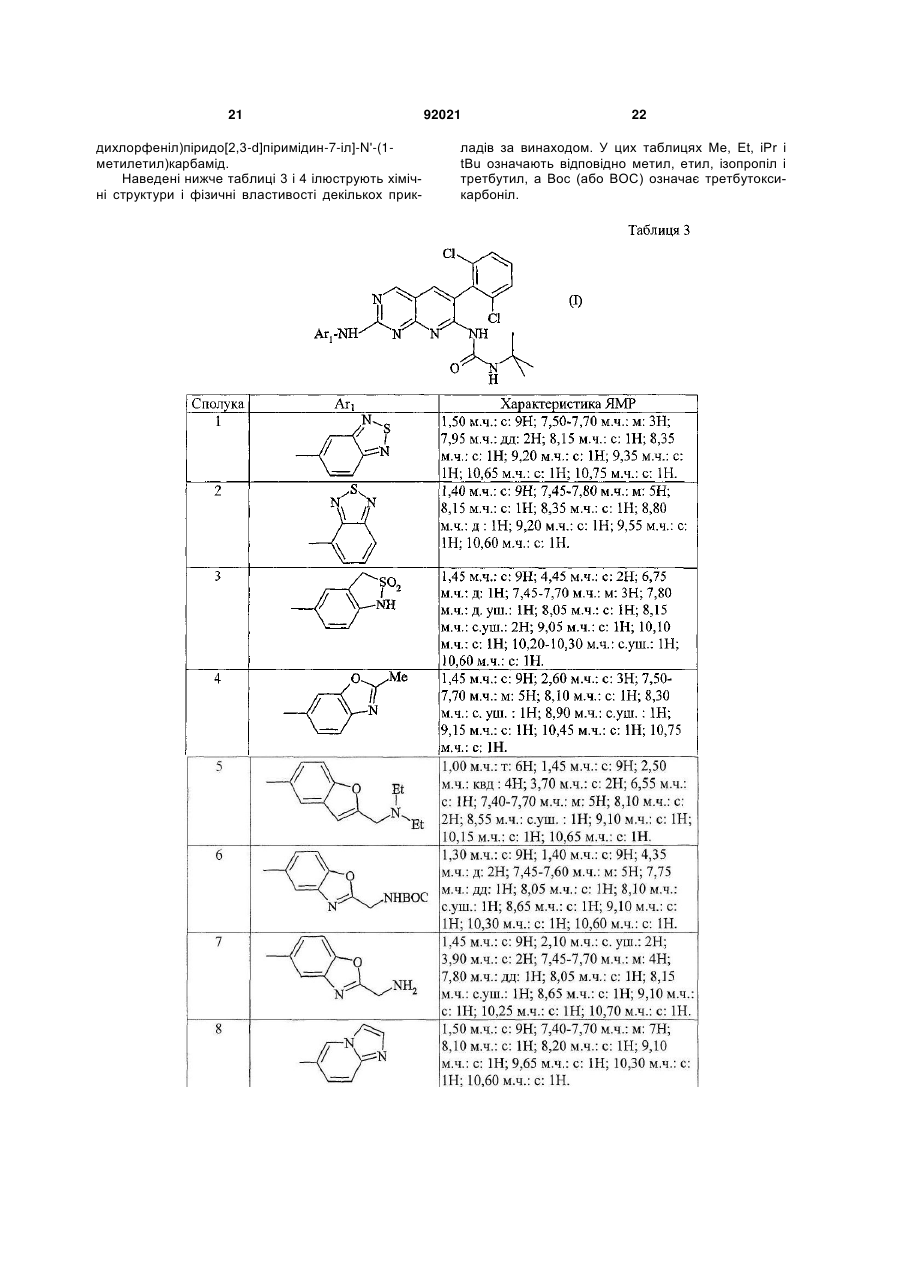
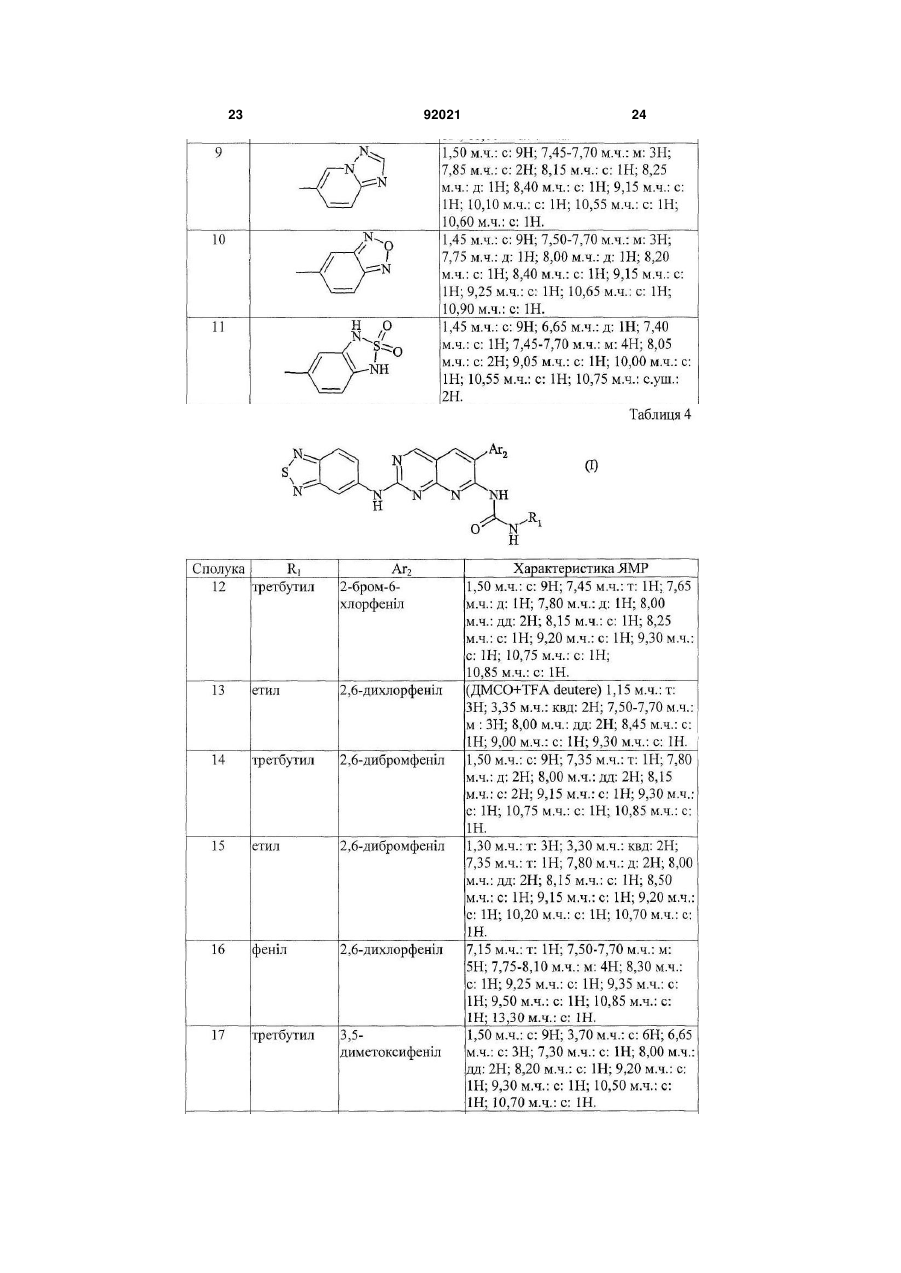
Похідні піридо[2,3-d]піримідину, їх одержання, їх застосування у терапії
Номер патенту: 92021
Опубліковано: 27.09.2010
Автори: Казелла П'єр, Мюно Клод, Жегам Самір, Буррі Бернар, Перро П'єр
Формула / Реферат
1. Сполука формули (І)
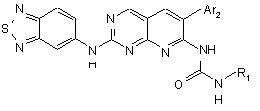 ,
,
в якій Аr2 і R1 є відповідно:
2,6-дихлорофеніл та трет-бутил
або 2-бромо-6-хлорфеніл та трет-бутил;
або 2,6-дихлорофеніл та етил;
або 2,6-дибромофеніл та трет-бутил;
або 2,6-дибромофеніл та етил;
або 2,6-дихлорофеніл та феніл;
або 3,5-диметилоксифеніл та трет-бутил;
або феніл та трет-бутил;
або 2,6-диметилфеніл та трет-бутил;
або 2,6-дифторофеніл та трет-бутил;
або 2,6-дихлорофеніл та ізопропіл.
2. Сполука формули
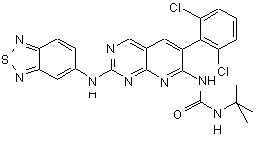 .
.
3. Сполука за п. 1 або 2, яка відрізняється тим, що вона знаходиться у:
- нехіральній або рацемічній формі, або у формі, збагаченій одним стереоізомером, або збагаченій одним енантіомером;
- може бутиперетворена у сіль;
- вона може бути гідратованою або сольватованою.
4. Фармацевтична композиція, яка відрізняється тим, що вона містить сполуку формули (І) за будь-яким з пп. 1-3, а також щонайменше один фармацевтично прийнятний ексципієнт.
5. Фармацевтична композиція за п. 4, яка відрізняється тим, що вона додатково містить щонайменше одну протиракову активну речовину.
6. Лікарський засіб, який відрізняється тим, що він містить сполуку за будь-яким з пп. 1-3 або сіль приєднання цієї сполуки з фармацевтично прийнятною кислотою, або гідрат або сольват такої сполуки.
7. Сполука за будь-яким з пп. 1-3 як протираковий агент.
8. Застосування сполуки за будь-яким з пп. 1-3 для одержання лікарського засобу, призначеного для лікування або запобігання захворюванням, викликаним або загостреним проліферацією клітин.
9. Застосування за п. 8 для запобігання або лікування лейкемій, солідних пухлин, первинних або метастатичних, карцином і раку.
10. Спосіб одержання сполуки за п. 1, який відрізняється тим, що проводять взаємодію сполуки формули
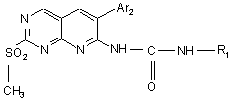 , (ІІ)
, (ІІ)
в якій R1 і Аr2 визначені в п. 1,
з аміном формули
 .
.
11. Спосіб одержання сполуки за п. 1, який відрізняється тим, що проводять взаємодію:
(і) сполуки формули
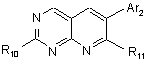 , (IIb)
, (IIb)
в якій
R10 означає відхідну групу, таку як:
(а) галоген, зокрема Сl або Вr, або
(b) алкіл-S(О)m-, де m=0, 1 або 2;
R11 означає NHC(O)-NH-R1;
і (ii) аміну формули  ,
,
в якій
(a) R10 означає галоген або алкіл-S(O)m-, де m=2,
взаємодію проводять у розчиннику, переважно полярному, за температури між кімнатною температурою та температурою кипіння розчинника;
(b) якщо R10 означає алкіл-S(О)m-, де m=0 або 1,
взаємодію здійснюють з

у розплавленому стані;
де у випадку необхідності аміногрупу сполуки  попередньо перетворена у сіль або захищена.
попередньо перетворена у сіль або захищена.
Текст
1. Сполука формули (І) 3 92021 9. Застосування за п.8 для запобігання або лікування лейкемій, солідних пухлин, первинних або метастатичних, карцином і раку. 10. Спосіб одержання сполуки за п.1, який відрізняється тим, що проводять взаємодію сполуки формули Ar2 N SO2 NH N N C NH , (II) , (ІІ) в якій R1 і Аr2 визначені в п.1, з аміном формули N N S N NH2 N S N S NH2 .. 11. Спосіб одержання сполуки за п.1, який відрізняється тим, що проводять взаємодію: (і) сполуки формули Ar2 N R10 (b) алкіл-S(О)m-, де m=0, 1 або 2; R11 означає NHC(O)-NH-R1; , і (ii) аміну формули, в якій (a) R10 означає галоген або алкіл-S(O)m-, де m=2, взаємодію проводять у розчиннику, переважно полярному, за температури між кімнатною температурою та температурою кипіння розчинника; (b) якщо R10 означає алкіл-S(О)m-, де m=0 або 1, взаємодію здійснюють з R1 O CH3 4 N N R11 N NH2 , у розплавленому стані; де у випадку необхідності аміногрупу сполуки N S N , (IIb) , (IIb) NH2 , попередньо перетворена у в якій R10 означає відхідну групу, таку як: (а) галоген, зокрема Сl або Вr, або сіль або захищена. Даний винахід стосується похідних піридо[2,3d]піримідину, їх одержання і їх застосування у терапії. Сполуки, що є похідними піридо[2,3d]піримідину описані у патентних заявках WO 01/55147 і WO 03/000011 та у патентах ЕР-В1790997 і US 5 733 913. Ці сполуки є потенційно придатними для лікування порушень проліферації клітин. Так, відповідно до першого аспекту, об'єктом даного винаходу є сполуки формули (І) (С1-С6)алкілу або (CH2)nNR4R5 і R'2 означає (CH2)nNR4R5. R4 і R5 означають, кожний незалежно один від іншого, замісник, вибраний з Н, (С1-С6)алкілу, (С1С6)алкіл(С3-С7)циклоалкілу, (С3-С7)циклоалкілу, C(=NH)NH2, SО2(С1-С6)алкілу, R5 може також означати СО-((С1-С4)алкіл, СО-(С3-С7)циклоалкіл, СО-арил, SO2-арил, третбутоксикарбоніл або бензилоксикарбоніл; або R4 і R-5 разом з атомом азоту, з яким вони зв'язані, утворюють азетидиніл, піролідиніл, піперидиніл, піперазиніл або морфолініл, причому зазначений радикал є незаміщеним або заміщеним один або два рази (С1-С4)алкільною, (С1-С6)алкілОН, СОО(С1-С6)алкільною групою; Аr1 означає фенільну групу, незаміщену або заміщену 1-5 разів подібними або різними замісниками, вибраними з атома галогену, (С1С4)алкільної, трифторметильної або (С1С4)алкокси групи; n означає 1, 2 або 3. Відповідно до переважного варіанту сполуки формули (І) мають замісник Аr1, що означає радикал, вибраний з: (I) в якій R1 вибирають з групи, що складається з (С1С6)алкілу, (С1-С6)алкіл(С3-С7)циклоалкілу, CH2COR3, фенілу або фенілу, заміщеного гідрокси і/або галогеном, і/або (С1-С6)алкілом. R3 означає гідроксильну групу, (С1-С4)алкокси, аміно, (С1-С4)алкіламіно, ді(С1-С4))алкіламіно; Аr1 означає радикал, вибраний з: в якому X означає О або S, Υ означає СН2 або ΝΗ і R2 вибирають з групи, що складається з Н, 5 в якому R2 означає СН3 або (CH2)nNR4R5 і R'2 означає CH2NR4R5, де R4 і R5 незалежно вибрані з Η і (С1-С6)алкілу, Υ означає СН2 або ΝΗ. Продукти за винаходом переважно мають замісник Аr2, що означає радикал: в якому кожний R6, R7 незалежно вибраний з групи, що складається з Н, СН3, ОСН3, F, СІ, Br, R6 і R7 переважно знаходяться у положенні 2 і 6. Продукти за винаходом переважно мають замісник Аr2, вибраний з фенілу, 2-метоксифенілу, 2,6-дихлорфенілу, 3,5-диметоксифенілу, 3,4диметоксифенілу, 2,6-дибромфенілу, 2-бром-6хлорфенілу, 2,4-дихлорфенілу, 3,5-дихлорфенілу, 2,6-диметилфенілу і 2,6-дифторфенілу. Відповідно до переважного варіанту, сполуки формули (І) мають замісник Аr1, що означає радикал, вибраний з Найбільш переважною сполукою за винаходом є (N-[2-(2,1,3-бензотіадіазол-5-іламіно)-6-(2,6дихлорфеніл)піридо[2,3-d]піримідин-7-іл]-N'-(1,1диметилетил)карбамід. Сполуки з наведених нижче прикладів є об'єктом даного винаходу. Сполука за винаходом може: (і) бути у нехіральній або рацемічній формі або збагаченою стереоізомером або збагаченою енантіомером; (іі) бути у вигляді солі і (ііі) бути гідратованою або сольватованою. Сполуки формули (І) можуть містити один або декілька асиметричних атомів вуглецю. Таким чином, вони можуть бути у формі енантіомерів або діастереоізомерів. Ці енантіомери, діастереоізомери, а також їх суміші, включаючи рацемічні суміші, належать до винаходу. Сполуки формули (І) можуть існувати у вигляді основ або солей приєднання з кислотою. Якщо сполуки формули (І) містять вільні кислотні групи, наприклад, карбоксильну, сульфонову, фосфонову, ці кислотні групи можуть бути перетворені у солі за допомогою основ для одержання солей приєднання. Такі солі приєднання належать до винаходу. Солі приєднання з кислотою або основою переважно одержують відповідно за допомогою фармацевтично прийнятних кислот або основ, але солі з іншими кислотами або основами, придатні, наприклад, для очищення або виділення сполук формули (І), також належать до винаходу. 92021 6 Сполуки формули (І) можуть також бути у вигляді гідратів або сольватів, а саме, у вигляді асоціацій або комбінацій з однією або декількома молекулами води або з розчинником. Такі гідрати або сольвати також належать до винаходу. У межах даного винаходу розуміють під: атомом галогену: фтор, хлор, бром або йод; алкільною групою: аліфатичну насичену групу, лінійну або розгалужену. Як приклад можна назвати: метил, етил, н-пропіл, н-бутил, н-пентил, нгексил, н-гептил, 1-метил етил, 1-метилпропіл, 2метилпропіл, 1,1-диметилетил, 1-метилбутил, 2метилбутил, 3-метилбутил, 1,1-диметилпропіл, 1,2-диметилпропіл, 2,2-диметилпропіл, 1метилпентил, 2-метилпентил, 3-метилпентил, 4метилпентил, 1,1-диметибутил, 1,2-диметибутил, 1,3-диметибутил, 2,2-диметибутил, 2,3диметибутил, 3,3-диметибутил, 1,1,2триметилпропіл, 1,2,2-триметилпропіл, 1-етил, 1метилпропіл, 1-етил,2-метилпропіл, 1-етилбутил, 2-етилбутил, 1-метилгексил, 2-метилгексил, 3метилгексил, 4-метилгексил, 5-метилгексил, 1,1диметилпентил, 1,2-диметилпентил, 1,3диметилпентил, 1,4-диметилпентил, 2,2диметилпентил, 2,3-диметилпентил, 2,4диметилпентил, 3,3-диметилпентил, 3,4диметилпентил, 4,4-диметилпентил, 1,1,2триметилбутил, 1,1,3-триметилбутил, 1,2,2триметилбутил, 1,2,3-триметилбутил, 1,3,3триметилбутил, 2,2,3-триметилбутил, 2,3,3триметилбутил, 1,1,2,2-тетраметилпропіл, 1етилпентил, 2-етилпентил, 3-етилпентил, 1-етил, 1-метилбутил, 1-етил, 2-метилбутил, 1-етил, 3метилбутил, 2-етил, 1-метилбутил, 2-етил, 2метилбутил, 2-етил, 3-метилбутил, 1-пропілбутил, 1-(1-метилетил)бутил, 1-(1-метилетил), 2метилпропіл. циклоалкільною групою: циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил, біцикло[2.2.1]гептил, циклооктил, біцикло[2.2.1]октил, біцикло[3.2.1]октил, адамантил. Сполуки формули (І) одержують шляхом взаємодії сполуки формули (II) (lI) в якій R1 і Аr2 такі, як визначені для (І), і аміну формули Аr'1NH2 (III), в якій Аr'1 означає Аr1, такий, як визначений для (І) або попередник Аr1; у випадку необхідності групу Аr'1 одержаної таким чином сполуки перетворюють у групу Ar1. Відповідно до винаходу можна одержати сполуки формули (І) способом, який відрізняється тим, що вводять у взаємодію: (і) сполуку формули (Ilb) в якій R10 означає вихідну групу, таку як: (а) галоген, зокрема, СІ або Вr, або (b) алкіл-S(O)m-, де m=0, 1 або 2; R11 означає NHC(O)-NH-R1; і 7 92021 8 (іі) амін формули Ar'1NH2 (llІ), в якій Ar'1 означає Аr1 такий, як визначений для (І) або попередник Аr1; у випадку необхідності групу Аr'1 одержаної таким чином сполуки перетворюють у групу Ar1. Якщо R10 означає галоген або алкіл-S(O)m-, де m=2, взаємодію проводять у розчиннику, переважно полярному: (і) наприклад, тетрагідрофурані, диметилсульфоксиді або етанолі, можливо, у присутності сліду кислоти, такої як соляна кислота; або (іі) у диметилсульфоксиді у присутності сильної основи, такої як tBuOk; при температурі від кімнатної температури до температури кипіння розчинника. Якщо Rio означає алкіл-S(O)m-, де m=0 або 1, можна здійснювати взаємодію з розплавом Ar'1NH2 (III), переважно при температурі приблизно 200°С без каталізатора. У випадку необхідності аміногрупи, присутні у групі Аr'1 сполуки (III), попередньо перетворені у сіль або захищені. Сполуки формули (II) одержують методом, описаним у європейському патенті 790997 і патенті US 5733913, як показано нижче на Схемі 1: Аміни формули (III) Ar'1NH2 відомі або можуть бути одержані відомими методами з відповідних нітропохідних Ar'1NO2 (IV) шляхом відновлення або (і) у кислому середовищі у присутності металу, такого як порошкоподібне залізо або цинк, або (іі) за допомогою водню у присутності каталізатора, такого як Pd/C. Аr' означає Аr або попередник Аr. Сполуки формули (IV) відомі або можуть бути одержані відомими способами. Сполуки за винаходом одержують у рацемічній формі; потім можна одержати оптично чисті ізомери, використовуючи методи розщеплення, відомі фахівцеві, такі як кристалізація шляхом утворення солей з хіральними агентами. Можна також одержувати сполуки за винаходом в оптично чистій формі, використовуючи методи асиметричного або стереоспецифічного синтезу, хроматографічних технологій з використанням хіральної фази. До того ж, продукти за винаходом можна виділяти шляхом утворення діастереоізомерів, їх розділення, з подальшим розкладанням фармакологічно придатного діастереоізомеру і одержанням його активного енантіомерно чистого продукту. Можна також застосовувати ферментативні технології. Можна додатково використовувати відомі технології розділення. До них належать розкриті у: Enantiomers, Racemates and Resolutions, John Willey and Sons, New York (1981). Сполуки за винаходом можна також одержати у формі, збагаченій стереоізомером при одержанні проміжних продуктів синтезу. Таким чином, роз щеплення енантіомерів амінів формули (III) або нітрованих попередників (IV) можна здійснювати зазначеними способами. Наведені нижче приклади описують одержання деяких проміжних продуктів і сполук за винаходом. Ці приклади не обмежують, а тільки ілюструють винахід. У прикладах використані наступні абревіатури: Вос: третбутоксикарбоніл; ВОР: бензотриазол-1ілокситри(диметиламіно)фосфонію гексафторфосфат; ТГФ: тетрагідрофуран; ТА: кімнатна температура; TFA: трифтороцтова кислота; DCM: дихлорметан; ДМСО: диметилсульфоксид; DMF: диметилформамід; МеОН: метанол; DCCI: дициклогексилкарбодіімід; DIPEA: діізопропілетиламін; KHSO4/K2SO4: 5%-ний розчин KHSO4/K2SO4. Спектри ядерного магнітного резонансу (ЯМР) протону реєструють при 200 або 250МГц у ДМСОd6, якщо не зазначено інше. Сигнал ДМСО-d6 реєструється у 2,5 м.ч. і служить контрольним. Для інтерпретації спектрів використовують наступні абревіатури: с: синглет, д: дублет, т: триплет, м: масив, мт: мультиплет, суш.: розширений синглет, дд: дублет дублета, кд: квадруплет, кт: квінтет. 9 92021 F: точка плавлення (у градусах Цельсію), така як виміряна на апараті Buchi В545 з градієнтом температури 1°С за хвилину. МН+: мас-спектр. Сполуки аналізують шляхом поєднання ВЕРХ-УФ-МС (рідинна хроматографіяУФ-детекція-мас-спектрометрія). Використовуваний пристрій, що випускається Agilent, складається з хроматографу HP 1100, обладнаного детектором з діодами Agilent і спектрометром квадриполярної маси MSD Quad. Умови аналізу наступні: Колонка: Symmetry C18 (50 2,1мм; 3,5мкм) Елюент A: H2O+TFA 0,005% при рН3,15 Елюент В: CH3CN+TFA 0,005% Градієнт: Час (хв.) 0 10 15 16 20 %В 0 90 90 0 0 Температура у колонці: 30°С Витрата: 0,4мл/хв. Детекція: =210нм Тr: час затримки ν: об'єм. Одержання сполуки формули (II) Одержання 1 N-(трет-бутил)-N'-[6(2,6-дихлорфеніл)-2(метилсульфоніл)піридо[2,3-d]піримідин-7іл]карбамід 1.1 Етил-4-аміно-2-(метилтіо)піримідин-5карбоксилат У суспензію 50,7г етил-4-хлор-2(метилтіо)піримідин-5-карбоксилату у 400мл ЕtOН вводять протягом 20 хвилин, підтримуючи температуру близько 20°С, 140мл 20%-ного розчину NH4OH. Після перемішування протягом 20 годин при кімнатній температурі реакційне середовище концентрують у вакуумі майже досуха, потім осад обробляють у 350мл води, перемішують протягом 20 хвилин, фільтрують, промивають 3×60мл води, потім сушать у вакуумі у присутності Р2О5. Одержують тверду речовину білого кольору, F=134135°C, m=39,9г. 1.2 [4-аміно-2-(метилтіо)піримідин-5іл]метанол У 39,68г складного ефіру, одержаного на попередній стадії, розчиненого в 1 літрі ТГФ, протягом 45 хвилин вводять 210мл розчину 1М LiAIH4 у ТГФ, підтримуючи температуру нижче 30°С. Перемішують ще протягом 1 години, потім знижують температуру до 5°С і послідовно вводять по краплях 9мл води, 6,5мл гідроксиду натрію 5Ν, потім 32мл води. Перемішують протягом 10 хвилин, тве 10 рду речовину фільтрують, потім промивають ТГФ. Фільтрат концентрують у вакуумі досуха, потім осад повторно розчиняють у 600мл толуолу при кипінні, швидко фільтрують у гарячому стані для видалення невеликої кількості речовини, що не розчинилася, і охолоджують фільтрат протягом ночі. Одержані білі кристали фільтрують, промивають невеликою кількістю толуолу, потім простого ефіру і сушать, F=124-127°C, m=23,9г. 1.3 4-аміно-2-(метилтіо)піримідин-5карбальдегід У суспензію 23,8г спирту, одержаного на попередній стадії, у 1600мл хлороформу вводять протягом 2 хвилин 79,5г активного МnО2 і перемішують протягом 1 ночі при кімнатній температурі; тверду речовину фільтрують, промивають 3 75мл СНСl3 і фільтрат концентрують у вакуумі досуха; білий твердий осад обробляють простим ефіром, фільтрують, сушать, F=184-186°C, m=21,05г. 1.4 6-(2,6-дихлорфеніл)-2-(метилтio)піридо [2,3-d]піримідин-7-амін В 21г альдегіду, одержаного на попередній стадії, розчиненого у 240мл ДМФ і охолодженого до 5°С протягом 5 хвилин, вводять 5,47г 60%-ного NaH, потім протягом 20 хвилин невеликими фракціями вводять 29,05г 2,6дихлорфенілацетонітрилу. Перемішують протягом 30 хвилин при 5°С, потім протягом ночі при кімнатній температурі. Реакційне середовище охолоджують до 5°С і вводять 65мл насиченого розчину NH4Cl, потім 500мл суміші вода/лід; утворюється червоний осад, який фільтрують, двічі промивають водою, максимально віджимають, промивають простим ефіром, 100мл хлороформу, потім знову простим ефіром; сушать і одержують тверду речовину бежевого кольору, F=250-253°C, m=29,92г. Фази простого ефіру і хлороформу після промивання концентрують досуха, обробляють невеликою кількістю хлороформу з додаванням простого ефіру: одержують другий струмінь 3,15г, загальна m=33,07г. 1.5 N-(трет-бутил)-N'-[6-(2,6-цихлорфеніл)-2(метилтіо)піридо[2,3-d]піримідин-7-іл]карбамід В 29,9г аміну, одержаного вище, у розчині у 300мл ДМФ вводять протягом 10 хвилин і підтримуючи температуру нижче 25°С, 4,6г 60%-ного NaH; перемішують ще протягом 20 хвилин, потім протягом 20 хвилин вводять 12,2мл ізоціанату терціобутилу, потім перемішують протягом ночі. Реакційне середовище повільно виливають на 800мл суміші вода/лід +100мл НСl 6N; осад, що утворився, фільтрують, промивають водою, віджимають, потім перемішують протягом 1 години у 300мл простого ефіру, потім фільтрують, промивають простим ефіром і сушать. Одержують тверду речовину бежевого кольору, F=195-196°С (розкл.), m=26,5г. 1.6 N-(трет-бутил)-N'-(2,6-дихлорфеніл)-2(метилсульфоніл)піридо[2,3-d]піримідин-7іл]карбамід В 21,95г карбаміду, одержаного вище, у розчині у 300мл хлороформу вводять протягом 25 хвилин і підтримуючи температуру нижче 25°С, 27г метахлорпербензойної кислоти (77%). Утворюється осад. Через 2 години реакційне середовище 11 розбавляють 1л дихлорметану і вводять Na2SO4, потім 14г Са(ОН)2. Після перемішування протягом 30 хвилин тверду речовину фільтрують, промивають дихлорметаном, потім фільтрат концентрують досуха. Осад обробляють 80мл простого ефіру у гарячому стані; охолоджують, потім білу тверду 92021 12 речовину фільтрують, промивають простим ефіром і сушать. F=138-140°C, m=20,5г. Сполуки наведеної нижче загальної формули (II) можна одержати також, як сполуку, описану в Одержанні 1: 13 Одержання сполук формули (III) Номери прикладів одержання відповідають номерам сполук з таблиці 2, наведеної нижче. Одержання 17 і 18 Комерційний продукт. Одержання 19 Одержано відповідно до J. Hetero. Chem. 1986, 23, 1645-1649 і виділено у вигляді хлоргідрату. Одержання 20 Одержано відповідно до J. Chem. Soc. 1928, 121. Одержання 21 21.1 В 1,12г етил-5-нітро-бензо[b]фуран-2карбоксилату у 50мл ТГФ вводять невеликими порціями 2,27г NaBH4 протягом 8 годин, потім перемішують протягом 40 годин. Додають 5мл метанолу, потім 5мл води. Реакційне середовище екстрагують за допомогою AcOEt, органічну фазу промивають водою, 5%-ним розчином KHSO4/K2SO4, водою, потім насиченим розчином NaCl. Сушать і концентрують при зниженому тиску і одержують 0,74г цільового продукту у твердій формі. 21.2 92021 14 730мг продукту, одержаного на стадії 21.1, розчиняють у 9мл DCM і витримують при 5°С. 1мл триетиламіну додають при 5°С, потім вводять протягом 15 хвилин 536мг метансульфонілхлориду. Підтримують температуру 5°С протягом 15 хвилин, потім реакційне середовище залишають на 55 хвилин до нагрівання до кімнатної температури. Потім реакційне середовище розбавляють DCM і водою. Органічну фазу декантують, промивають водою, насиченим розчином NaCl, сушать і випарюють при зниженому тиску. Одержують 0,98г масла, що містить суміш мезилату (цільовий продукт) і хлорид (продукт заміщення СН2ОН у положенні 2 бензо[b]фурану сполукою СН2Сl). 21.3 0,97г продукту, одержаного на стадії 21.2, у 10мл ДМФ обробляють за допомогою 1,05г діетиламіну протягом 18 годин. Реакційне середовище екстрагують за допомогою AcOEt, органічну фазу промивають водою, насиченим розчином NaCl, сушать, потім розчинники випарюють при зниженому тиску. Одержують 0,93г масла. 21.4 В 1,16г продукту, одержаного на стадії 21.3, у 40мл ТГФ вводять 4,48г порошкоподібного Zn, 15 потім при -5°С, 5мл оцтової кислоти протягом 25 хвилин. Через 1 годину 15 хв. від початку реакції твердий осад відфільтровують з реакційного середовища, тверду речовину промивають невеликою кількістю ТГФ, органічні фази збирають, розбавляють за допомогою AcOEt і води, потім доводять до рН=9 за допомогою NaOH 10N. Після декантації органічну фазу виділяють і промивають 15%-ним розчином Na2CO3, водою, насиченим розчином NaCl, сушать і випарюють. Одержують 900мг масла. Одержання 22 22.1 В 1,64г 2-хлорметил-5-нітробензоксазолу (одержаного відповідно до Synth. Communications 1989, 19, 2921-2924) у 25мл ДМФ вводять 1,26г азиду натрію і перемішують протягом ночі при кімнатній температурі. Реакційне середовище виливають у 150мл AcOEt і двічі промивають льодяною водою, потім насиченим розчином NaCl. Органічну фазу сушать і концентрують при зниженому тиску. Одержують 1,42г масла чорного кольору. 22.2 В 1,40г продукту, одержаного на стадії 22.1, у 30мл AcOEt вводять 2,84г трифенілфосфіну протягом 10 хвилин, потім через 10 хвилин 1,16мл води вводять протягом 2 хвилин. Після 24 годин перемішування при 60°С з подальшим охолодженням реакційне середовище розбавляють AcOEt, органічну фазу промивають водою, потім насиченим розчином NaCl. Органічну фазу сушать і концентрують при зниженому тиску. Осад обробляють в Et2O і двічі екстрагують за допомогою НСl 1N. Кислі фази збирають, вводять у контакт з AcOEt і доводять до рH=10 за допомогою NaOH 10N. Після декантації органічну фазу промивають водою, потім насиченим розчином NaCl. Органічну 92021 16 фазу сушать і концентрують при зниженому тиску для одержання 468мг цільового продукту у вигляді масла жовтого кольору. 22.3 Продукт, одержаний на стадії 22.2, розчиняють у 10мл DCM, потім вводять 0,4 еквіваленту триетиламіну, потім 1,1 еквіваленту ВОС2О. Через 5 годин реакційне середовище розбавляють СН2Сl2, потім послідовно промивають 5% розчином KHSO4/K2SO4, водою, потім насиченим розчином NaCl. Неочищений продукт сушать і випарюють при зниженому тиску для одержання 388мг цільового продукту. 22.4 Продукт, одержаний на стадії 19.3, кількісно відновлюють за допомогою Zn/AcOH методом, описаним у прикладі одержання 18.4. Одержання 23 23.1 Одержано відповідно до J. Hetero. Chem. 1973, 10, 755. 23.2 Відновлення продукту, одержаного на стадії 23.1 за допомогою Sn/HBr у воді відповідно до Chem. Abstr. 1950, 4474. Одержання 24 Одержано відповідно до J.Hetero. Chem. 1970, 7, 1019-1027. Одержання 25 Одержано відповідно до Boll. Sci. Fac. Chim. Ind. Bologna 1964, том 22, стор.33-37. Одержання 26 Одержано відповідно до методики, описаної у патенті WO 92/05164. Сполуки формули (III) охарактеризовані у наведеній нижче таблиці 2: 17 Номери сполук у прикладах відповідають номерам, наведеним у показаній нижче таблиці З, що ілюструє хімічні структури і фізичні властивості декількох сполук за винаходом. Якщо вони містять асиметричний вуглець, ці сполуки одержують у рацемічній формі. Приклад 1: (Сполука 1) N-[2-(2,1,3бензотіадіазол-5-іламіно)-6-(2,6дихлорфеніл)піридо[2,3-d]піримідин-7-іл]-N'-(1,1диметилетил)карбамід. У 3,32г (20ммоль) аміну з прикладу одержання 17 за таблицею 2 у 45мл ДМС вводять 3,21г (28,6ммоль) t-BuOK протягом 15 хвилин, потім вводять протягом 20 хвилин 7,71г (16,5ммоль) карбаміду з прикладу одержання 1 з таблиці 1. Через 2 години вводять 1г t-BuOK, потім ще через 2 години вводять 1г t-BuOK. Через 6 годин від початку реакції реакційне середовище розбавляють льодяною водою, потім екстрагують за допомогою AcOEt. Органічну фазу промивають двічі водою, один раз насиченим розчином NaCl, сушать, концентрують при зниженому тиску. Неочищений 92021 18 продукт обробляють у суміші Еt2О/гептан, осад фільтрують, потім піддають хроматографії на силікагелі, елююючи CHCl3/AcOEt 88/12 (об./об.). Одержують 5г цільового продукту. МН+=539. Приклад 2: (Сполука 2) N-[2-(2,1,3бензотіадіазол-4-іламіно)-6-(2,6дихлорфеніл)піридо[2,3-d]піримідин-7-іл]-N'-(1,1диметилетил)карбамід. Сполуку 2 одержують також, як сполуку 1, виходячи з аміну з прикладу одержання 18 за таблицею 2. Приклад 3: (Сполука 3) N-[6-(2,6дихлорфеніл)-2-[(1,3-дигідро-2,2-діоксидо-2,1бензизотіазол-5-іл)аміно]піридо[2,3-d]піримідин-7іл]-N'-(1,1-диметилетил)карбамід. Суміш 437мг аміну з прикладу одержання 19 за таблицею 2 у вигляді хлор гідрату і 750мг карбаміду з прикладу одержання 1 за таблицею 1 нагрівають у 15мл етанолу протягом 5 годин. Реакційне середовище випарюють досуха, потім обробляють у 50мл СНСl3 і 20мл насиченого розчину NaHCO3. Органічну фазу декантують, промивають 19 водою, потім насиченим розчином NaCl. Органічну фазу сушать і випарюють при зниженому тиску. Осад очищають флеш-хроматографією з градієнтом від 0 до 20% (об./об.) AcOEt у хлороформі. Одержують 275мг твердої речовини жовтого кольору. МН+: 572. Приклад 4: (Сполука 4) N-[6-(2,6-дихлорфетл)2-[(2-метил-6-бензоксазоліл)аміно]піридо[2,3d]піримідин-7-іл]-N'-(1,1-диметилетил)карбамід. 210мг аміну з прикладу одержання 20 за таблицею 2 і 562мг карбаміду з прикладу одержання 1 за таблицею 1 нагрівають протягом 8 годин до 45°С у 20мл етанолу, що містить 0,02мл концентрованої НСl. Після концентрування при зниженому тиску осад піддають хроматографії на силікагелі, елююючи СНСl3/МеOН:98/2 (об./об.). Одержують 300мг продукту у вигляді твердої речовини жовтого кольору. МН+: 536. Приклад 5: (Сполука 5) N-[6-(2,6дихлорфеніл)-2-[[2-[(діетиламіно)метил]-5бензофураніл]аміно]піридо[2,3-d]піримідин-7-іл]-N'(1,1-диметилетил)карбамід. Сполуку 5 одержують також як сполуку 4, виходячи з аміну 21.4 з прикладу одержання 21 за таблицею 2. Приклад 6: (Сполука 6) 1,1-диметилетил[[5-[[6(2,6-дихлорфеніл)-7-[[[(1,1диметилетил)аміно]карбоніл]аміно]піридо[2,3d]піримідин-2-іл]аміно]-2бензоксазоліл]метил]карбамат. Сполуку 6 одержують також як сполуку 4, виходячи з аміну 22.4 з прикладу одержання 22 за таблицею 2. Приклад 7: (Сполука 7) N-[2-[[2-(амінометил)-5бензоксазоліл]аміно]-6-(2,6дихлорфеніл)піридо[2,3-d]піримідин-7-іл]-N'-(1,1диметилетил)карбамід. 190мг сполуки 6 обробляють протягом 1 години 3мл ТГФ у 2мл DCM. Концентрують при зниженому тиску, осад обробляють у суміші DCM/вода, потім рН доводять до 9 шляхом додавання 15%ного розчину Na2CO3. Після декантації органічну фазу промивають водою, потім насиченим розчином NaCl, сушать, концентрують при зниженому тиску. Неочищений продукт обробляють шляхом флеш-хроматографії на силікагелі, елююючи від 0 до 10% (об./об.) метанолу у DCM. 100мг твердої білої речовини виділяють. МН+: 551. Приклад 8: (Сполука 8) N-[6-(2,6дихлорфеніл)-2-(імідазо[1,2-а]піридин-6іламіно)піридо[2,3-d]піримідин-7-іл]-N'-(1,1диметилетил)карбамід. Сполуку 8 одержують також як сполуку 4, виходячи з аміну 23.2 з прикладу одержання 23 за таблицею 2. Приклад 9: (Сполука 9) N-[6-(2,6дихлорфешл)-2-([1,2,4]триазол[1,5-а]піридин-6іламіно)піридо[2,3-d]тримідин-7-іл]-N'-(1,1диметилетил)карбамід. Сполуку 9 одержують також як сполуку 4 виходячи з аміну з прикладу одержання 24 за таблицею 2. Приклад 10: (Сполука 10) N-[2-(2,1,3бензоксадіазол-5-іламіно)-6-(2,6 92021 20 дихлорфеніл)піридо[2,3-d]піримідин-7-іл]-N'-(1,1диметилетил)карбамід. У суміш 0,468г продукту одержання 1 і 0,202г аміну (III) з прикладу одержання 25 за таблицею 2 у 6мл ДМСО, вводять 0,168г tBuOk протягом 25 хвилин, потім ще 0,168г протягом 1 години. Реакційне середовище перемішують протягом 2 годин, потім екстрагують етилацетатом, і послідовно промивають водою і насиченим розчином NaCl. Після сушіння над Na2SO4 і випарювання етилацетату, неочищений продукт обробляють шляхом флеш-хроматографії на силікагелі, елююючи з градієнтом від 0 до 8% (об./об.) етилацетату у дихлорметані. Одержують порошок білого кольору, m=0,22г. МН+=523. Приклад 11: (Сполука 11) N-[2-(1,3-дигідро-2,2діоксидо-2,1,3-бензотіадіазол-5-іламіно)-6-(2,6дихлорфеніл)піридо[2,3-d]піримідин-7-іл]-N'-(1,1диметилетил)карбамід. Сполуку 11 одержують також як сполуку 4, виходячи з аміну з прикладу одержання 26 за таблицею 2. Приклади 12-21 (Сполуки 12-21) Сполуки 12-21 одержують також як сполуку 1, виходячи з аміну (III) з прикладу одержання 17 за таблицею 2 і відповідного карбамату, вибраного з продуктів формули (II) з прикладів одержання за таблицею 1. Приклад 12: (Сполука 12) N-[2-(2,1,3бензотіадіазол-5-іламіно)-6-(2-бром-6хлорфеніл)піридо[2,3-d]піримідин-7-іл]-N'-(1,1диметилетил)карбамід. Приклад 13: (Сполука 13) N-[2-(2,1,3бензотіадіазол-5-іламіно)-6-(2,6дихлорфеніл)піридо[2,3-е]піримідин-7-іл]-N'етилкарбамід. Приклад 14: (Сполука 14) N-[-[2-(2,1,3бензотіадіазол-5-іламіно)-6-(2,6дибромфеніл)піридо[2,3-d]піримідин-7-іл]-N'-(1,1диметилетил)карбамід. Приклад 15: (Сполука 15) N-[2-(2,1,3бензотіадіазол-5-іламіно)-6-(2,6дибромфеніл)піридо[2,3-d]піримідин-7-іл]-N'етилкарбамід. Приклад 16: (Сполука 16) N-[2-(2,1,3бензотіадіазол-5-іламіно)-6-(2,6дихлорфеніл)піридо[2,3-d]піримідин-7-іл]-N'фенілкарбамід. Приклад 17: (Сполука 17) N-[2-(2,1,3бензотіадіазол-5-іламіно)-6-(3,5диметоксифеніл)піридо[2,3-d]піримідин-7-іл]-N'(1,1-диметилетил)карбамід. Приклад 18: (Сполука 18) N-[2-(2,1,3бензотіадіазол-5-іламіно)-6-фенілпіридо[2,3d]піримідин-7-іл]-N'-(1,1-диметилетил)карбамід. Приклад 19: (Сполука 19) N-[2-(2,1,3бензотіадіазол-5-іламіно)-6-(2,6диметилфеніл)піридо[2,3-d]піримідин-7-іл]-N'-(1Ддиметилетил)карбамід. Приклад 20: (Сполука 20) N-[2-(2,1,3бензотіадіазол-5-іламіно)-6-(2,6дифторфеніл)піридо[2,3-d]піримідин-7-іл]-N'-(1,1диметилетил)карбамід. Приклад 21: (Сполука 21) N-[2-(2,1,3бензотіадіазол-5-іламіно)-6-(2,6 21 дихлорфеніл)піридо[2,3-d]піримідин-7-іл]-N'-(1метилетил)карбамід. Наведені нижче таблиці 3 і 4 ілюструють хімічні структури і фізичні властивості декількох прик 92021 22 ладів за винаходом. У цих таблицях Me, Et, iPr і tBu означають відповідно метил, етил, ізопропіл і третбутил, а Вос (або ВОС) означає третбутоксикарбоніл. 23 92021 24 25 Сполуки за винаходом були об'єктом фармакологічних досліджень, що дозволяють визначити протиракову активність. Сполуки формули (І) за даним винаходом тестували in vitro на панелі ліній людських пухлинних клітин: Раку грудей: MDA-MB231 (American Type culture collection, Rockville, Maryland, USA, ATCCHTB26), MDA-A1 або MDA-ADR (яку називають лінією multi-drug resistant MDR і вона описана E.Collomb et al., у Cytometry, 12 (1): 15-25, 1991) і MCF7 (ATCC-HTB22); Раку простати: DU145 (ATCC-HTB81) і РСЗ (ATCC-CRL1435) Раку ободової кишки: НТС116 (ATCC-CCL247) і НСТ15 (ATCC-CCL225) Раку легенів: Н460 (описана Carmichael у Cancer Research 47 (4): 936-942, 1987, видається National Cancer Institute, Frederick Cancer Research and Development Center, Frederick, Maryland, USA), Гліобластоми: SF268 (описана Westphal у Biochemical & Biophysical Research Communications 132 (1): 284-289, 1985, видається National Cancer Institute, Frederick Cancer Research and Development Center, Frederick, Maryland, USA), Лейкемії: CMLT1 (описана Kuriyama et al., у Blood, 74: 1989, 1381-1387, Soda et al., у British Journal of Haematology, 59; 1985, 671-679 і Drexler у Leukemia Research, 18: 1994, 919-927 і видається фірмою DSMZ (Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH) Mascheroder Weg lb, 38124 Braunschweig, Germany), K-562 (описана Lozzio et al., J Natl Cancer Inst 50: 535 (1973), Lozzio et al., Blood 45: 321 (1975), видасться DSMZ n ACC 10), KG-la (описана Koeffler et al. Blood 56: 265 (1980), видається DSMZ n ACC421) і Kasumi-1 (описана Asou et al., Blood 77: 2031 (1991,) видається DSMZ n ACC 220). 92021 26 Клітинну проліферацію і життєздатність визначали тестом з використанням 3-(4,5диметилтіазол-2-іл)-5-(3-карбоксиметоксифеніл)-2(4-сульфофеніл)-2Н-тетразолію (MTS) за методом Fujishita Т. et al., Oncology, 2003, 64(4), 399-406. У цьому тесті вимірюють мітохондріальну здатність живих клітин трансформувати MTS у забарвлену сполуку після 72 годин інкубування сполуки формули (І) за винаходом. Концентрації сполуки за винаходом, які приводять до 50%-ної втрати проліферації клітин і життєздатності (ІС50) становлять від 1нМ до 10мкм в залежності від лінії пухлинних клітин і сполуки, що тестується. Наприклад, сполука пі приводить до ІС50 при 40нМ лінії К-562, ІС50 при 50нМ лінії KG-1a і ІС50 при 40нМ лінії Kasumi-1. Сполука n5 приводить до ІС50 при 5нМ, сполука п9 приводить до ІС50 при 19нМ, сполука n9 приводить до ІС50 при 74нМ лінії К-562. Сполука n7 приводить до ІС50 при 43нМ лінії SF268. Таким чином, відповідно до винаходу, виявилося, що сполуки формули (І) викликають зниження проліферації і життєздатності пухлинних клітин. Таким чином, виявилося, що сполуки за винаходом володіють протираковою активністю і активністю у лікуванні інших проліферативних захворювань, таких як псоріаз, рестеноз, артеріосклероз, СНІД, наприклад, а також захворювань, викликаних проліферацією клітин гладких судинних м'язів і ревматоїдного поліартриту. Таким чином, відповідно до іншого з аспектів, об'єктом винаходу є лікарські засоби, які містять сполуку формули (І) або сіль приєднання останньої з фармацевтично прийнятною кислотою або гідрат або сольват сполуки формули (І). Ці лікарські засоби використовуються у терапії, зокрема, у лікуванні або профілактиці захворювань, викликаних або загострених проліферацією клітин і, зокрема, пухлинних клітин. Продукт за винаходом можна використовувати для одержання 27 лікарського засобу, придатного для лікування патологічного стану, зокрема, раку. Як інгібітор проліферації пухлинних клітин ці сполуки придатні для профілактики і лікування лейкемій, твердих пухлин, як первинних, так і метастатичних, карцином і раку, зокрема: раку грудей; раку легенів; раку тонкої кишки, раку ободової кишки і прямої кишки; раку дихальних шляхів, ротоглотки і нижнього відділу глотки, раку стравоходу, раку печінки, раку шлунку, раку жовчних проток, раку жовчного міхура, раку підшлункової залози; раку сечовивідних шляхів, включаючи нирки, уротелій і сечовий міхур; раку жіночої статевої системи, включаючи рак матки, шийки матки, яєчників, хоріокарциному і трофобластому; раку чоловічої статевої системи, включаючи рак простати, сім'яних пухирців, яєчок, пухлин зародкових клітин; раку ендокринних залоз, включаючи рак щитовидної залози, гіпофізу, надниркових залоз; раку шкіри, включаючи гемангіоми, меланоми, саркоми, включаючи саркому Капоші; пухлин мозку, нервів, очей, оболонки головного мозку, включаючи астроцитоми, гліоми, гліобластоми, ретинобластоми, нейриноми, нейробластоми, невриноми, менінгіоми; злоякісні гемопоетичні пухлини; лейкемії (Acute Lymphocytic Leukemia (ALL), Acute Myeloid Leukemia (AML), Chronic Myeloid Leukemia (CML), Chronic lymphocytic leukemia (CLL)), хлороми, плазмоцитоми, лейкемії клітин Т або В, лімфоми неходжкінські або ходжкінські, мієломи, різні злоякісні хвороби крові. Відповідно до іншого зі своїх аспектів даний винахід стосується фармацевтичних композицій, що містять як активну речовину сполуку за винаходом. Ці фармацевтичні композиції містять ефективну дозу щонайменше однієї сполуки за винаходом або фармацевтично прийнятну сіль, гідрат або сольват зазначеної сполуки, а також щонайменше один фармацевтично прийнятний ексципієнт. Фармацевтична композиція може також додатково містити іншу активну протиракову сполуку. Зазначені ексципієнти вибирають в залежності від фармацевтичної форми і необхідного способу введення з традиційних ексципієнтів, відомих фахівцеві. У фармацевтичних композиціях за винаходом для введення перорального, сублінгвального, підшкірного, внутрішньом'язового, внутрішньовенного, місцевого, локального, інтратрахеального, через ніс, черезшкірного або ректального активну речовину зазначеної вище формули (І) або можливо її сіль, сольват або гідрат можна вводити у вигляді разової форми введення у суміші з традиційними фармацевтичними ексципієнтами тваринам і людям для профілактики або лікування порушень або захворювань, зазначених вище. До відповідних разових форм введення належать пероральні форми, такі як таблетки, м'які або тверді желатинові капсули, порошки, гранули і розчини або суспензії для перорального введення, форми для введення сублінгвального, орального, інтратрахеального, через очі, через ніс, шляхом інгаляції, форми введення місцевого, черезшкірного, підшкірного, внутрішньом'язового або внутрішньовенного, форми ректального введення або 92021 28 імплантати. Для місцевого застосування можна використовувати сполуки за винаходом у кремах, гелях, мазях або лосьйонах. Як приклад стандартна лікарська форма сполуки за винаходом у формі таблетки може містити наступні компоненти: Сполуку за винаходом - 50,0мг; Маніт - 223,75мг; Натрієву кроскармелозу - 6,0мг; Кукурудзяний крохмаль - 15,0мг; Гідроксипропілметилцелюлозу - 2,25мг; Стеарат магнію - 3,0мг. Сполуки формули (І), зазначені вище, можна використовувати у добових дозах від 0,002 до 2000мг на кг маси тіла ссавця, який підлягає лікуванню, переважно добова доза становить від 0,1 до 300мг/кг. Доза, яку вводять людині, може варіювати переважно від 0,02 до 10000мг на добу, більш конкретно від 1 до 3000мг в залежності від віку пацієнта або мети прийому: для профілактики або лікування. Існують окремі випадки, коли дози повинні бути збільшені або зменшені; такі дози не виходять за межі винаходу. Відповідно до традиційної практики дозування для кожного пацієнта підбирає лікар в залежності від способу введення, маси тіла або індивідуальної реакції пацієнта. Даний винахід відповідно до іншого свого аспекту стосується також способу лікування патологій, зазначених вище, що включає в себе введення пацієнту ефективної дози сполуки за винаходом або однієї з її фармацевтично прийнятних солей або гідратів, або сольватів. Відповідно до даного винаходу одну або декілька сполук формули (І) можна вводити у комбінації з однією або декількома протираковими активними речовинами, зокрема, такими протипухлинними сполуками, як алкілувальні агенти, такі як алкілсульфонати (бусульфан), дакарбазин, прокарбазин, азотвмісні гірчиці (хлорметин, мелфалан, хлорамбуцил), циклофосфамід, ізосфамід, сполуки нітросечовини, такі як кармустин, ломустин, семустин, стрептозоцин; протипухлинні алкалоїди, такі як вінкристин, вінбластин; таксани, такі як паклітаксел або таксотер; протипухлинні антибіотики, такі як актиноміцин; речовини, що утворюють сполуки проникнення; протиухлинні антиметаболіти, антагоністи фолатів, метотрексат, інгібітори синтезу пуринів; аналоги пурину, такі як меркаптопурин, 6-тіогуанін; інгібітори синтезу піримідинів, інгібітори ароматази, капецитабін, аналоги піримідину, такі як фторурацил, гемцитабін, цитарабін і цитозин арабінозид; брекінар; інгібітори топоізомераз, такі як камтотецин або етопозид; гормональні протиракові агоністи і антагоністи, включаючи тамоксифен; інгібітори кінази, імтиніб; інгібітори факторів росту; протизапальні, такі як пентозан полісульфат, кортикостероїди, преднізон, дексаметазон; антитопоізомерази, такі як етопозид, антрацикліни, включаючи доксорубіцин, блеоміцин, мітоміцин і метраміцин; протиракові металеві комплекси, комплекси платини, цисплатин, карбоплатин, оксоліплатин; інтерферон альфа, трифенілтіофосфорамід, алтретамін; антиангіо 29 92021 генні агенти; талідомід; імунотерапевтичні домішки; вакцини. Відповідно до даного винаходу сполуки формули (І) можна також вводити у комбінації з однією або декількома іншими активними речовинами, придатними відносно однієї із зазначених патоло Комп’ютерна верстка Т. Чепелева 30 гій, наприклад, протиблювотним, знеболюючим, протизапальним засобом, засобом від схуднення. Можна також поєднувати застосування сполук за даним винаходом з променевою терапією. Ці види лікування можуть використовуватися одночасно, окремо, послідовно. Лікування призначається лікарем в залежності від захворювання. Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюDerivatives of pyrido[2,3-d]pyrimidine, the preparation thereof, and the therapeutic application of the same
Автори англійськоюBourrie Bernard, Casellas Pierre, Gegam Samir, Muneaux Claude, Perreaut Pierre
Назва патенту російськоюПроизводные пиридо[2,3-d]пиримидина, их получение, их применение в терапии
Автори російськоюБурри Бернар, Казелла Пьер, Жегам Самир, Мюно Клод, Перро Пьер
МПК / Мітки
МПК: C07D 471/04, A61P 35/00, A61K 31/519
Мітки: похідні, застосування, терапії, одержання, піридо[2,3-d]піримідину
Код посилання
<a href="https://ua.patents.su/15-92021-pokhidni-pirido23-dpirimidinu-kh-oderzhannya-kh-zastosuvannya-u-terapi.html" target="_blank" rel="follow" title="База патентів України">Похідні піридо[2,3-d]піримідину, їх одержання, їх застосування у терапії</a>