Похідні ненасиченої жирної оксикислоти та їх дермакосметологічне застосування
Формула / Реферат
1. Похідна ненасиченої жирної гідроксикислоти, що відповідає загальній формулі (І):
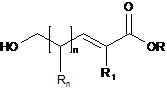 , (І)
, (І)
у якій:
Rn незалежно позначає Н або лінійну чи розгалужену алкільну групу, що містить від 1 до 6 атомів вуглецю, яка може бути заміщена атомом галогену, зокрема атомом фтору;
R1 позначає Н, F, Сl, Вr або CF3;
R позначає Н або лінійну чи розгалужену алкільну групу, що містить від 1 до 6 атомів вуглецю, яка може бути заміщена атомом галогену, зокрема атомом фтору, і 3£n£14, за винятком таких сполук:
етил-7-гідрокси-2-(Е)-гептеноат,
метил-8-гідрокси-2-(Е)-октеноат,
метил-8-гідрокси-7-метил-2-(Е)-октеноат,
метил-8-гідрокси-5-метил-2-(Е)-октеноат,
метил-8-гідрокси-6-метил-2-(Е)-октеноат,
метил-8-гідрокси-6-трет-бутил-2-(Е)-октеноат,
трет-бутил-8-гідрокси-6-трет-бутил-2-(Е)-октеноат та
трет-бутил-8-гідрокси-6-трет-бутил-2-(Z)-октеноат.
2. Похідна за п. 1, де R позначає Н;
R1, Rn і n мають значення, вказані в п. 1;
за умови, що, якщо n≠10, то щонайменше один з радикалів R1 і Rn не є воднем.
3. Похідна за п. 1, де
R1 позначає F, Сl, Вr або CF3;
R, Rn і n мають значення, вказані в п. 1.
4. Похідна за п. 1, де
R, R1 і Rn мають значення, вказані в п.1, і 6≤n≤14;
за умови, що, якщо n≠10, то щонайменше один з радикалів R1 і Rn не є воднем.
5. Похідна за п. 1, де
R1 позначає F, Сl, Вr або CF3;
Rn=Н.
6. Похідна за п. 1, де
R1 позначає F, Сl, Вr або CF3; і
щонайменше один з радикалів Rn позначає лінійну чи розгалужену алкільну групу, що містить від 1 до 6 атомів вуглецю, яка може бути заміщена атомом галогену, зокрема атомом фтору.
7. Похідна за п. 1 або 3, де
R1=F,
Rn=H.
8. Похідна за п. 7, де
R1=F,
Rn=H,
n=13.
9. Похідна за п. 3, де
R1=F,
Rn=H,
n=6.
10. Похідна за п. 1 або 2, де
R=R1=H,
тільки один з радикалів Rn позначає метильну групу, а інші є атомами водню, і
n=4.
11. Похідна за п. 1, де
R1=Rn=H, i
n=10.
12. Похідна за п. 3, де
R1=F,
Rn=H,
n=10.
13. Похідна за п. 3, де
R1=F,
Rn=H,
n=8.
14. Дерматокосметологічна композиція, що містить похідну ненасиченої жирної гідроксикислоти загальної формули (І), охарактеризовану в будь-якому з пп. 1-13, та дерматологічно прийнятний наповнювач.
15. Застосування похідної ненасиченої жирної гідроксикислоти загальної формули (І), охарактеризованої в будь-якому з пп. 1-13 для виготовлення дерматокосметологічної композиції, що має антирадикальну, протизапальну, протисвербіжну активність, призначеної для використання в лікуванні розладів, пов'язаних з кератинізацією і пігментацією та/або для прискорення загоєння.
16. Застосування за п. 15, де вищевказана композиція призначена для лікування псоріазу, сверблячки та/або атопічного дерматиту.
17. Застосування за п. 15, де вищевказана композиція призначена для лікування старіння шкіри та білих або коричневих вікових плям.
18. Застосування за п. 15, де вищевказана композиція призначена для відбілювання шкіри.
Текст
1. Похідна ненасиченої жирної гідроксикислоти, що відповідає загальній формулі (І): O OR n (13) 96429 , (І) у якій: Rn незалежно позначає Н або лінійну чи розгалужену алкільну групу, що містить від 1 до 6 атомів вуглецю, яка може бути заміщена атомом галогену, зокрема атомом фтору; R1 позначає Н, F, Сl, Вr або CF3; R позначає Н або лінійну чи розгалужену алкільну групу, що містить від 1 до 6 атомів вуглецю, яка може бути заміщена атомом галогену, зокрема атомом фтору, і 3n14, за винятком таких сполук: етил-7-гідрокси-2-(Е)-гептеноат, метил-8-гідрокси-2-(Е)-октеноат, метил-8-гідрокси-7-метил-2-(Е)-октеноат, метил-8-гідрокси-5-метил-2-(Е)-октеноат, метил-8-гідрокси-6-метил-2-(Е)-октеноат, метил-8-гідрокси-6-трет-бутил-2-(Е)-октеноат, трет-бутил-8-гідрокси-6-трет-бутил-2-(Е)-октеноат та трет-бутил-8-гідрокси-6-трет-бутил-2-(Z)-октеноат. 2. Похідна за п. 1, де R позначає Н; R1, Rn і n мають значення, вказані в п. 1; за умови, що, якщо n≠10, то щонайменше один з радикалів R1 і Rn не є воднем. 3. Похідна за п. 1, де R1 позначає F, Сl, Вr або CF3; R, Rn і n мають значення, вказані в п. 1. 4. Похідна за п. 1, де R, R1 і Rn мають значення, вказані в п.1, і 6≤n≤14; C2 R1 (11) Rn UA HO (19) (21) a200806451 (22) 20.10.2006 (24) 10.11.2011 (86) PCT/EP2006/067641, 20.10.2006 (31) 0510792 (32) 21.10.2005 (33) FR (46) 10.11.2011, Бюл.№ 21, 2011 р. (72) ШАРВЕРОН МАРІ, FR, ТАРРУ РОЖЕ, FR, БОРДА ПАСКАЛЬ, FR (73) ПЬЄР ФАБР ДЕРМО-КОСМЕТІК, FR (56) HANESSIAN, STEPHEN ET AL: "Synthesis of carbocycles from .omega.-substituted .alpha.,.beta.unsaturated esters via radical -induced cyclizations" CANADIAN JOURNAL OF CHEMISTRY , 65(8), 1859-66 CODEN: CJCHAG; ISSN: 0008-4042, 1987, XP002376764 GUINDON, Y. ET AL: "Stereoselective Hydrogen Transfer Reactions Involving Acyclic Radicals . Tandem Substituted Tetrahydrofuran Formation and Stereoselective Reduction: Synthesis of the C17-C22 Subunit of Ionomycin" JOURNAL OF ORGANIC CHEMISTRY , 59(5), 1166-78 CODEN: JOCEAH; ISSN: 0022-3263, 1994, XP002376741 EP 0632008 A (ONO PHARMACEUTICAL CO., LTD) 04.01.1995 NISHITANI, KIYOSHI ET AL: "Studies on the terpenoids and related alicyclic compounds. XXXIX. A synthesis of .alpha.-methylene-.gamma.-lactones fused to medium and large rings by intramolecular cyclization of formylated allyl halides" CHEMICAL & PHARMACEUTICAL BULLETIN , 38(1), 28-35 CODEN: CPBTAL; ISSN: 0009-2363, 1990, XP002376742 BROWN, RICHARD T. ET AL: "Synthesis of methyl secolonitoside" JOURNAL OF THE CHEMICAL SOCIETY, PERKIN TRANSACTIONS 1: ORGANIC AND BIO-ORGANIC CHEMISTRY , (11), 1633-1637 CODEN: JCPRB4; ISSN: 0300-922X, 1997, XP002376743 BARTLETT, PAUL A. ET AL: "A stereoselective total synthesis of the Prelog-Djerassi lactone" JOURNAL 2 3 96429 4 за умови, що, якщо n≠10, то щонайменше один з 12. Похідна за п. 3, де радикалів R1 і Rn не є воднем. R1=F, 5. Похідна за п. 1, де Rn=H, R1 позначає F, Сl, Вr або CF3; n=10. Rn=Н. 13. Похідна за п. 3, де 6. Похідна за п. 1, де R1=F, R1 позначає F, Сl, Вr або CF3; і Rn=H, щонайменше один з радикалів Rn позначає лінійну n=8. чи розгалужену алкільну групу, що містить від 1 до 14. Дерматокосметологічна композиція, що містить 6 атомів вуглецю, яка може бути заміщена атомом похідну ненасиченої жирної гідроксикислоти загагалогену, зокрема атомом фтору. льної формули (І), охарактеризовану в будь-якому 7. Похідна за п. 1 або 3, де з пп. 1-13, та дерматологічно прийнятний наповR1=F, нювач. Rn=H. 15. Застосування похідної ненасиченої жирної гід8. Похідна за п. 7, де роксикислоти загальної формули (І), охарактериR1=F, зованої в будь-якому з пп. 1-13 для виготовлення Rn=H, дерматокосметологічної композиції, що має антиn=13. радикальну, протизапальну, протисвербіжну акти9. Похідна за п. 3, де вність, призначеної для використання в лікуванні R1=F, розладів, пов'язаних з кератинізацією і пігментаціRn=H, єю та/або для прискорення загоєння. n=6. 16. Застосування за п. 15, де вищевказана компо10. Похідна за п. 1 або 2, де зиція призначена для лікування псоріазу, свербляR=R1=H, чки та/або атопічного дерматиту. тільки один з радикалів Rn позначає метильну гру17. Застосування за п. 15, де вищевказана компопу, а інші є атомами водню, і зиція призначена для лікування старіння шкіри та n=4. білих або коричневих вікових плям. 11. Похідна за п. 1, де 18. Застосування за п. 15, де вищевказана компоR1=Rn=H, i зиція призначена для відбілювання шкіри. n=10. Предметом даного винаходу є нові похідні ненасичених жирних оксикислот та їх застосування в дерматокосметології. Численні ненасичені жирні оксикислоти добре відомі та описані в літературі завдяки їх біологічним властивостям і, зокрема, завдяки їх косметичним і фармакологічним властивостям. Наприклад, основним ліпідним компонентом маточного молочка бджіл є ненасичена жирна оксикислота, а саме гідрокси-10-2(транс)деценова кислота (Edward Ε. Smissman et al., 1964. JOU. 29, 3517-3520). В різних документах сучасного рівня техніки описані способи одержання ненасичених жирних оксикислот та їхніх складних ефірів (Lee et al., 1993, J. Org. Chem., vol. 58, pages 2918-2919; Hurd et Saunders, 1952, J. Am. Chem. Soc, vol. 74, pages 5324-5328; Krishnamurthy et al., 1989, Indian J. Chem. Sect. A, vol. 28, pages 288-291; Plettener et al., 1995, J. Chem. Ecol., vol. 21, pages 1017-1030). Більш конкретно, даний винахід стосується похідних ненасичених жирних оксикислот, що відповідають загальній формулі (І): у якій: - Rn незалежно позначає Η або лінійну чи розгалужену алкильну групу, що містить від 1 до 6 атомів вуглецю, яка може бути заміщена атомом галогену, зокрема, атомом фтору; - R1 позначає Н, F, СІ, Br або CF3; - R позначає Η або лінійну чи розгалужену алкильну групу, що містить від 1 до 6 атомів вуглецю, яка може бути заміщена атомом галогену, зокрема, атомом фтору, і - 3n14. Відповідно до одніє з особливих ознак винаходу похідні ненасичених жирних оксикислот із загальною формулою (І) відповідають таким критеріям: - R позначає Н, - Rn незалежно позначає Η або лінійну чи розгалужену алкильну групу, що містить від 1 до 6 атомів вуглецю, і яка може бути заміщена атомом галогену, зокрема, атомом фтору; - R1 позначає Н, F, СІ, Br або CF3; - 3n14; за умови, однак, що, якщо n10, щонайменше один з радикалів R1 і Rn не є воднем. Відповідно до наступної особливої ознаки винаходу похідні ненасичених жирних оксикислот із загальною формулою (І) відповідають таким критеріям: - R1 позначає F, СІ, Br або CF3; - Rn незалежно позначає Η або лінійну чи розгалужену алкильну групу, що містить від 1 до 6 атомів вуглецю, яка може бути заміщена атомом галогену, зокрема, атомом фтору; - R позначає Η або лінійну чи розгалужену алкильну групу, що містить від 1 до 6 атомів вуглецю, яка може бути заміщена атомом галогену, зокрема, атомом фтору, і 5 96429 6 загальною формулою (І) відповідають таким кри- 3n14. теріям: Відповідно до наступної особливої ознаки ви- R1=Rn=Η; і находу похідні ненасичених жирних оксикислот із - n=10. загальною формулою (І) відповідають таким криВідповідно до наступної особливої ознаки витеріям: находу похідні ненасичених жирних оксикислот із - Rn незалежно позначає Η або лінійну чи роззагальною формулою (І) відповідають таким кригалужену алкильну групу, що містить від 1 до 6 теріям: атомів вуглецю, яка може бути заміщена атомом - R1=F; галогену, зокрема, атомом фтору; - Rn=Η; і - R1 позначає Н, F, СІ, Br або CF3; - n=10. - R позначає Η або лінійну чи розгалужену алВідповідно до наступної особливої ознаки викильну групу, що містить від 1 до 6 атомів вуглецю, находу похідні ненасичених жирних оксикислот із яка може бути заміщена атомом галогену, зокрезагальною формулою (І) відповідають таким крима, атомом фтору, і теріям: - 3n14. - R1=F; за умови, однак, що, якщо n10, щонайменше - Rn=Η; і один з радикалів R1 і Rn не є воднем. - n=8. Відповідно до наступної особливої ознаки виЗгідно з даним винаходом, похідні ненасиченаходу похідні ненасичених жирних оксикислот із них жирних оксикислот із загальною формулою (І), загальною формулою (І) відповідають таким кривизначеною вище, можуть бути використані як теріям: активні інгредієнти в сполученні з придатним на- R1 = F, СІ, Br або CF3; повнювачем для одержання дерматокосметологі- Rn=Η; і чних композицій з антирадикальною, протизапаль- 3n14. ною, протисвербіжною активністю, та/або для Відповідно до наступної особливої ознаки вивикористання в лікуванні розладів, пов'язаних з находу похідні ненасичених жирних оксикислот із кератинізацією та пігментацією, та/або для присзагальною формулою (І) відповідають таким крикорення загоєння. теріям: Похідні ненасичених жирних оксикислот із за- R1 позначає F, СІ, Br або CF3; гальною формулою (І) особливо придатні для ви- щонайменше один з радикалів Rn позначає користання в композиціях, призначених для лікулінійну чи розгалужену алкильну групу, що містить вання псоріазу, сверблячки та/або атопічного від 1 до 6 атомів вуглецю, яка може бути заміщена дерматиту, а також для лікування старіння шкіри атомом галогену, зокрема, атомом фтору, і та білих або коричневих вікових плям. - 3n14. Згідно з даним винаходом, похідні ненасичеВідповідно до наступної особливої ознаки виних жирних оксикислот із загальною формулою (І) находу похідні ненасичених жирних оксикислот із особливо придатні для використання в композицізагальною формулою (І) відповідають таким криях, призначених для відбілювання шкіри. теріям: Завдяки їхній антирадикальній активності по- R1=F; хідні ненасичених жирних оксикислот із загальною - Rn=Η; і формулою (І) також придатні для запобігання або - 3n14. обмеження ранніх стадій фотоканцерогенезу шкіВідповідно до наступної особливої ознаки вири, і тому їх можна використовувати для профілакнаходу похідні ненасичених жирних оксикислот із тики та лікування різних пухлинних захворювань загальною формулою (І) відповідають таким кришкіри. теріям: Похідні ненасичених жирних оксикислот із за- R1=F; гальною формулою (І) можна одержати: - Rn=Η; і - шляхом проведення реакції Віттіга-Хорнера, - n=13. а саме - реакції фосфонату формули (III): Відповідно до наступної особливої ознаки винаходу похідні ненасичених жирних оксикислот із загальною формулою (І) відповідають таким критеріям: - R1=F; - Rn=Η; і - n=6. Відповідно до наступної особливої ознаки винаходу похідні ненасичених жирних оксикислот із загальною формулою (І) відповідають таким критеріям: - R=R1=H; - один з радикалів Rn позначає метильну групу, а інші є атомами водню; і - n=4. Відповідно до наступної особливої ознаки винаходу похідні ненасичених жирних оксикислот із у якій: - R1 є таким, як визначено вище у формулі (І); - R2 позначає алкильну групу, лінійну чи розгалужену, що містить від 1 до 6 атомів вуглецю, яка краще є етильною або метильною групою, причому групи R2 можуть утворювати цикл із атомами кисню груп OR2 та із сусіднім атомом фосфору; і - R4 позначає алкильну групу, лінійну чи розгалужену, що містить від 1 до 6 атомів вуглецю, і краще є етильною групою; 7 96429 8 1 - або, якщо R1=Η, за допомогою реакції ДебН ЯМР (300 МГц, CDCI3): 1,42-1,49 (m, 4H), нера-Кневенагеля, а саме -реакції похідного мало1,65-1,75 (m, 6H), 2,30 (t, J=5,4 Гц, 2H), 4,30 (t, нової кислоти формули R4OOC-CH2COOR, де R є J=5,7 Гц, 2Н). таким, як визначено вище у формулі (І), з лакто2. Стадія часткового відновлення до лактолу лом формули (II): 26,6 г (187,2 ммоль) лактону розводять в 210 мл толуолу в атмосфері азоту. Середовище охолоджують до -78°С і додають по краплях 156,4 мл (189,1 ммоль) діізобутилалюмінію гідриди (Dibal-H) у вигляді розчину в толуолі з концентрацією 20%, підтримуючи температуру, рівну -78°C. Суміш перемішують протягом 2 годин при -78°C. При -78°C додають 200 мл насиченого розчину солі Розена. Після 18 годин енергійного перемішування при кімнатній температурі двофазну суміш фільтрують де Rn і n є такими ж, як визначено вище, через целіт, потім екстрагують етилацетатом. Орз одержанням складного гідроксіефіру формуганічні фази промивають насиченим розчином ли (IV): NaCI, сушать над MgSO4, фільтрують і концентрують під вакуумом з одержанням 26 г неочищеного продукту (25% якого є діольним похідним, тобто вихід складає приблизно 72%). Тому лактол, у якому врівноважені відкрита та циклічна форми, використовується без додаткового очищення. Визначення характеристик: ТСХ : Rf=0,4 (гептан/етилацетат 6/4) у якій n, R і R1 є такими ж, як визначено вище, 1 Н ЯМР (300 МГц, CDCI3): 1,34-1,68 (m, 10Н), і, можливо, якщо R позначає групу R4, визна2,45 (t, J=5,4 Гц, 2H), 3,66 (t, J=6,6 Гц, 2Н), 9,78 (t, чену вище, реакції сапоніфікації складного гідрокJ=1,8 Гц, 1Н). сіефіру формули (IV), з одержанням відповідного 3. Стадія 3: Реакція Віттіга-Хорнера похідного оксикислоти формули (І). 19 г (131,8 ммоль) лактолу розчиняють в 250 Даний винахід буде проілюстрований прикламл етанолу. До середовища додають 31,4 мл дами синтезу, наведеними нижче. (158,1 ммоль) триетилфосфонацетату в присутноПриклад 1 сті 27,3 г (197,5 ммоль) карбонату калію. Реакційне Процедура синтезу DHA (деценової оксикиссередовище нагрівають до 40°C протягом 18 голоти) дин. При кімнатній температурі реакційне середо1. Стадія 1: Одержання оксонан-2-ону вище гідролізують 200 мл дистильованої води та 43,5 г (345 ммоль) циклооктанону розчиняють екстрагують етилацетатом. Органічні фази промив 430 мл дихлоретану. Потім до розчину додають вають насиченим розчином NaCI, сушать над 170 г (985 ммоль) мета-хлорпербензойної кислоти. MgSO4, фільтрують і концентрують під вакуумом з Це середовище нагрівають до 80°C протягом 48 одержанням 20 г неочищеного продукту. годин. При кімнатній температурі додають 400 мл Отриманий складний ефір очищають за допонасиченого розчину Na2S2O5 і NaHCO3 (1/1; могою хроматографії з елююванням сумішшю гепоб./об.). Середовище енергійно перемішують протану/етилацетату в співвідношенні 7/3; одержують тягом 18 годин. Органічну фазу відокремлюють і 15 г продукту (вихід 53%). обробляють KІ та Н2О протягом 6 годин. Органічну Отриманий складний ефір є сполукою формуфазу відокремлюють і промивають насиченим роли: зчином ЫагЭгОз, насиченим розчином NaCI, потім сушать над MgSO4, фільтрують і концентрують під вакуумом з одержанням 36 г неочищеного продукту. Лактон очищають за допомогою концентрування в пентані (60 мол), потім - за допомогою фільтрації осаду мета-хлорбензойної кислоти, вихід - 26,6 г (54%). Отриманий лактон є сполукою формули: Визначення характеристик: ТСХ (тонкошарова хроматографія): Rf=0,3 (гептан/етилацетат 7/3) Визначення характеристик: ТСХ: Rf=0,4 (гептан/етилацетат 7/3) 1 Н ЯМР (300 МГц, CDCI3): 1,24-1,38 (m, 9H), 1,43-1,50 (m, 2H), 1,51-1,57 (m, 2H), 2,15-2,21 (q, 2H), 3,60-3,64 (t, 2H), 4,14-4,20 (t, 2H), 5,77-5,82 (d, J=15,6 Гц, 1Н), 6,91-6,98 (dt, J=15,6 Гц, 1Н). 4. Стадія 4: Реакція сапоніфікації 0,60 г (2,81 ммоль) складного гідроксіефіру розчиняють в 10 об'ємах тетрагідрофурану. Повільно додають 3,4 мл (6,75 ммоль) 2М розчину гідроксиду натрію. Середовище нагрівають до 65°C протягом 3 годин. По закінченні реакції середовище гідролізують шляхом додавання 3M розчину хлористоводневої кислоти до одержання рН=2. Суміш концентрують досуха і потім екстрагують 9 96429 10 водну фазу етилацетатом. Органічні фази промиПроцедура синтезу 11-гідрокси-2t-ундеценової вають насиченим розчином NaCI, сушать над кислоти MgSO4, фільтрують і концентрують під вакуумом з Протокол синтезу DHA застосовується до цикодержанням 0,6 г неочищеного продукту. лононанону для одержання 11-гідрокси-2tОчікуване похідне ненасиченої оксикислоти ундеценової кислоти. одержують у формі білої твердої речовини шляВизначення характеристик: хом перекристалізації з ацетонітрилу на холоді, ТСХ: Rf=0,1 (гептан/етилацетат 6/4) вихід - 0,37 г (71%). 1Н ЯМР (300 МГц, CDCI3): 1,33-1,61 (m, 12Н), Отримане похідне оксикислоти є сполукою 2,20-2,28 (m, 2H), 3,66 (t, J=6,0 Гц, 2H), 5,84 (dt, формули: J=15,9 Гц, 1H), 7,09 (dt, J=15,9 Гц, 1Н). Mac-спектроскопія: [M-Na]+ 223 (розрахункове значення 200). Приклад 5 Процедура синтезу 12-гідрокси-2t-додеценової кислоти Протокол синтезу DHA застосовується до цикВизначення характеристик: лодеканону для одержання 12-гідрокси-2tТСХ: Rf=0,1 (гептан/етилацетат 6/4) 1 додеценової кислоти. Н ЯМР (300 МГц, CDCI3): 1,33-1,37 (m, 6H), Визначення характеристик: 1,45-1,49 (m, 2H), 1,55-1,58 (m, 2H), 2,20-2,25 (q, ТСХ: Rf=0,1 (гептан/етилацетат 6/4) 2H), 3,62-3,66 (t, 2H), 5,79-5,84 (d, J=15,6 Гц, 1Н), 1Н ЯМР (300 МГц, CDCI3): 1,35-1,56 (m, 14Н), 7,03-7,10 (dt, J=15,6 Гц, 1Н). + 2,20-2,27 (m, 2H), 3,55 (t, J=6,6 Гц, 2H), 5,80 (dt, Mac-спектроскопія: [M-Na] 209 (розрахункове J=15,6 Гц, 1Н), 6,96 (dt, J=15,6 Гц, 1Н). значення 186). + Mac-спектроскопія: [M-Na] 237 (розрахункове Температура плавлення: 62,5°C±1°C. значення 214). Приклад 2 Приклад 6 Процедура синтезу -фторованого похідного Процедура синтезу 12-гідрокси-2-фтор-2t10-гідрокси-2-фтордеценової кислоти: (R1=F, n=6) додеценової кислоти Модифікована тільки стадія 3: починаючи з Протокол синтезу DHA, фторованого в пололактолу (0,89 г, 7,7 ммоль), проводять реакцію женні 2 (Приклад 2), застосовується до циклодеВіттіга-Хорнера в присутності метилдіетилфосфоканону для одержання 12-гідрокси-2-додеценової нфторацетату (2,1 г, 9,2 ммоль) і карбонату калію кислоти у формі цис/транс-суміші. (1,6 г, 11,5 ммоль) в етанолі (9 мл) при 40°C. СтаВизначення характеристик: дію 4 проводять відповідно до раніше описаного ТСХ: Rf=0,1 (гептан/етилацетат 6/4) протоколу. Продукт, отриманий після перекриста1 Н ЯМР (300 МГц, CDCI3): 1,34-1,56 (m, 14H), лізації, має форму цис/транс-сумші. 2,24-2,27 (m, 2H цис-форма) або 2,49-2,54 (m, 2H Отримане похідне оксикислоти є сполукою транс-структура), 3,55 (t, J=6,6 Гц, 2Н), 5,97 (dt, формули: J=21,9 Гц, 1 Η транс-структура) або 6,10 (dt, J=55,2 Гц, 1Н, цис-форма). + Mac-спектроскопія: [M-Na] 255 (розрахункове значення 232). Приклад 7 Процедура синтезу 13-гідрокси-2tтридеценової кислоти Визначення характеристик: Протокол синтезу DHA застосовується до окТСХ: Rf=0,1 (гептан/етилацетат 6/4) сациклододекан-2-ону для одержання 13-гідрокси1 2t-тридеценової кислоти. Н ЯМР (300 МГц, CDCI3): 1,36-1,62 (m, 20Н), Визначення характеристик: 2,27-2,30 (m, 2H, цис-форма), 2,50-2,58 (m, 2Н, ТСХ: Rf=0,1 (гептан/етилацетат 6/4) транс-форма), 3,69 (m, 4H), 6,05 (dt, J=21,6 Гц, 1Н, 1 транс-форма) і 6,25 (dt, J=40,8 Гц, 1Н, цис-форма). Н ЯМР (300 МГц, CDCI3): 1,27-1,63 (m, 16Н), + Mac-спектроскопія: [M-Na] 227 (розрахункове 2,21-2,28 (m, 2H), 3,64 (t, J=3,6 Гц, 2H), 5,84 (dt, значення 204). J=15,6 Гц, 1Н), 7,09 (dt, J=15,6 Гц, 1Н). Приклад З Mac-спектроскопія: [M-Na]+ 251 (розрахункове Процедура синтезу 9-гідрокси-2t-ноненової кизначення 228). слоти Приклад 8 Протокол синтезу DHA застосовується до цикПроцедура синтезу 14-гідрокси-2tлопентанону для одержання 9-гідрокси-2tтетрадеценової кислоти ноненової кислоти. Протокол синтезу DHA застосовується до окВизначення характеристик: ТСХ: сациклотридекан-2-ону для одержання 14Rf=0,1 (гептан/етилацетат 6/4) гідрокси-2t-тетрадеценової кислоти. 1 Визначення характеристик: Н ЯМР (300 МГц, CDCI3): 1,36-1,61 (m, 8H), ТСХ: Rf=0,1 (гептан/етилацетат 6/4) 2,22-2,27 (m, 2H), 3,67 (t, J=6,3 Гц, 2H), 5,84 (dt, 1 J=15,6 Гц, 1Н), 7,09 (dt, J=15,6 Гц, 1Н). Н ЯМР (300 МГц, CDCI3): 1,29-1,35 (m, 14Н), + Mac-спектроскопія: [M-Na] 195 (розрахункове 1,46-1,61 (m, 4H), 2,21- 2,29 (m, 2H), 3,66 (t, J=6,6 значення 172). Гц, 2Н), 5,84 (dt, J=15,6 Гц, 1Н), 7,09 (dt, J=15,6 Гц, Приклад 4 1Н). 11 96429 12 + Mac-спектроскопія: [M-Na] 265 (розрахункове Визначення характеристик: значення 242). ТСХ: Rf=0,1 (гептан/етилацетат 6/4). 1 Приклад 9 Н ЯМР (300 МГц, CDCI3): 1,27-1,32 (m, 18Н), Процедура синтезу 14-гідрокси-21,46-1,61 (m, 4H), 2,21- 2,28 (m, 2H), 3,66 (t, J=6,6 фтортетрадеценової кислоти Гц, 2Н), 5,85 (dt, J=15,6 Гц, 1Н), 7,09 (dt, J=15,6 Гц, Протокол синтезу DHA, фторованого в поло1Н). + женні 2 (Приклад 2), застосовується до оксациклоМас-спектроскопія: [M-Na] 293 (розрахункове тридекан-2-ону для одержання 14-гідрокси-2-фторзначення 270). тетрадеценової кислоти у формі цис/транс-суміші. Приклад реакції Дебнера-Кневенагеля з викоВизначення характеристик: ристанням оксациклотридеканолу ТСХ: Rf=0,1 (гептан/етилацетат 6/4). 1,4 г (7,0 ммоль) оксациклотридеканолу (отри1 Н ЯМР (300 МГц, CDCI3): 1,29 (m, 28Н), маного відповідно до протоколу часткового відно1,42-1,62 (m, 8H), 2,27-2,31 (m, 2H, цис-форма), влення лактолу) розчиняють під потоком азоту в 4 2,51-2,56 (m, 2H, транс-форма), 3,68 (t, J=6,6 Гц, об'ємах піридину в присутності 1,09 г (10,5 ммоль) 2Н), 3,70 (t, J=6,6 Гц, 2H), 6,04 (dt, J=21,3 Гц, 1H, малонової кислоти та 0,11 мл піперидину. Реактранс-форма), 6,27 (dt, J=33,0 Гц, 1Н, цис-форма). ційну суміш нагрівають до 80°C протягом 1 години + Mac-спектроскопія: [M-Na] 283 (розрахункове 30 хвилин, потім нагрівають із дефлегматором значення 260). протягом 2 годин. При кімнатній температурі розПриклад 10 чин виливають на 3M розчин НСІ (50 мл). ВідфільПроцедура синтезу 17-гідрокси-2tтровану тверду речовину промивають водою, погептадеценової кислоти тім перекристалізовують з ацетонітрилу (з Протокол синтезу DHA застосовується до цикодержанням 1,2 г, що відповідає виходу, рівному лопентадеканоліду для одержання 17-гідрокси-2t70%). гептадеценової кислоти. Похідні ненасичених жирних оксикислот згідно Визначення характеристик: з даним винаходом стали об'єктом численних ексТСХ: Rf=0,1 (гептан/етилацетат 6/4). периментів, які продемонстрували їхні переваги як 1 активних інгредієнтів дерматологічних та/або косН ЯМР (300 МГц, CDCI3): 1,27-1,32 (m, 20Н), метичних композицій. 1,46-1,61 (m, 4H), 2,20-2,29 (m, 2H), 3,67 (t, J=6,6 Дослідження антирадикального ефекту на акГц, 2Н), 5,84 (dt, J=15,6 Гц, 1Н), 7,08 (dt, J=15,6 Гц, тивованих формах кисню (АФК) 1Н). + В ході нормального метаболізму клітин під час Mac-спектроскопія: [M-Na] 307 (розрахункове епізодичного впливу на шкіру стресових агентів значення 284). або під час патологічних змін шкіри утворюються Приклад 11 хімічно активні форми кисню, які також називають Процедура синтезу 17-гідрокси-2Активованими Формами Кисню (АФК) (Y M.W. фторгептадеценової кислоти Janssen et al., 1993). Ці АФК, описані як дуже хіміПротокол синтезу DHA, фторованого в полочно активні метаболіти, відіграють важливу роль у женні 2 (Приклад 2), застосовується до циклопенбагатьох процесах, таких як запалення, старіння тадеканоліду для одержання 17-гідрокси-2та пухлинний ріст. фторгептадеценової кислоти у формі цис/трансАФК вважаються «вторинними месенджерасуміші. ми» у внутрішньоклітинних сигнальних процесах, Визначення характеристик: що стосуються окисного стресу, і, отже, ранніми ТСХ: Rf=0,1 (гептан/етилацетат 6/4). 1 медіаторами запалення (A. Van Der Vlietand A. Н ЯМР (300 МГц, CDCI3): 1,27 (m, 40Н), Bast, 1992). 1,45-1,62 (m, 8H), 2,24-2,32 (m, 2H, цис-форма), Їхня надлишкова продукція приводить до істо2,50-2,58 (m, 2H, транс-форма), 3,69 (t, J=6,6 Гц, тних порушень у клітині. Тому деякі клітинні ком4Н), 6,05 (dt, J=21,6 Гц, 1H, транс-форма) і 6,26 (dt, поненти є основними мішенями окисного стресу: J=40,8 Гц, 1H, цис-форма). можуть ушкоджуватися ліпідні компоненти плазмаМас-спектроскопія: [М-Н] 301 (розрахункове тичної мембрани (перекисне окиснення ліпідів), значення 302). білки (денатурація та деградація) і генетичний маТемпература плавлення: 77°C±1°C. теріал або ДНК (мутації). Клітини здатні обмежуваПриклад 12 ти ці окисні ушкодження за рахунок різних систем Процедура синтезу 18-гідрокси-2tантирадикального захисту (ферментних і нефероктадеценової кислоти: (R1=Η, n=14) ментних антиоксидантів) (В.Р. Yu, 1994; Η. Stelling Протокол синтезу DHA застосовується до гекet al., 1999). сациклодеканоліду для одержання 18-гідроксиПроте, у певних умовах АФК утворюються в 2йзктадеценової кислоти. таких кількостях, що внутрішньоклітинної антиокВизначення характеристик: сидантної активності недостатньо; тому такі АФК ТСХ: Rf=0,1 (гептан/етилацетат 6/4). 1 стають факторами, індукуючими запальні поруН ЯМР (300 МГц, CDCI3): 1,27-1,65 (m, 26Н), шення та старіння тканин (Y. Міуасhі et al., 1986; 2,19-2,39 (m, 2H), 3,67 (t, J=6,6 Гц, 2H), 5,83 (dt, Μ. Kress et al., 1995). J=15,6 Гц, 1Н), 7,09 (dt, J=15,6 Гц, 1Н). + Існують різні хімічні речовини (наприклад, Мас-спектроскопія: [M-Na] 321 (розрахункове Н2О2) або фізичні фактори (наприклад, УФ-А), здазначення 298). тні створювати окисний стрес in vitro. Продуковані Приклад 13 АФК ушкоджують різні клітинні мішені (мембрани, Визначення характеристик 16-гідрокси-2tДНК або білки), і це ушкодження можна аналізувагексадеценової кислоти 13 96429 14 ти з використанням широко використовуваних біоДля оцінки похідних ненасичених жирних оксихімічних методик, таких як аналіз субстратів тіобакислот розчин готують на свіжоприготовленому рбітурової кислоти (TBARS) у випадку перекисного культуральному середовищі з концентраціями в окиснення ліпідів або аналіз in vitro внутрішньоклідіапазоні 0,02, 0,2, 2 і 20 нг/мл. тинних АФК за допомогою зонда H2DCF-DA. e) Протокол: Ми розробили модель для дослідження in vitro Посів клітин: окисного стресу, викликуваного системою Клітини-фібробласти лінії L929 висівали на міН2О2/залізо, оскільки Η2Ο2 генерує велику кількість кропланшети з 96 лунками та плоскою основою в внутрішньоклітинних АФК в результаті ланцюгової 100 мкл DMEM з додаванням 10% фетальної сиреакції, що запускається окисненням мембранних роватки телят, потім їх інкубували протягом ночі ліпідів. при 37°C у вологій атмосфері з 5%-ним вмістом Цей спосіб оснований на використанні флуоСО2. ресцентного зонда 6-карбокси-2',7'Контрольний планшет без клітин оцінювали по дихлордигідрофлуоресцеїну діацетату діацеток6 лункам. симетилового ефіру (H2DCF-DA), що після проникПопередня обробка клітин: нення в клітину дезацетилюється внутрішньокліРозведення продуктів, що підлягають випротинними естеразами та утворює H2DCF. Цей буванню, і молекул порівняння робили з викориспродукт окиснюється внутрішньоклітинними АФК танням культурального середовища без ФСТ, подо яскраво флуоресціюючої сполуки - 2',7'тім наносили їх в 7 лунок у кількості 100 мкл на дихлорфлуоресцеїну (DCF) (Suematsu Μ. Et al., лунку. 1996, Free Radicals Practical Approach, Punchard Потім клітини інкубували протягом 3 годин при ed., p. 83-99). 37°C у вологій атмосфері, що містить 5% СО2. Матеріали та методи, використані для аналізу «Холості» (природна флуоресценція клітин), in vitro внутрішньоклітинних АФК, вказані нижче. «контрольні» (базальна продукція АФК) і «стимуа) Клітинний матеріал льовані» (продукція АФК після окисної обробки) Фібробластні клітини шкіри миші лінії L929. покривали 100 мкл DMEM. б) Матеріали: «Контрольні» клітини інкубували із зондом, - Мікропланшет з 96 лунками із плоскою осноале не проводили ні попередньої обробки, ані обвою. робки. Цитофлуориметр Cytofluor II: див. «Стимульовані» клітини інкубували із зондом і PERCEPTIVE BIOSYSTEMS. проводили обробку, але не попередню обробку. в) Реагенти «Холості» клітини не піддавали попередній Реагенти для культивування клітин: обробці, не інкубували із зондом і не обробляли. - Культуральне середовище Ігла в модифікації Інкубація клітин із зондом та окисним стресом: Дульбекко (DMEM) Клітини промивали PBS 1 у кількості 100 мкл - Фетальна сироватка телят (ФСТ) на лунку. Потім їх інкубували протягом 30 хвилин - Фосфатний буфер (PBS) із рН 7 при 37°C у вологій атмосфері, що містить 5% СО2, - Трипсин-ЕДТА (1) з 50 мкл зонда H2DCF-DA у концентрації 5 мкМ. Флуоресцентний зонд: Після 30 хвилин контакту із зондом клітини ін- 6-карбокси-2',7'-дихлордигідрофлуоресцеїну кубували протягом 30 хвилин при 37°C у вологій діацетату діацетоксиметиловий ефір (РМ. 675,43) атмосфері, що містить 5% СО2, з додаванням 25 Продукти для стимуляції клітин: мкл Н2О2 у концентрації 800 мкМ і 25 мкл розчину - Перекис водню (Н2О2) 3%: див. GIFRER тривалентного заліза та двовалентного заліза в (Gifrer Barbezat Laboratory) концентрації 8 мМ із одержанням кінцевої концен- Подвійний сульфат амонію та двовалентного трації Н2О2, рівної 200 мкМ, і концентрації трива2+ заліза (Fe ) лентного та двовалентного заліза, рівної 2 мМ. - Подвійний сульфат амонію та тривалентного Потім клітини промивали PBS 1 у кількості 3+ заліза (Fe ) 100 мкл на лунку, після чого інкубували їх протяг) Досліджені продукти: гом 30 хвилин при 37°C у вологій атмосфері, що Досліджені концентрації не є цитотоксичними містить 5% СО2, з 100 мкл PBS 1. концентраціями. Цитотоксичність визначали з виЦя інкубація протягом 1 години 30 хвилин при користанням способу з нейтральним червоним 37°C дає можливість внутрішньоклітинним естерапісля інкубації продукту протягом 3 годин. зам дезацетилювати зонд до H2DCF, що може Антирадикальним продуктом порівняння є вібути окиснений АФК до DCF - флуоресціюючої тамін Ε або α-токоферол (РМ: 430.7) (SIGMA, див.: сполуки, утворення якої є пропорційним вмісту Т-1539). внутрішньоклітинних АФК. Маточний розчин готують у концентрації 400 Інтенсивність флуоресценції визначають за мг/мл у ДМСО та зберігають при -20°C. Розчин для допомогою цитофлуориметра при збудження=485 нм попередньої обробки готують безпосередньо пеі випромінювання=530 нм. Вона відображає кількість ред дослідом у концентрації 400 мкг/мл у культуутворених внутрішньоклітинних АФК. ральному середовищі без фетальної сироватки Схема протоколу досліду: телят. 15 96429 16 Розрахунок % захисту проти продукції внутрішньоклітинних АФК. Наведене нижче співвідношення дозволяє розрахувати для кожної дослідженої концентрації продукту % захисту проти продукції внутрішньоклітинних АФК (оскільки інтенсивність флуоресценції (ІФ) відображає виділення внутрішньоклітинних АФК). [ІФ після впливу окисника (Н2О2/залізо) - ІФ після впливу (окисник+продукт)] χ 100 ІФ після впливу окисника (Н2О2/залізо) - ІФ у контролі АФК після екзогенного окисного стресу в порівнянні з «холостими» клітинами (100%) і «стимульованими» клітинами (0%). Середні відсотки захисту для 13 молекул, досліджених в 4 концентраціях на клітинах лінії L929, представлені в Таблиці 1 нижче. Значення, наведені в таблиці нижче, є відсотками інгібування внутрішньоклітинної продукції Таблиця 1 Аналіз захисту проти внутрішньоклітинної продукції АФК для 13 молекул, що є похідними ненасичених жирних оксикислот: Інгібування внутрішньоклітинної продукції АФК у відсотках Вітамін Ε 400 мкг/мл Сполука формули 1 n R Rn 3 Η Η 3 Η Η 4 Η Η 4 Η Η 5 Η Η 6 Η Η 6 Η Η 9 Η Η 10 Η Η 10 Η Η 13 Η Η 13 Η Η 14 Η Η R1 F Η F Η Η F Η Η F Η F Η F 0,02 нг/мл 3 21 10 17 56 15 9 29 11 36 3 6 47% Дози 0,2 нг/мл 2 нг/мл -3 -32 15 11 6 -4 9 9 47 46 4 5 33 10 6 16 0 4 -20 28 14 13 -1 -17 -26 20 нг/мл -51 14 -36 0 36 -9 -22 -19 -34 -9 -10 -42 Попередня інкубація: 3 години. Кількість випробувань = 3 для всіх сполук. Кількість випробувань = 18 для вітаміну Е. In vitro на клітинному рівні екзогенний стрес, 2+ 3+ викликаний H2O2/Fe -Fe , здатний індукувати продукцію внутрішньоклітинних АФК, що виявляється за допомогою флуоресцентного зонда. На закінчення необхідно відзначити, що нефторовані похідні ненасичених жирних оксикислот до короткими ланцюгами (С9 і С10), очевидно, є 17 96429 18 2+ 3+ особливо ефективними щодо антирадикального H2O2+Fe ОН'+ОН+Fe захисту клітин. Дослідження антирадикального ефекту. АнаПродукти оцінювали на клітинахліз перекисного окиснення ліпідів. фібробластах миші лінії L929. Клітини проходили Крім того, в ході нормального метаболізму попередню обробку різними концентраціями проклітин під час випадкового впливу на шкіру стредуктів протягом 16 годин, а потім їх стимулювали 2+ 3+ сових агентів або під час патологічних змін шкіри комплексом Н2О2-Fe /Fe (200 мкМ-1мМ) протяутворюються хімічно активні форми кисню, які гом 1 години. також називають Вільними Радикалами Кисню Маточні розчини: 100 мг/мл в етанолі при (ВРК) (Y.M.W. Janssen et al., 1993). Ці ВРК, опи4°C. сані як дуже хімічно активні метаболіти, відіграКінцеві розчини: 0,02 нг/мл. ють важливу роль у багатьох процесах, таких як Перекисне окиснення мембранних ліпідів запалення, старіння та пухлинний ріст. аналізували за допомогою виміру TBARS (див. ВРК вважаються «вторинними месенджераПротокол РLN°2 згідно Morliere et al., 1991). ми» у внутрішньоклітинних сигнальних процесах, Принцип аналізу: що стосуються окисного стресу, і, отже, ранніми У кислому середовищі при 95°C утворюються медіаторами запалення (A. Van Der Vliet and A. комплекси, називані TBARS (реакційноздатна Bast, 1992). речовина тіобарбітурової кислоти), між продуктаЇхня надлишкова продукція приводить до ісми окиснення ліпідів (малоновим діальдегідом, тотних порушень у клітині. Тому деякі клітинні або МДА) і тіобарбітуровою кислотою (ТБК), які компоненти є основними мішенями окисного можна аналізувати за їхньою флуоресценцією стресу: можуть ушкоджуватися ліпідні компоненшляхом порівняння зі стандартним діапазоном ти плазматичної мембрани (перекисне окиснення флуоресценції МДА. Результати аналізу TBARS ліпідів), білки (денатурація та деградація) і геневиражають у пмоль/мкг білка. Білки та TBARS тичний матеріал або ДНК (мутації). Клітини здатні аналізують у внутрішньоклітинному середовищі. обмежувати ці окисні ушкодження за рахунок різРозрахунок відсотка захисту клітинних мемних систем антирадикального захисту (ферментбран: них і неферментних антіоксидантів) (В.Р. Yu, За результатами розрахунку TBARS у 1994; Η. Stellingetal., 1999). пмоль/мкг білка ми розрахували ефективність Проте, у певних умовах ВРК утворюються в захисту проти окиснення мембранних ліпідів для таких кількостях, що внутрішньоклітинної антіокрізних продуктів. сидантної активності недостатньо; тому такі ВРК стають факторами, індукуючими запальні збудження та старіння тканин (Y. Miyachi et al., 1986; Μ. Kress et al., 1995). З метою оцінки антирадикальної активності Було виконано чотири незалежних експерирізних гідроксильованих похідних згідно з даним менти. В ході цих експериментів були оцінені різні винаходом ми проаналізували їхню здатність сполуки (аналіз не дозволяв оцінювати більше 10 забезпечувати захист проти порушень клітинних молекул одночасно). Сполуки, що оцінювалися мембран, викликаних окисним (хімічним) стрекілька разів, були вибрані за результатами, отрисом, у порівнянні зі стандартним антіоксидантом маними в іншому аналізі, у якому також вимірявітаміном Е. лася антирадикальна активність (кількісний анаПлазматична мембрана є основною та перліз на активовані форми кисню, АФК). винною мішенню ВРК і, оскільки в ній міститься Використана в даному експерименті модель багато ліпідів, вона є місцем посиленого переки(реакція Фентона) індукує значне перекисне окисного окиснення (A.W. Girotti, 1985). Перекиси, що снення ліпідів у фібробластах L929. Це масивне утворюються в ході цього окиснення ліпідів, тавиділення гідроксильного радикала ОН викликає кож є дуже хімічно активними та здатні руйнувати на клітинному рівні окисний стрес, зокрема, на білковий і генетичний матеріал. рівні мембран. Однак, у цьому типі окисної реакДля оцінки ушкоджень мембран ми вимірюції продукти перекисного окиснення ліпідів перевали перекисне окиснення ліпідів за допомогою бувають у клітинах, і тому вміст TBARS кількісно кількісного аналізу in vitro комплексів, що склавизначається у внутрішньоклітинному середовидаються із продуктів окиснення ліпідів і тіобарбіщі. турової кислоти. Такі комплекси називаються Вітамін Е в дозі 400 мкг/мл знижує перекисне TBARS (субстратами тіобарбітурової кислоти) і окиснення ліпідів, викликане комплексом H2O2дали аналізу назву: аналіз на TBARS. 2+ 3+ Fe /Fe , і дуже ефективно захищає клітинні Для імітації хімічного окисного стресу ми обмембрани. робляли клітини-фібробласти лінії L929 комплекУ Таблиці II представлені результати 4 екссом, що складався з перекису водню (Н2О2) і за2+ 3+ периментів. ліза (Fe /Fe ), відтворюючи в такий спосіб Очевидно, що гідроксильовані похідні виявреакцію Фентона, що є джерелом ВРК і, зокрема, ляють стабільну та відтворювану антіоксидантну гідроксильного радикала (ОН) (D.A. Vessey et al., активність. Це стосується, зокрема, похідних з 1992): коротким вуглецевим ланцюгом. 19 96429 20 Таблиця II Захист мембранних ліпідів різними гідроксильованими похідними n 6 6 4 13 3 13 10 4 10 14 4 9 3 Досліджені молекули Вітамін Ε 400 мкг/мл Сполука формули I R Rn Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η СН3 Η Η Η Η Η Η Η Η Η Η Захист мембранних ліпідів в % № експерименту Середнє значення Стандартний відхил 4 44,66 25,85 R1 Η F F Η F F Η Η F F Η Η Η Модель in vitro, представлена в даному дослідженні, відображає наслідки впливу значного окисного стресу на основну клітинну мішень, якою є плазматична мембрана. Тому кількісний аналіз перекисного окиснення ліпідів є гарним маркером окисного стресу та забезпечує можливість оцінки антіоксидантної дії активних інгредієнтів на гідроксильні радикали на рівні клітинною мембрани. Вітамін Е, антіоксидантна молекула, забезпечує можливість підтвердження правильності цієї моделі та ефективності захисту клітинних мембран проти окисного стресу. Диференціація кератиноцитів Епідерміс бере участь в основній функції шкіри, якою є стійкість до впливів навколишнього середовища та захист від них. Це багатошаровий плоский роговіючий епітелій, що постійно обновляється. Гомеостаз і регенерація тканин основані на клітинах-кератиноцитах, опорних клітинах і розчинних факторах, які в безпосередній близькості від клітин сприяють міжклітинним взаємодіям і взаємодіям клітин з міжклітинним матриксом. Роговий шар, остання стадія диференціації епідермісу, утворюється в результаті трьох основних процесів: утворення кератинових філаментів, «зроговіння» кератиноцитів і утворення міжклітинного ліпідного цементу, організованого у вигляді пластинчастих структур. Усередині епідермісу склад та природа ліпідів варіюють залежно від стадії диференціації, у якій перебувають кератиноцити. Так, під час руху базальних шарів клітин до клітин рогового шару, спостерігається значне зниження вмісту фосфоліпідів, які в шарах живих клітин відповідають за цілісність плазматичних мембран; паралельно відзначається підвищення вмісту нейтральних ліпідів (вільних жирних кислот і тригліцеридів) і стеролів (холестерину), а також дуже значне збільшення вмісту сфіголіпідів і, зокрема, церамідів. 3 3 3 1 1 3 1 2 3 1 2 3 2 52,91 40,65 36,54 22,10 38,14 7,39 27,18 57,75 13,13 35,30 37,88 8,72 15,7 8,81 16,83 41,69 16,23 3,15 13,37 26,28 48,78 29,93 На рівні рогового шару виявляється 40-50% сфінголіпідів, 20-27% холестерину та 9-26% вільних жирних кислот. Цераміди зв'язані ковалентними зв'язками із залишками глутамінової кислоти інволюкрину - попередника рогової оболонки. Жирні кислоти, завдяки своїй гідрофобній природі, беруть участь в регуляції непроникності шкіри, холестерин бере участь у регуляції плинності мембран. Численні специфічні білки рогового шару (або stratum corneum) (шару, що надає епідермісу бар'єрну функцію) утворюються на рівні зернистого шару, що складається з останніх кератиноцитів, які мають здатність до транскрипції та трансдукції, перш ніж відбудеться лізис ядра, що супроводжує зроговіння. Програма диференціації кератиноцитів основана, головним чином, на еволюції структурних білків, якими є кератини, і які сприяють архітектурній цілісності епідермісу. Їхня експресія варіює залежно від ступеня зрілості епідермальних клітин. У супрабазальних шарах з'являються основний кератин 1 і кислийкератин 10, так звані кератини термінальної диференціації. Поблизу рогового шару кератини взаємодіють із білками з високим вмістом гістидину з утворенням відносно гомогенної суміші, що заповнює корнеоцити. Ці білки є похідними попередника, профілагрину, що є великою молекулою ([MB]>450 кДа), запаси якої зберігаються на рівні зернистого шару. Це білок, N- і С-термінальні домени якого зв'язують кальцій, а його дефосфорилювання та частковий протеоліз приводять до утворення філагрину. Філагрин каталізує утворення дисульфідних містків між кератиновими філаментами та сприяє їхньому об'єднанню з утворенням внутрішньокорнеоцитарного матриксу. З іншого боку, в результаті протеолізу він є джерелом амінокислот і пептидних похідних, які 21 96429 22 надають роговому шару певні вологоутримувальНормальні кератиноцити людини (НКЛ), проні властивості. ліферують і диференціюються in vitro, з утворенУ роговому шарі корнеоцити містять, головням стратифікованих шарів, що імітують базову ним чином, кератинові філаменти, занурені в організацію шкіри. Позаклітинні концентрації кащільний матрикс, оточений товстою та міцною льцію, що перевищують 0,1 мМ, запускають касбілковою стінкою: роговою оболонкою. Білкикад геномних і негеномних явищ, які переводять попередники цієї структури, розташовані з внуткератиноцити з фази проліферації у фазу диферішнього боку плазматичної мембрани, синтезуренціації. Диференціацію кератиноцитів можна ються кератиноцитами остеподібного шару, але оцінити за допомогою аналізу експресії декількох їх зшивки - за участю ферментів трансглутаміназ маркерів, таких як кератини 1 і 10, трансглутамі-утворюються в остеподібному і зернистому шаназа 1, десатураза DES2, інволюцин, транспоррах. Численні білки цитозолю, які асоційовані з тери FATP4 і ABCG1. Тому ми оцінювали ефект мембранною фракцією кератиноцитів або зберідеяких гідроксіалкенових карбонових кислот у гаються в зернах кератогіаліну, беруть участь в моделі з культивуванням клітин in vitro. утворенні рогової оболонки. Можна, наприклад, План дослідження можна схематично предвідзначити інволюкрин (68 кДа) з високим вмістом ставити в такий спосіб: диференціація НКЛ in vitro глутаміну та лізину. і відбір проб для аналізу. Непроникність рогового шару обумовлена, головним чином, гідрофобним ліпідним міжклітинним цементом, що зв'язує один з одним корнеоцити. Вміст ліпідів в епідермісі є кінцевим результатом ліпогенезу в кератиноцитах і сальних залозах. У нормальному епідермісі в глибоких шарах переважає суміш нейтральних і полярних ліпідів, яка прогресивно заміняється більш неполярним вмістом, що включає цераміди. У цьому ліпогенезі, отже - і в синтезі церамідів, беруть участь численні білки. Серед них виявлений білок DES2 (сфінголіпід-С4-гідроксилаза/дельта-4Умови культивування клітин і відбору проб десатураза): він має активність гідроксилази дигіНормальні кератиноцити людини (НКЛ) видідроцерамідів, яка бере участь у синтезі фітоцеляли з експлантатів шкіри. їх культивували в середовищі KSFM (Gibco) з низькою концентрацією рамідів, а його експресія індукується процесом диференціації (Mizutani Y. et al., 2004). Ліпіди, кальцію (0,1 мм), що містить 25 мкг/мл ΒΡΕ (гіпосинтезовані кератиноцитами, рухаються до повефизарного екстракту корів) і 1,5 нг/мл EGF (епірхні шкіри в пластинчастих тільцях - кератиносотеліального фактора росту). Через двадцять четири години після посіву індукували мах. Вони секретуються в міжклітинні простори та утворюють безперервні шари, розташовані парадиференціацію шляхом додавання кальцію (кінлельно клітинним мембранам корнеоцитів. Ця цева концентрація 1,2 мМ). Активні речовини дореорганізація ліпідів, що відбувається в ході дидавали або не додавали одночасно з кальцієм у концентраціях, рівних 100 і 1 мкг/мл, щоб визнаференціації епідермісу, підключає деяке число чити, чи мають вони посилюючий ефект на дипереносників ліпідів із сімейства АВСтранспортерів (аденозинтрифосфат-зв'язуючих ференціацію. Клітини аналізували через 48 годин касетних транспортерів). Серед цих транспортепісля додавання кальцію та продуктів. Екстракція РНК і ПЛР зі зворотною транскрирів деякі виявляють експресію, індуковану в ході пцією (RT-PCR) у реальному часі диференціації кератиноцитів (АВСВ1, АВСС1, АВСС3, АВСС4 і АВС1), експресія інших пригніЗагальну РНК екстрагували з кератиноцитів чується (АВСВ9 і ФИС1), а треті не піддаються на холоді. Після зворотної транскрипції мРНК в кДНК ніякій регуляції. Роль транспортерів, експресія виконували ПЛР на планшетах з 96 лунками яких індукується, була вивчена: наприклад, ABCG1 бере участь у транслокації холестерину в (прилад для кількісної ПЛР iCycler, виробництва кератиноцити, що перебувають у процесі дифекомпанії BioRad). Експресію транскриптів трансглутамінази, десатурази (DES2), ABCG1 і FATP4 ренціації. Експресія деяких членів іншого сімейснормалізували по відношенню до експресії стантва транспортерів - FATP (білки-транспортери жирних кислот), таких як FATP1, FATP3, FATP4 і дартних генів (GAPDH, UBC, HPRT). Рівень ексFATP5, індукується в ході диференціації кератипресії в пробах, оброблених кальцієм і активною речовиною, порівнювали з рівнем експресії в ноцитів. Ці транспортери беруть участь у реоргапробах, оброблених тільки кальцієм. нізації пулу нейтральних ліпідів (Kielar et al., 2003). Результати щодо ефектів продуктів у концентрації 1 мкг/мл наведені в таблицях нижче. 23 Сполука формули 1 n R Rn R1 3 Η Η F 3 Η Η Η 4 Η Η F 4 Η Η Η 5 Η Η Η 6 Η Η F 6 Η Η Η 9 Η Η Η 10 Η Η F 10 Η Η Η 13 Η Η F 13 Η Η Η 14 Η Η F 96429 24 Фактор індукції проти контролю (СаСІ2 1,2 мМ) Вітамін D3 1 мкМ TG1 1,5 1,5 1,2 1,6 1,2 1,5 1,2 1,1 1,4 1,4 1,5 4,2 1,4 1,7 DES2 ABCG1 FATP4 2,0 2,0 1,1 1,7 1,5 1,2 1,6 1,5 1,4 2,2 2,6 1,3 1,0 1,2 1,0 1,8 2,7 1,0 1,3 1,3 1,0 1,7 1,9 1,2 1,8 1,5 1,2 1,6 1,4 1,0 2,0 1,4 1,2 9,0 4,8 2,2 3,0 3,0 1,4 2,8 4,0 1,0 В дозі 1 мкг/мл всі продукти чинили помірний ефект на експресію маркерів диференціації. Ефекти продуктів у концентрації 100 мкг/мл Сполука формули І n R Rn R1 3 Η Η F 3 Η Η Η 4 Η Η F 4 Η Η Η 6 Η Η F 6 Η Η Η 9 Η Η Η 10 Η Η F 10 Η Η Η Фактор індукції проти контролю (СаСІ2 1,2 мМ) Вітамін D3 10 мкМ Вітамін D3 в концентрації 10 мкм підсилює експресію транскриптів трансглутамінази 1, DES2 і ABCG1 у 8,3, 11,1 і 3,1 рази, відповідно, в порівнянні з контролем, обробленим тільки кальцієм, 3 іншого боку, експресія FATP4 не модулюється в результаті обробки вітаміном D3. Таким чином, був продемонстрований стимулюючий ефект похідних ненасичених жирних оксикислот згідно з даним винаходом на диференціацію. Аналіз протизапального ефекту на рівні ліпідних медіаторів запалення Кератиноцити - найбільш численні на рівні епідермісу клітини - у відповідь на численні позаклітинні фактори, присутні в їхньому навколишньому середовищі, виділяють біологічно активні медіатори, а саме - простагландини та лейкотриєни, які відіграють важливу роль в ініціації та модулюванні шкірної запальної реакції, а також беруть участь у регулюванні імунної відповіді. Простагландин PG6KF1-альфа є одним з основних метаболітів, продукованих стимульованими кератиноцитами, і представником модуляторів продукції метаболітів, що утворюються в результаті метаболізму арахідонової кислоти по циклооксигеназному шляху. Протокол: Суспензію кератиноцитів у культуральному середовищі DMEM з 10% фетальної сироватки телят розподіляли по планшетах з 6 лунками 6 (1,2·10 клітин/лунку) та інкубували протягом 16 TG1 8,3 0,9 2,6 1,7 1,7 7,8 12,3 14,8 3,5 31,4 DES2 ABCG1 FATP4 11,0 3,1 1,3 1,9 1,2 1.2 2,4 4,0 1,2 3,2 2,6 1,4 2,2 2,5 1,4 10,3 6,3 1,9 11,5 6,6 2,5 51,7 13,8 4,5 16,0 4,6 2,3 125,8 25,5 5,9 годин при 37°C в атмосфері, що містить 5% СО2. Потім кератиноцити промивали PBS для видалення незчеплених клітин, після чого діяли на них продуктами, що підлягають випробуванню, розведеними в DMEM без фетальної сироватки телят (яка може впливати на результати кількісного аналізу). Концентрація, досліджена в культурі, дорівнює 3 мкг/мл. Вона була вибрана після попереднього випробування, присвяченого оцінці цитотоксичності (з нейтральним червоним), і не є цитотоксичною. Кожна обробка була виконана на 3 лунках. Клітини попередньо інкубували протягом 60 хвилин із продуктами, що підлягають випробуванню, після чого додавали агент, що стимулює каскад арахідонової кислоти (іонофор кальцію), на 5 годин: іонофор кальцію А23187 використовували в концентрації 1 мкМ. Після культивування протягом 5 годин відбирали культуральне середовище з кожної лунки, центрифугували його при 3000 об./хв. і зберігали при -80°C. Продукцію простагландину 6KF1 в кожному аналізі вимірювали з використанням набору для імуноферментного твердофазового аналізу (ELISA) виробництва компанії EUROMEDEX. Результати: Результати виражені у відсотках активності по відношенню до стимульованого контролю. 25 96429 Сполука формули І n 3 4 4 4 8 8 9 10 10 13 13 R Η Η Η Η Η Η Η Η Η Η Η Rn Η Η Η СН3 Η Η Η Η Η Η Η R1 Η F Η Η Η F Η F Η F Η 26 % інгібуючої активності досліджуваної молекули на продукцію PG6KF1 Запалення 3 мкг/мл 29 30 Протизапальні властивості: Інгібування синтезу прозапального цитокіну 1L8 Бар'єрна функція шкіри забезпечує захист від факторів навколишнього середовища, а кератиноцити епідермісу можуть прямо реагувати на широкий спектр подразників або алергенів і брати активну участь у запальних та імунних процесах, що відбуваються в шкірі, зокрема - за рахунок продукції прозапальних цитокінів, медіаторів білкової природи. Серед цих біологічно активних молекул первинними цитокінами вважаються IL1 (інтерлейкін 1) і TNF (фактор некрозу пухлин а); їхнього виділення досить для того, щоб викликати запалення, оскільки вони індукують молекули адгезії на рівні ендотеліальних клітин і фактори хемотаксису, такі як хемокіни. Система хемокінів регулює рух лейкоцитів під час запальної реакції та необхідна для взаємодії між уродженою та адаптивною імунними відповідями. В даному дослідженні ми сконцентрувалися, зокрема, на хемокіні - інтерлейкіні 8, що бере велику участь у розвитку імунної відповіді, основною функцією якого є рекрутинг та активація полінуклеарних нейтрофілів, а саме - стимуляція вивільнення ними прозапальних молекул. В даному дослідженні, виконаному з використанням 96-лункових планшетів, ми оцінювали активність оксіалкенових кислот по відношенню до продукції інтерлейкіну 8, індукованої у кератиноцитах форболовим ефіром РМА та іонофором кальцію А23187. Протокол: 32 44 31 18 Не активна 14 25 Суспензію кератиноцитів в KSFM з добавка4 ми розподіляли по 96-лункових планшетах (310 клітин/лунку) та інкубували протягом 16 годин при 37°C в атмосфері, що містить 5% СО2. Потім кератиноцити промивали PBS з метою видалення незчеплених з лунками клітин, після чого діяли на них продуктами, що підлягають дослідженню, розведеними в KSFM без добавок (які могли вплинути на результати аналізу). Концентрація, досліджена на культурі клітин, дорівнювала 3 мкг/мл. Вона була вибрана за результатами попереднього випробування, у якому оцінювалася цитотоксичність (з нейтральним червоним), і не є цитотоксичною. Для кожної обробки було використано 3 лунки. Клітини попередньо інкубували протягом 60 хвилин із продуктами, що підлягають дослідженню, потім стимулювали; паралельно були проведені негативні контролі без стимулюючих речовин: форболміристатацетату (РМА) 1 мкМ + іонофора кальцію (А23187) 0,1 мкМ. Інкубація протягом 6 годин при 37°C в атмосфері вологого повітря, що містить 5% СО2. Культуральне середовище з кожною лунки відбирали, центрифугували при 3000 об./хв. і зберігали при -80°C. Аналіз на цитокін: IL8 визначали імуноферментним способом з використанням набору для імуноферментного твердофазового аналізу (ELISA) виробництва компанії Immunotech. Результати: Результати наведені у відсотках активності по відношенню до стимульованого контролю. 27 96429 Сполука формули 1 n 3 4 4 4 6 8 8 9 10 10 13 13 14 R Η Η Η Η Η Η Η Η Η Η Η Η Η Rn Η Η Η СН3 Η Η Η Η Η Η Η Η Η R1 Η F Η Η Η Η F Η F Η F Η Η % інгібуючої активності оцінюваних молекул на продукцію PG6KF1 Запалення 3 мкг/мл 50 Не активна 15 Не активна Не визначено Не активна Не активна 16 30 30 107 62 Не активна Сполуки згідно з даним винаходом оцінювалися щодо їхньої протизапальної активності через вплив на вивільнення інтерлейкіну 8 кератиноцитами людини (НКЛ), стимульованими складним ефіром форболу РМА та іонофором кальцію А23187. n 13 13 Сполука формули 1 R Rn Η Η Η Η 28 Було проведено три незалежних експерименти: об'єднання отриманих даних дозволило довести протизапальний потенціал таких двох сполук: n=13, R=Rn=H, R1=F n=13, R=Rn=R1=H Для концентрації, у якій оцінювалася кожна молекула, і після розрахунку ефективної 50%-ної дози, наші результати показують таке: % інгібування при 3 мкг/мл R1 F Η Запалення та сверблячка: аналіз потоку кальцію після стимуляції PAR2-рецепторів Рецептор під назвою «Активований протеазою рецептор-2» (PAR-2) бере участь у фізіопатології багатьох захворювань, які включають запальні реакції. PAR2 експресується різними типами клітин шкіри: кератиноцитами, міоепітеліальними клітинами потових залоз, волосяними фолікулами, дендритними клітинами дерми та ендотеліальними клітинами власне пластинки (lamina propria) та дерми (Steinhoff et al., 1999; Santulli et al., 1995). Меланоцити не експресують цей рецептор (Seiberg et al., 2000), хоча PAR-2 відіграє важливу роль у пігментації, сприяючи перенесенню меланіну з меланоцитів у кератиноцити (Sharlow et al., 2000). Серинові протеази, генеровані епідермісом, чинять хемотактичні ефекти, індукуючи рекрутинг лейкоцитів у шкірі. Вони також беруть участь в регуляції гомеостазу, мітогенезу та диференціації епідермісу і модулюють бар'єрну функцію шкіри. Крім того, серинові протеази беруть участь у фізіопатології шкірних хвороб, пов'язаних із запаленням, імунним захистом організму, канцерогенезом, фіброзом і стимуляцією нервів. Передбачається, що вплив серинових протеаз на фізіологічні та фізіопатологічні властивості шкіри почасти пов'язаний з PAR-рецепторами. Дійсно, рецептори PAR-2 гіперекспресовані в епідермісі, дермі та судинах при запальних за ED50 107 62
ДивитисяДодаткова інформація
Назва патенту англійськоюUnsaturated fatty hydroxy acid derivatives and the dermocosmetologic use thereof
Автори англійськоюCharveron Marie, Tarroux Roger, Bordat Pascal
Назва патенту російськоюПроизводные ненасыщенной жирной оксикислоты и их дермакосметологическое применение
Автори російськоюШарверон Мари, Тарру Роже, Борда Паскаль
МПК / Мітки
МПК: A61K 31/20, A61Q 19/08, C07C 59/42, A61Q 19/02, A61P 17/00
Мітки: похідні, дермакосметологічне, ненасиченої, застосування, жирної, оксикислоти
Код посилання
<a href="https://ua.patents.su/16-96429-pokhidni-nenasicheno-zhirno-oksikisloti-ta-kh-dermakosmetologichne-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Похідні ненасиченої жирної оксикислоти та їх дермакосметологічне застосування</a>
Попередній патент: Спосіб реєстрації швидких нейтронів
Наступний патент: Тканина з утоковим дротом
Випадковий патент: Спосіб визначення больової чутливості при дезадаптації до знімних зубних протезів












