Спосіб пригнічення росту небажаної рослинності, заміщені гетероциклами піридини, cпособи їх одержання та гербіцидна композиція
Формула / Реферат
1. Способ подавления роста нежелательных растений в очаге поражения путем обработки очага поражения эффективным количеством 2,6-замещенного пиридина, отличающийся тем, что в качестве 2,6-замещенного пиридина используют соединение формулы I:
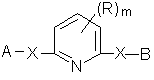 , (І)
, (І)
где Х обозначает атом кислорода;
А обозначает необязательно замещенную атомом галогена, С1-6-алкилом или галоген-C1-6-алкилом пиридильную или пиразолильную группу;
В обозначает пяти- или шестичленную циклическую углеводородную группу; С1-6-алкильную; С3-6-алкинильную; фенильную или фенил-С1-2-алкильную группу, необязательно замещенные атомами галогена, С1-6-алкилом, галоген-С1-6-алкилом, СN или NO2; или В является одним из значений, приведенных для А;
R означает атом галогена или C1-6-алкильную группу;
m равно 0 или 1.
2. Способ по п. 1, отличающийся тем, что В означает фенильную, бензильную, пиридильную или пиразолильную группу, необязательно замещенные атомом галогена, или С1-6-алкилом, или галоген-С1-6-алкилом.
3. Способ по пп. 1 или 2, отличающийся тем, что каждая из групп А или В имеет заместитель в положении 3, если это возможно, за исключением случая, когда В означает фенил-С1-2-алкил.
4. Способ по п. 3, отличающийся тем, что каждая из групп А и В замещены атомом хлора, метильной группой и/или трифторметильной группой.
5. Способ по п. 4, отличающийся тем, что А означает 2-хлорпирид-4-ильную или 1-метил-З-трифторметилпиразол-5-ильную группу, а В означает 3-трифторметилфенильную или бензильную группу или же имеет одно из значений, указанных для А.
6. Способ по любому из пп. 1-5, отличающийся тем, что m = 0.
7. Способ по п.1, где в соединении формулы I m = 0, а АХ и ВХ имеют следующие пары значений:
АХ ВХ
2'-хлорпирид-4'-илокси
2"-хлорпирид-4"-илокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-трифторметилфенокси
2'-хлорпирид-4'-илокси
6-бензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
6-бензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
1"-метил-3"-трифторметилпиразол-5"-илокси
2'-хлорпирид-4'-илокси
3"-трифторметилфенокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2"-хлорпирид-4"-илокси
пирид-2'-илокси
фенокси
1'-метил-3'-трифторметилпиразол-5'-илокси
фенокси
1'-метил-3'-трифторметилпиразол-5'-илокси
циклопентилокси
2'-хлорпирид-4'-илокси
фенилокси
2'-хлорпирид-4'-илокси
3"-трифторметил-4"-фторфенилокси
2'-хлорпирид-4'-илокси
2"-фторфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
4"-фторфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2"-фторфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2",4"-дифторфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2"-метилфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2"-пиридилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-хлорпирид-5"-илокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2"-хлорпирид-6"-илокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-фторфенилoкси
1'-метил-3'-метилпиразол-5'-илокси
3"-трифторметил-4"-фторфенилокси
1'-метил-3'-метилпиразол-5'-илокси
1"-метил-3"-метилпиразол-5"-илокси
1'-метил-3'-трифторметилпиразол-5'-илокси
1"-метил-3"-метилпиразол-5"-илокси
1'-метил-3'-т-бутилпиразол-5'-илокси
1"-метил-3"-метилпиразол-5"-илокси
1'-метил-3'-т-бутилпиразол-5'-илокси
1"-метил-3"-изопропилпиразол-5"-илокси
1'-метил-3'-трифторметилпиразол-5'-илокси
1"-метил-3"-т-бутилпиразол-5"-илокси
1'-метил-3'-метилпиразол-5'-илокси
1"-метил-3"-изопропилпиразол-5"-илокси
1'-метил-3'-этилпиразолил-5'-илокси
1"-метил-3"-этилпиразолил-5"-илокси
1'-метил-3'-трифторметил-1'-пиразол-5'-илокси
1"-метил-3"-изопропилпиразол-5"-илокси
1'-метил-3'-изопропилпиразол-5'-илокси
1"-метил-3"-изопропилпиразол-5"-илокси
1'-метил-3'-т-бутилпиразол-5'-илокси
1"-метил-3"-т-бутилпиразол-5"-илокси
1'-метил-3'-т-бутилпиразол-5'-илокси
2"-хлорпирид-4"-илокси
1'-метил-3'-т-бутилпиразол-5'-илокси
4"-фторфенилокси
1'-метил-3'-т-бутилпиразол-5'-илокси
3"-фторфенилокси
1'-метил-3'-т-бутилпиразол-5'-илокси
2"-фторфенилокси
2'-хлорпирид-4'-илокси
2"-метилфенилокси
2'-хлорпирид-4'-илокси
4"-фторфенилокси
2'-хлорпирид-4'-илокси
3"-фторфенилокси
3'-хлорпирид-5'-илокси
3"-хлорпирид-5"-илокси
1'-метил-3'-трифторметилпиразол-5'-илокси
З",4"-диметилфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-метил-4"-хлорфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-метил-4"-нитрофенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3",4"-дихлорфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-трифторметил-4"-фторфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-цианофенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-хлор-4"-цианофенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-хлор-4"-фторфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-фторбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
4"-фторбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2"-фторбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
4"-трифторметилбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-трифторбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
4"-метилбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2"-метилбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
4"-т-бутилбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-хлорбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-метилбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2",6"-дихлорбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
a-метилбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
4"-хлорбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2"-хлорбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2",4"-дифторбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2",4",5"-трифторбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2", 3",5"-трифторбензилокси
2'-хлорпирид-4'-илокси
4"-фторбензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
a-трифторметилбензилокси
1'-метил-3'-т-бутилпиразол-5'-илокси
2"-метилбензилокси
2'-хлорпирид-4'-илокси
2"-фторбензилокси
2'-хлорпирид-4'-илокси
3"-фторбензилокси
2'-хлорпирид-4'-илокси
2"-метилбензилокси
2'-хлорпирид-4'-илокси
2",4"-дифторбензилокси
1'-метил-3'-т-бутилпиразол-5'-илокси
4"-фторбензилокси
1'-метил-3'-т-бутилпиразол-5'-илокси
3"-фторбензилокси
1'-метил-3'-т-бутилпиразол-5'-илокси
2"-фторбензилокси
1'-метил-3'-т-бутилпиразол-5'-илокси
2",4"-дифторбензилокси
1'-метил-3'-т-бутилпиразол-5'-илокси
бензилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
1''-фенилэтилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2''-пропинилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
т-бутилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
1"-метил-3"-трифторметилпиразол-5"-илокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-фторфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2"-фторфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2",4"-дифторфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
2"-метилфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
3"-хлорпирид-5"-илокси
1'-метил-3'-трифторметилпиразол-5'-илокси
фенилокси
2'-хлорпирид-5'-илокси
фенилокси
2'-хлорпирид-5'-илокси
2"-метилфенилокси
1'-метил-3'-трифторметилпиразол-5'-илокси
бензилокси
8. Замещенные гетероциклами пиридины общей формулы I:
 ,
,
где X означает атом кислорода,
А означает пиридильную или пиразолильную группу, необязательно замещенную атомом галогена или C1-6-алкилом, или галоген-С1-6-алкилом;
В означает пяти- или шестичленную циклическую углеводородную группу, С1-6-алкильную; С3-6-алкинильную; фенильную, фенил-С1-2-алкильную, пиридильную или пиразолильную группу, необязательно замещенные атомом галогена, С1-6-алкилом или галоген-С1-6-алкилом, СN или NO2;
R - означает атом галогена или С1-6-алкил;
m равно 0 или 1.
9. Соединение по п. 8, где m, АХ и ВХ обозначают, как в любом из пп. 2 - 6.
10. Способ получения соединения по п. 8, где А и В идентичны, который включает взаимодействие 2,6-дигалогенопиридина формулы II:
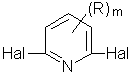
по меньшей мере с двукратным молярным избытком соли металла со спиртом формулы АХН, причем значения R, А, Х и m определены в п. 1 и Hal означает атом галогена.
11. Способ по п. 10, в котором реакцию проводят в полярном органическом растворителе.
12. Способ по пп. 10 или 11, в котором соль спирта со щелочным металлом взаимодействует с дигалогенопиридином при повышенной температуре.
13. Способ получения соединения по п. 8, где группа В отличается от группы А, который включает взаимодействие 2,6-дигалогенопиридина формулы II с не более чем эквимолярным количеством соли металла со спиртом формулы АХН, с последующим взаимодействием с по меньшей мере эквимолярным количеством соли металла со спиртом формулы ВХН.
14. Способ по п. 13, в котором реакцию проводят в полярном органическом растворителе.
15. Способ по пп. 13 или 14, в котором соль спирта со щелочным металлом взаимодействует с дигалогенопиридином при повышенной температуре.
16. Способ получения соединения по п. 8, где группа В отличается от группы А, который включает взаимодействие галогенопиридона формулы III:
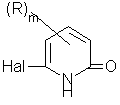
с гидроксидом щелочного металла, затем с галогенидом формулы BHal, где каждый Hal означает атом галогена, и, затем, взаимодействие продукта с солью металла со спиртом формулы АХН.
17. Гербицидная композиция, содержащая 2,6-замещенный пиридин, носитель и/или поверхностно-активное вещество, отличающаяся тем, что в качестве 2,6-замещенного пиридина она содержит соединение формулы І по пп. 8 или 9 в количестве 0,5-95% мас.
Текст
1 Способ подавления роста нежелательных растений в очаге поражения путем обработки очага поражения эффективным количеством 2,6замещенного пиридина, отличающийся тем, что в качестве 2,6-замещенного пиридина используют соединение формулы I ,(R)m А-Х где X обозначает атом кислорода, А обозначает необязательно замещенную атомом галогена, Сі є-алкилом или галоген-Сі є-алкилом пиридильную или пиразолильную группу, В обозначает пяти- или шестичленную циклическую углеводородную группу, Сі 6-алкильную, Сз 62'-хлорпирид-4'-илокси 1'-метил-3'-трифторметил пиразол -5'-илокси 2'-хлорпирид-4'-илокси 1'-метил-3'-трифторметил пиразол 5'-илокси 1'-метил-3'-трифторметилпира^пп 5'-илокси 2'-хлорпирид-4'-илокси 1'-метил-3'-трифторметилпир; -5'-илокси пирид-2'-илокси 1'-метил-3'-трифторметил пиразол- 5'-илокси 1'-метил-3'-трифторметил пиразол- 5'-илокси 2'-хлорпирид-4'-илокси 2'-хлорпирид-4'-илокси 2'-хлорпирид-4'-илокси 1'-метил-3'-трифторметилпиразол- 5'-илокси алкинильную, фенильную или фенил-Сі 2алкильную группу, необязательно замещенные атомами галогена, Сі є-алкилом, галоген-Сі єалкилом, CN или NO2, или В является одним из значений, приведенных для А, R означает атом галогена или Сі-є-алкильную группу, m равно 0 или 1 2 Способ по п 1, отличающийся тем, что В означает фенильную, бензильную, пиридильную или пиразолильную группу, необязательно замещенные атомом галогена, или Сі є-алкилом, или галоген-Сі 6-алкилом 3 Способ по пп 1 или 2, отличающийся тем, что каждая из групп А или В имеет заместитель в положении 3, если это возможно, за исключением случая, когда В означает фенил-Сі 2-алкил 4 Способ по п 3, отличающийся тем, что каждая из групп А и В замещены атомом хлора, метильной группой и/или трифторметильной группой 5 Способ по п 4, отличающийся тем, что А означает 2-хлорпирид-4-ильную или 1-метил-Зтрифторметилпиразол-5-ильную группу, а В означает 3-трифторметилфенильную или бензильную группу или же имеет одно из значений, указанных для А 6 Способ по любому из пп 1-5, отличающийся тем, что m = 0 7 Способ по п 1, где в соединении формулы I m = 0, а АХ и ВХ имеют следующие пары значений АХВХ 2"-хлорпирид-4"-илокси 3"-тр и фтор метил фен о кс и 6-бензилокси 6-бензилокси 1"-метил-3"-трифторметилпиразол-5"-илокси 3"-тр и фтор метил фен о кс и 2"-хлорпирид-4"-илокси фенокси фенокси циклопентилокси фенилокси 3"-трифторметил-4"-фторфенилокси 2"-фторфенилокси 4"-фторфенилокси о 00 0 0 ю 58478 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси і'-метил-З'-трифторметилпиразол-б'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-метилпиразол-5'-илокси 1'-метил-3'-метилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-т-бутилпиразол-5'-илокси 1'-метил-3'-т-бутилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-метилпиразол-5'-илокси 1'-метил-3'-этил пиразол ил-5'-илокси 1'-метил-3'-трифторметил-1'-пиразол-5'-илокси 1'-метил-3'-изопропилпиразол-5'-илокси 1'-метил-3'-т-бутилпиразол-5'-илокси 1'-метил-3'-т-бутилпиразол-5'-илокси 1'-метил-3'-т-бутилпиразол-5'-илокси 1'-метил-3'-т-бутилпиразол-5'-илокси 1'-метил-3'-т-бутилпиразол-5'-илокси 2'-хлорпирид-4'-илокси 2'-хлорпирид-4'-илокси 2'-хлорпирид-4'-илокси 3'-хлорпирид-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 2'-хлорпирид-4'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-т-бутилпиразол-5'-илокси 2'-хлорпирид-4'-илокси 2'-хлорпирид-4'-илокси 2'-хлорпирид-4'-илокси 2'-хлорпирид-4'-илокси 1'-метил-3'-т-бутилпиразол-5'-илокси 1'-метил-3'-т-бутилпиразол-5'-илокси 1'-метил-3'-т-бутилпиразол-5'-илокси 1'-метил-3'-т-бутилпиразол-5'-илокси 1'-метил-3'-т-бутилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 2"-фторфенилокси 2",4"-дифторфенилокси 2"-метилфенилокси 2"-пиридилокси 3"-хлорпирид-5"-илокси 2"-хлорпирид-6"-илокси 3"-фторфенилокси 3"-трифторметил-4"-фторфенилокси 1"-метил-3"-метилпиразол-5"-илокси 1"-метил-3"-метилпиразол-5"-илокси 1"-метил-3"-метилпиразол-5"-илокси 1"-метил-3"-изопропилпиразол-5"-илокси 1"-метил-3"-т-бутилпиразол-5"-илокси 1"-метил-3"-изопропилпиразол-5"-илокси 1 "-метил-3"-этил пиразол ил-5"-илокси 1"-метил-3"-изопропилпиразол-5"-илокси 1"-метил-3"-изопропилпиразол-5"-илокси 1"-метил-3"-т-бутилпиразол-5"-илокси 2"-хлорпирид-4"-илокси 4"-фторфенилокси 3"-фторфенилокси 2"-фторфенилокси 2"-метилфенилокси 4"-фторфенилокси 3"-фторфенилокси 3"-хлорпирид-5"-илокси 3",4"-диметилфенилокси 3"-метил-4"-хлорфенилокси 3"-метил-4"-нитрофенилокси 3",4"-дихлорфенилокси 3"-трифторметил-4"-фторфенилокси 3"-цианофенилокси 3"-хлор-4"-цианофенилокси 3"-хлор-4"-фторфенилокси 3"-фторбензилокси 4"-фторбензилокси 2"-фторбензилокси 4"-трифторметилбензилокси 3"-трифторбензилокси 4"-метилбензилокси 2"-метилбензилокси 4"-т-бутилбензилокси 3"-хлорбензилокси 3"-метилбензилокси 2"6"-дихлорбензилокси а-метилбензилокси 4"-хлорбензилокси 2"-хлорбензилокси 2",4"-дифторбензилокси 2",4",5"-трифторбензилокси 2", 3",5"-трифторбензилокси 4"-фторбензилокси а-трифторметилбензилокси 2"-метилбензилокси 2"-фторбензилокси 3"-фторбензилокси 2"-метилбензилокси 2"4"-дифторбензилокси 4"-фторбензилокси 3"-фторбензилокси 2"-фторбензилокси 2",4"-дифторбензилокси бензилокси 1 "-фенилэтилокси 2"-пропинилокси т-бутилокси 58478 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 2'-хлорпирид-5'-илокси 2'-хлорпирид-5'-илокси 1'-метил-3'-трифторметилпиразол-5'-илокси 8 Замещенные гетероциклами пиридины общей формулы І ,(R)m А-Х где Х означает атом кислорода, А означает пиридильную или пиразолильную группу, необязательно замещенную атомом галогена или Сі 6-алкилом, или галоген-Сі є-алкилом, 8 означает пяти- или шестичленную циклическую углеводородную группу, Сі 6-алкильную, Сз 6алкинильную, фенильную, фенил-Сі 2-алкильную, пиридильную или пиразолильную группу, необязательно замещенные атомом галогена, Сі єалкилом или галоген-Сі є-алкилом, CN или NO2, R - означает атом галогена или Сі є-алкил, m равно 0 или 1 9 Соединение по п 8, где т , АХ и ВХ обозначают, как в любом из пп 2 - 6 10 Способ получения соединения по п 8, где А и В идентичны, который включает взаимодействие 2,6-дигалогенопиридина формулы II ,(R)m по меньшей мере с двукратным молярным избытком соли металла со спиртом формулы АХН, причем значения R, А, X и m определены в п 1 и Hal означает атом галогена 11 Способ по п 10, в котором реакцию проводят в полярном органическом растворителе 12 Способ по пп 10 или 11, в котором соль спирта Настоящее изобретение относится к некоторым 2,6-замешенным пиридинам, способам их получения и их использованию в качестве гербицидов Пиридины и производные пиридина находят широкое применение, например, в качестве фармацевтических препаратов, пестицидов (гербицидов, акарицидов, противоглистных средств, веществ отпугивающих птиц), пищевых добавок, растворителей, реактивов, промежуточных соединений, и химических веществ для получения полимеров и в текстильной промышленности Для указанных целей были исследованы различные производные 2,6-диарилокси- или диарилметоксипиридина, причем, эти соединения часто содержали заместители в центральном пиридиновом 1"-метил-3"-трифторметилпиразол-5"-илокси 3"-фторфенилокси 2"-фторфенилокси 2",4"-дифторфенилокси 2"-метилфенилокси 3"-хлорпирид-5"-илокси фенилокси фенилокси 2"-мети л фенилокси бензилокси со щелочным металлом взаимодействует с дигалогенопиридином при повышенной температуре 13 Способ получения соединения по п 8, где группа В отличается от группы А, который включает взаимодействие 2,6-дигалогенопиридина формулы II с не более чем эквимолярным количеством соли металла со спиртом формулы АХН, с последующим взаимодействием с по меньшей мере эквимолярным количеством соли металла со спиртом формулы ВХН 14 Способ по п 13, в котором реакцию проводят в полярном органическом растворителе 15 Способ по пп 13 или 14, в котором соль спирта со щелочным металлом взаимодействует с дигалогенопиридином при повышенной температуре 16 Способ получения соединения по п 8, где группа В отличается от группы А, который включает взаимодействие галогенопиридона формулы III (R), с гидроксидом щелочного металла, затем с галогенидом формулы BHal, где каждый Hal означает атом галогена, и, затем, взаимодействие продукта с солью металла со спиртом формулы АХН 17 Гербицидная композиция, содержащая 2,6замещенный пиридин, носитель и/или поверхностно-активное вещество, отличающаяся тем, что в качестве 2,6-замещенного пиридина она содержит соединение формулы I по пп 8 или 9 в количестве 0,5-95% мае кольце Дибензилокси-аналог 2,6-дифеноксипиридина, упомянутый в публикациях JP-A-63250324, ЕР-А180188 и J Med, Chem , 10(2), рр 320-325, которые представляют собой научные публикации в области медицины, был получен в качестве примера гербицидного соединения, предложенного в патентной заявке США 3535328 и в опубликованной выделенной заявке 3687959 В обоих публикациях преимущественно раскрывается гербицидная, фунгицидная активность, а для соединений, заявленных в заявке США 3535328, нематоцидная и инсектицидная активность амидо- или аминотиоэтокси-производных Для заявленных 2,6дибензоксипиридинов не приводится данных об их гербицидной активности 58478 В рассматриваемой Европейской патентной заявке 92304795 (Т 1632 ЕРС), поданной 27 мая 1992г заявителями настоящего изобретения сообщается, что некоторые производные 2,6дифеноксипиридина и 2,6-дибензилоксипиридина, а также соответствующие асимметрические 2фенокси-6-бензилоксипиридины обладают целым спектром гербицид ной активности, значительно отличающейся от активности незамещенных аналогов тем, что указанные соединения обладают послевсходовой активностью как по отношению к травянистым растениям так и по отношению к широколиственным растениям Некоторые из этих соединений известны сами по себе, и в описании настоящего изобретения заявляется их использование в качестве гербицидов В ЕР-А-371947 раскрываются замещенные 3феноксипиразолы, которые могут быть использованы в качестве гербицидов В ЕР-А-109751 раскрываются, среди прочих, 2-замещенные фекокси-6-замещенные пиридины, которые могут быть использованы для избирательного уничтожения сорняков в присутствии культурных растений Было обнаружено, и именно это составляет сущность настоящего изобретения, что высокой гербицидной активностью обладают также новые производные пиридина, имеющие азотсодержащие гетероа ром этические заместители В одном из вариантов, настоящее изобретение относится к способу уничтожения нежелательной растительности в очаге ее произрастания, заключающемуся в обработке этого очага 2,6-замещенным пиридином формулы 1 А - X X где X обозначает атом кислорода или серы, А обозначает необязательно замещенную пяти- или шестичленную азотсодержащую гетероароматическую группу, В обозначает необязательно замещенную пяти и шестичленную циклическую углеводородную, алкильную, алкенильную, алкинильную, арильную или аралкильную группу или имеет одно из значений, приведенных для группы А, R обозначает атом галогена или алкильную группу, галогеналкильную группу, алкокси-группу, алкилтио-группу или диалкил-амино-группу, a m равно 0,1 или 2 Группа А может быть пиридилом, в частности, 4-пиридилом, или пиразолилом, в частности, 5пиразолилом, а группа В может быть одной из этих групп или же фенилом или бензилом Группы А и В могут быть одинаковыми или же различными и предпочтительно содержат заместители, в частности имеют заместители в мета-положении (за исключением случая, когда В - бензил) Заместителями могут быть любые группы, которые обычно используется для модифицирования и/или функционализации пестицидных соединений, в частности, ими могут быть заместители, которые поддерживают или усиливают гербицид ную 8 активность, проявляемую соединениями по настоящему изобретению, или же усиливают продолжительность действия пестицидов, способствуют проникновению их в почву или внутрь растений или улучшают какое-либо другое полезное свойство гербицидных соединений В каждом радикале может быть один заместитель или большее количество одинаковых или разных заместителей Необязательными заместителями в группах А и/или В являются атомы галогенов или нитрогруппа, циано-группа, алкильная группа, галогеналкильная группа, алкокси-группа, алкил-тиогруппа и арильная группа Предпочтительными заместителями являются атом галогена, в частности, атом хлора или алкильная или галогеналкильная группа, содержащая от 1 до 6 атомов углерода Алкильная группа, которая служит заместителем в одной или другой из групп А и В или же представляет собой группу R, может иметь прямую или разветвленную цепь, обычно содержащую до 12г предпочтительно от 1 до 6, атомов углерода В галогеналкильной группе, которая служит заместителем в той или другой из групп А и В или же является группой R, атом галогена может представлять собой один или большее количество атомов фтора, хлора, брома или иода, при этом атом фтора является предпочтительным, а трифторметил является предпочтительной галогеналкильной группой Предпочтительными являются соединения, в которых каждый X обозначает атом кислорода, а m равно 0 или 1 Настоящее изобретение также относится к соединению формулы 1, определенному выше, при условии, что соединением формулы 1 не является 2,6-бис[(6-бром-2-пиридинил)тио]пиридин, 2,2'тиобис[6-[(6-бром-2-пиридинил)тио]пиридин, 2,6бис[[(6-бром-2-пиридинил)тио]-2пиридинил]тио]пиридин, 2,2'-тиобис[6-[[6-[(6-бром2-пиридинил)тио]-2-пиридинил]тио]пиридин, 2метокси-6-[(1-метил-1Н-1,2,4-триазол-3ил)тио]пиридин, 2-[[4-(2-хлорфенил)тио]-1,3диметил-1Н-пиразол-5-ил]окси]-6-метоксипиридин, 4-[[[[[1,3-диметил-5-[[6-(метилтио)-2пиридинил]окси]-1 Н-пиразол-4ил]метилен]амино]окси]метил]бензойной кислоты 1,1-диметилэтиловый сложный эфир, 1,3-диметил5-[[6-(метилтио)-2-пиридинил]окси]-1Н-пиразол-4карбоксальдегид, 2-метокси-6-(1 Н-1,2,4-триазол-Зилтио)пиридин, 2-мето кс и-6-(2тиазолилтио)пиридин, 2,6-бис[(1-метил-1Нимидазол-2-ил)тио]пиридина дигидрохлорид или 3-[2-бром-2-[4-(хлорметил)-3метоксифенил]этенил]-2,2диметилциклопропанкарбоновой кислоты 1-[6-[(6метокси-2-пиридинил)окси]-2-пиридинил]этиловый эфир Соединения формулы 1, где X обозначает атом кислорода, могут быть получены при использовании соответствующим образом модифицированных обычных методов получения замещенных производных пиридина, при этом основная методика включает, например, взаимодействие соли металла подходящего спирта с соответствующим 58478 2,6-галогенпиридином в растворителе преимущественно при повышенной температуре, идеально при кипячении Для получения симметричных производных пиридина реакцию можно проводить в одну стадию, применяя молярное отношение алкоголята к пиридину, равное по крайней мере 2 1 Для несимметричных соединений формулы 1 необходимо использовать двухстадииныи процесс и разные методики введения двух заместителей В другом варианте, настоящее изобретение относится к способу получения соединения формулы 1, где А и В совпадают, который заключается во взаимодействии 2,6-дигалогенпиридина общей формулы 11 (П) с по крайней мере двойным молярным избытком металлической соли спирта или меркаптана формулы, АХН, где символы А, X, R и m имеют то же значение, что и формуле 1, a Hal обозначает атом галогена, предпочтительно атом хлора или брома В том случае, если группа В в формуле 1 отлична от группы А, то 2,6-дигалогенпиридин формулы 11, приведенный выше, вначале вступает во взаимодействие не более, чем с эквимолярным количеством металлической соли спирта или меркаптана формулы, АХН, а затем с по крайней мере эквимолярным количеством металлической соли спирта или меркаптана формулы, ВХН В качестве альтернативы, предпочтительный способ получения соединения формулы 1, где В отличен от А, включает взаимодействие галогенпиридона формула 111 Ш) с галогенпроизводным формулы, BHal, где каждый Hal обозначает атом галогена, преимущественно атом брома, с последующим взаимодействием с металлической солью спирта или меркаптана формулы, АХН Первую стадию этого процесса удобно проводить по реакции пиридона формулы 111с гидроксидом щелочного металла с образованием пиридоксилатной соли, которая затем реагирует с галогенпроизводным BHal, предпочтительно в растворителе, таком как диметилформамид Любая из указанных выше реакций предпочтительно проводится в органическом растворителе, выбор которого зависит от конкретной природы применяемых реагентов В общем случае подходит любой полярный растворитель, например, диметилформамид и тетрагидрофуран Металлической солью спирта или меркаптана преимущественно является соль щелочного металла, например, соль натрия или калия, которую предпочтительно получают по реакции спирта с подходящим основанием металла, например, кар 10 бонатом или гидридом металла Полученные соединения формулы 1 могут быть, в случае необходимости, выделены и очищены известными способами Соединения общей формулы 11 и спирты/меркаптаны формулы ВХН, как правило, известны и/или легко получаются стандартными способами Было обнаружено, что соединения формулы 1 проявляют интересную активность при использовании в качестве гербицидов, обладающих широким спектром действия по отношению к нежелательным биологическим видам до того, как появились их всходы, так и после их появления Таким образом, в настоящем изобретении заявляется гербицидная композиция, которая содержит соединение по настоящему изобретению вместе с носителем Настоящее изобретение включает также получение указанных гербицидных композиций путем смешения носителя с соединением по настоящему изобретению Композиция по настоящему изобретению содержит по крайней мере два носителя, по меньшей мере, один из которых является поверхностно-активным соединением В настоящем изобретении заявляется использование соединения по настоящему изобретению в качестве гербицида Далее, в соответствии с настоящим изобретением заявляется способ угнетения роста растения в пораженном месте путем внесения в очаг поражения композиции или соединения настоящего изобретения Очаг поражения может быть почвой или растениями на поле Обработку очага поражения можно проводить как до, так и после появления сорняков Применяемая доза активного ингредиента может, например, составлять от 0,01 до 10кг/га, преимущественно 9 от 0,01 до 4кг/га Носителем в композиции по настоящему изобретению может быть любое вещество, которое можно смешать с активным ингредиентом, с целью облегчить нанесение композиции на обрабатываемый очаг поражения, которым может быть, например, растение, семя или почва, или с целью улучшить хранение, транспортировку или переработку Носитель может быть твердым или жидким, в том числе веществом, которое при обычных условиях является газом, но может быть сжато так, что образует жидкость, и для формирования композиции могут использоваться любые носители, которые обычно применяются для создания гербицидной композиции Композиции по настоящему изобретению преимущественно содержат от 0,5 до 95% вес активного ингредиента Подходящие твердые носители включают природные и синтетические глины и силикаты, например, природные кремнеземы, такие как диатомитовые земли, силикаты магния, например, тальк, алюмосиликаты магния, например, аттапульгиты и вермикулиты, алюмосиликаты, например, каолиниты, монтмориллониты и слюда, карбонат кальция, сульфат кальция, сульфат аммония, синтетические гидратированные оксиды кремния и синтетические силикаты кальция или алюминия, элементы, например, углерод или се 12 11 58478 pa, натуральные или синтетические смолы, набыла подтверждена методами масспример, кумаронозые смолы, поливинилхлорид и спектрометрии и ядерного магнитного резонанса полимеры и сополимеры стирола, твердые полиПример 1 хлорфенолы, битумы, воски и твердые удобрения, Получение 2,6-ди(2'-хлорпирид-4'например, суперфосфаты илокси)пиридина Подходящими жидкими носителями являются Смесь 11,8г 2,6-дибромпиридина, 13г 2-хлорвода, спирты, например, изо-пропанол или глико4-гидроксипиридина и 13,8г карбоната калия в ли, кетоны, например, ацетон, метилэтилкетон, 20мл N.N-диметилформамида кипятят с обратным метилизобутилкетон и циклогексанон, эфир, арохолодильником в течение 12час Охлаждают, приматические или арилифатические углеводороды, бавляют 150мл воды и водный слой трижды по например, бензол/ толуол и ксилол, фракции пе100мл экстрагируют этилацетатом Органические регонки нефти, например, керосин и легкие миневытяжки объединяют и сушат над безводным ральные масла, хлорированные углеводороды, сульфатом магния Растворитель упаривают и например, четыреххлористый углерода, перхлорэоставшееся коричневое масло очищают испаритилен и трихлорэтан Часто более удобными явтельной колоночной хроматографией на силикаляются смеси различных жидкостей геле, элюируя смесью гексан/эти л ацетат (7/3) Целевое соединение получают в виде твердого Композиции, которые используются в сельвещества светло-коричневого цвета с т пл 95°С ском хозяйстве, обычно составляются и транспортируются в концентрированной форме и затем Элементный анализ разбавляются пользователем перед употреблением Присутствие небольшого количества носитевычислено С 53,9, Н 2,7, N 12,6%, ля, который является поверхностно-активным венайдено С 53,7, N 12,4% ществом, облегчает указанный процесс разбавления Поэтому, по крайней мере, один Пример 2 носитель в композиции по настоящему изобретеА) Получение 2-бром-6-(1 '-метил-3'нию является поверхностно-активным веществом трифторметилпиразол-5'-илокси)пиридина Например, композиция, может содержать, по Смесь 14,Зг 2,6-дибромпиридина, Юг 1-метилкрайней мере, два носителя, по меньшей мере, З-трифторметил-5-гидроксипиразола и 8,3г карбоодин из которых является поверхностно-активным ната калия в 20мл N.N-диметилформамида кипявеществом тят с обратным холодильником в течение 4час Поверхностно-активным веществом может Дают смеси остыть до комнатной температуры, быть эмульгатор, диспергатор или смачивающее прибавляют 150мл воды и водный слой трижды по средство, оно может быть неионогенным или ио100мл экстрагируют этилацетатом Органические ногенным Примеры подходящих поверхностновытяжки объединяют, сушат над безводным активных веществ включают натриевые или кальсульфатом магния и растворитель упаривают в циевые соли полиакриловой кислоты и лигнинвакууме Очищают 2-бром-6-(1'-метил-3'сульфоновых кислот, продукты конденсации жиртрифторметилпиразол-5-илокси)пиридин испариных кислот, или алифатических аминов, или тельной колоночной хроматографией на силикаамидов, содержащих, по крайней мере, 12 атомов геле, элюируя смесью гексан/эти л ацетат (8/2) и углерода в молекуле, с оксидом этилена и/или получают твердое вещество с т пл 53°С оксидом пропилена, сложные эфиры жирных киБ) Получение 2-(1'-метил-3'слот и глицерина, сорбита, сахарозы или пентатрифторметилпиразол-5'-илокси)-6-(3"эритритолэ, продукты конденсации указанных сотрифторметилфенокси)пиридина единений с оксидом этилена и оксидом 1,6г монозамещенного промежуточного сопропилена, продукты конденсации жирного спирта единения, полученного выше, 0,6мл 3или алкилфенола, например, п-октилфенола или гидроксибензолтрифторида и 0,7г карбоната каоктилкрезола с оксидом этилена и/или оксидом лия смешивают с 2мл N.N-диметилформамида и пропилена, сульфаты или сульфонаты указанных кипятят с обратным холодильником в течение продуктов конденсации, соли щелочных или ще12час Охлаждают, прибавляют 50мл воды и водлочноземельных металлов, преимущественно ный слой трижды по 50мл экстрагируют этилацесоли натрия, с эфирами серной или сульфоновой татом Органические вытяжки объединяют и сушат кислот, содержащими в молекуле, по крайней менад безводным сульфатом магния, растворитель ре, 10 атомов углерода, например, лаурилсульфаупаривают и сырой продукт очищают испарительты натрия, вторичные алкилсульфаты натрия, ной колоночной хроматографмией на силикагеле, натриевые соли сульфонилированного касторовоэлюируя смесью гексан/эти л ацетат (9/1) Целевое го масла и алкиларилсульфонаты натрия, такие соединение получают в виде масла бледнокак додецилбензилсульфонат, и полимеры оксида желтого цвета этилена и сополимеры оксида этилена и оксида Элементный анализ пропилена Гербицидные композиции по настоящему изобретению могут также содержать другие биологически активные ингредиенты, например, вычислено С 50,6, Н2,7, N 10,4%, соединения, обладающие гербицидной, инсектинайдено С 50,8, Н2,7, N 10,6%, цидной или фунгицидной активностью Пример 3 Изобретение поясняется следующими примеА) Получение 2-бром-6-бензилоксипиридина рами Структура полученных соединений по изо2,9мл бензилового спирта растворяют в 10мл бретению, полученных в указанных примерах, N.N-диметилформамида и медленно добавляют нз,о, 13 58478 0,7г гидрида натрия (чистота 95%) После того, как выделение газа прекратится, добавляют 6г 2,6дибромпиридина и смесь кипятят с обратным холодильником в течение Зчас Охлаждают, отфильтровывают через колонку с силикагелем, элюируя смесью гексан/эти л ацетат 1/1 Растворитель удаляют в вакууме и сырой продукт очищают испарительной колоночной хроматографией на силикагеле Целевое соединение получают в виде бесцветного масла Б) Получение 2-бром-6-(4'фторбензилокси)пиридина (альтернативный способ получения) Получают раствор 4,6г б-бром-2-пиридона (синтез этого соединения описан в Synthesis 707 (1974)) и 1,56г гидроксида калия в 20мл метанола Растворитель упаривают в вакууме, добавляют толуол и получают безводный пиридоксилат калия Его растворяют в 10мл N,Nдиметилформамида, добавляют 3,7мл 4фторбензилбромида и кипятят смесь с обратным холодильником в течение 2час После охлаждения добавляют 100мл воды и водный слой трижды экстрагируют этилацетатом Органические вытяжки объединяют, сушат над безводным сульфатом магния и растворитель удаляют в вакууме Остаток очищают испарительной колоночной хроматографией на силикагеле, элюируя смесью гексан/эти л ацетат (95/5) Целевое соединение получают в виде твердого вещества белого цвета (3,3г, 4 4 % ) с т п л 82°С В) Получение 2-(2'-хлорпирид-4'-илокси)-6бензилоксипиридина К раствору 0,65г 2-хлор-4-гидроксипиридина в 10мл N.N-диметилформамида медленно добавляют 0,1 Зг гидрида натрия После того, как выделение газа прекратится, добавляют 1,2г 2-бром-6бензилоксипиридина (получают на стадии А) и смесь кипятят с обратным холодильником в течение ЗОчас Охлаждают, отфильтровывают через колонку с силикагелем, элюируя смесью гексан/эти л ацетат (4/1) Растворитель удаляют в вакууме и сырой продукт очищают испарительной колоночной хроматографией на силикагеле, элюируя смесью гексан/эти л ацетат (9/1) Целевое соединение получают в виде желтого масла 14 їїри~ •тер А Темпера і у В ппав і 2 3 4 ЗлЗИІШТРЬЙ 3,іма 71 23 -ид •"ил-4 -фторфе 2 -ФторФенилок- 79 32 іиразоя-S• «икиопечтил Выход охси ниокси 19 2'-хлоргщрид~4'~ -ил 20 никокси 21 2'-хлорпирид-4'» 17 18 58478 Продолжение таблицы 113. Іримєр 1 '-метил-3 ' - ^^л" 4 ~фторф£нядо£Св 95 25 і'-метил-З'-Трй 2 -фторфениаокси 104 1 -иетил-3 -пи фторметилпиразол л-5-йлокси 1'-иетия~3'-Сі^ -пиразол-5'илокси .пл. Выхоз (°С) U) разол-5 -ипокси 2 4 -вифтоофеки ;• -лиразоя-5'нлокси 9S 58 1 -мэтил~3 -метил вуэилпкразол-5' локси гшразоя~5~илакеи -пиразоп-5' 1'-метил-3'-трет2 -метилфторфеяи изспо азо-просидпиразол-5 -клокей 1'-яетил-3'-^пи5' -нлоксн 1'-метил-3'-С^ 3 -хпорпиркп масло 42 85 масло 36 масло 18 1 -метил-3 -изопропилпнразол-ї илакси 32 5 -илокси і'-метил-З'-зтил і'-метил-З'-^І^" 2 -кяорпирнд-б -пярззол-S'-ялокси -йяокси 1'-метил-3'~£р*~ 3 -фторфеаилокск иас^з 27 І ~иетия~3 -этил пиразол~5'-илоксй -ЙІ1ОКОЙ пиразол-5 -влояся 1'-метил~3'-гриф 66 1 -.четил-3 -изо тор«етикг.нразол пропилпираэол~5 -5 ' -І1КОКСЕ -ИЛОКСИ 1'-метил-3'-йэс 1'~метнл~3'-изо Пропизширазол пропилпяразол-5 2Ї 5'-ялоксн -клоксн 4! 1'-иетиа-3-тратбутиягифазол-5'илокса 1'-метил'3'~ трет-йутклпиразол-5'-илокс5і 39 3'-трифтор«етил4 -фторфенилокси 1'-м.еткл-3'-мє І-МЄТНЛ-З-МЄ'ЇЙЛ тилпираэол-5'илокси пиразо#-5-клоксн иаспо масло масло 42 5 яяокси 1'-катил~3'-ие~ т»дпнразоя-5'илокск масло зол-5 -няоксії пнразол~5'-илоксн 135 90 трет-бутил пира 1'-метил-3'-метил 2 -пйрияилокси масло 1 -иетил-3 фгорметшширааол илокси -пиразол-5' 1 -кетнл-з" кпокск 40 лояси 1'-кетил-3'-C'PV" -пирааол-5'нлокск маспо 50 йяокси йутиипиразол-5'і'-иетил-З'-СР^ 73 -5'-ялокси 54 1 '-иетил-З'-тре-с і'-иеїнл-З'-Cf^ 35 масло 44 масло 33 19 58478 nocEcjiKeFve таблицы Ірииер 41 Т пл 1 '-четил-3'-трат 2 -хлоспирил-ч 6^т^лплраэот-5' 20 Ilia чато Вь; ;од нта^си 73 Гричер иіокси 42 * 1'-метил~3'-трат 4 -фторфенилоксн іасло 82 э7 43 1' -иетил-3' -трет 3 -фторфемлочсі иасло І'-МЄТИГ-З'-МЄТЙЛ 3 -фторбензи— глоаэол-5'-илочсн оксн 58 і'-метиі-З'-С^ ИЛОКСЙ 2 -фторфенилотси иасо 59 -пиоазоі-S' 2'-хлоспирид-4' 2 -четялфенил 4 -фторфенкл ияочси касло J2 33 масло часло 43 35 масло в-асло 38 И-ІОКСИ окси Зо 60 47 маяло окси OSCH 2'-хлорпирна~4'~ 46 44 2'-^орбачзил 1- -МЄ™ІІ—3' -CF, илокси ІЇДОКСИ stecio 4 -Ф^орбенз/і 53 бутиіпиразол-5' 45 скс/ -ггаразол-5' 1 '-четил-З'-трет 53 82 бутялпиразол-5' 44 иесіо 2'-хлорпирид-4'«лссси і 3 -фторфааидокси 4 -то^фтор^е -пкпазол-ї'игскси 6І 1 '-ке™иг-3'-СРт тм 1'-че'ня-3'-С!ч~ = 3 -тодфторче екз идокси ило^си илоксн 5 2 і ' - м е ' и л ~ 3 -СР 1'-мет^л-З'-С1^" 49 -пиоазол-5• -1 ' 4 -ішмети-г 88 70 50 нло^ск S3 і'-четлл-З'-С ^ 3'-M9THa-4 - х л о р -гшразол-5-игоксд 52 ФЄ^ЙЛОКС^ 1 '-•-іетиі-З'-СРд а пиоазол-5' 4А і'-четИЛ-З'-С'Г, 2'-че^илбегізл -пиаазол-5' час-о 39 ло^ск '5 Прододдввкв - а э л ^ ы Ш я , 3 -Ї!СТИТ~4 - к и т (%) 1 -мєтил-3' £4 іОЗ 55 4 -трет-бутич часло З C R - г и р а з о я - 5 ' - бензилочси рофеяяяоксл игокси илокси 52 1г-іа'/л-3'-О^ 1іЛОХС (°С) 51 3 окси фечи'окси илохси 1 J 4 '-^е-гиібечч.-л- м а с і с -пираэол-5 „ , З ,А -дихлоофене 65 92 1'-НВТЙЛ-3'~ 3 -ялорбекзидок -асло 3d масло 4І 27 3 -Cft; ітиоазол- сн нло^ои 53 1'-мвТ4Л-3'-СЯ, -пнразол-5' „ 3 -триф^оаматиг и 4 -клоофечило^ск 70 S3 56 3 -"ішанофвгіия 91 7„ 35 16 • Сг, • пира 1'-мвтит-З'-ІТ,- п н р а з о л - 5 ' З'-четитбеїїЗі'локсд зо-т-S -иаокси ЙЛОЕСИ 54 1 '-чйтіп-3' ~СР* пира эллокси O S C H илоксн ел 55 l ' - м е т н я - З ~CPS~ 3 -хлор-4 -ииа _„ - C f j - пира илоксн 56 l'-четял-З ~СР 3 -пнразол-5 3 -хаоз-4 -фтор 7о 65 фенилпжеи 69 ^оьси І'-І-ЄЇИЛ-З' 4 -хяорбензлюкси масла ,, ttJ зол-3'-илокси ПО Примеры 57-85 МеТОДИКаМ, анаЛОГИЧНЫМ -,. Приведенным примерам 17-48, получают соединения общей формулы XX, Приведенные В Т а б Л И Ц е Ш Ь і .„„,„„•, г"-хгообегізило'с-п ^оазоі-5'- сд часпо 57 ",4'-м4« Р ве Ч а Л - часю 20 CFi 71 -ллсъсу 1-ии„-Э 2 21 58478 Продолжение і а б л и і Ш ffi Пример 72 І'-4етия-3'~ 2 ,4 ,5 - т р и ф т о р - С ^ э - пира 73 5S 20 55 25 бензилокси 1'~неіил-3' 2 , 3 , 4 -трифторбен - CFj - пира зилокси зол-5'-илокси 74 2 ' -хяорпирия- -ї-фторбейзилоксй масло S 75 57 масло 51 масло 27 масло 55 2'-хяорпириа~ 2 -мйтилбензилагси масло 52 З'-клорпирид масло 34 4-ияокси 75 1'-метил-3' альфа-трифтормегил -СТ. бевзилокся пира І'-ивтил-З' 2 -меїйлбейзияокси тревб^тняпиразол-5'-ялок 77 2'-хаорпирид- 2 -фїорбензялокси 4-ияокси 78 2'-хлорпир*ш- 3 -фторбевэилокси 4'-илокси 73 80 4--ЙЯ0К0И 2 ,4 - д и ф і о р б е а з и ПОКСИ Пример 82 1'-иетил-З1 4 -фторбензия трет-бутнлпи 81 огсм S3 1'-МЄТНЛ-3' 3 -фторбвнзилок трет-бутилгіи масло 33 масло 43 61 50 масло 22 си 1'~мвтил-3' 2'-фторбензилок тре^бутилпира си зол-5'~клокси 84 і'-иетял-З' 2 ,4 -дкф-гораен трет-бутилпк ЗИІІОЕСЙ оазол-5'-илок 85 і'-иетия-З' бензилокси часло 29 треs*утилпиразоя~5'-иаожси Примеры 86-88 По методике, аналогичной приведенной в примере 17, получают соединения общей форму 22 23 58478 метил-6-гидроксипиридин(20г, 56%) в виде бесцветных кристаллов с т пл 152°С Полученное вещество смешивают с 24г фосфорилбромида в 100мл бромоформа и кипятят с обратным холодильником в течение Зчас После охлаждения реакционную смесь осторожно гидролизуют 50%-ным водным раствором гидроксида натрия и дважды экстрагируют по 100мл дихлорметаном Растворитель удаляют в вакууме и сырой продукт очищают испарительной колоночной хроматографией на силикагеле, элюируя смесью гексан/эти л ацетат (7/3), 2,6-дибром-4метилпиридин (6,9г, 25%) получают в виде бесцветного твердого вещества с т пл 77°С Примеры 90-99 Последовательными превращениями с использованием методик, приведенных в примерах 9-17 для 2,6-дибром-4-метил пиридина (синтез описан в примере 89), получают соединения общей формулы XX Они приведены в таблице 1У 24 Продолжение таблицы ІУ Пример (°С) () % фе яйл око и уасло 37 Фенилоксн масл 17 2 '-хлорпирип--4' 2 -метилі час л о ИІЇОКСИ НЯЛО5СИ і'-метиг-:І'-С (CL 3 7 0 0 2 9 ) бензклокси -пиразол-5' илокся 37 2 '-клорпирид-4' ;сЬ 370030) илокси 98 iCL 370031! 99 (Wl.396406) час до 66 -яиразол-5 , ипомеи Таблица Анализы 1У сн. Пример ^ (1 С(%) с ааикало лако найяеао вычис- найдено лено 1 53,9 53,? 2, 7 3,0 12, 6 12,4 2А 37,3 36,3 2, 2 2,0 13, 0 13,2 2В 50,6 5о,а 2, 7 2,7 10, 4 10,6 ЗА 54,6 54,7 3, 8 3,6 5, 3 5,3 ЗВ 51,1 51,1 3, 2 3 Д 5, 0 4,S зс 55,3 65,2 4, 2 3,9 5, 0 9,1 • Пример Т.ПЯ. (°С) 90 (WL 39640?) l'-метлл-З' (CL 37OQ22S) (%) І'-МЙТИЛ-З' -CFS- пиразол -CfJ-пиразол - 5 '-ИГОКСИ 90 ВеїХОЯ 5 '-ііЛОКСИ 1'-мет•ил-3' 3 -фторфевйл - С Р 5 -пира Примеры 4-а (СЬ37ОО223! 1'-иетил-З'-CFS -пира (CL370O24) 1 ' - И Є 'Е И Я - 3 ' -ся, пира а тайгице 1 4 2 , і. - д и ф т о р З34 21 3,7 12 ,0 11,9 44,3 2, 7 2,3 17 ,2 16,7 55,7 55,7 2, 7 2,5 7 ,6 7,3 43,6 48,7 2, 7 2,8 15 ,1 14,9 3 64,3 Пвимео іі 64,2 3, 7 3,7 9 ,4 9,2 46,0 си 4, 0 6 6Ї 53,0 44,2 7 2 -фторфеаилс_ £ MZIMI В растений Bg nO U И ... &Е> & 5 4 2 8 5 8 8 8 6 4 О 6 4 4 8 8 4 1 6 Ь Доза Распыление кг/га 2 0 7 2 7 8 8 6 2 О 5 О 2 7 8 2 5 1 6 6 5 4 8 7 8 6 6 8 9 8 5 8 9 8 6 5 9 7 7 8 9 6 2 2 8 6 7 8 8 5 6 Соединение по примеру № н 4 7 х 4 х 7 6 9 х 2 н 5 7 1 8 7 8 9 9 8 6 6 9 7 7 9 9 7 6 6 7 6 8 9 9 8 6 5 9 6 7 9 9 6 7 3 9 9 8 7 7 3 8 9 9 9 8 8 9 9 8 6 5 9 8 8 9 9 7 6 5 4 2 9 9 7 7 9 9 8 8 3 9 7 6 б О Смачивание почвы 1 0 к г / г а 8 7 8 7 6 8 5 1 хх 5 6 7 6 5 8 8 7 7 8 8 8 8 9 8 8 В 5 7 5 8 7 8 8 9 7 1 7 8 7 7 1 н 7 5 1 S Доза 7 5 8 7 8 8 9 6 Продолжение таблицы У 4 Распыление н а л и с т в у 7 8 4 5 7 6 2 2 2 5 1 2 4 5 О До п о я в л е н и я растений к г / г а M Е z 7 7 7 8 О В& О 8 О Ь М £В 7 8 8 4 О О 4 З О 5 1 7 6 6 8 5 8 M Е z В4 8 7 9 9 8 5 7 7 9 9 8 4 6 8 2 8 0 О L М ^В 0 6 7 8 9 6 5 6 8 8 5 5 2 1 8 6 5 7 9 2 О 0 О О О О О 1 18 З 6 Mz J В ? Й О Ь. М $& S g 0 0 7 О 2 6 6 1 0 О О О О О О О 19 а а а 21 6 О 7 6 8 О О 3 8 7 О 4 5 3 0 и к м м н я к и м к м к к х х к 4 2 6 4 4 8 6 5 1 1 2 3 0 6 2 0 6 4 7 О 0 9 9 0 5 2 3 8 6 5 7 9 2 0 0 0 О О О О О О 0 7 О 2 6 6 1 О О О О О О О О 5 7 5 8 7 8 9 9 8 6 5 8 7 5 8 9 6 ? 4 8 6 8 9 9 8 6 4 8 6 4 7 9 5 6 5 О 0 0 0 О 8 6 3 0 0 0 О О О О О 1 57 О 4 О а х 1 5 О к 1 20 0 0 3 к 5 1 н О О О O O G 4 O O 0 0 О О О О О 5 8 8 8 7 8 9 9 8 6 7 9 8 S 9 9 8 1 1 5 8 6 8 9 9 8 5 2 9 8 8 9 9 7 31 58478 32 Продолжение таблицы у Соедине- Смачиваниеипочвы ш 10м кг/га пне по g примеру Доза 8 8 7 ? 8 7 $ 3 й 8 8 5 8 7 8 9 9 8 б 8 9 S 8 7 6 57 Ms; 7 7 5 f! 7 7 6 9 3 7 BS 8 8 6 О 7 7 61 Э 2 4 О 3 6 О 7 4 6 2 2 8 2 8 7 З Соеяинеиие по при меру № О 6 5 7 8 8 4 Смачивание почвы 1О кг/га • 5 1 Доза кг/га 5 7 64 0 5 4 7 7 6 9 9 9 5 9 4 7 7 8 9 9 8 8 9 8 9 8 О О Б 7 Б 6 8 5 8 2 9 8 7 5 9 9 3 С - І 9 9 2 9 8 9 7 8 6 Й б Распыление на листву 5 1 1 4 8 7 7 6 7 7 8 9 8 5 О 9 5 7 7 97 4 О 9 Таблица У (продолжение) MZ 63 8 8 9 9 8 3 8 9 9 7 9 7 9 6 8 8 6 9 9 9 9 4 6 Ь 5 5 7 2 9 8 a 7 7 9 S 6 5 9 8 9 3 6 5 б 62 7 М Ь'& & 7 8 9 8 6 7 8 9 8 7 5 8 60 Ь Вё О 9 9 9 2 9 О Й 7 9 9 4 5 6 9 9 3 До появления растений 1. М 8 7 8 9 8 7 7 3 9 8 ма 6 5 К Вб о :ь м S& 5 4 9 9 8 і О О 7 2 О 7 5 2 О 0 5 О О 5 4 О іІ іі 9 9 9 7 9 6 2 0 66 8 5 7 4 5 3 7 7 9 8 О 7 6 7 7 9 8 9 7 9 7 6 2 8 7 S 6 7 9 9 8 3 9 6 4 9 9 4 6 65 2 0 7 9 9 7 0 8 5 2 9 8 0 0 0 9 8 6 5 4 3 9 8 9 2 8 0 О 69 0 0 0 0 О О 0 0 0 0 0 0 б 7 5 В 8 7 9 9 7 6 7 8 9 6 5 5 4 6 1 4 8 8 9 5 8 4 О О 0 0 S 4 0 О 7 7 О 0 0 О 8 2 67 4 5 2 >л 5 2 4 9 7 ? $ 8 4 2 О ой 0 2 о 1 4 5 9 В 7 8 7 8 9 9 8 7 6 8 9 9 7 О О О О О О О О О О о б д. о О 0 5 О О б 5 9 9 9 6 9 5 33 58478 34 Таблица у (продолжение) Смачивание почвы 10 кг/га Соединение по примеру в * • 71 1 кг/г й ВЙ О 5 70 Доза — 1 * 8 5 5 X К 54 S4 72 7 8 7 5 7 SB Mz Э4 R 7 6 5 1 ЕЙ 6 8 5 8 5 2 -13 X Я 7 До появления растений — — — • — S 3 5 73 М Распыление на листву а О 7 7 6 5 4 2 7 5 Я 7 6 8 5 8 5 1 74 8 7 8 9 9 J S K K Смачивание почвы 10 кг/га • Мк 5 Вб 0 О — 7 •••• ••• Доза к г / г • L М 8 6 5 7 7 4 7 4 9 9 7 6 7 6 9 9 9 9 9 8 6 6 5 4 8 8 9 9 4 2 Х 9 8 9 8 8 7 5 9 SB 8 8 9 8 9 9 7 Іі 9 6 £ї 8 6 5 7 6 7 4 7 5 8 9 2 М К К К *Е Я (окончание) До появления растений •• •• • ВИ О І. М Mz О Е L 5 7 6 8 8 7 9 9 8 4 3 9 7 4 8 8 3 1 90 9 Ь К K • О 6 5 Распыление на листву а ВЙ 5 3 5 8 9 8 9 8 X К 6 2 7 8 9 9 8 M — 6 5 9 Э 7 S Таблица У Соединение по приказу № Mz 8 8 9 9 8 8 7 9 9 8 8 8 5 K Н SB Й 7 7 9 9 8 5 7 9 9 8 7 6 5 1 Ь — 7 5 8 7 6 8 8 7 2 0 8 4 2 8 7 О 5 4 8 7 5 7 7 6 3 5 1 Комп'ютерна верстка О Воробей 7 8 7 8 8 9 8 4 5 3 7 8 9 9 6 6 5 8 7 7 7 9 8 3 О 8 7 7 8 9 5 7 5 7 5 8 7 8 9 8 6 5 9 8 8 9 9 7 7 9 8 6 5 9 8 8 9 9 7 Підписано до друку 05 09 2003 Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ТОВ "Міжнародний науковий комітет", вул Артема, 77, м Київ, 04050, Україна
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for growth supression of undesirable vegetation, heterocycle substituted pyridines, processes for preparation thereof and herbicidal composition
Назва патенту російськоюСпособы угнетения нежелательной растительности, замещенные гетероциклами пиридины, способы их получения и гербицидная композиция
МПК / Мітки
МПК: A01N 43/40, C07D 401/12, A01P 13/00, C07D 213/69, A01N 43/56
Мітки: заміщені, спосіб, гетероциклами, cпособи, небажаної, росту, рослинності, композиція, пригнічення, одержання, гербіцидна, піридини
Код посилання
<a href="https://ua.patents.su/17-58478-sposib-prignichennya-rostu-nebazhano-roslinnosti-zamishheni-geterociklami-piridini-cposobi-kh-oderzhannya-ta-gerbicidna-kompoziciya.html" target="_blank" rel="follow" title="База патентів України">Спосіб пригнічення росту небажаної рослинності, заміщені гетероциклами піридини, cпособи їх одержання та гербіцидна композиція</a>
Попередній патент: Спосіб одержання полівінілхлориду суспензійного марки пвх-с-89
Наступний патент: Спосіб кріплення шляхом склеювання оббивки до формованої основи, наприклад, із пінополіуретану
Випадковий патент: Кормова добавка












