Спосіб одержання складних ефірів 2,2-диметил-3-[(z)-1-пропеніл]циклопропанкарбонової кислоти та проміжні сполуки
Номер патенту: 39851
Опубліковано: 16.07.2001
Автори: КОЛЛАДАН Колетт, Бабен Дід'є, Бхатнагар Неєржа, Бріон Франсі
Формула / Реферат
1. Способ получения сложных эфиров 2,2-диметил-3-[(Z)-1-пропенил]циклопропанкарбоновой кислоты формулы (I)
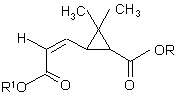 , (I)
, (I)
где R представляет собой сложноэфирный остаток, расщепляемый в нейтральной или кислой среде и являющийся линейным или разветвленным алкильным радикалом, включающим от 1 до 18 атомов углерода, возможно замещенным одним или несколькими атомами галогена, либо бензильным радикалом, возможно замещенным по вершинам ароматического кольца одним или несколькими атомами галогена, либо радикалом формулы
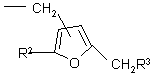 ,
,
где R2 - водород или метил;
R3 - арил;
либо радикалом формулы
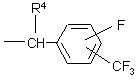 ,
,
где R4 - CN; водород;
либо радикалом формулы
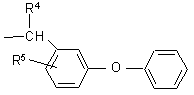 ,
,
где R4 указаны выше;
R5 - фтор или хлор, или бром, или водород;
либо радикалом формулы
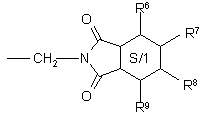 ,
,
где R6, R7, R8, R9 - водород или метил,
S/1 символизирует тетрагидроцикл,
при этом R1 является водородом или алкильным радикалом, являющимся насыщенным линейным или разветвленным и включающим от 1 до 18 атомов углерода, возможно замещенным одним или несколькими атомами галогена, в виде смеси изомеров или изомеров, разделенных на уровне циклопропанового кольца, отличающийся тем, что сложный эфир формулы (II)
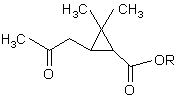 , (II)
, (II)
где R определен выше,
подвергают обработке примерно двумя эквивалентами галогенирующего средства с получением соединения формулы (III)
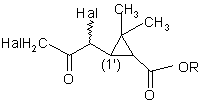 , (III)
, (III)
где R определен выше;
Hal является атомом галогена,
в виде смеси изомеров в положении (1’) атома углерода, после чего полученное соединение подвергают обработке основным средством в присутствии соединения формулы R1OH, для которого R1 определено выше, в случае необходимости в среде соответствующего сорастворителя.
2. Способ по п. 1, отличающийся тем, что в качестве галогенирующего средства используют хлорирующую или бромирующую добавку.
3. Способ по п. 2, отличающийся тем, что галогенирующее средство выбирается из группы, состоящей из бром- или хлорсодержащего соединения, являющегося N-бромсукцинимидом или N-хлорсукцинимидом, или N-хлор- или N-бромацетамидом, или пербромидом или перхлоридом пиридиния, или пербромидом или перхлоридом гидробромида, или хлоргидратом пиридиния.
4. Способ по пп. 1-3, отличающийся тем, что в качестве основного средства используют соединение, выбираемое из группы, состоящей из гидрида или алкоголята, или амида, или карбоната щелочного или щелочноземельного металла, или третичного амина.
5. Способ по пп. 1-4, отличающийся тем, что R представляет собой сложноэфирный остаток, расщепляемый в кислой или нейтральной среде и являющийся линейным или разветвленным алкильным радикалом, включающим от 1 до 18 атомов углерода и замещенным одним или несколькими атомами хлора или брома.
6. Способ по пп. 1-5, отличающийся тем, что R представляет собой алкильный радикал, включающий от 1 до 4 атомов углерода и являющийся трет.-бутилом или метилом, или этилом, замещенным одним или несколькими атомами хлора или брома, такими как бром- или хлорметил, или моно- или ди-, или трибром- или хлорэтил.
7. Способ по пп. 1-4, отличающийся тем, что R представляет сложноэфирный остаток, выбранный из группы, состоящей из бензильного радикала, замещенного от 1 до 5 атомами фтора, или радикала формулы
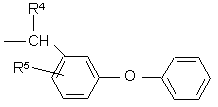 ,
,
где R4 и R5 указаны в п. 1, или радикала формулы
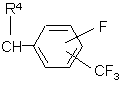 ,
,
где R4 указан в п. 1, или радикала формулы
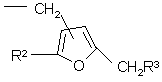 ,
,
где R2 и R3 указаны в п. 1, или радикала формулы
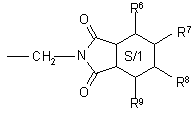 ,
,
где R6 - R9 указаны в п. 1;
символ S/1 означает тетрагидроцикл.
8. Способ по пп. 1-7, отличающийся тем, что в качестве соединения формулы R1OH используют соединение, в котором R1 представляет собой линейный или разветвленный алкильный радикал, включающий от 1 до 8 атомов углерода, такой как этильный или трет.-бутильный радикал или линейный или разветвленный алкильный радикал, включающий от 1 до 8 атомов углерода, замещенный одним или несколькими атомами фтора.
9. Способ по пп. 1-4, 7, 8, отличающийся тем, что используют соединение формулы II со структурой (1R, цис), в которой R представляет собой остаток (R, S) или (S)-a-цианофеноксибензилового спирта, или остаток (R, S) или (S)-a-циано-4-фтор-3-феноксибензилового спирта, и соединение формулы R1OH, где R1 - метильный или этильный, или 1,1,1,3,3,3-гексафторпропильный, или трет.-бутильный радикал.
10. Соединения формулы (I)
 , (I)
, (I)
где R - метил, замещенный хлором или бромом, или этил, замещенный 1 или 2, или 3 атомами хлора или брома,
R1 - водород либо алкильный радикал, являющийся насыщенным линейным или разветвленным радикалом и включающим от 1 до 18 атомов углерода, возможно замещенным одним или несколькими атомами галогена.
11. Соединения формулы (III)
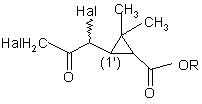 , (III)
, (III)
где R представляет собой сложноэфирный остаток, расщепляемый в кислой или нейтральной среде и являющийся линейным или разветвленным алкильным радикалом, включающим от 1 до 18 атомов углерода, возможно замещенным одним или несколькими атомами галогена либо бензильным радикалом, возможно замещенным по вершинам ароматического кольца одним или несколькими атомами галогена, либо радикалом формул:
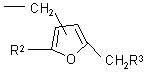 ,
, 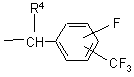 ,
,
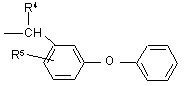 ,
, 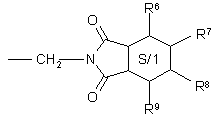 ,
,
в которых значения R2 - R9 указаны в п. 1;
символ S/1 означает тетрагидроцикл,
в виде смеси изомеров или отдельных изомеров относительно асимметричного атома углерода, связанного с циклопропановым кольцом, в качестве промежуточного соединения.
12. Соединения формулы (II)
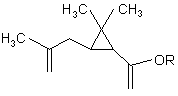 , (II)
, (II)
где R - сложноэфирный остаток, расщепляемый в нейтральной или кислой среде и являющийся линейным или разветвленным алкильным радикалом, содержащим от 1 до 18 атомов углерода, и замещенным одним или несколькими атомами галогена, либо радикалом формул
 ,
,  ,
,
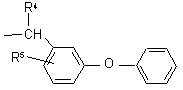 ,
, 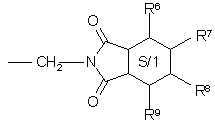 ,
,
в которых значения R2 - R9 указаны выше;
символ S/1 означает тетрагидроцикл,
в качестве промежуточного соединения.
Текст
1. Способ получения сложных эфиров 2,2-диметил-3-[(Z)-1-пропенил]циклопропанкарбоновой кислоты формулы (I) H3C CH3 39851 2. Способ по п. 1, отличающийся тем, что в качестве галогенирующего средства используют хлорирующую или бромирующую добавку. 3. Способ по п. 2, отличающийся тем, что галогенирующее средство выбирается из группы, состоящей из бром- или хлорсодержащего соединения, являющегося N-бромсукцинимидом или Nхлорсукцинимидом, или N-хлор- или N-бромацетамидом, или пербромидом или перхлоридом пиридиния, или пербромидом или перхлоридом гидробромида, или хлоргидратом пиридиния. 4. Способ по пп. 1-3, отличающийся тем, что в качестве основного средства используют соединение, выбираемое из группы, состоящей из гидрида или алкоголята, или амида, или карбоната щелочного или щелочноземельного металла, или третичного амина. 5. Способ по пп. 1-4, отличающийся тем, что R представляет собой сложноэфирный остаток, расщепляемый в кислой или нейтральной среде и являющийся линейным или разветвленным алкильным радикалом, включающим от 1 до 18 атомов углерода и замещенным одним или несколькими атомами хлора или брома. 6. Способ по пп. 1-5, отличающийся тем, что R представляет собой алкильный радикал, включающий от 1 до 4 атомов углерода и являющийся трет.-бутилом или метилом, или этилом, замещенным одним или несколькими атомами хлора или брома, такими как бром- или хлорметил, или моно- или ди-, или трибром- или хлорэтил. 7. Способ по пп. 1-4, отличающийся тем, что R представляет сложноэфирный остаток, выбранный из группы, состоящей из бензильного радикала, замещенного от 1 до 5 атомами фтора, или радикала формулы 4 R включающий от 1 до 8 атомов углерода, такой как этильный или трет.-бутильный радикал или линейный или разветвленный алкильный радикал, включающий от 1 до 8 атомов углерода, замещенный одним или несколькими атомами фтора. 9. Способ по пп. 1-4, 7, 8, отличающийся тем, что используют соединение формулы (II) со структурой (1R, цис), в которой R представляет собой остаток (R,S) или (S)-a-цианофеноксибензилового спирта, или остаток (R,S) или (S)-a-циано-4-фтор3-фен-оксибензилового спирта, и соединение формулы R1OH, где R1 - метильный или этильный, или 1,1,1,3,3,3-гексафторпропильный, или трет.бутильный радикал. 10. Соединения формулы (I) H 3C CH3 H R 1O , где R4 и R5 указаны в п. 1, или радикала формулы 4 R F CH CF3 , где R указан в п. 1, или радикала формулы CH2 4 2 CH2R 3 , где R2 и R3 указаны в п. 1, или радикала формулы 6 R O 7 R CH2 N O CH R 5 O , S/1 R O (1') , где R представляет собой сложноэфирный остаток, расщепляемый в кислой или нейтральной среде и являющийся линейным или разветвленным алкильным радикалом, включающим от 1 до 18 атомов углерода, возможно замещенным одним или несколькими атомами галогена либо бензильным радикалом, возможно замещенным по вершинам ароматического кольца одним или несколькими атомами галогена, либо радикалом формул: 4 CH2 R F 2 CH R 3 CH2R CF3 O , , 4 R O O O O 5 R O R (I) , где R - метил, замещенный хлором или бромом, или этил, замещенный 1 или 2, или 3 атомами хлора или брома, R1 - водород либо алкильный радикал, являющийся насыщенным линейным или разветвленным радикалом и включающим от 1 до 18 атомов углерода, возможно замещенным одним или несколькими атомами галогена. 11. Соединения формулы (III) CH3 Hal CH3 HalH2C OR (III) CH R OR 8 O R 6 R , где R6-R9 указаны в п. 1; символ S/1 означает тетрагидроцикл. 8. Способ по пп. 1-7, отличающийся тем, что в качестве соединения формулы R1OH используют соединение, в котором R1 представляет собой линейный или разветвленный алкильный радикал, CH2 N O 7 R 9 8 S/1 9 R , в которых значения R2-R9 указаны в п. 1; символ S/1 означает тетрагидроцикл, в виде смеси изо 2 39851 меров или отдельных изомеров относительно асимметричного атома углерода, связанного с циклопропановым кольцом, в качестве промежуточного соединения. 12. Соединения формулы (II) H3C CH3 H3C OR (II) O O , R CH R 5 O , R O 6 R 7 R 8 S/1 CH2 N где R - сложноэфирный остаток, расщепляемый в нейтральной или кислой среде и являющийся линейным или разветвленным алкильным радикалом, содержащим от 1 до 18 атомов углерода, и замещенным одним или несколькими атомами галогена, либо радикалом формул 4 CH2 R F 2 CH R 3 CH2R CF3 O , , O R 9 , в которых значения R2-R9 указаны выше; символ S/1 означает тетрагидроцикл, в качестве промежуточного соединения. Настоящее изобретение распространяется на способ получения сложных эфиров 2,2-диметил-3[(Z)1-пропенил]циклопропанкарбоновой кислоты и их промежуточных продуктов. Таким образом, предметом настоящего изобретения является способ получения соединений формулы (I): H3C CH3 H 4 в которой заменитель а представляет собой атом водорода или метильный радикал, а R3 является органическим алифатическим радикалом, включающим от 2 до 6 атомов углерода и одно или несколько ненасыщенных соединений углеродуглерод, г) либо группу H (Z) C 3 C CH 1 C R'O C OR (I) R4 B * R5 n (R,S,RS) в которой В представляет собой атом кислорода O O O в которой R представляет собой либо расщепляемый сложноэфирный остаток, либо сложноэфирный остаток, известный в химии пиретриноидов, а именно: а) либо бензильный радикал с возможностью замещения на уровне ароматических вершин одним или несколькими радикалами, выбранными в группе, состоящей из алкильных радикалов, включающих от 1 до 4 атомов углерода, алкиленных радикалов, включающих от 2 до 6 атомов углерода, алкиленоксильных радикалов, включающих от 2 до 6 атомов углерода, алкадиенильных радикалов, включающих от 4 до 8 атомов углерода, метилендиоксильного радикала и галогенных атомов, б) либо группу CH2 C или –СН2-, R4 являили серы или группу ется атомом водорода, атомом хлора, брома или йода, радикалом -CºN, метильным радикалом, радикалом –CONH2, радикалом –CSNH2 или радикалом -СºСН, R5 является галогенным атомом или метильным радикалом, а n представляет собой число, равное 0, 1 или 2, д) либо группу R6 O R7 CH2 N O S/I R8 R9 в которой заменители R6, R7, R8 и R9 являются атомом водорода, атомом хлора или метильным радикалом и в которой S/I символизирует ароматический цикл или аналогичный цикл дигидро, тетрагидро или гексагидро, е) либо (сукцимидо или малеимидо) метиленную группу, ж) либо группу R1 CH2R2 O в которой заменитель R1 представляет собой атом водорода или метильный радикал, а заменитель R2 является моноциклическим арилом или группой -CºCH, в) либо группу a R 3 O 3 39851 C CH O CH N CH2 C CH C CH R' R 18 в которой R18 представляет собой атом фтора или метильный радикал, a R'18 является метильным, этильным или пропаргильным радикалом, о) либо группу R 22 R 21 CH2 N O з) либо группу R 10 CH R 11 R 12 CH в которой R10 представляет собой атом водорода или радикал CN, R12 является радикалом -СН2или атомом кислорода, R11 является тиазолильным или тиадиазолильным радикалом, связь которого с может располагаться в любом из свободных положений, причем R12 связан с R11 атомом углерода, заключенным между атомом серы и атомом азота, и) либо группу (F) m R 13 N R 23 R 20 R 19 в которой R21 представляет собой атом водорода, группу -C≡N, -С≡СН, -CF3 или алкильный радикал, включающий от 1 до 3 атомов углерода, R20, R22 и R23 одинаковые или различные, представляют собой атом водорода, галогенный атом, алкильный радикал, включающий до 18 атомов углерода, арильный радикал, включающий до 14 атомов углерода, аралкильный радикал, включающий до 18 атомов углерода, цианильный радикал, радикал –СF3, -СО2-алкильный радикал, включающий до 8 атомов углерода, радикал NO2, алкоксильный радикал, включающий до 8 атомов углерода, раR 25 S R 24 N (O) n R 26 или , в котором n дикал равен 0, 1 или 2, а радикалы R24, R25 и R26 являются алкильным радикалом, включающим от 1 до 8 атомов углерода, причем радикалы R22 и R23 могут образовывать насыщенный или ненасыщенный углеродный гомоцикл, включающий до 8 атомов углерода, a R19 представляет собой: CH C C R 28 CH R 14 в которой R13 представляет собой атом водорода или радикал -CN или -CºCH, R14 является трифторметильным радикалом или алкильным, алкиленным или алкинильным радикалом, включающим не более 6 атомов углерода, a m представляет собой число, равное 1, 2, 3 или 4, к) либо группу O R 13 C HC в которой R13 определен, как указано выше, л) либо группу R4 R 27 , в котором либо радикал R27 и R28 одинаковые или различные, представляют собой атом водорода, галогенный атом, алкильный радикал, включающий от 1 до 8 атомов углерода, или арильный радикал, включающий до 14 атомов углерода, R' 28 C C C R" 28 R 27 либо радикал , в котором R'27, R'28 и R"28, одинаковые или различные, представляют собой одно из значений, указанных выше для R27 и R28, а пунктирные линии представляют возможную вторую связь, C R 29 HC R 15 O R 16 в которой R4 определен, как указано выше, R15 представляет собой атом фтора, хлора или брома, a R16 является атомом водорода, фтора, хлора или брома, м) либо группу H R4 CH N B' O либо радикал , в котором R29 может иметь значения, указанные выше для R22 и R23, за S R 24 (R17)p в которой R4 определен, как указано выше, а каждый из R17 представляет собой произвольно алкильную группу, включающую от 1 до 4 атомов углерода, алкоксильную группу, включающую от 1 до 4 атомов углерода, алкилтионильную группу, включающую от 1 до 4 атомов углерода, алкилсульфонильную группу, включающую от 1 до 4 атомов углерода, трифторметильную, 3,4-метилендиоксильную, хлорную, фторную или бромную, р представляет собой число, равное 0, 1, или 2, а В' является атомом кислорода или атомом серы, н) либо группу (O) n , исключением галогена, циано, NO2, R 25 N R 26 где n равен 1 или 2 и R 30 C N R 31 либо радикал , в котором R30 и R31, одинаковые или различные, представляют собой атом водорода, алкильный радикал, включающий от 1 до 18 атомов углерода, арильный радикал, включающий до 14 атомов углерода, 4 39851 ными функциональными группами, или R' представляет собой гетероциклический радикал с возможностью замещения одной или несколькими одинаковыми или различными функциональными группами в виде смеси изомеров или изомеров, разделенных на уровне циклопропанового цикла, с той особенностью, что сложный эфир формулы (II): CH3 H3C аралкильный радикал, включающий до 18 атомов углерода, радикал CF3, СО2-алкильный радикал, включающий до 8 атомов углерода, или алкоксильный радикал, включающий до 8 атомов углерода, п) либо группу R 34 X CH Y R 33 N R 32 в которой Х представляет собой атом серы или кислорода, Y представляет собой группу >С=0, >C=S или >СН2, R32 представляет собой атом водорода, алкильный радикал, линейный, разветвленный или циклический, насыщенный или ненасыщенный, включающий до 8 атомов углерода, с возможностью замещения одним или несколькими галогенными атомами, или арильный радикал, включающий до 14 атомов углерода, R33 представляет собой атом водорода, алкильный радикал, линейный, разветвленный или циклический, насыщенный или ненасыщенный, включающий до 8 атомов углерода, с возможностью замещения одним или несколькими галогенными атомами, или R33 представляет собой арильный радикал, включающий до 14 атомов углерода, радикал –СF3, -NO2, -C≡N, галогенный атом, алкоксильный радикал, включающий до 8 атомов углерода, или -СО2-алкильный радикал, включающий до 8 атомов углерода, R34 является атомом водорода, алкильным радикалом, включающим от 1 до 3 атомов углерода, радикал -С≡СН, р) либо группу R 36 R 35 H3C C CH2 3 1 C OR O (ІІ) O в которой R определен, как указано выше, подвергается обработке галогенирующим средством для получения соединения формулы (III): CH3 H3C Hal H 3 1 (ІІІ) H C C CH C OR Hal O O (1') в которой R определен, как указано выше, a Hal представляет собой галогенный атом, имеющий форму смеси изомеров на уровне атома углерода в положении 1', который подвергают обработке основным средством в присутствии соединения формулы R'-OH, в которой R' определен, как указано выше, для получения искомого соединения формулы (I). Когда R представляет собой расщепляемый сложноэфирный остаток, речь может идти о любом известном специалистам остатке, в частности об алкильном радикале, включающем от 1 до 18 атомов углерода, таком как метильный, этильный, n-пропильный, изопропильный, n-бутильный, изобутильный или, в первую очередь, трет.бутильный, или об алкильном радикале, как определено выше, замещенном одним или несколькими галогенными атомами, в первую очередь хлором или бромом, таким как бром- или хлорметил, моно-, ди- или три-бромэтил или хлорэтил; речь может также идти об алкилсилильном радикале, в котором алкил включает от 1 до 4 атомов углерода, таком как триалкилсилилметил, например трет.-бутилдиметилсилилметил, или арилалкилсилилметил, такой как дифенил-трет.-бутилсилилметил; речь может также идти об алкильном радикале, замещенном такими группами как Оалкильная, О-арильная или О-аралкильная, алкильная, включающая предпочтительно от 1 до 4 атомов углерода, арильная, включающая от 6 до 14 атомов углерода и представляющая собой, в первую очередь, фенильный или толильный радикал, и аралкильная, представляющая собой, в первую очередь, бензильный или фенетильный радикал. Следует только отметить, что вышеуказанный сложноэфирный остаток должен быть расщепляем в нейтральной или кислой среде. Когда R представляет собой бензильный радикал, замещенный одним или несколькими алкильными радикалами, речь в первую очередь идет о метильном, этильном, пропильном или изопропильном радикалах. Когда R представляет собой бензильный радикал, замещенный одним или несколькими алкиленными радикалами, речь в первую очередь идет CH R 37 R 38 в которой R35 представляет собой атом водорода, алкильный радикал, включающий от 1 до 3 атомов углерода, радикал -C≡N, -С≡СН или СF3, R36 и R38, одинаковые или различные, представляет собой атом водорода, алкильный радикал, включающий от 1 до 3 атомов углерода, с возможностью замещения одним или несколькими галогенными атомами, алкиленный радикал, включающий от 2 до 4 атомов углерода или галогенный атом, a R37 представляет собой фенильный радикал с возможностью замещения одним или несколькими алкильными радикалами, включающими от 1 до 3 атомов углерода, или одним или несколькими галогенными атомами, R' представляет собой атом водорода, алкильный радикал, включающий от 1 до 18 атомов углерода, линейный или разветвленный, насыщенный или ненасыщенный, с возможностью замещения одной или несколькими одинаковыми или различными функциональными группами, или R' представляет собой циклоалифатический радикал, включающий от 3 до 7 атомов углерода, с возможностью замещения одной или несколькими одинаковыми или различными функциональными группами, или R' представляет собой арильную группу, включающую от 6 до 14 атомов углерода, с возможностью замещения одной или несколькими одинаковыми или различ 5 39851 ствующем любому из вышеуказанных алкилтионильных радикалов. Когда R21 представляет собой алкильный радикал, речь идет о таком радикале, как метильный, этильный, пропильный или изопропильный, и, в первую очередь, о метильном радикале. Когда один или несколько радикалов R20, R22 и R23 или радикалов, содержащихся в определении R19, R20, R22 и R23, представляют собой галогенный атом, речь идет, в первую очередь, об атоме фтора, хлора или брома. Когда один или несколько радикалов R20, R22 и R23 или радикалов, содержащихся в определении R19, R20, R22 и R23, представляют собой алкильный радикал, речь идет, в первую очередь, о таком радикале, как метильный, этильный, пропильный, изопропильный, бутильный, изобутильный или nпентильный. Когда один или несколько радикалов R20, R22 и R23 или радикалов, содержащихся в определении R19, R20, R22 и R23 представляют собой арильный радикал, речь идет, в первую очередь, о фенильном радикале, с возможностью его замещения, в частности, алкильным или алкоксильным радикалом, включающим от 1 до 8 атомов углерода, или таким радикалом, как нитро, трифторметильный, гидроксильный, галогенный или аминный. Когда один или несколько радикалов R20, R22 и R23 или радикалов, содержащихся в определении R19, R20, R22 и R23 представляют собой аралкильный радикал, речь идет, в первую очередь, о бензильном радикале. Когда один или несколько радикалов R20, R22 и R23 или радикалов, содержащихся в определении R19, R20, R22 и R23 представляют собой -СО2алкильный или алкоксильный радикал, под алкильным понимают, в первую очередь, метильный, этильный, пропильный или изопропильный радикал, а под алкоксильным - метоксильный, этоксильный, пропоксильный или изопропоксильный радикал. Когда R32 или R33 представляет собой алкильный радикал, линейный, разветвленный или циклический, насыщенный или ненасыщенный, речь идет, в первую очередь, о радикале, таком как метильный, этильный, n-пропильный, изопропильный, циклопропильный, циклопропилметильный, бутильный, изобутильный, трет.-бутильный, циклобутильный, n-пентильный, циклопентильный, nгексильный или циклогексильный, или об аллильном, пропаргильном или бутинильном радикале. Когда указанные радикалы замещены одним или несколькими галогенными атомами, под галогеном понимают фтор, хлор, бром или йод. Когда R32 или R33 представляет собой арильный радикал, речь идет, в первую очередь, о фенильном радикале. Когда R33 представляет собой галогенный атом, речь идет, в первую очередь, об атоме фтора, хлора или брома. Когда R33 представляет собой алкоксильный радикал, речь идет, в первую очередь, о метоксильном, этоксильном, пропоксильном или изопропоксильном радикале. Когда R33 представляет собой -СО2-алкильный радикал, под алкильным понимают, в первую очередь, такой радикал, как метильный, этильный, о винильном, аллильном, 2-метилаллильном или изобутенильном радикалах. Когда R представляет собой бензильный радикал, замещенный одним или несколькими алкиленоксильными радикалами, речь в первую очередь идет о винилоксильном, аллилоксильном, 2метилаллилоксильном или изобутенилоксильном радикалах. Когда R представляет собой бензильный радикал, замещенный одним или несколькими алкадиенильными радикалами, речь в первую очередь идет о бутандиенильном или пентадиенильном радикале. Когда R представляет собой бензильный радикал, замещенный одним или несколькими галогенными атомами, речь в первую очередь идет об атоме хлора, брома или фтора. Когда R2 представляет собой арильный радикал, речь в первую очередь идет о фенильном радикале, а группа R в этом случае является, в первую очередь, 5-бензил-3-фурилметильной группой. R3 может представлять собой, в частности, радикал -CH2-CH=CH2, -СН2-СН= СН-СН3, -СН2СН= СН-СН-СН2, -СН2-СН= СН-СН2-СН3 или -СНС≡СН. В представляет собой, в частности, атом кислорода, а соответствующей группой в этом случае является, в первую очередь, такая группа, как 3-феноксибензильная, a-циано-3-феноксибензильная, a-этинил-3-феноксибензильная, 1-(3-феноксифенил)-этильная или a-тиоамидо-3-феноксибензильная. В представляет собой также группу -СО-, а соответствующей группой в этом случае является, в первую очередь, 3-бензоилбензильная группа. Когда R представляет собой алкильный радикал, речь в первую очередь идет о таком радикале, как метильный, этильный, пропильный, линейный или разветвленный, или бутильный, линейный или разветвленный. Когда R14 представляет собой алкиленный радикал, речь идет о таком радикале, как винильный, аллильный, бутенильный, пентенильный или гексаенильный. Когда R14 представляет собой алкинильный радикал, речь в первую очередь идет о таком радикале, как этинильный, пропаргильный или бутинильный. Когда R17 представляет собой алкильный радикал, речь идет о таком радикале, как метильный, этильный, пропильный, линейный или разветвленный, или бутильный, линейный или разветвленный. Когда R17 представляет собой алкоксильный радикал, речь идет о таком радикале, как метоксильный, этоксильный, пропоксильный, линейный или разветвленный, или бутоксильный, линейный или разветвленный. Когда R17 представляет собой алкилтионильный радикал, речь идет о таком радикале, как метилтионильный, этилтионильный, пропилтионильный, линейный или разветвленный, или бутилтионильный, линейный или разветвленный. Когда R17 представляет собой алкилсульфонильный радикал, речь идет о радикале, соответ 6 39851 или несколькими группами ОН, Oalc или alс, включающими от 1 до 8 атомов углерода, одной или несколькими группами СF3, ОСF3, SCF3 или группой (G): O H C (G) O H R' может также представлять собой алкильный радикал, замещенный на уровне двух соседних атомов углерода группой (G1): H O C (G1) O H пропильный, линейный или разветвленный, или бутильный, линейный или разветвленный. Когда R34 представляет собой алкильный радикал, речь идет, в первую очередь, о метильном радикале. Когда R33 представляет собой алкильный радикал, речь идет, в первую очередь, о метильном радикале. Когда R36 и/или R38 представляет собой алкильный радикал, речь идет, в первую очередь, о метильном или этильном радикале. Когда алкильный радикал замещен одним или несколькими галогенными атомами, под галогеном понимают, в первую очередь, фтор, хлор или бром. Когда R36 и/или R38 представляет собой алкиленный радикал, речь идет, в первую очередь, о винильном или аллильном радикале. Когда R36 и/или R38 представляет собой галогенный атом, речь идет, в первую очередь, об атоме фтора, хлора или брома. Когда R37 представляет собой фенильный радикал, замещенный алкильным радикалом или галогенным атомом, под алкилом и галогеном понимают, в первую очередь, соответствующие радикалы, указанные выше для R36 и R38. Когда R' представляет собой линейный или разветвленный алкильный радикал, под алкильным понимают, например, такие радикалы как метильный, этильный, пропильный, линейный или разветвленный, бутильный, линейный или разветвленный, гексильный, линейный или разветвленный, децильный, линейный или разветвленный, тетрадецильный, линейный или разветвленный, октадецильный, линейный или разветвленный. Когда R' представляет собой линейный или разветвленный алкильный радикал, под ненасыщенным алкильным понимают, например, такие радикалы как этенильный, пропенильный, бутенильный, линейный или разветвленный, гексенильный, линейный или разветвленный, деценильный, линейный или разветвленный, тетрадеценильный, линейный или разветвленный, октадеценильный, линейный или разветвленный, или же ненасыщенные алифатические радикалы, включающие две или несколько двойных связей. Когда R' представляет собой алкильный радикал, замещенный одной или несколькими функциональными группами, под функциональной группой понимают, в первую очередь, галогенный атом, группу ОН или SH, группу ORа или SRа, в которых Rа является алкильным радикалом, включающим от 1 до 8 атомов углерода, группу NO2 Rb N Rc , в которой Rb и Rс, одинаковые или или различные, представляют собой атом водорода, или алкильный радикал, включающий от 1 до 8 атомов углерода, группу C≡N, SO3Н или РO4Н2 или группу COalc1, SO2alc или SO3аlc3, в которых alc1, alc2, или аlc3 представляют собой алкильный радикал, включающий от 1 до 18 атомов углерода. R' может также представлять собой алкильный радикал, замещенный арильным радикалом, например бензильным или фенетильным, который, в свою очередь, может быть замещен одной O O или замещенный группой Когда R' представляет собой алкильный радикал, замещенный одной или несколькими функциональными группами, в качестве предпочтительных значений R' можно назвать радикалы: -(СН2)n-СНаl3, в котором n принимает целочисленное значение от 1 до 8, a Hal является галогенным атомом, например, радикал -СН2-ССl3, СН2-СF3, -СН2-СН2-ССl3 или -СН2-СН2-СF3, -(СН2)n1-СHНаl2, в котором Hal определен, как указано выше, а n принимает значение от 0 до 8, например, радикал, -СН2-СHСl2, -CH2-CHF2 или CHF2, -(СН2)n-СH2Наl, в котором n и Hal определены, как указано выше, например, радикал -СН2-СH2Сl или -CH2-CH2F, -С(СНаl3)3, в котором Hal определен, как указано выше, например, радикал -С(СF3)3 или CF3 CF3 CF3 C CH3 C CH3 CF3 C CF3 CH3 CCl3 , , или CF3 CF3 C CH3 CH3 C CH2 CH3 H , или CF3 CF3 H , C C CH3 CN CH3 C CH3 CN H , или, -(СН2)n-CN, в котором n определен, как указаCHalc3 C CN H но выше, , в котором Hal определен, указано выше, например, радикал CCl3 C CN H -(СН2)n-ORd, в котором n определен, как указано выше, а Rd представляет собой атом водорода или линейный или разветвленный алкильный радикал, включающий от 1 до 8 атомов углерода, например радикал -СН2-ОСН3, -CH2-CH2-O-CH3, CH2-CH2-О-СН2-СН3 или -CH2-CH2-OH, Rd (CH2)n N Rd , в котором n и Rd определены как указано выше, а два радикала Rd могут быть различными, например, радикал 7 как 39851 CH3 H , -CH2-CH2-N первую очередь, о фенильном радикале или о фенильном радикале, замещенном одной или несколькими группами ОН, Oalc или alc, причем alc представляет собой алкильный радикал, включающий от 1 до 8 атомов углерода, или группой СF3, ОСF3 или SСF3, или одним или несколькими галогенными атомами. Когда R' представляет собой гетероциклический радикал, с возможностью замещения, речь идет, в первую очередь, о таком радикале, как пиридильный, фурильный, тиофенильный, оксазолильный или тиазолильный, с возможностью замещения одной или несколькими из вышеперечисленных групп. Способ, являющийся предметом настоящего изобретения, отличается исключительной стандартностью. Он позволяет получить как расщепляемые сложные эфиры, то есть промежуточные сложные эфиры, превращаемые в биологически активные сложные эфиры обычными методами переэтерификации или гидролиза с последующей этерификацией, так и непосредственно биологически активные сложные эфиры. Кроме того, настоящий способ отличается исключительной избирательностью, поскольку он приводит к получению соединений формулы (I) с конфигурацией (Z), то есть к биологически активной форме этих соединений. Предметом настоящего изобретения является, в частности, вышеописанный способ, отличающийся тем, что галогенирующим средством является хлорирующая или бромирующая добавка, причем предпочтение отдается второй добавке. Среди галогенирующих средств, используемых в настоящем изобретении, можно назвать бром, используемый самостоятельно или на полимерной основе, хлор, N-бромсукцинимиды и Nхлорсукцинимиды, N-бромацетамиды и N-хлорацетамиды, пербромид пиридиния, пербромид гидробромида пиридиния, перхлорат гидрохлорида пиридиния, пербромид фенилтриметиламмония, пербромид 2-карбоксиэтилтрифенилфосфония, трибромид 2-гидропирролидона, дибромид и дихлорид меди, 5,5-дибром-2,2-диметил-4,6-диоксо-1,3-диоксан, три- и пентабромид и хлорид фосфора, смеси третичного триметилбром- и триметилхлорсилан-ДМСО-амина, трихлорид железа. Среди них можно назвать, в первую очередь, бром, хлор, N-бромсукцинимиды и N-хлорсукцинимиды и ацетамиды, пербромид и перхлорид пиридиния, пербромид и перхлорид гидробромида и гидрохлорида пиридиния. Реакция галогенирования проводится в среде растворителя, которым может быть галогенсодержащий растворитель, в частности метиленхлорид, хлороформ, тетрахлорметан, дихлорэтан или смесь этих растворителей, эфир, такой как тетрагидрофуран, диметоксиэтан, метил-трет.-бутилэфир или диоксан, ароматический растворитель, такой как бензол, толуол, ксилол или соответствующий насыщенный растворитель, в частности, циклогексан, спирт, такой как метанол или этанол, этилацетат или же диметилформамид или диметилсульфоксид. Выгодно максимальное ограничение образования моно- и тригалогенсодержащих производ , CH3 -CH2-CH2-N (CH2)n CH3 CH3 CH2-CH2-N CH2-CH3 CH CH2 O O H3C CH3 , в котором n определен, CH CH2 O как выше, например, радикал (CH2)n CH CH2 OH O H3C CH3 , OH , в котором n определен, CH2 CH CH2 OH как выше, например, радикал O (CH2) n O OH , , в котором n определен, O CH2 O как выше, например, радикал O CH2 CH2 O или , (CH2)n , в котором n определен, как выше, например, бензильный или фенетильный (CH2)n радикал, делен, как CH2 O O выше, , в котором n опренапример, радикал O O . Когда R' представляет собой циклоалифатический радикал, включающий от 3 до 7 атомов углерода, речь идет о таком радикале, как циклопропильный, циклобутильный, циклопентильный, циклогексильный или циклогептильный, который может быть связан с атомом кислорода с помощью алкильного радикала, включающего от 1 до 3 атомов углерода, в частности, с помощью метильного радикала. Когда R' представляет собой циклоалифатический радикал, включающий от 3 до 7 атомов углерода, замещенный одной или несколькими функциональными группами, под функциональной группой понимают, в первую очередь, галогенный атом, алкильный радикал, включающий от 1 до 6 атомов углерода, алкоксильный радикал, включающий от 1 до 6 атомов углерода, группу NO2. Когда R' представляет собой арильный радикал, с возможностью замещения, речь идет, в 8 39851 ных рядом с целевыми производными (III), поэтому предметом настоящего изобретения является, в частности, метод, отличающийся тем, что используются примерно 2 эквивалента галогенирующего средства. В предпочтительных условиях внедрения изобретения используемое основное вещество выбирают из группы, состоящей из гидридов, алкоголятов, амидидов, щелочных и щелочноземельных карбонатов, в частности, натрия или калия, третичных аминов, в частности, триэтиламина, пиридина или диметиламинопиридина. Операция выполняется в среде растворителя, которым является либо соединение формулы R'OH, либо смесь этого соединения с соответствующим сорастворителем. Этим сорастворителем может быть, в частности, галогенсодержащий растворитель, эфир, ароматический растворитель или соответствующий насыщенный растворитель из числа вышеперечисленных, или же диметилформамид или диметилсульфоксид. Операция выполняется при температуре, пригодной для используемого растворителя, причем эта температура может составлять, в зависимости от случая, примерно от -78°С до +40°С. Предметом настоящего изобретения, в частности, является вышеописанный способ, отличающийся тем, что R представляет собой сложноэфирный остаток, расщепляемый в нейтральной или кислой среде, выбранный из группы, состоящей из линейных или разветвленных алкильных радикалов, включающих от 1 до 18 атомов углерода, линейных или разветвленных алкильных радикалов, включающих от 1 до 18 атомов углерода, замещенных одним или несколькими галогенными атомами, алкильных радикалов, включающих от 1 до 4 атомов углерода, замещенных силильной группой, и алкильных радикалов, включающих от 1 до 4 атомов углерода, замещенных такими группами как О-алкильная, О-арильная или О-аралкильная, алкильная, включающая от 1 до 4 атомов углерода, и арильная, включающая от 6 до 14 атомов углерода. Предметом настоящего изобретения, в частности, является вышеописанный способ, отличающийся тем, что R представляет собой сложноэфирный остаток, расщепляемый в нейтральной или кислой среде, выбранный из группы, состоящей из алкильных радикалов, включающих от 1 до 4 атомов углерода, алкильных радикалов, включающих от 1 до 4 атомов углерода, замещенных одним или несколькими атомами хлора или брома, алкильных радикалов, включающих от 1 до 4 атомов углерода, замещенных алкилсилильной группой, и алкильных радикалов, включающих от 1 до 4 атомов углерода, замещенных такими группами как О-алкильная, О-арильная или Оаралкильная, как определено выше. Предметом настоящего изобретения является, в первую очередь, вышеописанный способ, отличающийся тем, что R представляет собой алкильный радикал, включающий от 1 до 4 атомов углерода, в первую очередь трет.-бутильный, или метильный или этильный радикал, замещенный одним или несколькими атомами хлора или брома, в первую очередь бром- или хлорметильный радикал или моно-, ди- или трибром- или хлорэтильный радикал. Предметом настоящего изобретения также является, вышеописанный способ, отличающийся тем, что R представляет собой сложноэфирный остаток, выбранный из группы, состоящей из: бензилового радикала, замещенного одним или несколькими галогенными атомами, радикалов формулы: CH2 CH2R2 R1 O в которой R1 и R2 определены как указано выше, радикалов формулы: a R3 O в которой а и R3 определены как указано выше, радикалов формулы: H C R4 B (R5)n в которой R4, R5 и n определены как указано выше, радикалов формулы: R6 O R7 S/I CH2 N R8 O R9 в которой R6, R7, R8, R9 и S/I определены как указано выше, радикалов формулы: (F) m R 13 CH R 14 в которой R13, R14 и m определены как указано выше, радикалов формулы: R4 HC R 15 O в которой R4, R15, и R16 выше, радикалов формулы: R 16 определены как указано C CH CH C CH R' 18 R 18 в которой R18 и R'18 определены как указано выше, радикалов формулы: 9 39851 в которой R36 представляет собой атом водорода, атом фтора или хрома, R37 является фенильным или 3-фторфенильным радикалом, а R38 - атом водорода, атом фтора или хлора или метильный радикал. Предметом настоящего изобретения также, в частности, является вышеописанный способ, отличающийся тем, что на начальном этапе используется соединение формулы R'-OH, вкоторой R' представляет собой атом водорода, линейный, разветвленный или циклический алкильный радикал, включающий от 1 до 8 атомов углерода, и, в частности, этильный радикал, трет.-бутильный радикал или же циклопропильный или циклопропилметильный радикал, линейный или разветвленный алкильный радикал, включающий от 1 до 8 атомов углерода, замещенных одним или несколькими галогенными атомами, и, в частности, одним или несколькими атомами фтора, радикал (СН2)m-О(СН2)n-CH3, в котором m имеет целочисленное значение от 1 до 8, а n имеет целочисленное значение от 0 до 8, и, в частности, радикал –СН2-О-СН3. Предметом настоящего изобретения является, в первую очередь, вышеописанный способ, отличающийся тем, что на начальном этапе используется соединение формулы (II) со структурой (1R, цис), в которой R представляет собой остаток (R, S) или (S) a-циано-феноксибензилового спирта или остаток (R, S) или (S) a-циано-4-фтор-3феноксибензилового спирта и соединение формулы R'-OH, в которой R' представляет собой метильный, этильный, трет.-бутильный или 1,1,1,3,3,3-гексафторпропильный радикал. Промежуточные соединения формулы (III) являются новыми соединениями, так что предметом настоящего изобретения также являются указанные соединения формулы (III) в виде смесей изомеров или отдельных изомеров на уровне циклопропанового цикла. Большая часть соединений формулы (I) известны и описаны в патентах или патентных заявках ЕЭС № 38271, 41021, 48186, 110769, 114012, 215701, 357742, 300898, 176387, 261035, 381563 или во французском патенте 2 612 184. Речь идет о биологически активных соединениях, обладающих, как правило, пестицидными свойствами, в частности, в отношении насекомых и клещей, или же о промежуточных соединениях в синтезе активных соединений. Соединениями формулы (I), в которой R представляет собой метильный радикал, замещенный атомом брома или хлора, или этильный радикал, замещенный 1, 2 или 3 атомами брома или хлора, являются расщепляемые сложные эфиры, то есть промежуточные веществ в синтезе биологически активных сложных эфиров. Они до настоящего времени не были описаны и также являются предметом настоящего изобретения. Расщепление сложных эфиров формулы (I), являющихся промежуточными веществами в синтезе биологически активных сложных эфиров, может производиться обычными методами, известными специалистам. Соответствующие примеры приводятся в патенте ЕЭС 48186, о котором уже шла речь выше, и, в более общих чертах, в статье R 36 R 35 CH R 37 R 38 в которой R35, R36, R37 и R38 определены как указано выше. Предметом настоящего изобретения является, в первую очередь, вышеописанный способ, отличающийся тем, что R представляет собой сложноэфирный остаток, выбранный из группы, состоящей из: бензилового радикала, замещенного от 1 до 5 атомами фтора, радикалов формулы: R3 O в которой R3 представляет собой радикал -CH2CH-CH или -СН2-СºСН, радикалов формулы: H C R4 O в которой R4 определен как указано выше, радикалов формулы: O CH2 N O радикалов формулы: (F) m CH2 R 14 в которой R14 и m определены как указано выше, радикалов формулы: R4 F HC O в которой R4 определен как указано выше, радикалов формулы: C CH CH C CH R' 18 R 18 в которой R18 и R'18 определены как указано выше, радикалов формулы: R 36 CH2 R 38 R 37 10 39851 Спектр ЯРМ СDСl3 250 МГц млн-1 1,22 (s), 1,27 (s), 1,34 (s): СН3 спарен.; 1,84 (d) и 1,98 (m): H1 и Н3 цис; 3,63 (s), 3,73 (s): СО2СН3; 5,50 (d, J=11), 5,67 ((d, J=11): Hal-CH-CH. Этап Б: (1R, цис) 2,2-диметил-3-[(Z)-2метоксикарбонил)-этенил]-циклопропан-1-метилкарбоксилат В среде инертного газа смешивают 0,16 г метилата натрия и 1,6 см3 метанола. Затем охлаждают примерно до 0°С и медленно добавляют 0,5 г (1R, цис) 2,2-диметил-3-(1,3-дибром-2оксопропил)-циклопропан-1-метилкарбоксилата, растворенного в 2,5 см3 метанола. После этого взбалтывают в течение 1 ч 30 мин при температуре примерно -50°С, выпаривают растворитель при пониженном давлении при температуре около +30°С и добавляют 10 см3 метиленхлорида. Затем раствор промывают водой, высушивают и концентрируют досуха. Таким образом, получают 0,324 г сырого продукта, который подвергают хроматографии на двуокиси кремния (элюант: циклогексан - этилацетат (6:4), в результате чего получают 0,262 г целевого продукта. Инфракрасный спектр (СНСl3) Поглощение С=O 1720 см-1 С=С 1634 см-1 Совместимость с изомером Z Спектр ЯРМ CDCl3 250 МГц млн-1 1,28 (s), 1,31 (s): СН3 спарен.; 1,96 (d, J=3,5), 3,25 (dd): Н1/Н3 цис; 3,46 (s), 3,72 (s): СН3 сложн. эфир в п. 3; 5,90 (dd), 6,65 (dd): Н в п. 1' – Изомер Z. Пример 2: (1R, цис) 2,2-диметил-3-[(Z)-2-трет.бутоксикарбонил)-этенил]-циклопропан-1-ме-тилкарбоксилат (Продукт А) и (1R, цис) 2,2-диме-тил3-[(Z)-2-карбоксиэтенил)-циклопропан-1метилкарбоксилат (Продукт Б) В среде инертного газа смешивают 12 см3 диметоксиэтана и 0,684 г трет.-бутилата калия. Затем медленно добавляют раствор 0,684 г (1R, цис) 2,2-диметил-3-(1,3-дибром-2-оксопропил)-циклопропан-1-метилкарбоксилата, полученного на этапе А примера 1, в 10 см3 диметоксиэтана и взбалтывают в течение 40 мин при температуре около 60°С. После этого добавляют 3 см3 диметоксиэтана и 2 см3 трет.-бутанола и взбалтывают в течение 15 мин при температуре около -60°С. За-тем добавляют воду и метиленхлорид, отстаивают, экстрагируют водную фазу с помощью метиленхлорида, промывают водой объединенные органические фазы, высушивают и концентрируют досуха при температуре около +30°С. Таким образом получают 0,219 г целевого продукта А. Затем подкисляют объединенные водные фазы 2 н. хлористоводородной кислотой и экстрагируют с помощью метиленхлорида. После этого концентрируют досуха органическую фазу и получают 0,211 г продукта Б, соответствующего сырому (1R, цис) 2,2-диметил-3-[(Z)-2-карбоксиэтенил)циклопропан-метилкарбоксилату. Затем продукты А и Б подвергают хроматографии на двуокиси кремния (элюант: метиленхлорид - гексан (8:2), а затем циклогексан - этилацетат (6:4)). Химический состав продукта А Инфракрасный спектр (СНСl3) Поглощение ТУ ГРИНА "Защитные группы в органическом синтезе". Соединения формулы (II), используемые на начальном этапе метода, являющегося предметом настоящего изобретения, могут быть получены по одному из методов, описанных ниже, в экспериментальной части, то есть путем этерификации соответствующей кислоты подходящим спиртом. Соединения формулы (II), за исключением тех из них, в которых R представляет собой метильный, этильный, 3-феноксибензильный или aциано-3-феноксибензильный радикал, являются новыми соединениями и в качестве таковых – одним из предметов настоящего изобретения. Вышеуказанная кислота в любой из своих конфигураций хорошо известна и может быть получена одним из методов, известных специалистам. Кислота (1R, цис) описана в журнале Agr. Biol. Chem., т. 29, № 8, с. 784, 1965; кислота (1S, цис) может быть получена по методу, описанному в патенте США 4296038; кислота (1R, транс) может быть получена по методу, описанному в журнале Synth. Comm., 1984, 14, с. 1239-46, а кислота (1S, транс) - тем же методом, беря за основу (-) 3карен; кислота (1R,S цис) может быть получена с использованием методов, описанных в вышеуказанном журнале Agr. Biol. Chem. или в патенте США 4296038, беря за основу рацемический 3карен, который может быть получен как описано в журнале J. Org. Chem., 1987, т. 52, с. 1493 или в Tet. Letters, 1984, с. 5255; кислота (1R,S транс), а также кислота (1R,S цис) могут быть получены с использованием методов, описанных в Japan Kokaї J 81079644. Соединения формулы (II), в которой R представляет собой метильный, 3-феноксибензильный или a-циано-3-феноксибензильный радикал, описаны, например, в журнале Synth. Comm., 1988, 18, с. 1139-49 и Tetrahedron, 1986, 42, с. 5717-28. Приводимые далее примеры иллюстрируют настоящее изобретение, вместе с тем, не ограничивая его. Пример 1: (1R, цис) 2,2-диметил-3-[(Z)-2метоксикарбонил)-этенил]-циклопропан-1-метилкарбоксилат Этап А: (1R, цис) 2,2-диметил-3-(1,3-дибром-2оксопропил)-циклопропан-1-метилкарбоксилат В среде инертного газа смешивают 2,4 г (1R, цис) 2,2-диметил-3-(2-оксопропил)-циклопропан-1метилкарбоксилата и 30 см3 метиленхлорида, затем охлаждают до +10°С и добавляют 1,3 см3 брома. После этого взбалтывают в течение 2 ч при комнатной температуре и вливают в смесь воды и льда. Затем экстрагируют с помощью метиленхлорида, высушивают органическую фазу и выпаривают досуха. Остаток подвергают хроматографии на двуокиси кремния (элюант: метиленхлорид - гексан (7:3), в результате чего получают 3,2 г искомого продукта. Химический состав С10Н14Вr2О3=342,04 С Н Вr % расчетный 35,11 4,12 46,72 % полученный 35,0 4,2 46,5 Инфракрасный спектр (СНСl3) Поглощение С=O 1736,1719 см-1 СООСН3 1438 см-1 11 39851 С=О 1721 см-1 (площадка 1705 см-1) С=С 1631 см-1 О-СН3 1439 см-1 О-tBu 1368 см-1 Спектр ЯРМ СDСl3 250 МГц млн-1 1,27 (s) и 1,31 (s): СН3 спарен.; 1,49: -CO2tBu; 1,92 (d, J=8,5) и 3,26 (m): H1 и Н3 цис; 3,65: О-СН3; 5,80 (d, J=11,5): CH=aCO; 6,51 (dd, J=10,5-11,5): CH=bСО. дельта Z. Химический состав продукта Б Инфракрасный спектр (СНСl3) Поглощение ОН кисл. 3518 см-1 С= О 1723, 1693 см-1 С=С 1628 см-1 СООМе 1440 см-1 Спектр ЯРМ СDСl3 250 МГц млн-1 1,28 (s) и 1,32 (s): СН3 спарен.; 1,99 (d) и 3,21 (m): H1 и Н3 цис; 3,67 (s): СО2СН3; 5,92 (d, J=11) и 6,77 (dd): CO-CH=CH-CH; 11,6 (m): 1H мобильн. Пример 3: (1R, цис) 2,2-диметил-3-[(Z)-2[(1,1,1,3,3,3-гексафтор)-пропоксикарбонил]-этенил]-циклопропан-1-метилкарбоксилат В среде инертного газа промывают циклогексаном 0,057 г гидрида натрия в виде 50процентной взвеси в масле, а затем добавляют 1 см3 диметоксиэтана. После этого в полученную таким образом взвесь добавляют 0,33 г гексафторизопропанола в 1 см3 диметоксиэтана и взбалтывают в течение 30 мин. Раствор охлаждают до +5°С и медленно добавляют раствор 0,173 г (1R, цис) 2,2-диметил-3-(1,3-дибром-2-оксопропил)циклопропан-1-метилкарбоксилата в 1 см3 диметоксиэтана. Затем взбалтывают в течение 1 ч при температуре +3/+5°С, вливают реакционную смесь в водный раствор 1 н. хлористоводородной кислоты, экстрагируют с помощью метиленхлорида, высушивают органическую фазу и концентрируют досуха. Остаток подвергают хроматографии на двуокиси кремния (элюант: метиленхлорид - гексан (7:3)), в результате чего получают 0,16 г искомого продукта. Спектр ЯРМ СDСl3 250 МГц 1,30 (s), 1,34 (s): СН3 спарен.; 3,68 (s): СН3 сложн. эфир; 2,06 (d, J=8,5): H1; 3,12 (dd): Н3; 6,99 (dd): H'1; 6,00 (d, J=11,5): H'2; 5,81: >CH-. Пример 4: (1R, цис) 2,2-диметил-3-[(Z)-2(1,1,1,3,3,3-гексафтор)-пропоксикарбонил]-этенил]циклопропан-1-метилкарбоксилат В среде инертного газа смешивают 1,5 см3 диметоксиэтана, 0,056 г трет.-бутилата калия и 0,2 г гексафторизопропанола, а затем добавляют при температуре +5°С раствор 0,170 г (1R, цис) 2,2-диметил-3-(1,3-дибром-2-оксопропил)-циклопропан-1-метилкарбоксилата в 0,5 см3 диметоксиэтана. После этого смесь взбалтывают в течение 18 ч при комнатной температуре, добавляют 1 н. хлористоводородную кислоту, экстрагируют с помощью метиленхлорида, высушивают и концентрируют досуха. Остаток подвергают хроматографии на двуокиси кремния (элюант: метиленхлорид - гексан (7: 3)), в результате чего получают 0,066 г искомого продукта. Инфракрасный спектр (СНСl3) Поглощение >С=О 1758, 1740 и 1718 см-1 С=С 1624 см-1 Пример 5: (1R, цис) 2,2-диметил-3-[(Z)-2(1,1,1,3,3,3-гексафтор)-пропоксикарбонил]-этенил]циклопропан-1-метилкарбоксилат Операции выполняются как указано в примере 4 с использованием вместо трет.-бутилата калия 0,027 г метилата натрия. В результате получают целевой продукт идентичный продукту, полученному в примере 4. Пример 6: (1R, цис) 2,2-диметил-3-[(Z)-2карбоксиэтенил]-циклопропан-1-метилкарбоксилат В среду инертного газа помещают 1 см3 1 н. раствора карбоната калия, после чего добавляют при температуре около +5°С раствор 0,342 г (1R, цис) 2,2-диметил-3-(1,3-дибром-2-оксопропил)-циклопропан-1-метилкарбоксилата в 1,5 см3 тетрагидрофурана. Затем взбалтывают в течение 1 ч 30 мин, дают температуре подняться до 20°С и взбалтывают в течение 4 ч. Затем добавляют воду, экстрагируют с помощью метиленхлорида, высушивают органическую фазу и выпаривают растворитель. Остаток подвергают хроматографии на двуокиси кремния (элюант: метиленхлорид – этанол (97: 3)), в результате чего получают 0,046 г целевого продукта. Спектр ЯРМ СDСl3 250 МГц 1,28 (s), 1,32 (s): СН3 спарен.; 1,98 (d, J=8,5), 3,20 (m): H1/Н3 цис; 3,67 (s): СН3 сложн. эфир; 5,91 (d, J=11,5), 6,77 (dd, J=11,5): Н(C=C). Пример 7: (1R, цис) 2,2-диметил-3-[(Z)-2(метоксикарбонил)-этенил]-циклопропан-1-карбоксилат (S) a-циано-3-феноксибензила Этап А: (1R, цис) 2,2-диметил-3-(1,3-дибром-2оксопропил)-циклопропан-1-карбоксилат (S) aциано-3-феноксибензила В среде инертного газа смешивают 1,75 г 2,2диметил-3-(2-оксопропил)-циклопропан-1-карбоксилата (S) a-циано-3-феноксибензила и 17,5 см3 тетрагидрофурана. Затем при температуре 0/+5°С медленно добавляют 3,29 г пербромида гидробромида пиридиния и взбалтывают в течение 6 ч при температуре +5°С. Затем смесь выдерживают в течение ночи в леднике, фильтруют и концентрируют фильтрат досуха при пониженном давлении при температуре +25°С. После этого продукт очищают хроматографией на двуокиси кремния (элюант: метиленхлорид - гексан (7: 3)). В результате получают 0,8 г искомого продукта. Химический состав C23H20NO4Br2=535,2 С Н Br N % расчетный 51,6 3,8 29,9 2,6 % полученный 51,4 4,0 29,4 2,5 Спектр ЯРМ СDСl3 250 МГц млн-1 Смесь изомеров на уровне брома в п. 1'. 1,16-1,23-1,25-1,27: diMe спарен.; 1,88: Н1; 2,07: Н3 циклопропила; 6,25 и 6,38: CN CO2 CH Ф; 4,06 (d) и 4,39 (d): -СН2Вr-СО-; 5,20 (d) и 5,36 (d): CHBr-CO; от 6,95 до 7,45: Н ароматич. Исходный сложный эфир получают следующим образом. В среде инертного газа смешивают 15 см3 метиленхлорида, 2 г 2,2-диметил-3-(2-оксопропил)циклопропан-1-карбоновой кислоты, 2,59 г дициклогексилкарбодиимида и 2,8 см3 пиридина, после чего добавляют за 20 мин при температуре +10°С 12 39851 смесь 2,74 г (S) a-циано-3-феноксибензилового спирта, 20 см3 метиленхлорида и 0,02 г диметиламинопиридина. Затем взбалтывают в течение 20 ч при температуре +20°С, фильтруют, концентрируют фильтрат досуха при пониженном давлении при температуре +30°С. Остаток подвергают хроматографии на двуокиси кремния (элюант: циклогексан - этилацетат (8:2)), в результате чего получают 3,71 г искомого продукта. Инфракрасный спектр (СНСl3) Поглощение Карбонил 1736 см-1 Фенокси 1588, 1498 см-1 Кислота и ОН Отсутствуют Спектр ЯРМ СDСl3 250 МГц 1,11 (s) и 1,21 (s): diMe спарен.; 1,63 (m): H1 и Н3 цис; 2,16 (s): СН3 в п. a карбонила; 2,87 (m): CN CH Ф; от СН3 в п. a карбонила; 6,27 (s): 7,00 до 7,45 (9Н): ароматические соединения. Круговой дихроизм (диоксан) Макс. 225 нм De=+1; 281 нм De=+0,3; 288 нм De=+0,3; 300 нм De=+0,07. Этап Б: (1R, цис) 2,2-диметил-3-[(Z)-2метоксикарбонил)-этенил]-циклопропан-1карбоксилат (S) a-циано-3-феноксибензила В среде инертного газа смешивают 0,165 г метилата натрия и 3 см3 метанола, после чего добавляют при температуре +5°С 0,770 г продукта, полученного как описано в этапе А, и 6 см3 метанола. Затем взбалтывают в течение 1 ч при температуре 0°С, а затем в течение 2 ч 30 мин при комнатной температуре и вливают в 25 см3 2 н. хлористоводородной кислоты при температуре около +5°С. После этого экстрагируют с помощью метиленхлорида, промывают водой и высушивают. После выпаривания растворителя получают 0,6 г сырого продукта, который очищают хроматографией на двуокиси кремния (элюант: метиленхлорид - гексан (8:2), а затем (7:3)). В результате получают 0,267 г смеси, содержащей целевой продукт. Пример 8: (1R, цис) 2,2-диметил-3-[(Z)-2(метоксикарбонил)-этенил]-циклопропан-1-карбоксилат (R,S) a-циано-3-феноксибензила Этап А: (1R, цис) 2,2-диметил-3-(1,8-дибром-2оксопропил)-циклопропан-1-карбоксилат (R, S) aциано-3-феноксибензила В среде инертного газа смешивают 0,380г (1R, цис) 2,2-диметил-3-(2-оксопропил)-циклопропан-1карбоксилата (R, S) a-циано-3-феноксибензила и 4 см3 тетрахлорметана, после чего при температуре около +15°С медленно добавляют 102 мкл брома в 1 см3 тетрахлорметана и взбалтывают в течение 4 ч. Затем концентрируют досуха при температуре около +30°С и получают 0,530 г искомого сырого продукта, используемого на следующем этапе без дополнительной обработки. Продукт может быть очищен путем хроматографии на двуокиси кремния (элюант: метиленхлорид - гексан (8: 2)). Спектр ЯРМ СDСl3 250 МГц млн-1 1,16-1,23-1,25-1,27: СН3 спарен.; 1,88 - 2,07: Н1 и Н3 цис; 4,06 (d) и 4,39 (d), 4,22: -CO-CH2Br; 5,20 (d) и 5,36 (d): -CO-CH-Br; 6,25 и 6,38: CO2-CH-CN; от 6,95 до 7,45: ароматические соединения. Исходный сложный эфир получают следующим образом. В среде инертного газа смешивают 0,344 г 2,2диметил-3-(2-оксопропил)-циклопропан-1-карбоновой кислоты, 3 см3 метиленхлорида, 0,48 см3 пиридина и 0,445 г дициклогексилкарбодиимида, а затем добавляют раствор 0,471 г (R,S) a-циано-3феноксибензилового спирта в 2 см3 метиленхлорида и несколько миллиграммов диметиламинопиридина. Затем взбалтывают при комнатной температуре в течение 18 ч, фильтруют и концентрируют досуха при температуре +30°С. Остаток подвергают хроматографии на двуокиси кремния (элюант: циклогексан - этилацетат (75: 25)), в результате чего получают 0,594 г целевого продукта. Спектр ЯРМ СDСl3 250 МГц От 1,11 до 1,28: СН3 спарен.; от 1,50 до 1,68: Н циклопропил; 2,10 (s), 2,16 (s) (3H): -СОСН3; 2,85 (m): =C-CH2-CH; 6,27 (s): -СО2-СН-; от 7,03 до 7,45: ароматические соединения. Инфракрасный спектр (СНСl3) Поглощение >С=О 1735, 1712 см-1 -Æ-О-Æ 1588, 1498 см-1 Этап Б: (1R, цис) 2,2-диметил-3-[(Z)-2метоксикарбонил)-этенил]-циклопропан-1-карбоксилат (R, S) a-циано-3-феноксибензила Операции выполняются так же, как на вышеописанном этапе Б примера 7, используя в качестве исходного продукта дибромистый продукт, полученный на вышеописанном этапе А. После очистки, как описано на вышеописанном этапе Б примера 7, получают целевой продукт. Пример 9: (1R, цис) 2,2-диметил-3-[(Z)-2[(1,1,1,3,3,3-гексафтор)-пропоксикарбонил]-этенил]-циклопропан-1-карбоксилат (R,S) a-циано-3феноксибензила В среде инертного газа промывают циклогексаном 0,030 г гидрида натрия в виде 50процентной взвеси в масле, а затем добавляют 1 см3 диметоксиэтана. После этого при температуре около 0°С медленно добавляют раствор 0,130 г гексафторизопропанола в 1 см3 диметоксиэтана и взбалтывают в течение 30 мин. при температуре 0/+5°С. Раствор охлаждают до -5°С и добавляют раствор 0,163 г (1R, цис) 2,2-диметил3-(1,3-дибром-2-оксопропил)-циклопропан-1-карбоксилата (R,S) a-циано-3-феноксибензила, полученного как описано на этапе А примера 8, в 1 см3 диметоксиэтана и взбалтывают в течение 1 ч 30 мин. Затем вливают в водный раствор 1 н. хлористоводородной кислоты, экстрагируют с помощью метиленхлорида, высушивают органическую фазу и выпаривают досуха. Остаток подвергают хроматографии на двуокиси кремния (элюант: метиленхлорид - гексан (8: 2)), в результате чего получают 0,056 г целевого продукта. Спектр ЯРМ СDСl3 250 МГц 1,26 (s), 1,30 (s), 1,35 (s), 1,36 (s): СН3 спарен.; 2,10 (d), 3,21 (m): H1/Н3 цис; 5,8 (септ): Н СО2СН(СF3)2; 6,02 (dm), 6,08 (dm): Н в п. 2'; 6,32 (s), 6,34 (s): Н в п. a; от 6,81 до 7,5 (m): Н ароматич. и Н в п. 1'. 13 39851 Пример 10: (1R, цис) 2,2-диметил-3-[(Z)-2[(1,1,1,3,3,3-гексафторпропокси)-карбонил]-этенил]-циклопропан-1-карбоксилат (R,S) a-циано-3феноксибензила Этап А: (1R, цис) 2,2-диметил-3-(1,3-дихлор-2оксопропил)-циклопропан-1-карбоксилат (R, S) aциано-3-феноксибензила В среде инертного газа смешивают 0,300 г (1R, цис) 2,2-диметил-3-(оксопропил)-циклопропан-1-карбоксилата (R, S) a-циано-3-феноксибензила, полученного как указано в примере 8, 6 см3 хлороформа и 160 мкл хлористого сульфурила. Затем смесь взбалтывают при комнатной температуре в течение 1 ч и концентрируют досуха. Таким образом, получают 0,546 г сырого искомого сырого продукта, используемого без дополнительной обработки на следующем этапе. Этап Б: (1R, цис) 2,2-диметил-3-[(Z)-2[(1,1,1,3,3,3-гексафтор)-пропоксикарбонил)-этенил]-циклопропан-1-карбоксилат (R, S) a-циано-3феноксибензила В среде инертного газа при температуре около -10°С смешивают 1 см3 толуола и 0,02 г гидрида натрия, растворенного на 50% в масле, а затем медленно добавляют 200 мкл гексафторизопропанола и 1 см3 толуола. Смесь взбалтывают при температуре -10°С в течение 35 мин. и добавляют 0,1 г сырого продукта, полученного на этапе А, растворенного в 0,5 см3 толуола. Затем температуре смеси дают подняться до комнатной, и взбалтывают в течение 2 ч. Растворитель выпаривают и остаток подвергают хроматографии на двуокиси кремния (элюант: циклогексан – этилацетат (85:15)), в результате чего получают целевой продукт, идентичный продукту, полученному в примере 9. Пример 11: (1R, цис) 2,2-диметил-3-[(Z)-2[(1,1,1,3,3,3-гексафторпропокси)-карбонил]-этенил]-циклопропан-1-карбоксилат трет.-бутила Этап А: (1R, цис) 2,2-диметил 3-(1,3-дибром-2оксопропил)-циклопропан-1-карбоксилат трет.бутила В среде инертного газа смешивают 0,113 г (1R, цис) 2,2-диметил-3-(2-оксопропил)-циклопропан-1-карбоксилата трет.-бутила, 3 см3 тетрагидро-фурана, а затем добавляют при температуре +5°С 0,34 г пербромида гидробромида пиридиния. После этого смесь взбалтывают при комнатной температуре в течение 1 ч, центрифугируют и концентрируют досуха. Остаток подвергают хроматогра-фии на двуокиси кремния (элюант: циклогексан - этилацетат (7:3)), в результате чего получают 0,165 г искомого продукта. Спектр ЯРМ СDСl3 250 МГц От 1,16 до 1,28: СН3 спарен.; 1,43 и 1,40: Н tBu; от 1,7 до 1,9: H1 и Н3; 4,08 (d), 4,36 (d) и 4,29: CO-CH2-Br; 5,24 (d) и 5,50 (d): CO-CHBr-. (1R, цис) 2,2-диметил-3-(2-оксопропил)циклопропан-1-карбоксилата трет.-бутила может быть получен нижеследующим способом. В среде инертного газа смешивают 0,17 г (1R, цис) 2,2-диметил-3-(1-оксопропил)-циклопропан-1карбоновой кислоты и 1,7 см3 этилацетата, после чего медленно добавляют раствор 0,36 г трет.бутилокси N,N'-диизопропилкарбодиимида в 1 см3 этилацетата. После 6-часового взбалтывания при комнатной температуре добавляют еще 0,15 г трет.-бутилокси N,N'-диизопропилкарбодиимида и продолжают взбалтывание еще в течение 16 ч. Затем центрифугируют и выпаривают растворитель. Остаток подвергают хроматографии на двуокиси кремния (элюант: циклогексан - этилацетат (7:3)), в результате чего получают 0,153 г искомого продукта. Инфракрасный спектр (СНСl3) Поглощение >С=О 1712, 1368 см-1 (СН3 tBu) Кислота Отсутствует Спектр ЯРМ СDСl3 250 МГц 1,18 (s) и 1,20 (s): СН3 спарен.; 1,35 (m), 1,50 (d, J=8,5): Н3 и Н1; 1,45 (s): Н tBu; 2,15 (s): Н СН3 в п. 3'; 2,79 (dd) и 2,93 (dd): Н СН2 в п. 1'. Трет.-бутилокси N,N'-диизопропилкарбодиимид может быть получен нижеследующим способом. В среде инертного газа смешивают 20 г трет.бутанола и 1,73 г монохлорида меди, после чего при температуре +30°С/+35°С добавляют 34 г N,N'-диизопропилкарбодиимида и взбалтывают, давая температуре дойти до уровня комнатной. Затем смесь центрифугируют, прополаскивают фильтр простым изопропиловым эфиром, выпаривают растворитель и перегоняют остаток при давлении 4-5 мм рт. ст. (t кип. 47-48°С). В результате получают 41,08 г искомого продукта. Спектр ЯРМ СDСl3 250 МГц 1,05 (d), 1,09 (d): СН3; 3,14 (m), 3,68 (m): -CH
ДивитисяДодаткова інформація
МПК / Мітки
МПК: C07C 69/747, C07C 253/30, C07C 67/00, C07C 323/19, C07C 255/39, C07C 67/14, C07C 327/00, C07C 67/313, A01N 53/00, C07C 67/307, C07C 235/06, C07B 41/00, C07D 209/48, C07D 307/28, C07C 69/743
Мітки: ефірів, 2,2-диметил-3-[(z)-1-пропеніл]циклопропанкарбонової, сполуки, складних, кислоти, проміжні, одержання, спосіб
Код посилання
<a href="https://ua.patents.su/18-39851-sposib-oderzhannya-skladnikh-efiriv-22-dimetil-3-z-1-propenilciklopropankarbonovo-kisloti-ta-promizhni-spoluki.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання складних ефірів 2,2-диметил-3-[(z)-1-пропеніл]циклопропанкарбонової кислоти та проміжні сполуки</a>












