Похідні дибензотіазепіну та їх застосування
Номер патенту: 105903
Опубліковано: 10.07.2014
Автори: Гульсізер Джеймс, Весоловскі Стівен, Шенві Ашоккумар Біккаппа, Відзовскі Ден, Піерсон Джр. М. Едвард, Едвардс Філ, Вуд Майкл, Муір Джеймс Кампбелл, Дамевуд Джеймс Р., Браун Дін
Формула / Реферат
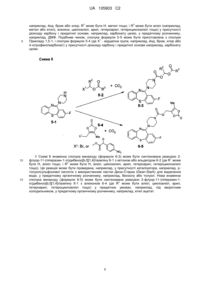
1. Сполука формули І
 І
І
або її фармацевтично прийнятна сіль,
де Z - Н, -C(=O)-R1, -C(=O)OR1, -CH(R1)-NHC(=O)R2, -C(=O)OCHR2OC(=O)R3, -CR1=CR2 або -CH=CHC(=O)R4,
R1, R2, R3 і R4 у кожному випадку незалежно є алкіл, циклоалкіл, арил, гетероарил або гетероциклоалкіл.
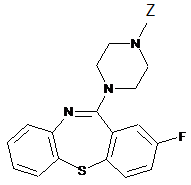
2. Сполука або її фармацевтично прийнятна сіль за п. 1, де Z - Н, та сполука є 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіном.
3. Фармацевтична композиція, яка містить сполуку або її фармацевтично прийнятну сіль за п. 1 або 2 і щонайменше один фармацевтично прийнятний носій.
4. Спосіб лікування психічного розладу, при якому здійснюють введення ссавцю, що потребує цього, терапевтично ефективної кількості сполуки або її фармацевтично прийнятної солі за п. 1 або 2.
5. Спосіб за п. 4, який відрізняється тим, що психічним розладом є біполярний розлад, тривожний розлад, розлад настрою, шизофренія або інший психічний розлад.
6. Спосіб за п. 4, який відрізняється тим, що психічним розладом є біполярний розлад.
7. Спосіб за п. 4, який відрізняється тим, що психічним розладом є шизофренія.
8. Застосування сполуки або її фармацевтично прийнятної солі за п. 1 або 2 для лікування психічного розладу.
9. Застосування за п. 8, яке відрізняється тим, що лікуванням є лікування біполярного розладу, тривожного розладу, розладу настрою, шизофренії або іншого психічного розладу.
10. Застосування за п. 8, яке відрізняється тим, що лікуванням є лікування біполярного розладу або шизофренії.
11. Застосування сполуки або її фармацевтично прийнятної солі за п. 1 або 2 для приготування медикаменту для лікування біполярного розладу, тривожного розладу, розладу настрою, шизофренії або іншого психічного розладу.
12. Застосування за п. 11, яке відрізняється тим, що лікуванням є лікування біполярного розладу або шизофренії.
13. Спосіб лікування психічного розладу, при якому здійснюють введення ссавцю, що потребує цього, терапевтично ефективної кількості фармацевтичної композиції за п. 3.
14. Спосіб за п. 13, який відрізняється тим, що психічним розладом є біполярний розлад, тривожний розлад, розлад настрою, шизофренія або інший психічний розлад.
15. Спосіб за п. 14, який відрізняється тим, що психічним розладом є біполярний розлад або шизофренія.
16. Спосіб отримання 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну, при якому здійснюють такі етапи:
реакція етилового естеру 5-флуор-2-меркаптобензойної кислоти з 1-флуор-2-нітробензолом з отриманням етилового естеру 5-флуор-2-(2-нітрофенілсульфаніл)бензойної кислоти;
перетворення етилового естеру 5-флуор-2-(2-нітрофенілсульфаніл)бензойної кислоти у етиловий естер 5-флуор-2-(2-амінофенілсульфаніл)бензойної кислоти;
циклізація етилового естеру 5-флуор-2-(2-амінофенілсульфаніл)бензойної кислоти з утворенням 2-флуор-10Н-дибензо[b,f][1,4]тіазепін-11-ону;
перетворення 2-флуор-10Н-дибензо[b,f][1,4]тіазепін-11-ону у 11-хлор-2-флуордибензо[b,f][1,4]тіазепін;
реакція 11-хлор-2-флуордибензо[b,f][1,4]тіазепіну з піперазином для отримання 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну.
17. Спосіб отримання 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну, при якому здійснюють такі етапи:
реакція 1-хлор-2-нітробензолу з 4-флуорбензолтіолом у присутності основи з отриманням 1-нітро-2-фенілсульфаніл-(4-флуорбензолу);
відновлення 1-нітро-2-фенілсульфаніл-(4-флуорбензолу) до 1-аміно-2-фенілсульфаніл-(4-флуорбензолу);
перетворення 1-аміно-2-фенілсульфаніл-(4-флуорбензолу) у феніловий естер [2-(4-флуорфенілсульфаніл)феніл]карбамінової кислоти;
циклізація такого естеру з утворенням 2-флуор-10Н-дибензо[b,f][1,4]тіазепін-11-ону;
перетворення 2-флуор-10Н-дибензо[b,f][1,4]тіазепін-11-ону у 11-хлор-2-флуордибензо[b,f][1,4]тіазепін;
реакція 11-хлор-2-флуор-дибензо[b,f][1,4]тіазепіну з піперазином для отримання 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну.
18. Спосіб отримання 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну, при якому здійснюють такі етапи:
реакція 2-амінобензолтіолу з метиловим естером 2,5-дифлуорбензойної кислоти з отриманням метилового естеру 2-[(Е)-2-аміно-1-ет-(Е)-иліденбут-2-енілсульфаніл]-5-флуорбензойної кислоти,
перетворення метилового естеру 2-[(Е)-2-аміно-1-ет-(Е)-иліденбут-2-енілсульфаніл]-5-флуорбензойної кислоти обробкою лугом з отриманням 2-[(Е)-2-аміно-1-ет-(Е)-иліденбут-2-енілсульфаніл]-5-флуорбензойної кислоти.
циклізація 2-[(Е)-2-аміно-1-ет-(Е)-иліденбут-2-енілсульфаніл]-5-флуорбензойної кислоти з отриманням 2-флуор-10Н-дибензо[b,f][1,4]тіазепін-11-ону;
перетворення 2-флуор-10Н-дибензо[b,f][1,4]тіазепін-11-ону у 11-хлор-2-флуордибензо[b,f][1,4]тіазепін;
реакція 11-хлор-2-флуордибензо[b,f][1,4]тіазепіну з піперазином для отримання 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну.
Текст
Реферат: Сполуки формули І, де Ζ визначено в описі, їх фармацевтично прийнятні солі, композиції, що містять їх, і способи лікування зазначеними сполуками біполярного розладу, тривожного розладу, розладу настрою або шизофренії, або іншого психозного розладу. UA 105903 C2 (12) UA 105903 C2 UA 105903 C2 5 10 15 20 25 30 35 40 45 50 55 60 Винахід стосується способів лікування біполярних розладів, розладів настрою, тривожних розладів, шизофренії і інших психозних розладів і сполук, придатних для використання у таких лікуваннях, їх фармацевтично прийнятних солей, фармацевтичних композиції, що містять такі сполуки, способу приготування таких сполук і їх проліків. Існують багато медикаментів, призначених для лікування біполярного розладу і шизофренії (наприклад, антиконвульсанти і атипові антипсихотики), а манії лікують декількома атиповими антипсихозниками (наприклад, рисперидоном, оланзапін і кетіапіном). Інші сполуки використовувались у клінічному лікуванні глибокого депресивного розладу (наприклад, ребоксетин і десимпрамін), а також біполярної депресії (кетіапін). Однак, бажаним є поліпшення терапії, тобто отримання кращих частот ремісії, більш ефективне лікування депресії і зниження побічної дії (наприклад, зниження седативної дії і набирання ваги). Починаючи з 1960-х p., наукові і клінічні дослідження були спрямовані на розуміння фармакології трициклічних нейролептичних сполук. Численні патенти і наукові публікації описували сотні різних трициклічних сполук з різними антипсихозними і антидепресивними якостями. У 1960-х у швейцарському патенті СН422793 (1961) і голландському патенті NL293210 (1963) було описано трициклічні сполуки. Через майже 50 років у роботі Behaviпероральн Approach to Nondyskinetic Antagonists: Identification of Seroquel, J. Med. Chem. 2001,44,372-380 було описано інші трициклічні сполуки. У 2009 р. у патентах США 7 491 715 В1 і 7 517 871 В1 були описані нові аналоги клозапіну. Незважаючи на високу фармакологічну активність, існуючі біполярні і антишизофренічні медикаменти виявляють змінну ефективність і профілі побічної дії. Хоча деякі існуючі медикаменти мають високу ефективність, частоти ремісії залишаються низькими. Проблемою залишаються безпечність і толерантність, оскільки приблизно 75% пацієнтів страждають від побічних явищ і відповідність лікування заслуговує значної уваги. Крім того, механізм дії атипових антипсихотиків є не дуже зрозумілим, наприклад, етикетка Seroquel стверджує: "механізм дії серекелю і інших медикаментів, ефективних у лікуванні шизофренії і гострих маніакальних епізодів, пов'язаних з біполярним розладом, є невідомим. Однак, було припущено, що ефективність цього медикаменту при шизофренії опосередковується антагонізмом комбінації допаміну типу 2 (D2) ι серотоніну типу 2 (5НТ2). Антагоністи, відмінні від допаміну і 5НТ2 з такою ж спорідненістю до рецептора, можуть прояснити деякі інші ефекти Seroquel. Антагонізм Seroquel до рецептора гістаміну Н1 може пояснити сонливість, що спостерігається при застосуванні цього медикаменту. Антагонізм Seroquel до адренергічних а1 рецепторів може пояснити ортостатичну гіпотонію, що викликається цим медикаментом" Подібним чином, етикетка оланзапіну стверджує: "механізм дії оланзапіну і інших медикаментів, ефективних у лікуванні шизофренії, є невідомим. Однак, було припущено, що ефективність цього медикаменту при шизофренії опосередковується антагонізмом комбінації допаміну типу 2 (D2) і серотоніну типу 2 і серотоніну типу 2 (5НТ2) антагонізм. Механізм оланзапіну у лікуванні гострих маніакальних епізодів, пов'язаних з біполярним розладом є невідомим. Антагоністи, відмінні від допаміну і 5НТ2 з такою ж спорідненістю до рецептора, можуть прояснити деякі інші терапевтичні якості і побічні явища оланзапіну. Антагонізм оланзапіну до мускаринових М1-5 рецепторів може пояснюватись його антихолінергічною дією. Антагонізм оланзапіну до рецептора гістаміну Н1 може пояснити сонливість, що спостерігається при застосуванні цього медикаменту. Антагонізм оланзапіну до адренергічних 1 рецепторів може пояснити ортостатичну гіпотонію, що викликається цим медикаментом" Отже, незважаючи на наявність описаних численних трициклічних сполук з антипсихозною і антидепресантною активністю, що використовуються у терапії, існує потреба у кращих шляхах лікування шизофренія і біполярної хвороби. Зокрема, бажаним є ефективне лікування депресивної фази біполярного розладу, а також лікування маніакальної фази, стабілізація настрою і підтримання хворих на біполярний розлад. Задачею винаходу є створення нового продукту, узгодженого з припустимою дією кетапіну у біполярному розладі (тобто, з потужними пригніченням NET і помірним антагонізмом D2). Клінічні дослідження кетіапіну дозволяють припустити, що наявність NET і D2 у межах від 30 до 60% може бути достатньою для отримання терапевтичної дії при біполярному розладі. Крім того, безпечність може бути підвищена зменшенням взаємодії з іншими об'єктами (наприклад, Н1, М1) при клінічних дозах до 50% NET. Терапевтичний агент з таким профілем, можна сподіватись, матиме переваги при лікуванні депресивної фази біполярного розладу, матиме потенціал для стабілізації настрою і підтримуватиме хворих на біполярний розлад з можливістю використання для полегшення манії, пов'язаною з біполярним станом. 1 UA 105903 C2 5 10 15 20 Отже, згідно з одним аспектом, бажано отримати щонайменше одну з таких властивостей: помірний антагонізм до D2; потужне пригнічення NET; або показник Kі зв'язування Н1 in vitro, близький до показника Kі для NET. B іншому аспекті бажано отримати щонайменше одну з властивостей in vitro: IK50 D2 GTPS менше приблизно 600 нМ; показник Kі зв'язування D2 менше приблизно 200 нМ; показник Kі пригнічення NET менше приблизно 50 нМ; або для Н1 Kі лежить у межах приблизно від щонайменше половини значення Kі для NET до більш, ніж Kі для NET. У ще одному аспекті, бажано ідентифікувати сполуку з потужним пригніченням норепінефринового транспортера (NET), з помірним антагонізмом до рецептора D2 і зниженою спорідненістю до вторинних об'єктів (наприклад, Н1, М1) порівняно з NET. У більш конкретному аспекті бажано ідентифікувати сполуку з потужним пригніченням NET (поглинання Kі < 50 нМ), помірним антагонізмом до D2 (IK50 GTPS < 500 нМ) і Кі Н1 і не більше Kі NET. Нами було ідентифіковано і описано тут сполуку 2-флуор-11-піперазин-1-ілдибензо[b,f][1,4]тіазепін, яка не була описана раніше і має бажані властивості, описані вище. Отже, далі описано фармакологічно активну сполуку 2-флуор-11-(піперазин-1іл)дибензо[b,f][1,4]тіазепін, її фармацевтично прийнятні солі, її проліки, композиції, що містять цю сполуку, її проліки або її фармацевтично прийнятну сіль і способи лікування біполярного розладу і шизофренії цією сполукою, її проліками або її фармацевтично прийнятною сіллю. Винахід стосується сполуки формули І: 1 25 30 35 40 1 1 або її фармацевтично прийнятної солі, де Z - H, -C(=O)-R , -C(=O)OR , -С(=О)ОСН2, -CH(R )2 2 3 1 2 4 1 2 3 4 NHC(=O)R , -C(=O)OCHR OC(=O)R , -CR =CR або -CH=CHC(=O)R і кожна R , R , R і R у кожному випадку є незалежно алкіл, циклоалкіл, арил, гетероарил або гетероциклоалкіл або як описано тут. Винахід також включає щонайменше одну композицію, яка містить сполуку формули І або її фармацевтично прийнятну сіль. У деяких втіленнях композиції включають фармацевтично прийнятний носій, розріджувач або ексципієнт. Винахід також стосується також способів лікування психічних розладів, які включають введення ссавцю терапевтично ефективної кількості сполуки формули І або її фармацевтично прийнятної солі, і, зокрема, стосується способів лікування психічних розладів, які включають введення ссавцю терапевтично ефективної кількості сполуки формули II: або її фармацевтично прийнятної солі. Винахід, крім того, стосується способів лікування біполярного розладу, розладів настрою, шизофренії і інших психозних розладів або тривожних розладів, який включає введення суб'єкту терапевтично ефективної кількості сполуки формули І або формули II, або їх фармацевтично прийнятної солі. Зокрема, винахід стосується способів лікування біполярного розладу, розладу настрою, шизофренії і інших психозних розладів або тривожного розладу, який включає введення суб'єкту терапевтично ефективної кількості сполуки формули Il або її фармацевтично прийнятної солі. 2 UA 105903 C2 5 10 Винахід включає сполуку формули І або формули Il або їх фармацевтично прийнятну сіль, призначені для використання у лікуванні шизофренії і інших психозних розладів, тривожного розладу і/або розладу настрою. Винахід включає також сполуку формули І або формули Il або їх фармацевтично прийнятну сіль, призначені для використання у виготовленні медикаменту для лікування шизофренії і інших психозних розладів, біполярного розладу, тривожного розладу і/або розладу настрою. Крім того, винахід включає спосіб приготування сполук формули І або формули Il і їх фармацевтично прийнятних солей; інтермедіатів, корисних у приготуванні таких сполук і способи приготування і використання таких інтермедіатів. Винахід включає сполуки формули І: 1 15 20 25 30 1 1 і їх фармацевтично прийнятні солі, де Z - H, -C(=O)-R , -C(=O)OR , -C(O)OCH2, -CH(R )2 2 3 1 2 4 1 2 3 4 NHC(=O)R , -C(=O)OCHR OC(=O)R , -CR =CR або -CH=CHC(=O)R і кожна R , R , Rі R у кожному випадку незалежно є алкіл, циклоалкіл, арил, гетероарил або гетероциклоалкіл або згідно з описом. Зокрема, винахід включає сполуку формули І, де Z є H формули II: тобто 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепін і його фармацевтично прийнятні солі. Сполуки, описані тут, можуть бути приготовлені описаними тут способами органічного синтезу, які є відомими фахівцям, або є їх варіантами. Вихідні матеріали і попередник, використані в описаних процесах є комерційно доступними можуть бути легко приготовлені відомими способами органічного синтезу, або як описано тут. Зрозуміло, що функціональності у різних частинах молекули мають бути сумісними з запропонованими реагентами і реакціями. Такі обмеження для замісників, що мають бути сумісними з умовами реакції, є очевидними для фахівця і, у такому випадку слід використовувати інші способи. На Схемі 1 амідна сполука винаходу (формула 1-3) може бути приготовлена реакцією 1 сполуки Прикладу 1 з кислотою або кислотною похідною 1-2 (де X - OH або відщепна група, 1 1 така, як бром, хлор,4-нітрофенокси, OC(=O)R тощо; a R може бути алкіл, циклоалкіл, арил, гетероарил, гетероциклоалкіл тощо) у належних умовах, відомих фахівцям з органічного синтезу. 3 UA 105903 C2 5 10 15 20 25 30 Наприклад, сполучення амінної сполуки 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну 1 1-1 з кислотою 1-2 (де X - OH) може бути проведене звичайним способом створення амідного зв'язку, наприклад, з сполучаючим реагентом. Для створення амідного зв'язку можуть бути використані різні придатні сполучаючі реагенти, відомі фахівцям. Деякі необмежуючі приклади придатних сполучаючих реагентів включають (не лише) бензотріазоловмісні сполучаючі реагенти, наприклад, N-гідроксибензотріазол (HOBt), бензотріазол-1ілокситрис(диметиламіно)фосфонію (BOP) і гексафлуорфосфат 2-(1Н-бензотріазол-1-іл)-1,1,3,3тетраметилуронію (HBTU); азабензотріазоловмісний реагент, наприклад, гексафлуорфосфат O(7-азабензотріазол-1-іл)-N, N, N'N'-тетраметилуронію (HATU); і дикарбоіміди, наприклад, 1-етил3-(3-диметиламінопропіл)-карбодіімід (EDC) і дициклогексил карбодіімід (DCC). Реакція сполучення може бути проведена у придатному органічному розчиннику. Деякі придатні органічні розчинники включають полярні органічні розчинники наприклад, спирт (метанол, етанол або ізопропанол) або тетрагідрофуран (ТГФ). Деякі придатні органічні розчинники включають апротонні розчинники і полярні апротонні органічні розчинники, наприклад, Ν,Νдиметилформамід (ДМФ), ТГФ, диметилсульфоксид (ДМСО) або метилен хлорид. Сполучаюча реакція може бути проведена у присутності придатної основи при придатній температури протягом часу, достатнього для утворення амідної сполуки 1-3. Придатні основи включають органічні основи, наприклад, третинні аміни (наприклад, тріетиламін (Et 3N або TEA), діізопропілетиламін (iPr2NEt або DIPEA) і/або диметила-мінопіридин (DMAP)). У деяких втіленнях реакційну суміш нагрівають до підвищеної температур (вище кімнатної). У деяких втіленнях реакційну суміш нагрівають до температури приблизно 40°C, приблизно 50°C, приблизно 60°C, приблизно 70°C, приблизно 80°C, приблизно 90°C, приблизно 100°С, приблизно 110°C, приблизно 120°C, приблизно 130°C, приблизно 140°С, приблизно 150°С або приблизно 160°С. Проходження реакції можна спостерігати звичайними способами, наприклад, ТШХ або ЯМР. 1 В іншому варіанті кислота 1-2 (де X - OH) може бути перетворена у більш реактивну 1 1 кислотну похідну 1-2 (де X - бром, хлор, 4-нітрофенокси, OC(=O)R тощо) наприклад, кислотний хлорид, естер, (змішаний) ангідрид і кислотні похідні можуть бути, як варіант, відділені. Кислотна похідна може далі реагувати з 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіном 1-1, утворюючи амід 1-3 у придатних умовах, наприклад, у присутності придатної основи (наприклад, тріетиламіну або піридину). На Схемі 2 карбаматна сполука винаходу (формули 2-3) може бути синтезована реакцією 1 сполуки Прикладу 1,2-1) з хлорформатом 2-2 (де R може бути алкіл, арилалкіл тощо). 35 4 UA 105903 C2 5 10 15 20 25 Ця реакція може бути проведена у придатному органічному розчиннику, наприклад, полярному апротонному органічному розчиннику (наприклад, метилен хлориді) у присутності придатної основи, наприклад, третинного аміну (наприклад, тріетиламіну (Et 3N або TEA), діізопропілетиламіну (JPr2NEt або DIPEA), піридину і/або диметила-мінопіридину (DMAP)). У Схемі 3 карбаматна сполука винаходу (формули 3-5) може бути синтезована через 4нітрофеніл карбонатний інтермедіат 3-3. 4-нітрофеніл хлорформат 3-1 може бути введений у реакцію з спиртом 3-2 у придатному органічному розчиннику, наприклад, полярному апротонному органічному розчиннику (наприклад, хлороформі) у присутності придатної основи, наприклад, третинного аміну (наприклад, тріетиламіну (Et3N або TEA), діізопропілетиламіну (JPr2NEt або DIPEA), піридину і/або диметиламінопіридину (DMAP)) з утворенням 4-нітрофеніл карбонатного інтермедіату 3-3, який може бути введений у реакцію з 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіном 3-4 у придатному органічному розчиннику, наприклад, полярному апротонному органічному розчиннику (наприклад, ДМФ або гексаметилфосфораміді) з утворенням карбамату 3-5. У Схемі 4, карбаматна сполука винаходу (формули 4-4) може бути синтезована реакцією сполуки Прикладу 1, (4-1) з хлорформатом 4-2 або 4-нітрофеніл карбонатною сполукою 4-3 (де 2 3 R може бути H, метил тощо; і R може бути алкіл (наприклад, метил або етил), алкокси, циклоалкіл, арил, гетероарил, гетероциклоалкіл тощо). Ці реакції можуть бути проведені в умовах, подібних до описаних у Схемах 2 і 3. Хлорформати 4-2 можуть бути приготовлені способами, наприклад, подібними до описаного Folkmann et al., Synthesis, 1990,1159-1166. Нітрофеніл карбонати 4-3 можуть приготовлені способами, наприклад, подібними описаному Александером () і співробітниками у J. Med. Chem., 1988,31,318-322, включеному посиланням. У Схемі 5, використовуючи спосіб, подібний до описаного Lin et al., Bioorganic and Medicinal Chemistry Letters, 1997,7,2909-2912, можна приготовити карбаматну сполуку винаходу (формули 5-3) реакцією сполуки Прикладу 1,5-1, з сполукою формули 5-2 (де X - відщепна група, 5 UA 105903 C2 2 5 10 15 3 наприклад, йод, бром або хлор; R може бути H, метил тощо; і R може бути алкіл (наприклад, метил або етил), алкокси, циклоалкіл, арил, гетероарил, гетероциклоалкіл тощо) у присутності діоксиду карбону і придатної основи, наприклад, карбонату цезію, у придатному розчиннику, наприклад, ДМФ. Подібним чином, сполука формули 5-5 може бути приготовлена з сполуки 1 Прикладу 1,5-1, і сполуки формули 5-4 (де X - відщепна група, наприклад, йод, бром, хлор або 4-нітрофенілкарбонат) у присутності діоксиду карбону і придатної основи наприклад, карбонату цезію. У Схемі 6 енамінна сполука винаходу (формули 6-3) може бути синтезована реакцією 21 флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну 6-1 з кетоном або альдегідом 6-2 (де R може 2 бути H, алкіл тощо; і R може бути H, алкіл, циклоалкіл, арил, гетероарил, гетероциклоалкіл тощо). Ця реакція може бути проведена, наприклад, у присутності каталізатора, наприклад, ртолуолсульфонової кислоти з використанням пастки Дина-Старка (Dean-Stark) для видалення води, у придатному органічному розчиннику, наприклад, бензолу або толуол. Нова енамінна сполука винаходу (формули 6-5) може бути синтезована реакцією 2-флуор-11-(піперазин-14 іл)дибензо[b,f][1,4]тіазепіну 6-1 з алкіноном 6-4 (де R може бути алкіл, циклоалкіл, арил, гетероарил, гетероциклоалкіл тощо) у придатних умовах, наприклад, під зворотним холодильником, у придатному органічному розчиннику, наприклад, етил ацетат. 6 UA 105903 C2 5 10 15 20 25 У Схемі 7 нова сполук винаходу основного типу Маніха (Mannich) (формули 7-4) може бути 1 приготовлена реакцією сполуки Прикладу 1,7-1, з альдегідом 7-2 (де R може бути H, алкіл, циклоалкіл, арил, гетероарил, гетероциклоалкіл тощо) і нуклеофілом, наприклад, амідом 7-3 (де 2 R може бути алкіл, циклоалкіл, арил, гетероарил, гетероциклоалкіл тощо) у придатних умовах, наприклад, під зворотним холодильником. Наприклад, 2-флуор-11-(піперазин-1іл)дибензо[b,f][1,4]тіазепін, водний розчин формальдегіду і амід 7-3 нагрівати до флегми 1 спиртовому розчиннику, наприклад, етанолі для отримання сполуки формули 7-4, де R - H. Слід відзначити, що в усіх схемах, описаних тут, якщо на групі-заміснику є функціональні 1 2 3 (реактивні) групи, наприклад, R , R , R тощо, за бажання є можливою подальша модифікація. Наприклад, група CN може бути гідролізована до амідної групи; карбонова кислота може бути перетворена в амід або в естер, який може бути відновлений до спирту, який також може бути додатково модифікований. В іншому прикладі група OH може бути перетворена в іншу відщепну групу, наприклад, мезилат, придатний для нуклеофільного заміщення, наприклад, CN. Фахівцю такі модифікації є зрозумілими. Отже, сполука формули І, яка має замісника, що містить функціональну групу, може бути перетворена в іншу сполуку формули І з іншим замісником. Визначення, наведені далі призначено роз'яснювати терміни, використані в описі. "Тут" означає всю заявку. Сполуки у винаході можуть існувати у конкретних стереоізомерних формах. Винахід включає усі такі сполуки, включаючи цис- і транс-ізомери, R- і S-енантіомери, діастереомери, (D)ізомери, (L)-ізомер, їх рацемічні суміші і інші їх суміші, що входять в об'єм винаходу. У заміснику можуть бутиприсутні додаткові асиметричні атоми карбону, наприклад, алкільна група. Всі так ізомери, а також їх суміші включено в об'єм винаходу. Сполуки, тут описані, можуть мати асиметричні центри. Сполуки винаходу, що містять асиметрично заміщений атом, можуть бути ізольовані в оптично активній або рацемічній формах. Приготування оптично активних форм є добре відомим, наприклад, розрізненням рацемічних форм або синтезом з оптично активних 7 UA 105903 C2 5 10 15 20 25 30 35 40 45 50 55 60 матеріалів. За потреби розділення рацемічних матеріалів може бути здійснене відомими способами. Оптично активні форми сполуки винаходу можуть бути приготовлені, наприклад, хіральним хроматографічною сепарацією рацемату, синтезом з оптично активних матеріалів або асиметричним синтезом, базованим на процедурах, описаних нижче. Коли сполуки містять хіральні центри, усі індивідуальні оптичні форми, наприклад, енантіомери, епімери і діастереоізомери, а також рацемічні суміші сполук входять в об'єм винаходу. Оптичні ізомери можуть бути отримані у чистій формі за стандартними процедурами, які включають (не лише) формування діастереомерних солей, кінетичне розрізнення і асиметричний синтез, (див., наприклад, Jacques et al., Enantiomers, Racemates and Reрозчинs (Wiley lnterscience, New York, 1981); Wilen et al., Tetrahedron, 1977,33,2725; Eliel, Stereochemistry of Carbon Compounds (McGraw-Hill, NY,1962); Wilen, S.H. Tables of Resolving Agents and Optical Reрозчинs p. 268 (E. L. Eliel, Ed., Univ. of Notre Dame Press, Notre Dame, IN 1972), включені посиланням. Винахід включає усі можливі регіоізомери і їх суміші, які можуть бути отримані у чистій формі стандартними процедурами сепарації, включаючи (не лише), колонну хроматографію, тонкошарову хроматографію, рідинну хроматографію високої ефективності. Деякі сполуки винаходу можуть існувати як геометричні ізомери, наприклад E і Z ізомери алкенів. Сполука винаходу 2-флуор-11-піперазин-1-іл-дибензо[b,f][1,4]тіазепін, може (теоретично) існувати у (E) або (Z) формах, однак, спостереженим був (Е)-2-флуор-11піперазин-1-іл-дибензо[b,f][1,4]тіазепін. Винахід включає будь-які геометричні ізомери сполуки винаходу. Тут термін "арил" означає ароматичну кільцеву структуру з 5-14 атомів карбону. Кільцеві структури, що містять 5, 6, 7 і 8 атомів карбону є однокільцевими ароматичними групами, наприклад, фенілом. Кільцеві структури, що містять 8, 9, 10, 11, 12, 13, або 14 є поліциклічними компонентами, в яких щонайменше один карбон є спільним з будь-якими двома суміжними кільцями (наприклад, кільця є "злитими кільцями"), наприклад, нафтилом. Ароматичне кільце може бути заміщене в одній або більше кільцевих позицій замісниками, описаними вище. Термін "арил" також включає поліциклічні кільцеві системи з двома або більше циклічними кільцями, в яких два або більше карбонів є спільними з двома суміжними кільцями (кільця є "злитими кільцями"), де щонайменше одне з кілець є ароматичним, наприклад, іншими циклічними кільцями можуть бути цикло-алкіли, циклоалкеніли або циклоалкінілами. Термін орто, мета і пара відповідають 1,2-, 1,3- і 1,4-дизаміщеним бензолам, відповідно. Наприклад, назви 1,2-диметилбензол і орто-диметилбензол є синонімами. Терміни "алкіл", "алкіленіл" або "алкілен", використані як такі або як суфікс або префікс включають як розгалужені, так і лінійні насичені аліфатичні гідрокарбонові групи з 1-12 атомами карбону або, якщо зазначено конкретну кількість атомів карбону, то ця кількість присутня. Наприклад "C1-6 алкіл" означає алкіл з 1, 2, 3, 4, 5 або 6 атомами карбону. Приклади алкілу включають (не лише), метил, етил, n-пропіл, і-пропіл, n-бутил, і-бутил, втор-бутил, t-бутил, пентил і гексил або будь-яку їх підмножину. "C1-3 алкіл" як кінцевий замісник або алкіленова (або алкіленільна) група, що зв'язує два замісники, конкретно включають як розгалужені, так і лінійні метил, етил і пропіл. "Алкокси" або "алкілокси" репрезентує алкільну групу, визначену вище, з вказаною кількістю атомів карбону, з'єднаними оксигеновим містком. Приклади алкокси включають (не лише), метокси, метокси, n-пропокси, ізопропокси, n-бутокси, ізобутокси, t-бутокси, n-пентокси, ізопентокси, циклопропілметокси, алілокси, і пропаргілокси або будь-яку їх підмножину. Подібним чином, "алкілтіо" або "тіоалкокси" репрезентують алкільну групу, визначену вище, з вказаною кількістю атомів карбону, з'єднаних сульфуровим містком. Тут "фармацевтично прийнятний" стосується сполук, матеріалів, композицій, і/або дозованих форм, які є, згідно з обґрунтованими медичними міркуваннями, придатними для використання у контакті з тканинами людини і тварин без надмірної токсичності, подразнення, алергічних реакцій або інших проблем або ускладнень, з урахуванням розумного відношення корисність/ризик. Термін "фармацевтично прийнятні солі" стосується похідних описаних сполук, де первісна сполука пов'язана з кислотним або основним контріоном. Наприклад, фармацевтично прийнятні солі включають солі неорганічних кислот, наприклад, гідрохлорної кислоти, нітрокислоти, фосфорної, сульфурової, гідройодної, азотистої і фосфористої кислоти. Фармацевтично прийнятні солі можуть також бути отримані з органічними кислотами, включаючи аліфатичні моно-ідикарбоксилати і ароматичні кислоти. Інші фармацевтично прийнятні солі включають (не лише), гідрохлорид, сульфат, піросульфат, бісульфат, бісульфіт, нітрат, фосфат, солі оцтової, гліколевої, молочної, піровиноградної, малонової, бурштинової, глютарової, фумарової, 8 UA 105903 C2 5 10 15 20 25 30 35 40 45 50 55 яблочної, виннокам'яної, лимонної, аскорбінової, малеїнової, гідроксималеїнової, бензойної, гідроксибензойної, фенілоцтової, цинамової, силіцилової, 2-феноксибензойної, ртолуолсульфонової кислоти і інших сульфонових кислот, наприклад, метансульфонової кислоти і 2-гідроксиметан-сульфонової кислоти. Сполуки можуть існувати, різних таутомерних формах і посилання на сполуки включають усі такі форми. Для визначеності, коли сполука може існувати в одній з декількох таутомерних форм і лише одна з них конкретно описана або показана, усі інші все одно входять в об'єм винаходу. Сполуки винаходу можуть включати гідрати і сольвати, і деякі сполуки винаходу можуть існувати у сольватованій, наприклад, гідратованій, а також у несольватованій формах. Винахід включає усі такі сольватовані форми сполук винаходу. Похідні, що є проліками сполуки, можуть перетворюватись in vivo або in vitro у первісну сполуку. Звичайно щонайменше одна з біологічних активностей сполуки відновлюється у проліках сполуки і може бути активована перетворенням проліків з вивільненням сполуки або її метаболітів. Деякі проліки є естерами активної сполуки (наприклад, фізіологічно прийнятним метаболічно лабільним естером). Під час метаболізму естерна група (-C(=O)OR) розщеплюється, утворюючи активний медикамент. Такі естери можуть бути створені естерифікацією, наприклад, будь-якої з карбонокислотних груп (-С(=О)ОН) у первісній сполуці з (якщо потрібно) попереднім захистом будь-яких інших реактивних груп первісної сполуки і з подальшим зняттям захисту (за потреби). Приклади таких метаболічно лабільних естерів включають (не лише) сполуки формули C(=O)OR, де R є С1-7алкіл (наприклад, Me, Et, -nPr, -iPr, -nBu, -sBu, -iBu, tBu); С1-7аміноалкіл (наприклад, аміноетил; 2-(N, N-діетиламіно)етил; 2-(4-морфолін)етил); і ацилокси-С1-7алкіл (наприклад, ацилоксиметил; ацилоксиетил; півалоїлоксиметил; ацетоксиметил; 1-ацетоксиетил; 1-(1-метокси-1-метил)етил-карбонілоксиетил; 1-(бензоїлокси)етил; ізопропоксикарбонілоксиметил; 1-ізопропокси-карбонілоксиетил; циклогексилкарбонілоксиметил; 1-циклогексил-карбонілоксиетил; циклогексилокси-карбонілоксиметил; 1циклогексилокси-карбонілоксиетил; (4-тетрагідропіранілокси)-карбонілоксиметил; 1-(4тетрагідропіранілокси)карбонілоксиетил; (4-тетрагідропіраніл)-карбонілоксиметил; і 1-(4тетрагідропіраніл)карбонілоксиетил), або будь-яку їх підмножину. Сполука формули І або формули Il або її фармацевтично прийнятна сіль, або фармацевтична композиція або рецептура, що містить сполуку формули І або формули Il або її фармацевтично прийнятну сіль, можуть бути введені одночасно, паралельно, послідовно або окремо разом з іншими сполуками вибраними з групи, яку складають: (і) антидепресанти, наприклад, амітриптилін, амоксапін, бупропіон, циталопрам, кломіпрамін, дезипрамін, доксепін, дулоксетин, ельзасонан, есциталопрам, флуоксамін, флуоксетин, гепірон, іміпрамін, інсапірон, мапротилін, нортриптилін, нефазодон, пароксетин, фенельзин, протриптилін, ребоксетин, робальзотан, сертралін, сибутрамін, тіонізоксетин, транілципромаїн, традозон, триміпрамін, венлафаксин і їх еквіваленти і фармацевтично активні ізомери і/або метаболіти; (іі) атипові антипсихотики, включаючи, наприклад, кетіапін і його фармацевтично активні ізомери і/або метаболіти; (ііі) антипсихотики, включаючи, наприклад, амісульприд, арипіпразол, азенапін, бензізоксидил, біфепрунокс, карбамазепін, клозапін, хлорпромазин, дебензапін, дивалопрекс, дулоксетин, езопіклон, галоперидол, ілоперидон, ламотригін, доксапін, мезоридазин, оланзапін, паліперидон, перфеназин, фенотіазин, фенілбутліперидон, пімозид, прохлорперазин, рисперидон, сертиндол, сульприд, супроклон, суриклон, тіоридазин, трифлуоперазин, триметозин, вальпроат, вальпрову кислоту, зопіклон, зотепін, ципразидон і їх еквіваленти і фармацевтично активні ізомери і/або метаболіти; (iv) анксіолітики, включаючи, наприклад, альнеспірон, аазапірони, бензодіазепіни, барбітурати і їх еквіваленти і фармацевтично активні ізомери і/або метаболіти. Типові анксіолітики включають адиназолам, альпіразолам, бальзепам, бентазепам, бромазепам, бротизолам, буспралін, клоназепам, клоразенат, хлордіазероксид, ципразепам, діазепам, дифенгідрамін, естазолам, фенобам, флунітразепам, флуразепам, фоказепам, форазепам, лорметазепам, мепробамат, мідазолам, нітразепам, оксазепам, празепам, квазепам, реклазепам, траказолат, трепіпам, темазепам, тріазолам, ульдизепам, золазепам і їх еквіваленти і фармацевтично активні ізомери і метаболіти; (ν) антиконвульсанти, включаючи, наприклад, карбамазепін, вальпроат, ламотрогін, габапентин і їх еквіваленти і фармацевтично активні ізомери і метаболіти; 9 UA 105903 C2 5 10 15 20 25 30 35 40 45 50 55 60 (vi) антиальцгеймерні терапії, включаючи, наприклад, донепезил, мемантин, такрин і їх еквіваленти і фармацевтично активні ізомери і метаболіти; (vii) антипаркінсонівські терапії, включаючи, наприклад, депреніл, L-допа, інгібітори Requip, Mirapex, MAOB, наприклад, селегін і разагілин, інгібітори comР, наприклад, TaBMar, інгібітори А2, інгібітори поглинання допаміну, антагоністи NMDA, агоністи нікотину, агоністи допаміну і інгібітори нейронної синтази нітрооксиду і їх еквіваленти і фармацевтично активні ізомери і метаболіти; (viii) антимігренні терапії, включаючи, наприклад, альмотриптан, амантадин, бромкриптин, булальбітал, каберголін, дихлоральфеназон, елетриптан, фровітриптан, лізурид, наратриптан, перголід, праміпексол, ризатриптан, ропінірол, суматриптан, зольмітриптан, зомітриптан і їх еквіваленти і фармацевтично активні ізомери і метаболіти; (іх) антиінсультні терапії, включаючи, наприклад, абциксимаб, активаз, NXY-059, цитіколін, кробенетин, десмотеплазу, репінотан, траксопродил і їх еквіваленти і фармацевтично активні ізомери і метаболіти; (х) терапії нетримання сечі, включаючи, наприклад, дарафенацин, фальвоксат, оксибутинін, пропіверин, робальзотан, соліфенацин, тольтеродин і їх еквіваленти і фармацевтично активні ізомери і метаболіти; (хі) терапії нейропатичного болю, включаючи, наприклад, габапентин, лідодерм, прегаблін і їх еквіваленти і фармацевтично активні ізомери і метаболіти; (хіі) терапії ноцицептичного болю, наприклад, целекоксиб, еторикоксиб, лумаракоксиб, рофекоксиб, вальдекоксиб, диклофенак, локсопрофен, напроксен, парацетамол і їх еквіваленти і фармацевтично активні ізомери і метаболіти; (хііі) терапії безсоння, включаючи, наприклад алобарбітал, алонімід, амобарбітал, бензоктамін, бутабарбітал, капурид, хлорал, клоперидон, клоретат, декскламол, етхлорвінол, етомідат, глютетімід, галазепам, гідроксизин, мклоквалон, елатонін, мефобарбітал, метаквалон, мідафлур, нізобамат, пентобарбітал, фенобарбітал, пропофол, ролетамід, триклофос, секобарбітал, залеплон, золпідем і їх еквіваленти і фармацевтично активні ізомери і метаболіти або (xiv) стабілізатори настрою, включаючи, наприклад, карбамазепін, дивалпроекс, габапентин, ламотригін, літій, оланзапін, кветипамін, вальпроат, вальпроатову кислоту, верапаміл і їх еквіваленти і фармацевтично активні ізомери і метаболіти. (xv) ліганди 5НТ1В, наприклад, сполуки, описані y WO99/05134, WO02/08212; (xvi) агоністи mGluR2 наприклад, (1S,3R)-1-аміноциклопентан-1,3-дикарбонова кислота, (2S,3S,4S)альфа-(карбоксициклопропіл)гліцин і 3,5-дигідроксифенілгліцин або модулятори mGluR2, наприклад, описані у WO2004092135, WO2006071730, WO2008100715, WO2008150232 і WO2008150233; (xvii) альфа 7 нікотинові агоністи, наприклад, сполуки, описані у WO96/006098, WO97/030998, WO99/003859, WO00/042044, WO01/029034, WO01/160821, WO01/136417, WO02/096912, WO03/087102, WO03/087103, WO03/087104, WO04/016617, WO04/016616 і WO04/019947; (xviii) інгібітори рецептора хемокіну CCR1; (хіх) дельта опіоїдні агоністи, наприклад, сполуки, описані у WO97/23466 і WO02/094794; і (хх) ліганди 5HT10, антагоністи mGluR5, антагоністи рецептора NK1 і інгібітори повторного поглинання серотоніну. У таких комбінованих продуктах можуть бути використані сполуки формули І або формули Il або їх фармацевтично прийнятні солі в описаних тут дозах, а також інші фармацевтично активні агенти у відповідних межах дозування і/або дозах, наприклад, описані у згаданих тут публікаціях. Належні режими дозування, кількість введених доз кожного активного агенту і конкретні інтервали між введеннями доз кожного активного агенту залежать від суб'єкта, що отримує лікування, конкретного активного агенту і природи і важкості конкретного розладу або стану, що підлягає лікуванню. Композиції включають рецептуру активного компоненту або його фармацевтично прийнятної солі з фармацевтично прийнятним носієм, і, як варіант, іншими інгредієнтами. У фармацевтичних композиціях інертні фармацевтично прийнятні носії можуть бути твердими або рідкими. Наприклад, композиціям можуть бути надані відомі форми, наприклад, таблеток, капсул, водних або масляних розчинів, суспензій, емульсій, кремів, мазей, желе, носових уприскувань, супозиторіїв, тонко подрібнених порошків або аерозолів або розпилювачів для інгаляції, і, зокрема, для парентерального використання (включаючи внутрішньовенні, внутрішньом'язові ін'єкції або інфузії) стерильні водні або масляні розчини або суспензії, або стерильні емульсії. 10 UA 105903 C2 5 10 15 20 25 30 35 40 45 50 55 60 Рідкі форми композицій включають розчини, суспензії і емульсії. Стерильні вода або водопропіленгліколеві розчини активної сполуки можуть бути прикладами рідких препаратів, придатних для парентерального введення. Рідкі композиції можуть також мати форму водопропіленгліколевих розчинів. Водні розчини для перорального введення можуть бути приготовлені розчиненням активного компонента у воді і додання (за бажання) придатних забарвлювачів, смакових добавок, стабілізаторів і загущувачів. Водні суспензії для перорального використання можна приготовляти диспергуванням тонко подрібненого активного компоненту у воді разом з в'язким матеріалом, наприклад, природною або синтетичною гумою, смолами, метилцелюлозою, натрійкарбоксиметил целюлозою і іншими суспендувальними агентами, відомими у фармацевтиці. Тверді форми композицій включають порошки, таблетки, дисперсні гранули, капсули, облатки і супозиторії. Твердим носієм можуть бути одна або більше речовин, які можуть бути також розріджувачами, смаковими агентами, солюбілізаторами, змащувачами, суспендувальними агентами, зв'язуючими або дезінтеграторами таблетки; ним може бути також інкапсуляційний матеріал. У порошках носієм є тонко подрібнена тверда речовина, домішана до тонко подрібненого активного компоненту. У таблетках активний компонент змішано з носієм, який має необхідні зв'язувальні властивості, у придатних пропорціях, з подальшими пресуванням для надання бажаних форми і розміру. Для приготування супозиторних композицій, легкоплавкий віск, наприклад, суміш гліцеридів жирних кислот і масла какао спочатку розплавляють і диспергують активний інгредієнт з перемішуванням. Розплавлену гомогенну суміш вливають у належні форми і залишають охолонути і затвердіти. Придатними носіями є карбонат магнію, стеарат магнію, тальк, лактоза, цукор, пектин, декстрин, крохмаль, трагант, метилцелюлоза, натрієва карбоксиметил целюлоза, легкоплавкий віск, масло какао тощо. Термін композиція також включає рецептуру активного компонента з інкапсуляційним матеріалом як носієм тобто капсулу, в якій активний компонент (з іншими носіями або без них) оточено носієм. Подібними чином облатки побудовано облатки. Фармацевтичні композиції можуть мати дозовану форму. У такій формі композиція поділена на одиничні дози, що містять належну кількість активного компоненту. Одиничні дози можуть бути пакетованими препаратами, де пакет містить дискретні кількості препаратів, наприклад, пакетованих таблеток, капсул і порошків у флаконах або ампулах. Одиничні дозовані форми можуть мати форму капсул, облаток або таблеток, або будь-якої іншої пакетованої форми. Способи приготування дозованих форм описано, наприклад, у Remington's Pharmaceutical Sciences, Mack Publishing Company, Easton, Pennsylvania, 15th Edition, 1975. Композиції можуть бути виготовлені придатними для будь-яких способів і засобів введення. Фармацевтично прийнятними носіями або розріджувачами є ті, що використовуються у рецептурах, придатних для перорального, ректального, назального, топікального (включаючи букальне і під'язичне), вагінального або парентерального (включаючи підшкірне, внутрішньом'язове, внутрішньовенне, інтрадермальне, інтратекальне, епідуральне, інтраперитонеальне, інтраторакальне, інтрацеребровентрикулярне і ін'єкцією у суглоби) введення. Рецептури можуть бути виготовлені як одиничні дозовані форми будь-якими відомими способами. Конкретна кількість сполуки формули І або формули Il або її фармацевтично прийнятної солі, яку можна вводити, становить від приблизно 0,25 мг/кг до приблизно 10 мг/кг, зокрема, пацієнту можна вводити від приблизно 0,25 мг/кг до приблизно 5 мг/кг of 2-флуор-11-(піперазин1-іл)дибензо[b,f][1,4]тіазепіну або його фармацевтично прийнятної солі, бажано, зокрема, вводити пацієнту, що страждає від біполярного розладу, від приблизно 0,25 мг/кг до приблизно 0,5 мг/кг 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну або його фармацевтично прийнятної солі. Бажано, зокрема, вводити пацієнту, що страждає від депресивної фази біполярного розладу, меншу кількість, а саме, від приблизно 0,25 мг/кг до приблизно 0,5 мг/кг 2флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну або його фармацевтично прийнятної солі, а пацієнту, що страждає від маніакальної фази біполярного розладу, можна вводити більшу кількість, а саме, від приблизно 0,25 мг/кг до приблизно 0,5 мг/кг 2-флуор-11-(піперазин-1іл)дибензо[b,f][1,4]тіазепіну або його фармацевтично прийнятної солі. Кількість активного інгредієнту у комбінації з одним або більше ексципієнтами для отримання одної дозованої форми залежить від суб'єкта і конкретного способу введення. Розмір терапевтично ефективної дози активних сполук для терапії або профілактики може бути різним згідно з природою і важкістю симптомів або станів, віку і статі тварини або пацієнта і способу 11 UA 105903 C2 5 10 15 20 25 30 35 40 45 50 55 60 введення відповідно до добре відомих принципів медицини. Клініцист може легко визначити ефективну кількість численними добре відомими способами; усі такі ефективні кількості входять в об'єм винаходу. Винахід включає способи лікування, які полягають у введенні ефективної кількості сполуки формули І або формули Il або її фармацевтично прийнятної солі ссавцю, що страждає від щонайменше одного симптому або стану, пов'язаного з психічним розладом. У деяких втіленнях психічний розлад включає (не лише): 1) тривожні розлади, включаючи (не лише), панічні розлади без агорафобії, панічні розлади з агорафобією, агорафобію без історії панічного розладу, специфічні фобії, соціальну фобію, обсесивно-компульсивні розлади, розлади, пов'язані з стресом, посттравматичні стресові розлади, гострі стресові розлади, загальні тривожні розлади і загальні тривожні розлади, пов'язані з загальним медичним станом; 2) розлади настрою включаючи (не лише), глибокі депресивні розлади і дистимічні розлади; b) біполярну депресію і/або біполярну манію, включаючи (не лише), депресивні або змішані епізоди; с) циклотимічні розлади і d) розлади настрою, зумовлені загальним медичним станом; і 3) шизофренію і інші психозні розлади, включаючи (не лише), психозний розлад, шизофреніформний розлад, шизоафективний розлад, маячний розлад, короткочасний психозний розлад, спільний психозний розлад і психозні розлади, зумовлені загальним медичним станом, деменцію і інші когнітивні розлади. Приклади визначень наведених вище станів і розладів можуть бути знайдені, наприклад, у American Psychiatric Association: Diagnostic and Statistical Manual of Mental Disorders, Fourth Edition, Text Revision, Washington, DC, American Psychiatric Association,2000 (далі "DSM-IV"). Зокрема, запропоновано способи лікування, біполярного розладу І, включаючи (не лише) пов'язані з депресивними, маніакальними або змішаними епізодами, і біполярного розладу II, циклотимічного розладу і розладу настрою, зумовленого загальним медичним станом; і шизофренії, який включає введення терапевтично ефективної кількості сполуки формули І або її фармацевтично прийнятної солі пацієнту, що потребує цього. Зокрема, способи лікування біполярних розладів включаючи (не лише) пов'язані з депресивними, маніакальними або змішаними епізодами, які включають введення терапевтично ефективної кількості сполуки формули І, де Z - H, або її фармацевтично прийнятної солі пацієнту, що потребує цього. У деяких втіленнях симптоми і стани включають (не лише), тривожність, збудження, ворожість, паніку, розлади вживання їжі, афективні симптом, симптоми настрою, негативні і позитивні психозні симптоми, взагалі пов'язані з психозом і нейродегенеративними розладами. У деяких втіленнях сполуку формули І або її фармацевтично прийнятну сіль вводять ссавцю як проліки 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну або його фармацевтично прийнятної солі. Необмежуючими прикладами таких проліків можуть бути ті, в яких Z - -C(=O)1 1 1 2 2 3 1 2 R , -C(=O)OR , -C(O)OCH2, -CH(R )-NHC(=O)R , -C(=O)OCHR OC(=O)R , -CR =CR або 4 1 2 3 4 CH=CHC(=O)R , де кожна R , R , R і R у кожному випадку незалежно є алкіл, циклоалкіл, арил, гетероарил або гетероциклоалкіл або згідно з описом. Термін "лікування" згідно з винаходом включає введення терапевтично ефективної кількості сполуки винаходу для послаблення або пригнічення існуючого хворобливого стану, гострого або хронічного, або повторних симптомів або станів. Цей термін також включає профілактичні терапії для відвернення повторення станів і продовження терапії хронічних розладів. Термін "ссавець" стосується будь-якого теплокровної тварини, наприклад, людини. У деяких втіленнях ссавець потребує лікування, оскільки страждає від або має схильність до розвитку одного або більше симптомів, хвороб або розладів, описаних тут. Термін "введення" включає введення фармацевтично активного інгредієнту або його проліків, які можуть перетворитись після введення у фармацевтично активний інгредієнт. Одною з очікуваних переваг введення 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]-тіазепіну або його фармацевтично прийнятної солі є зменшення частоти появи щонайменше одного потенційного побічного явища, наприклад, наприклад, сонливості, седативності, серцевосудинних явищ або явищ, пов'язаних з антагоністами D2 (наприклад, розладів рухів). Можна сподіватись, що проліки 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну або його фармацевтично прийнятних солей забезпечать зменшення щонайменше одного шлунковокишкового побічного явища. Отже, можна сподіватись, що лікування 2-флуор-11-(піперазин-1іл)дибензо[b,f][1,4]тіазепіном або його фармацевтично прийнятною сіллю принесе сприятливі результати завдяки потужному пригніченню цією сполукою норепінефринового транспортера (NET), помірному антагонізму до рецептора D2 і відновленню спорідненості до вторинних об'єктів (наприклад, Н1 або М1), пов'язаних з NET, у лікуванні біполярних станів і супутніх станів настрою, класифікованих згідно з кодами DSM-IV 296 і їх частинами. Відповідно, можна 12 UA 105903 C2 5 10 15 очікувати, що сполуки формули І і, зокрема,2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепін або його фармацевтично прийнятна сіль можуть бути використані для лікування біполярних станів і супутніх станів настрою, які класифікуються у майбутньому у DSM-V. Можна також сподіватись, що 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепін або його фармацевтично прийнятна сіль можуть бути використані у лікуванні тривожних станів, класифікованих у DSM-IV кодом 300 і його частинами. Відповідно, можна очікувати, що сполуки формули І і, зокрема, 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]-тіазепін або його фармацевтично прийнятна сіль можуть бути використані для лікування тривожних станів, які класифікуються у майбутньому у DSM-V. Можна вважати, що 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепін або його фармацевтично прийнятна сіль можуть бути використані у лікуванні шизофренічних станів, класифікованих у DSM-IV кодом 295 і його частинами. Відповідно, можна очікувати, що сполуки формули І і, зокрема, 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]-тіазепін або його фармацевтично прийнятна сіль можуть бути використані для лікування шизофренічних станів, які класифікуються у майбутньому у DSM-V. Інтермедіати Далі проміжні сполуки формули (А), які можуть бути використані у синтезі сполук формули І або формули II, розглядаються у прикладах і схемах. 5 6 20 де R - NH2 або NO2 і R - H або С1-4алкіл. У більш конкретному втіленні сполуки формули A 6 R - NH2 і R - H, метил або етил. Описано також інші інтермедіати формули (В), які можуть бути використані у синтезі сполук формули І або формули II. 25 де X - Cl або фенокси. Винахід ілюструється наведеними нижче прикладами. Ці приклади є лише ілюстративними і не обмежують винаходу. Приклади Приклад 1А: 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепін Схема А визначає один способів приготування 2-флуор-11-(піперазин-1іл)дибензо[b,f][1,4]тіазепін (Vl). 30 5 13 UA 105903 C2 5 10 15 20 25 30 35 40 Схема А ілюструє п'яти стадійний процес: етил-естер 5-флуор-2-меркапто-бензойної кислоти може бути введений у реакцію з 1-флуор-2-нітробензолом для отримання етил-естеру 5-флуор-2-(2-нітро-фенілсульфаніл)-бензойної кислоти; цей етил-естер може бути перетворений у етил-естер 5-флуор-2-(2-аміно-фенілсульфаніл)-бензойної кислоти; амінофенільна сполука може бути циклізована з утворенням 2-флуор-10Ндибензо[b,f][1,4]тіазепін-11-ону, який може бути перетворений у 11-хлор-2-флуордибензо[b,f][1,4]тіазепін, який потім може бути введений у реакцію з піперазином для отримання названої сполуки. Операція 1: До розчину етил 5-флуор-2-меркаптобензоату (І) (25,0 г, 124,9 ммоль) і 1-флуор-2нітробензол (13,2 мл, 124,9 ммоль) в ацетоні (700 мл) додають K 2CO3 (34,5 г, 249,7 ммоль) при зовнішній температурі. Жовту суспензію нагрівають до температури флегми (60°C) протягом 5 год. Реакційну суміш гасять 1N HCI (500 мл), розріджують EtOAc (1000 мл) і фільтрують через шар діатомової землі. Водний шар видаляють, шар EtOAc промивають 1N HCI (250 мл x 2) і розсолом (200 мл х 1), сушать і розчинник видаляють під зниженим тиском. Матеріал використовують без очищення, отримуючи етил 5-флуор-2-(2-нітрофенілтіо)бензоат (II) (39,3 г, 1 95 %) як темножовту тверду речовину, m/z (ES+) M + 1 = 322,1; PXBE t R = 0,88 хвил. H ЯМР (300 МГц, ДMCO-d6): 1,09 (t, 3H, J = 7.2 Гц), 4,16 (q, 2H, J = 7,2 Гц), 7,07 (d, 1H, J = 7,2 Гц), 7,407,75 (m, 5H), 8,20 (d,1H, J = 7,2 ГЦ). Операція 2: До розчину етил 5-флуор-2-(2-нітрофенілтіо)бензоату (II) (39,0 г, 121,4 ммоль) у MeOH (530 мл) додають дигідрат хлориду олова(ІІ) (301 г, 1335,1 ммоль) при зовнішній температурі. Молочно-жовту суспензію нагрівають до температури флегми (65°С) протягом 5 год. і потім охолоджують. До охолодженої суміші додають EtOAc (1000 мл) і твердий Na 2CO3 (141,5 г, 1335 ммоль). З ретельним перемішуванням повільно додають воду до появи піни і припинення утворення солі олова. Додають діатомову землю (500 г) і реакційну суміш перемішують 30 хвил. і фільтрують. Водний шар видаляють і органічний шар промивають розсолом (500 мл x 1), сушать і розчинник видаляють під зниженим тиском. Матеріал використовують без очищення, отримуючи анілін-естер (III) (17,7 г, 60,6%) як блідожовтий густий сироп, m/z (ES+) M + 1 = 292,1; 1 PXBE tR = 0,88 хвил. H ЯМР (300 МГц, ДМСО-d6): 1,34 (t, 3H, J = 7,2 Гц), 4,35 (q, 2H, J = 7,2 Гц), 5,36 (s, 2H), 6,57-6,70 (m, 2H), 6,85 (d, 1H, J = 9,3 Гц), 7,18-7,35 (m, 3H), 7,70 (dd, 1H, 9,3 Гц). Операція 3: До розчину анілін-естеру (III) (17,6 г, 60,5 ммоль) у толуолі (300 мл) додають ртолуолсульфонову кислот (11,6 г, 60,5 ммоль) при зовнішній температур під нітрогеном. Після нагрівання суміші при 110°C протягом 16 год. реакційну суміш охолоджують до кімнатної температури. Отриманий білий осад циклічного лактаму збирають (3,9 г) і фільтрат концентрують під зниженим тиском. Реакційну суміш перетирають з MeOH (100 мл), отриманий циклічний лактам збирають (5,8 г) і фільтрат концентрують під зниженим тиском. Матеріал очищають колонною хроматографією на силікагель, використовуючи 0-10 % MeOH у CH2CI2 як 14 UA 105903 C2 5 10 15 20 25 30 35 елюент, отримуючи циклічний лактам (1,8 г) як білий порошок. Об'єднання порцій продукту дає кінцевий циклічний лактам (IV) (11,2 г, 75%) як білуватий порошок, m/z (ES+) M + 1 = 246,1; 1 PXBE tR = 0,71 хвил. H ЯМР (300 МГц, ДМСО-d6): 7,15 (t, 1H, J = 9,3 Гц), 7,24 (d, 1H, J = 9,3 Гц), 7,36 (m, 2H), 7,45 (dd,1H, J = 9.3 Гц), 7,55 (m, 2H), 10,78 (s,1 H). Операція 4: Суспензію циклічного лактаму (IV) (3,0 г, 12,2 ммоль) і N, N-диметиланіліну (0,03 мл, 0,24 ммоль) у POCI3 (6,8 мл, 73,4 ммоль) нагрівають при 125°C 2 год. Реакційну суміш концентрують під зниженим тиском. Залишок розчиняють у CH2CI2 (100 мл), промивають холодною водою (50 мл x 2) і розсолом (50 мл x 1), сушать і розчинник видаляють під зниженим тиском. Матеріал використовують без очищення, отримуючи імінохлорид (V) (3,1 г, 95%) як бурштиновий сироп, m/z (ES+) M + 1 = 264,1; PXBE tR = 0,95 хвил. Операція 5: До розчину імінохлориду (V) (3,0 г, 11,5 ммоль) у ксилолі (115 мл) додають піперазин (7,9 г, 92,2 ммоль) при зовнішній температурі під нітрогеном. Після нагрівання суміші при 138°C протягом 2 год. реакцію охолоджують до кімнатної температури, потім гасять 2N HCI до рН 2,0, кислотний водний шар відділяють і промивають CH2CI2 (2 x 100 мл). До залишку кислотного водного шару додають твердий K2CO3 до рН 10 і додають EtOAc (200 мл). Отриману емульсію фільтрують через діатомову землю і органічний шар відділяють. Органічний шар промивають розсолом (1x50 мл), сушать над MgSO4, фільтрують і концентрують під зниженим тиском. Матеріал очищають колонною хроматографією на силікагелі, використовуючи 0-5% 7N NH3/MeOH у CH2CI2 як елюент і отримуючи названу сполуку (2,0 г, 55%) як блідожовтий 1 порошок, m/z (ES+) M + 1 = 314,2; PXBE tR = 0,50 хвил. H ЯМР (300 МГц, ДМСО-d6): 2,68 (m, 2H), 2,72 (m, 2H), 3,40 (m, 4 H), 6,86 (t, 1H, J = 8,1 Гц), 6,98 (d, 1H, J = 8,1 Гц), 7,15-7,38 (br m, 4H), 7,58 (dd, 1H, J = 8,1 Гц), 8,92 (br s, 1H). Приклад 1В: 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепін Схема В ілюструє інший можливий спосіб приготуванн 2-флуор-11-(піперазин-1іл)дибензо[b,f][1,4]тіазепіну. У цьому тристадійному процесі: 2,2'-дисульфандіілдіанілін може бути введений у реакцію з 2-бром-5-флуор-бензойною кислотою з утворенням 2-(2-аміно-фенілсульфаніл)-5-флуорбензойної кислоти; бензойна кислота може бути циклізована з утворенням 2-флуор-10Ндибензо[b,f][1,4]тіазепін-11-ону, який може бути перетворений у 11-хлор-2-флуордибензо[b,f][1,4]тіазепін, який може бути введений у реакцію піперазиним для отримання названої сполуки. Синтез 2-флуордибензо[b,f][1,4]тіазепін-11 (10Н)-ону: 15 UA 105903 C2 5 10 15 20 25 30 35 Суспензію броміду нікелю (5 ммоль, 1,09 г), біпіридилу (5 ммоль, 0,78 г) і цинкового порошку (200 ммоль, 13,08 г) у 200 мл сухого ацетонітрилу перемішують магнітним перемішувачем, обробляють 2,2'-дисульфандіілдіанілін (52 ммоль, 12,92 г) і нагрівають у масляній ванні при 75°C протягом 30 хвил. після досягнення максимальної внутрішньої температури. Після цього реакційну суміш обробляють 2-бром-5-флуорбензойною кислотою (100 ммоль, 21,90 г) порціями і перемішують при 75°С протягом 1 год. і ванну видаляють. Реакційну суміш охолоджують кімнатної температури, переносять у колбу і концентрують під зниженим тиском. Отриману темну тверду речовину суспендують у 200 мл метанолу, охолоджують у льоду і обробляють 100 мл трифлуороцтової кислоти, додаючи через крапельну воронку. Отриманий темний розчин перемішують 30 хвил. до припинення виходу газу і фільтрують через 3 см подушку діатомової землі і фільтрувальну подушку промивають, використовуючи 400 мл метанол. Отриману сіру суспензію витримують під зворотним холодильником 1,5 год., охолоджують до кімнатної температури, перемішують 16 год. і фільтрують, отримуючи тверду речовину. Фільтрат випарюють і отриману піну обробляють 300 мл 15%-м розчином хлориду амонію і 500 мл етил ацетату. Суспензію обробляють твердим бікарбонату натрію до рН 6-7 (16,8 г, 20 ммоль). Отриману білу суспензію перемішують 1 год. і фільтрують. Твердий залишок промивають 500 мл етил ацетату. Органічний шар відділяють від водного шар, сушать над сульфатом натрію і випарюють, отримуючи масло, яке суспендують у 200 мл етеру, перемішують 1 год., фільтрують і промивають 100 мл етер. Об'єднані тверді речовини перемішують з 250 мл гарячого метанолу протягом 10 хвил. і фільтрують, отримуючи бажану 2-(2-амінофенілтіо)-5-флуорбензойну 1 кислоту як тверду речовину. (17,42 г, 66%) MS (М+1) 264; H ЯМР (300 МГц, ДМСО-d6) 1/млн 3,06 - 3,45 (m, 1 H) 4,84 - 5,70 (m, 2 H) 6,53 - 6,70 (m, 2 H) 6,82 (d, J=7,6 Гц,1 H) 7,09 - 7,25 (m, 2 H) 7,26 - 7,36 (m, 1 H) 7,66 (dd, J=9,5,3,0 Гц,1 H). Суспензію 2-(2-амінофенілтіо)-5-флуорбензойної кислоти (64,57 ммоль, 17,51 г) у 500 мл ксилолів обробляють моногідратом р-толуолсульфонової кислоти (64,57 ммоль, 12,2 г) і нагрівають. Додають ще 200 мл ксилолу нагрівання продовжують з азеотропним видаленням води протягом 16 год. Отриману рожеву реакційну суміш охолоджують до кімнатної температури і додають до 300 мл вод. Після перемішування протягом 15 хвил. тверду речовину видаляють фільтрацією, промивають 3x100 мл води і сушать у повітрі 4 год., і потім у вакуумі 20 год., отримуючи 2-флуордибензо[b,f][1,4]тіазепін-11(10Н)-он як білувату тверду речовину (11,6 г, 1 73% ); MS (М+1) 246; H ЯМР (300 МГц, ДМСО-d6) 1/млн 7,16 (t, 1 H) 7,24 (d, J=7,2 Гц,1 H) 7,29 - 7,42 (m, 2 H) 7,47 (dd, J=9,3,2,9 Гц, 1 H) 7,52-7,71 (m, 2 H) 10,47 - 11,20 (m, 1 H), MS 081119 М+1 246 (0,72). 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепін може бути приготовлений з 2флуордибензо[b,f][1,4]тіазепін-11(10Н)-ону як описано в операціях 4 і 5 Прикладу 1а. Приклад 1С: 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепін Схема C ілюструє інший можливий спосіб приготування 2-флуор-11-(піперазин-1іл)дибензо[b,f][1,4]тіазепіну. 16 UA 105903 C2 5 10 15 20 25 30 35 1-хлор-2-нітробензол може бути введений у реакцію з 4-флуорбензометіолом у присутності основи для отримання 1-нітро-2-фенілсульфаніл-(4-флуорбензол). Нітрофлуорбензол може бути відновлений 1-аміно-2-фенілсульфаніл-(4-флуорбензол)у, який може бути перетворений, наприклад, у феніл-естер [2-(4-флуор-фенілсульфаніл)-феніл]-карбамову кислоту. Такий естер може бути циклізований з утворенням 2-флуор-10Н-дибензо[b,f][1,4]тіазепін-11-ону, який може бути перетворений у 11-хлор-2-флуор-дибензо[b,f][1,4]тіазепін, який потім може бути введений у реакцію з піперазином для отримання названої сполуки. Приклад 1D: 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепін Схема D ілюструє інший можливий спосіб приготуванн 2-флуор-11-(піперазин-1іл)дибензо[b,f][1,4]тіазепіну. 2-амінобензолтіол може бути введений у реакцію з метил-естером 2,5-дифлуор-бензойної кислоти для отримання інтермедіату метил-естеру 2-[(Е)-2-аміно-1-мет-(Е)-іліден-бут-2енілсульфаніл]-5-флуор-бензойної кислоти, яка може бути перетворена обробкою лугою з отриманням 2-[(Е)-2-аміно-1-мет-(Е)-іліден-бут-2-енілсульфаніл]-флуор-бензойної кислоти. Бензойна кислота може бути циклізована з отриманням 2-флуор-10Н-дибензо[b,f][1,4]тіазепін11-ону, який може бути перетворений у 11-хлор-2-флуор-дибензо[b,f][1,4]тіазепін, який потім може бути введений у реакцію з піперазином для отримання названої сполуки. Приклад 2: 1-(4-(2-флуордибензо[b,f][1,4]тіазепін-11-іл)піперазин-1-іл)метанон Сполуку 1 1 формули І, де Z - -C(=O)R і R - метил, приготовляють за такою процедурою. До розчину 2флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну Vl (Схема А) (0,05 г, 0,16 ммоль) і тріетиламіну (0,05 мл, 0,32 ммоль) у ДХМ (3 мл) краплями додають ацетил хлорид (0,02 мл, 0,32 ммоль) при 0°C під нітрогеном. Після перемішування суміші при 0°C протягом 1 год. розчинник видаляють під зниженим тиском. Реакційну суміш перетирають з етером (1x20 мл), нерозчинені матеріали відфільтровують і фільтрат концентрують під зниженим тиском, отримуючи 1-(4-(2-флуордибензо[b,f][1,4]тіазепін-11-іл)піперазин-1-іл)метанон (0,05 г, 80%) 1 блідожовтий порошок, m/z (ES+) M + 1 = 356,0; PXBE t R = 0,64 хвил. H ЯМР (300 МГц, ДМСОd6): 2,03 (s, 3H), 3,35-3,61 (br m, 8Н), 6,90 (t, 1H, J = 7,8 Гц), 7,01 (d, 1H, J = 7,8 Гц), 7,22 (t, 1H, J = 7,8 Гц), 7,31-7,40 (br m, 3H), 7,60 (dd, 1H, J = 5,7 Гц). Приклад 3: етил-4-(2-флуордибензо[b,f][1,4]тіазепін-11-іл)піперазин-1-карбоксилат 6 6 Сполуку формули І, де Z - -C(=O)OR і R - етил, приготовляють за такою процедурою. До розчину 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну Vl (Схема А) (0,05 г, 0,16 ммоль) і тріетиламіну (0,05 мл, 0,32 ммоль) у ДХМ (3 мл) додають етил карбонхлоридат (етил хлорформат) (0,03 мл, 0,32 ммоль) краплями при 0°C під нітрогеном. Після перемішування суміші при 0°C протягом 1 год. розчинник видаляють під зниженим тиском. Реакційну суміш 17 UA 105903 C2 5 10 15 20 25 30 35 40 45 50 55 60 перетирають з етером (1x20 мл), нерозчинені матеріали відфільтровують і фільтрат концентрують під зниженим тиском, отримуючи етил-4-(2-флуордибензо[b,f][1,4]тіазепін-11іл)піперазин-1-карбоксилат (0,05 г, 76%) як жовтий порошок, m/z (ES+) M + 1 = 386,4; PXBE t R = 1 0,82 хвил. H ЯМР (300 МГц, ДМСО-d6): 1,19 (t, 3H, J = 7,2 Гц), 3,09 (brs, 1H), 3,32-3,61 (br m, 7H), 4,07 (q, 2H, J = 7,2 Гц), 6,92 (t, 1H, J = 7,5 Гц), 7,02 (d, 1H, J = 7,8 Гц), 7,22 (t, 1H, J = 7,2 Гц), 7,30-7,42 (brm, 3H), 7,60 (dd, 1H, J = 5,4 Гц). Приклад 4: бензил-4-(2-флуордибензо[b,f][1,4]тіазепін-11-іл)піперазин-1-карбоксилат 6 6 Сполуку формули І, де Z - -C(=O)OR і R - бензил, приготовляють за такою процедурою. До розчину 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну Vl (Схема А) (0,05 г, 0,16 ммоль) і тріетиламіну (0,05 мл, 0,32 ммоль) у ДХМ (3 мл) краплями додають бензил карбонхлоридат (бензил хлорформат) (0,03 мл, 0,32 ммоль) при 0°C під нітрогеном. Після перемішування суміші при 0°C протягом 1 год. розчинник видаляють під зниженим тиском. Реакційну суміш перетирають з етером (1x20 мл), нерозчинені матеріали відфільтровують і фільтрат концентрують під зниженим тиском, отримуючи бензил-4-(2-флуордибензо[b,f][1,4]тіазепін-11іл)піперазин-1-карбоксилат (0,06 г, 90%) як блідо жовту воскоподібну тверду речовину, m/z 1 (ES+) M + 1 = 448,2; PXBE tR = 0,94 хвил. H ЯМР (300 МГц, ДМСО-d6): 3,33-3,59 (br m, 8H), 5,12 (s, 2H), 6,93 (t, 1H, J = 7,5 Гц), 7,01 (d, 1H, J = 7,8 Гц), 7,23 (t, 1H, J = 7,2 Гц), 7,25-7,42 (br m, 8H), 7,60 (m, 1H). Приклад 5: Аналізи D2 Експериментальні аналізи in vitro можуть взагалі бути проведені, як описано тут. В експериментах можуть бути використані клітини СНО-K1, стабільно трансфектовані рецептором допаміну D2 і підтримуватись у культурному середовищі Ham's F12 з 2 мМ L-глютаміну,10% FBS і 500 мкг/мл Hygromycin. Аналіз зв'язування рецептора D2 3 Здатність випробуваної сполуки витісняти Н-раклоприд на рецепторі D2 можна визначити на мембранах від трансфектованих D2 клітин CHO (Вmax 13 пкмоль/мг протеїну). Для аналізу можна використати стандартний 96-комірковий скловолоконний фільтрувальний планшет для 3 затримання радіоліганду, зв'язаного рецептором. Затримання H можна визначити сцинтиляційним планшетним лічильником TopCount після додання рідкого сцинтилятора у кожну комірку. Сполуки можна оцінити за їх потужністю, використовуючи аналіз конкурентних кривих, отриманих обчисленням значень Ki. Один з таких аналізів, проведений з 2-флуор-11(піперазин-1-іл)дибензо[b,f][1,4]тіазепіном, показав середнє значення Ki при зв'язуванні D2 приблизно 11 нМ. Функціональні аналізи рецептора D2 in vitro: Аналіз GTPgS може бути проведений, як описано у Lazareno, Methods in Molecular Biology, 1999,106,231-245. Антагоністична активність сполук може бути визначен через здатність 35 випробуваних сполук блокувати стимульоване допаміном зв'язування [ S]-GTPS з мембранами клітин CHO, стабільно трансфектованими D2. Один з таких аналізів, проведений з 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]-тіазепіном, показав середнє значення IK50 при зв'язуванні GTPS приблизно 404 нМ. Приклад 6: Індукована D-амфетаміном гіперлокомоторна активність (LMA) Дослідження in vivo можуть бути використані для визначення антипсихозної дії і проводяться звичайно як описано далі. Індукована D-амфетаміном гіперлокомоторна активність (LMA) у моделі тренованих щурів може бути оцінена на самцях щурів Long Evans, з використанням процедури, яка включає фазу навчання з подальшим введенням 1 мг/кг D-амфетаміну. Тваринам дозволяють звикнути до випробувального приміщення протягом 1 год. перед зважуванням і розміщенням в активних камерах. Через 30 хвил. після початку вимірювання LMA, тварин можна короткочасно видалити, ввесті (підшкірно) носій або випробуваний медикамент у різних дозах і повернути у камери. Через 30 хвил. тварин знову видаляють і вводять носій або D-амфетамін (1 мг/кг підшкірно). Після повернення тварин в активні камер LMA оцінюють протягом ще 60 хвил. Галоперидол (0,1 мг/кг розчину у H2O) може бути введений підшкірно за 15 хвил. перед D-амфетаміном. Статистичний аналіз може бути проведений, базуючись на повній відстані, пройденій після введення D-амфетаміну з використанням post hoc аналізу ANOVA і Tukey's. Усі значення можуть бути репрезентовані як середнє і стандартне відхилення. Один з таких аналізів, проведений з 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіном, показав активність при 30 мг/кг і при 60 мг/кг (підшкірно). Приклад 7: Аналіз реакції зумовленого уникнення (CAR) Самці щура Long-Evans були треновані переходити після звукового і візуального стимулювання на протилежний бік стандартної транспортної клітки, що уникнути електричного удару через підлогу клітки. Денний сеанс може включати до 80 експериментів. Після створення 18 UA 105903 C2 5 10 15 20 25 електроудару тварини мають можливість уникнути цього, переходячи на протилежний бік клітки. Медикамент можна вводити підшкірно або перорально за 60 хвил. перед випробуванням і реєструвати процент експериментів, в яких відбулось уникнення. Один з таких аналізів, проведений з 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]-тіазепіном, показав активність при 30 мг/кг і при 60 мг/кг (підшкірно). Приклад 8: Поглинання норепінефрину Аналіз з вимірюванням поглинання норепінефрину може бути проведений, як описано нижче. Випробувану сполуку оцінюють у 11-точках кривої IK50 на її здатність пригнічувати поглинання флуоресцентного субстрату (забарвлення) з пристрою Molecular Devices, який імітує біогенні амінні нейротрансмітери. Стабільну популяцію клітин HEK293F, трансфектованих людським норепінефриновитм транспортером (культурованим у експресійному середовищі Freestyle 293 з 75 мг/мл гідроміцину В) після кріозбереження вносили у день експерименту у планшет і використовували для аналізу (60 К/коміркаІ; забарвлення 7% (кінцеве) від рекомендованого постачальником реконституційного об'єму (100%). Сполуки можуть бути розріджені 1:20 у буфері і інкубовані з клітинами протягом 30 хвил. перед доданням забарвлювача. У цьому аналізі інтенсивності флюоресценції планшети можна зчитувати через 20 хвил. інкубації барвника для визначення ефективності (у %) відносно повного сигналу (0,5% ДМСО, кінцева) і фонового сигналу (10 мкМ дезипраміну, кінцева). IK 50 (половина контрольної реакції) може бути перетворена у Ki, з використанням стандартного рівняння Чена-Прусофа (Cheng-Prusoff). Один з таких аналізів, проведений з 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]-тіазепіном, показав середній результат Ki пригнічення NET приблизно 10 нМ. Приклад 9: Зв'язування рецептора Н1 Аналіз на зв'язування рецептора Н1 може бути проведений згідно з De Backer et al., Biochem. Biophys. Res. Commun., 1993,197(3), 1601. Один з таких аналізів, проведений з 2флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]-тіазепіном, показав середній результат Ki зв'язування Н1 приблизно 7,1 нМ. Фармакологічні дані для сполуки Приклад 1 і інших піперазин-1-іл-дибензо[b,f][1,4]тіазепінів наведено у таблиці нижче. Таблиця Назва сполуки (Приклад 1) 2-флуор-11піперазин-1-ілдибензо[b,f][1,4]тіазепін 11-піперазин-1-ілдибензо[b,f][1,4]тіазепін 2-хлор-11-піперазин-1-ілдибензо[b,f][1,4]тіазепін 2-хлор-11-(4-метилпіперазин-1-іл)дибензо[b,f][1,4]тіазепін 2-флуор-11-(4-метилпіперазин-1-іл)дибензо[b,f][1,4]тіазепін Поглинання hNET D2 антаг. D2 антаг. Зв'язування HEK FLInt CR, GTPS GTPS, D2 w/NaCI Ki середнє Ki (M) (нМ) IK50 макс. дія Н1 Hu, середнє зв'язування Ki (M) 9,60Е-09 4,00Е-07 97 11 7,12Е-09 2,40Е-08 8,00Е-07 89 37 3,33Е-09 4,10Е-08 3,50Е-08 100 0,7 3,87Е-09 5,10Е-08 8,40Е-09 100 0,49 1,52Е-09 5,90Е-08 1,70Е-07 100 1,1 1,82Е-09 30 Припустимими є різні модифікації винаходу на додаток наведеного опису у межах об'єму Формули винаходу. Тимчасову заявку 60/074,417 і згадані вище публікації включено у даний опис посиланням. ФОРМУЛА ВИНАХОДУ 35 1. Сполука формули І 19 UA 105903 C2 Z N N N F S 5 10 15 20 25 30 35 40 45 І або її фармацевтично прийнятна сіль, 1 1 1 2 2 3 1 2 де Z - Н, -C(=O)-R , -C(=O)OR , -CH(R )-NHC(=O)R , -C(=O)OCHR OC(=O)R , -CR =CR або 4 CH=CHC(=O)R , 1 2 3 4 R , R , R і R у кожному випадку незалежно є алкіл, циклоалкіл, арил, гетероарил або гетероциклоалкіл. 2. Сполука або її фармацевтично прийнятна сіль за п. 1, де Z - Н, та сполука є 2-флуор-11(піперазин-1-іл)дибензо[b,f][1,4]тіазепіном. 3. Фармацевтична композиція, яка містить сполуку або її фармацевтично прийнятну сіль за п. 1 або 2 і щонайменше один фармацевтично прийнятний носій. 4. Спосіб лікування психічного розладу, при якому здійснюють введення ссавцю, що потребує цього, терапевтично ефективної кількості сполуки або її фармацевтично прийнятної солі за п. 1 або 2. 5. Спосіб за п. 4, який відрізняється тим, що психічним розладом є біполярний розлад, тривожний розлад, розлад настрою, шизофренія або інший психічний розлад. 6. Спосіб за п. 4, який відрізняється тим, що психічним розладом є біполярний розлад. 7. Спосіб за п. 4, який відрізняється тим, що психічним розладом є шизофренія. 8. Застосування сполуки або її фармацевтично прийнятної солі за п. 1 або 2 для лікування психічного розладу. 9. Застосування за п. 8, яке відрізняється тим, що лікуванням є лікування біполярного розладу, тривожного розладу, розладу настрою, шизофренії або іншого психічного розладу. 10. Застосування за п. 8, яке відрізняється тим, що лікуванням є лікування біполярного розладу або шизофренії. 11. Застосування сполуки або її фармацевтично прийнятної солі за п. 1 або 2 для приготування медикаменту для лікування біполярного розладу, тривожного розладу, розладу настрою, шизофренії або іншого психічного розладу. 12. Застосування за п. 11, яке відрізняється тим, що лікуванням є лікування біполярного розладу або шизофренії. 13. Спосіб лікування психічного розладу, при якому здійснюють введення ссавцю, що потребує цього, терапевтично ефективної кількості фармацевтичної композиції за п. 3. 14. Спосіб за п. 13, який відрізняється тим, що психічним розладом є біполярний розлад, тривожний розлад, розлад настрою, шизофренія або інший психічний розлад. 15. Спосіб за п. 14, який відрізняється тим, що психічним розладом є біполярний розлад або шизофренія. 16. Спосіб отримання 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну, при якому здійснюють такі етапи: реакція етилового естеру 5-флуор-2-меркаптобензойної кислоти з 1-флуор-2-нітробензолом з отриманням етилового естеру 5-флуор-2-(2-нітрофенілсульфаніл)бензойної кислоти; перетворення етилового естеру 5-флуор-2-(2-нітрофенілсульфаніл)бензойної кислоти у етиловий естер 5-флуор-2-(2-амінофенілсульфаніл)бензойної кислоти; циклізація етилового естеру 5-флуор-2-(2-амінофенілсульфаніл)бензойної кислоти з утворенням 2-флуор-10Н-дибензо[b,f][1,4]тіазепін-11-ону; перетворення 2-флуор-10Н-дибензо[b,f][1,4]тіазепін-11-ону у 11-хлор-2флуордибензо[b,f][1,4]тіазепін; реакція 11-хлор-2-флуордибензо[b,f][1,4]тіазепіну з піперазином для отримання 2-флуор-11(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну. 17. Спосіб отримання 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну, при якому здійснюють такі етапи: 20 UA 105903 C2 5 10 15 20 25 реакція 1-хлор-2-нітробензолу з 4-флуорбензолтіолом у присутності основи з отриманням 1нітро-2-фенілсульфаніл-(4-флуорбензолу); відновлення 1-нітро-2-фенілсульфаніл-(4-флуорбензолу) до 1-аміно-2-фенілсульфаніл-(4флуорбензолу); перетворення 1-аміно-2-фенілсульфаніл-(4-флуорбензолу) у феніловий естер [2-(4флуорфенілсульфаніл)феніл]карбамінової кислоти; циклізація такого естеру з утворенням 2-флуор-10Н-дибензо[b,f][1,4]тіазепін-11-ону; перетворення 2-флуор-10Н-дибензо[b,f][1,4]тіазепін-11-ону у 11-хлор-2флуордибензо[b,f][1,4]тіазепін; реакція 11-хлор-2-флуор-дибензо[b,f][1,4]тіазепіну з піперазином для отримання 2-флуор-11(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну. 18. Спосіб отримання 2-флуор-11-(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну, при якому здійснюють такі етапи: реакція 2-амінобензолтіолу з метиловим естером 2,5-дифлуорбензойної кислоти з отриманням метилового естеру 2-[(Е)-2-аміно-1-ет-(Е)-иліденбут-2-енілсульфаніл]-5-флуорбензойної кислоти, перетворення метилового естеру 2-[(Е)-2-аміно-1-ет-(Е)-иліденбут-2-енілсульфаніл]-5флуорбензойної кислоти обробкою лугом з отриманням 2-[(Е)-2-аміно-1-ет-(Е)-иліденбут-2енілсульфаніл]-5-флуорбензойної кислоти, циклізація 2-[(Е)-2-аміно-1-ет-(Е)-иліденбут-2-енілсульфаніл]-5-флуорбензойної кислоти з отриманням 2-флуор-10Н-дибензо[b,f][1,4]тіазепін-11-ону; перетворення 2-флуор-10Н-дибензо[b,f][1,4]тіазепін-11-ону у 11-хлор-2флуордибензо[b,f][1,4]тіазепін; реакція 11-хлор-2-флуордибензо[b,f][1,4]тіазепіну з піперазином для отримання 2-флуор-11(піперазин-1-іл)дибензо[b,f][1,4]тіазепіну. Комп’ютерна верстка А. Крулевський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 21
ДивитисяДодаткова інформація
Назва патенту англійськоюDibenzothiazepine derivatives and use thereof
Автори російськоюBrown, Dean, Damewood, James R., Edwards, Phil, Hulsizer, James, Muir, James Campbell, Pierson Jr., M. Edward, Shenvi, Ashokkumar Bhikkappa, Wesolowski, Steven, Widzowski, Dan, Wood, Michael
МПК / Мітки
МПК: C07D 281/00, A61K 31/554, A61P 25/18, A61P 25/24
Мітки: похідні, застосування, дибензотіазепіну
Код посилання
<a href="https://ua.patents.su/23-105903-pokhidni-dibenzotiazepinu-ta-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Похідні дибензотіазепіну та їх застосування</a>
Попередній патент: Об’ємна дозувальна система з секційним перекриттям на основі зчеплення
Наступний патент: Пристрій для стабілізації обертального руху літального апарата в набігаючому потоці
Випадковий патент: Аеродинамічний сепаратор для насіння