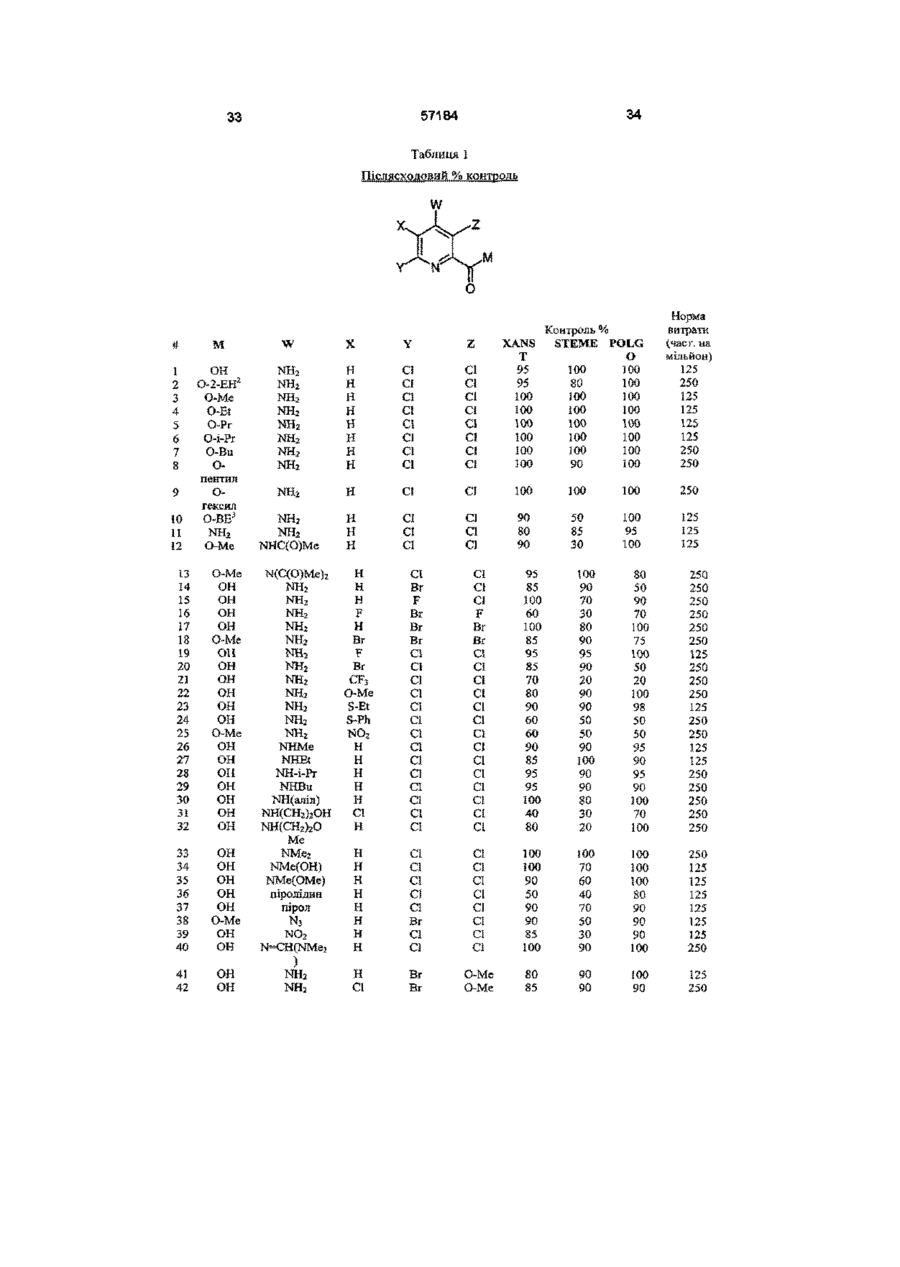
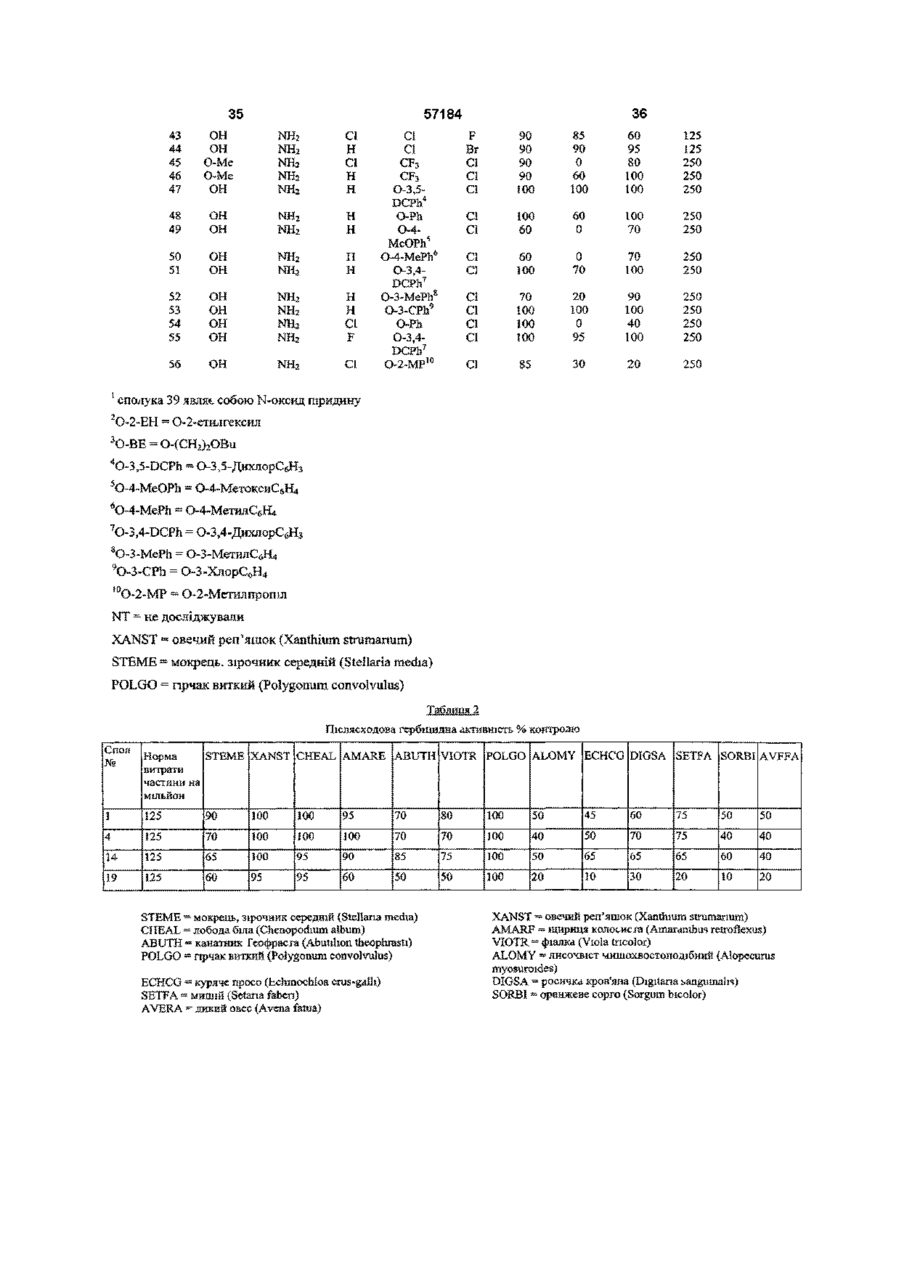
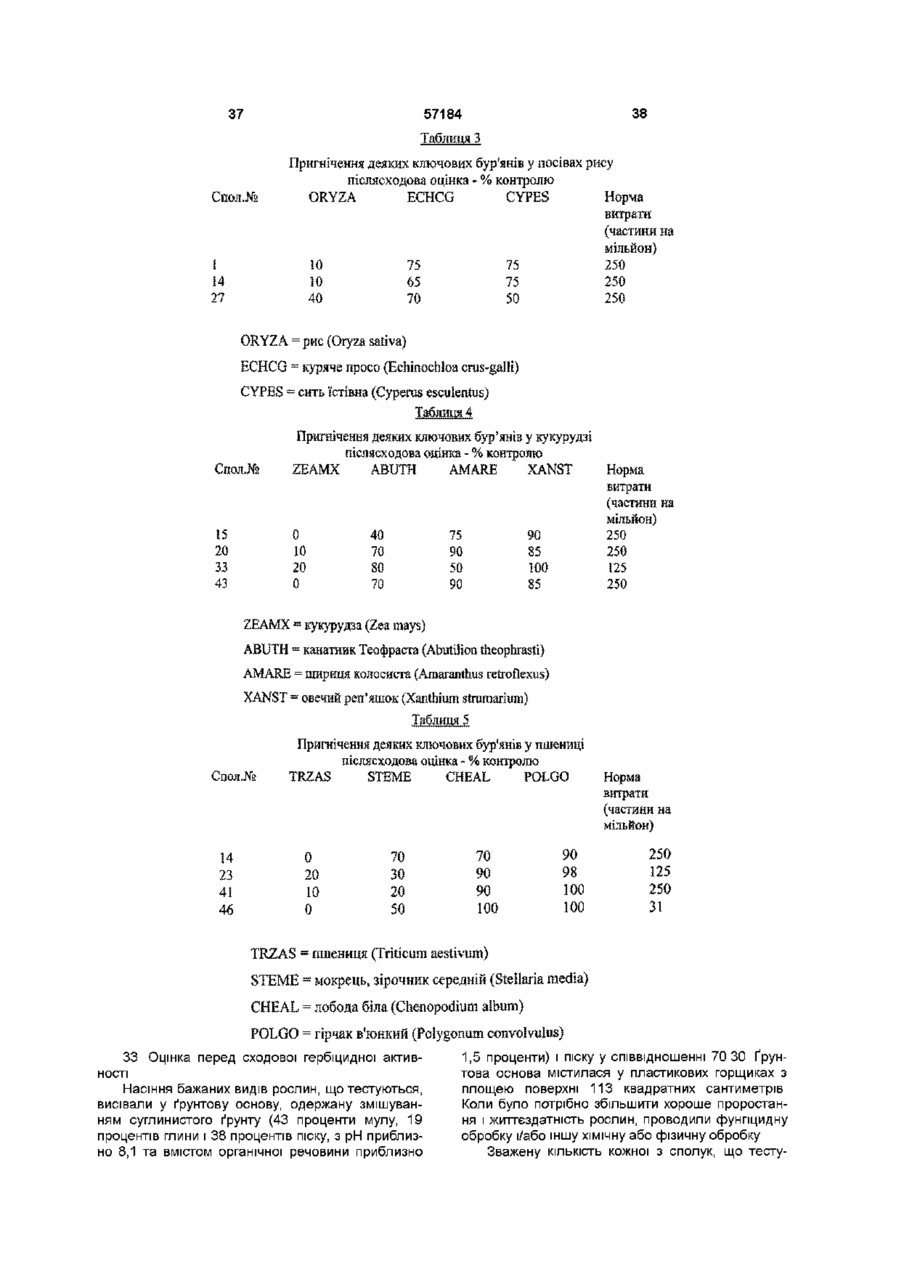
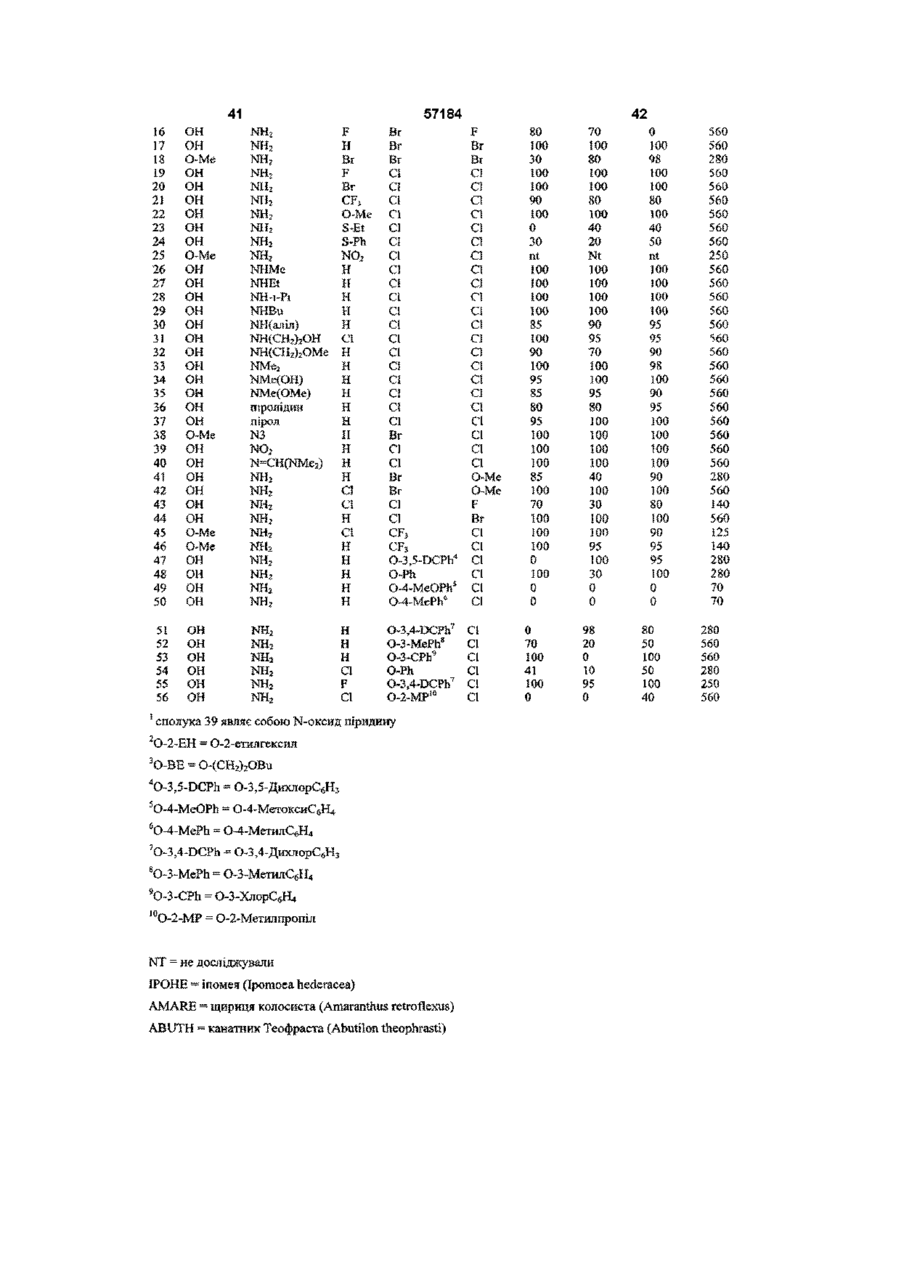
4-амінопіколінати та їх застосування як гербіцидів
Номер патенту: 57184
Опубліковано: 16.06.2003
Автори: Лоуе Крістіан Томас, Руіз Джеймс Мелвін, Александер Аніта Ленора, Кісе Рене Джоан, Філдз Стефен Крейг, Ло Вілльям Чі-Леунг, Бюісс Енн Марі, Балко Террі Вілльям, Річбург Джон Сандерс, Б'єльк Леслі Енні, Крумел Карл Леопольд
Формула / Реферат
1. Сполука формули І
, (І)
де
Х означає Н, галоген, С1-С6 алкокси, С1-С6 алкілтіо, арилокси, нітро або трифторметил;
Y означає галоген, С1-С6 алкокси, С1-С6 алкілтіо, арилокси, гетероарилокси або трифторметил;
Z означає галоген, С1-С6 алкокси, С1-С6 алкілтіо, арилокси або нітро; і
W означає -NO2, -N3, -NR1R2, -N=CR3R4 або -NHN=CR3R4,
де
R1 і R2 незалежно означають Н, С1-С6 алкіл, С3-С6 алкеніл, С3-С6 алкініл, арил, гетероарил, гідрокси, С1-С6 алкокси, аміно, С1-С6 ацил, С1-С6 карбалкокси, С1-С6 алкілкарбаміл, С1-С6 алкілсульфоніл, С1-С6 триалкілсиліл або С1-С6 діалкілфосфоніл, або R1 і R2, взяті разом з N, означають 5- або 6-членне насичене або ненасичене кільце, яке може містити додаткові О, S або N гетероатоми; і
R3 і R4 незалежно означають Н, С1-С6 алкіл, С3-С6 алкеніл, С3-С6 алкініл, арил або гетероарил, або R3 і R4, взяті разом з =С, означають 5- або 6-членне насичене кільце; і
прийнятні в сільському господарстві похідні карбонової кислоти за умови, що коли Х означає Н або Сl, тоді обидва Y і Z не є Сl, або коли обидва Х і Z означають Сl, тоді Y не є Вr.
2. Сполука за п. 1, де
Х означає Н, галоген або трифторметил;
Y означає галоген, арилокси, гетероарилокси або трифторметил;
Z означає галоген; і
W означає -NR1R2,
де
R1 і R2 незалежно означають Н, С1-С6 алкіл, С3-С6 алкеніл, С3-С6 алкініл, або R1 і R2, взяті разом з N, означають 5- або 6-членне насичене кільце, яке може містити додаткові О або N гетероатоми; і
прийнятні в сільському господарстві солі, складні ефіри або аміди карбонової кислоти.
3. Сполука за п. 1 або п. 2, де
Х означає Н або F;
Y означає F, Сl, Вr або арилокси;
Z означає Сl; і
W означає -NH2.
4. Сполука за будь-яким з пп. 1-3, де Y означає феноксигрупу, заміщену галогеном або С1-С4 алкільними групами у 3-положенні.
5. Гербіцидна композиція, що містить гербіцидно ефективну кількість 4-амінопіколінату формули І
, (I)
де
Х означає Н, галоген, С1-С6 алкокси, С1-С6 алкілтіо, арилокси, нітро або трифторметил;
Y означає галоген, С1-С6 алкокси, С1-С6 алкілтіо, арилокси, гетероарилокси або трифторметил;
Z означає галоген, С1-С6 алкокси, С1-С6 алкілтіо, арилокси або нітро; і
W означає -NO2, -N3, -NR1R2, -N=CR3R4 або -NHN=CR3R4,
де
R1 і R2 незалежно означають Н, С1-С6 алкіл, С3-С6 алкеніл, С3-С6 алкініл, арил, гетероарил, гідрокси, С1-С6 алкокси, аміно, С1-С6 ацил, С1-С6 карбалкокси, С1-С6 алкілкарбаміл, С1-С6 алкілсульфоніл, С1-С6 триалкілсиліл або С1-С6 діалкілфосфоніл, або R1 і R2, взяті разом з N, означають 5- або 6-членне насичене або ненасичене кільце, яке може містити додаткові О, S або N гетероатоми; і
R3 і R4 незалежно означають Н, С1-С6 алкіл, С3-С6 алкеніл, С3-С6 алкініл, арил або гетероарил, або R3 і R4 взяті разом з =С, означають 5- або 6-членне насичене кільце; і
прийнятні в сільському господарстві похідні карбонової кислоти за умови, що коли Х означає Сl, тоді обидва Y і Z не є Сl, у суміші з прийнятним в сільському господарстві ад'ювантом або носієм.
6. Гербіцидна композиція за п. 5, де:
Х означає Н, галоген або трифторметил;
Y означає галоген, арилокси, гетероарилокси або трифторметил;
Z означає галоген; і
W означає -NR1R2,
де
R1 і R2 незалежно означають Н, С1-С6 алкіл, С3-С6 алкеніл, С3-С6 алкініл, або R1 і R2, взяті разом з N, означають 5- або 6-членне насичене кільце, яке може містити додаткові О або N гетероатоми; і
прийнятні в сільському господарстві солі, складні ефіри або аміди карбонової кислоти.
7. Гербіцидна композиція за п. 5 або п. 6, де
Х означає Н або F;
Y означає F, Сl, Вr або арилокси;
Z означає Сl; і
W означає -NH2.
8. Гербіцидна композиція за будь-яким з пп. 5-7, де: Y означає феноксигрупу, заміщену галогеном або С1-С4 алкільними групами у 3-положенні.
9. Гербіцидна композиція за п. 5, що містить 4-аміно-3,6-дихлорпіридин-2-карбонову кислоту або її прийнятну в сільському господарстві сіль, складний ефір або амід.
10. Спосіб боротьби з небажаною рослинністю, який включає контактування рослинності чи місця її виростання, або внесення у грунт для запобігання появі сходів рослинності гербіцидно-ефективної кількості гербіцидної композиції за будь-яким з пп. 5-9.
Текст
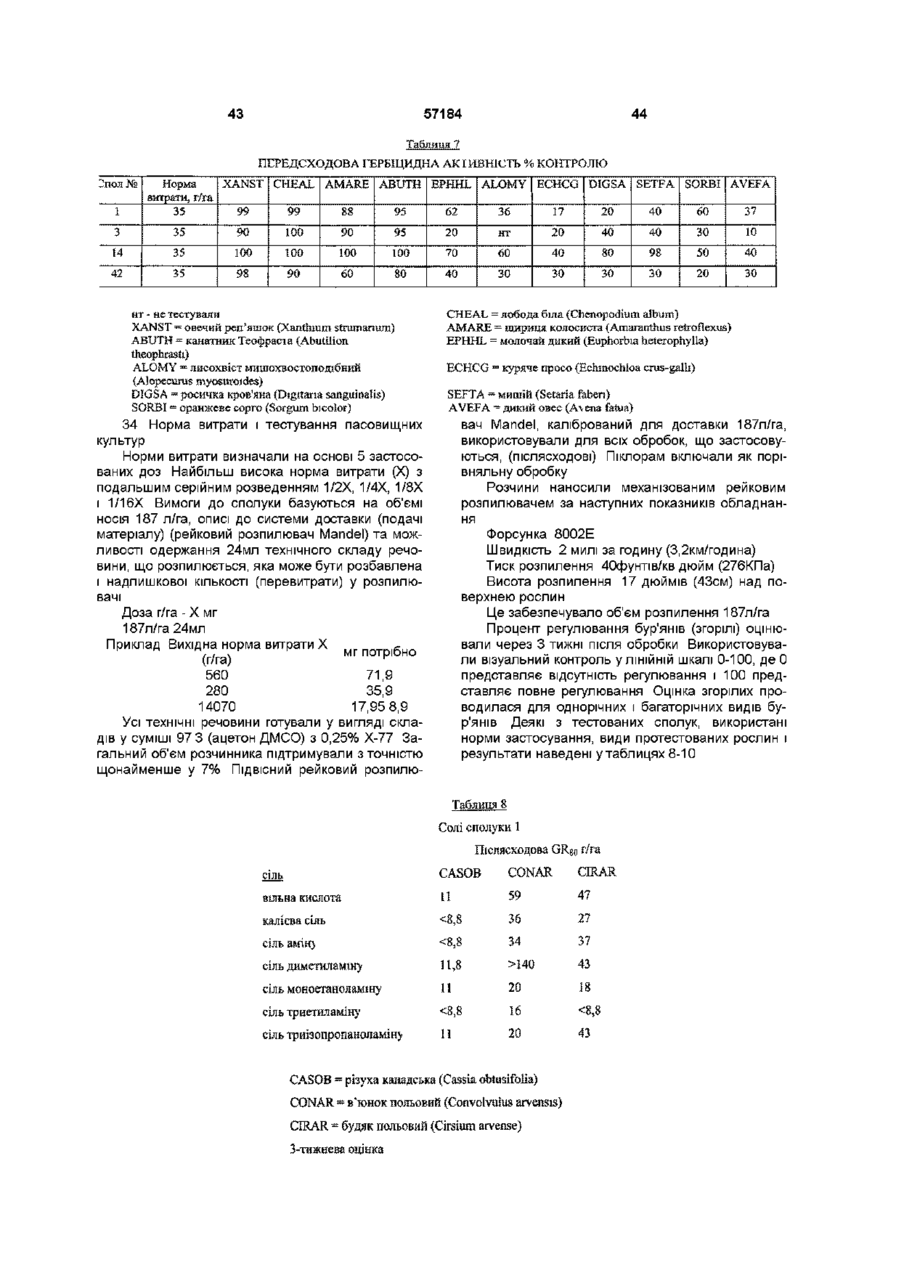
1 Сполука формули І X означає Н, галоген, Сі-Сє алкокси, Сі-Сє алкілтю, арилокси, нітро аботрифторметил, Y означає галоген, Сі-Сє алкокси, Сі-Сє алкілтю, арилокси, гетероарилокси аботрифторметил, Z означає галоген, Сі-Сє алкокси, Сі-Сє алкілтю, арилокси або нітро, і W означає -NO 2 , -N 3 , -NR1R2, -N=CR 3 R 4 або NHN=CR 3 R 4 , Де Ri і R2 незалежно означають Н, і є алкіл,, з є алкеніл, Сз-Сє алкініл, арил, гетероарил, гідрокси, Сі-Сє алкокси, аміно, Сі-Сє ацил, Сі-Сє карбалкокси, Сі-Сє алкіл карбам іл, Сі-Сє алкілсульфоніл, С г Сє триалкілсиліл або Сі-Сє діалкілфосфоніл, або Ri і R2, взяті разом з N, означають 5- або 6-членне насичене або ненасичене кільце, яке може містити додаткові О, S або N гетероатоми, і R3 і R4 незалежно означають Н, Сі-Сє алкіл, Сз-Сє алкеніл, Сз-Сє алкініл, арил або гетероарил, або R3 і R4, взяті разом з =С, означають 5- або 6членне насичене кільце, і прийнятні в сільському господарстві ПОХІДНІ карбонової кислоти за умови, що коли X означає Н або СІ, тоді обидва Y і Z не є СІ, або коли обидва X і Z означають СІ, тоді Y не є Вг 2 Сполука за п 1, де X означає Н, галоген або трифторметил, Y означає галоген, арилокси, гетероарилокси або трифторметил, Z означає галоген, і W означає -NRiR 2 , Де Ri і R2 незалежно означають Н, Сі-Сє алкіл, Сз-Сє алкеніл, Сз-Сє алкініл, або Ri і R2, взяті разом з N, означають 5- або 6-членне насичене кільце, яке може містити додаткові О або N гетероатоми, і прийнятні в сільському господарстві солі, складні ефіри або аміди карбонової кислоти 3 Сполука за п 1 або п 2, де X означає Н або F, Y означає F, СІ, Вг або арилокси, Z означає СІ, і W означає -NH 2 4 Сполука за будь-яким з пп 1-3, де Y означає феноксигрупу, заміщену галогеном або С1-С4 алкільними групами уЗ-положенні 5 Гербіцидна композиція, що містить гербіцидно ефективну КІЛЬКІСТЬ 4-амінопіколшату формули І О 00 ю X означає Н, галоген, Сі-Сє алкокси, Сі-Сє алкілтю, арилокси, нітро аботрифторметил, Y означає галоген, Сі-Сє алкокси, Сі-Сє алкілтю, арилокси, гетероарилокси аботрифторметил, Z означає галоген, Сі-Сє алкокси, Сі-Сє алкілтю, арилокси або нітро, і W означає -NO 2 , -N 3 , -NRiR 2 , -N=CR 3 R 4 або NHN=CR 3 R 4 , Де Ri і R2 незалежно означають Н, Сі-Сє алкіл, Сз-Сє алкеніл, Сз-Сє алкініл, арил, гетероарил, гідрокси, 57184 С-і-Сб алкокси, аміно, С-і-Сє ацил, С-і-Сє карбалкокси, Сі-Сє алкіл карбам іл, С-і-Сє алкілсульфоніл, d Сє триалкілсиліл або С-і-Сє діалкілфосфоніл, або Ri і R2, взяті разом з N, означають 5- або 6-членне насичене або ненасичене кільце, яке може містити додаткові О, S або N гетероатоми, і R3 і R4 незалежно означають Н, С-і-Сє алкіл, Сз-Сє алкеніл, Сз-Сє алкініл, арил або гетероарил, або R3 і R4 взяті разом з =С, означають 5- або 6членне насичене кільце, і прийнятні в сільському господарстві ПОХІДНІ карбонової кислоти за умови, що коли X означає СІ, тоді обидва Y і Z не є СІ, у суміші з прийнятним в сільському господарстві ад'ювантом або носієм 6 Гербіцидна композиція за п 5, де X означає Н, галоген або трифторметил, Y означає галоген, арилокси, гетероарилокси або трифторметил, Z означає галоген, і W означає -NRiR2, Де Ri і R2 незалежно означають Н, С-і-Сє алкіл, Сз-Сє алкеніл, Сз-Сє алкініл, або Ri і R2, взяті разом з N, означають 5- або 6-членне насичене кільце, яке може містити додаткові О або N гетероатоми, і прийнятні в сільському господарстві солі, складні ефіри або аміди карбонової кислоти 7 Гербіцидна композиція за п 5 або п 6, де X означає Н або F, Y означає F, СІ, Вг або арилокси, Z означає СІ, і W означає -NH2 8 Гербіцидна композиція за будь-яким з пп 5-7, де Y означає феноксигрупу, заміщену галогеном або С1-С4 алкільними групами у 3-положенні 9 Гербіцидна композиція за п 5, що містить 4амшо-3,6-дихлорпіридин-2-карбонову кислоту або и прийнятну в сільському господарстві сіль, складний ефір або амід 10 Спосіб боротьби з небажаною рослинністю, який включає контактування рослинності чи місця и виростання, або внесення у грунт для запобігання появі сходів рослинності гербіцидно-ефективної КІЛЬКОСТІ гербіцидної композиції за будь-яким з пп 5-9 Даний винахід відноситься до деяких нових 4амінопіколінатів та їх похідних і до застосування даних сполук як гербіцидів Ряд ПІКОЛІНОВИХ кислот і їх пестицидні властивості описані у даній області Наприклад, у патенті США 3285925 описані ПОХІДНІ 4-амшо-3,5,6трихлорпіколінової кислоти та їх застосування як регуляторів росту рослин і гербіцидів У патенті США 3325272 описані ПОХІДНІ 4-амшо-3,5дихлорпіколінової кислоти та їх застосування як регуляторів росту рослин У патенті США 3317549 описані ПОХІДНІ 3,6-дихлорпіколшовоі кислоти та їх застосування як регуляторів росту рослин У патенті США 3334108 описані хлоровані ПОХІДНІ ДИТІОПІКОЛІНОВОІ кислоти та їх застосування як засобів для знищення паразитів (паразитицидів) У патенті США 3234229 описані 4-амінополіхлор-2трихлорметилпіридини та їх застосування як гербіцидів У публікації Applied and Environmental Microbiology, Vol 59, №7, липень 1993, crop 22512256, 4-аміно-3,6-дихлорпіколшова кислота визначена як продукт анаеробного розкладу 4-аміно3,5,6-трихлорпіколшовоі кислоти, комерційне доступного гербіциду піклораму широким спектром бур'янів з чудовою селективністю відносно сільськогосподарських культур Крім того сполуки володіють чудовими токсикологічним або екологічним (що відноситься до навколишнього середовища) профілями Винахід включає сполуки формули І W Хоча піклорам рекомендований для боротьби з лісовою рослинністю й широколистими бур'янами при ряді застосувань, його властивості не є ідеальними Було б вельми бажано розробити споріднені сполуки, які є більш ефективними (сильнодіючими), більш селективними або такими, що володіють ширшим спектром гербіцидної активності, і/або мають поліпшені ТОКСИКОЛОГІЧНІ властивості, або властивості, поліпшені відносно навколишнього середовища У наш час встановлено, що деякі 4амінопіколінові кислоти та їх ПОХІДНІ, ЯКІ мають підібрані замісники у 3-, 5- і 6-положеннях, являють собою СИЛЬНОДІЮЧІ гербіциди для боротьби з Де X представляє Н, галоген, С-і-Сє алкокси, С-і-Сє алкілтю, арилокси, нітро або трифторметил, Y представляє галоген, С-і-Сє алкокси, С-і-Сє алкілтю, арилокси, гетероарилокси або трифторметил, Z представляє галоген, С-і-Сє алкокси, С-і-Сє алкілтю, арилокси або нітро, і W представляє -NO2, -N3, -NRiR2, -N=CR3R4 або -NHN=CR3R4 Де Ri і R2 незалежно представляють Н, С-і-Сє алкіл, Сз-Сє алкеніл, Сз-Сє алкініл, арил, гетероарил, гідрокси, С-і-Сб алкокси, аміно, С-і-Сє ацил, С-і-Сє карбалкокси, С-і-Сє алкіл карбам іл, С-і-Сє алкілсульфоніл, С-і-Сб триалкілсиліл або С-і-Сє діалкілфосфоніл, або Ri і R2, взяті разом з N, представляють 5- або 6-членне насичене або ненасичене кільце, яке може містити додаткові О, S або N гетероатоми, і R3 і R4 незалежно представляють Н, С-і-Сє алкіл, Сз-Сє алкеніл, Сз-Сє алкініл, арил або гетероарил, або R3 і R4 взяті разом з =С, представляють 57184 5- або 6-членне насичене кільце, і по- сільськогосподарському прийнятні ПОХІДНІ карбонової кислоти за умови, що коли X представляє Н або СІ, тоді обидва Y і Z не є СІ Сполуки формули І, де X представляє Н або F, де Y представляє F, СІ, Вг або арилокси, де Z представляє СІ, і де Ri і F 2 представляють Н, є ? незалежно переважними Винахід включає гербіцидні композиції, що містять гербіцид но-ефективну КІЛЬКІСТЬ 4амінопіколінату формули І W г Y Де X представляє Н, галоген, Сі-Сє алкокси, Сі-Сє алкілтю, арилокси, нітро аботрифторметил, Y представляє галоген, Сі-Сє алкокси, Сі-Сє алкілтю, арилокси, гетероарилокси або трифторметил, Z представляє галоген, Сі-Сє алкокси, Сі-Сє алкілтю, арилокси або нітро, і W представляє -NO2, -N3, -NR1R2, -N=CR3R4 або -NHN=CR3R4, Де Ri і R2 незалежно представляють Н, Сі-Сє алкіл, Сз-Сє алкеніл, Сз-Сє алкініл, арил, гетероарил, гідрокси, Сі-Сє алкокси, аміно, Сі-Сє ацил, Сі-Сє карбалкокси, Сі-Сє алкіл карбам іл, Сі-Сє алкілсульфоніл, Сі-Сє триалкілсиліл або Сі-Сє діалкілфосфоніл, або Ri і R2, взяті разом з N, представляють 5- або 6-членне насичене або ненасичене кільце, яке може містити додаткові О, S або N гетероатоми, і R3 і R4 незалежно представляють Н, Сі-Сє алкіл, Сз-Сє алкеніл, Сз-Сє алкініл, арил або гетероарил, або R3 і R4, взяті разом з =С, представляють 5- або 6-членне насичене кільце, і по- сільськогосподарському прийнятні ПОХІДНІ карбонової кислоти за умови, що коли X представляє СІ, тоді обидва Y і Z не є СІ, у суміші з по-сільсь ко господарсько му прийнятним ад'ювантом або носієм Винахід також включає спосіб застосування сполук і композицій даного винаходу для винищування або пригнічення небажаної рослинності шляхом нанесення гербіцидної КІЛЬКОСТІ сполуки на рослинність або на місце виростання, а також на/у грунт перед появою сходів рослинності Застосування сполук для винищування або пригнічення лісових рослин та широколистих бур'янів у трав'янистих сільськогосподарських культурах є переважним застосуванням і післясходова обробка сполуками небажаної рослинності є переважним способом застосування Гербіцидні сполуки за даним винаходом являють собою ПОХІДНІ 4-амінопіколшових кислот Дані сполуки характеризуються наявністю галогену, Сі-Сє алкокси, Сі-Сє алкілтю, арилокси або нітро-замісників у 3-положенні, при цьому галоген є переважним, і хлор є найбільш переважним, наявністю водню, галогену, Сі-Сє алкокси, Сі-Сє алкілтю, арилокси, нітро або трифторметильного замісників у 5-положенні, при цьомуводень і фтор є переважними, і наявністю галогену, Сі-Сє алкокси, Сі-Сє алкілтю, арилокси, гетероарилокси або трифторметильного замісників у 6-положенні, при цьому фтор, хлор, бром або арилокси є переважними Переважними арилоксигрупами у 6положенні є 3-заміщені феноксигрупи, найбільш переважно феноксигрупи, заміщені галогеном або С1-С4 алкільними групами у 3-положенні Аміногрупа у 4-положенні може бути незаміщеною або заміщеною одним або декількома такими замісниками, як Сі-Сє алкіл, Сз-Сє алкеніл, Сз-Сє алкініл, арил, гетероарил, гідрокси, Сі-Сє алкокси або аміно Аміногрупа може бути додатково перетворена в амід, карбамат, сечовину, сульфонамід, силіламш, фосфорамідат, ІМІН або пдразон Такі ПОХІДНІ здатні розщеплюватися до аміну Незаміщена аміногрупа або аміногрупа, заміщена одним або декількома алкільними замісниками, є переважними Передбачається, що карбонові кислоти формули І є сполуками, які дійсно знищують або пригнічують небажану рослинність і звичайно є переважними Аналоги даних сполук, в яких кислотна або змінна група ПІКОЛІНОВОІ кислоти перетворена з утворенням спорідненого замісника, який може трансформуватися у рослинах або навколишньому середовищі до кислотної групи, володіють по суті такою ж гербіцидною дією та включені в об'єм винаходу Таким чином «посільськогосподарському прийнятне похідне», коли даний термін використовується для опису функціональності карбонової кислоти у 2-положенні, визначається у вигляді будь-якої солі, складного ефіру, ацилпдразиду, імідату, тюімідату, амідину, аміду, ортоефіру, ацил ціаніду, ацил галогеніду, складного тюефіру, складного тюнового ефіру, дитюлового складного ефіру, нітрилу або будьякого іншого кислотного похідного, добре відомого у даній області, яке (а) по суті не впливає негативним чином на гербіцидну активність активного інгредієнта, тобто 4-амінопіколшовоі кислоти, і (Ь) гідролізується або може гідролізуватися у рослинах або ґрунті до ПІКОЛІНОВОІ кислоти формули І, яка, в залежності від рН, знаходиться у дисоційованій або недисоційованій формі Таким самим чином, «по-сільськогосподарському прийнятне похідне», при використанні для опису функціональності аміну у 4-положенні, визначається як будьяка сіль, силіламін, фосфориламін, фосфінімін, фосфорамідат, сульфонамід, сульфінімін, сульфоксимін, аміналь, полуамшаль, амід, тюамід, карбамат, тюкарбамат, амідин, сечовина, ІМІН, 57184 нітро, нітрозо, азид або будь-яке інше азотвмісне похідне, добре відоме у даній області, яке (а) по суті не впливає негативним чином на гербіцидну активність активного інгредієнта, тобто 4амінопіколінової кислоти, і (Ь) гідролізується або може гідролізуватися у рослинах або ґрунті до вільного аміну формули І N-оксиди, які також здатні розщеплюватися до вихідного піридину формули І, також попадають в об'єм даного винаходу ВІДПОВІДНІ СОЛІ включають ті, які одержані з лужних або лужноземельних металів і одержані з аміаку та амінів Переважні катіони включають катіони натрію, калію, магнію та амінієві катіони, що мають формулу RsReRyNH" де кожний з R5, R61 R7 незалежно представляє водень або С-І-С-І2 алкіл, С3-С12 алкеніл або, С3-С12 алкініл, кожний з яких необов'язково заміщений однією або декількома гідрокси, С1-С4 алкокси, d С4 алкілтю або фенільною групами, за умови, що R5, R6 і R7 сумісні стерично Додатково, будь-які два з R5, R6 і R7 разом можуть представляти аліфатичний дифункційний фрагмент, що містить від 1 до 12 атомів вуглецю та до двох атомів кисню або сірки Солі сполук формули і можна одержувати обробкою сполук формули І гідроксидом металу, таким як гідроксид натрію, або аміном, таким як аміак, триметиламін, діетаноламш, 2метилтюпропіламін, бісаліламін, 2бутоксіетиламш, морфолін, циклододециламш або бензиламін Солі амінів часто являють собою переважні форми сполук формули І, оскільки вони розчинні у воді і можуть застосовуватися для одержання бажаних гербіцидних композицій на водній основі ВІДПОВІДНІ складні ефіри включають одержані з С-І-С-І2 алкілових, С3-С12 алкенілових або С3-С12 алкінілових спиртів, таких як метанол, ізопропанол, бутанол, 2-етилгексанол, бутоксіетанол, метоксипропанол, аліловий спирт, пропарпловий спирт або циклогексанол Складні ефіри можуть бути одержані конденсацією ПІКОЛІНОВОІ кислоти зі спиртом з використанням будь-якого числа активуючих агентів, таких як ті, що використовують для пептидних конденсацій, такі як дициклогексилкарбодммід (DCC) або карбонілдммідазол (CDI), взаємодією ВІДПОВІДНОГО хлорангідриду ПІКОЛІНОВОІ КИСЛОТИ формули І з ВІДПОВІДНИМ спиртом або взаємодією відповідної ПІКОЛІНОВОІ КИСЛОТИ фор мули І з ВІДПОВІДНИМ спиртом у присутності кислотного каталізатора ВІДПОВІДНІ аміди включають ті, що одержані з аміаку або з С1-С12 алкіл, С3-С12 алкеніл або С3-С12 алкініл моно- або дизаміщених амінів, таких як, але не обмежуючись ними, диметиламін, діетаноламш, 2-метилтюпропіламін, бісаліламін, 2-бутоксіетиламш, циклододециламш, бензиламін або циклічних або ароматичних амінів, що мають або не мають додаткові гетероатоми, такі як, але не обмежуючись ними, азиридин, азетидин, піролідин, пірол, імідазол, тетразол або морфолін Аміди можуть бути одержані взаємодією ВІДПОВІДНОГО хлорангідриду ПІКОЛІНОВОІ КИСЛОТИ, змішаного ангідриду або карбонового складного ефіру формули І з аміаком або ВІДПОВІДНИМ аміном Терміни «алкіл», «алкеніл» або «алкініл», а та 8 кож термши-похідні, такі як «алкокси», «ацил», «алкілтю» та «алкілсульфоніл», як це використано у даному винаході, включають в свій об'єм ЛІНІЙНІ, розгалужені і ЦИКЛІЧНІ фрагменти Якщо спеціально не вказано інше, кожний з них може бути незаміщеним або заміщеним одним або декількома замісниками, вибраними з, але не обмежуючись ними, галогену, гідрокси, алкокси, алкілтю, С-і-Сє ацилу, формілу, ціано, арилокси або арилу, за умови, що замісники стерично сумісні та задовольняють правилам ХІМІЧНОГО зв'язування і енергетичного напруження Мається на увазі те, що терміни «алкеніл» і «алкініл» включають один або декілька ненасичених зв'язків Термін «арил», так само як і ПОХІДНІ терміни, такі як «арилокси», відноситься до фенільної або нафтильної групи Термін «гетероарил», так само як і ПОХІДНІ терміни, такі як «гетероарилокси», відноситься до 5- або 6-членного ароматичного кільця, що містить один або декілька гетероатомів, а саме N, О або S, такі гетероароматичні кільця можуть бути сконденсованими з іншими ароматичними системами Арильні або гетероарильні замісники можуть бути незаміщеними або заміщеними одним або декількома замісниками, вибраними з галогену, гідрокси, нітро, ціано, арилокси, формілу, С-і-Сб алкілу, Сг-Сб алкенілу, Сг-Сє алкініл у, С-і-Сє алкокси, галогенованого С-і-Сє алкілу, галогенованого С-і-Сб алкокси, С-і-Сє ацилу, С-і-Сє алкілтю, d Сє алкілсульфшілу, С-і-Сє алкілсульфонілу, арилу, Сі-С6 ОС (О) алкілу, С Г С 6 NHC (О) алкілу, С (О) ОН, Сі-С6 С (О) О алкілу, С (О) NH2, C r C 6 С (О) NH алкілу або С-і-Сє С (О) N (алкілі, за умови, що замісники стерично сумісні та задовольняють правилам ХІМІЧНОГО зв'язування і енергетичного напруження Якщо спеціально не обмежено інше, термін галоген включає фтор, хлор, бром і йод Сполуки формули І можуть бути одержані з використанням добре відомих ХІМІЧНИХ способів Необхідні ВИХІДНІ речовини є комерційне доступними або легко синтезованими з використанням стандартних методик Загалом, для одержання ВІДПОВІДНИХ піколінатів можна використовувати відновлення N-оксидів піколінатів Електролітичне дегалогенування 5галогенованих піколінатів можна використовувати для одержання 5-Н (незаміщених) піколінатів, а гідроліз піридинів, заміщених у 2-положенні нітрилами, амідами, складними ефірами та іншими функціональними групами, що гідролізуються, можна використовувати для одержання цільових піколінатів АМІНОПОХІДНІ - 4-ІЧ-амід, карбамат, сечовина, сульфонамід, силіламін і фосфорамідат, можуть бути одержані реакцією вільного аміносполучення, наприклад, з ВІДПОВІДНИМ галогенанпдридом кислоти, хлорформіатом, карбамілхлоридом, сульфонілхлоридом, силілхлоридом або хлорфосфатом Імш або пдразон можуть бути одержані взаємодією вільного аміну або гідразину з ВІДПОВІДНИМ альдегідом або кетоном 6-Бром-аналоги можуть бути одержані відновленням декількох ключових проміжних сполук, наприклад, ВІДПОВІДНИХ 6-бром-4-азидо, 6-бром-4нітро та аналогів N-оксиду 6-бром-4-нітропіридину 57184 10 Такі проміжні сполуки, в свою чергу, можуть бути цільової сполуки формули І, яка може бути очищеодержані або нуклеофільним заміщенням 6-бромна стандартними методами, такими як перекрис4-галоген-аналопв №N3 або електрофільним нітталізація або хроматографія руванням ВІДПОВІДНИХ б-бромпіридин-ІЧ-оксидів Було встановлено, що сполуки формули І коАльтернативно, такі аналоги можуть бути одержані рисні як передсходові та ПІСЛЯСХОДОВІ гербіциди, їх безпосереднім амінуванням ВІДПОВІДНИХ 4,6можна використовувати при неселективних (видибром-аналопв щих) рівнях нанесення для боротьби з широким спектром рослинності на даній площі або при ниж6-Фтор-аналоги можуть бути одержані безпочих рівнях застосування для селективної боротьби середнім амінуванням ВІДПОВІДНИХ 4,6-дифторз небажаною рослинністю Площі для застосувананалопв ня включають вигони і пасовищні землі, узбіччя З- і 5-алкокси-та арилокси-аналоги можуть будоріг і розділяючі смуги доріг, посіви сільськогости одержані відновленням ВІДПОВІДНИХ 4подарських культур, таких як кукурудза, рис та азидопохідних, які, в свою чергу, можуть бути одезлакові Загалом є переважним застосування споржані заміщенням ВІДПОВІДНИХ 4-бромпіридинів луки для боротьби з широким спектром широколиNaN3 Необхідні 3- і 5-алкокси-4-бромпіридини мостих бур'янів, включаючи, серед іншого, різновиди жуть бути одержані ВІДПОВІДНО до літературних щавлю (Rumex spp), будяк польовий (Cirsium способів arvense), різновиди щириці (Amaranthus spp), різ6-Алкокси-, алкілтю-, арилокси- і гетероарилоновиди каси (Cassia spp), різновиди молочаю кси-аналоги можуть бути одержані нуклеофільним (Euphorbia spp), різновиди амброзії (Ambrosia заміщенням ВІДПОВІДНОГО 6-галогенпіридину з виspp), різновиди грудинки (Sida spp), в'юнок користанням алкоксиду, тюалкоксиду, арилоксиду польовий (Convolvulus arvensis) та різновиди воабо гетероарилоксиду лошки (Centaurea spp) Особливо вказується на З- і 5-алкілтю-аналоги можуть бути одержані застосування сполук для боротьби з небажаною літіюванням ВІДПОВІДНИХ хлорпіридинів при низькій рослинністю на трав'янистих площах Хоча кожна з температурі та подальшою обробкою алкілдисусполук 4-амшопіколінату, що охоплюється формульфідами і дюксидом вуглецю Реакція одержаних лою І, включена в об'єм винаходу, рівень гербіциПІКОЛІНОВИХ кислот з гідроксидом амонію давала дної активності, селективність до культур і одерЦІЛЬОВІ продукти жаний спектр контролю бур'янів змінюються в 6-Ціано-аналоги можуть бути одержані амінузалежності від присутнього замісника Відповідна ванням ВІДПОВІДНОГО 4-галоген-6-ціанопіколінату сполука для будь-якого конкретного гербіцидного 4-галоген-6-ціанопіколінати можуть бути одержані застосування може бути ідентифікована з викоридією триметилсилілціаніду (TMSCN) на ВІДПОВІДстанням наведеної у даному описі інформації та НИЙ піридин-ІЧ-оксид, який може бути одержаний звичайного тестування окисленням ВІДПОВІДНОГО пірідину перекисом водню Термін «гербіцид» використовується у даному З-1 5-ціано-аналоги можуть бути одержані дією описі для позначення активного інгредієнта, який KCN на ВІДПОВІДНИЙ фторпіридин за високої темзнищує, пригнічує або яким-небудь іншим чином ператури 3- і 5-фтор-, бром-, йод- та нітронегативно модифікує ріст рослин Гербіцидноаналоги можуть бути одержані електрофільною ефективна або пригнічуюча рослини КІЛЬКІСТЬ ЯВреакцією незаміщеного попередника з позитивним ЛЯЄ собою КІЛЬКІСТЬ активного інгредієнта, яка вигалогеном або нітро-джерелами, такими як газокликає негативно модифікуючу дію та включає подібний фтор, бром, йод і димляча азотна кисловідхилення від природного розвитку, знищення, та, ВІДПОВІДНО регулювання, десикацію (висушування), ретардну (що сповільнює ріст) дію і тому подібне Терміни 6-Трифторметильні аналоги можуть бути оде«рослини» і «рослинність» включають насіння, ржані амінуванням легко доступного метил триоброблене речовинами, що сприяють проростанфторметилпіколінату (окислювальне галогенуванню, пророслу розсаду та сталу рослинність ня у 4-положення з подальшим заміщенням еквівалентом аміаку або аміну) з подальшим хлоГербіцидна активність виявляється сполуками руванням 3-1 5-положень даного винаходу у тому випадку, коли їх безпосередньо наносять на рослину або на область вироЗ- і 5-трифторметильні аналоги можуть бути стання рослини на будь-якій стадії росту або пеодержані стандартними методиками, відомими ред посадкою або проростанням Дія, що фахівцям у даній області, виходячи з відомих споспостерігається, залежить від виду рослин, які колук - 2-фтор-3-хлор-5-трифторметилпіридину і 2,5нтролюються, стадії росту рослини, параметрів дихлор-3-трифторметил піридину розведення, що використовуються, і розміру крапЗаміщені 4-амшо-аналоги можуть бути одерлі, яка розбризкується, розміру часток твердих жані взаємодією ВІДПОВІДНОГО 4-галогенпіридин-2компонентів, умов навколишнього середовища під карбоксилату або будь-якого іншого здатного до час застосування конкретної сполуки, що викорисзаміщення 4-замісника з заміщеним аміном товується, конкретних допоміжних речовин та носіСполуки формули І, одержані будь-яким з цих їв, які використовуються, типу ґрунту і тому подібспособів, можуть бути виділені звичайними спосоного, а також від КІЛЬКОСТІ хімікату, що бами Звичайно, реакційну суміш підкисляють водзастосовується Ці та ІНШІ ЧИННИКИ можна регулюною кислотою, такою як соляна кислота, і екстравати, як відомо у даній області, для промотування гують органічним розчинником, таким як неселективної або селективної гербіцидноі дії етилацетат або дихлорметан Органічний розчинЗвичайно переважним є післясходове застосуванник та ІНШІ летючі компоненти можуть бути виданя сполук формули І на відносно незрілій небажалені відгонкою або упарюванням з одержанням 12 11 57184 ній рослинності для досягнення максимального сільськогосподарських культурах, яким була надаконтролю бур'янів на толерантність або резистентність до цих або інших гербіцидів за допомогою генетичного маніДля після сходового застосування звичайно пулювання або мутації і селекції Наприклад, можвикористовується норма обробки від 1 до 500г/га, на обробляти кукурудзу, пшеницю, рис, сою, цукдля передпосівних обробок звичайно використоровий буряк, бавовну, рапс та ІНШІ вують норми застосування від 10 до 1000г/га Посільськогосподарські культури, яким була надана значені більш високі норми витрат звичайно притолерантність або резистентність до сполук, які є водять до неселективного пригнічення великої інгібіторами ацетолактатсинтази у чутливих росКІЛЬКОСТІ небажаної рослинності Більш низькі нолин Також можна обробляти толерантні до гліформи витрат звичайно приводять до селективного сату і глуфосинату сільськогосподарські культури, контролю і можуть використовуватися у МІСЦІ виабо окремо, або в поєднанні з вказаними гербіциростання сільськогосподарських культур дами Деяким культурам (наприклад, бавовні) моГербіцидні сполуки за даним винаходом часто же бути надана толерантність до ауксинових гернайкращим чином застосовують у поєднанні з одбіцидів, таких як 2,4-дихлорфеноксюцтова ним або декількома іншими гербіцидами для досякислота Дані гербіциди можна використовувати гнення пригнічення широкого ряду небажаної росдля обробки таких резистентних сільськогосполинності При використанні у поєднанні з іншими дарських культур або інших толерантних до ауксигербіцидами сполуки, що заявляються у даному ну сільськогосподарських культур описі, можуть бути введені до складу разом з іншим гербіцидом або гербіцидами, змішані у резерХоча можливе безпосереднє застосування 4вуарі з іншим гербіцидом або гербіцидами чи заамінопіколінатних сполук формули І як гербіцидів, стосовуватися послідовно з іншим гербіцидом або переважним є їх застосування у суміші, що містить гербіцидами Деякі з гербіцидів, які можна викоригербіцид но ефективну КІЛЬКІСТЬ сполуки разом, стовувати у поєднанні з сполуками за даним винапринаймні, з одним по-сільсь ко господарсько му ходом, включають сульфонаміди, такі як метосуприйнятним ад'ювантом або носієм ВІДПОВІДНІ лам, флуметсулам, клорансулам-метил, ад'юванти або носи не повинні бути фітотоксичнидиклосулам і флорасулам, сульфонсечовини, такі ми відносно цінних сільськогосподарських культур, як хлоримурон, нікосульфурон і метсульфурон, особливо у концентраціях, що використовуються імідазолінони, такі як імазаквін, імазапік, імазетапір при застосуванні композицій для селективної боі імазамокс, феноксіалканові кислоти, такі як 2,4-Д ротьби з бур'янами у присутності сільськогоспоі МСРА, піридинілоксюцтові кислоти, такі як тридарських культур, і не повинні ХІМІЧНО взаємодіяти клопір і флуроксипір, карбонові кислоти, такі як з сполуками формули І або іншими інгредієнтами клопіралід і дикамба, динітроаніліни, такі яктрифкомпозицій Такі суміші можуть бути розроблені луралін і пендиметалін, хлорацетаніліди, такі як для безпосереднього нанесення на бур'яни або алахлор, ацетохлор і метолахлор та ІНШІ звичайні місце їх виростання або можуть являти собою гербіциди, включаючи ацифлуорфен, бентазон, концентрати або склади, які нормальним чином кломазон, фуміклорак, флуометурон, фомезафен, розводять додатковими носіями та ад'ювантами лактофен, лінурон, ізопротурон і метрибузин Осоперед застосуванням Вони можуть бути твердибливо переважними є комбінації з флорасуламом, ми, такими, наприклад, як дуети, гранули, вододи2,4-Д та флуроксипіром, які проти деяких видів сперговані гранули або змочувані порошки, або бур'янів можуть дійсно виявляти синергізм Синерідинами, такими наприклад як концентрати, що рптична реакція у ВІДПОВІДЬ також може бути одеемульгуються, розчини, емульсії або суспензії ржана при змішуванні сполук за даним винаходом ВІДПОВІДНІ сільськогосподарські ад'юванти і з інгібіторами транспорту ауксину, такими як дифноси, які можна використовувати при одержанні луфензопір і хлорфлуренол Гербіцидні сполуки за гербіцидних сумішей за винаходом, добре ВІДОМІ даним винаходом можна, крім того, використовуфахівцям у даній області вати у поєднанні з гліфосатом і глуфосинатом на РІДКІ НОСИ, ЯКІ можна використовувати, вклюгліфосат-толерантних або глуфосинатчають воду, толуол, ксилол, петролейний ефір, толерантних культурах Звичайно переважним є рослинну олію, ацетон, метилетилкетон, циклогекзастосування сполук винаходу у комбінації з гербісаном, трихлоретилен, перхлоретилен, етилацецидами, які є селективними для культури, що обтат, амілацетат, бутилацетат, монометиловий робляється, і які доповнюють спектр бур'янів, що ефір пропіленгліколю і монометиловий ефір діетипригнічуються даними сполуками при нормах обленгліколю, метанол, етанол, ізопропанол, амілоробки, які використовуються Крім того, звичайно вий спирт, етиленгліколь, пропіленгліколь, гліцепереважним є одночасне застосування сполук рин і тому подібні Звичайно для розбавлення винаходу та інших доповнюючих гербіцидів, або у концентратів переважною є вода вигляді комбінованого складу, або у вигляді резервуарноїсуміші ВІДПОВІДНІ тверді носи включають тальк, пірофілітову глину, дюксид кремнію, атапульговану глину, каолінову глину, кізельгур, крейду, діатомоСполуки даного винаходу звичайно можна виву землю, вапно, карбонат кальцію, бентонітову користовувати у поєднанні з добре відомими герглину, Фуллерову землю, лушпиння бавовняного біцидними захисними засобами, такими як клоквіннасіння, пшеничне борошно, соєве борошно, пемтоцет, фурилазол, дихлормід, беноксакор, зу, деревне борошно, борошно з шкаралупи воломефенпір-етил, фенклоразол-етил, флуразол і ського горіху, ЛІГНІН і тому подібне флуксофенім, для посилення їх селективності Додатково вони можуть використовуватися для Звичайно є бажаним включення до композицій боротьби з небажаною рослинністю у багатьох за даним винаходом одного або декількох повер 14 13 57184 хово-активних агентів Такі поверхово-активні агерозглядати як обмеження формули винаходу нти вигідно використовуються як у твердих, так і у Приклади рідких композиціях, особливо у розроблених для 1 Одержання 4-аміно-3,6-дихлорпіридин-2розбавлення носієм перед застосуванням Поверкарбонової кислоти (Сполука 1) хово-активні агенти можуть бути аніонними, катіУ 3-літрову (л) хімічну склянку додавали 2000 онними або неюнними за своїм характером і мограмів (г) гарячої води, 115,1г 50-процентного по жуть використовуватися як емульгуючі агенти, вазі NaOH і 200г вологої 4-амшо-3,5,6змочувальні агенти, суспендуючі агенти або в інтрихлорпіридин-2-карбоновоі кислоти (79,4 процеших цілях нти) Розчин перемішували протягом ЗО хвилин (хв), фільтрували через паперовий фільтр і переТипові поверхово-активні агенти включають носили до 5-л подаючого/рециркуляціиного резерсолі алкілсульфатів, такі як лаурилсульфатдіетавуару Даний розчин важив 2315г і містив 6,8 пронол амонію, алкіларилсульфонатні солі, такі як центи 4-амшо-3,5,6-трихлорпіридин-2-карбоновоі додецилбензолсульфонат кальцію, продукти прикислоти Завантажувальний розчин рециркулював єднання алкілфенол-алкіленоксид, такі як нонілзі швидкістю приблизно 9,46л/хв при температурі фенол-Сі8-етоксилат, продукти приєднання спирт30°С через єдину (неподілену) електрохімічну коалкіленоксид, такі як тридециловий спирт-Сіємірку, що має анод Hastelloy С і суцільнорешітчасетоксилат, мила, такі як стеарат натрію, алкілнафтий срібний сітчастий растровий катод Після норталінсульфонатні солі, такі як дибутилнафталінсумальної анодизацм при +0,7 вольта (В), полярність льфонат натрію, діалкілові складні ефіри сульфокомірки змінювали і починали електроліз Робочий сукцинатних солей, такі як ди(2потенціал катода контролювали від -1,1 до -1,4 В етилгексил)сульфосукцинат натрію, складні ефіри відносно Ag/AgCI (3,0 М CL) електрода порівнянсорбіту, такі як сорбітололеат, четвертинні аміни, ня При рециркулюванні завантажувального розтакі як хлорид лаурилтриметиламонію, поліетилечину до рециркуляційного резервуару повільно нгліколеві ефіри жирних кислот, такі як поліетилеподавали насосом 50-процентний NaOH для піднглікольстеарат, блок-сополімери етиленоксиду і тримки концентрації NaOH при 1,5-2,0 процентнопропіленоксиду, та солі моно- і діалкілфосфатних му надлишку Приблизно через 15 годин (година) складних ефірів електроліз закінчували і витікаючий з комірки стік Інші ад'юванти, що звичайно застосовуються у фільтрували через паперовий фільтр Розчин нейсільськогосподарських композиціях, включають тралізували концентрованою НСІ і концентрували агенти сумісності, протиспінюючі агенти, комплекдо приблизно 750г сирого концентрату Концентсоутворювальні агенти, нейтралізуючі агенти та рат нагрівали до 85°С при перемішуванні і рН добуфери, інгібітори корозії, барвники, віддушки, водили до значення менше 1 концентрованої НСІ спредери, розподіляючі агенти, агенти прилипання протягом ЗО хвилин Одержану суспензію охоло(адгезії), диспергуючі агенти, загусники, агенти, що джували до температури навколишнього середознижують температуру замерзання, протимікробні вища і фільтрували Осад на фільтрі промивали агенти і тому подібні Композиції також можуть порціями води Зх200мілілітрів (мл) і сушили у вамістити ІНШІ сумісні компоненти, наприклад, ІНШІ куумі при 80°С Висушений продукт, 118,1г являв гербіциди, регулятори росту рослин, фунгіциди, собою за даними аналізу цільовий продукт з чисінсектициди і тому подібне й можуть бути одержані тотою 90,6 проценти, газова хроматографія (ГХ) у вигляді складу з рідкими добривами або твердипоказала наявність приблизно 4 процентів 4-аміноми сипучими добривами-носіями, такими як нітрат 3,5,6-трихлорпіридин-2-карбоновоі кислоти, що амонію, сечовина і тому подібне залишається як домішок Очищений зразок 4амшо-3,6-дихлорпіридин-2-карбоновоі кислоти мав Концентрація активних інгредієнтів у гербіцидтемпературу плавлення (т пл ) 185-187°С (розкл ), них композиціях за даним винаходом звичайно 1 Н ЯМР (ДМСО-de) 5 13,9 (ушир, 1Н), 7,0 (ушир м, складає від 0,001 до 98 процентів по вазі Часто 2Н), 6,8 (с, 1Н), 13С ЯМР {1Н} (ДМСО-de) 5 165 4 використовуються концентрації від 0,01 до 90 про(1С), 153,4 (1С), 149,5 (1С), 147,7 (1С), 111,0 (1С), центів по вазі У композиціях, розроблених для 108,1 (1С) застосування як концентратів, активний інгредієнт звичайно присутній у концентрації від 5 до 98 вагових процентів, переважно від 10 до 90 вагових 2 Одержання 2-етил гексил 4-амшо-3,6процентів Такі композиції перед застосуванням дихлорпіридин-2-карбоксилату (Сполука 2) звичайно розбавляють інертним носієм, таким як До розчину 2-етилгексанолу (Юмл) і сірчаної вода Розбавлені композиції, які звичайно нанокислоти (1 мл) додавали 4-амшо-3,6сяться на бур'яни або на місце виростання бур'ядихлорпіридин-2-карбонову кислоту (0,0097моль, нів, звичайно містять від 0,0001 до 1 вагового про2,0г) Після нагрівання реакційної суміші при КИПІНценту активного інгредієнта і переважно містять НІ ЗІ зворотним холодильником протягом ночі реавід 0,001 до 0,05 вагових процентів кційну суміш охолоджували, виливали у воду (75мл) і екстрагували етилацетатом (75мл) ОргаДані композиції можна наносити на бур'яни нічну фазу промивали бікарбонатом натрію (75мл), або місця їх виростання з використанням звичайсушили (Na2SO4) і концентрували Одержану тверних наземних або повітряних пристосувань для ду речовину перекристалізовували з дихлорметапосипання, розпилювачів і пристосувань для нанену та гексану і фільтрували, одержуючи 2сення гранул, за допомогою додання до води для етил гексил 4-амшо-3,6-дихлорпіридин-2поливу та іншими звичайними засобами, відомими фахівцям у даній області карбоксилат (0,0074моль, 2,36г) у вигляді кристаНаступні приклади представлені для ілюстралічної твердої речовини (т пл 55°С) 1Н ЯМР ції різних аспектів даного винаходу і їх не треба (CDCI3) 5 0,9 (7Н, м), 1,3 (7Н, м), 1,7 (1Н, м), 4,3 16 15 57184 (2H, д), 5,1 (2Н, ушир с), 6,7 (Н, с) трію (150мл) Одержану тверду речовину збирали і сушили у вакуумі, одержуючи білу тверду речовиНаступні ефіри 4-аміно-3,5,6-трихлорпіридин1 ну (0,08моль, 21,4г) Н ЯМР (CDC13) 5 4,1 (ЗН, с), 2-карбоновоі кислоти одержували ВІДПОВІДНО ДО 7,3 (1Н, д), 7,7(1 Н, д) методики прикладу 2 метил 4-амшо-3,6-дихлорпіридин-2В N-оксид метил 6-бром-3-хлор-4карбоксилат (Сполука 3), т пл 134-135°С нітропіридин-2-карбоксилату етил 4-амшо-3,6-дихлорпіридин-2-карбоксилат До розчину димлячої азотної кислоти (Юмл) і (Сполука 4), т пл 98-99°С димлячої сірчаної кислоти (Юмл) додавали Nн-пропіл 4-аміно-3,6-дихлорпіридин-2оксид метил б-бром-З-хлорпіридин-2-карбоксилату карбоксилат (Сполука 5), т пл 94-95°С і реакційну суміш нагрівали при 70°С на масляній бані протягом 4 годин Суміш виливали на льодяну ізопропіл 4-аміно-3,6-дихлорпіридин-2воду (ЮОмл) і екстрагували етилацетатом карбоксилат (Сполука 6), т пл 114-І15°С (Зх75мл) та здійснювали зворотну промивку об'єдн-бутил 4-амшо-3,6-дихлорпіридин-2наних екстрактів насиченим розчином солі, сушикарбоксилат (Сполука 7), т пл 78-79°С ли (Na2SO4) і концентрували Темну олію хроматон-пентил 4-амшо-3,6-дихлорпіридин-2графували на дюксиді кремнію у суміші 4 1 карбоксилат (Сполука 8), т пл 71-73°С ЕЮАс/гексан, одержуючи N-оксид метил 6-бром-Зн-гексил 4-аміно-3,6-дихлорпіридин-2хлор-4-нітропіридин-2-карбоксилату (0,007моль, карбоксилат (Сполука 9), т пл 65-66°С 2,2г) 1 НЯМР(СОСІ 3 ) 5 4,1 (ЗН, с), 8,4(1 Н, с) бутоксіетил 4-амшо-3,6-дихлорпіридин-2карбоксилат (Сполука 10), т пл 64-7°С у вигляді С Метил 4-амшо-6-бром-3-хлорпіридин-2моногідрату карбоксилат 3 Одержання 4-аміно-3,6-дихлорпіридин-2До розчину тетрахлориду титану (0,015моль, карбоксаміду (Сполука 11) 2,8г) у тетрапдрофурані (50мл) додавали літійаУ 250мл 3-горлу круглодонну колбу, обладналюмшійпдрид (0,0175моль, 0,7г) Чорну суспензію ну механічною мішалкою, додавали метил 750 перемішували 15хв перед доданням N-оксиду ме(10,0г, 45моль) і 28% водн NH4OH (35мл) при 0°С тил 6-бром-3-хлор-4-нітропіридин-2-карбоксилату Суспензію інтенсивно перемішували протягом 24 (0,007моль, 2,3г) у ТГФ (25мл) Розчин перемішугодин, при поступовому нагріванні до 25°С Сували 1 годину перед виливанням у суміш 1 1 спензію фільтрували з відсмоктуванням у вакуумі і H2O/NH4OH та фільтруванням Фільтрат екстрагуосад на фільтрі промивали на фільтрі холодною вали ЕЮАс (2х75мл) Органічну фазу сушили водою (2x100 мл) Після сушки на повітрі на філь(Na2SO4) і концентрували Червону тверду речовитрі збирали аналітичне чистий білий твердий прону хроматографували на дюксиді кремнію у суміші дукт, одержуючи 4-амшо-3,6-дихлорпіридин-24 1 ЕЮАс/гексан, одержуючи метил 4-амшо-6карбоксамід 11 (8,58г, 92% вихід), т пл 240-241 °С бром-З-хлорпіридин-2-карбоксилат (О.ООЗмоль, 0,8г), т п л 194-5°С 1Н ЯМР (CDCI3) 5 3,95 (ЗН, с), 4 Одержання метил N-ацетил 4-амшо-3,65,3 (2Н, уширс), 6,9 (1Н, с) дихлорпіридин-2-карбоксилату (Сполука 12) та N.N-діацетил 4-амшо-3,6-дихлорпіридин-2D 4-Амшо-6-бром-3-хлорпіридин-2-карбонова карбоксилату (Сполука 13) кислота (Сполука 14) Розчин оцтового ангідриду (75мл) і метил 4До метил 4-амшо-6-бром-3-хлорпіридин-2амшо-3,6-дихлорпіридин-2-карбоксилату карбоксилату (200мг, 0,8моль) у Юмл метанолу (0,00904моль, 2,0г) перемішували і нагрівали при додавали надлишок 2н NaOH (Юмл) Суміш переКИПІННІ зі зворотним холодильником протягом ночі мішували протягом 1 години при температурі наРозчин охолоджували, концентрували, вміщували вколишнього середовища і потім упарювали досув етилацетат (ЮОмл) і промивали водою (ЮОмл) ха у вакуумі Залишок розчиняли у воді та Органічну фазу промивали насиченим розчином діетиловому ефірі Після розділення фаз водний бікарбонату натрію (ЮОмл), сушили (Na2SO4) і шар підкисляли 1н НСІ до рН=2 Водний шар упаконцентрували Розчин очищали хроматографією рювали досуха і залишок розчиняли у 50мл метана силікагелі Попереду йдуча пляма була виділенолу та фільтрували Фільтрат упарювали при на, даючи жовту олію, ідентифіковану як діацилозниженому тиску і залишок розтирали з 51 ваний 4-амід -Сполука 13 (0,0023моль, 0,700г) Н процентним діетиловим ефіром у петролейному ЯМР 2,2 (6Н, с), 3,9 (ЗН, с), 7,3 (1Н, с) Друга пляефірі, одержуючи 70мг 4-амшо-6-бром-3ма давала жовту тверду речовину, ідентифіковану хлорпіридин-2-карбоновоі кислоти, т пл 182як моноацилований 4-амід -Сполука 12 183°С (0,0035моль, 0,920г), т пл 102-103°С 6 Одержання метил 4-амшо-3-хлор-65 Одержання 4-амшо-6-бром-3-хлорпіридин-2фторпіридин-2-карбоксилату (Сполука 15) карбонової кислоти (Сполука 14) А Метил 3-хлор-4,6-дифторпіридин-2А N-оксид метил 6-бром-3-хлорпіридин-2карбоксилат карбоксилату До розчину метил 3,4,6-трихлорпіридин-2До розчину метил 6-бром-3-хлорпіридин-2карбоксилату (О.ОЮмоль, 2,4г) у ДМСО (Юмл) карбоксилату (0,13моль, 32,1г) у трифтороцтовій додавали фторид цезію (0,038моль, 3,8г) і суспенкислоті (75мл) і трифтороцтовому ангідриді (40мл) зію нагрівали протягом 2 годин при Ю0°С Реакобережно додавали 50%-ний перекис водню ційну суміш розчиняли у розбавленій НСІ та екст(0,17моль, 13г) Екзотермічна реакція приводила рагували етилацетатом (ЕЮАс) Органічний шар до кипіння зі зворотним холодильником Після пеобробляли (триметилсиліл)діазометаном ремішування протягом ЗО хвилин, розчин вилива(TMSCHN2) для переетерифікацм та гідролізу ли у суміш льоду і 10-процентного бісульфіту наскладного ефіру Суміш концентрували і одержа 17 57184 ний залишок хроматографували на дюксиді кремнію з використанням 10-процентного ЕЮАс/гексану, одержуючи метил З-хлор-4,6дифторпіридин-2-карбоксилат (0,0072моль, 1,5г) ] Н ЯМР (CDCI3) 5 4,00 (ЗН, с), 6,95-6,90 (1Н, м) 19 РЯМР {1Н} 5 -65,0 (д, J = 17Гц), 95,8 (д,и=17Гц) В Метил 4-амшо-3-хлор-6-фторпіридин-2карбоксилат (Сполука 15) Азид натрію (0,0086моль, 0,60г) додавали до розчину метил 3-хлор-4,6-дифторпіридин-2карбоксилату (0,0072моль, 1,5г) у 15мл диметилформаміду (ДМФ) Розчин перемішували Юхв при температурі навколишнього середовища перед виливанням у 350мл води та екстрагуванням водної суміші з використанням ЕЮАс (2х100мл) Органічну фазу сушили (Na2SO4) і потім обробляли надлишком NaBbU протягом ЗО хвилин Надлишок NaBbU гасили водним ЕЮН і суміш розбавляли водою (200мл) Органічний шар ВІДДІЛЯЛИ І ВОДНИЙ шар екстрагували ЕЮАс (2х200мл) Об'єднані органічні шари сушили (Na2SO4) і концентрували, одержуючи не зовсім білий порошок, який очищали ВЕРХ з оберненою фазою, одержуючи метил 4амшо-3-хлор-6-фторпіридин-2-карбоксилат (0,0059моль, 1,2г) 1Н ЯМР(СОСІ3) 5 3,95 (ЗН,с), 5,2-5,1 (2Н, уширс), 6,36 (1Н, с) 19РЯМР { 1 Н}5 72,7 7 Одержання 4-амшо-3,5-дифтор-6бромпіридин-2-карбоновоі кислоти (Сполука 16) А Одержання 4-амшо-3,5,6-трифтор-2ціанопіридину До розчину 3,4,5,6-тетрафтор-2-ціанопіридину у ДМФ (75мл) при 0°С повільно додавали концентрований гідроксид амонію (15мл) Реакційну суміш перемішували додатково протягом 15 хвилин і розчин розбавляли водою (150мл) Тверду речовину збирали і сушили на повітрі, одержуючи 4амшо-3,5,6-трифтор-2-ціанопіридин (25,5г, 0,16моль, 92%), т пл 291-3°С 8 Одержання метил 4-амшо-6-бром-3,5дифторпіридин-2-карбоксилату (Сполука 16) Розчин 4-амшо-3 5,6-трифтор-2-ціанопіридину (19г, 0,12моль) у тридцятипроцентному бромистому водні в оцтовій кислоті (150мл) вміщували в апарат Парра і нагрівали при 110°С протягом З годин Реакційну суміш розбавляли водою (ЗООмл) і збирали твердий (4-амшо-6-хлор-3,5дифторпіридин-2-карбоксамід) Цю речовину, без додаткового очищення, суспендували у метанолі (500мл) та додавали концентровану соляну кислоту Суспензію нагрівали при КИПІННІ ЗІ зворотним холодильником протягом 4 годин та після охолодження до кімнатної температури розбавляли водою (ЮООмл) і тверду речовину збирали і сушили, одержуючи метил 4-амшо-6-бром-3,5дифторпіридин-2-карбоксилат (9,6г, 0,04моль, 25%),тпл 110-111 °С 8 Одержання 4-амшо-3,6-дибромпіридин-2карбонової кислоти (Сполука 17) 3,4,5,6-Тетрабромпірідш-2-карбоксамід (5,0г) селективно амінували газоподібним аміаком при кімнатній температурі у ЮОмл метанолу Одержаний розчин концентрували до не зовсім білої твердої речовини і пдролізували концентрованою сірчаною кислотою (25мл) при 140°С протягом З годин Суміш підлуговували NaOH, екстрагували 18 ЕЮАс (2х100мл), підкислювали і фільтрували, одержуючи 1,4г чистої 4-амшо-3,6-дибромпіридин2-карбоновоі кислоти, т пл 205°С розкл 9 Одержання метил 4-амшо-3,5,6трибромпіридин-2-карбоксилату (Сполука 18) Метил 4-амшо-3,5,6-трибромпіридин-2карбоксилат одержували амінуванням метил 3,4,5,6-тетрабромпіридин-2-карбоксилату ВІДПОВІ ДНО до методики прикладу 6В 1НЯМР (CDCI3) 5 3,95 (ЗН, с), 6,9-6,8 (2Н, ушир с) 10 Одержання 4-амшо-3,6-дихлор-5фторпіридин-2-карбоновоі кислоти (Сполука 19) До розчину 4-амшо-3,6-дихлорпіридин-2карбоксилату (1,5г, 6,8моль) у 20мл сухого ацетонітрилу додавали біс(тетрафторборат) 1(хлорметил)-4фтор-1,4-діазонійбіцикло[2 2 2]октану (Selectfluor™ від Aldnch Chemical Company, Inc / 2,9г, 2,59моль [F+]/r) Одержану суміш нагрівали при КИПІННІ ЗІ зворотним холодильником протягом 3 годин, потім залишали охолоджуватися до кімнатної температури Цю речовину вміщували в Et20 1 промивали НгО Органічний шар сушили над MgSO4, фільтрували і концентрували, одержуючи коричневу олію Сирий продукт очищали за допомогою ВЕРХ з оберненою фазою (50% ацетонітрил/вода), одержуючи 0,37г білої твердої речовини, яку перемішували протягом 1 години у 1 н NaOH, а потім підкислювали концентрованою НСІ Білу тверду речовину, що випала в осад збирали з відсмоктуванням у вакуумі, промивали НгО і сушили у вакуумі, одержуючи 170мг 4амшо-3,6-дихлор-5-фторпіридин-2-карбоновоі кислоти (вихід 11%), т пл 214°С розкл 11 Одержання 4-амшо-3,6-дихлор-5бромпіридин-2-карбоновоі кислоти (Сполука 20) До розчину метил 4-амшо-3,6-дихлорпіридин2-карбоксил ату (18г, 81 моль) у ЮОмл димлячої сірчаної кислоти додавали бром (15мл, надлишок) Одержану суміш нагрівали при 70°С протягом ЗО хвилин, потім залишали охолоджуватися до кімнатної температури Цю речовину виливали у льодяну воду (1000мл) та екстрагували ЕЮАс (4х500мл) Об'єднані органічні екстракти сушили (MgSO4) фільтрували і концентрували, одержуючи коричневу тверду речовину Сирий продукт очищали за допомогою ВЕРХ з оберненою фазою (50% ацетонітрил/вода), одержуючи 21г 4-аміно3,6-дихлор-5-бромпіридин-2-карбоновоі кислоти у вигляді білої твердої речовини (91% вихід), Т ПЛ 201-202°С 12Одержання 4-аміно-3,6-дихлор~5трифторметилпіридин-2-карбоновоі кислоти (Сполука 21) Розчин 4-амшо-3,6-дихлор-5-трифторметил-2ціанопіридину (0,5г, 1,96моль) у 10мл 85%-ноі H2SO4 перемішували при 140°С протягом 0,5 години Реакційну суміш залишали охолоджуватися і додавали до льоду Білу тверду речовину, що випала в осад, збирали з відсмоктуванням у вакуумі, промивали ще декілька разів водою і залишали сушитися на повітрі, одержуючи 0,33г продукту у вигляді білої твердої речовини (вихід 61,4%), т пл 173°С 13 Одержання 4-амшо-3,6-дихлор-5метоксипіридин-2-карбоновоі кислоти (Сполука 22) А N-оксид метил 3-хлор-5-метоксипіридин-2 19 57184 карбоксилату У суху 3-горлу крутлодонну колбу додавали до 25мл метанолу N-оксид метил 3,5-дихлорпіридин2-карбоксилат (5,0г, 22,5моль), одержуючи суспензію Додавали 25%-ний розчин метоксиду натрію у метанолі (5,40мл, 23,62моль) та нагрівали при КИПІННІ зі зворотним холодильником протягом 1,5 години Реакційну суміш розбавляли етилацетатом і додавали до НгО Шари розділяли і водний шар насичували насиченим розчином солі та екстрагували ще 2 рази етилацетатом Об'єднані органічні шари сушили (MgSO4) і концентрували, одержуючи білу тверду речовину Очищення колонковою хроматографією (силікагель) з використанням як елюенту суміші 50% ЕЬО/петролейний ефір (1,5л), потім 100% Et20 давало 1,76г білої твердої речовини, т пл 154156°С В N-оксид метил 3-хлор-5-метокси-4нітропіридин-2-карбоксилату До N-оксиду метил 3-хлор-5-метоксипіридин-2карбоксилату (1,41г, 5,97моль) у H2SO4, охолодженому до 0°С, повільно додавали суміш 50/50, що складається з 30%-ного олеуму та димлячої НІЧОз Реакційну суміш перемішували протягом ЗО хвилин при кімнатній температурі і потім нагрівали при 70°С протягом 3 днів Реакційну суміш розбавляли етилацетатом і охолоджували до 0°С Обережно додавали насичений розчин бікарбонату натрію і шари розділяли Водний шар промивали ще 2 рази етилацетатом Об'єднані органічні шари сушили (MgSO4) та концентрували досуха Очищення колонковою хроматографією (силікагель) з використанням як елюенту суміші 20% етилацетат/гексан давало ЗООмг жовтої твердої речовини, т п л 160°С С Метил 3,6-дихлор-5-метокси-4нітропіридин-2-карбоксилат До N-оксиду метил 3-хлор-5-метокси-4нітропіридин-2-карбоксилату (0,300г, 1,12моль) у 5мл хлороформу додавали РСІз (0,664мл, 7,62моль) Реакційну суміш нагрівали при КИПІННІ ЗІ зворотним холодильником протягом 8 годин і потім концентрували досуха у вакуумі, одержуючи ЗООмг білої твердої речовини D Метил 4-амшо-3,6-дихлор-5метоксипіридин-2-карбоксилат До метил 3,6-дихлор-5-метокси-4нітропіридин-2-карбоксилату (0,300г, 1,06моль) у 5мл етилацетату додавали SnCb x 2H2O (1,60г, 7,1 моль) Реакційну суміш нагрівали при 70°С протягом ЗО хвилин і потім охолоджували до кімнатної температури До реакційної суміші додавали насичений розчин бікарбонату натрію і насичений розчин KHF2 Суміш екстрагували етилацетатом і шари розділяли Водний шар промивали ще 2 рази етилацетатом Об'єднані органічні шари сушили (MgSO4) і концентрували досуха, одержуючи 0,250г жовтої твердої речовини Е 4-Амшо-3,6-дихлор-5-метоксипіридин-2карбонова кислота (Сполука 22) 4-Амшо-3,6-дихлор-5-метоксипіридин-2карбонову кислоту одержували омиленням метилового складного ефіру ВІДПОВІДНО ДО методики прикладу 17(D), т пл 154-156°С 14 Одержання 4-амшо-3,6-дихлор-5 20 метилтюпіридин-2-карбоновоі кислоти (Сполука 23) 4-Амшо-3,6-дихлор-5-метилтюпіридин-2карбонову кислоту одержували по аналогії з одержанням 4-амшо-3,6-дихлор-5-метоксипіридин-2карбонової кислоти ВІДПОВІДНО ДО методики прикладу 13, використовуючи тюметоксид натрію замість метоксиду натрію, т пл 160°Срозкл 15 Одержання 4-амшо-3,6-дихлор-5фенілтюпіридин-2-карбоксилату (Сполука 24) 4-Амшо-3,6-дихлор-5-фенілтюпіридин-2карбонову кислоту одержували по аналогії з одержанням 4-амшо-3,6-дихлор-5-метоксипіридин-2карбонової кислоти ВІДПОВІДНО ДО методики прикладу 13, використовуючи тюфеноксид натрію замість метоксиду натрію, т пл 160°С розкл 16 Одержання метил 4-амшо-3,6-дихлор-5нітропіридин-2-карбоксилату (Сполука 25) До розчину, що містить 4-амшо-3,6дихлорпіридин-2-карбонову кислоту (0,5г, 2,43моль) і Юмл конц H2SO4 додавали по краплях суміш конц HNO3/H2SO4 (1мл/1мл) при кімнатній температурі Після перемішування протягом 5 хвилин реакційну суміш додавали до льоду і тверду речовину збирали фільтруванням у вакуумі Одержану тверду речовину розчиняли у 20% МеОН/ЕЮАс і потім додавали триметилсилілдіазометан (TMSCHN2) до завершення реакції Реакційну суміш концентрували при зниженому тиску, вміщували в Et20 і промивали водним Nah-ІСОз, сушили над MgSO4, фільтрували і концентрували, одержуючи коричневу олію Сирий продукт очищали хроматографією, елююючи сумішшю 10% етилацетату-гексану, одержуючи 80мг метилового складного ефіру у вигляді жовтої твердої речовини, т п л 127-8°С 17 Одержання 4-^метиламшо-3,6дихлорпіридин-2-карбоновоі кислоти (Сполука 26) А Метил 3,6-дихлорпіридин-2-карбоксилат У 3-горлу круглодонну колбу, обладнану зворотним холодильником додавали 3,6дихлорпіридин-2-карбонову кислоту (50,0г, 260,42моль) у метанолі (200мл), Барботували НСІ (г) до насичення розчину і перемішували при кімнатній температурі протягом 2 годин Розчин концентрували досуха у вакуумі Діетиловий ефірдодавали для одержання суспензії, яку згодом додавали у колбу, наповнену сумішшю насичений бікарбонат натрію/діетиловий ефір у співвідношенні 1 1 та перемішували протягом 10 хвилин Водну фазу екстрагували діетиловим ефіром (ЗхЗООмл) Об'єднані екстракти сушили (MgSO4) і концентрували, одержуючи 46,6г світло-жовтої твердої речовини 1 Н ЯМР (CDCI3) 5 4,00 (с, ЗН), 7,41 (д, 1Н), 7,80 (Д, 1Н) В N-оксид метил 3,6-дихлорпіридин-2карбоксилату Метил 3,6-дихлорпіколшат (20,0г, 97,07моль) розчиняли у мінімальній КІЛЬКОСТІ трифтороцтової кислоти (ТФОК) В окремій колбі перемішували трифтороцтовий ангідрид (ТФОА, 38мл) і 50% Н2О2 (9,9г, 145,61 моль), які додавали до ТФОК розчину Реакційну суміш перемішували при КИПІННІ ЗІ зворотним холодильником протягом 1 години і концентрували досуха Оранжеву олію розчиняли в етилацетаті та насиченому бікарбонаті натрію 21 57184 Фази розділяли і водну фазу екстрагували етилацетатом (2х200мл) Об'єднані екстракти сушили (MgSO4) і концентрували, одержуючи жовту тверду речовину Очищення колонковою хроматографією (силікагель) з використанням як елюенту суміші 50% етилацетат/гексан, давало 12,13г жовтої твердої речовини 1Н ЯМР (CDCI3) 5 4,00 (с, ЗН), 7,25 (д, 1Н), 7,50 (д, 1Н) С Метил ЗЛ6-трихлорпіридин-2-карбоксилат До N-оксиду метил 3,6-дихлорпіколшату (5,0г, 22,52моль), розчиненому у 15мл ацетонітрилу додавали РОСІз (4,20мл, 45,04моль) Реакційну суміш перемішували при КИПІННІ ЗІ зворотним холодильником протягом 5 годин, охолоджували до кімнатної температури і концентрували досуха у вакуумі Одержану оранжеву олію розчиняли у діетиловому ефірі Обережно додавали насичений бікарбонат натрію і водну фазу екстрагували діетиловим ефіром (2х100мл) Об'єднані екстракти сушили (MgSO4) і концентрували досуха Очищення колонковою хроматографією (силікагель) з використанням як елюенту суміші 20% етилацетат/гексан давало 5,89 г світло-жовтої твердої речовини 1Н ЯМР (CDCI3) 5 4,00 (с, ЗН), 7,55 (с, 1Н) D 3,4,6-Трихлорпіридин-2-карбонова кислота До метил 3,4,6-трихлорпіколшату (3,57г, 14,85моль) у 20мл метанолу додавали 1н NaOH (14,85мл, 14,85моль) Реакційну суміш перемішували при кімнатній температурі протягом 1 години і потім концентрували досуха у вакуумі Додавали по ЮОмл діетилового ефіру та ЬЬО Водний шар підкисляли 1н НСІ до рН=2, додавали хлористий метилен і водну фазу екстрагували додатковою КІЛЬКІСТЮ СН2СІ2 (2x100мл) Об'єднані екстракти сушили (MgSO4) і концентрували, одержуючи 3,13г білої твердої речовини 1Н ЯМР (CDCI3) 5 7,50 (с, 1Н) Е 4-М-Метиламшо-3,6-дихлорпіридин-2карбонова кислота (Сполука 26) 3,4,6-Трихлорпіридин-2-карбонову кислоту (1,56г, 6,89моль) розчиняли у метиламіні та вміщували в апарат Парра при 80°С на 2 дні Реакційну суміш охолоджували до кімнатної температури і розбавляли етилацетатом Додавали 1н НСІ до рН=2 Водну фазу екстрагували етилацетатом (2х50мл) і об'єднані екстракти сушили (MgSO4) та концентрували досуха Цільовий продукт розтирали у суміші 5% діетиловий ефір/петролейний ефір, тверду речовину відфільтровували і сушили, одержуючи 0,600г світло-жовтої твердої речовини Н ЯМР (CDCI3) 5 2,75 (с, ЗН), 5,70 (с, 1Н), 6,30 (с, 1Н),тпл 170-172°С Наступні N-алкілові аналоги 4-амшо-3,6дихлорпіридин-2-карбоновоі кислоти одержували ВІДПОВІДНО до методики прикладу 17 4-г\І-етиламшо-3,6-дихлорпіридин-2-карбонова кислота (Сполука 27), т пл 136-137°С 4-І\І-ізопропіламшо-3,6-дихлорпіридин-2карбонова кислота (Сполука 28), т пл 146-147°С 4-г\І-бутиламіно-3,6-дихлорпіридин-2карбонова кислота (Сполука 29), т пл 96-97°С 4-І\І-аліламіно-3,6-дихлорпіридин-2-карбонова кислота (Сполука ЗО), т пл 128-131 °С 4-г\І-пдроксіетиламіно-3,6-дихлорпіридин-2 22 карбонова кислота (Сполука 31), т пл 140-141°С 4-г\І-метоксіетиламшо-3,6-дихлорпіридин-2карбонова кислота (Сполука 32), т пл 97-99°С 4-г\І,г\І-диметиламіно-3,6-дихлорпіридин-2карбонова кислота (Сполука 33), т пл, 110°С 4-М-пдрокси-г\І-метиламіно-3,6-дихлорпіридин2-карбонова кислота (Сполука 34), т пл 140-1 °С 4-г\І-метокси-г\І-метил-3,6-дихлорпіридин-2карбонова кислота (Сполука 35), т пл 98-99°С 4-піролідино-3,6-дихлорпіридин-2-карбонова кислота (Сполука 36), т пл 153-5°С 4-піроло-3,6-дихлорпіридин-2-карбонова кислота (Сполука 37), т пл 155-156°С 18 Одержання метил 4-азидо-6-бром-3хлорпіридин-2-карбоновоі кислоти (Сполука 38) До розчину метил 4,6-дибром-З-хлорпіридин2-карбоксил ату (6,0г, 0,018моль) у ДМФ (50мл) додавали азид натрію (2,0г, О.ОЗмоль) і розчин нагрівали при 50°С протягом 1 години Реакційну суміш розбавляли водою (200мл) та охолоджували до 0°С протягом 1 години Тверду речовину збирали, одержуючи метил 4-азидо-6-бром-3хлорпіридин-2-карбоксилат (4,4г, 0,012моль, 66%), т п л 84-86°С 19 Одержання 4-нітро-3,6-дихлорпіридин-2карбонової кислоти (Сполука 39) N-оксид метил 3,6-дихлорпіридин-2карбоксилату (5,0г, 22,52моль) розчиняли у мінімальній КІЛЬКОСТІ H2SO4 Суміш охолоджували на бані лід/вода і повільно додавали до неї 30%-ний олеум (9,6мл) та димлячу НІЧОз (9,6мл), поступово нагрівали до 65°С і перемішували протягом 48 годин Охолоджену реакційну суміш розбавляли етилацетатом (200мл) та обережно додавали до неї насичений розчин бікарбонату натрію Продукт екстрагували етилацетатом (2х150мл) і об'єднані екстракти сушили (MgSO4) і концентрували, одержуючи 0,01г жовтої твердої речовини, т п л 192193°С 20 Одержання 4-г\І,г\І-диметилформамідино3,6-дихлорпіридин-2-карбоновоі кислоти (Сполука 40) До суспензії метил 4-амшо-3,6-дихлорпіридин2-карбоновоі кислоти (2,07г, Ю.Омоль) у ТГФ (50мл) додавали 5,0 еквівалента диметилацеталю N.N-диметилформаміду (50моль) Суміш нагрівали при 50°С протягом 1 години, протягом даного часу суспензія перетворювалася у гомогенний розчин Охолоджену реакційну суміш концентрували у вакуумі, розтирали з гексанами, одержуючи білу аморфну тверду речовину і сушили у високому вакуумі, одержуючи 2,5г дуже гігроскопічного білого порошку (вихід 95%), Н ЯМР (ДМСО) 5 8,21 (1Н, с), 7,95 (1Н, с), 3,25 (ЗН, с), 3,17 (ЗН, с) 21 Одержання 4-амшо-6-бром-3метоксипіридин-2-карбоновоі кислоти (Сполука 41) А Метил 4,6-дибром-3-метоксипіридин-2карбоксилат До метил 4,6-дибром-3-пдроксипіридин-2карбоксилату (3,98г, 12,81 моль) у 40мл ацетону додавали К2СО3 (2,0г, 14,47моль) і диметилсульфат (1,20мл, 12,37моль) Реакційну суміш нагрівали при КИПІННІ зі зворотним холодильником протягом ночі і концентрували досуха Залишок розчиняли в етилацетаті та насиченому розчині бікарбонату натрію Фази розділяли і водну фазу 23 57184 екстрагували етилацетатом (ЗхЮОмл) Об'єднані екстракти сушили (MgSO4) і концентрували досуха Залишок очищали хроматографією (силікагель) Елюювання сумішшю 15% етилацетат/гексан давало 0,980г білої твердої речовини 1 НЯМР (CDCI3) 5 3,95 (с, ЗН), 3,90 (с, ЗН), 7,80 (с, 1Н) Е, Метил 4-азидо-6-бром-3-метоксипіридин-2карбоксилат Метил 4,6-дибром-3-метоксипіридин-2карбоксилат (0,980г, 3,02моль) розчиняли у мінімальній КІЛЬКОСТІ ДМФ Повільно додавали азид натрію (0,216г, 3,32моль) з подальшим доданням НгО для утворення гомогенного розчину Реакційну суміш нагрівали при 60°С та перемішували протягом 2 днів Реакційну суміш додавали у колбу, наповнену льодяною водою і екстрагували етилацетатом (Зх 50мл) Екстракти об'єднували і знову промивали НгО, сушили (MgSO4) й концентрували, одержуючи 0,500 г оранжевої олії 1Н ЯМР (CDCI3) 5 3,90 (с, ЗН), 3,95 (с, ЗН), 7,20 (с, 1Н) С Метил 4-амшо-6-бром-3-метоксипіридин-2карбоксилат До метил 4-азидо-6-бром-3-метоксипіридин-2карбоксилату (0,500г, 1,74моль) у Юмл метанолу додавали NaBH4 (0,046г, 1,22моль) Реакційну суміш перемішували при кімнатній температурі протягом 10 хвилин Додавали етилацетат і воду і фази розділяли Органічну фазу промивали НгО, сушили (MgSO4) і концентрували досуха у вакуумі Залишок очищали хроматографією (силікагель) Елюювання 100%-ним етилацетатом давало 0,300г білої твердої речовини 1Н ЯМР (CDCI3) 5 3,90 (с, 1Н), 3,95 (с, 1Н), 4,60 (с, 2Н), 6,85 (с, 1Н) D 4-Амшо-6-бром-3-метоксипіридин-2карбонова кислота (Сполука 41) До метил 4-амшо-6-бром-3-метоксипіридин-2карбоксилату (0,300г, 1,15моль) у Юмл метанолу додавали 1н NaOH (1,15мл, 1,15моль) Реакційну суміш перемішували при кімнатній температурі протягом 1 години і концентрували досуха у вакуумі Додавали діетиловий ефір і НгО Водний шар підкисляли 1н НСІ до рН=2 та концентрували досуха До білої твердої речовини додавали метанол (50мл) Суміш фільтрували і фільтрат концентрували досуха Розтирання з сумішшю 5% діетиловий ефір/петролейний ефір давало 0,180г світлорожевої твердої речовини 1НЯМР(ДМСО) 5 3,60 (с, ЗН), 6,80 (с, 1Н) 22 Одержання 4-амшо-6-бром-5-хлор-3метоксипіридин-2-карбоновоі кислоти (Сполука 42) А Метил 4-амшо-6-бром-5-хлор-3метоксипіридин-2-карбоксилат До метил 4-амшо-6-бром-3-метоксипіридин-2карбоксилату (1,45г, 5,56моль) у Юмл ацетонітрилу додавали піпеткою у надлишку хлористий сульфурил до пожовтіння розчину Розчин нагрівали при КИПІННІ зі зворотним холодильником протягом 5 хв Реакційну суміш додавали до насиченого розчину бікарбонату натрію і водну фазу екстрагували діетиловим ефіром (Зх) Об'єднані органічні екстракти сушили (MgSO4), фільтрували і концентрували у вакуумі, одержуючи жовту тверду речовину Тверду речовину промивали сумішшю 10% діетиловий ефір/петролейний ефір і тверду речовину відфільтровували, одержуючи 0,580г білої 24 твердої речовини В, 4-Амшо-6-бром-5-хлор-3-метоксипіридин-2карбонова кислота (Сполука 42) До метил-4-амшо-6-бром-5-хлор-3метоксипіридин-2-карбоксилату (0,300 г, 1,02моль) у Юмл метанолу додавали 1н NaOH (1,10мл, 1,10моль) Реакційну суміш перемішували при кімнатній температурі протягом 4 годин і потім концентрували досуха у вакуумі Одержаний водний шар підкисляли концентрованою НСІ Білу тверду речовину збирали фільтруванням і промивали НгО Тверду речовину сушили при 50°С у вакуумі, одержуючи 0,230г білої пухнастої твердої речовини, т пл 154-156°С 23, Одержання 4-амшо-5,6-дихлор-3фторпіридин-2-карбоновоі кислоти (Сполука 43) А 4-Амшо-5,6-дихлор-2-трихлорметилпіридин До розчину 4,5,6-трихлор-2трихлорметилпіридину (2г, 6,7моль) у водному ДМФ додавали ІЧаІЧз (0,5г, 7,7моль) Одержану суміш нагрівали при 70°С протягом 2 годин, додавали у НгО і екстрагували (Зх) Et20 Органічний шар концентрували, одержуючи білу тверду речовину, яку розчиняли у Юмл МеОН Додавали надлишок NaBH4 і реакційну суміш перемішували при кімнатній температурі протягом 0,5 години Цю речовину додавали у НгО, екстрагували (Зх) Et20, сушили над MgSO4 і концентрували у вакуумі Одержану тверду речовину промивали декілька разів гексаном, одержуючи 1,3г 4-амшо-5,6дихлор-2-трихлорметил піридину В 4-Амшо-5,6-дихлор-3-фторпіридин-2карбонова кислота (Сполука 43) До розчину 4-амшо-5,6-дихлор-2трихлорметилпіридину (1,25г, 4,46моль) у 20мл сухого ацетонітрилу додавали Selectfluor™ (1,9г, 2,59моль [F*]/r) Одержану суміш нагрівали при КИПІННІ зі зворотним холодильником протягом 72 годин, потім залишали охолоджуватися до кімнатної температури Цю речовину вміщували у Et20 і промивали НгО Органічний шар сушили над MgSO4, фільтрували і концентрували, одержуючи темну олію Сирий продукт очищали за допомогою ВЕРХ з оберненою фазою (75% ацетонітрил/вода), одержуючи 0,2г білої твердої речовини, яку перемішували у 80%-ній H2SO4 при 155°С протягом 0,5 години Реакційну суміш залишали охолоджуватися і екстрагували декілька разів сумішшю 10% МеОН/СНгСІг Органічний шар сушили над MgSO4, фільтрували і концентрували, одержуючи білу тверду речовину, яку промивали декілька разів сумішшю гексан-діетиловий ефір, одержуючи 60мг 4-амшо-5,6-дихлор-3-фторпіридин-2карбоиової кислоти, т пл 208°С розкл 24 Одержання 4-амшо-3-бром-6-хлорпіридин2-карбоновоі кислоти (Сполука 44) А Метил 3-бром-4-хлорпіридин-2-карбоксилат До розчину 3-бром-4-хлорпіридин-2карбонової кислоти (1,75г, 7,4моль) у МеОН додавали безводний НСІ Одержану суміш перемішували при кімнатній температурі протягом 18 годин Реакційну суміш концентрували, одержуючи тверду речовину, яку розподіляли між Et20 і насиченим МаНСОз Органічний шар сушили над MgSO4, фільтрували і концентрували, одержуючи коричневий залишок Цю речовину очищали колонковою 26 25 57184 флеш-хроматографією, одержуючи 1,35г продуїсгу продукту у вигляді білої твердої речовини, т пл у вигляді блідо-жовтої олії 62-3°С В Метил 3-бром-4,6-дихлорпіридин-2В Метил 4-амшо-6-трифторметилпіридин-2карбоксилат карбоксилат До розчину метил 3-бром-4-хлорпіридин-2До розчину метил 4-хлор-6карбоксилату (1,35г, 5,4моль) у 5мл ТФОК додатрифторметилпіридин-2-карбоксилату (2,44г, вали 30% Н2О2 (1г, 9,8моль) Одержану суміш пе10,2моль) у водному ДМФ додавали ІЧаІЧз (0,7г, ремішували при 15°С протягом 0,5 години і зали10,8моль) Одержану суміш нагрівали при 70°С шали охолоджуватися до кімнатної температури протягом 18 годин, додавали у НгО і екстрагували Додавали Et2
ДивитисяДодаткова інформація
Назва патенту англійською4-aminopicolinates and their application as herbicides
Автори англійськоюFields Steven Craigh, Balco Terri William
Назва патенту російською4-аминопиколинати и их применение в качестве гербицидов
Автори російськоюФилдз Стефен Крэйг, Балко Терри Вилльям
МПК / Мітки
МПК: C07D 401/04, A01N 43/40, C07D 213/89, C07D 213/81, C07D 213/79
Мітки: гербіцидів, застосування, 4-амінопіколінати
Код посилання
<a href="https://ua.patents.su/23-57184-4-aminopikolinati-ta-kh-zastosuvannya-yak-gerbicidiv.html" target="_blank" rel="follow" title="База патентів України">4-амінопіколінати та їх застосування як гербіцидів</a>
Попередній патент: Повітрозабирач вентилятора двоконтурного турбореактивного двигуна
Наступний патент: g-кристалічна форма трет-бутиламінової солі періндоприлу, спосіб її одержання і фармацевтична композиція, що її містить
Випадковий патент: Система поверхнево-активних речовин, спосіб її одержання та пестицидна композиція