Композиція модафінілу
Номер патенту: 96117
Опубліковано: 10.10.2011
Автори: Петерсон Меттью, Алмарссон Орн, Бургхол Хікі Магалі, Олівейра Марк
Формула / Реферат
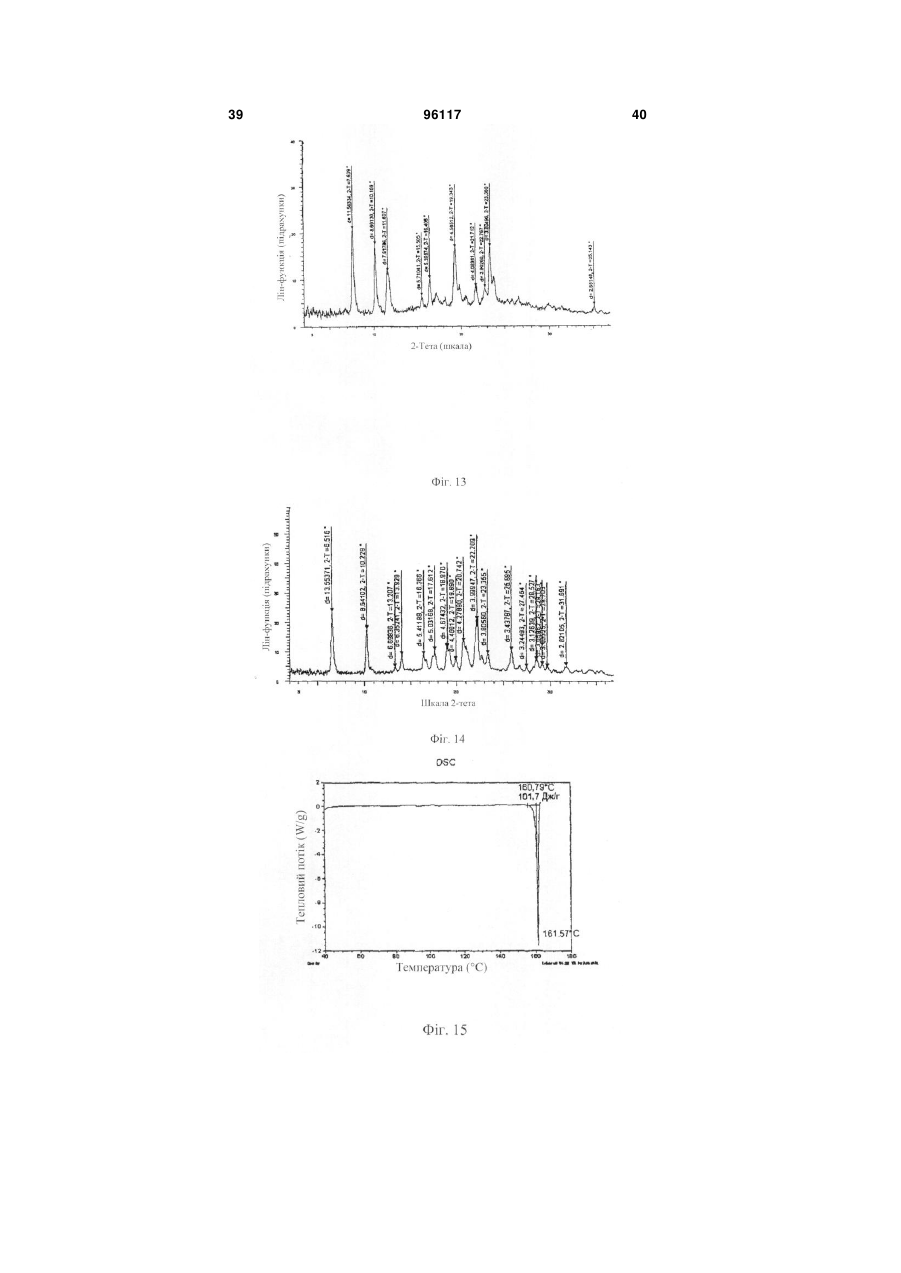
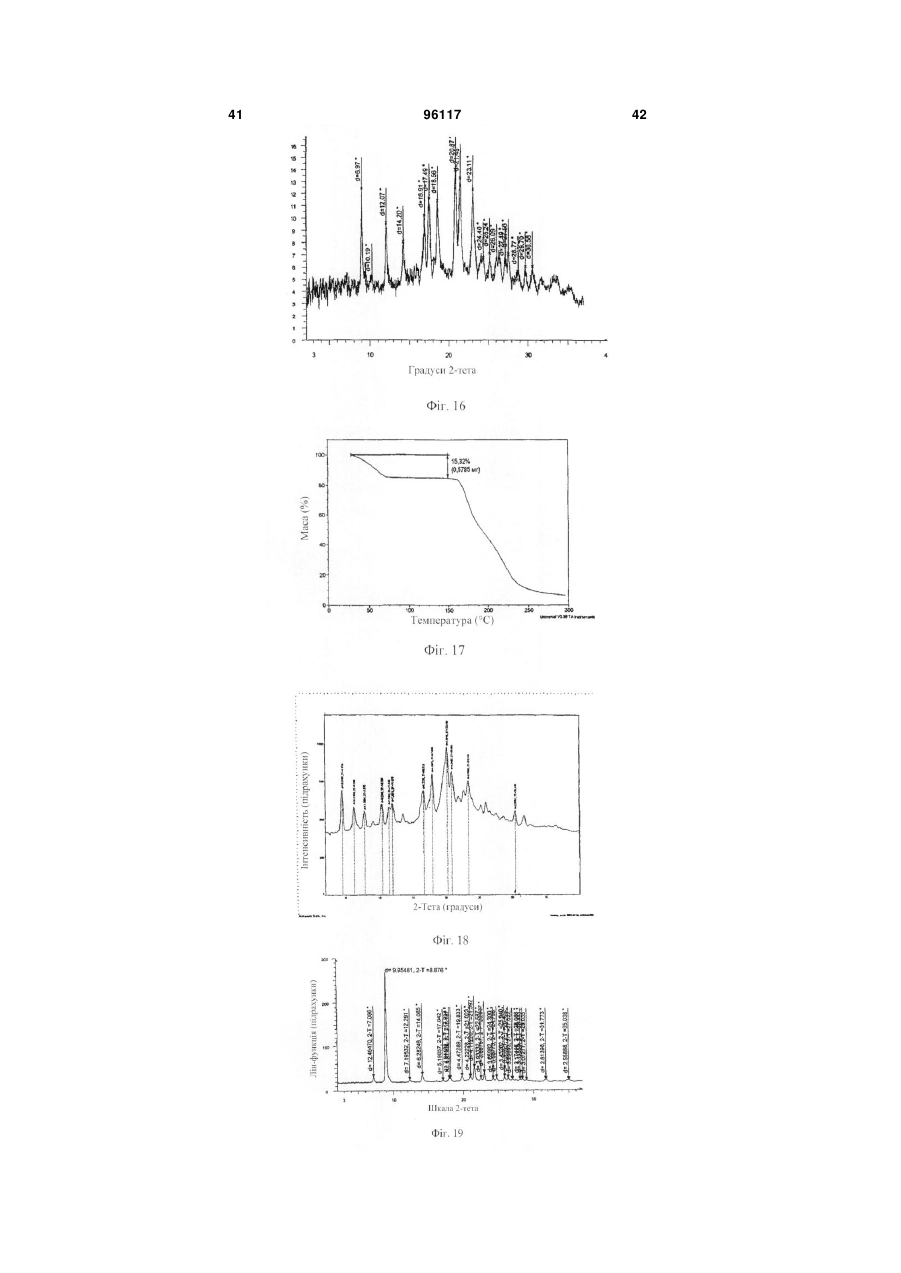
1. Спосіб лікування суб'єкта, що страждає на надмірну сонливість у денний час, пов'язану з нарколепсією, нападами апное уві сні або міопатією, згідно з яким суб'єкту вводять терапевтично ефективну кількість форми V R-(-)-модафінілу, де форма V R-(-)-модафінілу характеризується порошковою рентгенограмою, яка включає піки, що відповідають наступним значенням кутів 2-тета:
(a) 6,61, 10,39 і 16,49 градусів;
(b) 6,61 і 10,39 градусів;
(c) 13,99 і 17,73 градусів;
(d) 20,87 і 22,31 градусів; або
(e) 6,61 градуса.
2. Спосіб за п. 1, де надмірна сонливість у денний час пов'язана з нарколепсією або нападами апное уві сні.
3. Спосіб лікування суб'єкта, що страждає на розлад, який виражається в гіперактивності, що приводить до порушення уваги (ADHD), згідно з яким суб'єкту вводять терапевтично ефективну кількість форми V R-(-)-модафінілу, де форма V R-(-)-модафінілу характеризується порошковою рентгенограмою, яка включає піки, що відповідають наступним значенням кутів 2-тета:
(а) 6,61, 10,39 і 16,49 градусів;
(b) 6,61 і 10,39 градусів;
(c) 13,99 і 17,73 градусів;
(d) 20,87 і 22,31 градусів; або
(e) 6,61 градуса.
4. Фармацевтична композиція, що включає форму V R-(-)-модафінілу, де форма V R-(-)-модафінілу характеризується порошковою рентгенограмою, яка включає піки, що відповідають наступним значенням кутів 2-тета:
(а) 6,61, 10,39 і 16,49 градусів;
(b) 6,61 і 10,39 градусів;
(c) 13,99 і 17,73 градусів;
(d) 20,87 і 22,31 градусів; або
(e) 6,61 градуса.
Текст
1. Спосіб лікування суб'єкта, що страждає на надмірну сонливість у денний час, пов'язану з нарколепсією, нападами апное уві сні або міопатією, згідно з яким суб'єкту вводять терапевтично ефективну кількість форми V R-(-)-модафінілу, де форма V R-(-)-модафінілу характеризується порошковою рентгенограмою, яка включає піки, що відповідають наступним значенням кутів 2-тета: (a) 6,61, 10,39 і 16,49 градусів; (b) 6,61 і 10,39 градусів; (c) 13,99 і 17,73 градусів; (d) 20,87 і 22,31 градусів; або (e) 6,61 градуса. 2. Спосіб за п. 1, де надмірна сонливість у денний час пов'язана з нарколепсією або нападами апное уві сні. 3. Спосіб лікування суб'єкта, що страждає на розлад, який виражається в гіперактивності, що приводить до порушення уваги (ADHD), згідно з яким суб'єкту вводять терапевтично ефективну кількість форми V R-(-)-модафінілу, де форма V R-(-)модафінілу характеризується порошковою рентгенограмою, яка включає піки, що відповідають наступним значенням кутів 2-тета: (а) 6,61, 10,39 і 16,49 градусів; (b) 6,61 і 10,39 градусів; (c) 13,99 і 17,73 градусів; (d) 20,87 і 22,31 градусів; або (e) 6,61 градуса. 4. Фармацевтична композиція, що включає форму V R-(-)-модафінілу, де форма V R-(-)-модафінілу характеризується порошковою рентгенограмою, яка включає піки, що відповідають наступним значенням кутів 2-тета: (а) 6,61, 10,39 і 16,49 градусів; (b) 6,61 і 10,39 градусів; (c) 13,99 і 17,73 градусів; (d) 20,87 і 22,31 градусів; або (e) 6,61 градуса. UA (21) a200609589 (22) 01.02.2005 (24) 10.10.2011 (86) PCT/US2005/002782, 01.02.2005 (31) 60/542,752 (32) 06.02.2004 (33) US (31) 60/560,411 (32) 06.04.2004 (33) US (31) 60/573,412 (32) 21.05.2004 (33) US (31) 60/579,176 (32) 12.06.2004 (33) US (31) 60/581,992 (32) 22.06.2004 (33) US (31) 60/586,752 (32) 09.07.2004 (33) US (31) 60/588,236 (32) 15.07.2004 (33) US (31) 60/631,786 (32) 30.11.2004 (33) US (31) PCT/US04/29013 (32) 04.09.2004 (33) US (46) 10.10.2011, Бюл.№ 19, 2011 р. (72) БУРГХОЛ ХІКІ МАГАЛІ, US, ПЕТЕРСОН МЕТТЬЮ, US, АЛМАРССОН ОРН, US, ОЛІВЕЙРА МАРК, US (73) СЕФАЛОН, ІНК., US (56) FR 2 849 029 A1 WO 02/10125 A1 US 4 927 855 A OSORIO-LOZADA et al., Tetrahedron: Asymmetry, 2004, Vol. 15, No. 23, pages 3811-3815 especially third complete paragraph, second column, page 3813 2 (19) 1 3 Даний винахід стосується композицій, що містять модафініл, фармацевтичних композицій, які включають у себе модафініл, і способів їх одержання. Активні фармацевтичні інгредієнти (АРІ або APIs (безліч)) у фармацевтичних композиціях можуть бути одержані у вигляді цілого ряду різних форм. Такі APIs можна одержати так, щоб мати цілий ряд різних хімічних форм, що включають у себе хімічні похідні, сольвати, гідрати, співкристали або солі. Такі APIs можна також одержати, щоб мати різні фізичні форми. Наприклад, APIs можуть бути аморфними, можуть мати різні кристалічні поліморфи або можуть існувати в різних станах сольватації або гідратації. Змінюючи форми АРІ. можна змінювати його фізичні властивості. Наприклад, кристалічні поліморфи звичайно мають розчинності, які відрізняються одна від одної, так що більш термодинамічно стабільний поліморф с менш розчинним, ніж менш термодинамічно стабільний поліморф. Фармацевтичні поліморфи можуть також розрізнятися за властивостями, такими як термін придатності, біологічна доступність, морфологія, тиск нари, густина, колір і стисливість. Відповідно до цього, зміна кристалічного стану АРІ с одним з багатьох шляхів для модулювання його фізичних властивостей. Було б вигідно мати у своєму розпорядженні нові форми цих APIs, які мають поліпшені властивості, зокрема у вигляді пероральних препаратів. Особливо бажано ідентифікувати поліпшені форми APIs, які проявляють значно поліпшені властивості, у тому числі підвищену розчинність у воді і стабільність. Крім того, бажано поліпшити оброблюваність або одержання фармацевтичних препаратів. Наприклад, голкоподібні кристалічні форми або габітуси APIs можуть викликати агрегацію, навіть у композиціях, в яких АРІ змішаний з іншими речовинами, так що одержують неоднорідну суміш. Голкоподібні морфології можуть також створювати проблеми при фільтруванні (див., наприклад, Mirmehrabi el al. J. Pharm. Sci. Vol.93, № 7, pp. 1692-1700, 2004). Бажано також підвищити швидкість розчинення фармацевтичних композицій, що містять АРІ, у воді, підвищити біологічну доступність композицій, що вводяться перорально, і забезпечити більш швидкий початок терапевтичної дії. Бажано також мати форму АРІ, яка при введенні суб'єкту швидше досягає пікового рівня в плазмі, має терапевтичну концентрацію, що триваліше зберігається у плазмі, і сильнішу загальну дію порівняно з еквівалентними кількостями АРІ у його відомій у цей час формі. Модафініл, АРІ, що застосовується для лікування суб'єктів із нарколепсією, є практично нерозчинним у воді. Модафініл (номер реєстрації CAS: 68693-11-8) представлений структурою (І): 96117 4 Модафініл є хіральною молекулою внаслідок хіральної групи S=O. Тому модафініл існує у вигляді двох ізомерів, R-(-)-модафінілу і S-(-)модафінілу. Було б вигідно мати нові форми модафінілу, які мають поліпшені властивості, особливо, у вигляді пероральних препаратів. Особливо бажано ідентифікувати поліпшені форми модафінілу, які проявляють значно підвищену розчинність у воді і, як хімічну стабільність, так і стабільність форми. Бажано також підвищити швидкість розчинення у воді фармацевтичних композицій, що містять АРІ. підвищити біологічну доступність композицій, що вводяться перорально, і забезпечити більш швидкий початок терапевтичної дії. Бажано також мати форму АРІ, яка при введенні суб’єкту швидше досягає пікового рівня в плазмі і/або має терапевтичну концентрацію, що триваліше зберігається у плазмі, і сильнішу загальну дію порівняно з еквівалентними кількостями АРІ у його відомій у цей час формі. Тепер виявлено, що можна одержати поліморфи і сольвати модафінілу. Деякі з них можуть мати властивості, які відрізняються від властивостей вільної форми АРІ. Варіанти здійснення даного винаходу, що включають у себе, але не обмежуються перерахованим, поліморфи і сольвати, можуть включати в себе рацемічний модафініл, енантіомерно чистий модафініл (тобто R-(-)-модафініл або S-(+)модафініл) або збагачений модафініл (наприклад, такий, що містить між приблизно 55 і приблизно 90 відсотками її). Аналогічно до цього, у різних варіантах здійснення даного винаходу молекули розчинника (наприклад, у сольваті) можуть також існувати у вигляді рацемічної, енантіомерно чистої або збагаченої форми. В іншому варіанті здійснення даного винаходу пропонуються наступні сольвати модафінілу: із хлороформом, із хлорбензолом, з етилацетатом і оцтовою кислотою. Згідно з даним винаходом, способи можуть включати в себе, кожний, додаткову стадію або стадії, в яких поліморф або сольват модафінілу, одержаний таким чином, включають до фармацевтичної композиції. У наступному варіанті здійснення даного винаходу пропонується новий поліморф R-(-)модафінілу. У конкретному варіанті здійснення даного винаходу пропонуються форми III, IV і V R(-)-модафінілу. Даний винахід стосується також способу одержання поліморфа R-(-)-модафінілу. У наступному варіанті здійснення даного винаходу пропонується спосіб одержання поліморфа R-(-)-модафінілу, що включає в себе: (a) забезпечення R-(-)-модафінілу; 5 96117 6 (b) кристалізацію поліморфа R-(-)-модафінілу з кості форми III R-(-)-модафінілу. форми IV R-(-)придатного розчинника. модафінілу або форм V R-(-)-модафінілу. У наступному варіанті здійснення поліморф RФіг. 1 - дифрактограма PXRD поліморфа 2:1 R(-)-модафінілу кристалізують з органічного розчин(-)-модафініл:S-(+)-модафініл. ника. У конкретних варіантах здійснення органічФіг. 2 - термограма ДСК поліморфа 2:1 R-(-)ним розчинником може бути ацетонітрил. диметимодафініл:S-(+)-модафініл. лформамід (ДМФА). метанол, метилетилкетон. NФіг. 3 - дифрактограма PXRD поліморфа R-(-)метилпіролідон, етанол, ізопропанол, ізобутанол, модафінілу (форма III). формамід, ізобутилацетат, 1,4-діоксан, тетрагідФіг. 4 - термограма ДСК поліморфа R-(-)рофуран (ТГФ), етилацетат, о-ксилол, ізопропіламодафінілу (форма III). цетат, дихлорметан, пропіленгліколь, оцтова кисФіг. 5 - дифрактограма PXRD поліморфа R-(-)лота, вода, ацетон, нітрометан, толуол і модафінілу (форма III). бензиловий спирт. Згідно з винаходом, як органічФіг. 6 - дифрактограма PXRD поліморфа R-(-)ний розчинник розглядаються як індивідуальні модафінілу (форма IV). розчинники, так і змішані розчинники. У конкретФіг. 7 - термограма ДСК поліморфа R-(-)ному варіанті здійснення органічним розчинником модафінілу (форма IV). є етанол. В іншому варіанті здійснення для крисФіг. 8 - дифрактограма PXRD поліморфа R-(-)талізації поліморфа R-(-)-модафінілу застосовують модафінілу (форма IV). змішану систему розчинників. Змішаними систеФіг. 9 - дифрактограма PXRD поліморфа R-(-)мами розчинників можуть бути, наприклад, етанол модафінілу (форма V). та ізопропіловий спирт або етилацетат і етанол. У Фіг. 10 - дифрактограма PXRD поліморфа R-(наступному варіанті здійснення кристалізацію в )-модафінілу (форма V). стадії (b) завершують за допомогою термічної криФіг. 11 - дифрактограма PXRD 2:1 R-(-)сталізації. У наступному варіанті здійснення крисмодафініл:S-(+)-модафініл. талізацію в стадії (b) завершують за допомогою Фіг. 12 - термограма ДСК 2:1 R-(-)випарювання розчинника. модафініл:S-(+)-модафініл. В іншому варіанті здійснення фармацевтична Фіг. 13 - дифрактограма PXRD форми IV R-(-)композиція має модифікований профіль вивільмодафінілу. нення однієї або декількох форм модафінілу: раФіг. 14 - дифрактограма PXRD форми VR-(-)цемічного модафінілу, R-(-)-модафінілу і S-(+)модафінілу. модафінілу. Модифікований профіль вивільнення Фіг. 15 - термограма ДСК форми VR-(-)може включати в себе, наприклад, два або більше мoдaфiнiлy. максимумів концентрації в плазмі, наприклад, Фіг. 16 - дифрактограма PXRD сольвату R-(-)профіль подвійного вивільнення. модафінілу з хлороформом. Винахід далі пропонує лікарський засіб, що Фіг. 17 - термограма ΤΓA сольвату R-(-)включає в себе поліморф або сольват модафінілу, модафінілу з хлороформом. і способи його одержання. Звичайно лікарський Фіг. 18 - дифрактограма PXRD сольвату R-(-)засіб додатково включає в себе один або декілька модафінілу з хлорбензолом. фармацевтично прийнятних носіїв, розріджувачів Фіг. 19 - дифрактограма PXRD канального соабо ексципієнтів. Лікарські засоби згідно з винахольвату рацемічного модафінілу з етилацетатом. дом описані більш детально нижче. Фіг. 20 - термограма ΤΓA канального сольвату Способи згідно з даним винаходом можуть, рацемічного модафінілу з етилацетатом. кожний, включати в себе стадію або стадії, в яких Фіг. 21 - дифрактограма PXRD сольвату R-(-)поліморф або сольват модафінілу, одержаний модафінілу з оцтовою кислотою. відповідним чином, включають до лікарського заФіг. 22 - термограма ΤΓA сольвату R-(-)собу. модафінілу з оцтовою кислотою. Ще в одному аспекті винаходу запропоноваФіг. 23 - термограма ДСК сольвату R-(-)ний спосіб лікування суб’єкта, переважно, суб’єктамoдaфiнiлy з оцтовою кислотою. людини, страждаючої на надмірну сонливість у Структура модафінілу включає в себе стереоденний час, пов'язану з нарколепсісю, стомлення, центр і тому він може існувати у вигляді рацемату, пов'язане із розсіяним склерозом, безплідність, одного з двох чистих ізомерів або пари двох ізопорушення апетиту, розлад, що виражається в мерів у будь-якому співвідношенні. Хімічною нагіперактивності, яка призводить до порушення увазвою рацемічного модафінілу є (±)-2ги (ADHD), хворобу Паркінсона, нетримання, на[(дифенілметил)сульфініл]ацетамід. Ізомерними пади апное уві сні або міопатією, де модафініл є парами рацемічного модафінілу є R-(-)-2ефективним фармацевтичним засобом для зазна[(дифенілметил)сульфініл]ацетамід або R-(-)ченого порушення. Спосіб включає в себе введенмoдaфiнiл і S-(+)-2ня суб'єкту терапевтично ефективної кількості по[(дифенілметил)сульфініл]ацетамід або S-(+)ліморфа або сольвату модафінілу. модафініл. В іншому варіанті здійснення запропонований Застосовуваний тут термін, якщо не домовлеспосіб лікування суб'єкта, страждаючого на однин но особливо, "енантіомерно чистий" включає в або декілька зазначених вище станів або порусебе композицію, яка є по суті енантіомерно чисшень, що включають у себе, але що не обмежутою і включає в себе, наприклад, композицію з ються зазначеним, порушення сну, такі як наркоенантіомерним надлишком, який дорівнює або лепсія, де зазначений спосіб включає в себе більший ніж приблизно 90, 91, 92, 93, 94, 95, 96, введення суб'єкту терапевтично ефективної кіль97, 98 або 99 відсотків. Енантіомерний надлишок 7 96117 8 визначають відсотком енантіомеру А - відсоток або S-модафініл і молекулу розчинника. В іншому енантіомера В або формулою: варіанті здійснення сольват даного винаходу відсоток її = 100*([R]-[S]/([R]+[S]), де R являє включає в себе модафініл і/або молекулу розчинсобою число молів R-(-)-модафінілу і S являє соника з епантіомерним надлишком приблизно 1 бою число молів S-(+)-модафінілу. відсоток, 2 відсотки, 3 відсотки, 4 відсотки, 5 відсоЗастосовуваний тут термін "модафініл" вклютків, 10 відсотків, 15 відсотків, 20 відсотків, 25 відчає в себе рацемат, інші суміші R- і S-ізомерів та сотків, 30 відсотків, 35 відсотків, 40 відсотків, 45 індивідуальні енантіомери, але може бути конкревідсотків, 50 відсотків, 55 відсотків, 60 відсотків, 65 тно визначений як рацемат, R-ізомер, S-ізомер або відсотків, 70 відсотків, 75 відсотків, 80 відсотків, 85 будь-яка суміш як R-, так і S-ізомерів. відсотків, 90 відсотків, 95 відсотків, 96 відсотків, 97 Застосовуваний тут термін, якщо не домовлевідсотків, 98 відсотків, 99 відсотків, більше, ніж 99 но особливо, "рацемічний" стосується речовини відсотків, або будь-якої проміжної величини. В (наприклад, поліморфа або сольвату), яка складаіншому варіанті здійснення поліморф або сольват ється з еквімолярної суміші енантіомерів модафіданого винаходу може включати в себе модафініл нілу, розчинника або обох. Наприклад, сольват, з енантіомерним надлишком приблизно 1 відсоток, що включає в себе модафініл і нестереоізомерну 2 відсотки, 3 відсотки, 4 відсотки, 5 відсотків, 10 молекулу розчинника є рацемічним сольватом, відсотків, 15 відсотків, 20 відсотків, 25 відсотків, 30 тільки коли тут присутня еквімолярна суміш енанвідсотків, 35 відсотків, 40 відсотків, 45 відсотків, 50 тіомерів модафінілу. Аналогічно цьому, сольват, відсотків, 55 відсотків, 60 відсотків, 65 відсотків, 70 що включає в себе модафініл і молекулу стереоівідсотків, 75 відсотків, 80 відсотків, 85 відсотків, 90 зомерного розчинника, є рацемічним сольватом, відсотків, 95 відсотків, 96 відсотків, 97 відсотків, 98 тільки коли тут присутня еквімолярна суміш енанвідсотків, 99 відсотків, більше, ніж 99 відсотків або тіомерів модафінілу та енантіомерів молекули будь-якої проміжної величини. розчинника. "Збагачений" модафініл згідно з даним винаЗастосовуваний тут термін, якщо не домовлеходом включає в себе як R-(-)-, так і S-(+)- ізомери но особливо, "енантіомерно чистий" стосується модафінілу в кількостях, які дорівнюють або більші речовини, яка складається з модафінілу і неоніж приблизно 5, 6, 7, 8, 9 або 10 мас. %, або які бов’язково молекули стереоізомерного або нестедорівнюють або менші ніж 90, 91, 92, 93, 94 або 95 реоізомерного розчинника, де енантіомерний надмас. %. Наприклад, композиція, яка включає в селишок стереоізомерної сполуки більший або бе 67 мас. % R-(-)-модафінілу і 33 мас. % S-(+)дорівнює приблизно 90 відсоткам її (енантіомермодафінілу, є збагаченою композицією модафініний надлишок). лу. У такому прикладі композиція не є ні рацемічДля цілей даного винаходу хімічні та фізичні ною, ні енантіомерно чистою. Термін "збагачений властивості модафінілу у формі сольвату або поR-(-)-модафініл" можна застосовувати для опису ліморфа можна порівняти з еталонною сполукою, композиції модафінілу з більше ніж 50 відсотками якою є модафініл в іншій формі. Еталонна сполука R-(-)-модафінілу, і менше ніж 50 відсотками S-(+)може бути визначена як вільна форма або, більш модафінілу. Подібним же чином, термін "збагачевизначено, ангідрат (безводна сполука) або гідрат ний S-(+)-модафініл" можна застосовувати для вільної форми, або, більш конкретно, наприклад, опису композиції модафінілу з більше ніж 50 відсонапівгідрат, моногідрат, дигідрат, три гідрат, тетратками S-(+)-модафінілу і менше ніж 50 відсотками гідрат, пентагідрат; або сольват вільної форми. R-(-)-модафінілу. Еталонна сполука може бути також визначена як Терміни "R-(-)-модафініл" і "S-(+)-модафініл" кристалічна або аморфна. Еталонна сполука може можна застосовувати для опису збагаченого мобути також визначена як найбільш стабільний відафінілу, енантіомерно чистого модафінілу або по домий поліморф певної форми еталонної сполуки. суті енантіомерно чистого модафінілу, але можуть Модафініл і молекули деяких розчинників датакож зокрема включати в себе збагачений моданого винаходу мають один або декілька хіральних фініл, енантіомерно чистий модафініл і/або по суті центрів і можуть існувати в різних стереоізомерних енантіомерно чистий модафініл. конфігураціях. Як результат цих хіральних центрів Сольвати і поліморфи, що включають у себе модафініл і декілька сольватів даного винаходу енантіомерно чисті і/або енантіомерно збагачені існують у вигляді рацематів. сумішей енантіомерів компоненти (наприклад, модафініл або молекулу і у вигляді індивідуальних енантіомерів, а також розчинника), можуть обумовлювати хімічні і/або діастереомерів і сумішей діастереомерів. Всі такі фізичні властивості, які модульовані відносно тарацемати, енантіомери і діастереомери знахоких властивостей відповідної форми, що включає в дяться в межах обсягу даного винаходу, у тому себе рацемічний компонент. числі, наприклад, цис- і транс-ізомери, R- і SПоліморфи і сольвати модафінілу можна одеенантіомери і (D)- і (L)-ізомери. Сольвати даного ржати з рацемічним модафінілом, енантіомерно винаходу можуть включати в себе ізомерні форми чистим модафінілом або з будь-якою сумішшю R-(або модафінілу, або молекул розчинника або того )- і S-(+)-модафінілів (наприклад, збагаченим мой іншого. Ізомерні форми модафінілу і молекул дафінілом) згідно з даним винаходом. розчинника включають у себе, але не обмежуютьВ іншому варіанті здійснення композиції або ся зазначеним, стереоізомери, такі як енантіомери лікарські засоби, що включають у себе сольвати і і діастереомери. В одному варіанті здійснення сополіморфи даного винаходу, можна порівняти з льват включає в себе рацемічний модафініл і мовільною формою модафінілу, як PROVIGIL® лекулу розчинника. В іншому варіанті здійснення (Cephalon. Inc.). (Див. патент США, що заміняє. № сольват включає в себе енантіомерно чистий RRE37516). 9 96117 10 В іншому варіанті здійснення даного винаходу ської форми зі швидкістю, яка буде відшкодовувапропонуються наступні сольвати модафінілу: із ти кількість лікарського засобу, який метаболізухлороформом, хлорбензолом, етилацетатом і оцється та екскретується з організму. Регульоване товою кислотою. вивільнення активного інгредієнта можна стимуФармацевтично прийнятні форми можна вволювати різними умовами, що включають у себе, дити способами з регульованим або уповільненим але не обмежуються перерахованим, рН, іонну вивільненням. Фармацевтичні продукти з регульосилу, осмотичний тиск, температуру, ферменти, ваним вивільненням мають загальну мету поліпводу та інші фізіологічні умови або сполуки. шення лікарської терапії порівняно з терапією, що Для застосування із сольватами, поліморфами досягається їх аналогами без регульованого вивіі композиціями винаходу можна адаптувати різні льнення. В ідеальному випадку застосування опвідомі лікарські форми, препарати і пристрої з ретимально розробленого препарату з регульованим гульованим або уповільненим вивільненням. Прививільненням при консервативному лікуванні хаклади їх включають у себе, але не обмежуються рактеризується мінімальною кількістю лікарської перерахованим, приклади, описані в патентах речовини, що застосовується для лікування або США №№ 3845770; 3916899; 3536809; 3598123; усунення стану за мінімально короткий термін ча4008719; 5674533; 5059595; 5591767; 5120548; су. Переваги препаратів із регульованим вивіль5073543; 5639476; 5354556; 5733566 і 6365185 В1; ненням включають у себе: 1) розширену активкожний з яких включений тут як посилання. Ці ліність лікарського засобу; 2) знижену частоту карські форми можна застосовувати для забезпевведення дози; 3) підвищену сприйнятливість пачення повільного або регульованого вивільнення цієнта; 4) вживання меншої загальної кількості одного або декількох активних інгредієнтів із залікарського засобу; 5) зниження локальних або стосуванням, наприклад, гідроксипропілметилцесистемних побічних дій; 6) мінімізацію накопичення люлози. інших полімерних матриць, гелей, пронилікарського засобу; 7) зниження коливань рівня кних мембран, осмотичних систем (таких як вмісту в крові, 8) підвищення ефективності лікуOROS® (Alza Corporation, Mountain View, Calif. вання; 9) зниження потенціювання або втрати акUSA)), багатошарових покриттів, мікрочастинок, тивності лікарського засобу і 10) підвищення швиліпосом або мікросфер або їх комбінації для задкості пригнічення захворювань або станів. (Kim, безпечення необхідного профілю вивільнення у Cherng-ju, Controlled Release Dosage Form Design, варійованих пропорціях. Крім того, для одержання 2 Technomic Publishing, Lancaster, Pa.: 2000). іммобілізованих, абсорбованих поліморфів. і, таЗагальноприйняті лікарські форми звичайно ким чином, здійснення регульованої доставки лізабезпечують швидке або негайне вивільнення карського засобу можна застосовувати іонообмінні лікарського засобу з препарату. Залежно від фарматеріали. Приклади конкретних апіонообмінників макології і фармакокінетичних характеристик лівключають у себе, але не обмежуються перерахокарського засобу застосування загальноприйнятих ваним. Дуоліт® А568 і Дуоліт® АР 143 (Rohm & лікарських форм може призвести до широких коHaas, Spring House, PA. USA). ливань у концентраціях лікарського засобу в крові Один варіант здійснення винаходу включає в та інших тканинах пацієнта. Ці коливання можуть себе стандартну лікарську форму, яка включає в впливати на ряд параметрів, таких як частота ввесебе фармацевтично прийнятний сольват, гідрат, дення дози, початок дії, тривалість ефективності дегідрат, безводну або аморфну форму та один дії, підтримка терапевтичних рівнів у крові, токсичабо декілька фармацевтично прийнятних ексципіність, побічні дії і тощо. Препарати з регульованим єнтів або розріджувачів, де фармацевтичну комповивільненням переважно можна застосовувати зицію, лікарський засіб або лікарську форму вигодля регулювання початку дії, тривалості дії, рівнів товляють для регульованого вивільнення. У у плазмі в межах терапевтичного вікна і пікових специфічних лікарських формах застосовують осрівнів у крові лікарського засобу. Зокрема, лікарсьмотичну систему доставки лікарського засобу. кі форми або препарати з регульованим або упоКонкретна і добре відома осмотична система вільненим вивільненням можна застосовувати для доставки лікарського засобу називається OROS® гарантії того, що максимальна ефективність лікар(Alza Corporation, Mountain View, Calif. USA). Ця ського засобу досягається при мінімізації потентехнологія може бути легко адаптована для досційних негативних дій і турбування за безпеку, які тавки сполук і композицій винаходу. Різні аспекти можуть мати місце як через недостатню дозу літехнології описані в патентах США №№ 6375978 карського засобу (тобто такого, що діє при рівні, В1; 6368626 В1; 6342249 В1; 6333050 В2; 6287295 який є нижчим від мінімальних терапевтичних рівВ1; 6283953 В1; 6270787 В1; 6245357 В1 і нів), так і перевищення рівня токсичності для лі6132420, кожний з яких включений тут як посиланкарського засобу. ня. Конкретні адаптації OROS®. які можна застоБільшість препаратів із регульованим вивільсовувати для введення сполук і композицій винаненням розроблені для початкового вивільнення ходу, включають у себе, але не обмежуються кількості лікарського засобу (активного інгредієнперерахованим, системи OROS® Push-Pull™, та), який швидко викликає необхідну терапевтичну Delayed Push-Pull™, Multi-Layer Push-Pull™ і Pushдію, та поступового і безперервного вивільнення Stick™, всі з яких добре відомі. Див., наприклад, інших кількостей лікарського засобу для підтримки http://www.alza.com. Додаткові системи OROS®, які цього рівня терапевтичної або профілактичної дії можна застосовувати для регульованої пероральпротягом тривалого періоду часу. Для підтримки ної доставки сполук і композицій винаходу, вклюцього постійного рівня лікарського засобу в органічають у себе OROS®-CT і L-OROS®. Там же; див. змі лікарський засіб повинен вивільнятися з лікар 11 96117 12 також Delivery Times, vol.11, issue II (Alza В іншому варіанті здійснення фармацевтична Corporation). композиція або лікарський засіб включає в себе Загальноприйняті пероральні лікарські форми суміш нової форми модафінілу даного винаходу OROS® одержують пресуванням порошку лікарсь(наприклад, поліморфа або сольвату) і рацемічнокого засобу в тверду таблетку, покриттям таблетки го модафінілу. Цей варіант здійснення можна запохідними целюлози з утворенням напівпроникної стосовувати, наприклад, як лікарську форму з ремембрани і потім свердлінням отворів у покритті гульованим, безперервним або уповільненим (наприклад, лазером). Kim, Cherng-ju, Controlled вивільненням. В іншому варіанті здійснення лікарRelease Dosage Form Design, 231-238 (Technomic ська форма з уповільненим вивільненням включає Publishing, Lancaster, Pa.: 2000). Перевагою таких в себе рацемічний модафініл і поліморф або сольлікарських форм є те, що на швидкість доставки ват даного винаходу. лікарського засобу не впливають фізіологічні або В іншому варіанті здійснення фармацевтична експериментальні умови. Навіть лікарський засіб із композиція або лікарський засіб має модифіковарН-залежною розчинністю можна доставляти при ний профіль вивільнення одного або декількох постійній швидкості, незалежно від рН середовища компонентів із рацемічного модафінілу, R-(-)доставки. Але через те, що ці переваги забезпемодафінілу і S-(+)-модафінілу. Модифікований чуються створенням осмотичного тиску всередині профіль вивільнення може включати в себе, налікарської форми після введення загальноприйняприклад, два або більше максимумів концентрації тих систем доставки лікарського засобу. OROS® в плазмі, такий як профіль із подвійним вивільненне можна застосовувати для ефективної доставки ням. Такий профіль із модифікованим вивільненлікарських засобів із низькою розчинністю у воді. ням може допомогти, наприклад, пацієнту, який Там же: с.234. страждає на втрату неспання пополудні, який підКонкретна дозована лікарська форма згідно з дається лікуванню композицією або лікарським винаходом включає в себе: порожнину, що визназасобом. Другий "сплеск" або вивільнення АРІ, чається стінкою, стінку, яка мас вихідний отвір, принаймні, через 2, 3, 4, 5 або 6 годин після ввеутворений або що утворюється в ній, причому, дення може допомогти подолати такий ефект. В принаймні, частина стінки є напівпроникною; розіншому варіанті здійснення можна застосовувати ширюваний шар. розташований всередині порожфармацевтичну композицію або лікарський засіб, нини, віддалений від вихідного отвору, і зв’язаний що включає в себе невелику дозу, що завантажуіз напівпроникною частиною стінки за допомогою ється, яка вивільняється відразу після введення, із рідини; шар лікарського засобу в сухому або по подальшим вивільненням АРІ за профілем прибсуті сухому стані, вміщений у цій порожнині поруч лизно нульового порядку протягом наступних 2, 3, із вихідним отвором і в прямому або непрямому 4, 5 або 6 годин. У такій композиції пікові рівні в контакті з розширюваним шаром, і активуючий плазмі можуть бути досягнуті приблизно опівдні. потік шар, розташований між внутрішньою поверхВ іншому варіанті здійснення фармацевтична нею стінки і, принаймні, зовнішньою поверхнею композиція або лікарський засіб, що мас модифішару лікарського засобу, розташованого в порожкований профіль вивільнення модафінілу, може нині, де шар лікарського засобу включає в себе включати в себе R-(-)-модафініл і S-(+)-модафініл. поліморф або його сольват, гідрат, дегідрат, безде R-(-)-модафініл забезпечує початкове підвиводну або аморфну форму. Див. патент США № щення (початкова Сmaх, зумовлена R-(-)6368626, який включений тут у всій його повноті як модафінілом) концентрації в плазмі і S-(+)посилання. модафініл забезпечує затримане підвищення (поІнша конкретна дозована лікарська форма видальша Сmax, зумовлена S-(+)-модафінілом) коннаходу включає в себе: порожнину, що визначацентрації в плазмі. Уповільнене підвищення до ється стінкою, стінку, що має вихідний отвір, утвоСmax, зумовлене S-(+)-модафінілом. може бути рений або що утворюється в ній, причому, через 2, 3, 4, 5, 6 або більше годин після початкопринаймні, частина стінки є напівпроникною; розвого підвищення до Сmax, зумовленого R-(-)ширюваний шар. розташований всередині порожмодафінілом. В іншому варіанті здійснення затринини, віддалений від вихідного отвору, і зв'язаний мана Сmax є приблизно такою, що дорівнює початз напівпроникною частиною стінки за допомогою ковому Сmax. В іншому варіанті здійснення затрирідини; шар лікарського засобу, вміщений у цій мана Сmax більша, ніж початкова Сmax. В іншому порожнині поруч із вихідним отвором і в прямому варіанті здійснення затримана С max менша, ніж або непрямому контакті з розширюваним шаром: початкова Сmax. В іншому варіанті здійснення зашар лікарського засобу, що включає в себе склад тримана Сmax зумовлена рацемічним модафінілом рідкого активного агента, абсорбованого в порисзамість S-(+)-модафінілу. В іншому варіанті здійстих частинках, причому пористі частинки адаптонення затримана Сmax зумовлена R-(-)вані для опору силам здавлювання з утворенням модафінілом замість S-(+)-модафінілу. В іншому ущільненого шару лікарського засобу без значного варіанті здійснення початкова Сmax зумовлена равиділення складу рідкого активного агента, причоцемічним модафінілом замість R-(-)-модафінілу. В му лікарська форма необов’язково мас шар плаіншому варіанті здійснення початкова Сmax зумовцебо між вихідним отвором і шаром лікарською лена S-(+)-модафінілом замість R-(-)-модафінілу. засобу, де шар лікарського засобу включає в себе В іншому варіанті здійснення модифікований прополіморф або його сольват, гідрат, дегідрат, безфіль вивільнення має 3, 4, 5 або більше "сплесків" водну або аморфну форму. Див. патент США № концентрації в плазмі. 6342249, який включений тут у всій його повноті як В іншому варіанті здійснення фармацевтична посилання. композиція або лікарський засіб має модифікова 13 96117 14 ний профіль вивільнення модафінілу, коли один може бути у формі, наприклад, супозиторію. У цей або декілька компонентів із рацемічного модафінічас переважними с пероральні лікарські форми, лу, R-(-)-модафінілу або S-(+)-модафінілу присутні які с дискретними стандартними дозами, причому у формі сольвату або поліморфа. кожна містить заздалегідь визначену кількість АРІ, В іншому варіанті здійснення фармацевтична такі як таблетки або капсули. композиція або лікарський засіб має модифіковаНижче зазначаються необмежувальні прикланий профіль вивільнення, коли R-(-)-модафініл ди ексципієнтів, які можна застосовувати для одезастосовують у пероральному препараті. Така ржання фармацевтичних композицій або лікарськомпозиція може мінімізувати метаболізм першого ких засобів винаходу. проходу модафінілу в сульфон. В іншому варіанті Фармацевтичні композиції та лікарські засоби здійснення фармацевтична композиція або лікарвинаходу необов'язково включають у себе один ський засіб має модифікований профіль вивільабо декілька фармацевтично прийнятних носіїв нення, коли рацемічний модафініл застосовують у або розріджувачів як ексципієнтів. Придатні носії пероральному препараті. В іншому варіанті здійсабо розріджувачі ілюстративно включають у себе, нення фармацевтична композиція або лікарський але не обмежуються перерахованим, або окремо, засіб мас модифікований профіль вивільнення, або в комбінації, лактозу, у тому числі безводну коли S-(+)-модафініл застосовують у пероральнолактозу і моногідрат лактози: крохмаль, у тому му препараті. В іншому варіанті здійснення фарчислі крохмаль, що безпосередньо пресується, і мацевтична композиція або лікарський засіб мас гідролізовані крохмалі (наприклад, Celutab™ і модифікований профіль вивільнення, коли рацеміEmdex™): маніт; сорбіт: ксиліт; декстрозу (напричний модафініл і R-(-)-модафініл застосовують у клад, Cerelose™ 2000) і моногідрат декстрози; дипероральному препараті. В іншому варіанті здійсгідрат гідрофосфату кальцію; розріджувачі на оснення фармацевтична композиція або лікарський нові сахарози: кондитерський цукор; моногідрат засіб мас модифікований профіль вивільнення, сульфату кальцію; дигідрат сульфату кальцію; коли рацемічний модафініл і S-(+)-модафініл загранульований тригідрат лактату кальцію: декстосовують у пероральному препараті. В іншому страти; інозит, тверді речовини гідролізованих варіанті здійснення фармацевтична композиція хлібних злаків; амілозу; целюлози, у тому числі або лікарський засіб мас модифікований профіль мікрокристалічну целюлозу, альфа-целюлозу та вивільнення, коли S-(+)-модафініл і R-(-)аморфну целюлозу з джерел харчової категорії модафініл застосовують у пероральному препара(наприклад, Rexcel J). порошкоподібну целюлозу, ті. В іншому варіанті здійснення фармацевтична гідроксипропілцелюлозу (НРС) і гідроксипропілмекомпозиція або лікарський засіб мас модифіковатилцелюлозу (НРМС); карбонат кальцію: гліцин; ний профіль вивільнення, коли рацемічний модабентоніт; блок-співполімери; полівінілпіролідон і фініл, S-(+)-модафініл і R-(-)-модафініл застосовутощо. Такі носії або розріджувачі, якщо вони приють у пероральному препараті. сутні, складають всього від приблизно 5% до приВ іншому варіанті здійснення фармацевтичну близно 99%, переважно, від приблизно 10% до композицію або лікарський засіб, що мас модифіприблизно 85%, і, більш переважно, від приблизно кований профіль вивільнення модафінілу, вводять 20% до приблизно 80% загальної маси композиції. трансдермально. Така трансдермальна (TD) досВибраний носій, носії, розріджувач або розріджутавка може запобігти метаболізму першого проховачі, переважно, виявляють придатні характерисду. Крім того, можна застосовувати стратегію "пітики сипкості та, коли потрібні таблетки, пресовалюля-пластир", при якій тільки частину добової ність. дози доставляють через шкіру, щоб забезпечити Лактоза, маніт, гідрофосфат натрію і мікрокриосновні системні рівні, до яких додають дози перосталічна целюлоза (особливо, мікрокристалічна ральної терапії, щоб забезпечити ефект неспання. целюлоза авіцел РН, така як авіцел РН 101), або Ексципієнти, що застосовуються у фармацевокремо, або в комбінації, є переважними розріджутичних композиціях і лікарських засобах, можуть вачами. Ці розріджувачі с хімічно сумісними з APIs. бути твердими, напівтвердими, рідкими або їхніми Екстрагранульовану мікрокристалічну целюлозу комбінаціями. Переважно, ексципієнти є твердими. (тобто мікрокристалічну целюлозу, додану до граКомпозиції та лікарські засоби винаходу, що міснульованої композиції) можна застосовувати для тять ексципієпти, можна одержувати відомою мезбільшення твердості (для таблеток) і/або часу тодикою фармації, яка включає в себе змішування дезінтеграції. Лактоза, особливо моногідрат лактоексципієнта з АРІ або терапевтичним агентом. зи, є особливо переважною. Лактоза в типовому Фармацевтична композиція або лікарський засіб випадку забезпечує одержання композицій, що винаходу містить необхідну кількість АРІ на станмають придатні швидкості вивільнення APIs, стадартну дозу і, якщо він призначений для перорабільність, сипкість перед пресуванням і/або власльного введення, може бути у формі, наприклад, тивості сушіння при відносно низькій вартості розтаблетки, маленької капсули, пілюлі, твердої або ріджувача. Вона забезпечує одержання субстрату м'якої капсули, коржика, крохмальної капсули, поз високою щільністю, який допомагає ущільненню рошку, що дозується, гранул, суспензії, еліксиру, під час грануляції (коли застосовують мокру градисперсії, рідини або будь-якої іншої форми, доснуляцію) і, отже, поліпшує властивості сипкості татньо адаптованої для такого введення. Якщо суміші та властивості таблетки. композиція призначена для парентерального ввеФармацевтичні композиції і лікарські засоби дення, вона може бути у формі, наприклад, сувинаходу необов'язково включають у себе один спензії або черезшкірного пластиру. Якщо компоабо декілька фармацевтично прийнятних дезінтегзиція призначена для ректального введення, вона рувальпих засобів як ексципієнтів, особливо для 15 96117 16 препаратів у вигляді таблеток. Придатні дезінтегповідон K-15, K-30 і K-29/32; поліметакрилати; рувальні засоби включають у себе, але не обмеНРМС; гідроксипропілцелюлоза (наприклад, жуються перерахованим, або окремо, або в комбіKlucel™ of Aqualon); і етилцелюлоза (наприклад, нації, крохмаль, у тому числі натрієву сіль Ethocel™ of the Dow Chemical Company). Такі гліколяту крохмалю (наприклад. Explotab™ або зв’язувальні агенти і/або адгезиви, якщо вони приPen West) і попередньо клейстеризований кукурусутні, складають всього від приблизно 0,5% до дзяний крохмаль (наприклад. National™ 1551 of приблизно 25%, переважно, від приблизно 0,75% National Starch and Chemical Company. National™ до приблизно 15%, і більш переважно, від прибли1550, and Colocorn™ 1500). глини (наприклад, зно 1% до приблизно 10% загальної маси фармаVeegum™ HV of R.T. Vanderbilt), целюлози, такі як цевтичної композиції або лікарського засобу. очищена целюлоза, мікрокристалічна целюлоза, Багато зв'язувальних агентів є полімерами, що метилцелюлоза, карбоксиметилцелюлоза і натрієвключають у себе групи аміду, складного ефіру, ва сіль карбоксиметилцелюлози, натрієва сіль простого ефіру, спирту або кетону, і як такі, перекроскармелози (наприклад. Ac-Di-Sol™ of FMC), важно, включаються у фармацевтичні композиції і альгінати, кросповідон і камеді, такі як агар, калікарські засоби даного винаходу. Полівінілпіролімедь ріжкового дерева, камедь бобів ріжкового дони, такі як повідон K-30, є особливо переважнидерева, камедь карай,. пектин і трагакантова ками. Полімерні зв'язувальні агенти можуть мати медь. різні молекулярні маси, ступені зшивання і марки Дезінтегрувальні засоби можна додавати на полімерів. Полімерні зв'язувальні агенти можуть будь-якій придатній стадії до часу одержання комбути також співполімерами, такими як блокпозиції, особливо, перед грануляцією або під час співполімери, які містять суміші ланок етиленоксистадії змащування перед пресуванням. Такі дезінду і пропіленоксиду. Зміна у відносинах цих ланок тегрувальні засоби, якщо вони присутні, складау даному полімері впливає на властивості та харають всього від приблизно 0,2% до приблизно 30%, ктеристики. Прикладами блок-співполімерів зі переважно, від приблизно 0,2% до приблизно 10%, змінними складами ланок блоків є полоксамер 188 і більш переважно, від приблизно 0,2% до приблиі полоксамер 237 (BASF Corporation). зно 5% загальної маси композиції. Фармацевтичні композиції та лікарські засоби Натрієва сіль кроскармелози є переважним винаходу необов'язково включають у себе один дезінтегрувальним засобом для дезінтеграції табабо декілька фармацевтично прийнятних звололетки або капсули і, якщо є присутньою, переважжуючих агентів як ексципієнтів. Такі зволожуючі но складає від приблизно 0,2% до приблизно 10%, агенти, переважно, вибрані для збереження АРІ у більш переважно, від приблизно 0,2% до приблизтісному зв'язку з водою, умова, яка. як вважається, но 7% і, ще більш переважно, від приблизно 0,2% підвищує біологічну доступність композиції. до приблизно 5% загальної маси композиції. НаНеобмежувальні приклади поверхневотрієва сіль кроскармелози надає кращі характериактивних речовин, які можна застосовувати як стики інтрагранулярної дезінтеграції гранульовазволожуючі агенти у фармацевтичних композиціях ним фармацевтичним композиціям і лікарським і лікарських засобах винаходу, включають у себе засобам даного винаходу. четвертинні амонієві сполуки, наприклад, хлорид Фармацевтичні композиції і лікарські засоби бензалконію, хлорид бензетонію і хлорид цетилпівинаходу необов'язково включають у себе один ридинію, натрієву сіль діоктилсульфосукцинату, або декілька фармацевтично прийнятних зв'язуваполіоксістиленалкілфенілові прості ефіри, наприльних агентів або адгезивів як ексципієнтів, особклад, ноноксинол 9, ноноксинол 10 і октоксинол 9, ливо для препаратів у вигляді таблеток. Такі зв'яполоксамери (блок-співполімери поліоксіетилену і зувальні агенти і адгезиви, переважно, надають поліоксипропілену), гліцериди полоксіетиленжирдостатню когезію порошку, який таблетують, щоб них кислот і олії, наприклад, моно- і дигліцериди забезпечити можливість нормальних операцій поліоксіетилен(8)каприлової/капринової кислот обробки, таких як проклейка, змащування, пресу(наприклад, Labrasol™ of Gatterosse), поліоксіетивання та упаковування, але все ж дозволяють лен(35)рицинова олія і поліоксіетитаблетці дезінтегрувати і композиції абсорбуватилен(40)гідрогенізована рицинова олія; поліоксіетися після прийому всередину. леналкілові прості ефіри, наприклад, Такі зв’язувальні агенти можуть також запобіполіоксіетилен(20)цетостеариловий простий ефір, гати або інгібувати кристалізацію або перекристаефіри поліоксіетиленжирних кислот, наприклад, лізацію АΡΙ даного винаходу після того, як сіль поліоксіетилен(40)стеарат, складні ефіри поліоксірозчиниться в розчині. Придатні зв'язувальні агенетиленсорбітану, наприклад, полісорбат 20 і політи і адгезиви включають у себе, але не обмежусорбат 80 (наприклад. Tween™ 80 ІСІ), ефіри проються перерахованим, або окремо, або в комбінапіленгліколю і жирних кислот, наприклад, лаурат ції, камедь акації: трагакантову камедь; сахарозу; пропіленгліколю (наприклад, Lauroglycol™ of желатин; глюкозу; крохмалі, такі як, але без обмеGattefosse), лаурилсульфат натрію, жирні кислоти ження зазначеним, попередньо клейстеризовані та їхні солі, наприклад, олеїнову кислоту, олеат крохмалі (наприклад, National™ 1511 and натрію та олеат триетаноламіну, гліцерилові ефіри National™ 1500); целюлози, такі як, але без обмежирних кислот, наприклад, гліцерилмоностеарат, ження перерахованим, метилцелюлоза і натрієва складний ефір сорбітану, наприклад, монолаурат сіль кармелози (наприклад, Tylose™): альгінова сорбітану, моноолеат сорбітану, монопальмітат кислота і солі альгінової кислоти; силікат магніюсорбітану і моностеарат сорбітану, тилоксапол та алюмінію; ПЕГ; камедь ріжкового дерева; полісаїхні суміші. Такі зволожуючі засоби, якщо вони харидні кислоти; бентоніти: повідон, наприклад, присутні, складають всього від приблизно 0,25% 17 96117 18 до приблизно 15%, переважно, від приблизно 0,4% цевтичній галузі та їх можна застосовувати у фардо приблизно 10% і, більш переважно, від приблимацевтичних композиціях і лікарських засобах дазно 0,5% до приблизно 5% загальної маси фарманого винаходу. Таблетки можуть бути покритими, цевтичної композиції або лікарського засобу. наприклад, ентеросолюбільним покриттям, або Переважними зволожуючими засобами є аніоможуть бути непокритими. Композиції винаходу ногенні поверхнево-активні речовини. Особливо можуть далі включати в себе, наприклад, буферні переважним зволожуючим агентом є лаурилсульагенти. фат натрію. Лаурилсульфат, якщо він присутній, Необов'язково можна застосовувати один або складає від приблизно 0,25% до приблизно 7%, декілька агентів для надання шипучості як дезінтебільш переважно, від приблизно 0,4% до приблизгрувальні агенти і/або для підсилення органолепно 4%, і ще більш переважно, від приблизно 0,5% тичних властивостей фармацевтичних композицій до приблизно 2% загальної маси фармацевтичної або лікарських засобів винаходу. Коли один або композиції або лікарського засобу. декілька агентів для надання шипучості присутні у Фармацевтичні композиції і лікарські засоби фармацевтичних композиціях або лікарських засовинаходу необов’язково включають у себе одну бах для сприяння дезінтеграції лікарських форм, або декілька фармацевтично прийнятних змащувони, переважно, присутні в загальній кількості від вальних речовин (які включають агенти проти приприблизно 30 мас. % до приблизно 75 мас. % і, липання і/або агенти, що надають ковзання) як переважно, від приблизно 45 мас. % до приблизно ексципієнтів. Придатні змащувальні речовини 70 мас. %, наприклад, приблизно 60 мас. % фарвключають у себе, але не обмежуються перерахомацевтичних композиції або лікарського засобу. ваним, або окремо, або в комбінації, гліцерилбегаЗгідно з особливо переважним варіантом здійпат (наприклад. Compritol™ 888 of Gatlefosse); снення винаходу, агент для надання шипучості, стеаринову кислоту та її солі, у тому числі стеараприсутній у твердій лікарській формі в кількості, ти магнію, кальцію і натрію; гідрогенізовані росменшій, ніж кількість, що є ефективною для сприлинні олії (наприклад, Stcrotex™ of Abitec), колоїяння дезінтеграції лікарської форми, забезпечує дальний діоксид кремнію; тальк; віск; борну підвищене диспергування АРІ у водному середокислоту: бензоат натрію; ацетат натрію; фумарат вищі. Без зв'язку з теорією вважають, що агент для натрію; хлорид натрію; DL-лейцин: ПЕГ (напринадання шипучості є ефективним для прискорення клад, Carbowax™ 4000 and Carbowax™ 6000 of the диспергування АРІ з лікарської форми в шлунковоDow Chemical Company); олеат натрію; лаурилсукишковому тракті, тим самим додатково підвищульфат натрію і лаурилсульфат магнію. Такі змаючи абсорбцію і забезпечуючи швидкий початок щувальні речовини, якщо вони присутні, складатерапевтичної дії. Коли агент для надання шипують від приблизно 0,1% до приблизно 10%, чості присутній у фармацевтичній композиції або переважно, від приблизно 0,2% до приблизно 8% і лікарському засобі винаходу для сприяння диспербільш переважно, від приблизно 0,25% до приблигуванню в шлунково-кишковому тракті, але не для зно 5% загальної маси фармацевтичної композиції підвищення дезінтеграції, він, переважно, присутабо лікарського засобу. ній у кількості від приблизно 1 мас. % до приблизСтеарат магнію є переважною змащувальною но 20 мас. %, більш переважно, від приблизно 2,5 речовиною, що застосовується, наприклад, для мас. % до приблизно 15 мас. %, і ще більш перезниження тертя між обладнанням і гранульованою важно, від приблизно 5 мас. % до приблизно 10 сумішшю під час пресування для одержання премас. % фармацевтичної композиції або лікарського паратів у вигляді таблеток. засобу. Придатні агенти проти прилипання включають "Агент для надання шипучості'" тут є агентом, у себе, але не обмежуються перерахованим, що включає в себе одну або декілька сполук, які, тальк, кукурудзяний крохмаль, DL-лейцин, лаурилдіючи разом або окремо, виділяють газ при контасульфат натрію і стеарати металів. Тальк є перектуванні з водою. Газом, що виділяється, звичайно важним агентом проти прилипання або агентом, є кисень або, частіше за все, діоксид вуглецю. Пеякий надає ковзання, що застосовується, наприреважні агенти для надання шипучості включають клад, для зниження прилипання препарату до поу себе кислоту та основу, які взаємодіють у присуверхонь обладнання, а також для зменшення статності води з виділенням газоподібного діоксиду тики в суміші. Тальк, якщо він присутній, складає вуглецю. Переважно, основа включає в себе карвід приблизно 0,1% до приблизно 10%, більш пебонат або бікарбонат лужного металу або лужнореважно, від приблизно 0,25% до приблизно 5% і, земельного металу і кислота включає в себе аліще більш переважно, від приблизно 0,5% до прибфатичну карбонову кислоту. лизно 2% загальної маси фармацевтичної компоНеобмежувальні приклади придатних основ як зиції або лікарського засобу. компоненти агентів для надання шипучості, придаАгенти, що надають ковзання, можна застосотних для винаходу, включають у себе карбонатні вувати для сприяння сипкості порошкоподібного солі (наприклад, карбонат кальцію), бікарбонатні твердого препарату. Придатні агенти, що надають солі (наприклад, бікарбонат натрію), напівкарбонаковзання, включають у себе, але не обмежуються тні солі та їхні суміші. Карбонат кальцію є переваперерахованим, колоїдальний діоксид кремнію, жною основою. крохмаль, тальк, фосфат кальцію, порошкоподібну Необмежувальні приклади придатних кислот целюлозу і трисилікат магнію. Особливо переважяк компоненти агентів для надання шипучості і/або ним є колоїдальний діоксид кремнію. твердих кислот, придатних для винаходу, включаІнші ексципієнти, такі як барвники, коригенти і ють у себе лимонну кислоту, щавлеву кислоту (D-, підсолоджувальні речовини, є відомими у фармаL- або D/L-щавлеву кислоту), яблучну кислоту, 19 96117 20 малеїнову кислоту, фумарову кислоту, адипінову дію таблетування або капсулювання суміші з утвокислоту, бурштинову кислоту, кислі ангідриди таренням таблеток або капсул, відповідно. ких кислот, кислі солі таких кислот та їхні суміші. У переважному способі тверді лікарські форми Лимонна кислота є переважною кислотою. одержують способом, що включає в себе (а) стаУ переважному варіанті здійснення винаходу, дію змішування солі АРІ винаходу з одним або в якому агент для надання шипучості включає в декількома ексципієнтами з утворенням суміші, (b) себе кислоту та основу, масове відношення кислостадію грануляції суміші з утворенням грануляту і ти до основи складає від приблизно 1:100 до при(с) стадію таблетування або капсулювання суміші близно 100:1, більш переважно, від приблизно з утворенням таблеток або капсул, відповідно. 1:50 до приблизно 50:1, ще більш переважно, від Стадію (b) можна виконувати будь-яким способом приблизно 1:10 до приблизно 10:1. У наступному сухої або мокрої грануляції, відомим у даній галузі, переважному варіанті здійснення винаходу, в якоале переважною є стадія сухої грануляції. Сіль му агент для надання шипучості включає в себе даного винаходу переважно гранулюють з утвокислоту та основу, відношення кислоти до основи ренням часточок від приблизно 1 мікрометра до є приблизно стехіометричним. приблизно 100 мікрометрів, від приблизно 5 мікЕксципієнти, які розчиняють солі металів APIs, рометрів до приблизно 50 мікрометрів або від звичайно мають як гідрофільні, так і гідрофобні приблизно 10 мікрометрів до приблизно 25 мікрообласті, або є, переважно, амфіфільними або маметрів. Переважно додають один або декілька ють амфіфільні області. Один тип амфіфільного розріджувачів, один або декілька дезінтегрувальабо частково амфіфільного ексципієнта включає в них агентів і один або декілька зв’язувальних агенсебе амфіфільний полімер або є амфіфільним тів, наприклад, на стадії змішування, можна неополімером. Конкретним амфіфільним полімером є бов’язково додавати зволожуючий агент,поліалкіленгліколь який звичайно складається з наприклад, на стадії грануляції, що переважно, субодиниць етиленгліколю і/або пропіленгліколю. додають один або декілька дезінтегрувальних агеТакі поліалкіленгліколі можуть бути етерифіковані нтів після грануляції, але перед таблетуванням в їхніх кінцевих положеннях карбоновою кислотою, або капсулюванням. Змащувальну речовину перескладним ефіром, ангідридом карбонової кислоти важно додають перед таблетуванням. Змішування або іншою придатною частиною. Приклади таких і грануляцію можна проводити незалежно при ниексципієнтів включають у себе полоксамери (сизькому або високому зсувному зусиллі. Переважметричні блок-співполімери етиленгліколю і пропіно, вибирають спосіб, при якому утвориться граленгліколю, наприклад, полоксамер 237), поліалкінулят. який є однорідним за вмістом АРІ, який ленглікольовані складні ефіри токоферолу легко дезінтегрується, який досить легко сипкий, (включаючи ефір, утворений із ди- або поліфункцітак що зміну маси можна легко регулювати під час ональних карбонових кислот; наприклад, сукцинат заповнення капсул або таблетування, і який є доd-альфа-токоферолполіетиленгліколь-1000) і максить щільним у масі, так що завантаження можна роголгліцериди (одержані алкоголізом масла і обробляти у вибраному обладнанні та окремі дози етерифікацією поліалкіленгліколю з утворенням заповнювати у певні капсули або штампи для табсуміші моно-, ди- і тригліцеридів і складних моно- і летування. діефірів; наприклад, гліцеридів стеароїлмакрогоВ альтернативному варіанті здійснення тверді лу-32). Такі фармацевтичні композиції і лікарські лікарські форми одержують способом, який вклюзасоби переважно вводять перорально. чає в себе стадію розпилювального сушіння, в якій Фармацевтичні композиції і лікарські засоби АРІ суспендують з одним або декількома ексципієданого винаходу можуть включати в себе від принтами в одній або декількох рідинах, що розбризблизно 10 мас. % до приблизно 50 мас. %, від куються, переважно, непротонної (наприклад, неприблизно 25 мас. % до приблизно 50 мас. %, від водної або неспиртової) рідини, що приблизно 30 мас. % до приблизно 45 мас. % або розбризкується, і потім швидко піддають розпилювід приблизно 30 мас. % до приблизно 35 мас. % вальному сушінню над потоком теплого повітря. АРІ: від приблизно 10 мас. % до приблизно 50 мас. Гранулят або висушений розпиленням поро%, від приблизно 25 мас. % до приблизно 50 мас. шок, одержаний будь-яким із зазначених вище %, від приблизно 30 мас. % до приблизно 45 мас. ілюстративних способів, можна пресувати або фо% або від приблизно 30 мас. % до приблизно 35 рмувати для одержання таблеток або капсулювати мас. % ексципієнта, який інгібує кристалізацію, і від для одержання капсул. Можна застосовувати заприблизно 5 мас. % до приблизно 50 мас. %, від гальноприйняті способи таблетування і капсулюприблизно 10 мас. % до приблизно 40 мас. %, від вання, відомі в даній галузі. Коли потрібні таблетки приблизно 15 мас. % до приблизно 35 мас. % або з покриттями, придатними є загальноприйняті сповід приблизно 30 мас. % до приблизно 35 мас. % соби покриття. зв'язувальних речовини. В одному прикладі масоЕксципієнти для таблетованих композицій виве відношення АРІ до ексципієнта, який інгібує находу переважно вибирають для забезпечення кристалізацію, до зв’язувального агента становить часу дезінтеграції менше, ніж приблизно 30 хвиприблизно 1:1. лин, переважно, приблизно 25 хвилин або менше, Тверді лікарські форми винаходу можна одербільш переважно, приблизно 20 хвилин або менше жати будь-яким придатним способом, не обмежеі ще більш переважно, приблизно 15 хвилин або ним способами, що описані тут. менше в стандартному аналізі дезінтеграції. Ілюстративний спосіб включає в себе (а) стаВ іншому варіанті здійснення даного винаходу дію змішування солі винаходу з одним або декільможна одержати фармацевтичну композицію або кома ексципієнтами з утворенням суміші і (b) сталікарський засіб, що включає в себе модафініл і 21 96117 22 додатковий АРІ. Модафініл і додатковий АРІ моодин або декілька зазначених вище станів або жуть бути включені у вигляді суміші або комбінації порушень, що включають у себе, але не обмежуактивних фармацевтичних інгредієнтів. Наприються перерахованим, порушення сну, такі як нарклад, композиція може включати в себе модафініл колепсія, де спосіб включає введення суб'єкту теі кофеїн у вигляді комбінації. Композицію, що рапевтично ефективної кількості форми III R-(-)включає в себе модафініл і кофеїн, можна застомодафінілу, форми IV R-(-)-модафінілу або форм совувати як терапевтичний агент для лікування V R-(-)-модафінілу. тих же станів, для яких застосовують модафініл. У В іншому варіанті здійснення композицію датакій композиції, що включає в себе модафініл і ного винаходу можна вводити ссавцеві за допомокофеїн, кофеїн може забезпечувати характеристигою ін'єкції. Ін'єкції включають у себе, але не обку швидкого вивільнення (невелике Тmax відносно межуються перерахованим, внутрішньовенні, модафінілу) для профілю розчинення, годі як мопідшкірні і внутрішньом'язові ін'єкції. В іншому вадафініл викликає терапевтичну дію, яка продовжуріанті здійснення композицію даного винаходу виється протягом годин після введення. Наприклад, готовляють для ін'єкції ссавцеві, що потребує теТmax кофеїну може бути 0,001, 0,01, 0,05, 0,1, 0,2, рапевтичної дії. 0,3, 0,4, 0,5, 0,6, 0,7 або 0,8 від величини Тmax моПриклади дафінілу. Комбіновані терапії включають у себе Аналітичні способи введення двох або більше APIs в одному і тому ж Диференціальні скануючі калориметричні анапрепараті або в двох або більше препаратах, що лізи (ДСК) зразків проводили із застосуванням вводяться разом. диференціального скануючого калориметра Q1000 APIs молена вводити разом в один і той же (ТА Instruments, New Castle, DE, U.S.A.), який вичас або окремо з певними інтервалами часу. користовує перевагу для QW-Series, version У наступному варіанті здійснення даного вина1.0.0.78. Thermal Advantage Release 2.0 (2001 ТА ходу пропонується новий поліморф R-(-)Instruments-Water LLC). Крім того, програмним модафінілу. У конкретному варіанті здійснення забезпеченням, що застосовується для аналізу, даний винахід пропонує форми III, IV і V R-(-)був Universal Analysis 2000 for Windows модафінілу. Даний винахід пропонує також спосіб 95/98/2000/NT, version 3.1E; Build 3.1.0.40 (2001 ТА одержання поліморфа R-(-)-модафінілу. Instruments-Water LLC). У наступному варіанті здійснення даного винаДля аналізу ДСК газом, що застосовується для ходу пропонується спосіб одержання поліморфа продування, був сухий азот, еталонним матеріаR-(-)-модафінілу, що включає в себе: лом була пуста чашка, виготовлена з гофрованого (a) забезпечення R-(-)-модафінілу; алюмінію, і зразок продували при 50 мл/хвилину. (b) кристалізацію поліморфа R-(-)-модафінілу з Аналіз зразка ДСК проводили вміщенням зрапридатного розчинника. зка модафінілу в алюмінієву чашку з кришкою для У наступному варіанті здійснення даного винагофрованої чашки. Початкова температура була ходу поліморф R-(-)-модафінілу кристалізують з звичайно 20°С зі швидкістю нагріву 10°С/хвилину і органічного розчинника. У конкретному варіанті кінцева температура була 200°С. Всі зазначені здійснення органічним розчинником є етанол. В переходи (фазові) ДСК являють собою температуіншому варіанті здійснення для кристалізації поліру ендотермічного або екзотермічного переходу морфа R-(-)-модафінілу застосовують змішану при їх відповідних піках із похибкою +/-2°С. якщо систему розчинників. Змішаними системами розне зазначено особливо. чинників можуть бути, наприклад, етанол та ізопТермогравіметричний аналіз (TLA) зразків ропіловий спирт або етилацетат і етанол. У наступроводили із застосуванням термогравіметричного пному варіанті здійснення кристалізацію на стадії аналізатора Q500 (ТА Instruments, New Castle, DE, (b) завершують за допомогою термічної перекрисU.S.A.), який використовує перевагу для QWталізації. В іншому варіанті здійснення кристалізаSeries, version 1.0.0.78. Thermal Advantage Release цію на стадії (b) завершують за допомогою випа2.0 (2001 ТА Instruments-Water LLC). Крім того, рювання розчинника. програмним забезпеченням, що застосовується Застосування модафінілу є добре відомими в для аналізу був Universal Analysis 2000 for даній галузі і включають у себе лікування наркоWindows 95/98/2000/NT, version 3.1Е; Build 3.1.0.40 лепсії, пов'язаного з розсіяним склерозом стом(2001 ТА Instruments-Water LLC). лення, безплідності, порушення апетиту, розладу, Для експериментів ТГА газом, що застосовущо виражається в гіперактивності, яка призводить ється для продування, був сухий азот, продування до порушення уваги (ADHD), хвороби Паркінсона, для досягнення рівноваги проводили при 40 нетримання, приступів апное уві сні або міопатій. В мл/хвилину N2, і продування зразка проводили при іншому варіанті здійснення одну або декілька ком60 мл/хвилину N2. позицій модафінілу даного винаходу можна застоТГА проводили на зразку вміщенням зразка совувати при лікуванні одного або декількох замодафінілу в платинову чашку. Початкова темпезначених вище станів. Дозу і введення для ратура була звичайно 20°С при швидкості нагріву композицій модафінілу згідно з даним винаходом 10°С/хвилину і кінцева температура була 300°С. можна визначити із застосуванням стандартних Порошкову рентгенограму (PXRD) для зразків методів у даній галузі, але звичайно вона знижуодержували із застосуванням D/Max Rapid, Contact ється до величини між приблизно 50 і приблизно (Rigaku/MSC, The Woodlands, TX, U.S.А), який за700 мг/день. стосовує як його контрольне програмне забезпеВ іншому варіанті здійснення запропонований чення RINT Rapid Control Software, Rigaku спосіб для лікування суб'єкта, страждаючого на Rapid/XRD, version 1.0.0 (1999 Rigaku Co). Крім 23 96117 24 того, програмним забезпеченням, що застосовуНа основі даних PXRD. наведених тут, вклюється для аналізу було RINT Rapid display чаючи таблиці та фігури, кожна композиція даного software, version 1/18 (Rigaku/MSC) і JADE XRD винаходу може бути охарактеризована будь-яким Pattern Processing, versions 5.0 and 6.0 (1995-2002, одним, будь-якими двома, будь-якими трьома, Materials Data, Inc). будь-якими чотирма, будь-якими п'ятьма, будьДля аналізу PXRD параметри при зборі даних якими шістьма, будь-якими сімома або будь-якими були наступними: джерелом був Сu із лінією K у вісьмома або більше піками кута 2-тета. Для хара1.5406 Å; стадія х-у була з ручним керуванням; ктеризування композицій даного винаходу можна розмір коліматора був 0,3 мм: капілярна трубка також застосовувати будь-який один, два. три. (Charles Supper Company, Natick, MA, U.S.A.) мала чотири, п'ять або шість фазових переходів ДСК. ID (внутрішній діаметр) 0,3 мм; застосовували споДля характеризування композицій даного винахосіб відбиття: потужність для рентгенівської трубки ду можна також застосовувати будь-який один, була 46 кВ; струм для рентгенівської трубки був 40 будь-які два, три, чотири, п’ять або шість перехомА; омега-вісь осцилювали в діапазоні 0-5 градусів дів ДСК. Для характеризування композицій можна при швидкості 1 градус/хвилин); фі-вісь обертали також застосовувати різні комбінації піків PXRD і під кутом 360 градусів при швидкості 2 градуфазових переходів ДСК. си/секунду; коліматор 0,3 мм: час збору був 60 Термічну (із нагрівальним столиком) мікроскохвилин, температура була кімнатна і нагрівач не пію виконували на мікроскопі Zeiss Axioplan 2, застосовували. Зразок піддавали дії джерела реноснащеному регулятором Mettler Toledo FP90. Затгенівських променів у капілярі зі скла, багатого стосовуваним нагрівальним столиком був Mettler бором. Toledo FP82HT. Всі визначення точок плавлення Крім того, параметри аналізу були наступнипроводили вміщенням зразка на предметне скло ми: 2-тета-діапазон інтеграції був 2-60 градусів; Хімікроскопа і накриванням його накривним склом. діапазон інтеграції був 0-360 градусів; число ХіПочаткову температуру встановлювали 30°С і тесегментів було 1; застосовуваний розмір кроку був мпературу підвищували зі швидкістю 0,02; ефективність інтеграції була CYLINT; засто10°С/хвилину. Плавлення спостерігали через об'єсовували нормалізацію; темнові швидкості рахунку ктив мікроскопа 5х. були 8; омега-зсув був 180 і Хі і Фі-зсуви були 0. Метод ВЕРХ (адаптований із методу Donovan Дифрактограми PXRD одержували також за et al. Therapeutic Drug Monitoring 25:197-202): допомогою рентгенівського дифрактомера Barker колонка: Astec Cyclobond I 2000 RSP, 250x4,6 AXS D8 Discover. Цей інструмент був обладнаний мм (Part № 411121), GADDS™ (General Area Diffraction Detection рухома фаза А: 20 мМ фосфат натрію, рН 3,0, System), детектором площі Bruker AXS Hi-Star на В: суміш 70:30 рухома фаза А:ацетонітрил. відстані 15,05 см згідно з калібруванням системи, швидкість потоку: 1,0 мл/хвилину (1500 мідним джерелом випромінювання (Сu/К 1,54056 фунт/кв.дюйм), ангстрем), автоматизованою стадією x-y-z і коліпрограма потоку: градієнтна, матором 0,5 мм. Зразок пресували у форму кульки час досліду: 35 хвилин. і встановлювали на стадії х-y-z. Дифрактограму Детектування: УФ @ 225 нм. одержували в умовах навколишнього середовища Об'єм ін'єкції: 10 мікролітрів. (25°С) при встановленні потужності 40 кВ і 40 мА у Температура колонки: 30+/-1°С. методі відбиття, тоді як зразок залишався в стаціСтандартний розріджувач: суміш 90:10 (об./ онарному стані. Час впливу змінювали і визначали об.) рухома фаза:ацетонітрил. для кожного зразка. Одержану дифрактограму Промивання голки: ацетонітрилом. піддавали процедурі просторового перетворення Розчинник для очищення & промивальна рідидля обчислення геометричної подушкоподібної на для герметизуючого матеріалу: суміш 90:10 дисторсії детектора площі, потім інтегрували (об./об.) вода:ацетонітрил. вздовж кута ші від 118,8 до 61,8 градусів і кута 2Одержання рухомої фази: тета 2,1-37 градусів при розмірі кроку 0,02 градуса 1. Одержання 1М дигідрофосфату натрію: 120 зі встановленням нормалізації, щоб нормалізувати г дигідрофосфату натрію розчиняють у воді та накопичувач. об’єм доводять до 1000 мл, розчин фільтрують. Відносна інтенсивність піків на дифрактограмі 2. Одержання рухомої фази А (20 мМ фосфат не обов’язково є обмеженням картини PXRD. оскінатрію, рН 3.0): для одержання кожного літра 20 льки інтенсивність піків може варіювати від зразка мл 1 Μ фосфату натрію розводять до 1000 мл водо зразка, наприклад, внаслідок кристалічних додою, рН регулюють до 3,0 фосфорною кислотою. мішок. Крім того, кути кожного піка можуть варію3. Одержання рухомої фази В (суміш 70:30 вати приблизно на +/-0,1 градуса, переважно. +/(об./об.) 20 мМ фосфат натрію. рН 0,05. Вся картина рентгенограми або більшість 3,0:ацетонітрил): для одержання кожного літра піків картини можуть також зсуватися від приблиззмішують 700 мл рухомої фази А і 300 мл ацетоніно +/-0,1 градуса до приблизно +/-0,2 градуса внатрилу. слідок відмінностей у калібруванні, регулюванні та Одержання зразка: інших змін від інструмента до інструмента і від 1. Зразки розчиняють у суміші 90:10 (об./об.) оператора до оператора. Всі наведені піки PXRD 20 мМ фосфат натрію, рН 3,0,:ацетонітрил до прина фігурах, у прикладах і в іншому місці тут, зазнаблизної концентрації 20 мікрограмів/мл. чаються з похибкою приблизно ±0,1 градуса 2Зняття спектрів Рамана тета. Зразок або залишали в скляній пробірці, в якій його готували, або аліквоту зразка переносили на 25 96117 26 скляне предметне скло. Скляну пробірку або премодафініл у вигляді безбарвної твердої речовини дметне скло вміщували в камеру для зразка. Ви(580 мг). Аналіз PXDR і ДСК проводили з одержамірювання проводили із застосуванням системи ною твердою речовиною і виявили, що тверда реАlmega™ Dispersive Raman (Almega™ Dispersive човина є чистою формою R-(-)-модафінілу і S-(+)Raman, Thermo-Nicolet, 5225 Verona Road, модафінілу приблизно в масовому відношенні 2:1. Madison, WI 53711-4495), оснащеної лазерним Тверду суміш 2:1 R-(-)-модафініл:S-(+)джерелом із 785 нм. Зразок ручним способом домодафініл, одержану вище, можна характеризуваводять до фокуса із застосуванням мікроскопної ти будь-яким одним, будь-якими двома, будьчастини приладу зі збільшенням об'єктиву 10х якими трьома, будь-якими чотирма, будь-якими (якщо не зазначено особливо), таким чином спряп’ятьма або будь-якими шістьма або більшою кільмовуючи лазер на поверхню зразка. Спектр знімакістю піків на фіг. 1, що включають у себе, але що ють із застосуванням параметрів, зазначених у не обмежуються перерахованим, піки у 8,97, 10,15, таблиці А. (Час експонування і кількість експону12,87, 14,15, 15,13, 15,77, 18,19 і 20,39 градусів 2вань може змінюватися; зміни для параметрів бутета (одержані дані без обробки). дуть зазначені для кожного зняття спектра). ДСК твердої речовини, описаної вище, показала ендотермічний перехід фази приблизно при Таблиця А 167°С (див. фіг. 2). Приклад 2 Параметри зняття спектрів Рамана Поліморфи R-(-)-модафінілу Досліджували декілька поліморфів R-(-)модафінілу, кожний характеризували PXRD. На Значення парамефіг. 3, 6 і 9 показані ці дифрактограми PXRD (одеПараметр тра, що застосовуржані дані без обробки) поліморфів форми III, фоється рми IV і форми V. Час експонування (секунди) 2,0 Доведено, що перекристалізація є ефективним Кількість експонувань 10 способом для одержання і виявлення поліморфів Довжина хвилі лазерного джеR-(-)-модафінілу. Придатні розчинники для крисрела (нм) 785 талізації одного або декількох поліморфів R-(-)Потужність лазера (%) 100 модафінілу включають у себе, але не обмежуютьФорма отвору Точковий отвір ся перерахованим, ацетонітрил, диметилформаРозмір отвору (мкм) 100 мід (ДМФА), метанол, метилетилкетон, NСпектральна область 104-3428 метилпіролідон, етанол, ізопронанол, ізобутанол, Положення дифракційних ґрат Окреме формамід, ізобутилацетат, 1,4-діоксан, тетрагідТемпература при знятті спектрофуран (ТГФ), етилацетат, о-ксилол, ізопропілара (градуси С) 24,0 цетат, дихлорметан, пропіленгліколь, оцтову кислоту, воду, ацетон, нітрометан, толуол і Зняття ІЧ-спектрів бензиловий спирт. Для кристалізації одного або ІЧ-спектр одержували із застосуванням Nexus декількох поліморфів R-(-)-модафінілу можна заTM 470 FT-IR, Thermo-Nicolet, 5225 Verona Road, стосовувати окремі розчинники або суміші розчинMadison, WI 53711-4495 й аналізували із застосуників. ванням програмного забезпечення для контролю Форма III R-(-)-модафінілу та аналізу: OMNIC, Version 6.0а, (С) ThermoБезводний газоподібний аміак барботували Nicolet, 1995-2004. через розчин, що містить RПриклад 1 бензгідрилсульфінілметиловий складний ефір (8,3 Суміш 2:1 (R)-(-)-модафініл:(S)-(+)-модафініл г. 0,0288 моль) у метанолі (75 мл), протягом 10 Безводний газоподібний аміак барботують чехвилин. Реакційну суміш потім перемішували на рез розчин, що містить Rльодяній бані при 5°С протягом 1 години і газопобензгідрилсульфінілметиловий складний ефір дібний аміак барботували через розчин протягом (8,62 г, 0,0299 моль, суміш із масовим відношендодаткових 10 хвилин. Перемішування продовжуням приблизно 80:20 R-ізомер:S-ізомер) у метановали протягом додаткових 2 годин і аміак знов лі, протягом 10 хвилин. Тиск, що утворюється внабарботували через розчин протягом 10 хвилин. слідок реакції, спричиняє зворотну течію Після перемішування протягом ще однієї години бікарбонату натрію з пастки до реакційної суміші. утворювався осад (575 мг). який збирали. Фільтрат Реакцію зупиняють і осад збирають. Фільтрат конпотім нейтралізували із застосуванням концентроцентрують при зниженому тиску, одержуючи при ваної НСl і додатково утворений осад збирали. цьому жовтий твердий залишок (2,8 г). Жовту твеТвердий залишок потім перекристалізовували із рду речовину пропускають через колонку (силікасуміші 1:1 об./об., етанолу та ізопропілового спиргель, сорт 9385, 230-400 меш, 60 ангстрем) із зату нагріванням суміші до її кип'ятіння і потім охостосуванням суміші 3:1 об./об., етилацетат: гексан лодженням до кімнатної температури, одержуючи як елюенту. Фільтрати потім об'єднують і концентпри цьому форму III R-(-)-модафінілу у вигляді рують при зниженому тиску, одержуючи при цьому безбарвної твердої речовини (1,0.1 г). ясно-жовту тверду речовину (велика частина жовФорму III R-(-)-модафінілу можна характеризутого забарвлювання залишається на колонці). вати будь-яким одним, будь-якими двома, будьТверду речовину потім перекристалізовують з якими трьома, будь-якими чотирма, будь-якими етанолу нагріванням суміші до її кип'ятіння і потім п’ятьма або будь-якими шістьма або більшою кільохолодженням до кімнатної температури, одержукістю піків на фіг. 3, що включають у себе, але що ючи при цьому суміш 2:1 R-(-)-модафініл:S-(+) 27 96117 28 не обмежуються перерахованим, піки у 7,21, 10,37, Одержували другу порцію форми IV R-(-)17,73, 19,23, 21,17, 21,77 і 23,21 градусів 2-тета модафінілу для додаткового аналізу за допомогою (Rigaku PXRD, одержані дані без обробки). термічної мікроскопії і PXRD. Одержують також ДСК форми III R-(-)-модафінілу, охарактеризодану розчинність. Ці дані обговорюються нижче. ваної на фіг. 3, виявляв ендотермічний перехід Розчинність форми IV R-(-)-модафінілу дорівфази приблизно при 161 °С. нювала приблизно 3,5-4,0 мг/мл. Розчинність виОдержували другу порцію форми III R-(-)мірювали в суспензії, що перемішується в ізопромодафінілу для додаткового аналізу за допомогою пілацетаті при 25°С. Вимірювання розчинності термічної мікроскопії і PXRD. Одержували також проводили за допомогою ВЕРХ. Тверду речовину дані розчинності. Ці дані обговорюються нижче. із зразків для визначення розчинності сушили в Розчинність форми III R-(-)-модафінілу доріватмосфері азоту і характеризували PXRD і термічнювала приблизно 6,1-7,0 мг/мл. Розчинність виною мікроскопією. Під час проведення аналізу не мірювали в суспензії, що перемішується в ізопроспостерігали перетворення форми. пілацетаті при 25°С. Вимірювання розчинності Термічну (із нагрівальним столиком) мікроскопроводили за допомогою ВЕРХ. Тверду речовину пію застосовували при швидкості нагріву із зразків для визначення розчинності сушили в 10°С/хвилину для вимірювання точки плавлення атмосфері азоту і характеризували PXRD і термічформи IV R-(-)-модафінілу, яка. як визначено, була ною мікроскопією. Під час проведення аналізів не приблизно 147-158°С. спостерігали перетворення форми. Форму IV R-(-)-модафінілу можна характеризуТермічну (із нагрівальним столиком) мікросковати будь-яким одним, будь-якими двома, будьпію застосовували при швидкості нагріву якими трьома, будь-якими чотирма, будь-якими 10°С/хвилину для вимірювання точки плавлення п'ятьма або будь-якими шістьма або більшою кільформи III R-(-)-модафінілу, яка. як визначено, була кістю піків на фіг. 8, що включають у себе, але що приблизно 156-158°С. не обмежуються перерахованим, піки у 7,77, 10,33, Форму III R-(-)-модафінілу можна характеризу11,75, 16,53, 19,43, 19,89, 21,87, 23,49 і 26,69 гравати будь-яким одним, будь-якими двома, будьдусів 2-тета (Rigaku PXRD, дані з віднятим фоякими трьома, будь-якими чотирма, будь-якими ном). п'ятьма або будь-якими шістьма або більшою кільФорма V R-(-)-модафінілу кістю піків на фіг. 5. що включають у себе, але що Форму IV R-(-)-мoдaфiнілy (одержана за зане обмежуються перерахованим, піки у 7,19, 10,37, значеною вище методикою) нагрівали в розчині 12,11, 14,41, 17,73, 19,17, 21,71, 23,17, 24,39, етанолу до кип'ятіння суміші і потім охолоджували 25,17, 26,07 і 27,91 градусів 2-тета (Rigaku PXRD, до кімнатної температури. Тверду речовину потім дані з віднятим фоном). збирали і характеризували як форму V R-(-)Форма IV R-(-)-модафінілу модафінілу. Безводний газоподібний аміак барботували Форму V R-(-)-модафінілу можна характеризучерез розчин, що містить Rвати будь-яким одним, будь-якими двома, будьбензгідрилсульфінілметиловий складний ефір (8,3 якими трьома, будь-якими чотирма, будь-якими г, 0,0288 моль) у метанолі (75 мл) протягом 10 п’ятьма або будь-якими шістьма або більшою кільхвилин. Реакційну суміш потім перемішували на кістю піків на фіг. 9, то включають у себе, але що льодяній бані при 5°С протягом 1 години і газопоне обмежуються перерахованим, піки у 6,61, 10,39, дібний аміак барботували через розчин протягом 13,99, 16,49, 17,73, 19,03, 20,87, 22,31 і 25,99 градодаткових 10 хвилин. Після перемішування продусів 2-тета (Rigaku PXRD, одержані дані без обтягом ще однієї години утворювався осад (422 мг), робки). який збирали. Фільтрат потім нейтралізували із Одержували другу порцію форми V R-(-)застосуванням концентрованої НСl і додатково модафінілу для додаткового аналізу за допомогою утворений осад збирали. Тверду речовину (3 г) термічної мікроскопії і PXRD. Одержували також пропускали через колонку (силікагель, сорт 9385, дану розчинність. Ці дані обговорюються нижче. 230-400 меш, 60 ангстрем) із застосуванням суміші Розчинність форми V R-(-)-модафінілу дорів3:1 об./об., етилацетату і гексану як елюенту. Конювала приблизно 2,1-2,6 мг/мл. Розчинність вилонку потім промивали струменем етилацетату мірювали в суспензії, що перемішується в ізопро(250 мл). Фільтрати об'єднували і концентрували пілацетаті при 25°С. Вимірювання розчинності при зниженому тиску, одержуючи при цьому форпроводили за допомогою ВЕРХ. Тверду речовину му IV R-(-)-модафінілу у вигляді безбарвної тверіз зразків для визначення розчинності сушили в дої речовини (590 мг). атмосфері азоту і характеризували PXRD і термічФорму IV R-(-)-модафінілу можна характеризуною мікроскопією. Під час проведення аналізу не вати будь-яким одним, будь-якими двома, будьспостерігали перетворення форми. якими трьома, будь-якими чотирма, будь-якими Термічну (із нагрівальним столиком) мікроскоп'ятьма або будь-якими шістьма або більшою кільпію застосовували при швидкості нагріву кістю піків на фіг. 6, що включають у себе, але що 10°С/хвилину для вимірювання точки плавлення не обмежуються перерахованим, піки у 7,79, 10,31, форми V R-(-)-модафінілу, яка, як визначено, була 11,77, 16,49, 17,33, 19,47 і 23,5 градусів 2-тета приблизно 159°С. (Rigaku PXRD, одержані дані без обробки). Форму V R-(-)-модафінілу можна характеризуДСК форми IV R-(-)-модафінілу, охарактеризовати будь-яким одним, будь-якими двома, будьваної на фіг. 7, виявляла ендотермічний перехід якими трьома, будь-якими чотирма, будь-якими фази приблизно при 147°С. п'ятьма або будь-якими шістьма або більшою кількістю піків на фіг. 10. що включають у себе, але що 29 96117 30 не обмежуються перерахованим, піки у 6,53, 10,19, Форму IV R-(-)-модафінілу виділяли також за 13,90, 16,56, 17,35, 17,62, 18,99, 20,93, 22,08, 23,36 допомогою термічної перекристалізації з етанолу і і 25,91 градусів 2-тета (Bruker PXRD, одержані дані за допомогою повільного випарювання розчинника без обробки). етанолу. Поліморфи R-(-)-модафінілу називають форПриклад 5 мами III, IV і V на основі знайденої схожості в їхніх Форма V R-(-)-модафінілу дифрактограмах PXRD із такими дифрактограма107,7 мг R-(-)-модафінілу суспендували в 3 мл ми для відповідних форм III, IV і V рацемічного етилацетату. Суспензію нагрівали на нагрівальномодафінілу в заявці на патент США № му столику (60°С) для розчинення твердої речови20020043207, опублікованій 18 квітня 2002. ни. Приблизно від однієї третини до половини наПриклад 3 грітого розчинника випарюють із потоком R-(-)-модафініл:S-(+)-модафініл, 2:1 газоподібного азоту. Суміш потім охолоджували до Одержували розчин, що містить R-(-)кімнатної температури (25°С). Фільтрувальну модафініл (80,16 мг, 0,293 ммоль) і рацемічний центрифугу застосовували для відділення твердої модафініл (20,04 мг, 0.0366 ммоль) в етанолі (2 речовини від рідини. Тверду речовину, що утворимл). Суміш нагрівали до кип'ятіння, щоб розчинити лася, аналізували за допомогою PXRD і ДСК і вивсю тверду речовину і потім охолоджували до кімявили, що вона с формою V R-(-)-модафінілу (фіг. натної температури (25°С). Після витримування 14 і 15). при кімнатній температурі протягом 15 хвилин роФорму V R-(-)-модафінілу можна характеризузчин витримували при 5°С протягом ночі. Розчин вати будь-яким одним, будь-якими двома, будьпотім декантували і кристали, що залишилися, якими трьома, будь-якими чотирма, будь-якими сушили під потоком газоподібного азоту і характеп’ятьма або будь-якими шістьма або більшою кільризували із застосуванням ВЕРХ, PXRD, ДСК і кістю піків на фіг. 14. що включають у себе, але що термічної мікроскопії. не обмежуються перерахованим, піки у 6,52, 10,23, Одержані кристали містили від приблизно 63 13,93, 16,37, 17,61, 18,97, 20,74, 22,21, 23,36 і до приблизно 67 відсотків R-(-)-модафінілу, інша 25,90 градусів 2-тета (Bruker PXRD. одержані дані частина кристалів є S-(+)-модафінілом. Аналіз без обробки). ВЕРХ показав, що кристали були фазою 2:1, що Виконували аналіз ДСК форми V R-(-)містить дві молекули R-(-)-модафінілу на кожну мoдaфiнiлy. На фіг. 15 показаний ендотермічний одну молекулу S-(+)-модафінілу. перехід фази приблизно при 161-162 (161,57)°С. PXDR проводили на зразку монокристала R-(Приклад 6 )-модафініл:S-(+)-модафініл, 2:1. Монокристал R-(Сольват R-(-)-модафінілу з хлороформом )-модафініл:S-(+)-модафініл, 2:1, можна характе200 мікролітрів хлороформу додавали до 30,5 ризувати будь-яким одним, будь-якими двома, мг R-(-)-модафінілу. Суміш нагрівали при 75°С будь-якими трьома, будь-якими чотирма, будьпротягом 30 хвилин і потім додавали додаткові якими п'ятьма або будь-якими шістьма або біль200 мікролітрів хлороформу. Через додаткові 30 шою кількістю піків на фіг. 6. що включають у себе, хвилин тверда речовина повністю розчинялася. але що не обмежуються перерахованим, 8,95, Зразок нагрівали протягом додаткових 2 годин. 10,17, 11,87, 14,17, 15,11, 17,39, 18,31, 20,39, Після нагрівання зразок охолоджували до 5 граду21,09, 24,41 і 26,45 градусів 2-тета (Rigaku PXRD, сів при швидкості приблизно 1 градус/хвилину. одержані дані без обробки). Після досягнення 5°С зразок все ще був гомогенДСК R-(-)-мoдaфiнiл:S-(+)-мoдaфiнiл, 2:1, оханим рідким розчином. Зразок потім вміщували під рактеризована на фіг. 12, виявляв ендотермічний потік азоту на одну хвилину, викликаючи тим саперехід приблизно при 168°С. мим початок утворення кристалів. Зразок знову Термічну (із нагрівальним столиком) мікроскоінкубували при 5°С і одержували додаткову тверду пію застосовували при швидкості нагріву речовину. Зразок потім сушили під потоком азоту і 5°С/хвилину для вимірювання точки плавлення Rхарактеризували PXRD і ТГА. (-)-модафініл:S-(+)-модафініл 2:1. яка, як визначеАналіз PXRD виконували для сольвату R-(-)но, була приблизно 160-166°С. модафінілу з хлороформом. Сольват R-(-)Приклад 4 модафінілу з хлороформом можна характеризуваФорма IV R-(-)-модафінілу ти будь-яким одним, будь-якими двома, будь105,9 мг R-(-)-мoдaфiнiлy суспендували в 1,5 якими трьома, будь-якими чотирма, будь-якими мл етанолу протягом 2 днів. Рідину відділяли фіп'ятьма або будь-якими шістьма або більшою кільльтруванням і потім сушили над потоком газоподікістю піків на фіг. 16. що включають у себе, але що бного азоту. не обмежуються перерахованим, піки у 8,97, 12,07, Тверду речовину, що утворилася, аналізували 14,20, 16,91, 17,49, 18,56, 20,87, 21,45, 23,11 і за допомогою PXRD і визначили, що вона є фор25,24 градусів 2-тeта (Bruker PXRD, одержані дані мою IV R-(-)-модафінілу (фіг. 13). без обробки). Форму IV R-(-)-модафінілу можна характеризуПроводили ΤΓА сольвату R-(-)-модафінілу з вати будь-яким одним, будь-якими двома, будьхлороформом. На фіг. 17 показано, що приблизно якими трьома, будь-якими чотирма, будь-якими 15 мас. % втрачалося між приблизно 25 і приблизп'ятьма або будь-якими шістьма або більшою кільно 150°С. кістю піків на фіг. 13, що включають у себе, але що Приклад 7 не обмежуються перерахованим, піки у 7,64, 10,17, Сольват R-(-)-модафінілу з хлорбензолом 11,61, 16,41, 19,34, 21,71, 22,77 і 23,36 градусів 2R-(-)-модафініл (102,6 мг, 0,375 ммоль) сутета (Bruker PXRD, одержані дані без обробки). спендували в хлорбензолі (5 мл) і суспензію нагрі 31 96117 32 вали на нагрівальному столику при 60°С. Суміші цетатом можна характеризувати будь-яким одним, давали можливість охолонути приблизно до 25°С. будь-якими двома, будь-якими трьома, будь-якими Суспензію знов нагрівали і додавали ГГФ до розчотирма, будь-якими п'ятьма або будь-якими шісчинення всіх твердих речовин. Розчину потім датьма або більшою кількістю піків на фіг. 19, що вали можливість охолонути при зберіганні при кімвключають у себе, але що не обмежуються перенатній температурі протягом 4 днів у рахованим, піки у 8,88, 14,09, 19,83, 21,59, 23,04 і герметизованій ампулі. Після зберігання тверду 25,94 градусів 2-тета (Bruker PXRD, одержані дані речовину, що утворилася, збирали за допомогою без обробки). вакуумного фільтрування і характеризували за Проводили ТГА канального сольвату з етиладопомогою PXRD. цетатом рацемічного модафінілу. На фіг. 20 покаPXRD виконували на сольваті R-(-)-модафінілу зано, що приблизно 3,6 мас. % втрачається між з хлорбензолом. Сольват R-(-)-модафінілу з хлорприблизно 25 і приблизно 150°С. бензолом можна характеризувати будь-яким одПриклад 9 ним, будь-якими двома, будь-якими трьома, будьСольват R-(-)-модафінілу з оцтовою кислотою якими чотирма, будь-якими п'ятьма або будьСольват R-(-)-модафінілу з оцтовою кислотою якими шістьма або більшою кількістю піків на фіг. одержували розмелюванням R-(-)-модафінілу 18, що включають у себе, але що не обмежуються (105,5 мг) у 0,066 мл оцтової кислоти протягом 10 перерахованим, піки у 4,51, 6,25, 7,77, 10,37, хвилин у циліндрі з неіржавіючої сталі дробар11,43, 11,97, 16,61, 17,95, 20,19, 20,89, 23,41 і кою/змішувачем Wig-L-Bug. Порошок потім аналі30,43 градусів 2-тета (Bruker PXRD, одержані дані зували ДСК, ТГА і PXRD. без обробки). Одержували PXRD сольвату R-(-)-модафінілу Приклад 8 з оцтовою кислотою. Сольват можна характеризуКанальний сольват рацемічного модафінілу з вати будь-яким одним, будь-якими двома, будьетилацетатом якими трьома, будь-якими чотирма, будь-якими Канальний сольват рацемічного модафінілу з п'ятьма або будь-якими шістьма або більшою кільетилацетатом одержували з розчину рацемічного кістю піків на фіг. 21, що включають у себе, але що модафінілу (53,7 мг, 0,196 ммоль) та 1-гідрокси-2не обмежуються перерахованим, піки у 9,17, 10,20, нафтойної кислоти (75,5 мг, 0,401 ммоль) у 2.4 мл 16,61, 17,59, 18,90, 21,11 і 24,11 градусів 2-тета етилацетату, одержаного розчиненням на нагріва(Bruker PXRD, одержані дані без обробки). льному столику при 60°С. Після охолодження до Проводили ТГА сольвату R-(-)-модафінілу з розчину вносили затравку подрібнених співкристаоцтовою кислотою. На фіг. 22 показано, що приблів R-(-)-модафініл:1-гідрокси-2-нафтойна кислота лизно 11 мас. % втрачається між приблизно 25 і (див. приклад 17 заявки № PCT/US2004/29013). приблизно 125°С. Аналіз PXRD проводили з канальним сольваПроводили аналіз ДСК сольвату R-(-)том рацемічного модафінілу з етилацетатом. Камодафінілу з оцтовою кислотою. На фіг. 23 поканальний сольват рацемічного модафінілу з етилазаний ендотермічний перехід приблизно при 56°С. 33 96117 34 35 96117 36 37 96117 38 39 96117 40 41 96117 42 43 96117 44 45 Комп’ютерна верстка Л. Купенко 96117 Підписне 46 Тираж 23 прим. Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюModafinil compositions
Автори англійськоюHickey Magali Bourghol, Peterson Matthew, Almarsson Orn, Oliveira Mark
Назва патенту російськоюКомпозиция модафинила
Автори російськоюБургхол Хики Магали, Петерсон Меттью, Алмарссон Орн, Оливейра Марк
МПК / Мітки
МПК: C07C 317/10, A61K 31/165
Мітки: композиція, модафінілу
Код посилання
<a href="https://ua.patents.su/23-96117-kompoziciya-modafinilu.html" target="_blank" rel="follow" title="База патентів України">Композиція модафінілу</a>
Попередній патент: Вагонний залізничний візок та його елементи
Наступний патент: Пристрій для визначення положення поверхні поділу шлакового шару
Випадковий патент: Спосіб виробництва харчового екструдованого продукту з начинкою "подушечки "корисні"