Похідні 1,2,4-триамінобензолу, придатні для лікування розладів центральної нервової системи
Номер патенту: 79666
Опубліковано: 10.07.2007
Автори: Рітсен Андреас, Венсель Торньое Крістіан, Ханжин Ніколай, Банг Ньоргор Мортен, Роттлондер Маріо
Формула / Реферат
1. Похідні 1,2,4-триамінобензолу формули І
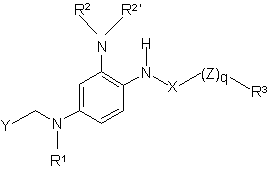 , (I)
, (I)
де:
R1 вибраний з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, ацилу, гідроксі-С1-6-алк(ен/ін)ілу і гідрокси-С3-8-циклоалк(ен)ілу;
R2 і R2' незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, арилу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, арил-С1-6-алк(ен/ін)ілу, ацилу, гідроксі-С1-6-алк(ен/ін)ілу і гідрокси-С3-8-циклоалк(ен)ілу;
R3 вибраний з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, арилу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, арил-С1-6-алк(ен/ін)ілу, гідроксі-С1-6-алк(ен/ін)ілу, арил-С3-8-циклоалк(ен)ілу, NR10R10'-С1-6-алк(ен/ін)ілу, NR10R10'-С3-8-циклоалк(ен)ілу і гідрокси-С3-8-циклоалк(ен)ілу; де
R10 і R10' незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, гідроксі-С1-6-алк(ен/ін)ілу,гідрокси-С3-8-циклоалк(ен)ілу,гідрокси-С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, галоген-С3-8-циклоалк(ен)ілу, галоген-С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, ціано-С1-6-алк(ен/ін)ілу, ціано-С3-8-циклоалк(ен)ілу і ціано-С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, або
R10 і R10' разом з атомом азоту, з яким вони зв'язані, утворюють 4-8-членне насичене або ненасичене кільце, яке необов'язково містить 1, 2 або 3 додаткові гетероатоми;
Х являє собою CO або SO2;
Z являє собою О або NR4, де
R4 вибраний з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, гідроксі-С1-6-алк(ен/ін)ілу і гідрокси-С3-8-циклоалк(ен)ілу; або
R3 і R4 разом з атомом азоту, з яким вони зв'язані, утворюють 4-8-членне насичене або ненасичене кільце, яке необов'язково містить 1, 2 або 3 додаткові гетероатоми, кільце, утворене R3 і R4 і атомом азоту, необов'язково заміщено одним або більше замісниками, незалежно вибраними з С1-6-алк(ен/ін)ілу, арилу і арилу-С1-6-алк(ен/ін)ілу;
q дорівнює 0 або 1;
і Y являє собою гетероарил формули II або III
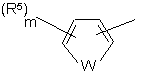 , (II)
, (II)
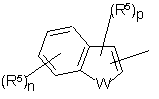 , (III)
, (III)
де:
W являє собою О або S;
m дорівнює 0, 1, 2 або 3;
n дорівнює 0, 1, 2, 3 або 4;
р дорівнює 0 або 1; і
кожний R5 незалежно вибраний з групи, що складається з С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, арилу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, арил-С1-6-алк(ен/ін)ілу, ацилу, атома галогену, галоген-С1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси, -CO-NR6R6', ціано, нітро, -NR7R7'; -S-R8, -SO2R8, SO2OR8;
де
R6 і R6' незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу і арилу;
R7 і R7' незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, арилу і ацилу;
і
R8 вибраний з групи, що складається з С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, арилу і –NR9R9'; де
R9 і R9' незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу і С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу;
або їх фармацевтично прийнятні солі.
2. Сполука за п. 1, де R1 вибраний з групи, що складається з атома водню і С1-6-алк(ен/ін)ілу.
3. Сполука за будь-яким одним з пп. 1 і 2, де принаймні один із замісників R2 і R2' являє собою атом водню.
4. Сполука за будь-яким одним з пп. 1-3, де обидва R2 і R2' являють собою атоми водню.
5. Сполука за будь-яким одним з пп. 1-4, де Х являє собою CO.
6. Сполука за будь-яким одним з пп. 1-5, де q дорівнює 0.
7. Сполука за будь-яким одним з пп. 1-5, де q дорівнює 1, і Z являє собою атом кисню.
8. Сполука за будь-яким одним з пп. 1-7, де R3 вибраний з групи, що складається з С1-6-алк(ен/ін)ілу і арил-С1-6-алк(ен/ін)ілу.
9. Сполука за п. 8, де R3 являє собою С1-6-алк(ен/ін)іл.
10. Сполука за п. 8, де R3 являє собою арил-С1-6-алк(ен/ін)іл.
11. Сполука за будь-яким одним з пп. 1-10, де W являє собою атом кисню.
12. Сполука за будь-яким одним з пп. 1-11, де W являє собою атом сірки.
13. Сполука за будь-яким одним з пп. 1-12, де Y має формулу II.
14. Сполука за будь-яким одним з пп. 1-12, де Y має формулу ІІІ.
15. Сполука за будь-яким одним з пп. 1-14, де Y має формулу ІІb або IIIb
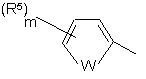 , (IIb)
, (IIb)
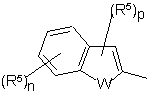 , (IIIb)
, (IIIb)
де W, m, n, р і R5 є такими, як визначено вище.
16. Сполука за будь-яким одним з пп. 1-14, де Y має формулу IIc або IIIс
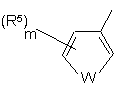 , (IIc)
, (IIc)
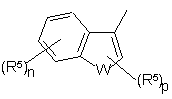 , (IIIc)
, (IIIc)
де W, m, n, р і R5 є такими, як визначено вище.
17. Сполука за будь-яким одним з пп. 1-16, де кожний R5 незалежно вибраний з групи, що складається з С1-6-алк(ен/ін)ілу, арилу, атома галогену, С1-6-алк(ен/ін)ілокси, -NR7R7', -SO2R8.
18. Сполука за будь-яким одним з пп. 1-17, де вказана сполука вибрана з групи, що складається з:
етилового естеру {2-аміно-4-[(5-хлортіофен-2-ілметил)метиламіно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(5-хлортіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(5-метилтіофен-2-ілметил)метиламіно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(5-бромтіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(6-хлор-3-метоксибензо[b]тіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(бензо[b]тіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(5-метилтіофен-2-ілметил)аміно]феніл} -карбамінової кислоти;
етилового естеру {2-аміно-4-[(4-бром-3-метокситіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(5-фенілтіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(3-хлортіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру (2-аміно-4-{[4-(4-хлорбензолсульфоніл)-3-метилтіофен-2-ілметил]аміно}феніл)-карбамінової кислоти;
етилового естеру {2-аміно-4-[(3-метилтіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(5-фторбензофуран-3-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(тіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(4-бромтіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(5-етилтіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(тіофен-3-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(5-хлортіофен-2-ілметил)етиламіно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(бензо[b]тіофен-3-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(5-диметиламінобензо[b]тіофен-3-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(5-диметиламіно-3-метилбензо[b]тіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
етилового естеру {2-аміно-4-[(5-фтортіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
пропілового естеру {2-аміно-4-[(бензо[b]тіофен-2-ілметил)аміно]феніл}-карбамінової кислоти;
пропілового естеру {2-аміно-4-[(бензо[b]тіофен-3-ілметил)аміно]феніл}-карбамінової кислоти;
N-{2-аміно-4-[(5-хлортіофен-2-ілметил)аміно]феніл}-2-(4-фторфеніл)ацетаміду і
N-{2-аміно-4-[(5-хлортіофен-2-ілметил)аміно]феніл}-3,3-диметилбутираміду;
і їх фармацевтично прийнятних солей.
19. Фармацевтична композиція, що містить сполуку за будь-яким одним з пп. 1-18 в терапевтично ефективній кількості разом з одним або більше фармацевтично прийнятними носіями або розріджувачами.
20. Застосування сполуки за будь-яким одним з пп. 1-19 для виробництва фармацевтичного препарату для профілактики, лікування і/або пригнічення розладу центральної нервової системи.
21. Застосування за п. 20, яке відрізняється тим, що розлад центральної нервової системи вибраний з групи, що складається з судомних нападів, таких як конвульсії, епілепсія та епілептичний статус.
22. Застосування за п. 21, яке відрізняється тим, що розлад центральної нервової системи вибраний з групи, що складається з невропатичних болів і мігрені, таких як алодинія, гіпералгічний біль, фантомний біль, невропатичний біль, пов'язаний з діабетичною невропатією, і невропатичний біль, пов'язаний з мігренню.
23. Застосування за п. 21, яке відрізняється тим, що розлад центральної нервової системи вибраний з групи, що складається з тривожних розладів, таких як страх, генералізований тривожний розлад, панічна тривога, обсесивно-компульсивний розлад, соціальна фобія, страх діяльності, посттравматичний стресовий розлад, гостра стресова реакція, розлад пристосовування, іпохондричні розлади, страх розлуки, агорафобія, специфічні фобії, тривожний розлад як наслідок загального хворобливого стану або тривожний розлад, викликаний хімічними речовинами.
24. Застосування за п. 21, яке відрізняється тим, що розлад центральної нервової системи вибраний з групи, що складається з нейродегенеративних захворювань, таких як хвороба Альцгеймера, хорея Гентінгтона, розсіяний склероз, аміотрофічний бічний склероз, індуковані СНІДом енцефалопатії та інші пов'язані з інфекціями енцефалопатії, викликані вірусами коревої краснухи, герпесвірусами, спірохетами і невідомими патогенами, хвороба Крейтцфельда-Якоба, хвороба Паркінсона, викликані травмою нейродегенерації.
25. Застосування за п. 21, яке відрізняється тим, що розлад центральної нервової системи вибраний з групи, що складається із станів гіперзбудження нейронів, таких як ті, що виникають при відміні препаратів, або таких, що викликані інтоксикацією.
Текст
1. Похідні 1,2,4-триамінобензолу формули І 2 (19) 1 3 79666 (R 5)p (R5) m W (R5 )n W (II) (III) де: W являє собою О або S; m дорівнює 0, 1, 2 або 3; n дорівнює 0, 1, 2, 3 або 4; р дорівнює 0 або 1; і кожний R5 незалежно вибраний з групи, що складається з С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, арилу, С3-8-циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу, арилС1-6-алк(ен/ін)ілу, ацилу, атома галогену, галогенС1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси, -CO-NR6R6' , ціано, нітро, -NR 7R7' ; -S-R8, -SO 2R8, SO2 OR8; де R6 і R6' незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу і арилу; R7 і R7' незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу, арилу і ацилу; і R8 вибраний з групи, що складається з С1-6алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу, арилу і –NR9R9' ; де R9 і R9' незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу і С 3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу; або їх фармацевтично прийнятні солі. 2. Сполука за п.1, де R1 вибраний з групи, що складається з атома водню і С 1-6-алк(ен/ін)ілу. 3. Сполука за будь-яким одним з пп.1 і 2, де принаймні один із замісників R2 і R2' являє собою атом водню. 4. Сполука за будь-яким одним з пп.1-3, де обидва R2 і R2' являють собою атоми водню. 5. Сполука за будь-яким одним з пп.1-4, де Х являє собою CO. 6. Сполука за будь-яким одним з пп.1-5, де q дорівнює 0. 7. Сполука за будь-яким одним з пп.1-5, де q дорівнює 1, і Z являє собою атом кисню. 8. Сполука за будь-яким одним з пп.1-7, де R3 вибраний з групи, що складається з С1-6-алк(ен/ін)ілу і арил-С 1-6-алк(ен/ін)ілу. 9. Сполука за п.8, де R3 являє собою С1-6алк(ен/ін)іл. 10. Сполука за п.8, де R3 являє собою арил-С 1-6алк(ен/ін)іл. 11. Сполука за будь-яким одним з пп.1-10, де W являє собою атом кисню. 12. Сполука за будь-яким одним з пп.1-11, де W являє собою атом сірки. 13. Сполука за будь-яким одним з пп.1-12, де Y має формулу II. 14. Сполука за будь-яким одним з пп.1-12, де Y має формулу ІІІ. 15. Сполука за будь-яким одним з пп.1-14, де Y має формулу ІІb або IIIb 4 (R5)p (R5 ) m W (R5 )n W (IIb) (IIIb) де W, m, n, р і R5 є такими, як визначено вище. 16. Сполука за будь-яким одним з пп.1-14, де Y має формулу IIc або Ібіс (R5 ) m W (R5)n W (R5)p (IIc) (IIIc) де W, m, n, р і R5 є такими, як визначено вище. 17. Сполука за будь-яким одним з пп.1-16, де кожний R5 незалежно вибраний з групи, що складається з С1-6-алк(ен/ін)ілу, арилу, атома галогену, С1-6-алк(ен/ін)ілокси, -NR7R7' , -SO2R8. 18. Сполука за будь-яким одним з пп.1-17, де вказана сполука вибрана з групи, що складається з: етилового естеру {2-аміно-4-[(5-хлортіофен-2ілметил)метиламіно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(5-хлортіофен-2ілметил)аміно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(5-метилтіофен-2ілметил)метиламіно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(5-бромтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(6-хлор-3метоксибензо[b]тіофен-2-ілметил)аміно]феніл}карбамінової кислоти; етилового естеру {2-аміно-4-[(бензо[b]тіофен-2ілметил)аміно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(5-метилтіофен-2ілметил)аміно]феніл} -карбамінової кислоти; етилового естеру {2-аміно-4-[(4-бром-3метокситіофен-2-ілметил)аміно]феніл}карбамінової кислоти; етилового естеру {2-аміно-4-[(5-фенілтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(3-хлортіофен-2ілметил)аміно]феніл}-карбамінової кислоти; етилового естеру (2-аміно-4-{[4-(4хлорбензолсульфоніл)-3-метилтіофен-2ілметил]аміно}феніл)-карбамінової кислоти; етилового естеру {2-аміно-4-[(3-метилтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(5-фторбензофуран3-ілметил)аміно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(тіофен-2ілметил)аміно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(4-бромтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(5-етилтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(тіофен-3ілметил)аміно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(5-хлортіофен-2ілметил)етиламіно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(бензо[b]тіофен-3ілметил)аміно]феніл}-карбамінової кислоти; етилового естеру {2-аміно-4-[(5диметиламінобензо[b]тіофен-3ілметил)аміно]феніл}-карбамінової кислоти; 5 79666 етилового естеру {2-аміно-4-[(5-диметиламіно-3метилбензо[b]тіофен-2-ілметил)аміно]феніл}карбамінової кислоти; етилового естеру {2-аміно-4-[(5-фтортіофен-2ілметил)аміно]феніл}-карбамінової кислоти; пропілового естеру {2-аміно-4-[(бензо[b]тіофен-2ілметил)аміно]феніл}-карбамінової кислоти; пропілового естеру {2-аміно-4-[(бензо[b]тіофен-3ілметил)аміно]феніл}-карбамінової кислоти; N-{2-аміно-4-[(5-хлортіофен-2ілметил)аміно]феніл}-2-(4-фторфеніл)ацетаміду і N-{2-аміно-4-[(5-хлортіофен-2ілметил)аміно]феніл}-3,3-диметилбутираміду; і їх фармацевтично прийнятних солей. 19. Фармацевтична композиція, що містить сполуку за будь-яким одним з пп.1-18 в терапевтично ефективній кількості разом з одним або більше фармацевтично прийнятними носіями або розріджувачами. 20. Застосування сполуки за будь-яким одним з пп.1-19 для виробництва фармацевтичного препарату для профілактики, лікування і/або пригнічення розладу центральної нервової системи. 21. Застосування за п.20, яке відрізняється тим, що розлад центральної нервової системи вибраний з групи, що складається з судомних нападів, таких як конвульсії, епілепсія та епілептичний статус. 22. Застосування за п.21, яке відрізняється тим, що розлад центральної нервової системи вибраний з групи, що складається з невропатичних болів і мігрені, таких як алодинія, гіпералгічний біль, фа Цей винахід відноситься до нових похідних 1,2,4-триамінобензолу, які відкривають калієві канали сімейства KCNQ. Сполуки придатні для профілактики, лікування і/або пригнічення розладів центральної нервової системи. Іонні канали є клітинними білками, які регулюють потік іонів, включаючи потік іонів калію, кальцію, хлору і натрію, в і з клітин. Такі канали є у всіх клітинах тварин і людини, та вони впливають на різні процеси, включаючи нейрональну передачу, скорочення м'язів і клітинну секрецію. У людей є більше 70 субодиниць калієвих каналів [Jentsch Nature Reviews Neuroscience 2000, 1, 21-30] з великою різноманітністю відносно структури і функції. Калієві канали нейронів, які виявляють в мозку, в основному відповідні за підтримку негативного потенціалу спокою мембран, а також регуляцію реполяризації мембран після потенціалу дії. Однією підгрупою генів калієвих каналів є сімейство KCNQ. Було показано, що мутації в чо тирьох з п'яти генів KCNQ приводять до розвитку захворювань, включаючи серцеві аритмії, глухоту і епілепсію [Jentsch Nature Reviews Neuroscience 2000, 1, 21-30]. Вважають, що ген KCNQ4 кодує молекулярний корелят калієвих каналів, виявлених в зовнішніх волосних клітинах равлика і у волосних клітинах 6 нтомний біль, невропатичний біль, пов'язаний з діабетичною невропатією, і невропатичний біль, пов'язаний з мігренню. 23. Застосування за п.21, яке відрізняється тим, що розлад центральної нервової системи вибраний з групи, що складається з тривожних розладів, таких як страх, генералізований тривожний розлад, панічна тривога, обсесивно-компульсивний розлад, соціальна фобія, страх діяльності, посттравматичний стресовий розлад, гостра стресова реакція, розлад пристосовування, іпохондричні розлади, страх розлуки, агорафобія, специфічні фобії, тривожний розлад як наслідок загального хворобливого стану або тривожний розлад, викликаний хімічними речовинами. 24. Застосування за п.21, яке відрізняється тим, що розлад центральної нервової системи вибраний з групи, що складається з нейродегенеративних захворювань, таких як хвороба Альцгеймера, хорея Гентінгтона, розсіяний склероз, аміотрофічний бічний склероз, індуковані СНІДом енцефалопатії та інші пов'язані з інфекціями енцефалопатії, викликані вірусами коревої краснухи, герпесвірусами, спірохетами і невідомими патогенами, хвороба Крейтцфельда-Якоба, хвороба Паркінсона, викликані травмою нейродегенерації. 25. Застосування за п.21, яке відрізняється тим, що розлад центральної нервової системи вибраний з групи, що складається із станів гіперзбудження нейронів, таких як ті, що виникають при відміні препаратів, або таких, що викликані інтоксикацією. типу І вестибулярного апарату, мутації в якому приводять до спадкової глухоти. KCNQ1 (KvLQT1) організовується з продуктом гена KCNE1 (мінімальний K(+)-білок каналу) у серці з утворенням подібного до випрямляча K(+) струму, що уповільнює роботу серця. Мутації в даному каналі можуть призвести до розвитку спадкового синдрому довгого зубця QT типу 1 (LQT1), а також вони пов'язані з формою глухоти [Robbins Pharmacol. Ther. 2001, 90,1-19]. Гени KCNQ2 і KCNQ3 були відкриті в 1988p., і виявилось, що вони є мутантами при спадковій формі епілепсії, відомої як доброякісні сімейні судоми новонароджених [Rogawski Trends in Neurosciences 2000, 23, 393-398]. Білки, що кодуються генами KCNQ2 і KCNQ3, розташовуються в пірамідальних нейронах кори головного мозку і гіпокампа людини, ділянках мозку, пов'язаних з виникненням і розвитком судомних нападів [Cooper et al. Proceedings National Academy of Science USA 2000, 97, 4914-4919]. KCNQ2 і KCNQ3 є двома субодиницями калієвих каналів, які утворюють "М-стр уми" при експресії in vitro. М-стр ум є не-інактивуючим калієвим струмом, виявленим в багатьох типах нейронів. У кожному типі клітин він є домінантним в регуляції збудливості мембран, будучи єдиним постійним струмом при ініціації потенціалу дії [Marrion Annual Review Physiology 1997, 59, 483-504]. Модуляція 7 79666 М-струму значно впливає на збудливість нейронів, наприклад, активація струму буде призводити до зниження збудливості нейронів. Таким чином, речовини, що відкривають дані канали KCNQ, знижуватимуть надмірну активність нейронів при таких станах, як судомні напади і захворювання, що характеризуються надмірною активністю нейронів, наприклад, при епілепсії та невропатичному болю. Ретигабін (D-23129, етиловий естер N-(2аміно-4-(4-фторбензиламіно)феніл)-карбамінової кислоти) та його аналоги розкриті [в патенті ЕР 554543]. Ретигабін є антиконвульсивною сполукою широкого спектра дії та з сильними антиконвульсивними властивостями як в умовах in vitro, так і in vi vo. Він є активним при пероральному і внутрішньочеревинному введенні щурам і мишам у ряді антиконвульсивних тестів, включаючи: індуковані електрикою судомні напади, судомні напади, що індукуються хімічною дією пентилентетразолу, пікротоксину і N-метил-D-аспартату (NMD A), і тест на генетичній тваринній моделі - мишах DBA/2 [Rostock et al. Epilepsy Research 1996, 23, 211-223]. Крім того, ретигабін є активним на моделі складних парціальних нападів, викликаних стимуляцією мигдалика, що додатково вказує на те, що дані сполуки мають потенційну можливість для застосування в антиконвульсивній терапії. У нещодавно проведених клінічних випробуваннях було показано, що ретигабін виявляє ефективність в зниженні частоти судомних нападів у пацієнтів з епілепсією [Bialer et al. Epilepsy Research 2002, 51, 31-71]. Було показано, що ретигабін активує K(+)струм в нейронах, і фармакологія даного індукованого струму узгоджується з опублікованими даними по фармакології М-каналу, що свідчать про кореляцію з гетеромультимером KCNQ2/3 K(+) каналу. На підставі цього можна припустити, що активація каналів KCNQ2/3 може бути частково відповідальна за антиконвульсивну активність даного засобу [Wickenden et al. Molecular Pharmacology 2000, 58, 591-600] і що інші засоби, які діють за таким ж механізмом, можуть мати аналогічні застосування. Повідомлялося, що канали KCNQ2 і 3 стимулювалися на моделях невропатичного болю [Wickenden et al. Society for Neuroscince Abstracts 2002, 454, 7], і була висловлена гіпотеза про те, що модулятори калієвих каналів є активними при невропатичному болю і епілепсії [Schroder et al. Neuropharmacology 2001, 40, 888-898; BlackburnMunro and Jensen European Journal of Pharmacology 2003, 460, 109-116]. Крім того, повідомлялося, що присутність мРНК каналів KCNQ в мозку та інших частинах центральної нервової системи пов'язана з болем [Goldstein et al. Society for Neuroscience Abstracts 2003, 53, 8]. У доповнення до ролі при невропатичному болю, експресія мРНК KCNQ 2-5 в ганглії тригемінального і дорсального кореня і в тригемінальному хвостатому ядрі свідчить про те, що речовини, які відкривають дані канали, можуть також впливати на сенсорний процесинг мігрені [Goldstein et al. Society for Neuroscience Abstracts 2003, 53, 8]. У недавно опублікованих повідомленнях було показано, що мРНК KCNQ 3 і 5, в доповнення до 8 KCNQ2, експресується в астроцитах і гліальних клітинах. Таким чином, канали KCNQ2, 3 і 5 можуть модулювати синаптичну активність в ЦНС і вносити свій внесок в нейропротекторну дію речовин, які відкривають канали KCNQ [Noda et al., Society for Neuroscience Abstracts 2003, 53, 9]. Так, ретигабін і інші модулятори KCNQ можуть виявляти захисну дію відносно нейродегенеративних аспектів епілепсії, оскільки було показано, що ретигабін запобігає нейродегенерації лімба і експресії маркерів апоптозу після індукованого каїновою кислотою епілептичного статусу у щурів [Ebert et al. Epilepsia 2002, 43 Suppl. 5, 86-95]. Це може мати відношення до попередження прогресування епілепсії у пацієнтів, тобто виражається в антиепілептогенній дії. Також було показано, що ретигабін уповільнює прогресування збудження гіпокампа у щурів, який є додатковою моделлю розвитку епілепсії [Tober et al. European Journal of Pharmacology 1996, 303, 163-169]. З ура хуванням того, що антиконвульсивні сполуки, такі як бензодіазепіни і хлорметіазол, клінічно застосовуються для лікування синдрому відміни вживання етанолу, і що інші антиконвульсивні препарати, наприклад, габапентин, є дуже ефективними на тваринних моделях даного синдрому [Watson et al. Neuropharmacology 1997, 36, 13691375], заявники припустили, що інші антиконвульсивні сполуки, такі як речовини, що відкривають KCNQ, будуть також ефективними при даному стані. мРНК субодиниць KCNQ2 і 3 виявлені в ділянках мозку, пов'язаних з тривогою і емоційною поведінкою, такою як біполярний розлад, наприклад, в гіпокампі і мигдалику [Saganich et al. Journal of Neuroschience 2001, 21, 4609-4624], і повідомлялося, що ретигабін є активним на деяких тваринних моделях станів, подібних тривозі [Harts et al. Journal of Psychopharmacology 2003, 17 suppl. 3 А28, В16], і інші клінічно використовувані антиконвульсивні сполуки застосовуються для лікування біполярного розладу. У [заявці WO 200196540] розкривається застосування модуляторів М-стр уму, утвореного експресією генів KCNQ2 і KCNQ3, для лікування безсоння, тоді як в [заявці WO 2001092526] розкривається, що модулятори KCNQ5 можна використовувати для лікування порушень сну. У [заявці WO01/022953] розкривається застосування ретигабіну для профілактики і лікування невропатичного болю, такого як алодинія, гіпералгічний біль, фантомний біль, невропатичний біль, пов'язаний з діабетичною невропатією, і невропатичний біль, пов'язаний з мігренню. У [заявці WO 02/049628] розкривається застосування ретигабіну для профілактики, лікування, пригнічення і ослаблення тривожних розладів, таких як страх, генералізований тривожний розлад, панічна тривога, обсесивно-компульсивний розлад, соціальна фобія, страх діяльності, посттравматичний стресовий розлад, гостра стресова реакція, розлад пристосовування, іпохондричні розлади, страх розлуки, агорафобія та специфічні фобії. 9 79666 У [заявці WO 97/15300] розкривається застосування ретигабіну для лікування нейродегенеративних захворювань, таких як хвороба Альцгеймера, хорея Гентінгтона, розсіяний склероз, аміотрофічний бічний склероз, індукована СНІДом енцефалопатія та інші пов'язані з інфекціями енцефалопатії, викликані вірусами коревої краснухи (rubella вірусами), герпесвірусами, спірохетами і невідомими патогенами, хвороба КрейтцфельдаЯкоба, хвороба Паркінсона, викликані травмою нейродегенерації і станів гіперзбудження нейронів, таких як ті, що виникають при відміні препаратів, або таких, що викликані інтоксикацією, нейродегенеративних захворювань периферичної нервової системи, таких як поліневропатії і поліневрити. Отже, є велика потреба в нових сполуках, які відкривають калієві канали сімейства KCNQ. Також бажаними є нові сполуки з поліпшеними в порівнянні з відомими сполуками властивостями, які відкривають калієві канали сімейства KCNQ, такі як ретигабін. Бажано поліпшення одного або більше з наступних параметрів: періоду напіввиведення, кліренсу, вибірковості, взаємодії з іншими лікарськими препаратами, біодоступності, ефективності, здатності змішуватися, хімічної стабільності, метаболічної стабільності, проникності через мембрани, розчинності та терапевтичного індексу. Поліпшення даних параметрів може призвести до таких поліпшень, як: - поліпшена схема введення при зменшенні кількості необхідних доз на день; - простота введення пацієнтам при багатократному застосуванні; - знижені побічні ефекти; - підвищений терапевтичний індекс; - підвищена переносність і/або - поліпшене сприйняття. Отже, метою винаходу є забезпечення новими сполуками, які ефективно відкривають калієві канали сімейства KCNQ. Сполуки за винаходом є похідними 1,2,4триамінобензолу загальної формули І або їх фармацевтично прийнятними солями де: R1, R2, R2, R3, Χ, Ζ, Υ і q є такими, як визначено нижче. Винахід додатково відноситься до фармацевтичної композиції, яка містить сполуку формули І, і до її застосування. Детальний опис винаходу Цей винахід відноситься до нових похідних 1,2,4триамінобензолу формули І 10 де: R1 вибраний з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу, ацилу, гідроксиС1-6-алк(ен/ін)ілу і гідрокси-С 3-8-циклоалк(ен)ілу; R2 і R2’ незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу, арилу, С 3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу, арил-С 1-6-алк(ен/ін)ілу, ацилу, гідрокси-С1-6-алк(ен/ін)ілу і гідрокси-С 3-8циклоалк(ен)ілу; R3 вибраний з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, арилу, С3-8-циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу, арилС1-6-алк(ен/ін)ілу, гідрокси-С 1-6-алк(ен/ін)ілу, арилС3-8-циклоалк(ен)ілу, NR10R10’-С1-6-алк(ен/ін)ілу, 10 10’ NR R -С3-8-циклоалк(ен)ілу і гідрокси-С 3-8циклоалк(ен)ілу; де R10 і R10’ незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу, гідрокси-С 1-6-алк(ен/ін)ілу, гідроксиС3-8-циклоалк(ен)ілу, гідрокси-С 3-8-циклоалк(ен)ілС1-6-алк(ен/ін)ілу, галоген-С 1-6-алк(ен/ін)ілу, галоген-С 3-8-циклоалк(ен)ілу, галоген-С3-8циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу, ціано-С 1-6алк(ен/ін)ілу, ціано-С 3-8-циклоалк(ен)ілу і ціано-С 38-циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу, або R10 і R10’ разом з атомом азоту, з яким вони зв'язані, утворюють 4-8-членне насичене або ненасичене кільце, яке необов'язково містить 1, 2 або 3 додаткові гетероатоми; X являє собою CO або SO2 , Ζ являє собою О або NR4, де R4 вибраний з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу, гідрокси-С 1-6алк(ен/ін)ілу і гідрокси-С 3-8-циклоалк(ен)ілу; або R3 і R4 разом з атомом азоту, з яким вони зв'язані, утворюють 4-8-членне насичене або ненасичене кільце, яке необов'язково містить 1, 2 або 3 додаткові гетероатоми, кільце, утворене R3 і R4 і атомом азоту, необов'язково заміщено одним або більше замісниками, незалежно вибраними з С 1-6алк(ен/ін)ілу, арилу і арил-С 1-6-алк(ен/ін)ілу; q дорівнює 0 або 1; і Υ являє собою гетероарил формули II або III де: W являє собою О або S; m дорівнює 0, 1, 2 або 3; 11 79666 n дорівнює 0,1,2, 3 або 4; p дорівнює 0 або 1; і кожний R5 незалежно вибраний з групи, що складається з С 1-6-алк(ен/іл)ілу, С3-8циклоалк(ен)ілу, арилу, С 3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу, арил-С 1-6-алк(ен/ін)ілу, ацилу, атома галогену, галоген-С1-6-алк(ен/ін)ілу, С1-6алк(ен/ін)ілокси, -CO-NR6R6' , ціано, нітро, -NR7R7' , S-R8, -SO 2R8 і SO 2OR8 ; де R6 і R6’ незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу і арилу; R7 і R7' незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу, арилу і ацилу; і R8 вибраний з групи, що складається з С1-6алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу, арилу і -NR9R9’; де R9 і R9' незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу і С 3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу; або їх фармацевтично прийнятних солей. Коли q дорівнює 0, тоді R3 сполучений з X, коли q дорівнює 1, тоді R3 сполучений з Z, який сполучений з X. Таким чином, X-(Z)q -R3 може бути XR3, X-O-R3 або X-NR 3R4. У конкретному варіанті здійснення цей винахід відноситься до сполук формули І де: R1, R2, R2, X і q є такими, як визначено вище; і R3 вибраний з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, арилу, С3-8-циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу, арилС1-6-алк(ен/ін)ілу, гідрокси-С 1-6-алк(ен/ін)ілу і гідрокси-С3-8-циклоалк(ен)ілу; і Ζ є таким, як визначено вище, за умови, що R4 вибраний з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу, гідрокси-С 1-6алк(ен/ін)ілу і гідрокси-С 3-8-циклоалк(ен)ілу; і Υ є таким, як визначено вище, за умови, що кожний R5 незалежно вибраний з групи, що складається з С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, арилу, С3-8-циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу, арилС1-6-алк(ен/ін)ілу, ацилу, атома галогену, галогенС1-6-алк(ен/ін)ілу, -CONR6R6' , ціано, нітро, -NR 7R7' , S-R8, -SO 2R8 і SO 2OR8 ; або їх фармацевтично прийнятних солей. У одному варіанті здійснення R1 вибраний з групи, що складається з ацилу, гідрокси-С 1-6алк(ен/ін)ілу і гідрокси-С 3-8-циклоалк(ен)ілу. У іншому варіанті здійснення винахід відноситься до таких сполук, де R1 вибраний з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу і С 3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу. У одному переважному варіанті здійснення винахід відноситься до таких сполук, де R1 вибра 12 ний з групи, що складається з атома водню і С1-6алк(ен/ін)ілу. У конкретному варіанті здійснення винахід відноситься до таких сполук, де R1 являє собою атом водню. У іншому конкретному варіанті здійснення винахід відноситься до таких сполук, де R1 являє собою С1-6-алк(ен/ін)іл. У одному варіанті здійснення принаймні один з R2 і R2' вибраний з групи, що складається з арилу, арил-С 1-6-алк(ен/ін)ілу, ацилу, гідрокси-С 1-6алк(ен/ін)ілу і гідрокси-С 3-8-циклоалк(ен)ілу. У іншому варіанті здійснення принаймні один з R2 і R2' вибраний з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу і С 38-циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу. У ще одному варіанті здійснення винахід відноситься до таких сполук, де принаймні один із замісників R2 і R2’ являє собою атом водню. У ще одному варіанті здійснення винахід відноситься до таких сполук, де обидва R2 і R2' являють собою атоми водню. У одному варіанті здійснення R3 вибраний з групи, що складається з гідрокси-С 1-6-алк(ен/ін)ілу, арил-С 3-8-циклоалк(ен)ілу, NR10R10’-С1-610 10’ алк(ен/ін)ілу, NR R -С3-8-циклоалк(ен)ілу і гідрокси-С3-8-циклоалк(ен)ілу; де R10 і R10' незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу, гідрокси-С 1-6-алк(ен/ін)ілу, гідроксиС3-8-циклоалк(ен)ілу, гідрокси-С 3-8-циклоалк(ен)ілС1-6-алк(ен/ін)ілу, галоген-С 1-6-алк(ен/ін)ілу, галоген-С 3-8-циклоалк(ен)ілу, галоген-С3-8циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу, ціано-С 1-6алк(ен/ін)ілу, ціано-С 3-8-циклоалк(ен)ілу і ціано-С 38-циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу; або R10 і R10' разом в атомом азоту, з яким вони зв'язані, утворюють 4-8-членне насичене або ненасичене кільце, яке необов'язково містить 1, 2 або 3 додаткові гетероатоми. У ще одному варіанті здійснення винахід відноситься до таких сполук, де q дорівнює 1, Ζ являє собою NR4, a R3 являє собою атом водню. У ще одному варіанті здійснення винахід відноситься до таких сполук, де R є іншим атомом, ніж атом водню. У ще одному варіанті здійснення R3 вибраний з групи, що складається з С1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу, арилу, С 3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу і арил-С 1-6-алк(ен/ін)ілу. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких R3 вибраний з групи, що складається з С 1-6-алк(ен/ін)ілу і арил-С 16-алк(ен/ін)ілу. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких R3 являє собою С1-6-алк(ен/ін)іл. У ще одному варіанті здійснення R3 являє собою С 3-8-циклоалк(ен)іл-С 1-6-алк(ен/ін)іл. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких R3 являє собою арил-С 1-6-алк(ен/ін)іл. У одному варіанті здійснення винахід відноситься до таких сполук, в яких X являє собою SO2. 13 79666 У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких X являє собою CO. У одному варіанті здійснення q дорівнює 0. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких X являє собою CO, a q дорівнює 0. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких X являє собою CO, a q дорівнює 0, і R3 є іншим, ніж арил. У іншому варіанті здійснення q дорівнює 1. У одному варіанті здійснення винахід відноситься до таких сполук, в яких q дорівнює 1, a Z являє собою NR4. У одному варіанті здійснення q дорівнює 1, Ζ являє собою NR4, a R3 і R4 разом з атомом азоту, з яким вони зв'язані, утворюють 4-8-членне насичене або ненасичене кільце, яке необов'язково містить 1, 2 або 3 додаткові гетероатоми, кільце, утворене R3 і R4 і атомом азоту, необов'язково заміщене одним або більше замісниками, незалежно вибраними з С 1-6-алк(ен/ін)ілу, арилу і арил-С 16-алк(ен/ін)ілу. У іншому варіанті здійснення q дорівнює 1, Ζ являє собою NR4, a R4 вибраний з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу, С3-8-циклоалк(eн)іл-С1-6алк(ен/ін)ілу, гідрокси-С 1-6-алк(ен/ін)ілу і гідроксиС3-8-циклоалк(ен)ілу. У ще одному варіанті здійснення q дорівнює 1, Ζ являє собою NR4, a R4 являє собою атом водню. У одному варіанті здійснення q дорівнює 1, Ζ являє собою NR4, а принаймні один з R3 і R4 являє собою атом, інший ніж атом водню. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких q дорівнює 1, a Z являє собою атом водню. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких X являє собою CO, q дорівнює 1, a Z являє собою атом водню. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких R2 і R являють собою атоми водню, X являє собою CO, q дорівнює 1, a Z являє собою атом кисню. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких W являє собою атом кисню. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких W являє собою атом сірки. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких W являє собою атом сірки, а X являє собою CO. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких W являє собою атом сірки, a q дорівнює 0. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких W являє собою атом сірки, X являє собою CO, a q дорівнює 0. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких W являє собою атом сірки, q дорівнює 1, a Z являє собою атом кисню. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких W являє собою 14 атом сірки, X являє собою CO, q дорівнює 1, a Z являє собою атом кисню. У ще одному варіанті здійснення m дорівнює 0. У ще одному варіанті здійснення m дорівнює 1. У ще одному варіанті здійснення m дорівнює 2. У ще одному варіанті здійснення m дорівнює 3. У ще одному варіанті здійснення n дорівнює 0. У ще одному варіанті здійснення n дорівнює 1. У одному варіанті здійснення n дорівнює 2, 3 або 4. У одному варіанті здійснення p дорівнює 0. У іншому варіанті здійснення p дорівнює 1. У одному варіанті здійснення принаймні один R5 вибраний з групи, що складається з ацилу, -CONR6R6’, нітро, -S-R 8 і SO2 OR8. У іншому варіанті здійснення кожний R5 незалежно вибраний з групи, що складається з С1-6алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, арилу, С3-8циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу, арил-С 1-6алк(ен/ін)ілу, атома галогену, галоген-С1-6алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси, ціано, -NR7R7’ і SO2R8. У ще одному варіанті здійснення кожний R5 незалежно вибраний з групи, що складається з Сіарилу, атома галогену, Сі-66-алк(ен/ін)ілу, алк(ен/ін)ілокси, -NR7R7’ і SO2R8. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких кожний R5 незалежно вибраний з групи, що складається з С1-6алк(ен/ін)ілу, атома галогену і -SO2R8 , де R8 являє собою арил. У ще одному варіанті здійснення принаймні один замісник R5 являє собою С 1-6-алк(ен/ін)іл. У ще одному варіанті здійснення принаймні один замісник R5 являє собою арил. У ще одному варіанті здійснення принаймні один замісник R5 являє собою С 1-6-алк(ен/ін)ілокси. У ще одному варіанті здійснення принаймні один замісник R5 являє собою -SO2R8. У ще одному варіанті здійснення принаймні один замісник R5 являє собою атом галогену. У ще одному варіанті здійснення принаймні один замісник R5 являє собою атом галогену, який вибраний з групи, що складається з атомів хлору, брому і йоду. У ще одному варіанті здійснення принаймні один замісник R5 являє собою атом фтору. У ще одному варіанті здійснення принаймні один замісник R5 являє собою атом хлору. У ще одному варіанті здійснення принаймні один замісник R5 являє собою атом брому. У ще одному варіанті здійснення принаймні один замісник R5 являє собою –NR7R7’. У одному варіанті здійснення принаймні один замісник R5 являє собою -NR7R7’; і принаймні один з R7 і R7' являє собою арил або ацил. У одному варіанті здійснення принаймні один замісник R5 являє собою -NR7R7’; і принаймні один з R7 і R7' вибраний з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу і С 38-циклоалк(ен)іл-С 1-6-алк(ен/ін)ілу. 15 79666 У іншому варіанті здійснення принаймні один замісник R5 являє собою -NR7R7’; і принаймні один з R7 і R7' вибраний з групи, що складається з атома водню і С 1-6-алк(ен/ін)ілу. У ще одному варіанті здійснення принаймні один замісник R5 являє собою -NR7R7’; і принаймні один з R7 і R7’ являє собою С 1-6-алк(ен/ін)іл. У ще одному варіанті здійснення принаймні один замісник R5 являє собою -NR7R7’; і обидва R7 і R7' являють собою С 1-6-алк(ен/ін)іл. У одному варіанті здійснення принаймні один замісник R5 являє собою -SO2R8; і R8 являє собою –NR9R9’, де R9 і R9’ незалежно вибрані з групи, що складається з атома водню, С1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу і С 3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу. У одному варіанті здійснення принаймні один замісник R5 являє собою -SO2R8; і R8 вибраний з групи, що складається з С 1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С 1-6алк(ен/ін)ілу і арилу. У ще одному варіанті здійснення принаймні один замісник R5 являє собою -SO2R8; і R8 являє собою арил. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу II. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу III. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу IIb або IIIb. де W, m, n, p і R5 є такими, як визначено вище. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу IIb. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких m дорівнює 0, а Υ має формулу IIb. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу IIIb. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких n дорівнює 0, а Υ має формулу IIIb. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких p дорівнює 0, а Υ має формулу IIIb. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких n дорівнює 0, ρ дорівнює 0, а Υ має формулу IIIb. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу IIIb, а n+p дорівнює 1, та в його конкретному аспекті n дорівнює 1, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 0, а р дорівнює 1. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу 16 IIIb, а n+ρ дорівнює 2, та в його конкретному аспекті n дорівнює 2, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 1, і p дорівнює 1. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формули lIb1, lIb2, lIb3, IIIb 1, IIIb2 , IIIb3 або IIIb4 , що представлені нижче де: W є таким, як визначено вище; r дорівнює 0,1 або 2; s дорівнює 0, 1, 2 або 3; і R5 і R5" незалежно мають значення, як R5, і кожний R5 незалежно є таким, як визначено вище. У ще одному варіанті здійснення винахід відноситься до таких сполук, де: - m дорівнює 0, a Y має формулу llb; або - n дорівнює 0, а Υ має формулу lllb; або - p дорівнює 0, а Υ має формулу lllb; або - n дорівнює 0, p дорівнює 0, а Υ має формулу lllb; або - Υ має формулу lllb, а n+p дорівнює 1, та в його конкретному аспекті n дорівнює 1, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 0, а р дорівнює 1; або - Υ має формулу lllb, а n+p дорівнює 2, та в його конкретному аспекті n дорівнює 2, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 1, і p дорівнює 1; або - Υ має формулу llb1, або llb2, або llb3, або lllb1, або lllb2, lllb3, або lllb4. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу 17 79666 llb1, або llb2, або llb3, або в яких m дорівнює 0, a Y має формулу llb. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу llb1. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу llb2. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу llb3. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких: - Υ має формулу lllb1, або lllb2, або lllb3, або 4 lllb ; або - n дорівнює 0, а Υ має формулу lllb; або - p дорівнює 0, а Υ має формулу lllb; або - n дорівнює 0, p дорівнює 0, а Υ має формулу lllb; або - Υ має формулу lllb, а n+p дорівнює 1, та в його конкретному аспекті n дорівнює 1, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 0, а р дорівнює 1; або - Υ має формулу lllb, а n+p дорівнює 2, та в його конкретному аспекті n дорівнює 2, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 1, і p дорівнює 1. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу lllb1. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу lllb2. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу lllb3. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу lllb4. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу llс або lllс. де W, m, n, p і R5 є такими, як визначено вище. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу llс. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких m дорівнює 0, а Υ має формулу llс. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу lllс. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких n дорівнює 0, a Y має формулу lllс. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких p дорівнює 0, a Y має формулу lllс. 18 У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких n дорівнює 0, p дорівнює 0, a Y має формулу lllс. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу lllс, а n+p дорівнює 1, та в його конкретному аспекті n дорівнює 1, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 0, а р дорівнює 1. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу lllс, а n+p дорівнює 2, та в його конкретному аспекті n дорівнює 2, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 1, і p дорівнює 1. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу llс1, llс2, llс3, lllс1, lllс2, lllс3 або lllс4, які представлені нижче: де: W є таким, як визначено вище; r дорівнює 0, 1 або 2; s дорівнює 0, 1, 2 або 3; і R5 і R5" незалежно мають значення як R5, а кожний R5 незалежно є таким, як визначено вище. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких: - m дорівнює 0, a Y має формулу llс; або - n дорівнює 0, a Y має формулу lllс; або - p дорівнює 0, a Y має формулу lllс; або - n дорівнює 0, p дорівнює 0, a Y має формулу lllс; або - Υ має формулу lllс, а n+p дорівнює 1, та в його конкретному аспекті n дорівнює 1, а р дорівнює 19 79666 0, та в його іншому конкретному аспекті n дорівнює 0, а р дорівнює 1; або - Υ має формулу lllс, а n+p дорівнює 2, та в його конкретному аспекті n дорівнює 2, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 1, і p дорівнює 1; або - Υ має формулу llс1, або llс2, або llс3, або lllс1, 2 lllс , або lllс3, або lllс4. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу llс1, або llе2, або llс3, або m дорівнює 0, a Y має формулу llc. У ще одному варіанті здійснення винахід відноситься до таки х сполук, в яких Υ має формулу llc1. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу llc2. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу llc3. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких: - Υ має формулу lllс1, або lllс2, або lllс3, або 4 lllс ; або - n дорівнює 0, a Y має формулу lllс; або - p дорівнює 0, a Y має формулу lllс; або - n дорівнює 0, p дорівнює 0, a Y має формулу lllс; або - Υ має формулу lllс, а n+p дорівнює 1, та в його конкретному аспекті n дорівнює 1, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 0, а р дорівнює 1; або - Υ має формулу lllс, а n+p дорівнює 2, та в його конкретному аспекті n дорівнює 2, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 1, і p дорівнює 1. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу lllс1. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу lllс2. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу lllс3. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ має формулу lllс4. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких r дорівнює 0. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких r дорівнює 1. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких r дорівнює 2. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких s дорівнює 0. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких s дорівнює 1, 2 або 3. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ формули II являє собою: - llb1, або llb2, або llb3, або llс1, або llс2, або llc3; або 20 - груп у формули llb, де m дорівнює 0; або - груп у формули llс, де m дорівнює 0. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ формули II являє собою: - llb1, або llb2, або llb3; або - груп у формули llb, де m дорівнює 0; або - груп у формули llc, де m дорівнює 0. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ формули III являє собою: - lllb1, або lllb2, або lllb3, або lllb4, або lllс1, або 2 lllс , або lllс3, або lllс4; або - груп у формули lllb, де n дорівнює 0; або - груп у формули lllb, де p дорівнює 0; або - групу формули lllb, де n дорівнює 0, і p дорівнює 0; або - груп у формули lllb, де n+p дорівнює 1, та в його конкретному аспекті n дорівнює 1, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 0, а р дорівнює 1; або - Υ має формулу lllb, а n+p дорівнює 2, та в його конкретному аспекті n дорівнює 2, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 1, і p дорівнює 1; - груп у формули lllс, де n дорівнює 0; або - груп у формули lllс, де p дорівнює 0; або - групу формули lllс, де n дорівнює 0, і p дорівнює 0; або - груп у формули lllс, де n+p дорівнює 1, та в його конкретному аспекті n дорівнює 1, а р дорівнює 0, та в його іншому конкретному аспекті n дорівнює 0, а р дорівнює 1; або - Υ має формулу lllс, а n+p дорівнює 2, та в його конкретному аспекті n дорівнює 2, а р дорівнює 0, та і в його іншому конкретному аспекті n дорівнює 1, і p дорівнює 1. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких Υ формули III являє собою: - Illb2 або Ніс3; або - групу формули Illb, де n дорівнює 0, і р дорівнює 0; або - групу формули lllс, де n дорівнює 0, і p дорівнює 0. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких m дорівнює 0, а Υ має формулу II, та в його конкретних аспектах Υ має формулу llb або llс. У ще одному варіанті здійснення m дорівнює 1, a Y має формулу II, та в його конкретному аспекті Υ має формулу llb, та в його конкретніших аспектах Υ має формулу llb 1, llb2 або llb3. У ще одному варіанті здійснення m дорівнює 1, і R5 вибраний з групи, що складається з С1-6алк(ен/ін)ілу і атома галогену, і Υ має формулу II, та в його конкретному аспекті Υ має формулу llb, та в його конкретніших аспектах Υ має формулу llb1, llb2 або llb3. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких m дорівнює 1, і R5 являє собою С 1-6-алк(ен/ін)іл, і Υ має формулу II, та в його конкретному аспекті Υ має формулу llb, і в його конкретніших аспектах Υ має формулу llb1 або llb3. 21 79666 У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких m дорівнює 1, і R5 являє собою атом галогену, такий як атом брому, або хлору, або фтору, і Υ має формулу II, та в його конкретному аспекті Υ має формулу llb, та в його конкретніших аспектах Υ має формулу llb1, llb2 або llb3. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких m дорівнює 1, і R5 являє собою атом брому або хлору, і Υ має формулу ll, та в його конкретному аспекті Υ має формулу llb, і в його конкретніших аспектах Υ має формулу llb1, llb2 або llb3. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких m дорівнює 1, і R3 являє собою С 1-6-алк(ен/ін)іл, і Υ має формулу II, та в його конкретному аспекті Υ має формулу llb, і в його конкретніших аспектах Υ має формулу llb1, llb2 або llb3, і вйого найбільш конкретному аспекті Υ має формулу llb3. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких R1 являє собою С1-6-алк(ен/ін)іл, m дорівнює 1, R5 являє собою С16-алк(ен/ін)іл або атом галогену, і Υ має формулу II, та в його конкретному аспекті Υ має формулу llb, і в його конкретнішому аспекті Υ має формулу llb3. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких n дорівнює 0, p дорівнює 0, і Υ має формулу llІ, та в його конкретних аспектах Υ має формулу lllb або lllc. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких n дорівнює 1, і Υ має формулу III, та в його конкретних аспектах Υ має формулу lllb або lllс, і в його конкретніших аспектах Υ має формулу lllb2, lllb3 або lllс2. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких n+p дорівнює 1, і Υ має формулу III, та в його конкретному аспекті Υ має формулу lllс, і в його конкретнішому аспекті Υ має формулу lllс2. У ще одному варіанті здійснення винахід відноситься до таких сполук, в яких n+p дорівнює 2, і Υ має формулу III, та в його конкретному аспекті Υ має формулу lllb, і в його конкретніших аспектах Υ має формулу lllb2 або lllb3. У ще одному варіанті здійснення Υ не має формулу II, коли W являє собою атом кисню. У ще одному варіанті здійснення сполука формули І містить не більше, ніж 3 арильні групи, як визначено тут. Сполуки з наступного переліку та їх фармацевтично прийнятні солі є кращими: Етиловий естер {2-аміно-4-[(5-хлортіофен-2ілметил)метиламіно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(5-хлортіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(5-метилтіофен-2ілметил)метиламіно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(5-бромтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(6-хлор-3метоксибензо[b]тіофен-2-ілметил)аміно] феніл}карбамінової кислоти; 22 Етиловий естер {2-аміно-4-[(бензо[b]тіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(5-метилтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(4-бром-3метокситіофен-2-ілметил)аміно]феніл}карбамінової кислоти; Етиловий естер {2-аміно-4-[(5-фенілтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(3-хлортіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер (2-аміно-4-{[4-(4хлорбензолсульфоніл)-3-метилтіофен-2ілметил]аміно}феніл)-карбамінової кислоти; Етиловий естер {2-аміно-4-[(3-метилтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(5фторбензофуран-3-ілметил)аміно]феніл}карбамінової кислоти; Етиловий естер {2-аміно-4-[(тіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(4-бромтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(5-етилтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(тіофен-3ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(5-хлортіофен-2ілметил)етиламіно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(бензо[b]тіофен-3ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(5диметиламінобензо[b]тіофен-3ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(5-диметиламіно-3метилбензо[b]тіофен-2-ілметил)аміно]феніл}карбамінової кислоти; Етиловий естер {2-аміно-4-[(5-фтортіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Пропіловий естер {2-аміно-4-[(бензо[b]тіофен2-ілметил)аміно]феніл}-карбамінової кислоти; Пропіловий естер {2-аміно-4-[(бензо[b]тіофен3-ілметил)аміно]феніл}-карбамінової кислоти; N-{2-Аміно-4-[(5-хлортіофен-2ілметил)аміно]феніл}-2-(4-фторфеніл)ацетамід і N-{2-Аміно-4-[(5-хлортіофен-2ілметил)аміно]феніл}-3,3-диметилбутирамід. У конкретному аспекті сполуки з наступного переліку і їх фармацевтично прийнятні кислотноадитивні солі є кращими: Етиловий естер {2-аміно-4-[(5-хлортіофен-2ілметил)метиламіно]феніл}-карбамінової кислоти Етиловий естер {2-аміно-4-[(5-хлортіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(5-метилтіофен-2ілметил)метиламіно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(5-бромтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(6-хлор-3метоксибензо|b]тіофен-2-ілметил)аміно]феніл}карбамінової кислоти; Етиловий естер {2-аміно-4-[(бензо)[b]тіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(5-метилтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; 23 79666 Етиловий естер {2-аміно-4-[(4-бром-3метокситіофен-2-ілметил)аміно]феніл}карбамінової кислоти; Етиловий естер {2-аміно-4-[(5-фенілтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(3-хлортіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер (2-аміно-4-{[4-(4хлорбензолсульфоніл)-3-метилтіофен-2ілметил]аміно}феніл)-карбамінової кислоти; Етиловий естер {2-аміно-4-[(3-метилтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(5фторбензофуран-3-ілметил)аміно]феніл}карбамінової кислоти; Етиловий естер (2-аміно-4-[(тіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(4-бромтіофен-2ілметил)аміно]феніл}-карбамінової кислоти Етиловий естер {2-аміно-4-[(5-етилтіофен-2ілметил)аміно]феніл}-карбамінової кислоти; Етиловий естер {2-аміно-4-[(тіофен-3ілметил)аміно]феніл}-карбамінової кислоти і Етиловий естер {2-аміно-4-[(5-хлортіофен-2ілметил)етиламіно]феніл}-карбамінової кислоти. У одному аспекті винаходом пропонується фармацевтична композиція, що містить принаймні одну сполуку формули І, як визначено вище, або її фармацевтично прийнятну сіль в терапевтично ефективній кількості разом з одним або більше фармацевтично прийнятними носіями або розріджувачами. У одному конкретному аспекті винаходом пропонується фармацевтична композиція, що містить принаймні одну сполуку формули І, як визначено вище, або її фармацевтично прийнятну кислотноадитивну сіль в терапевтично ефективній кількості разом з одним або більше фармацевтично прийнятними носіями або розріджувачами. Винаходом пропонується фармацевтична композиція для перорального або парентерального введення, де вказана фармацевтична композиція містить принаймні одну сполуку формули І або її сіль в терапевтично ефективній кількості разом з одним або більше фармацевтично прийнятними носіями або розріджувачами. У одному варіанті здійснення сполуку за винаходом можна вводити як тільки одну терапевтично ефективну сполуку. У іншому варіанті здійснення сполуку за винаходом можна вводити як частину комбінованої терапії, тобто сполуку за винаходом можна вводити в комбінації з іншими терапевтично ефективними сполуками, що мають, наприклад, антиконвульсивні властивості. Ефекти таких інши х сполук, що мають антиконвульсивні властивості, можуть включати, але не обмежуватися тільки ними, активність у відношенні: - іонних каналів, таких як натрієвий, калієвий або кальцієвий канали; - збудливих амінокислотних систем, наприклад, блокадою або модуляцією NMDAрецепторів; 24 - інгібіторних систем нейромедіаторів, наприклад, при посиленні вивільнення ГАМК або блокаді поглинання ГАМК і/або - ефектів стабілізації мембрани. Антиконвульсивні препарати, що є в даний час, включають, але не обмежуються тільки ними, тіагабін, карбамазепін, вальпроат натрію, ламотригін, габапентин, прегабалін, етосуксимід, леветирацетам, фенітоїн, топірамат, зонісамід, а також члени групи бензодіазепіну і барбітуратів. Сполуки за винаходом розглядаються як придатні для збільшення іонного потоку у потенціалозалежному калієвому каналі. Сполуки за винаходом розглядаються як придатні для профілактики, лікування і/або пригнічення розладу або стану, реактивного на підвищений іонний потік в калієвому каналі, такому як калієві іонні канали сімейства KCNQ. У одному аспекті було встановлено, що сполуки за винаходом впливають на калієві канали сімейства KCNQ, зокрема, на субодиницю KCNQ2. Згідно з одним аспектом, сполуки за винаходом розглядаються як придатні для профілактики, лікування і/або пригнічення різних розладів центральної нервової системи, таких як судомні напади, такі як конвульсії, епілепсія та епілептичний статус; тривожні розлади, такі як страх, генералізований тривожний розлад, панічна тривога, обсесивно-компульсивний розлад, соціальна фобія, страх діяльності, посттравматичний стресовий розлад, гостра стресова реакція, розлад пристосовування, іпохондричні розлади, страх розлуки, агорафобія та специфічні фобії. Отже, сполуки за винаходом розглядаються як придатні для профілактики, лікування і/або пригнічення різних розладів центральної нервової системи, таких як: - судомні напади, такі як конвульсії, епілепсія та епілептичний статус; - невропатичний біль, такий як алодинія, гіпералгічний біль, фантомний біль, невропатичний біль, пов'язаний з діабетичною невропатією, і невропатичний біль, пов'язаний з мігренню; - тривожні розлади, такі як страх, генералізований тривожний розлад, панічна тривога, обсесивно-компульсивний розлад, соціальна фобія, страх діяльності, посттравматичний стресовий розлад, гостра стресова реакція, розлад пристосовування, іпохондричні розлади, страх розлуки, агорафобія, специфічні фобії; - нейродегенеративні захворювання, такі як хвороба Альцгеймера, хорея Гентінгтона, розсіяний склероз, аміотрофічний бічний склероз, індукована СНІДом енцефалопатія та інші пов'язані з інфекціями енцефалопатії, викликані вірусами коревої краснухи (rubella вірусами), герпесвірусами, спірохетами і невідомими патогенами, хвороба Крейтцфельда-Якоба, хвороба Паркінсона, викликані травмою нейродегенерації; - стани гіперзбудження нейронів, такі як ті, що виникають при відміні препаратів, або такі, що викликані інтоксикацією, нейродегенеративні захворювання периферичної нервової системи, такі як поліневропатії і поліневрити. 25 79666 Отже, сполуки за винаходом розглядаються як придатні для профілактики, лікування і/або пригнічення розладів або станів, таких як судомні напади, невропатичні болі і мігрень, тривожні розлади і нейродегенеративні захворювання. Згідно з одним конкретним аспектом, сполуки за винаходом розглядаються як придатні для профілактики, лікування і/або пригнічення судомних нападів, таких як конвульсії, епілепсія та епілептичний статус. Згідно з іншим конкретним аспектом, сполуки за винаходом розглядаються як придатні для профілактики, лікування і/або пригнічення невропатичних болів і мігрені, таких як алодинія, гіпералгічний біль, фантомний біль, невропатичний біль, пов'язаний з діабетичною невропатією, і невропатичний біль, пов'язаний з мігренню. Додатково сполуки за винаходом розглядаються як придатні для профілактики, лікування і/або пригнічення тривожних розладів, таких як страх, генералізований тривожний розлад, панічна тривога, обсесивно-компульсивний розлад, соціальна фобія, страх діяльності, посттравматичний стресовий розлад, гостра стресова реакція, розлад пристосовування, іпохондричні розлади, страх розлуки, агорафобія, тривожний розлад як наслідок загального хворобливого стану або тривожний розлад, викликаний хімічними речовинами та специфічні фобії. Додатково сполуки за винаходом розглядаються як придатні для профілактики, лікування і/або пригнічення нейродегенеративних захворювань, таких як хвороба Альцгеймера, хорея Гентінгтона, розсіяний склероз, аміотрофічний бічний склероз, індукована СНІДом енцефалопатія та інші пов'язані з інфекціями енцефалопатії, викликані вірусами коревої краснухи, герпесвірусами, спірохетами і невідомими патогенами, хвороба Крейтцфельда-Якоба, хвороба Паркінсона, викликана травмою нейродегенерація і стани гіперзбудження нейронів, такі як ті, що виникають при відміні препаратів, або такі, що викликані інтоксикацією. У іншому аспекті винаходом пропонуються сполуки, що демонструють ефект в одному або більше з наступних тестів: - "відносний потік через канал KCNQ2", який є показником активності сполуки відносно каналу-мішені; - "максимальний електрошок", який є показником судомних нападів, індукованих неспецифічною стимуляцією ЦНС електрикою; - "індуковані пілокарпіном судомні напади", індуковані пілокарпіном судомні напади часто важко лікувати багатьма наявними протисудомними препаратами і, таким чином, вони є моделлю "стійких до препаратів судомних нападів"; - "електричні тести по встановленню судомного порогу" і "хімічні тести по встановленню судомного порогу". На даних моделях визначають поріг, при якому виникають судомні напади, таким чином, на даних моделях визначають, наскільки сполуки можуть уповільнювати розвиток судом; - "стимуляція мигдалика", 26 який використовується як показник прогресування захворювання, оскільки у здорових тварин судоми на даній моделі стають більш суворими при додатковій стимуляції тварин. Згідно з одним конкретним аспектом винаходу, сполуки є активними у відношенні KCNQ2 із значенням ЕС50 менше 15000нМ за даними тесту "відносний потік через канал KCNQ2", який описаний нижче. Згідно з одним конкретним аспектом винаходу, сполуки є активними у відношенні KCNQ2 із значенням ЕС50 менше 1500нМ за даними тесту "відносний потік через канал KCNQ2", який описаний нижче. Згідно з іншим конкретним аспектом винаходу, сполуки є активними у відношенні KCNQ2 із значенням ЕС50 менше 150нМ заданими тесту "відносний потік через канал KCNQ2", який описаний нижче. Згідно з іншим конкретним аспектом винаходу, сполуки мають значення ED50 менше 15мг/кг за тестом "максимальний електрошок", який описаний нижче. Згідно з ще іншим конкретним аспектом винаходу, сполуки мають значення ED50 менше 5мг/кг за тестом "максимальний електрошок", який описаний нижче. Згідно з одним конкретним аспектом винаходу, сполуки мають значення ED50 менше 5мг/кг за "електричним тестом по встановленню судомного порогу" і/або за "хімічним тестом по встановленню судомного порогу", які описані нижче. Деякі сполуки мають незначні або клінічно малозначимі побічні ефекти. Таким чином, деякі сполуки протестовані на моделях стосовно небажаної седативної, гіпотермічної і атаксичної дії цих сполук. Деякі сполуки мають таке значення відповідного періоду напіввиведення або відповідного кліренсу, що пацієнтам потрібно приймати пігулки, наприклад, один або двічі на день. Пацієнти легко запам'ятовують це, і, таким чином, це сприяє кращому сприйняттю лікування препаратом. Деякі сполуки мають високий терапевтичний індекс між протисудомною дією і побічними ефектами, такими як порушення рухової активності або атаксичні ефекти, що визначають постановкою "тесту на стрижні, що обертається". Це означає, що сполуки, як і слід було чекати, добре будуть переноситися пацієнтами, що дозволить використовувати високі дози до прояву побічних ефектів. При цьому сприйняття лікування буде гарним, і введення високих доз дозволить зробити лікування ефективнішим у пацієнтів з побічними ефектами від інших препаратів. Визначення Термін "гетероатом" відноситься до атомів азоту, кисню або сірки. Атом галогену означає атоми фтору, хлору, брому або йоду. Вираз "С1-6-алк(ен/ін)іл" означає C1-6-алкіл, С26-алкеніл або С 2-6-алкініл. Термін "С1-6-алкіл" відноситься до розгалуженого або нерозгалуженого алкілу, що містить 1-6 атомів вуглецю включно, включаючи але не обме 27 79666 жуючись тільки ними, метил, етил, 1-пропіл, 2пропіл, 1-бутил, 2-бутил, 2-метил-2-пропіл, 2,2диметил-1-пропіл і 2-метил-1-пропіл. Аналогічно "C1-6-алкеніл" і "C1-6-алкініл" відповідно означають такі групи, які містять 2-6 атомів вуглецю, що включають один подвійний зв'язок і один потрійний зв'язок, відповідно, включаючи але не обмежуючись тільки ними, етеніл, пропеніл, бутеніл, етиніл, попініл і бутиніл. Вираз "С3-8-циклоалк(ен)іл" означає С3-8циклоалкіл- або циклоалкеніл. Термін "С3-8-циклоалкіл" означає моноциклічний або біциклічний карбоцикл, що містить 3-8 Сатомів, включаючи але не обмежуючись тільки ними, циклопропіл, циклопентил, циклогексил тощо. Термін "С3-8-циклоалкеніл" означає моноциклічний або біциклічний карбоцикл, що містить 3-8 Сатомів і включає один подвійний зв'язок. Коли два замісники разом з атомом азоту, з яким вони зв'язані, утворюють 4-8-членне насичене або ненасичене кільце, яке необов'язково містить 1, 2 або 3 додаткові гетероатоми, тоді моноциклічна кільцева система утворена 4-8 атомами, вибраними з атома азоту, 1-7 атомів вуглецю і 0-3 гетероатомів, вибраних з N, S або О. Прикладами таких кільцевих систем є азетидин, бета-лактам, піролідин, піперидин, піперазин, морфолін, пірол, оксазолідин, тіазолідин, імідазолідин, тетразол і піразол. Термін "арил" відноситься до ароматичних систем, таких як піридин, тіазол, оксазол, феніл, нафтил, тіо фен і фуран, які необов'язково заміщені одним або більше замісниками, що незалежно являють собою гідрокси, атом галогену, С1-6алк(ен/ін)іл, С3-8-циклоалк(ен)іл, С3-8циклоалк(ен)іл-С 1-6-алк(ен/ін)іл, галоген-С 1-6алк(ен/ін)іл, С1-6-алкокси, С3-8-алкокси, ацил, нітро або ціано, -СО-NH-С1-6-алк(ен/ін)іл, -CO-N(C1-6алк(ен/ін)іл)2, -NН-С1-6-алк(ен/ін)ілу, -N(С1-6алк(ен/ін)іл)2, -S-С1-6-алк(ен/ін)іл, -SO2-C1-6алк(ен/ін)іл, -SО2О-С1-6-алк(ен/ін)іл, -NH2, SО2Н(С1-6-алк(ен/ін)іл)2 або -SO2NH-C1-6алк(ен/ін)іл; або два суміжні замісники разом з ароматичною групою, з якою вони зв'язані, можуть утворювати 4-8-членне кільце, яке необов'язково містить один або два гетероатоми. Коли два суміжні замісники разом з ароматичною групою, з якою вони зв'язані, утворюють 4-8членне кільце, яке необов'язково містить один або два гетероатоми, тоді кільцева система утворена 4-8-атомами, вибраними з 3-8 атомів вуглецю і 0-2 гетероатомів, вибраних з N, S або О. Такі два суміжні замісники можуть разом утворити: -(CH2) n”CH2-, -CH=CH-(CH 2)m”-, -СН2-СН=СН-(СН2)р”-, -СН=СН-СН=СН -, -(CH2)n”-O-, -О-(СН2)m”-О-, -СН2О-(СН2)р”-О-, -СН2-О-СН2-О-СН2-, -(СН2)n"-S-, -S(CH2)m”-S-, -CH2-S-(CH2)p”-S-, -СН2-S-СН2-S-СН2-, -(CH2)n”-NH-, -NH-(CH 2)m”-NH-, -CH2-NH-(CH2)p”-NH-, -CH=CH-NH-, -O-(CH 2)m”-NH-, -CH2-O-(CH2)p”-NH або -O-(CH2)p*-9+ ” -NH-CH2-, -S-(CH2)m”-NH-, -N=CH-NH-, -N=CH-O- або -N=CH-S-, де m" дорівнює 1, 2 або 3, n" дорівнює 2, 3 або 4, та р" дорівнює 1 або 2. 28 У тому сенсі, як використано тут, термін "ацил" відноситься до формілу, С1-6-алк(ен/ін)ілкарбонілу, С3-8-циклоалк(ен)ілкарбонілу, арилкарбонілу, арилСі-6-алк(ен/ін)ілкарбонілу або С3-8-циклоалк(ен)ілС1-6-алк(ен/ін)ілкарбонілу, де С 1-6-алк(ен/ін)іл, С3-8циклоалк(ен)іл і арил є такими, як визначено вище. Термін "галоген-С1-6-алк(ен/ін)іл" означає С1-6алк(ен/ін)іл, заміщений одним або більше атомами галогену, включаючи, але не обмежуючись тільки ним, трифторметил. Аналогічно "галоген-С3-8циклоалк(ен)іл" означає С3-8-циклоалк(ен)іл, заміщений одним або більше атомами галогену, і галоген-С 3-8-циклоалк(ен)іл-С 1-6-алк(ен/ін)іл означає С 38-циклоалк(ен)іл-С 1-6-алк(ен/ін)іл, заміщений одним або більше атомами галогену. У терміні "С3-8-циклоалк(ен)іл-С 1-6-алк(ен/ін)іл", С3-8-циклоалк(ен)іл і С 1-6-алк(ен/ін)іл є такими, як визначено вище. Крім того, терміни, такі як "гідрокси-С1-6алк(ен/ін)іл", "гідрокси-С 3-8-циклоалк(ен)іл", "арилС1-6-алк(ен/ін)іл", "С1-6-алк(ен/ін)ілокси", "С3-8циклоалк(ен)ілокси", "С1-6-алк(ен/ін)ілкарбоніл", "С3-8-циклоалк(ен)ілкарбоніл", "арилкарбоніл", "арил-С 1-6-алк(ен/іл)ілкарбоніл", "С3-8циклоалк(ен)іл-С 1-6-алк(ен/ін)ілкарбоніл", "арил-С38-циклоалк(ен)іл", "гідрокси-С 3-8-циклоалк(ен)іл-С 1"гідрокси-С 1-6-алк(ен/іл)іл-С 3-86-алк(ен/ін)іл", циклоалк(ен)іл", "ціано-С1-6-алк(ен/ін)іл", ціано-С 3-8циклоалк(ен)іл", "вдано-С 3-8-циклоалк(ен)іл-С 1-6алк(ен/іл)іл", "NR10R10-C1-6-алк(ен/ін)іл" і "NR10R10С3-8-циклоалк(ен)іл" тощо означають групи, в яких С1-6-алк(ен/ін)іл, С3-8-циклоалк(ен)іл і арил є такими, як визначено вище. Солі за винаходом переважно є фармацевтично прийнятними солями. Такі солі включають фармацевтично прийнятні кислотно-адитивні солі, фармацевтично прийнятні солі металів, солі амонію і алкілованого амонію. Фармацевтично прийнятні солі за винаходом переважно є кислотно-адитивними солями. Кислотно-адитивні солі включають солі неорганічних кислот, а також органічних кислот. Кислотно-адитивні солі за винаходом переважно є фармацевтично прийнятними солями сполук за винаходом, утвореними нетоксичними кислотами. Прикладами таких солей органічних кислот є солі, одержані з малеїновою, фумаровою, бензойною, аскорбіновою, бурштиновою, щавлевою, бісметиленсаліциловою, метансульфоновою, етандисульфоновою, оцтовою, пропіоновою, винною, саліциловою, лимонною, глюконовою, молочною, яблучною, мигдалевою, коричною, цитраконовою, аспарагіновою, стеариновою, пальмітиновою, ітаконовою, гліколевою, п-амінобензойною, глутаміновою, бензолсульфоновою і теофіліноцтовою кислотами, а також з 8-галогентеофілінами, наприклад, 8-бромтеофіліном. Прикладами таких солей неорганічних кислот є солі, одержані з соляною, бромистоводневою, сірчаною, сульфаміновою, фосфорними і азотними кислотами. Такі кислотно-адитивні солі можна одержати за способами, відомими фахівцям в даній галузі. Додаткові приклади фармацевтично прийнятних адитивних солей неорганічної або ор 29 79666 ганічної кислоти включають фармацевтично прийнятні солі, перелічені в J. Pharm. Sci. 1977, 66, 2, який включено сюди шляхом посилання. Також призначеними як фармацевтично прийнятні кислотно-адитивні солі є гідрати, які здатні утворити ці сполуки. Крім того, якщо в молекулі є подвійний зв'язок або повністю або частково насичена кільцева система, то можуть бути одержані геометричні ізомери. Мається на увазі, що будь-які геометричні ізомери, виділені, чисті або частково очищені геометричні ізомери або їх суміші включені в обсяг цього винаходу. Аналогічно молекули, що мають зв'язок з обмеженим обертанням, можуть утворювати геометричні ізомери. Вони також призначені до включення в обсяг цього винаходу. Крім того, деякі сполуки за цим винаходом можуть знаходитися в різних таутомерних формах, і мається на увазі, що будь-які таутомерні форми, які здатні утворити сполуки, включені в обсяг цього винаходу. Крім того, сполуки за даним винаходом можуть знаходитися в несольватованих, а також в сольватованих формах з фармацевтично прийнятними розчинниками, такими як вода, етанол і тому подібне. Як правило, сольватовані форми розглядаються як рівноцінні з несольватованими формами для цілей винаходу. Деякі зі сполук за цим винаходом містять хіральні центри, і такі сполуки знаходяться у формі ізомерів (тобто енантіомерів). Винахід включає всі такі ізомери та їх будь-які суміші, включаючи рацемічні суміші. Рацемічні форми можна розділити на оптичні антиподи за відомими способами, наприклад, розділенням їх діастереоізомерних солей за допомогою оптично активної кислоти і виділенням оптично активного аміну обробкою основою. Інший метод розділення рацематів на оптичні антиподи заснований на хроматографії на оптично активній матриці. Рацемічні сполуки за цим винаходом можна також розділити на їх оптичні антиподи, наприклад, фракційною кристалізацією d- або 1тартратів, манделатів або камфорсульфонатів. Сполуки за цим винаходом можна також розділити отриманням діастереоізомерних похідних. Можна використовува ти додаткові способи розділення оптичних ізомерів, відомі фахівцям в даній галузі. Такі способи включають ті, [що описані у J. Jaques, A. Collet and S. Wilen в "Enantiomers, Racemates, and Resolutions", John Wiley and Sons, New York (1981)]. Оптично активні сполуки можна також одержати з оптично активних початкових речовин. Винахід також включає проліки цих сполук, які при введенні зазнають хімічне перетворення в результаті метаболічних процесів перед тим, як вони перетворюються на фармакологічно активні сполуки. В основному такими проліками будуть функціональні похідні сполук загальної формули І, які легко перетворюються in vivo в необхідні сполуки формули І. Описані загальноприйняті методи відбору і одержання відповідних проліків, [наприклад, в "Design of Prodrugs", ed. H.Bundgaard, Elsevier, 1985]. 30 Винахід також включає активні метаболити цих сполук. При їх використанні по відношенню до сполук формули І терміни "епілепсія" і "епілепсії" включають будь-які епілепсії, епілептичні синдроми і епілептичні напади, наявні в [International League Against Epilepsy: Proposal for revised clinical and electrocephalographic classification of epileptic seizures. Commission on Classification, і в Terminology of the International League Against Epilepsy. Epilepsia 1981, 22: 489-501, і в International League Against Epilepsy: Proposal for revised classification of epilepsies and epileptic syndromes. Commission on Classification and Terminology of the International League Against Epilepsy. Epilepsia 1989, 30(4): 389399]. Фармацевтичні композиції Сполуки за цим винаходом в основному застосовуються у вигляді вільної основи або у вигляді її фармацевтично прийнятної солі. Типові приклади згадані вище. Якщо бажано, то фармацевтична композиція за винаходом може містити сполуку формули І в комбінації з додатковими фармакологічно активними сполуками, такими як описані нижче. Фармацевтичні композиції можуть бути спеціально складені для введення будь-яким відповідним шляхом, таким як пероральний, ректальний, інтраназальний, інгаляційний, місцевий (включаючи букальний і сублінгвальний), трансдермальний, інтрацистернальний, внутрішньочеревинний, інтравагінальний і парентеральний (включаючи підшкірний, внутрішньом'язовий, інтратекальний, внутрішньовенний і внутрішньошкірний) шляхи, переважним є пероральний шлях введення. Фахівцям зрозуміло, що переважний шлях залежатиме від загального стану і віку суб'єкта, який піддається лікуванню, природи стану, який лікується, і вибраного активного інгредієнта. Фармацевтичні композиції за цим винаходом або такі, які одержують згідно з цим винаходом, можна вводити будь-яким відповідним шляхом, наприклад, перорально у формі пігулок, капсул, порошків, гранул, пілюльок, драже, пілюль або коржиків, розчинів або суспензій у водних або неводних рідинах або рідких емульсіях олія-в-воді або вода-в-олії, еліксирів, сиропів тощо, або парентерально у формі розчинів для ін'єкцій. Інші фармацевтичні композиції для парентерального введення включають дисперсії, суспензії або емульсії, а також стерильні порошки для відновлення в стерильних ін'єкційних розчинах або дисперсіях перед застосуванням. Також в обсяг цього винаходу включаються ін'єкційні композиції-депо. Інші відповідні форми для введення включають супозиторії, спреї, мазі, креми, гелі, аерозолі, дермальні пластири, імплантати тощо. Для отримання таких композицій можна використовувати методи, добре відомі в даній галузі, і можна використовувати будь-які фармацевтично прийнятні носії, розріджувачі, наповнювачі або інші добавки, звичайно використовувані в даній галузі. Звичайно сполуки за винаходом вводять в стандартній лікарській формі, що містить вказані сполуки в кількості приблизно 0,01-100мг. Як пра 31 79666 вило, загальна добова доза знаходиться в межах приблизно 0,05-500мг, або навіть 0,05-1500мг, або 0,05-3000мг, а найбільш переважно біля 0,1-50мг активної сполуки за винаходом. Звичайно для парентеральних шляхів введення, таких як внутрішньовенний, інтратекальний, внутрішньом'язовий, і для аналогічного введення дози знаходяться на рівні приблизно половини від дози, використовуваної для перорального введення. Сполуки за винаходом можна вводити самостійно або в комбінації з фармацевтично прийнятними носіями або наповнювачами в одній або множинних дозах. Фармацевтичні композиції за винаходом можна складати з використанням фармацевтично прийнятних носіїв або розріджувачів, а також будь-яких інших відомих ад'ювантів і ексципієнтів згідно зі звичайними методами, [наприклад, розкритими в Remington: The Science and Practice of Pharmacy, 19 Edition, Gennaro, Ed., Mack Publishing Co., Easton, PA, 1995]. Композиції звичайно можуть бути представлені в стандартній дозованій формі з використанням методів, відомих у галузі фармації. Можна використовувати будь-які інші ад'юванти або добавки, звичайно вживані для даних цілей, такі як фарбники, ароматизатори, консерванти тощо, за умови, що вони сумісні з активними інгредієнтами. Фармацевтичні композиції за цим винаходом можна одержати з використанням загальноприйнятих в даній галузі методів. Наприклад, таблетки можна одержати змішуванням активного інгредієнта із звичайними ад'ювантами і/або розріджувачами і потім пресуванням суміші у звичайній таблетувальній машині. Приклади ад'ювантів або розріджувачів включають: кукурудзяний крохмаль, картопляний крохмаль, тальк, стеарат магнію, желатин, лактозу, камедь тощо. Можна використовувати будь-які інші ад'юванти або добавки, які звичайно використовують для даних цілей, такі як фарбники, ароматизатори, консерванти тощо, за умови, що вони сумісні з активними інгредієнтами. У тих випадках, коли це є відповідним, то можна приготувати тверду лікарську форму з покриттям, таким як ентеросолюбільне покриття, або їх можна скласти для забезпечення контрольованого вивільнення активного інгредієнта, наприклад, безперервного або тривалого вивільнення, згідно з методами, добре відомими в даній галузі. Якщо використовується рідкий носій, то препарат може знаходитися у формі сиропу, емульсії, м'якої желатинової капсули або стерильного ін'єкційного розчину, такого як суспензія або розчин у водній або неводній рідині. Для парентерального введення можна використовувати розчини нових сполук за цим винаходом в стерильному водному розчині, водному розчині пропіленгліколю, водному розчині вітаміну Ε або кунжутній або арахісовій олії. Розчини для ін'єкцій можна приготува ти розчиненням активного інгредієнта і можливих добавок в частині розчинника для ін'єкцій, переважно в стерильній воді, доведенням розчину до бажаного об'єму, стерилізацією розчину і наповненням ним відповідних ампул або флаконів. Можна внести будь-яку від 32 повідну добавку, звичайно використовувану в даній галузі, таку як агенти ізотонічності, консерванти, антиоксиданти тощо. Отже, такі водні розчини повинні бути відповідним чином забуферені, якщо це необхідно, і на початку рідкий розріджувач роблять ізотонічним за допомогою достатньої кількості сольового розчину та глюкози. Водні розчини є особливо придатними для внутрішньовенного, внутрішньом'язового, підшкірного і внутрішньочеревинного введення. Використовувані стерильні водні середовища легко одержати з використанням звичайних методів, відомих фахівцям в даній галузі. Відповідні фармацевтичні носії включають інертні тверді розріджувачі або наповнювачі, стерильний водний розчин і різні органічні розчинники. Прикладами рідких носіїв є сироп, арахісова олія, оливкова олія, фосфоліпіди, жирні кислоти, аміни жирних кислот, поліоксіетилен і вода. Аналогічно, носій або розріджувач може включати будьяку речовину для безперервного вивільнення, відому в даній галузі, таку як гліцерилмоностеарат або гліцерилдистеарат, одну або в суміші з воском. Типовими прикладами рецептури композицій за винаходом є наступні: 1) таблетка, що містить 5,0мг сполуки за цим винаходом в розрахунку на вільну основу: сполука формули І 5,0мг лактоза 60мг кукурудзяний крохмаль 30мг гідроксипропілцелюлоза 2,4мг мікрокристалічна целюлоза 19,2мг натрієва сіль кроскармелози типу А 2,4мг стеарат магнію 0,84мг 2) таблетка, що містить 0,5мг сполуки за цим винаходом в розрахунку на вільну основу: сполука формули І 0,5мг лактоза 46,9мг кукурудзяний крохмаль 23,5мг повідон 1,8мг мікрокристалічна целюлоза 14,4мг натрієва сіль кроскармелози типу А 1,8мг стеарат магнію 0,63мг 3) сироп, що містить на мілілітр: сполука формули І 25мг сорбіт 500мг гідроксипропілцелюлоза 15мг гліцерин 50мг метилпарабен 1мг пропілпарабен 0,1мг етанол 0,005мл ароматизатор 0,05мг натрієва сіль сахарину 0,5мг вода до 1мл 4) розчин для ін'єкцій, що містить на мілілітр: сполука формули І 0,5мг сорбіт 5,1мг оцтова кислота 0,05мг натрієва сіль сахарину 0,5мг вода до 1мл Одержання сполук за винаходом Сполуки за винаходом загальної формули І де R1, R2, R2', R3, Χ, Υ, Ζ і q є такими, як визначено вище 33 79666 одержують за способами, представленими на У подальшому будь-який з R1, R2, R2' , R3, R4 , R , R6, R6' , R7, R7' , R8, R9, R9' , R10, R10' , Χ, Υ, Ζ, W, m, n, p і q є таким, як визначено вище. Сполуки загальної формули VII одержують за способами, відомими хімікам в даній галузі (v. Bebenburg et al. Chemiker Zeitung 1979, Sonderdruck 103, 3-15) і схематично описаними нижче. Сполуки загальної формули IV одержують взаємодією 4-нітроаніліну з відповідними електрофільними реагентами, такими як, але не обмежуючись тільки ними, хлорангідриди кислот, бромангідриди кислот, йодангідриди кислот, сульфонілхлориди, ізоціанати, ангідриди карбонових кислот, активовані естери і алкілгалогенформіати з або без додавання основ, таких як триалкіламіни, карбонат калію або алкоголяти літію, натрію або калію, у відповідному розчиннику, такому як етилацетат, діоксан, тетрагідрофуран, ацетонітрил або діетиловий етер, при відповідній температурі, такій як кімнатна температура або температура кипіння, що досягається звичайним нагріванням або мікрохвильовим опромінюванням, з подальшим відновленням нітрогрупи з використанням відповідного відновника, такого як дитіоніт натрію, порошкоподібне залізо або цинк у водному розчині соляної кислоти або газоподібний водень у присутності відповідного каталізатора для гідрування, такого як паладій на активованому вуглецю, у відповідних розчинниках, таких як метанол або етанол, при відповідній температурі. Сполуки загальної формули V одержують взаємодією сполук загальної формули IV з реагентом, утворюючим захисну гр упу по аніліновій групі, на5 34 схемі та описаними нижче: приклад, з ангідридом фталевої кислоти, у відповідному розчиннику, такому як льодяна оцтова кислота, при відповідній температурі. Сполуки загальної формули VI одержують із сполук загальної формули V реакціями нітрування, відомими фахівцям в даній галузі, такими як реакція з димною азотною кислотою, у відповідному розчиннику, такому як льодяна оцтова кислота, при відповідній температурі. Сполуки загальної формули VII одержують із сполук загальної формули IV зняттям захисту з анілінової функціональної групи гідратом гідразину у відповідному розчиннику, такому як 1,2-діоксан, при відповідній температурі. Альтернативно сполуки загальної формули VII можна одержати з 2-нітро-1,4-діамінобензолу в 3 стадії, як представлено на схемі та описано нижче. На першій стадії менш утр уднений в рухливості та більш реакційноздатний азот аніліну захищають відповідною захисною групою PG [Protecti ve Groups in Organic Synthesis, 3rd Edition T.W.Greene, P.G.M.Wuts, Wiley Interscience, 1999], такою як трет-бутилоксикарбоніл (Вос-група), взаємодією з відповідним реагентом, утворюючим захисну гр упу, наприклад ди-третбутилдикарбонатом, у відповідному розчиннику, такому як ацетонітрил, при відповідній температурі, з одержанням сполук загальної формули XI. Сполуки загальної формули XII одержують із сполук загальної формули XI взаємодією з відповідними електрофільними реагентами, утворюючими R3-(Z)q -X-груп у, таку як алкіл-, арил- або гетероарилхлорформіати або карбамоїлхлориди, хлорангідриди кислот, бромангідриди кислот, йодангідриди кислот, сульфонілхлориди, ізоціанати, ангідриди карбонових кислот, активовані карбонові кислоти, з активуючими реагентами, такими як карбодііміди або інші, відомі хімікам в даній галузі, у відповідних розчинниках, таких як ацетонітрил, тетрагідрофуран, 1,2-дихлоретан або метиленхлорид, при відповідній температурі, такій як кімнатна температура або температура кипіння, що досягається звичайним нагріванням або мікрохвильовим опромінюванням, з або без додавання основи, такої як оксид магнію, карбонат калію, триалкіламіни, піридин або бікарбонат натрію, як описано вище для сполук загальної формули IV. Захисну гр упу видаляють за способами, відомими хімікам в даній галузі. Зокрема, Вос-групу можна відщепити обробкою відповідною кислотою, наприклад, трифтороцтовою кислотою, у відсутності або у присутності розчинника, такого як метиленхлорид або толуол, при відповідній температурі, з одержанням сполук загальної формули VII. Одержання сполук загальної формули VIII Сполуки загальної формули VII піддають реакціям відновного алкілування, відомим хімікам в даній галузі, з альдегідом загальної формули Па або lllа, де R5, W, m, n і p є такими, як визначено вище, з використанням відновників, таких як борогідрид натрію або ціаноборогідрид натрію, у відповідному розчиннику, такому як метанол, етанол, тетрагідрофуран, вода, діоксан або їх суміші, з або без додавання каталітичних кількостей кислоти, 35 79666 такої як оцтова кислота, при відповідній температурі, з одержанням сполук загальної формули VIII, де R1 є атомом водню. Альтернативно сполуки загальної формули VII можна піддати взаємодії з альдегідом загальної формули llа або lllа у відповідному розчиннику, такому як метанол, етанол, тетрагідрофуран, діоксан, ксилол або їх суміші, з або без додавання каталітичних кількостей кислоти, такої як оцтова кислота, або кислої іонообмінної смоли, при відповідній температурі, з утворенням імінів, які можна виділити кристалізацією або випаровуванням розчинника. Потім іміни можна відновити з використанням відновників, таких як борогідрид натрію або ціаноборогідрид натрію, у відповідному розчиннику, такому як метанол, етанол, тетрагідрофуран, вода, діоксан або їх суміші, з отриманням сполук загальної формули VIII, де R1 є атомом водню. Необов'язково для модифікації R1 одержані сполуки загальної формули VIII можна піддати додатковому відновному алкілуванню з використанням відповідних альдегідів і відновників, таких як борогідрид натрію або ціаноборогідрид натрію, у відповідному розчиннику, такому як метанол, етанол, тетрагідрофуран, вода, діоксан або їх суміші, з або без додавання каталітичних кількостей кислоти, такої як оцтова кислота, при відповідній температурі, як описано вище. Дану реакцію також можна проводити in situ після першого відновного алкілування альдегідом загальної формули llа або lllа. Альтернативно для модифікації R1 одержані сполуки загальної формули VIII можна піддати ацилюванню з використанням відповідних електрофільних реагентів, таких як хлорангідриди кислот, бромангідриди кислот, йодангідриди кислоти, сульфонілхлориди і алкілгалогенформіати, з додаванням основ, таких як триалкіламіни, карбонат калію або алкоголяти літію, натрію або калію, у відповідному розчиннику, такому як етилацетат, діоксан, тетрагідрофуран або діетиловий етер, при відповідній температурі, як описано вище. Сполуки загальної формули IX одержують відновленням сполук загальної формули VIII з використанням відповідного відновника, такого як дитіоніт натрію, порошкоподібне залізо або цинк, у водному розчині соляної кислоти або оцтової кислоти, у відсутності або присутності органічних розчинників, таких як тетрагідрофуран або етанол, або газоподібного водню у присутності відповідного каталізатора для гідрування, такого як паладій на активованому вуглецю, у відповідних розчинниках, таких як метанол або етанол або суміш вода/тетрагідрофуран, при відповідній температурі. Одержані сполуки ідентичні сполукам за винаходом загальної формули І, де R2 і R2 являють собою атоми водню, і де R1, R3, Χ, Υ, Ζ і q є такими, як визначено вище. Сполуки загальної формули І, де R1 не є атомом водню і де R2 і необов'язково R2 не є атомом водню, одержують взаємодією сполук загальної формули IX, де R1 не є атомом водню, з використанням наступних способів: 36 введенням R2 відновним алкілуванням з використанням відповідних альдегідів і відновників, таких як борогідрид натрію або ціаноборогідрид натрію, у відповідному розчиннику, такому як метанол, етанол, тетрагідрофуран, вода, діоксан або їх суміші, з або без додавання каталітичних кількостей кислоти, такої як оцтова кислота, при відповідній температурі, як описано вище; необов'язковим введенням R2' додатковим відновним алкілуванням з використанням відповідних альдегідів і відновників, таких як борогідрид натрію або ціаноборогідрид натрію, у відповідному розчиннику, такому як метанол, етанол, тетрагідрофуран, вода, діоксан або їх суміші, з або без додавання каталітичних кількостей кислоти, такої як оцтова кислота, при відповідній температурі, як описано вище. Альтернативно R2' або R2 вводять ацилюванням з використанням відповідних електрофільних реагентів, таких як хлорангідриди кислот, бромангідриди кислот, йодангідриди кислот, сульфонілхлориди і алкілгалогенформіати, з додаванням основ, таких як триалкіламіни, карбонат калію або алкоголяти літію, натрію або калію, у відповідному розчиннику, такому як етилацетат, діоксан, тетрагідрофуран або діетиловий етер, при відповідній температурі, як описано вище. Для отримання сполук загальної формули І, де R1 є атомом водню і де R2 і необов'язково R2’ не є атомом водню, вводять захисну гр упу - таку як трет-бутилоксикарбоніл - як R1 до відновлення нітрогрупи, за способами, відомими хімікам в даній галузі. Дану захисну груп у відщеплюють після введення R2 і необов'язково R2' за відомими способами. Сполуки загальних формул Ilа і lllа одержують за звичайними способами, відомими хімікам в даній галузі та схематично представленими нижче: відновленням естеру карбонової кислоти відповідним відновником, таким як гідрид діізобутилалюмінію з подальшим окисненням одержаного бензилового спирту відповідним окисником, таким як суміш перутенат тетрапропіламонію/Мметилморфолін-N-оксид, хлорхромат піридинію, суміш диметилсульфоксид/оксалілхлорид. Альтернативно сполуки загальних формул llа і lllа можна одержати формілуванням з використанням дихлорметилметилового етеру і тетрахлориду титану [Gross et al., Org. Synth. Coll, 1973, Vol. V, 365; Fanghaenel et al., J. Prakt. Chem. 1997, 339, 277]. Альтернативно сполуки загальних формул II і lllа можна одержати за способами, відомими хімікам в даній галузі, такими як депротонування гетероароматичної сполуки сильною основою, такою як алкіллітій, і подальшою взаємодією з Ν,Νдиметилформамідом. Альтернативно сполуки загальних формул Ilа і lllа можна одержати за способами, відомими хімікам в даній галузі, такими як обмінна реакція галоген-метал галогензаміщених гетероароматичних сполук, таких як броміди або йодиди, взаємодією з металувальним агентом, таким як галід алкіллітію або алкілмагнію або діалкілмагній. Альтернативно сполуки загальних формул llа і lllа можна одержати за способами, відомими хімікам в даній галузі, наприклад, 37 79666 взаємодією тіофенів і бензотіофенів з фосфорилхлоридом у присутності N-метил-Nфентформаміду [King et al. J. Org. Chem. 1949, 14, 638] або Ν,Ν-диметилформаміду [Vilsmeier formylation, Raimimdo et al. J. Org. Chem. 2002, 67, 205]. Приклади Дані аналітичної РХ/МС одержували на устаткованні РЕ Sciex АРІ 150ЕХ, забезпеченому джерелом іонного потоку IonSpray і РХ-системою Shimadzu LC-8A/SLC-10А. Колонка: 30´4,6мм Waters Symmetry C18 з розміром частинок 3,5мкм; система розчинників: А - суміш вода/три фтороцтова кислота (100:0,05) і В суміш вода/ацетонітрил/трифтороцтова кислота (5:95:0,03); метод: елюювання в лінійному градієнті від 90% А до 100% В протягом 4 хвилин і з витратою 2мл/хв. Чистоту визначали інтеграцією УФ - (254нм) і ELSD сліду. Час утримування (RT або tR) виражали в хвилинах. Препаративне очищення РХ/МС проводили на тому ж устаткованні. Колонка: 50´20мм YMC ODSA з розміром частинок 5мкм; метод: елюювання в лінійному градієнті від 80% А до 100% В протягом 7 хвилин і з витратою 22,7мл/хв. Збір фракцій проводили при МС-детектуванні з розгалуженим потоком. 1 Н ЯМР-спектри записували при 500,13МГц на устаткованні Bruker Avance DRX500 або при 250,13МГц на устаткованні Bruker AC 250. Дейтерований хлороформ (99,8% D) або диметилсульфоксид (99,8%D) використовували як розчинник. ТМС використовували як внутрішній стандарт. Значення хімічних зсувів виражали в млн.-1 (ppm). Для різноманітних ЯМР-сигналів застосовували наступні скорочення: с - синглет, д - дублет, т триплет, кв - квартет, кві - квінтет,г - гептет, дд дублет дублетів, ддд - дублет дублетів дублетів, дт - дублет триплетів, дкв - дублет квартетів, тт триплет триплетів, м - мультиплет і шир - широкий синглет. В деяких випадках представлені значення констант сполучання J. Точки плавлення визначали на пристрої Büchi B-540, та вони не коректувалися. Одержання проміжних сполук Етиловий естер (4-амінофеніл)-карбамінової кислоти 4-Нітроанілін (100г, 0,72моль) розчиняли в етилацетаті (800мл) і додавали діізопропілетиламін (89,6мл, 0,936моль). Додавали етилхлорформіат (252мл, 1,45моль), розчинений в етилацетаті (200мл), і розчин перемішували протягом 18 годин при кімнатній температурі. Суміш промивали 2М НСI (300мл) і насиченим розчином солі (300мл), висушували (MgSO4) і концентрували у вакуумі до половини первинного об'єму. До одержаного розчину додавали паладій на активованому вуглецю (10г, 5% Pd, 50% Н2О) і суміш гідрували в апараті Пара (рН2=3 бар) при кімнатній температурі протягом 12 годин. Суміш профільтрували через Celite (броунмілерит) і розчинник випаровували у вакуумі з одержанням 118г (90%) вказаної в заголовку сполуки у вигляді кристалічного продукту. РХ/МС (m/z) 180,9 (МН+); tR=0,60хв. 1Н ЯМР (CDCI3): 1,27 (т, 3Н); 3,42 (шир, 2Н, ΝΗ2); 4,19 (кв, 2Н); 6,52 (шир, 1H, ΝΗ); 6,64 (м, 2Н); 7,14 (м, 2Н). 38 Аналогічним чином одержували наступну сполуку: Пропіловий естер (4-амінофеніл)-карбамінової кислоти Вихід: 98%. 1Н ЯМР (CDCI3): 0,96 (т, 3Н); 1,68 (м, 2Н); 3,51 (шир, 2Н); 4,09 (т, 2Η); 6,46 (шир, 1Н); 6,63 (д, 2Н); 7,14 (м, 2Н). Етиловий естер (4-фталімідофеніл)карбамінової кислоти Етиловий естер (4-амінофеніл)-карбамінової кислоти (118г, 0,65моль) розчиняли в льодяній оцтовій кислоті (2,0л) в атмосфері азоту і суміш нагрівали до 90°С. Додавали порціями ангідрид фталевої кислоти (102,0г, 0,69моль) протягом 30 хвилин і реакційну суміш витримували при 90°С протягом 2 годин. Суміші давали охолодитися до кімнатної температури і одержаний осад відфільтрували. Осад промивали на фільтрі водою (2л), потім діетиловим етером (3л) і потім висушували у вакуумі. Вихід 127г (62%) вказаної в заголовку сполуки у вигляді білої кристалічної речовини. РХ/МС (m/z) 311,3 (МН+); tR=2,57хв. 1Н ЯМР (ДМСО-d6): 1,26 (т, 3Н); 4,15 (кв, 2Н); 7,34 (дд, 2Н); 7,58 (дд, 2Н); 7,90 (ддд, 2Н); 7,95 (двд, 2Н); 9,80 (с, 1H, ΝΗ). Аналогічним чином одержували наступну сполуку: Пропіловий естер (4-фталімідофеніл)карбамінової кислоти Вихід: 81%. Етиловий естер (2-нітро-4-фталімідофеніл)карбамінової кислоти Етиловий естер (4-фталімідофеніл)карбамінової кислоти (99,0г, 0,32моль) суспендували в льодяній оцтовій кислоті (1,5л) і нагрівали до 90°С. Димну азотну кислоту (17,2мл, 0,41моль) додавали по краплях протягом 30 хвилин при 9095°С. Потім реакційну суміш перемішували при 100°С протягом 1 години і охолоджували до кімнатної температури. Кристалічні тверді частинки відфільтровували і промивали на фільтрі льодяною оцтовою кислотою (500мл), водою (1л) і діетиловим етером (1л), потім висушували у вакуумі з одержанням 101г (90%) вказаної в заголовку сполуки у вигляді жовтої твердої речовини. РХ/МС (m/z) 355,0 (МН+); tR=3,34хв. 1Н ЯМР (ДМСО-d6): 1,25 (т, 3Н); 4,16 (кв, 2Н); 7,81 (м, 2Н); 7,93 (ддд, 2Н); 7,99 (ддц, 2Н); 6,15 (дд, 1H); 9,99 (с, 1Н, NH). Аналогічним чином одержували наступну сполуку: Пропіловий естер (2-нітро-4-фталімідофеніл)карбамінової кислоти Вихід: 70%. Етиловий естер (4-аміно-2-нітрофеніл)карбамінової кислоти 1,2-Диметоксіетан (1,0л) додавали до етилового естеру (2-нітро-4-фталімідофеніл)карбамінової кислоти (101г, 0,28моль) і суміш кип'ятили із зворотним холодильником. Додавали гідразину моногідрат (19,6г, 0,39моль) по краплях протягом 10 хвилин і суміш перемішували при кип'ятінні зі зворотним холодильником протягом 1,5 години. Після охолоджування до кімнатної температури суміш профільтрували і тверді частинки промивали на фільтрі диметоксіетаном (250мл). 39 79666 Фільтрат концентрували випарюванням і кристалічний продукт червоного кольору перекристалізовували з толуолу (350мл), одержаний осад відфільтрували і висушували у вакуумі. Маточний розчин концентрували до половини первинного об'єму та витримували протягом 16 годин. Осаджену речовину відфільтрували і перекристалізовували, як описано раніше. Перекристалізовані тверді частинки об'єднували з одержанням в цілому 57,6г (90%) темно-червоної сполуки, вказаної в заголовку. РХ/МС (m/z) 225,1 (МН+); tR=2,08хв. 1Н ЯМР (CDCI3): 1,33 (т, 3Н); 3,77 (с, 2Н, ΝΗ2); 4,23 (кв, 2Н); 6,98 (дд, 1Н); 7,45 (д, 1Н); 8,28 (д, 1Н); 9,39 (с, 1Н, ΝΗ). Аналогічним чином одержували наступну сполуку: Пропіловий естер (4-аміно-2нітрофеніл)-карбамінової кислоти Вихід: 91%. 1Н ЯМР (CDCI3): 0,98 (т, 3Н); 1,71 (м, 2Н); 3,78 (шир, 2Н); 4,13 (т, 2Η); 6,98 (дд, 1Н); 7,44 (д, 1Н); 8,27 (д, 1Н); 9,39 (с, 1Н). Трет-бутиловий естер (4-сшіно-3-нітрофеніл)карбамінової кислоти До розчину 2-нітро-1,4-діамінобензолу (10,135г, 66,18ммоль), що нагрівався із зворотним холодильником, в тетрагідрофурані (100мл) додавали порціями Вос2О (ди-трет-бутилдикарбонат, 32,6г, 149ммоль) протягом 2 годин. Одержаний розчин виливали в гептан (2л), обробляли ультразвуком протягом 15хв., фільтрували і висушували у вакуумі з одержанням 13,40г вказаної в заголовку сполуки у вигляді червоної твердої речовини. Вихід 80%. РХ/МС (m/z) 295,4 ([M+H+MeCN]+); tR=2,54 (УФ, ELSD) 96%, 100%. 1Н ЯМР (ДМСО-d6): 1,47 (с, 9Н); 6,96 (д, 1Н); 7,24 (с, 2Н, NH 2), 7,41 (дд, 1Н); 8,20 (с, 1Н); 9,28 (с, 1Η, ΝΗ). [4-(4-Хлорбензолсульфоніл)-3-метилтіофен-2іл]метанол Розчин метилового естеру 4-(4хлорбензолсульфоніл)-3-метилтіофен-2карбонової кислоти (992мг, 3,00ммоль) в сухому тетрагідрофурані (20мл) і сухому СН 2Сl2 (10мл) охолоджували до 0°С в атмосфері Ν 2 і додавали DIBAL-H (9,0мл, 9,0ммоль, 1М розчин в толуолі). Через 3 години додавали ще порцію DIBAL-H (4,5мл, 4,5ммоль) і перемішування продовжували ще протягом 2 годин. Реакційну суміш гасили додаванням насиченого розчину сегнетової солі (30мл) і суміш перемішували протягом 1 години при кімнатній температурі. Фази розділяли, водну фазу екстрагували ЕtOАс (2 ´50мл) і об'єднані органічні шари висушували над Na2SO4 і випарювали у вакуумі. Продукт очищали хроматографією на силікагелі на системі FlashMaster з використанням як елюенту суміші гептан/етилацетат (елюювання в лінійному градієнті від 1:0 до 6:4). Об'єдн ували фракції, що містили продукт, і випарювали у вакуумі з одержанням бажаної сполуки (788мг, 87%). РХ/МС (m/z)=285,2 (М-Н2О+Н+), розраховано для C12H10ClO2S 2:284,9805; tR=2,45хв. 1H Я МР (CDCI3): 1,84 (т, J=5,7Гц, 1Н), 2,20 (с, 3Н), 4,73 (д, J=5,7Гц, 2Н), 7,49 (д, J=8,5Гц, 2Н), 7,84 (д, J=8,5Гц, 2Н), 8,18 (с, 1Н). Аналогічним чином одержували наступні сполуки: (3-Хлортіофен-2-іл)метанол 40 Вихід: 73%. 1Н ЯМР (CDCI3): 1,92 (шир, 1Н), 4,81 (с, 2Н), 6,91 (д, J=5,2Гц, 1Н), 7,25 (д, J=5,2Гц, 1Н). (5-Диметипамінобензо[b]тіофен-3-іл)метанол Вихід: 63%. 1H ЯМР (CDCI3): 1,62 (шир, 1Н), 3,01 (с, 6Н), 4,89 (с, 2Н), 6,96 (дд, 1Н), 7,11 (д, 1Н), 7,34 (с, 1Н), 7,68, (д, J=9,0Гц, 1Н). (5-Диметиламіно-3-метилбензо[b]тіофен-2іл)метанол Вихід: 56%. 1Н ЯМР (CDCI3): 1,69 (т, J=5,9Гц, 1Н), 2,35 (с, 3Н), 3,00 (с, 6Н), 4,88 (д, 2Н), 6,90 (д, 1Н), 6,93 (дд, 1Н), 7,63, (д, 1Н). (4-Бром-3-метокситіофен-2-іл)метанол Суспензію метилового естеру 4-бром-3гідрокситіофен-2-карбонової кислоти (948мг, 4,00ммоль), диметилсульфату (0,57мл, 6,0ммоль) і K2СО3 (1,11г, 8,0ммоль) у ацетоні (10мл) кип'ятили зі зворотним холодильником протягом 4 годин. Після охолоджування до кімнатної температури додавали воду (25мл). Суміш екстрагували ЕtOАс (2´25мл) і екстракти об'єднували, висушували над Na2SO4 і випарювали у вакуумі. Залишок розчиняли в сухому те трагідрофурані (20мл), розчин охолоджували до 0°С в атмосфері азоту і додавали DIBAL-H (12мл, 12ммоль, 1М розчин в толуолі). Через 2 години додавали ще порцію DIBAL-H (6мл, 6ммоль) і перемішування продовжували ще протягом 2 годин. Реакційну суміш гасили додаванням насиченого розчину сегнетової солі (30мл) і суміш перемішували протягом 1 години при кімнатній температурі. Фази розділяли, водну фазу екстрагували ЕtOАс (2´50мл) і об'єднані органічні шари висушували над Na2SO4 і випарювали у вакуумі. Продукт очищали хроматографією на силікагелі на системі FlashMaster з використанням як елюенту суміші гептан/етилацетат (елюювання в лінійному градієнті від 1:0 до 2:1). Об'єдн ували фракції, що містили продукт, і випарювали у вакуумі з одержанням бажаної сполуки (482мг, 54%). 1 H ЯМР (CDCI3): 1,86 (шир, 1Н), 3,90 (с, 3Н), 4,77 (с, 2Н), 7,15 (с, 1Н). Аналогічним чином одержували наступну сполуку: (6-Хлор-3-метоксибензо[b]тіофен-2-іл)метанол Вихід: 75%. 1H ЯМР (CDCI3): 1,92 (т, J=5,9Гц, 1Н), 3,99 (с, 3Н), 4,90 (д, J=5,7Гц, 2Н), 7,33 (дд, J=1,9,8,5Гц, 1Н), 7,64 (д, J=8,5Гц, 1Н), 7,73 (д, J=1,9Гц, 1Н). Одержання гетероарильних альдегідів загальної формули Ilа і lllа 4-(4-Хлорбензолсульфоніл)-3-метилтіофеи-2карбальдегід До суспензії [4-(4-хлорбензолсульфоніл)-3метилтіофен-2-іл]метанолу (786мг, 2,60ммоль), Nоксиду 4-метилморфоліну (0,46г, 3,9ммоль) і порошкоподібних молекулярних сит 4Å (1,3 г, активованих нетривалим нагріванням у вакуумі) в СН2Сl2 (7мл) додавали перутенат тетрапропіламонію (46мг, 0,13ммоль). Одержану суміш перемішували протягом 1 години, після чого її профільтрували крізь шар силікагелю (приблизно 25г), елюючи ЕtOАс. Елюат випарювали у вакуумі та продукт очищали хроматографією на силікагелі на системі FlashMaster з використанням як елюенту суміші гептан/етилацетат (елюювання в лінійному градіє 41 79666 нті від 1:0 до 1:1). Об'єднували фракції, що містили продукт, і випарювали у вакуумі з одержанням вказаної в заголовку сполуки (644мг, 82%). 1H ЯМР (CDCI3): 2,60 (с, 3Н), 7,53 (д, J=9,0Гц, 2Н), 7,87 (д, J=8,5Гц, 2Н), 8,53 (с, 1Н), 10,01 (с, 1Н). Аналогічним чином одержували наступні альдегіди: 3-Хлортіофен-2-карбальдегід Вихід: 94%. 1H ЯМР (CDCI3): 7,07 (д, J=5,2Гц, 1Н), 7,72 (д, J=0,5, 4,7Гц, 1Н), 10,07 (д, J=0,9Гц, 1Н). 4-Бром-3-метокситіофен-2-карбальдегід Вихід: 45%. 1Н ЯМР (CDCI3): 4,18 (с, 3Н), 7,60 (д, J=1,4Гц, 1Н), 10,08 (д, J=1,4Гц, 1Н). 6-Хлор-3-метоксибензо[b]тіофен-2карбальдегід Вихід: 86%. 1H ЯМР (CDCI3): 4,34 (с, 3Н), 7,36 (дд, J=1,7, 8,7Гц, 1Н), 7,75 (д, J=1,4Гц, 1H), 7,82 (д, J=8,5Гц, 1Н), 10,36 (с, 1Н). 5-Диметжамінобензо[b]тіофен-3-карбальдегід Вихід: 72%. 1Н ЯМР (CDCI3): 3,05 (с, 6Н), 7,00 (дд, J=2,4, 9,0Гц, 1Н), 7,68 (д, J=9,0Гц, 1Н), 7,99 (д, J=2,8Гц, 1Н), 8,24 (с, 1Н), 10,11 (с, 1Н). 5-Диметипаміно-3-метилбензо[b]тіофен-2карбальдегід Вихід: 73%. 1Н ЯМР (CDCI3): 2,74 (с, 3Н), 3,03 (с, 6Н), 7,00 (д, J=2,4Гц, 1Н), 7,12 (дд, J=2,4, 9,0Гц, 1Н), 7,69 (д, J=9,0Гц, 1Н), 10,30 (с, 1Н). 5-Фторбензофуран-3-карбальдегід При постійній температурі -60°С диметилсульфоксид (3,27г, 41,8ммоль) в дихлорметані (10мл) додавали до розчину оксалілхлориду (2,65г, 20,9ммоль) в дихлорметані (30мл) і розчин перемішували протягом 15хв. 1-(5Фторбензофуран-3-іл)метанол (3,16г, 19,0ммоль), розчинений в дихлорметані (60мл), додавали по краплях при -60°С. Суміш перемішували протягом 20 хвилин з подальшим додаванням триетиламіну (9,61г, 0,095ммоль). Після перемішування протягом 10 хвилин, реакційній суміші давали нагрітися до кімнатної температури та її перемішували ще протягом 20хв. Органічну фракцію послідовно промивали порціями по 50мл водою, 1N водним розчином НСI, насиченим водним розчином бікарбонату натрію і насиченим розчином солі, потім висушували (MgSO 4) і концентрували у вакуумі з одержанням сирої вказаної в заголовку сполуки з кількісним виходом у вигляді бежевої кристалічної твердої речовини. 1H ЯМР (CDCI3): 7,13 (дт, 1Н); 7,50 (дд, 1Н); 7,86 (дд, 1Н); 8,30 (с, 1Н); 10,15 (с, 1Н). 5-Фтортіофен-2-карбальдегід До розчину тіофену (4,8мл, 60ммоль) в сухому Et2O (200мл) при 0°С додавали n-BuLi (70мл, 66ммоль, 0,95Μ розчин в гексані) по краплях і розчин перемішували протягом 1 години при -5°С 0°С. Потім температуру до водили до -70°С і додавали розчин (PhSO2)2NF (28,4г, 90ммоль) в сухому тетрагідрофурані (200мл), підтримуючи температуру нижче -50°С. Потім одержаній суміші давали поволі нагрітися до кімнатної температури протягом ночі, додавали 2N розчин NaOH (300мл), суміш профільтрували і органічний шар промивали 2N розчином NaOH (2´300мл) і насиченим розчином NH4CI (300мл), а потім висушували над 42 Na2SO4. Перегонка з використанням колонки Vigreux завдовжки 40см видаляла велику частину Et2O, а кінцева сумісна перегонка з гептаном (50мл) давала розчин 20,7ммоль 2-фтортіофену і 4,6ммоль тіофену (визначали 1H ЯМР з використанням 200мкл DME як внутрішній стандарт) приблизно в 100мл тетрагідрофурану і гептану (т. кип.60-100°С). Даний розчин охолоджували до 0°С і додавали по краплях n-BuLi (44мл, 41ммоль, 0,95Μ розчин в гексані). Через 1 годину додавали по краплях розчин ДМФА (4,8мл, 62ммоль) в Et2O (15мл) і перемішування продовжували ще протягом 1 години при 0°С. Реакційну суміш гасили насиченим розчином NH4CI (200мл) і екстрагували Et2O (2´200мл), а екстракт висушували над Na2SО4. Більшу частину розчинника видаляли випаровуванням при атмосферному тиску (колонка Vigreux завдовжки 40см) і потім темний залишок випаровували у вакуумі з одержанням суміші 5фтортіофен-2-карбальдегіду та тіофен-2карбальдегіду в співвідношенні приблизно 10:1 (т. кип.78-79°С, 25мм рт.ст.) у вигляді золотистої олії (1,32г, 44%). Дану суміш використовували без додаткового очищення. 1Н ЯМР (CDCl3): 6,65 (д, J=4,2,1Н), 7,50 (д, J=3,8Гц, 1Н), 9,76 (д, J=4,2Гц, 1Н). Одержання проміжних сполук загальної формули VII Проміжні сполуки загальної формули VII одержували загальним способом, як описано нижче для одержання етилового естеру {4-[(5фторбензофуран-3-ілметил)аміно]-2-нітрофеніл}карбамінової кислоти, або загальним способом, як описано нижче для одержання N-(4-аміно-2нітрофеніл)-2-(4-фторфеніл)ацетаміду. Етиловий естер {4-[(5-фторбензофу'ран-3ілметил)аміно]-2-нітрофеніл}-карбамінової кислоти У 3-горловій круглодонній колбі, забезпеченій апаратом Діна-Старка, змішували 5фторбензофуран-3-карбальдегід (3,59г, 21,9ммоль) і етиловий естер (4-аміно-2нітрофеніл)-карбамінової кислоти (4,48г, 19,9ммоль) в о-ксилолі (80мл) і додавали каталітичну кількість кислої іонообмінної смоли (Amberlite IRC-84, 100мг). Суміш нагрівали до кипіння протягом 5 годин, профільтрували теплою і концентрували у вакуумі. Даний сирий продукт розчиняли в суміші діоксан:метанол (4:1) (90мл) і порціями додавали борогідрид натрію (1,50г, 39,8ммоль) протягом 30хв. Реакційну суміш перемішували при кімнатній температурі протягом ночі, потім виливали у воду (200мл) і екстрагували етилацетатом (3´75мл). Об'єднані органічні фракції промивали насиченим розчином солі, висушували (MgSO4) і випарювали з одержанням сирої твердої речовини, яку очищали хроматографією на силікагелі (елюент: суміш е тилацетат:гептан 1:2). Це давало 4,50г (61%) вказаної в заголовку сполуки у вигляді червоної кристалічної речовини. 1H ЯМР (CDCI3): 1,33 (т, 3Н); 4,07 (т, 1Н); 4,23 (кв, 2Н); 4,42 (д, 2Н); 6,99 (дд, 1Н); 7,05 (дт, 1Н); 7,25 (дд, 1Н); 7,42 (т, 1Н); 7,44 (д, 1Н); 7,65 (с, 1Н); 8,31 (д, 1Н); 9,39 (с, 1Н). Аналогічним чином одержували наступні проміжні сполуки: 43 79666 Етиловий естер {4-[(5-метилтіофен-2ілметил)аміно]-2-нітрофеніл}-карбамінової кислоти Вихід: 73%. РХ/МС (m/z) 336 (МН+); tR=3,41хв. Етиловий естер {4-[(3-метилтіофен-2ілметил)аміно]-2-нітрофеніл}-карбамінової кислоти Вихід: 89%. РХ/МС (m/z). Етиловий естер {4-[(тіофен-2-ілметил)аміно]-2нітрофеніл}-карбамінової кислоти Вихід: 71%. РХ/МС (m/z) 321 (МН+); tR=3,24хв. Етиловий естер {4-[(тіофен-3-ілметил)аміно]-2нітрофеніл}-карбамінової кислоти Вихід: 69%. РХ/МС (m/z) 320 (МН+); tR=3,08хв. Етиловий естер {4-[(бензо[b]тіофен-3ілметил)аміно]-2-нітрофеніп}-карбамінової кислоти Вихід: 87%. Т. пл. 151-152°С. РХ/МС (m/z) 371 (МН+); tR=3,59 хв. N-(4-Аміно-2-нітрофеніл)-2-(4фтор феніл)ацетамід До перемішуваної суспензії трет-бутилового естеру {4-[(2-(4-фторфеніл)-ацетиламіно]-3нітрофеніл}-карбамінової кислоти (2,40г, 6,16ммоль) в метиленхлориді (5мл) додавали трифтороцтову кислоту (5мл). Через 15 хвилин метиленхлорид випаровували і розчин, що залишився, переносили в насичений водний розчин NаНСО3 (200мл) при обробці ультразвуком. Осад відфільтрували, промивали водою і висушували у вакуумі з одержанням 1,70г вказаної в заголовку сполуки у вигляді червоно-коричневої твердої речовини. Вихід: 96,3%. РХ/МС; tR=2,25 (УФ, ELSD) 89%, 100%. 1H ЯМР (ДМСО-d6): 3,59 (с, 2Н); 5,65 (шир, 2Н, ΝΗ2); 6,83 (дд, 1Н); 7,08 (д, 1Н); 7,15 (т, 2Η), 7,21 (д, 1Н); 7,32 (дд, 2Н); 9,91 (с, 1Н, ΝΗ). Аналогічним чином одержували наступну сполуку: N-(4-Аміно-2-нітрофеніл)-3,3диметилбутирамід Вихід: 680мг, 93%. РХ/МС (m/z) 293,43 ([M+H+MeCN]+); tR=2,29 (УФ, ELSD) 99,5%, 99,1%. 1 Н ЯМР (ДМСО-d 6): 1,00 (с, 9Н); 2,12 (с, 2Н); 3,45 (шир, H2O+NH2); 6,84 (дд, 1Н); 7,06 (д, 1Н); 7,14 (д, 1Н); 9,64 (с, 1H, NH). Одержання проміжних сполук загальної формули VIII N-{4-[(5-Хлортіофен-2-ілметил)аміно]-2нітрофеніл}-2-(4-фторфеніл)ацетамід Розчин Н-(4-аміно-2-нітрофеніл)-2-(4фтор феніл)ацетаміду (306мг, 1,06ммоль) і 5-хлор2-тіофенкарбоксальдегіду (186мг, 1,2екв.) в безводному етанолі (40мл) нагрівали при 70°С протягом 30хв. Одержаний розчин концентрували до невеликого об'єму (приблизно 3мл) і гасили гептаном (15мл). Коричневий кристалічний продукт відокремлювали фільтруванням з одержанням 350мг проміжного іміну N-{4-[(5-хлортіофен-2ілметилен)аміно]-2-нітрофеніл}-2-(4фтор феніл)ацетаміду. Вихід: 79,2%. 1H ЯМР (ДМСО-d6): 3,71 (с, 2Н); 7,17 (т, 2Н); 7,29 (д, 1Н); 7,36 (дд, 2Н); 7,62 (д, 1Н); 7,63 (дд, 1Н); 7,71 (д, 1Н); 8,83 (с, 1Н); 10,44 (с, 1Н). Тверду речовину суспендували в метанолі (5мл), додавали NаВН3СN (200мг), потім оцтову кислоту (2мл). Одержаний розчин перетворювався на суспензію. Через 15 хвилин її обробляли водою (50мл) і продукт відокремлювали фільтруванням з одержанням після висушування у вакуумі 330мг червоної 44 твердої речовини. Вихід: 93,8%. РХ/МС (m/z) 420 ([М+Н]+); tR=3,34 (УФ, ELSD) 97%, 100%. 1Н ЯМР (ДМСО-d6): 3,60 (с, 2Н); 4,45 (д, 2Н); 6,87 (т, 1Н, NH); 6,93 (дд, 1Н); 6,94 (д, 1Н); 6,97 (д, 1Н); 7,11 (д, 1Н); 7,14 (т, 2Н); 7,28 (д, 1Н); 7,32 (дд, 2Н); 9,98 (с, 1Н). Аналогічним чином одержували з відповідного аніліну наступн у сполуку: N-{4-[(5-Хлортіофен-2-ілметил)аміно]-2нітрофеніл}-3,3-диметилбутирамід Сирий проміжний імін виділяли випаровуванням і відновленням, як описано вище. Потім реакційну суміш упарювали до невеликого об'єму, обробляли насиченим водним розчином NаНСО3 і етилацетатом і органічний шар випарювали. Залишок розчиняли в гарячому діізопропіловому етері, осаджували гептаном і фільтрували. Вихід: 880мг, 87,6%. РХ/МС (m/z) 382,48 ([М+Н]+); tR=3,46 (УФ, ELSD) 88%, 91%. 1 Н ЯМР (ДМСО-d6): 0,99 (с, 9Н); 2,12 (с, 2Н); 4,45 (д, 2Н); 6,84 (т, 1Н, NH); 6,92 (дд, 1Н); 6,94 (д, 1Н); 6,97 (д, 1Н); 7,07 (д, 1Н); 7,19 (д, 1Н); 9,69 (с, 1Н). Одержання проміжних сполук загальної формули XII Трет-бутиловий естер [4-[2-(4фтор феніл)ацетиламіно]-3-нітрофеніл}карбамінової кислоти До суспензії трет-бутилового естеру (4-аміно3-нітрофеніл)-карбамінової кислоти (1,992г, 7,87ммоль) і NаНСО3 (5,4г) у ацетонітрилі (20мл) додавали (4-фторфеніл)-ацетилхлорид (1,8мл, 1,3екв.). Одержану суспензію обробляли ультразвуком протягом 5 хвилин і перемішували при кімнатній температурі протягом 16 годин. її виливали у воду (200мл), обробляли ультразвуком протягом 5хв., фільтрували і промивали водою і гептаном. Одержаний залишок розчиняли в гарячому етилацетаті (30мл), додавали насичений водний розчин NaHCO3 (50мл) і одержану суміш гасили гептаном (200мл). Одержану суспензію обробляли ультразвуком протягом 5 хвилин і фільтрували. Залишок промивали водою і гептаном і висушували у вакуумі з одержанням 2,48г коричнево-жовтої твердої речовини. Вихід: 80,9%. РХ/МС (m/z) 412,54 ([M+Na]+), 453,58 ([M+MeCN+Na]+); tR=3,33 (УФ, ELSD) 97%, 100%. 1H ЯМР (ДМСО-d6): 1,48 (с, 9Н); 3,66 (с, 2Н); 7,16 (т, 2Н), 7,34 (дд, 2Н); 7,54 (д, 1Н); 7,64 (дд, 1Н); 8,16 (д, 1Н); 9,79 (с, 1H, NH), 10,29 (с, 1Η,ΝΗ). Аналогічним чином з використанням відповідного хлорангідриду кислоти одержували наступну сполуку: Трет-бутиловий естер [4-(3,3диметилбутирилсшіно)-3-нітрофеніл]-карбамінової кислоти Реакційну суміш перемішували при 45°С протягом 30 хвилин з надлишком третбутилацетилхлориду (3екв.). Сирий продукт виділяли після обробки сумішшю етилацетатнасичений водний розчин NаНСО3 і очищали флеш-хроматографією на SiO2 (50 г) з використанням суміші 10-15% етилацетат-гептан як елюент. Вихід: 2,20г (78,6%), жовта тверда речовина. РХ/МС (m/z) 415,58 ([M+MeCN+Na]+); tR=3,31 (УФ, 45 79666 ELSD) 99,5%, 99,9%. 1H ЯМР (ДМСО-d6): 1,01 (с, 9Н); 1,49 (с, 9Н); 2,17 (с, 2Н); 7,43 (д, 2Н); 7,63 (дд, 1Н); 8,11 (д, 1Н); 9,77 (с, 1H, ΝΗ); 10,01 (с, 1H, ΝΗ). Сполуки за винаходом Кислотно-адитивні солі сполук за винаходом можна легко одержати за способами, відомими фа хівцям в даній галузі. Приклад 1 1а Етиловий естер {2-аміно-4-[(5фторбензофуран-3-ілметил)аміно]феніл}карбамінової кислоти Етиловий естер {4-[(5-фторбензофуран-3ілметил)аміно]-2-нітрофеніл}-карбамінової кислоти (4,50г, 12,1ммоль) розчиняли в абсолютному етанолі (140мл), до цього додавали 6Ν водний розчин НСI (38мл) і порошкоподібне залізо (5,70г, 0,10моль). Червону суміш нагрівали при 60°С до зникнення інтенсивного забарвлення (20хв.). Тверді частинки відфільтрували і етанол видаляли з фільтрату випаровуванням у вакуумі. До залишку додавали водний аміак (насичений розчин), який потім екстрагували етилацетатом (3´100мл). Об'єднані органічні фракції промивали насиченим розчином солі, висушували (MgSO4) і концентрували у вакуумі. Сирий продукт очищали хроматографією на силікагелі (елюент: суміш етилацетат:гептан 1:1) з одержанням 2,70г (66%) вказаної в заголовку сполуки у вигляді твердої речовини. Т. пл. 150-151°С. Розраховано для C18H18FN3O3 ; С 62,96; Η 5,28; Ν 12,24. Знайдено: С 63,00; Η 5,38; Ν 12,13. PX/MC (m/z) 344 (ΜΗ+); tR=2,00хв. 1Η ЯМР (ДМСО-d6): 1,19 (т, 3Н); 4,03 (кв, 2Н); 4,26 (д, 2Н); 4,55 (с, 2Н, ΝΗ2); 5,79 (т, 1Н); 5,91 (дд, 1Н); 6,02 (д, 1Н, NH); 6,72 (д, 1H); 7,13 (дт, 1H); 7,56 (м, 2H); 7,95 (с, 1Н); 8,16 (шир, 1H, NH). Аналогічним чином одержували наступні сполуки і виділяли їх у ви гляді кислотно-адитивних гідрохлоридних солей: 1b Етилового естеру {2-аміно-4-[(5метилтіофен-2-ілметил)аміно]феніл}-карбамінової кислоти дигідрохлорид Осадження сирого продукту з етилацетату додаванням розчину соляної кислоти в діетиловому етері давало вказану в заголовку сполуку. Т. пл. 190°С (з розкладанням). Розраховано для C15H19N3 O2S, 2HCl: С 47,00; Η 5,67; Ν 10,97. Знайдено: С 46,84; Η 5,86; Ν 11,10. PX/MC (m/z) 306 (ΜΗ+); tR=1,77хв. 1H ЯМР (ДМСО-d6): 1,22 (т, 3Н); 2,37 (с, 3Н); 4,08 (кв, 2Н); 4,37 (с, 2Н); 6,64 (м, 1Н); 6,67 (дд, 1Н); 6,72 (д, 1Н); 6,86 (д, 1Н); 7,13 (д, 1Н); 8,93 (шир, 1H, NH). 1с Етилового естеру {2-аміно-4-[(3метилтіофен-2-ілметил)аміно]феніл}-карбамінової кислоти дигідрохлорид Осадження сирого продукту з етилацетату додаванням розчину соляної кислоти в діетиловому етері давало вказану в заголовку сполуку. PX/MC (m/z) 306 (МН+); tR=1,68 хв. 1Н Я МР (CDCI3) (вільна основа): 1,25 (т, 3Н); 2,23 (с, 3Н); 3,78 (шир, 3Н); 4,13 (кв, 2Н); 4,32 (с, 2Н); 6,05-6,10 (м, 2Н+NH); 6,82 (д, 1Н); 6,93 (д,Ш); 7,11 (д,1Н). Id Етилового естеру {2-аміно-4-[(тіофен-2ілметил)аміно]феніл}-карбамінової кислоти дигідрохлорид 46 Осадження сирого продукту з етанолу додаванням розчину соляної кислоти в діетиловому етері давало вказану в заголовку сполуку. Т. пл. 195°С. Розраховано для C14H17N3O2S, 2HCl: С 46,16; Η 5,26; Ν 11,54. Знайдено: С 46,34; Η 5,43; Ν 11,28. PX/MC (m/z) 292 (MH+); tR=1,58 хв. 1 Н ЯМР (ДМСО-d6): 1,22 (т, 3Н); 4,08 (кв, 2Н); 4,48 (с, 2Н); 6,71 (дд, 1Н); 6,79 (д, 1Н); 6,97 (дд, 1Н); 7,10 (д, 1Н); 7,16 (д, 1Н); 7,40 (д, 1Н); 8,97 (шир, 1H, ΝΗ). 1е Етилового естеру {2-аміно-4-[(тіофен-3ілметил)аміно]феніл}-карбамінової кислоти дигідрохлорид Осадження сирого продукту з етилацетату додаванням розчину соляної кислоти в діетиловому етері давало вказану в заголовку сполуку. Т. пл. 196-197°С. Розраховано для C14H17N3 O2S, 2HCl: С 46,16; Η 5,26; Ν 11,54. Знайдено: С 46,23; Η 5,47; Ν 11,30. PX/MC (m/z) 292 (MH+); tR=1,54хв. 1Н ЯМР (ДМСО-d 6): 1,21 (т, 3Н); 4,08 (кв, 2Н); 4,29 (с, 2Н); 6,66 (дд, 1Н); 6,73 (д, 1Н); 7,14 (дд, 1Н); 7,16 (д, 1Н); 7,45 (м, 1Н); 7,51 (дд, 1Н); 8,86 (шир, 1H, ΝΗ). If Етилового естеру {2-аміно-4[(бензо[b]тіофен-3-ілметил)аміно]феніл}карбамінової кислоти дигідрохлорид Осадження сирого продукту з етилацетату додаванням розчину соляної кислоти в діетиловому етері давало вказану в заголовку сполуку. Т. пл. 213-214°С. Розраховано для C18H21N3Cl2О 2S: С 51,68; Η 4,95; Ν 10,05. Знайдено: С 51,88; Η 5,35; Ν 9,95. PX/MC (m/z) 342,2 (M+H+); tR=2,08хв. 1Н Я МР (ДМСО-^): 1,22 (т, 3Н); 4,08 (кв, 2Н); 4,53 (с, 2Н); 6,81 (дд, 1Н); 6,93 (д, 1Н); 7,19 (д, 1Н); 7,41 (м, 2Н); 7,70 (с, 1Н); 7,98 (м, 2Н); 8,97 (шир, 1H, ΝΗ). Приклад 2 2а Етиловий естер (2-аміно-4-{[4-(4хлорбензолсульфоніл)-3-метилтіофен-2ілметил]аміно}феніл)-карбамінової кислоти Суспензію 4-(4-хлорбензолсульфоніл)-3метилтіофен-2-карбальдегіду (301мг, 1,00ммоль) і етилового естеру (4-аміно-2-нітрофеніл)карбамінової кислоти (293мг, 1,30ммоль) в абсолютному етанолі (10мл) кип'ятили зі зворотним холодильником протягом 20 годин в атмосфері Ν2. Після охолоджування утвореного іміну оранжевочервоного кольору, його збирали фільтруванням і висушували у вакуумі з одержанням сирого продукту (312мг, 61%), який суспендували в суміші метанол:оцтова кислота 10:1 (10мл). Додавали NaBH 3CN (0,19г, 3,0ммоль) і суміш перемішували протягом 1 години при кімнатній температурі. Потім додавали ще порцію NaBH3CN (0,19г, 3,0ммоль) і ще через 1 годину додавали насичений водний розчин бікарбонату натрію (20мл). Утворений амін - тверду речовину червоного кольору - збирали фільтруванням і висушували у вакуумі з одержанням сирого продукту (293мг, 94%), який суспендували в абсолютному етанолі (10мл). До цього додавали 6N НСI (1,1мл, 6,6ммоль) і порошкоподібне залізо (193мг, 3,46ммоль) і суміш червоного кольору нагрівали до 60°С, поки червоне забарвлення не переходило в жовте, приблизно протягом 10-20хв. Суміш ви 47 79666 ливали в насичений водний розчин бікарбонату натрію (50мл) і EtOAc (50мл), одержану суміш фільтрували, фази розділяли і потім водну фазу екстрагували EtOAc (2´50мл). Об'єднані органічні фази висушували (Na2SO4) і розчинник випаровували у вакуумі. Продукт виділяли хроматографією на силікагелі на системі FlashMaster з використанням як елюенту суміші гептан/етилацетат (елюювання в лінійному градієнті, як правило, від 8:2 до 1:1). Об'єдн ували фракції, що містили продукт, і випарювали у вакуумі з одержанням вказаної в заголовку сполуки у вигляді блідо-жовтої твердої речовини (213мг, 78%). РХ/МС (m/z)=480,1 (М+H+); розраховано для C21H23CIN3O 4S2: 480,0813; tR=2,35хв.; чистота за даними УФ-аналізу=72,4%, чистота за ELS=86,5%. 1Н ЯМР (ДМСО-d6): 1,19 (шир, 3Н), 2,16 (с, 3Н), 4,02 (кв, J=6,9Гц, 2Н), 4,23 (д, J=6,1Гц, 2Н), 4,57 (с, 2Н), 5,81 (дд, J=2,4, 8,5Гц, 1Н), 5,91-5,95 (м, 2Н), 6,72 (шир д, J=6,6Гц, 1Н), 7,72 (д, J=8,5Гц, 2Н), 7,90 (д, J=8,5Гц, 2Н), 8,15 (шир, 1Н), 8,31 (с, 1Н). Аналогічним чином одержували наступні сполуки: 2b Етиловий естер {2-аміно-4-[(3-хлортіофен2-ілметил)аміно]феніл}-карбамінової кислоти Вихід: 76%. РХ/МС (m/z)=326,0 (М+Н+), розраховано для C4H17CIN3O2S: 326,0725; tR=1,95хв., чистота за даними УФ-аналізу=85,8%; чистота за ELS=98,1%. 1Н ЯМР (ДМСО-d6): 1,19 (шир, 3Н), 4,03 (кв, J=7,1Гц, 2Н), 4,30 (д, J=6,1Гц, 2Н), 4,57 (с, 2Н), 5,83 (дд, J=2,4, 8,5Гц, 1Н), 5,93-5,97 (м, 2Н), 6,73 (шир д, J=7,1Гц, 1Н), 6,99 (д, J=5,2Гц, 1Н), 7,48 (д, J=5,2Гц, 1Н), 8,16 (шир, 1Н). 2с Етиловий естер {2-аміно-4-[(4-бром-3метокситіофен-2-ілметил)амгно]феніл}карбамінової кислоти Вихід: 66%. РХ/МС (m/z)=402,0 (М+Н+), розраховано для C15H19BrN3O 3S: 400,0325 (100%), 402,0310 (97,3%); tR=1,97хв., чистота за даними УФ-аналізу=87,9%; чистота за ELS=98,2%. 1Н ЯМР (ДМСО-d6): 1,20 (шир, 3Н), 3,83 (с, 3Н), 4,03 (кв, J=6,9Гц, 2Н), 4,32 (д, J=6,1Гц, 2Н), 4,58 (с, 2Н), 5,84-5,89 (м, 2Н), 5,97 (д, J=2,4Гц, 1Н), 6,74 (шир, 1Н), 7,46 (с, 1Н), 8,17 (шир, 1Н). 2d Етиловий естер {2-аміно-4-[(6-хлор-3метоксибензо[b]тіофен-2-ілметил)аміно]феніл}карбамінової кислоти Вихід: 60%. РХ/МС (m/z)=405,3 (М+Н+), розраховано для C19H21CIN3O 3S: 406,0987; tR=2,39хв., чистота за даними УФ-аналізу=95,0%; чистота за ELS=99,6%. 1Н ЯМР (ДМСО-d6): 1,19 (шир, 3Н), 3,95 (с, 3Н), 4,02 (кв, J=7,1Гц, 2Н), 4,43 (д, J=6,1Гц, 2Н), 4,56 (с, 2Н), 5,90 (дд, J=2,4, 8,5Гц, 1Н), 5,96 (т, J=5,9Гц, 1Н), 6,00 (д, J=2,8Гц, 1Н), 6,73 (шир д, J=6,6Гц, 1Н), 7,39 (дд, J=1,9, 8,5Гц, 1Н), 7,68 (д, J=8,5Гц, 1Н), 7,98 (д, J=1,9Гц, 1Н), 8,15 (шир, 1Н). 2e Етиловий естер {2-аміно-4-[(5диметиламінобензо[b]тіофен-3-ілметил) аміно] феніл}-карбамінової кислоти Вихід: 13%. РХ/МС (m/z)=385,0 (М+Н+), розраховано для C20H25N 4O2S: 385,1693; tR=1,29хв., чистота за даними УФ-аналізу=87,8%; чистота за ELS=93,5%. 1H ЯМР (ДМСО-d6): 1,19 (шир, 3Н), 2,94 (с, 6Н), 4,02 (кв, J=6,9Гц, 2Н), 4,34 (д, J=5,7Гц, 2Н), 4,53 (с, 2Н), 5,81 (т, J=5,9Гц, 1Н), 5,93 (дд, 48 J=2,4, 8,5Гц, 1Н), 6,03 (д, J=2,4Гц, 1Н), 6,72 (шир, 1Н), 6,95 (дд, J=2,4, 9,0Гц, 1Н), 7,08 (д, J=2,4Гц, 1Н), 7,38 (с, 1Н), 7,71 (д, J=8,5Гц, 1Н), 8,15 (шир, 1Н). 2f Етиловоий естер {2-аміно-4-[(5диметиламіно-3-метилбензо[b]тіофен-2ілметил)аміно]феніл}-карбаміновоїкислоти Вихід: 36%. РХ/МС (m/z)=399,2 (М+Н+), розраховано для C21H27N 4O2S: 399,1849; tR=1,31хв., чистота за даними УФ-аналізу=98,4%; чистота за ELS=99,4%. 1Н ЯМР (ДМСО-d6): 1,19 (шир, 3Н), 2,33 (с, 3Н), 2,93 (с, 6Н), 4,02 (кв, J=6,9Гц, 2Н), 4,37 (д, J=5,7Гц, 2Н), 4,54 (с, 2Н), 5,86 (дд, J=2,4, 8,5Гц, 1Н), 5,89 (т, J=6,6Гц, 1Н), 5,96 (д, J=2,4Гц, 1Н), 6,71 (шир, 1Н), 6,84-6,89 (м, 2Н), 7,58 (д, J=8,5Гц, 1Н), 8,16 (шир, 1Н). Приклад 3 3а Етиловий естер {2-аміно-4-[(5-метилтіофен2-ілметил)-(метил)аміно]феніл}-карбамінової кислоти Суміш 5-метил-2-тіофенкарбоксальдегіду (108мкл, 1,00ммоль), етилового естеру (4-аміно-2нітрофеніл)-карбамінової кислоти (225мг, 1,00ммоль) і Amberlite IRC-84 (10мг) у о-ксилолі (4мл) кип'ятили зі зворотним холодильником в атмосфері Аг протягом 5 годин. Леткі речовини видаляли випаровуванням у вакуумі та залишок розчиняли в ацетонітрилі (5мл). До одержаного розчину додавали NaBH3CN (0,25г, 4,0ммоль), потім НОАс (5 крапель). Після перемішування протягом 5 хвилин розчин ставав темно-червоним. Додавали формальдегід (37% розчин у воді, 0,89мл, 12ммоль) і перемішування продовжували протягом 30 хвилин при періодичному додаванні НОАс. Реакційну суміш випарювали до сухо го стану у вакуумі і залишок розподіляли між насиченим водним розчином бікарбонату натрію (50мл) і EtOAc (50мл). Водну фазу екстрагували EtOAc (50мл) і об'єднані органічні шари висушували (Na2SO4) і розчинники випаровували у вакуумі. Потім залишок розчиняли в етанолі (10мл). Додавали 6 N водний розчин НСI (2,0мл, 12ммоль) і порошкоподібне залізо (0,34г, 6,0ммоль) і суміш червоного кольору нагрівали при 60°С, поки червоне забарвлення не переходило в жовте, приблизно протягом 15хв. Суміш виливали в насичений водний розчин бікарбонату натрію (50мл) і EtOAc (50мл), одержану суміш фільтрували, розділяли фази і потім водну фазу екстрагували EtOAc (2´50мл). Об'єднані органічні шари висушували (Na2SO4) і розчинники випаровували у вакуумі. Продукт очищали хроматографією на силікагелі на системі FlashMaster з використанням як елюенту суміші гептан/етилацетат (елюювання в лінійному градієнті, як правило, від 8:2 до 1:1). Об'єднували фракції, що містили продукт, і випарювали у вакуумі з одержанням вказаної в заголовку сполуки у вигляді блідо-жовтої твердої речовини (145мг, 45% в цілому). РХ/МС (m/z)=319,9 (М+Н+), розраховано для C16H22N3O2 S: 320,1427; tR=1,80хв., чистота за даними УФаналізу=98,4%; чистота за ELS=97,2%. 1Н ЯМР (CDCI3): 1,29 (т, J=7,1, 3Н), 2,41 (с, 3Н), 2,91 (с, 3Н), 3,76 (шир, 2Н), 4,19 (кв, J=7,1Гц, 2Н), 4,52 (с, 2Н), 6,02 (шир, 1Н), 6,17 (д, J=2,8Гц, 1Н), 6,25 (дд, 49 79666 J=2,8, 8,5Гц, 1Н), 6,53-6,58 (м, 1Н), 6,66 (д, J=3,3Гц, 1Н), 6,98 (д, J=8,5Гц, 1Н). Аналогічним чином одержували наступну сполуку: 3b Етиловий естер {2-аміно-4-[(5-хлортіофен2-ілметил)-(метил)-аміно]феніл}-карбамінової кислоти Вихід: 34%. РХ/МС (m/z)=340,0 (М+Н+), розраховано для C15H19ClN3O2S: 340,0881; tR=2,14хв., чистота за даними УФ-аналізу=82,3%; чистота за ELS=90,2%. 1Н ЯМР (CDCI3): 1,29 (т, J=6,8, 3Н), 2,91 (с, 3Н), 3,78 (шир, 2Н), 4,20 (кв, J=7,2Гц, 2Н), 4,49 (с, 2Н), 6,05 (шир, 1Н), 6,16 (д, J=2,4Гц, 1Н), 6,24 (дд, J=2,4, 8,5Гц, 1Н), 6,73 (д, J=3,8Гц, 1Н), 6,99 (д, J=8,5Гц, 1Н). Аналогічним чином одержували наступну сполуку, за винятком того, що замість формальдегіду використовували ацетальдегід: 3с Етиловий естер {2-аміно-4-[(5-хлортіофен2-ілметил)-(етил)аміно]феніл}-карбамінової кислоти Вихід: 12%. РХ/МС (m/z)=353,9 (М+Н+), розраховано для C16H21ClN3O2S: 354,1038; tR=2,02хв., чистота за даними УФ-аналізу=97,5%; чистота за ELS=99,0%. 1Н ЯМР (CDCI3): 1,16 (т, J=7,1, 3Н), 1,29 (т, J=6,8, 3Н), 3,36 (кв, J=7,1Гц, 2Н), 3,76 (шир, 2Н), 4,19 (кв, J=7,2Гц, 2Н), 4,47 (с, 2Н), 6,05 (шир, 1Н), 6,13 (д, J=2,4Гц, 1Н), 6,19 (дд, J=2,4, 9,0Гц, 1Н), 6,73 (д, J=3,8Гц, 1Н), 6,96 (д, J=8,0Гц, 1Н). Аналогічним чином одержували наступну сполуку, за винятком того, що не виконували додавання формальдегіду: 3d Етиловий естер {2-аміно-4-[(5-фтортіофен2-ілметил)аміно]феніл}-карбамінової кислоти Вихід: 65% (25% після проведення очищення препарат. РХ/МС для видалення нефторованих побічних продуктів). РХ/МС (m/z)=310,2 (М+Н+), розраховано для C14H17FN3 O2S: 310,1020; tR=1,76хв., чистота за даними УФ-аналізу=96,6%; чистота за ELS=83,4%. 1Н ЯМР (CDCI3): 1,29 (шир, 3Н), 3,82 (шир, 2Н), 4,19 (кв, J=7,2Гц, 2Н), 4,31 (д, J=2,0Гц, 2Н), 6,05 (шир, 1Н), 6,09 (д, J=8,0Гц, 1Н), 6,29 (дд, J=1,5, 3,8Гц, 1Н), 6,58 (т, J - 3,5Гц, 1Н), 6,94 (д, J=8,0Гц, 1Н). Приклад 4 4а Етиловий естер {2-аміно-4-[(5-хлортіофен2-ілметил)аміно]феніл}-карбамінової кислоти Розчин 5-хлортіофен-2-карбальдегіду (240мкл, 111мкмоль, 463мм в 1,2-дихлоретані) додавали до розчину етилового естеру 4-аміно-2нітрофенілкарбамінової кислоти (240мкл, 111мкмоль, 463мм в 1,2-дихлоретані). Додавали триацетоксиборогідрид натрію (118мг, 555мкмоль) і одержану суміш перемішували протягом 3,5 годин при 40°С. Суміші давали охолодитися до кімнатної температури і додавали воду (100мкл). Суміш фільтрували крізь силікагель (500мг) і колонку промивали 1,2-дихлоретаном (3мл). Об'єднані органічні фази випарювали до сухого стан у у вакуумі. Одержану тверду речовину розчиняли в етанолі (3мл). До однієї третини одержаного розчину (1мл) додавали залізо (19мг) з подальшим додаванням водного розчину соляної кислоти (96мкл, 6М розчин). Одержану суміш поміщали в ультразвукову баню на 10хв. Потім додавали насичений 50 водний розчин бікарбонату натрію (2мл). Суміш екстрагували етилацетатом (3мл). Органічну фазу промивали водою (3мл) і насиченим розчином солі (3мл), висушували над сульфатом магнію, фільтрували і випарювали до сухого стану у вакуумі. Одержаний продукт розчиняли в 190мкл диметилсульфоксиду і піддавали очищенню препаративною РХ-МС. Одержаний розчин випарювали до сухого стану у вакуумі. Вихід (6,8мг, 56%). РХ/МС (m/z) (M+H)+ 326,1; RT=1,90 (УФ, ELSD) 92%, 99%. Аналогічним чином одержували наступні сполуки: 4b Етиловий естер {2-аміно-4-[(5-(бромтіофен2-ілметил)-аміно]феніл}-карбамінової кислоти РХ/МС (m/z) (М+Н)+ 371,9; RT=1,94 (УФ, ELSD) 89%, 98%. 4с Етиловий естер {2-аміно-4-[(4-(бромтіофен2-ілметил)аміно]феніл}-карбамінової кислоти РХ/МС (m/z) (М+Н)+ 372,0; RT=1,96 (УФ, ELSD) 76%, 100%. 4d Етиловий естер {2-аміно-4-[(5-етилтіофен2-ілметил)амгно]феніл}-карбамінової кислоти РХ/МС (m/z) (М+Н)+ 320,1; RT=1,90 (УФ, ELSD) 72%, 96%. 4c Етиловий естер {2-аміно-4-[(бензо[b]тіофен2-ілметил)аміно]феніл}-карбамінової кислоти РХ/МС (m/z) (М+Н)+ 342,1; RT=2,06 (УФ, ELSD) 75%, 100%. 4f Етиловий естер {2-аміно-4-[(5-фенілтіофен2-ілметил)аміно]феніл}-карбамінової кислоти РХ/МС (m/z) (М+Н)+ 368,2; RT=2,21 (УФ, ELSD) 90%, 99%. Приклад 5 5а Пропіловий естер {2-аміно-4[(бензо[b]тіофен-2-ілметил)аміно]феніл}карбамінової кислоти Бензо[b]тіофен-2-карбальдегід (1,36г, 8,38ммоль) додавали до розчину пропілового естеру (4-аміно-2-нітрофеніл)-карбамінової кислоти (2,00г, 8,36ммоль) в ацетонітрилі (10мл). Суміш нагрівали до 160°С протягом 2 хвилин в герметично закритому 20мл флаконі для обробки в мікрохвильовій печі. Після охолоджування додавали NaBH 3CN (1,06г, 16,7ммоль) і АСОН (48мкл, 0,84ммоль) і суміш перемішували протягом 30 хвилин при 25°С. Додавали суміш вода/насичений розчин солі (1:1,100мл) і екстрагували етилацетатом (3´100мл). Органічну фазу висушували над сульфатом магнію, фільтрували і концентрували у вакуумі. Неочищену проміжну сполуку очи щали флеш-хроматографією на силікагелі (елюент: суміш етилацетатхептан 1:9) і випарювали до сухого стану. Потім проміжну сполуку розчиняли в тетрагідрофурані (20мл) і додавали Na2S2O4 (3,67г, 21ммоль), розчинений у воді (50мл). Одержану суміш перемішували при 40°С протягом 5 годин в атмосфері аргону. Одержану суміш екстрагували етилацетатом (3´100мл), об'єднані органічні фази висушували над сульфатом магнію, фільтрували і концентрували у вакуумі. Очищення флешхроматографією (елюент: суміш етилацетат:гептан 1:1) давало 0,3г (10%) вказаної в заголовку сполуки у вигляді твердої речовини. РХ/МС (m/z) 356 ([М+Н]+); RT=2,45хв. 1Н ЯМР (CDCI3): 0,95 (т, 3Н); 1,67 (м, 2Н); 4,08 (т, 2Н); 4,55 (с, 2Н); 6,08 (д, 1Н); 51 79666 6,13 (дд, 1Н); 6,93 (д, 1Н); 7,20 (с, 1Н); 7,27 (дт, 1Н); 7,32 (дт, 1Н); 7,68 (д, 1Н); 7,77 (д, 1Н). Аналогічним чином одержували наступну сполуку: 5b Пропіловий естер {2-амто-4[(бензо[b]тіофен-3-ілметил)аміно]феніл}карбамінової кислоти Вихід: 16%. РХ/МС (m/z) 356 ([М+Н]+); RT=2,24хв. 1H Я МР (CDCI3): 0,96 (т, 3Н); 1,68 (м, 2Н); 4,10 (т, 2Н); 4,51 (с, 2Н); 6,12 (д, 1Н); 6,14 (дд, 1Н); 6,95 (д, 1Н); 7,36 (с, 1Н); 7,39 (дт, 1Н); 7,40 (дт, 1Н); 7,79 (дд, 1Н); 7,87 (дд, 1Н). Приклад 6 6a N-{2-аміно-4-[(5-хлортіофен-2ілметил)аміно]феніл}-2-(4-фторфеніл)ацетамід До перемішуваного розчину червоного кольору Ν-{4-[(5-хлортіофен-2-ілметил)аміно]-2нітрофеніл}-2-(4-фторфеніл)ацетаміду (320мг, 0,762ммоль) в тетрагідрофурані (25мл) і оцтовій кислоті (8мл) періодично додавали порошкоподібний цинк (розмір частинок менше 10мкм, 10 г) порціями протягом 30хв. Через 5 хвилин розчин ставав безбарвним. Одержану безбарвну суспензію фільтрували крізь шар SiO2 (10г) з використанням етилацетату як елюенту і одержаний розчин випарювали у вакуумі. Одержану тверду речовину розчиняли в суміші етилацетат/ацетон/трифтороцтова кислота (3мл/3мл/0,2мл), обробляли насиченим водним розчином NaHCO3 (50мл) і гептаном (30мл) і продукт відокремлювали фільтруванням з одержанням 280мг блідо-сірої твердої речовини. Вихід: 94,2%. РХ/МС (m/z) 390,4 ([М+Н]+); RT=2,26 (УФ, ELSD) 99%, 100%. 1Н ЯМР (ДМСО-d6): 3,56 (с, 2Н); 4,28 (д, 2Н); 4,57 (с, 2Н, ΝΗ2); 5,87 (дд, 1Н); 52 5,98 (м, 2Н, ΝΗ та аром. Н); 6,74 (д, 1Н); 6,86 (д, 1Н); 6,93 (д, 1Н);7,13 (т, 2Н); 7,35 (дд, 2Н); 9,10 (с, 1Н). Аналогічним чином одержували наступну сполуку з відповідної нітросполуки: 6b N-{2-аміно-4-[(5-хлортіофен-2ілметил)аміно}феніл}-3,3-диметилбутирамід Після фільтрування крізь SiO2 і випарювання продукт осаджували з біфазного розчину етилацетат/насичений водний NaHCО3 (5мл/20мл) з гептаном (50мл). Вихід: 580мг, 71,5%. РХ/МС (m/z) 352,48 ([М+Н]+); RT=2,16 (УФ, ELSD) 96%, 99%. 1Н ЯМР (ДМСО-d 6): 1,01 (с, 9Н), 2,11 (с, 2Н); 4,29 (д, 2Н); 4,54 (с, 2Н, ΝΗ2); 5,88 (дд, 1Н); 5,97 (т, 1H, ΝΗ); 5,99 (д, 1Н); 6,72 (д, 1Н); 6,87 (д, 1Н); 6,93 (д, 1Н); 8,82 (с, 1Н). Тестування in vitro та in vivo Сполуки за винаходом тестували, і була показана їх дія на одній або більше моделей, представлених нижче: Відносний потік через канал KCNQ2 Клітини, що стабільно експресують потенціалозалежні канали KCNQ2, висівали за день до здійснення досліду та мітили [86Rb+]. В день здійснення досліду клітини промивали буфером, що містить HBSS. Клітини заздалегідь інкубували з препаратом і включення [86Rb+] стимулювали субмаксимальною концентрацією KСl, яка дорівнювала 15мМ, в присутності препарату. Після відповідного інкубаційного періоду супернатант видаляли і визначали радіоактивність на сцинтиляційному лічильнику (Tricarb). Клітини лізували 2мм NaOH і визначали кількість 86Rb+. Розраховували відносний потік ((СРМc упернатант /СРМc упернатант +CРМклітин)Спол уки(СРМс упернатант /СРМс упернатант +СРМклітин)15мМ KCl)*100-100, СРМ - імпульси за хвилину. Значення ЕС50 сполук за винаходом складає менше 20000нМ, в більшості випадків менше 2000нМ і у бага тьох випадках менше 200нМ. Отже, сполуки за винаходом розглядаються як придатні для лікування захворювань, пов'язаних з калієвими каналами сімейства KCNQ. Максимальний електрошок Тест проводили на групах мишей-самців з використанням корнеальних електродів і дією прямокутних електричних імпульсів силою 26мА протягом 0,4сек. для викликання судом, що проявляються в тонічних витягуваннях задніх кінцівок [Wlaz et al. Epilepsy Research 1998, 30, 219229]. Індуковані пілокарпіном судомні напади Індуковані пілокарпіном судомні напади викликали внутрішньочеревинним введенням пілокарпіну в дозі 250мг/кг групам мишей-самців і спостерігали за розвитком судомних нападів, що проявляються у втраті здібності до зміни положення, протягом 30 хвилин [Starr et al. Pharmacology Biochemistry and Behavior 1993, 45, 321-325]. Електричний тест по встановленню судомного порогу На групах мишей-самців застосовували модифікацію метода "більше-менше" [Kimball et al. Radiation Research 1957, 1-12] для визначення середнього порогу індукування тонічного витягнення задніх кінцівок у відповідь на корнеальний електрошок. Перша миша з кожної групи одержувала електрошок силою 14мА (0,4сек., 50Гц), а потім проводили спостереження за розвитком судомного нападу. Якщо судоми спостерігалися, то для наступної миші струм зменшували на 1мА, якщо судоми не спостерігалися, то струм збільшували на 1мА. Дану процедуру повторювали для всіх 15 мишей в дослідній групі. Хімічний тест по встановленню судомного порогу Визначали порогову дозу пентилентетразолу, необхідну для індукції клонічних судом при інфузії пентилентетразолу з певною швидкістю (5мг/мл із швидкістю 0,5мл/хв.) в бічну хвостову вен у мишейсамців [Nutt et al. J. Pharmacy and Pharmacology 1986, 38, 697-698]. Стимуляція мигдалика Щурів піддавали оперативному втручанню з метою імплантації триполярних електродів в дорсолатеральний мигдалик. Після операції тваринам давали відновитися перед введенням групам щурів або тестовної сполуки в різних дозах, або носія сполук. Тварин стимулювали первинним порогом розряду післядії +25мкА щодня протягом 3-5 тижнів і у кожному випадку реєстрували тяжкість судомних нападів, тривалість судомних нападів і 53 79666 тривалість розряду післядії [Racine. Electroencephalography and Clinical Neurophysiology 1972, 32, 281-294]. Побічні ефекти Побічні ефекти стосовно центральної нервової системи оцінювали при визначенні часу знаходження мишей на стрижні, що обертається [Capacio et al. Drug and Chemical Toxicology 1992, 15, 177-201], або при визначенні їх р ухової активності за кількістю перетнутих ін фрачервоних променів в дослідній клітці [Watson et al. Neuropharmacology 1997, 36, 1369-1375]. Гіпотермічну дію сполуки на Комп’ютерна в ерстка Т. Чепелев а 54 внутрішню температуру тіла у тварин визначали ректальним зондом або імплантованим датчиком радіотелеметрії, здатними вимірювати температуру [Keeney et al. Physiology and Behaviour 2001, 74, 177-184]. Фармакокінетика Фармакокінетичні параметри сполуки визначали при внутрішньовенному або пероральному введенні щурам Spraque Dawley та відборі проб крові протягом 20 годин. Концентрацію сполук в плазмі крові визначали за допомогою РХ/МС/МС. Підписне Тираж 26 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійською1,2,4-triaminobenzene derivatives suitable for the treatment of the central nervous system disorders
Автори англійськоюRottlaender Mario, Ritzen, Andreas, Khanzhin Nikolay, Wenzel Tornoe Christian
Назва патенту російськоюПроизводные 1,2,4-триаминобензола, пригодные для лечения расстройств центральной нервной системы
Автори російськоюРоттлондер Марио, Ханжин Николай, Венсель Торньое Кристиан
МПК / Мітки
МПК: C07D 333/20, C07D 307/52, A61P 25/00, C07D 333/32, C07D 333/58, C07D 333/64, C07D 333/28, C07D 333/34, C07D 307/81
Мітки: центральної, системі, 1,2,4-триамінобензолу, придатні, похідні, нервової, лікування, розладів
Код посилання
<a href="https://ua.patents.su/27-79666-pokhidni-124-triaminobenzolu-pridatni-dlya-likuvannya-rozladiv-centralno-nervovo-sistemi.html" target="_blank" rel="follow" title="База патентів України">Похідні 1,2,4-триамінобензолу, придатні для лікування розладів центральної нервової системи</a>
Попередній патент: Спосіб одержання модифікованих жирів
Наступний патент: Датчик для реєстрації шкірно-гальванічної реакції
Випадковий патент: Спосіб розливу сталі в глуходонні виливниці












